La enfermedad venosa crónica (EVC) es la enfermedad vascular más frecuente en el ser humano y sigue siendo infradiagnosticada e infratratada en todos los niveles asistenciales. Los nuevos tiempos que vivimos suponen un aumento de la incertidumbre entre los pacientes crónicos sobre su diagnóstico, tratamiento y seguimiento por parte de los médicos de familia y especialmente en la EVC. Con el fin de abordar estos nuevos tiempos, el Grupo de Vasculopatías de Semergen ha diseñado el cuestionario Venocheck, que valora aspectos etiológicos, clínicos (clasificación CEAP), de severidad y calidad de vida, terapéuticos, presencia de complicaciones y criterios de derivación.
Chronic venous disease (CVD) is the most common vascular disease in humans and continues to be underdiagnosed and undertreated at all levels of care. The new times we live in have led to an increase in uncertainty among chronic patients about their diagnosis, treatment and follow-up by family doctors and especially in CVD. In order to analyze these new times, the Semergen Vasculopathies Group has created the Venocheck questionnaire, which assesses aetiological, clinical (CEAP classification), severity and quality of life, therapeutic aspects, presence of complications and referral criteria.
La enfermedad venosa crónica (EVC) se define como cualquier anormalidad morfológica y/o funcional del sistema venoso, manifestada mediante signos y/o síntomas. Está catalogada como la enfermedad vascular más frecuente en el ser humano con un pico de incidencia entre los 40-49 años en mujeres y 70-79 años en hombres1,2. De acuerdo a los datos españoles del Estudio DETECT realizado en atención primaria (AP) en 20063, el 71% de la población mayor de 16 años presentaba algún signo o síntoma de EVC, de los que un 49% los califican como importante y/o grave. En el estudio Vein Consult Program, realizado en centros de AP en España, se determinó una prevalencia de enfermedad venosa crónica de un 48,5%, de los cuales 7% requerían derivación a cirugía vascular y un 4% terminaron en cirugía4.
A pesar de todos estos datos, se trata de una enfermedad que está infradiagnosticada e infratratada en todos los niveles asistenciales, porque solo cuando el paciente refiere alguna molestia o síntoma es cuando acude a la consulta y se le presta atención sanitaria3. La EVC tiene un gran impacto socioeconómico debido al número de personas afectadas, al coste de las consultas y tratamiento, así como al deterioro de la calidad de vida por situaciones incapacitantes que conducen a un gran número de bajas laborales (costes indirectos). Todas estas situaciones hacen que en la actual situación pandémica por SARS-CoV-2 (COVID-19) siga siendo una de las enfermedades crónicas «abandonadas» en el vigente modelo asistencial y especialmente en AP.
El correcto funcionamiento del sistema vascular venoso exige la adecuada funcionalidad de las válvulas venosas, que direccionan el flujo en sentido ascendente y centrípeto e impiden el reflujo retrógrado y centrífugo. El fracaso del aparato valvular constituye el mecanismo fundamental de la EVC, aunque de forma clásica se ha asumido que el elemento fisiopatológico inicial y principal de la EVC residía en el reflujo y la hipertensión venosa mantenida, secundarios al fallo valvular y al proceso inflamatorio que dicha hipertensión generaba. No obstante, existe una evidencia creciente de que en un elevado porcentaje de pacientes con EVC primaria, las alteraciones inflamatorias de la pared venosa constituyen el elemento inicial del proceso5.
Existen factores de tipo congénito y frecuentemente hereditario (angiodisplasia, agenesias valvulares, enfermedades neurovasculares, etc.), así como idiopáticos y también causas secundarias (trombosis venosa profunda, iatrogenias, compresiones extrínsecas, etc.)5.
Los factores de riesgo que se asocian con mayor frecuencia al desarrollo de la EVC son la distribución genética familiar, edad, género o raza/etnia, los cuales no son modificables, mientras que otros sí pueden modificarse en mayor o menor medida (obesidad, sedentarismo, bipedestación prolongada, exposición al calor, uso de hormonas, embarazo, utilización de prendas ajustadas, hábitos tóxicos y la alimentación). Es clásica la relación entre la historia familiar de EVC y el riesgo de padecerla, aunque aún no se han podido identificar los genes específicos implicados que permitan confirmar la base genética6,7. La EVC se transmite de forma variable, unas veces con carácter recesivo y otras dominante. Algunos trabajos muestran que el riesgo de que los hijos desarrollen venas varicosas es del 89% si ambos padres sufren EVC, del 47% si solo un progenitor la sufre y del 20% si ninguno de ellos tiene evidencia de EVC6,8,9.
Claramente, la prevalencia de EVC se incrementa con la edad, considerada junto con el género como los factores de riesgo más importantes. Los datos de Europa, América Latina, Oriente Medio y el Lejano Oriente están disponibles en el Programa Vein Consult a gran escala con 91.545 sujetos mayores de 18 años, en relación a las escalas de CEAP: C1-C6 involucró al 63,9% de los sujetos. La incidencia de C2 fue significativamente menor en el Medio Oriente, mientras que C1 fue significativamente mayor. C5 y C6 estaban desigualmente distribuidos en las regiones. Además, observamos que la EVC es más frecuente en raza blanca y muy poco común en raza negra y asiática. Se ha descrito una mayor frecuencia de aparición en países nórdicos y centroeuropeos que en países mediterráneos10.
En relación con el género, observamos que es predominante en la mujer a razón de 2-8:1 con respecto al hombre, aunque en estudios poblacionales no hay diferencia de género, presentando varices con la misma frecuencia. Sin embargo, hay una mayor incidencia de varices reticulares y telangiectasias en la mujer, mientras que en el hombre predominan las tronculares y estadios más avanzados de enfermedad11. También se ha demostrado una relación entre la EVC y la obesidad, de forma que un índice de masa corporal mayor de 30kg/m2 incrementa el riesgo de EVC de forma más intensa en hombres (OR: 6,5) que en mujeres (OR: 3,1), y en éstas con un mayor riesgo tras la menopausia (OR: 5,8)7. Los siguientes factores de riesgo se han relacionado con la EVC, pero no existen datos concluyentes de relación causal8: tabaquismo, sedentarismo, uso de hormonas (terapia hormonal sustitutiva o anticoncepción hormonal oral), diabetes, hipertensión arterial, utilización de prendas ajustadas, posturas relacionadas en el ambiente laboral (mantener las piernas cruzadas, bipedestación prolongada, etc.).
El conjunto de factores de riesgo de la EVC se expone en la tabla 1.
Factores de riesgo para enfermedad venosa crónica
THS: terapia hormonal sustitutiva ACO: anticonceptivos orales
Modificado de Wittens C, et al.7
La presentación clínica de la EVC es diversa y variable12. Su evolución puede abarcar desde problemas estéticos hasta la presencia de signos graves, entre ellos la aparición de úlceras. Los síntomas, aunque son inconstantes e inespecíficos, pueden orientarnos hacia su presencia, prestando también atención a los trastornos dérmicos asociados.
Se debe establecer el estado evolutivo, determinar el grado de discapacidad y la afectación de la calidad de vida13.
SíntomasLos síntomas pueden acompañar a todas las etapas de la EVC. Todo paciente con várices u otros signos de EVC debe ser interrogado sobre síntomas específicos de esta enfermedad14, antes de iniciar cualquier estudio diagnóstico7.
- •
Dolor: generalmente es difuso, sordo, no localizado, pudiendo tener carácter subagudo o crónico. Habitualmente es bilateral y se exacerba con el sedentarismo, bipedestación prolongada y temperaturas elevadas. Los dolores puntuales, generalmente agudos, suelen ser manifestaciones de complicaciones como una trombosis venosa superficial.
- •
Síntomas de neuropatía venosa: sensaciones de presión, opresión, quemazón, pinchazos, palpitaciones u hormigueos. Empeoran con el calor, se alivian con el frío y no aumentan al caminar. Su origen está relacionado con el estado inflamatorio de la enfermedad.
- •
Pesadez tras bipedestación prolongada y suele ser generalmente vespertina y de intensidad gradual.
- •
Calambres que suelen aparecer de noche o ligados al esfuerzo y al calor.
La exploración física se debe realizar con el paciente en bipedestación, buscando presencia de los siguientes signos13–15:
VaricesEs el signo más prevalente y se pueden clasificar en:
- -
Telangiectasias: varices intradérmicas de hasta 1mm de calibre, que tienden a confluir.
- -
Reticulares: varices subdérmicas, tortuosas y de color azulado, entre 1 y 3mm.
- -
Tronculares: venas subcutáneas dilatadas mayores de 3mm de diámetro.
- -
Corona flebectásica: patrón en abanico de numerosas pequeñas venas intradérmicas sobre cara medial o lateral del tobillo. Constituye un signo temprano de EVC avanzada.
Edema generalmente blando, no doloroso, aumenta en bipedestación a lo largo del día y con el calor. Aparece inicialmente a nivel maleolar, pero puede extenderse hasta la rodilla, respetando el pie. Provoca un aumento del volumen de la pierna y al ser palpado produce signo de fóvea. No es específico de la EVC, pudiendo aparecer asociado especialmente a insuficiencia cardiaca e insuficiencia renal. El edema mejora o desaparece con la elevación del miembro, la compresión elástica o el tratamiento farmacológico.
Alteraciones cutáneas- -
Hiperpigmentación ocre: aparece cuando hay un oscurecimiento parduzco de la piel por la extravasación y depósito de hemosiderina en la piel. Suele localizarse en el tobillo, pero puede extenderse hacia el pie o la pierna.
- -
Eccema: eritema y descamación de la piel que afecta inicialmente a la cara inferointerna de la pierna, pero que puede progresar extendiéndose a toda la extremidad. A veces evoluciona hacia la formación de costras.
- -
Lipodermatoesclerosis (o hipodermitis): inflamación crónica localizada con fibrosis de la piel y tejido subcutáneo. Existe un endurecimento con aumento del grosor del tejido dérmico/subdérmico. Es un signo de EVC avanzada.
- -
Atrofia blanca: placa cutánea mal delimitada, de coloración blanquecina, surcada por telangiectasias y petequias rodeadas de un halo hiperpigmentado. Suelen localizarse en el tercio inferior de piernas y pies.
- -
Úlcera venosa: solución de continuidad de la piel, sin tendencia a la cicatrización espontánea. Suelen localizarse en región perimaleolar interna, su tamaño y profundidad son variables. Clínicamente son redondeadas y de bordes delimitados. Tienen un fondo sucio, con fibrina y áreas de tejido de granulación. Las zonas de necrosis son poco frecuentes y no llegan a adentrarse a planos profundos.
Aunque la evaluación clínica permite realizar el diagnóstico de EVC en un elevado porcentaje de pacientes, siempre que exista disponibilidad es conveniente complementarlo con una prueba de imagen como el eco-Doppler.
Clasificación CEAPEn el año 1994, el American Venous Forum elaboró un documento de consenso para la clasificación y gradación de la EVC basado en las manifestaciones clínicas (C), factores etiológicos (E), distribución anatómica (A) y hallazgos fisiopatológicos (P), que ha sido actualizado en años posteriores, publicándose la última revisión en 202016. El objetivo de esta clasificación es determinar la presencia de signos y síntomas, gravedad clínica, localización y tipo de enfermedad venosa (primaria, secundaria o congénita). Es la clasificación aceptada de forma general en todo el mundo y, desde su adopción, las comunicaciones del ámbito venoso se han sistematizado. Se recomienda emplear la clasificación CEAP en todo paciente con EVC.
En el ámbito de la AP se utiliza la clasificación clínica (C) por ser la más asequible y sencilla de utilizar. Se puede evaluar mediante una inspección visual y distingue siete grados:
- •
C0: ausencia de signos palpables o visibles.
- •
C1: telangiectasias/varices reticulares.
- •
C2: varices tronculares.
- •
C3: edemas.
- •
C4: cambios cutáneos.
- -
4a: pigmentación o eccema.
- -
4b: lipodermatoesclerosis o atrofia blanca.
- -
4c: corona flebectásica.
- •
C5: úlcera cicatrizada.
- •
C6: úlcera activa.
Después de la categoría se añade una A si el sujeto está asintomático o una S si presenta síntomas.
En las categorías C2 y C6 se añade un subíndice «r» si existe recurrencia de venas varicosas o úlceras, como consecuencia de la progresión de la enfermedad después de un tratamiento previo17.
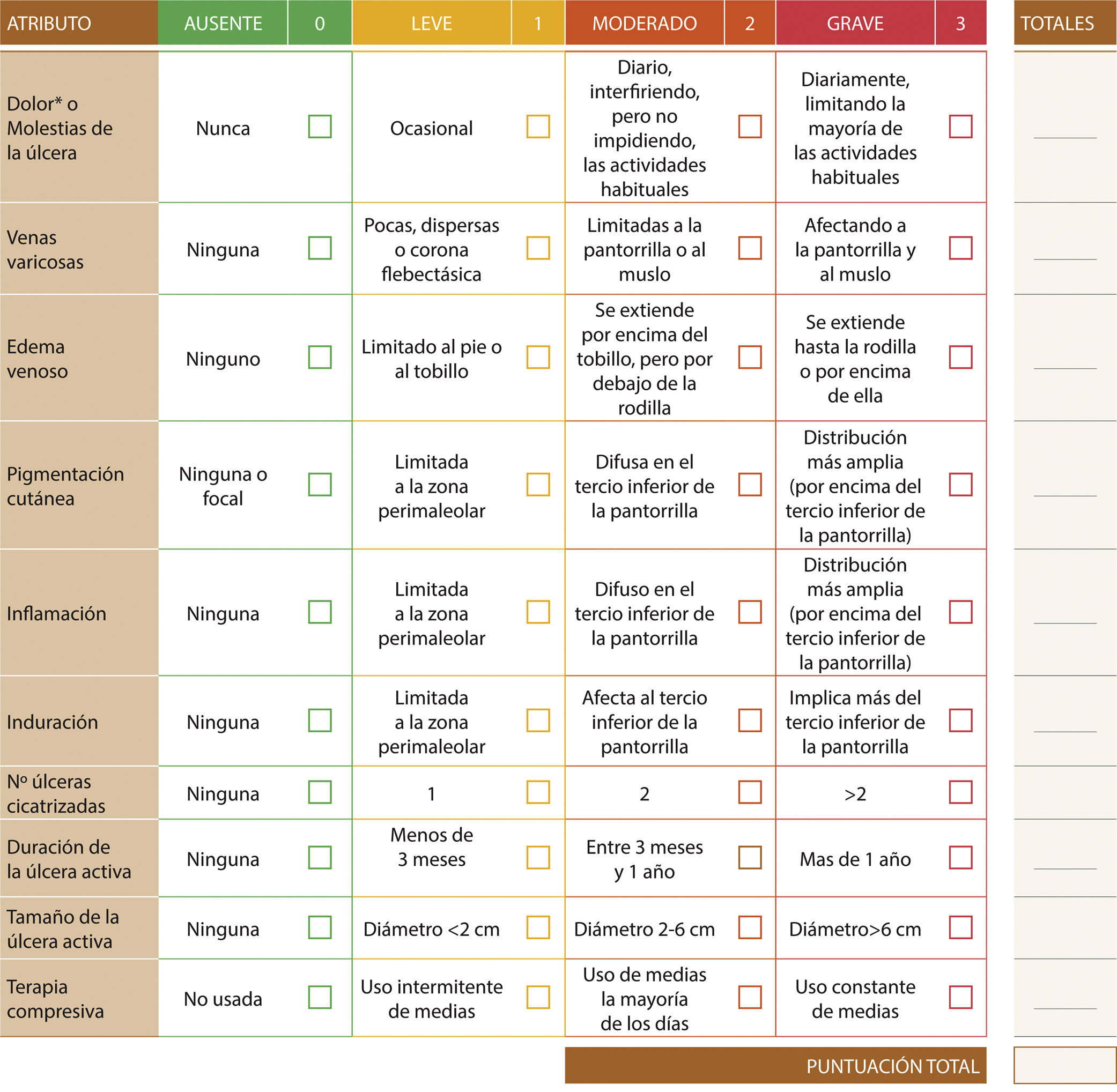
Severidad y afectación de la calidad de vidaSeveridadLa clasificación CEAP es útil para caracterizar la EVC, pero no permite valorar su gravedad y evolución. A este respecto, la clasificación más aceptada es el Venous Clinical Severity Score (VCSS) en su versión revisada18(tabla 2), que contiene 10 ítems (dolor, varices, edema venoso, pigmentación cutánea, inflamación, induración, número de úlceras cicatrizadas, duración y tamaño de úlcera activa y uso de terapia compresiva) que se clasifican según su gravedad. El VCSS permite una valoración evolutiva de la enfermedad y de su respuesta al tratamiento.
Escala de severidad clínica venosa (r-VCSS)
INTERPRETACIÓN: Los 10 items de la escala se clasifican según su gravedad. Cuanto mayor sea la cifra de la suma de los ítems mayor será la gravedad de la EVC, pudiendo oscilar entre 0 (ninguna gravedad) y 30 puntos (máxima gravedad)
*Dolor, pesadez, fatiga, malestar y ardor presumiblemente de origen venoso.
Modificado de Maeseneer et al.18.
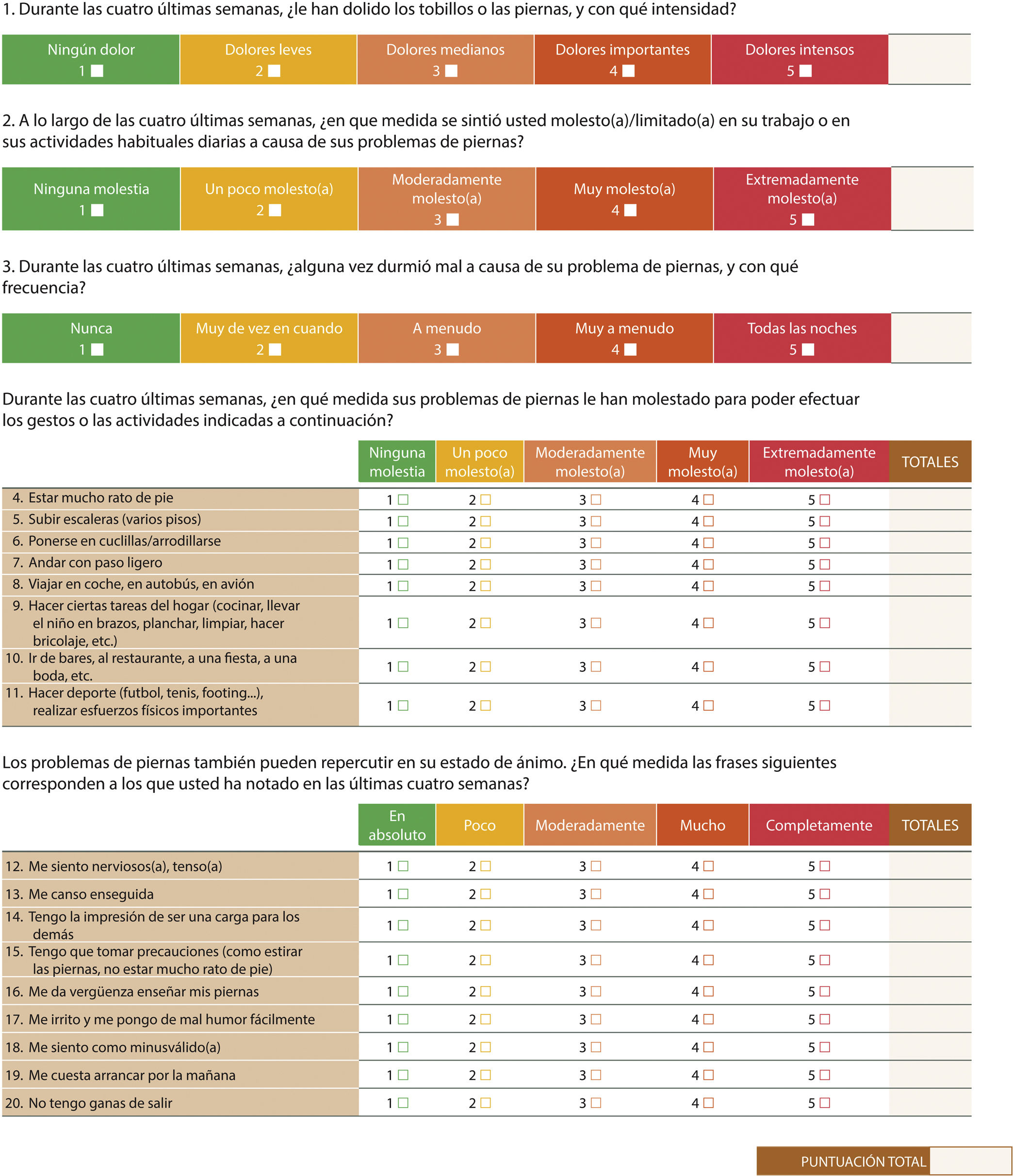
Durante los últimos años la calidad de vida ha adquirido una importancia fundamental como criterio mayor de salud. La EVC implica una afectación significativa de la calidad de vida de los pacientes y debe ser valorada adecuadamente. El único cuestionario específico de este aspecto en EVC validado en España, es el CIVIQ-2019(tabla 3). Presenta una excelente consistencia interna y una alta fiabilidad, con un tiempo de realización que no suele superar los 10 minutos. Incluye 20 ítems que identifican 4 dimensiones: repercusiones psicológicas, repercusión del dolor, repercusión física y social. El CIVIQ-20 resulta un instrumento útil para evaluar la mejora en la calidad de vida en respuesta al tratamiento y se ha usado también en pacientes con síndrome postrombótico20.
Cuestionario para valorar la calidad de vida del paciente con enfermedad venosa crónica. CIVIQ-20
NTERPRETACIÓN: Las preguntas están agrupadas en cuatro dimensiones: dolor (preguntas 1,2,3 y 4), social (preguntas 8,10 y 11), física (preguntas 5,6,7 y 9) y psicológica (preguntas de la 12 a la 20). El valor obtenido es directamente proporcional al grado de deterioro de la calidad de vida; es decir, tanto mayor cuanto peor es el estado de salud. Así, la puntuación global mínima es de 20 puntos (mejor estado de salud) y la máxima de 100 (deterioro importante). Para el cálculo automático de la puntuación global del cuestionario, se puede utilizar la calculadora que aparece en el enlace siguiente: https://www.civiq-20.com/scoring-missing-data/calculation-global-index-score/
Modificado de Lozano FS et al.19.
El cálculo de la puntuación global del cuestionario se puede realizar mediante la calculadora que aparece en el enlace siguiente: https://www.civiq-20.com/scoring-missing-data/calculation-global-index-score/
Tratamiento médico de la EVCEl objetivo del tratamiento médico en la EVC es doble:
- 1.
Tratar la hipertensión venosa con:
- -
Medidas posturales y cambios de estilo de vida.
- -
Terapia compresiva.
- 2.
Tratar el daño en la pared venosa (lesión endotelial) con fármacos venoactivos.
Con este doble objetivo, lo que pretendemos en definitiva es mejorar los síntomas, prevenir, evitar complicaciones y mejorar la calidad de vida de los pacientes.
Cambios en los estilos de vidaEs fundamental practicar ejercicio habitualmente (caminar, bicicleta, natación, gimnasia, baile, etc.). La contracción de los músculos de las piernas estimula la corriente de sangre hacia el corazón y facilita el retorno venoso.
También es importante llevar calzado adecuado con tacón cómodo menor de 4cm de alto, evitar la ropa ajustada (comprime las venas y dificulta el retorno venoso), evitar fuentes de calor (estimula la dilatación de las venas), combatir el estreñimiento, evitar el exceso de peso con una dieta mediterránea pobre en grasas saturadas y recomendar la ingesta de 1,5 litros de agua al día.
Es muy recomendable mover las piernas cuando se está mucho tiempo sentado o de viaje, además de masajearlas desde el pie hasta el muslo. También realizar ejercicios antiestasis venoso (ponerse alternativamente de puntillas y talones en bipedestación, hacer movimientos de bicicleta a la hora de irse a dormir) y elevar los pies de la cama 10-15cm para reducir la estasis venosa mientras se duerme21.
Terapia compresiva. Medias de compresión gradualExisten varias consideraciones a tener en cuenta sobre las medias de compresión gradual (MCG)5:
- -
Constituyen la piedra angular del tratamiento de la EVC.
- -
Aplican una presión decreciente desde el tobillo hasta la parte proximal de la extremidad.
- -
Reducen el reflujo, la hipertensión venosa y mejoran la función valvular.
- -
Aumentan la eficacia de la bomba muscular de la pantorrilla.
- -
Alivian los síntomas, el edema y mejoran los trastornos dérmicos.
- -
Mejoran la cicatrización, dolor y recurrencia de la úlcera venosa.
De acuerdo con su nivel de compresión (en el tobillo), las MCG se clasifican en:
- -
Compresión ligera: 15-20mmHg.
- -
Compresión normal: 21-30mmHg.
- -
Compresión fuerte: 31-40mmHg.
- -
Compresión extrafuerte: más de 40mmHg.
Es conveniente indicar la presión más baja que reduzca síntomas y edema:
- -
Presiones ligeras (15-20mmHg) pueden reducir síntomas.
- -
En el edema se precisan presiones superiores a 20mmHg.
En fases iniciales de las úlceras venosas, emplear el grado más elevado que soporte el paciente (a partir de 40mmHg). Para prevenir su recurrencia se recomienda utilizar una alta compresión (30-40mmHg).
Es fundamental utilizar la talla adecuada a la pierna de paciente y conviene informarle de sus efectos para aumentar la adherencia.
Las MCG deben ser colocadas desde primera hora de la mañana y renovadas cada 3-6 meses, si se llevan diariamente.
Hay que tener en cuenta valorar las posibles contraindicaciones de la terapia compresiva:
- -
Enfermedad arterial periférica (contraindicación absoluta si el índice tobillo brazo [ITB] <0,5).
- -
Insuficiencia cardiaca crónica avanzada o descompensada/edema pulmonar.
- -
Neuropatía periférica avanzada.
- -
Piel muy frágil sobre prominencias óseas.
- -
Celulitis o infecciones dérmicas importantes.
Todas las guías internacionales reconocen el efecto de la MCG en el control de los síntomas venosos y en la prevención de la recurrencia de las úlceras venosas, aunque con diferente grado de evidencia en sus recomendaciones22.
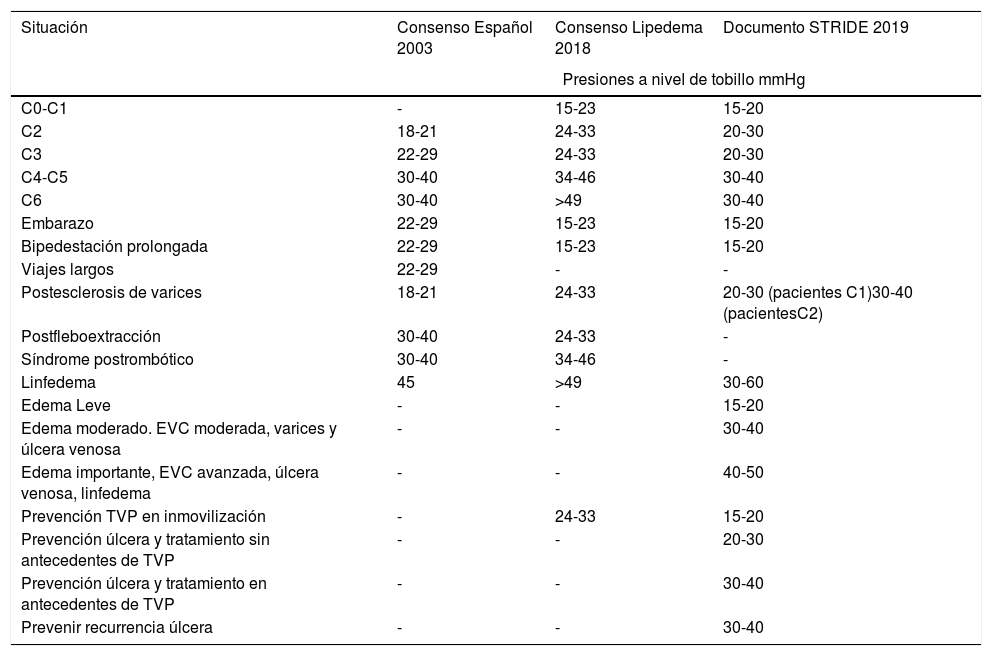
Existen varios consensos sobre el uso de MCG en distintas situaciones. Se exponen en la tabla 423.
Utilización de la compresión elástica en diferentes situaciones
| Situación | Consenso Español 2003 | Consenso Lipedema 2018 | Documento STRIDE 2019 |
|---|---|---|---|
| Presiones a nivel de tobillo mmHg | |||
| C0-C1 | - | 15-23 | 15-20 |
| C2 | 18-21 | 24-33 | 20-30 |
| C3 | 22-29 | 24-33 | 20-30 |
| C4-C5 | 30-40 | 34-46 | 30-40 |
| C6 | 30-40 | >49 | 30-40 |
| Embarazo | 22-29 | 15-23 | 15-20 |
| Bipedestación prolongada | 22-29 | 15-23 | 15-20 |
| Viajes largos | 22-29 | - | - |
| Postesclerosis de varices | 18-21 | 24-33 | 20-30 (pacientes C1)30-40 (pacientesC2) |
| Postfleboextracción | 30-40 | 24-33 | - |
| Síndrome postrombótico | 30-40 | 34-46 | - |
| Linfedema | 45 | >49 | 30-60 |
| Edema Leve | - | - | 15-20 |
| Edema moderado. EVC moderada, varices y úlcera venosa | - | - | 30-40 |
| Edema importante, EVC avanzada, úlcera venosa, linfedema | - | - | 40-50 |
| Prevención TVP en inmovilización | - | 24-33 | 15-20 |
| Prevención úlcera y tratamiento sin antecedentes de TVP | - | - | 20-30 |
| Prevención úlcera y tratamiento en antecedentes de TVP | - | - | 30-40 |
| Prevenir recurrencia úlcera | - | - | 30-40 |
EVC: enfermedad venosa crónica; TVP: trombosis venosa profunda.
Los fármacos venoactivos (FVA) no están globalmente definidos de forma precisa, identificándose generalmente como sustancias que actúan sobre el sistema venoso y especialmente dirigidos al manejo de la EVC. Se pueden clasificar en:
- •
Bioflavonoides: fracción flavonoide purificada micronizada (FFPM), rutósidos (hidroxietilrutósido, troxerutina).
- •
Flavonoides de síntesis: hidrosmina, diosmina sintética.
- •
Saponinas: escina, ruscus.
- •
Glucosaminoglucanos naturales: sulodexida.
- •
Otros: cumarina (Melilotus officinalis), Ginkgo biloba, dobesilato de calcio, naftazona, pentoxifilina.
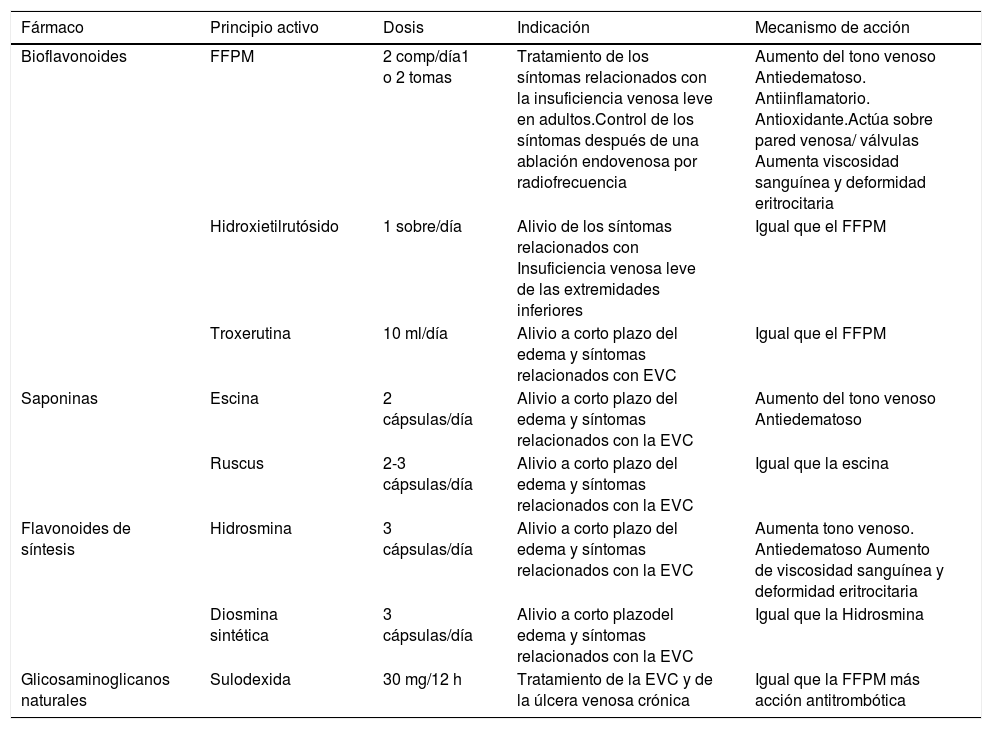
No todos los FVA son iguales, por lo que deben seleccionarse de acuerdo con sus propiedades, eficacia, estado evolutivo de la enfermedad, características del paciente y contraindicaciones. Las indicaciones y mecanismos de acción de estos fármacos se exponen en la tabla 55,24. El grado de evidencia sobre el uso de FVA en síntomas venosos varía de 2B a 1A en las distintas guías22.
Indicaciones y mecanismo de acción de los fármacos venoactivos
| Fármaco | Principio activo | Dosis | Indicación | Mecanismo de acción |
|---|---|---|---|---|
| Bioflavonoides | FFPM | 2 comp/día1 o 2 tomas | Tratamiento de los síntomas relacionados con la insuficiencia venosa leve en adultos.Control de los síntomas después de una ablación endovenosa por radiofrecuencia | Aumento del tono venoso Antiedematoso. Antiinflamatorio. Antioxidante.Actúa sobre pared venosa/ válvulas Aumenta viscosidad sanguínea y deformidad eritrocitaria |
| Hidroxietilrutósido | 1 sobre/día | Alivio de los síntomas relacionados con Insuficiencia venosa leve de las extremidades inferiores | Igual que el FFPM | |
| Troxerutina | 10 ml/día | Alivio a corto plazo del edema y síntomas relacionados con EVC | Igual que el FFPM | |
| Saponinas | Escina | 2 cápsulas/día | Alivio a corto plazo del edema y síntomas relacionados con la EVC | Aumento del tono venoso Antiedematoso |
| Ruscus | 2-3 cápsulas/día | Alivio a corto plazo del edema y síntomas relacionados con la EVC | Igual que la escina | |
| Flavonoides de síntesis | Hidrosmina | 3 cápsulas/día | Alivio a corto plazo del edema y síntomas relacionados con la EVC | Aumenta tono venoso. Antiedematoso Aumento de viscosidad sanguínea y deformidad eritrocitaria |
| Diosmina sintética | 3 cápsulas/día | Alivio a corto plazodel edema y síntomas relacionados con la EVC | Igual que la Hidrosmina | |
| Glicosaminoglicanos naturales | Sulodexida | 30 mg/12 h | Tratamiento de la EVC y de la úlcera venosa crónica | Igual que la FFPM más acción antitrombótica |
FFPM: fracción flavonoide purificada micronizada; EVC: enfermedad venosa crónica
Entre todos los FVA, destacan la FFPM y la sulodexida, que tienen una destacada acción para el tratamiento de la EVC por su actividad antiinflamatoria, sus efectos en la pared tanto venosa como valvular, y sobre la viscosidad sanguínea (actividad hemorreológica)25.
La sulodexida se distingue de la FFPM por su actividad antitrombótica, actuando en la hemostasia, fibrinólisis y agregación plaquetaria. Varios estudios muestran que sulodexida es el único FVA que podría estar indicado en prevención del síndrome postrombótico por su acción antinflamatoria, antitrombótica, profibrinolítica y por su papel en la conservación y reparación del glicocálix endotelial26.
En definitiva, las guías de práctica clínica reconocen y recomiendan el uso de los FVA para aliviar los síntomas y edemas relacionados con las EVC en pacientes en cualquier etapa de la enfermedad, asociados a terapia compresiva, escleroterapia y cirugía, o solos cuando hay alguna contraindicación en los otros tratamientos2,27.
En referencia a la úlcera venosa, la FFPM y la sulodexida son los principales fármacos recomendados en el tratamiento de las úlceras (aunque con distinto grado de evidencia en las distintas guías), combinados con terapia compresiva22. Hay mayor controversia respecto al uso de pentoxifilina y otros FVA (diosmina, rutósidos).
Existe una recomendación de la Agencia Española del Medicamento limitando el uso de los FVA a 2-3 meses para el alivio de los síntomas y edema. Sin embargo, el profesional debe valorar la posibilidad de utilizarlos en cualquier momento de la evolución de la EVC, prolongando el tratamiento o intercalando periodos de descanso.
Tratamiento quirúrgico de la EVCEl tratamiento quirúrgico es un complemento de los distintos tratamientos anteriormente descritos para las varices (medidas higiénico-dietéticas, terapia compresiva y tratamiento farmacológico).
El objetivo de la cirugía es conseguir la desaparición de las propias venas varicosas con su repercusión clínica y estética, reducir el edema, y los cambios tróficos, mediante la eliminación del reflujo venoso, tanto superficial como profundo, elementos fisiopatológicos fundamentales en el desarrollo de la EVC, consiguiendo restablecer la normalidad hemodinámica y extirpar las varices visibles, minimizando así sus complicaciones.
El tratamiento intervencionista actual ha cambiado radicalmente en las últimas dos décadas debido al uso generalizado de la ecografía, lo que ha permitido la aparición de nuevas técnicas percutáneas mínimamente invasivas basadas en la eliminación mediante mecanismos físicos, mecánicos, químicos o quirúrgicos de los segmentos insuficientes. Técnicas que no requieren de anestesia general o regional, ampliando las indicaciones quirúrgicas en determinadas patologías como la recidiva varicosa, la úlcera o las malformaciones venosas y en determinados pacientes como los mayores o los pacientes anticoagulados15,28–30. La utilización de las distintas modalidades se determina por la presencia de reflujo en safena, existencia de dilataciones varicosas y la disponibilidad de los distintos métodos, sin dejar de considerar la preferencia del paciente25.
Para poder establecer las indicaciones y contraindicaciones del tratamiento quirúrgico, utilizamos el sistema CEAP de clasificación clínica, con el que es posible realizar, al igual que en cualquier otra cirugía, una evaluación individualizada de su riesgo/beneficio.
Indicaciones de cirugía- 1.
Pacientes con EVC grado C2-C6 de la CEAP.
- 2.
Varices (CEAP C2) sintomáticas.
- 3.
Pacientes con trombosis venosas de repetición.
- 4.
Varices que hayan sangrado, con edema (CEAP C3).
- 5.
Pacientes con trastornos tróficos de piel (CEAP C4).
- 6.
Úlcera (CEAP C6), primero se busca cicatrizar la úlcera, luego eliminar la insuficiencia venosa superficial29,31.
Contraindicaciones absolutas para cirugía:
- 1.
Riesgo de complicaciones anestésicas o de presentar tromboembolismo pulmonar.
- 2.
Oclusión trombótica del sistema venoso profundo.
- 3.
Agenesia de sistema venoso profundo.
- 4.
Varices secundarias a malformación arteriovenosas congénitas.
- 5.
Enfermedad arterial crónica de miembros inferiores en estado avanzado.
- 6.
Embarazo o lactancia.
- 7.
Infección sistémica.
- 8.
Obesidad mórbida.
- 9.
Enfermedades como cáncer, hepatitis progresiva, insuficiencia cardíaca, enfermedad arterial coronaria e insuficiencia renal31.
La EVC es una enfermedad de curso crónico y progresivo que, por su elevada frecuencia y elevada morbilidad, supone un problema de salud generando un importante número de visitas, tanto en atención primaria como en atención hospitalaria.
La mayoría de los pacientes pueden ser atendidos adecuadamente en AP siguiendo un tratamiento conservador, el cual se recomienda en pacientes asintomáticos, con síntomas leves o con contraindicaciones para tratamiento quirúrgico.
Cuando la evolución no es la esperada, hay una indicación de tratamiento quirúrgico por parte del cirujano vascular. Las técnicas intervencionistas se han de valorar cuando los síntomas afecten de forma importante a la calidad de vida de los pacientes, cuando surjan complicaciones, pero nunca por un problema estético30.
Será necesaria una derivación a cirugía vascular en las siguientes situaciones:
- -
Cuando la EVC incida significativamente en la calidad de vida de los pacientes.
- -
Varices tronculares sintomáticas.
- -
Pacientes asintomáticos, pero con varices tronculares de gran calibre.
- -
Cualquier EVC complicada (trombosis venosa superficial, varicorragia, úlceras venosas de evolución tórpida que no responden al tratamiento convencional).
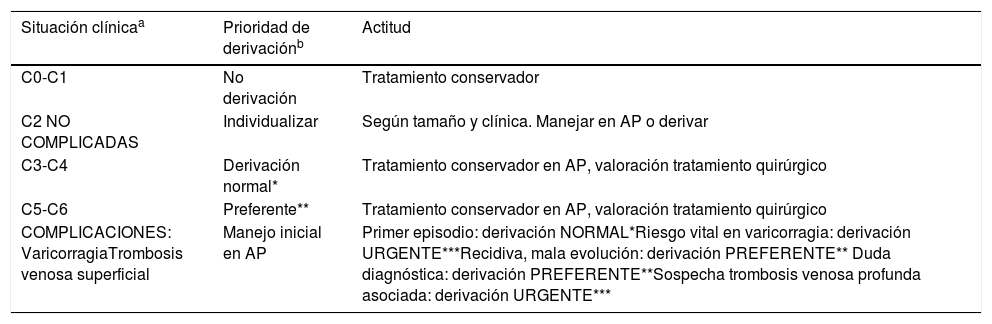
En este sentido, en un documento publicado por la Sociedad Española de Medicina Familiar y Comunitaria y la Sociedad Española de Angiología y Cirugía Vascular, se recogen los criterios de derivación entre ambos niveles y su prioridad (tabla 6). En el documento también se define el perfil del paciente que debe ser atendido en cada nivel asistencial, con el objetivo de mejorar la calidad de la atención, disminuyendo los tiempos de demora y evitando la duplicidad de las actuaciones32.
Criterios de derivación en enfermedad venosa crónica
| Situación clínicaa | Prioridad de derivaciónb | Actitud |
|---|---|---|
| C0-C1 | No derivación | Tratamiento conservador |
| C2 NO COMPLICADAS | Individualizar | Según tamaño y clínica. Manejar en AP o derivar |
| C3-C4 | Derivación normal* | Tratamiento conservador en AP, valoración tratamiento quirúrgico |
| C5-C6 | Preferente** | Tratamiento conservador en AP, valoración tratamiento quirúrgico |
| COMPLICACIONES: VaricorragiaTrombosis venosa superficial | Manejo inicial en AP | Primer episodio: derivación NORMAL*Riesgo vital en varicorragia: derivación URGENTE***Recidiva, mala evolución: derivación PREFERENTE** Duda diagnóstica: derivación PREFERENTE**Sospecha trombosis venosa profunda asociada: derivación URGENTE*** |
AP: atención primaria
La pandemia del SARS-CoV-2 (COVID-19) ha supuesto un aumento de la incertidumbre entre los pacientes crónicos sobre su seguimiento por parte de los médicos de familia. Frente a esta situación debemos realizar un cambio en el modelo asistencial, especialmente en AP. En el caso de la EVC, estamos obligados a vigilar de una forma más exhaustiva el diagnóstico, tratamiento y seguimiento de estos pacientes, considerando el importante deterioro de la calidad de vida que produce esta patología.
Se ha producido un incremento significativo de las consultas no presenciales (sobre todo telefónicas) en detrimento de las presenciales. Pensamos que, utilizadas adecuadamente, la consulta telefónica y la telemedicina en general, no deben contemplarse como sustitutos de la atención presencial, sino como un recurso más en AP. Resultan una forma útil de asistencia sanitaria, especialmente en circunstancias en las que el objetivo es reducir el riesgo de infección33.
A pesar de que no se deben olvidar los inconvenientes de las consultas telefónicas (mayor grado de incertidumbre, necesidad de mayor tiempo en situaciones de elevada complejidad, dificultad para la comunicación con algunos pacientes, etc.), presentan indudables ventajas: mayor accesibilidad, ahorro de tiempo para los pacientes, reducción del tiempo de consulta respecto a las visitas presenciales34. Su utilización en el seguimiento de patologías crónicas puede resultar especialmente adecuada. No obstante, siempre se debe tener presente la posibilidad de programar una visita presencial en caso de ser necesario.
El desarrollo de herramientas prácticas que ayuden a la planificación, reduciendo la complejidad de algunos de los procesos crónicos como en la EVC a través de una lista de comprobaciones (checklist), puede ayudarnos en la práctica clínica a mejorar el seguimiento de los pacientes.
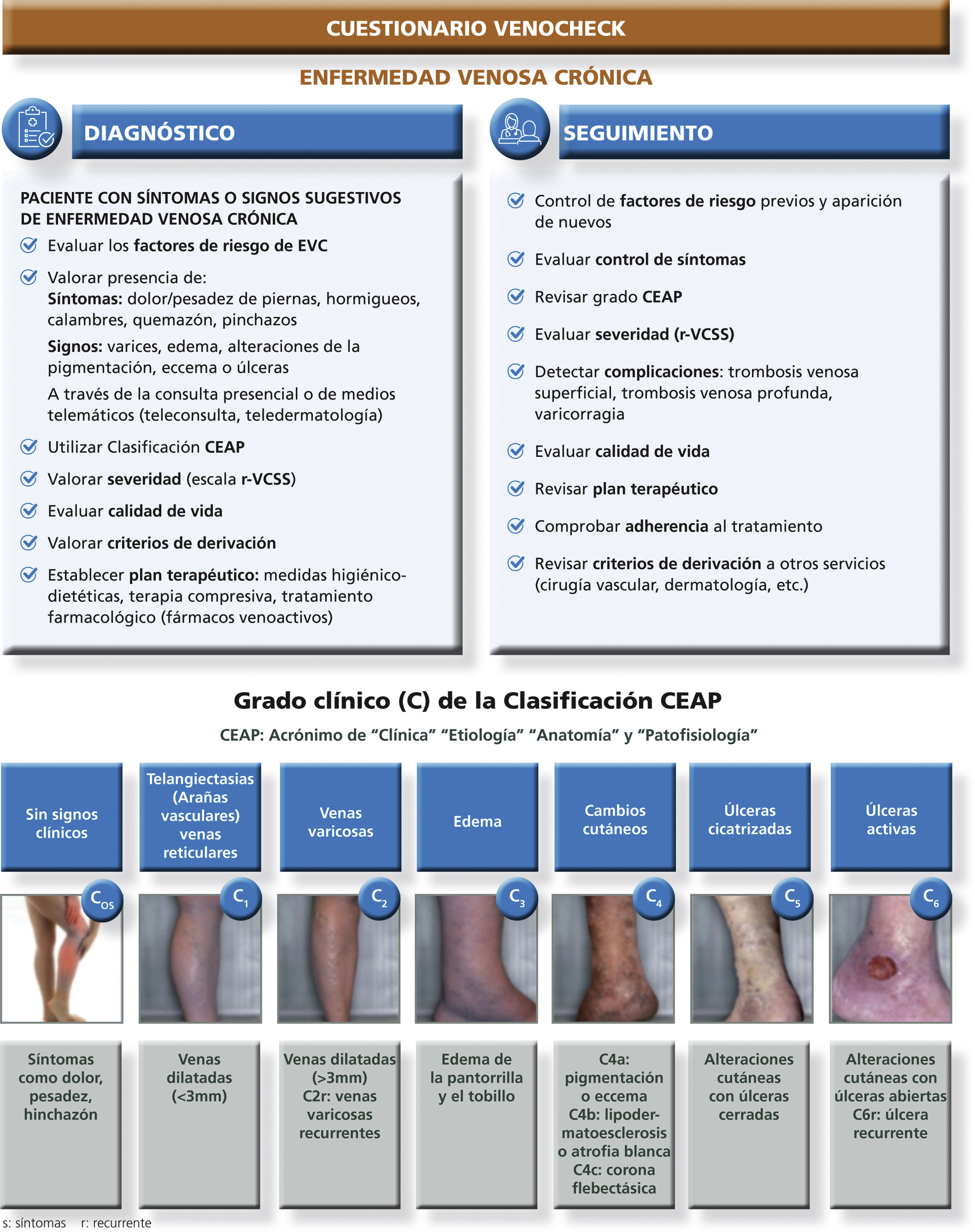
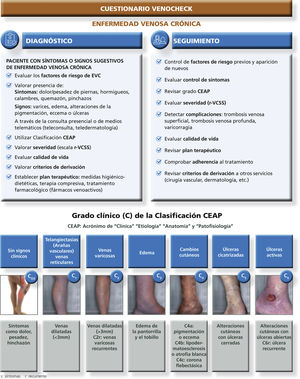
Con el fin de abordar los diferentes apartados a considerar en la revisión de un paciente con EVC, el Grupo de Vasculopatías de Semergen ha diseñado el cuestionario Venocheck, que valora aspectos etiológicos, clínicos (clasificación CEAP), de severidad y calidad de vida, terapéuticos, presencia de complicaciones y criterios de derivación.
El Venocheck es aplicable tanto en el diagnóstico de un paciente con síntomas/signos sugestivos de EVC, como en el seguimiento de un paciente ya identificado. Puede ser útil tanto en teleconsultas como en consultas presenciales, permitiendo sistematizar la valoración de estos pacientes y su seguimiento a lo largo del tiempo.
El cuestionario Venocheck se expone en la figura 1.
Recomendaciones en estos nuevos tiemposEl médico de atención primaria debe participar de manera multidisciplinar con otras especialidades médicas en el diagnóstico, tratamiento y seguimiento de la EVC. Debemos tener en cuenta en nuestro día a día los siguientes puntos para mejorar su valoración:
- •
Determinar de forma sistemática los factores de riesgo más importantes de la EVC (ver tabla 1).
- •
Valorar los signos y síntomas de la EVC, así como la clasificación CEAP para establecer un plan terapéutico eficaz (ver fig. 1).
- •
Evaluar la severidad y el impacto sobre la calidad de vida mediante escalas adecuadas (ver tablas 2 y 3).
- •
Detectar la presencia de complicaciones.
- •
Revisar el plan terapéutico, incluyendo las medidas higiénicas dietéticas, el tratamiento compresivo y la terapia farmacológica, y verificando la adherencia del paciente (ver tablas 4 y 5).
- •
Finalmente, comprobar la existencia de criterios de derivación (ver tabla 6).
Los autores declaran que no hay financiación en este manuscrito de beca o ayuda de entidad financiadora.
Conflicto de interesesJosé Manuel Ramírez Torres en los últimos 5 años ha recibido honorarios por becas, ponencias o labores de asesoría de Servier, AlfaSigma, Sanofi y Andaru Pharma. Estas relaciones no han influido directa ni indirectamente con la autoría ni en el contenido de este manuscrito.
Julia Caballer Rodilla en estos 5 últimos años ha realizado alguna sesión o ponencia con Esteve, Almirall, Novartis, Lilly e Italfarmaco. En ningún momento directa o indirectamente han influido con la auditoría o el contenido de este manuscrito.
Manuel Frías Vargas en los últimos 5 años ha recibido honorarios por becas, ponencias o labores de asesoría de Servier, AlfaSigma, Almirall, Astra Zeneca, Daichii-Sankyo, Ferrer, Italfarmaco, Lilly, MSD, Novartis, Rovi y Viatris. Estas relaciones no han influido directa ni indirectamente con la autoría ni en el contenido de este manuscrito.
Inés Gil Gil, médico de familia, ha recibido en los últimos 5 años honorarios por ponencias o labores de asesoría de Servier y Ferrer. Estas relaciones no han influido directa ni indirectamente con la autoría ni con el contenido del manuscrito.
Olga García Vallejo en los últimos 5 años ha recibido honorarios por becas, ponencias o labores de asesoría de Servier, AlfaSigma, ASPEN, Ferrer, Esteve, MSD, Pfizer, Lundbeck y Viatris. Estas relaciones no han influido directa ni indirectamente con la autoría ni en el contenido de este manuscrito.
Aguado Castaño Ana Carlota. Centro de Salud Parque Lo Morant, Alicante.
Aicart Bort María Dolores. Médica Jubilada.
Babiano Fernández Miguel Ángel. Centro de Salud Argamasilla de Calatrava. Ciudad Real.
Caballer Rodilla Julia. Centro de Salud Algete, Madrid.
Cabrera Ferriols María Ángeles. Centro de Salud San Vicente del Raspeig I, Alicante.
Carrasco Carrasco Eduardo. Centro de Salud de Abarán, Murcia.
Frías Vargas Manuel. Centro de Salud Comillas, Madrid.
Fuertes Domínguez Diana. Centro de Salud Cervera de Pisuerga, Palencia.
García Lerín Aurora. Centro de Salud, Almendrales, Madrid.
García Vallejo Olga. Centro de Salud Comillas, Madrid
Gil Gil Inés. Centro de Salud Vielha, Lleida.
Lahera García Ana. Hospital Universitario de Getafe, Madrid.
López Téllez Antonio. Centro de Salud Puerta Blanca, Málaga.
Lozano Bouzon Víctor Manuel. Hospital Universitario de Getafe, Madrid.
Padilla Sáez, Alicia. Centro de Salud San Vicente del Raspeig I, Alicante.
Peiró Morant Juan. Centro de Salud Ponent, Islas Baleares.
Perdomo García Frank J. Urgencias, Hospital La Paz, Madrid.
Pérez Vázquez Estrella. Centro de Salud Vielha, Lleida.
Piera Carbonell Ana. Centro de Salud Luanco-Gozón. SESPA, Asturias.
Pietrosanto Teresa. Centro de Salud San Vicente del Raspeig I, Alicante.
Ramírez Torres José Manuel. Centro de Salud Puerta Blanca, Málaga.
Vázquez Gómez Natividad. Centro de Salud Auxiliar Moncófar, Castellón.
Este documento ha sido validado por la Comisión Nacional de Validación de la Sociedad Española de Atención Primaria (SEMERGEN) con el aval n° 0058-2021.