La enfermedad pulmonar obstructiva crónica (EPOC) tiene una prevalencia en España del 10,2%. El principal factor etiológico es el tabaco. La exposición al humo de biomasa y el déficit de alfa-1 antitripsina (DAAT) también se relacionan con su desarrollo. El DAAT es una condición genética en la que subyace el 2-3% de los pacientes con EPOC.
El objetivo de este estudio descriptivo transversal fue descartar el DAAT en pacientes con EPOC del CS Culleredo, A Coruña. Para ello se realizó la prueba de la gota de sangre gruesa en papel secante y el estudio de variantes PI*S y PI*Z del gen SERPINA1 mediante análisis de curvas de desnaturalización tras amplificación simultánea por reacción en cadena de la polimerasa.
El estudió analizó 80 pacientes entre 40-80 años. Un 30% eran portadores de un alelo deficitario en heterocigosis, que en el 80% de ellos se trataba del alelo S. Se detectó un caso PiSZ (1,25%) y ninguno PiZZ. Esto representa una frecuencia alélica de 3,1% para el PiZ y 13,1% para el PiS. Las frecuencias alélicas detectadas son superiores a las descritas previamente para la población española.
Este trabajo excluye el déficit grave de AAT en el 98,75% de la población estudiada. El caso con genotipo Pi*SZ fue diagnosticado en una fase precoz de la enfermedad. El estudio cumple con uno de los indicadores de calidad asistencial recomendados por GesEPOC y constata una elevada frecuencia alélica PiS y PiZ en la zona, que será referencia de futuros estudios en Galicia.
The prevalence of chronic obstructive pulmonary disease (COPD) in Spain is 10.2%. Although tobacco is the main aetiological factor, biomass smoke exposure and alpha-1 antitrypsin deficiency (AATD) have also been related to its development. AATD is a genetic condition which could be causing 2-3% of COPD cases.
The aim of this cross-sectional descriptive study was to exclude the existence of AATD in a population of COPD patients from CS Culleredo, A Coruña. The thick blood drop test on blotting paper, as well as the analysis of the mutations PI*S and PI*Z of the gene SERPINA 1 by the analysis of denaturing gradients after simultaneous amplification related to PCR (polymerase chain reaction).
The study population included 80 patients between 40-80 years old, of whom 30% were carriers of a deficient allele (heterozygous), and 80% of them were the allele PiS. Only one PiSZ (1.25%) individual and no PiZZ was detected. This represents an allelic frequency of 3.1% (PiZ), and 13.1% (PiS). The detected allelic frequencies are higher than previously reported in the Spanish population.
Severe AATD has been excluded in 98.75% of the study population. The Pi*SZ patient has been diagnosed in an early stage of the disease. We have also achieved one of the quality indicators recommended by GesEPOC. Our area has shown a high PiS and PiZ frequency, thus our study could be used as a reference for further research in the Galician population.
La enfermedad pulmonar obstructiva crónica (EPOC) se caracteriza por la presencia de obstrucción crónica no totalmente reversible al flujo aéreo, asociada a una reacción inflamatoria anómala, principalmente frente al humo del tabaco. Se considera que hay obstrucción al flujo aéreo cuando el FEV1/FVC es inferior a 0,7 tras la administración de un broncodilatador1.
La prevalencia de EPOC en adultos de entre 40 a 80 años es del 10,2% en España2, y es causante del 10% de las consultas de atención primaria, el 40% de las consultas en neumología, el 7% de las hospitalizaciones al año y del 35% de las incapacidades laborales permanentes, por lo que el impacto sanitario, social y económico es muy elevado3.
El tabaquismo es el principal factor etiológico de la EPOC. Otros factores como la exposición al humo de biomasa y el déficit de alfa 1 antitripsina (DAAT) también han sido relacionados con su desarrollo1.
El DAAT es una condición genética que predispone al desarrollo de enfisema pulmonar y diversos tipos de hepatopatías en niños y adultos, y con menor frecuencia paniculitis neutrofílica y vasculitis sistémicas4. Se caracteriza por la producción de proteína alfa-1 antitripsina anómala debido a diversas mutaciones genéticas, las más frecuentes PiZ y PiS. La proteína anormal queda, en su mayor parte, retenida en el hígado, pudiendo ocasionar daño hepático, y su ausencia en el órgano diana, el pulmón, favorece la aparición de enfisema. La función principal de la AAT es inhibir la elastasa de los neutrófilos, que a su vez es capaz de digerir la elastina, las membranas basales y otros componentes de la matriz extracelular y, de esta forma, la deficiencia del inhibidor contribuye a la destrucción del parénquima y la aparición de enfisema4.
La condición se transmite por herencia autosómica codominante mediante 2 alelos, uno de cada progenitor. En la práctica clínica el riesgo de presentar enfermedad se limita a los individuos con los genotipos PiZZ y variantes nulas y, en menor grado, PiSZ y otras variantes raras4,5.
En España, la prevalencia de los genotipos deficitarios en la población general para PiZZ es de 1:3.344 (y de 1:278 para PiSZ, lo que significa que habría unos 12.000 sujetos PiZZ y unos 145.000 SZ). En el Noroeste del país (Galicia, Asturias) la prevalencia de PiZZ es de 1:2.500, próxima a la de los países nórdicos de Europa6–8.
Se estima que el DAAT causa el 2-3% de los casos de EPOC y, en concreto, teniendo en cuenta los datos de prevalencia tanto de la EPOC como del DAAT se ha estimado que en España podría haber alrededor de 2.500 adultos con EPOC y DAAT8.
La OMS, y más recientemente la guía GesEPOC1, recomienda la determinación de la alfa 1 antitripsina (AAT) al menos una vez en la vida en los pacientes diagnosticados de EPOC1.
En los pacientes con DAAT el descenso del FEV1 está directamente relacionado con la cantidad de tabaco consumido, que es superior al de los individuos con EPOC no deficitarios y se relaciona con la mortalidad. Así, el DAAT representa no solo una susceptibilidad al desarrollo de enfisema, sino que los individuos con déficit y EPOC tienen una pérdida de función pulmonar más rápida y potencialmente una mortalidad más precoz4,9,10. En concreto, la edad media de fallecimiento en los casos incluidos en el Registro español de déficit alfa 1 antitripsina (REDAAT) es de 59 años11.
El DAAT está infradiagnosticado en todo el mundo12. En nuestro medio el REDAAT tiene registrados en la actualidad únicamente a 632 pacientes (genotipos Pi ZZ, SZ y portadores de variantes raras) lo que representaría <1% de los casos existentes, según los estudios de prevalencia13.
Además, existe un gran retraso en el diagnóstico. En España se estima que hay un retraso de 5 a 10 años entre el diagnóstico de EPOC y en el del DAAT, 6 en Alemania y 7,2 en los EE. UU.; antes de llegar al diagnóstico un 43% de los casos habían consultado a 3 médicos y un 12% a más de 614.
El objetivo de este trabajo fue descartar la existencia del DAAT en la población de pacientes con EPOC en el área sanitaria del CS de Acea da Ma, Culleredo, A Coruña, siguiendo la recomendación de GesEPOC1 y, con ello, calcular la frecuencia alélica de las mutaciones deficitarias más frecuentes.
Pacientes y métodoSe realizó un estudio descriptivo transversal entre marzo y diciembre del año 2014, en el centro de salud Acea da Ma, en Culleredo, A Coruña, con una población adscrita de 28.000 personas de las cuales 14.013 tenían una edad entre los 40 y 80 años y 480 de ellos estaban registrados en el centro con diagnóstico de EPOC, lo que representaría un prevalencia de EPOC del 3,4% en el municipio.
El protocolo del estudio y su consentimiento informado fueron aprobados por el Comité Autonómico de Ética de la Investigación de Galicia con el número 2013/385.
Se incluyeron pacientes entre 40 a 80 años de edad con EPOC documentada por espirometría forzada, con un FEV1/CVF posbroncodilatación<70%, y con una prueba broncodilatadora negativa. Los criterios de exclusión fueron: tener una prueba broncodilatadora positiva, asma, bronquiectasias, neumonía u otras infecciones pulmonares activas, disponer de una determinación de AAT con anterioridad al inicio del estudio, haber participado en el proyecto IDDEA (Información y detección de alfa 1 antitripsina en pacientes con EPOC, estudio nacional de DAAT)15. Para ello, se revisaron las espirometrías realizadas en el centro desde su instauración en 2007 hasta 2014 y se revisaron las historias clínicas para verificar el diagnóstico.
Tras la obtención del consentimiento informado se recogió la muestra de sangre según el protocolo previamente publicado16 y las siguientes variables de cada paciente: datos antropométricos, sociodemográficos, hábito tabáquico, el consumo acumulado de tabaco en paquetes/año, antecedentes de infecciones respiratorias (bronquitis aguda y neumonía) en los últimos 10 años, la exposición laboral de riesgo a polvo y a sustancias químicas, la exposición a combustibles de biomasa, el grado de severidad de la EPOC según el índice Body mass index, airflow obstruction, dysnea and severe exacerbations1; índice de masa corporal, FEV1 posbroncodilatación, escala de disnea modificada de MRC (mMRC) y exacerbaciones graves definidas como aquellas agudizaciones de la EPOC que precisaron el ingreso hospitalario del paciente en el último año.
La recogida de la muestra de sangre se realizó usando los kits que el REDAAT pone a disposición de los médicos a través de su página web (www.redaat.es). Mediante punción del pulpejo del dedo se extrae una gota gruesa con la que se impregna el papel (fig. 1). Una vez recogida la muestra puede enviarse al laboratorio por correo postal.
El procesamiento de las muestras se realizó por el Departamento de Genética Humana del Instituto de Investigación de Enfermedades Raras, Instituto de Salud Carlos III de Madrid, laboratorio de referencia del Registro español de pacientes con déficit de alfa-1 antitripsina.
El estudio de las variantes PI*S y PI*Z del gen SERPINA1 se realizó mediante análisis de curvas de desnaturalización tras amplificación simultánea por PCR de 2 fragmentos con prímers específicos de las regiones a estudiar y sondas fluorescentes para detectar los productos17.
Se realizó análisis de frecuencias de variables y medidas de tendencia central y dispersión.
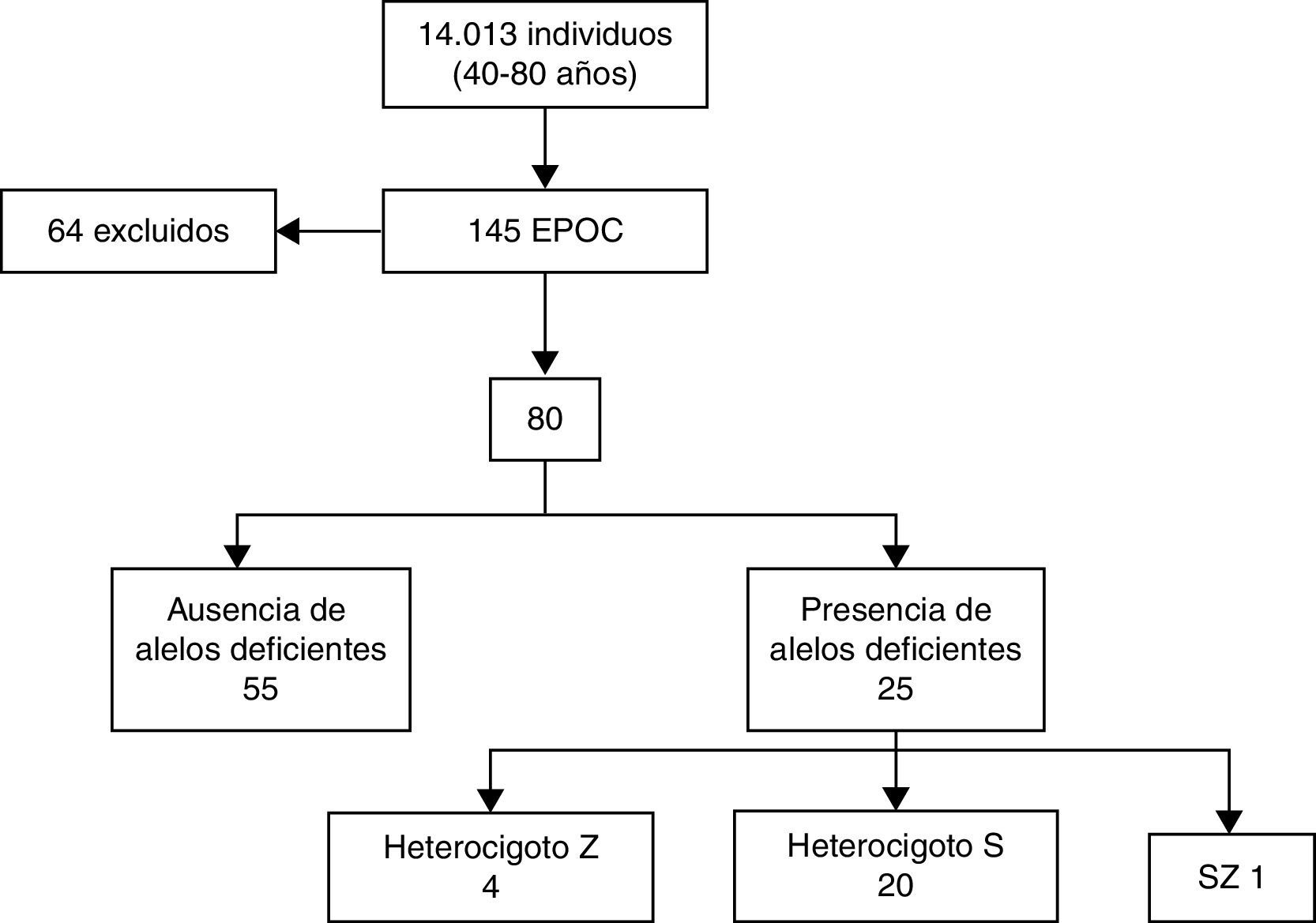
ResultadosUn total de 145 pacientes fueron diagnosticados en el propio centro desde 2007, y constituyeron la población inicial de estudio. En 51 casos (35%) la determinación de AAT se había realizado con anterioridad al inicio de este trabajo, por lo que quedaron excluidos. Catorce (9,7%) pacientes declinaron la invitación a participar, por lo que finalmente se incluyeron 80 pacientes.
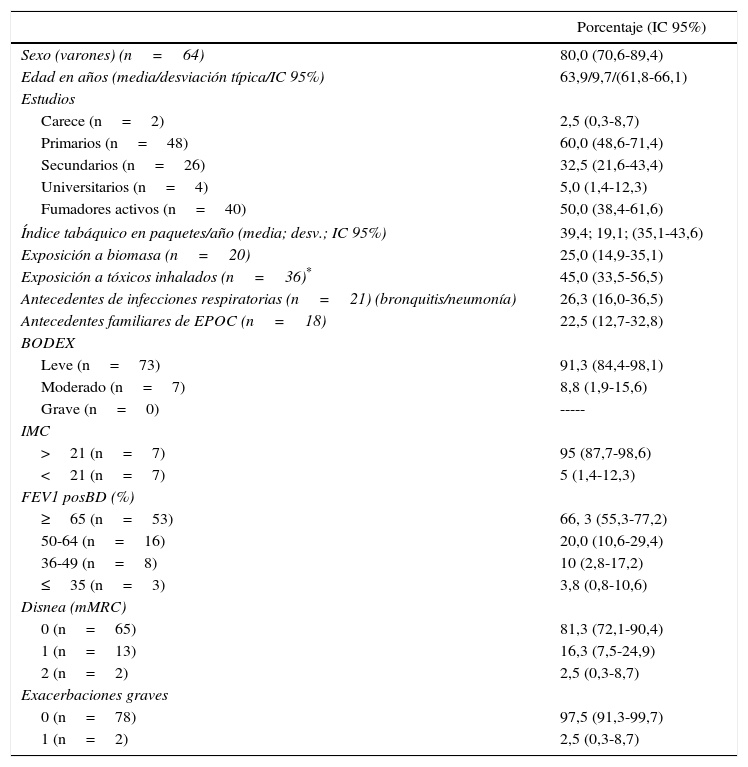
En la tabla 1 se reflejan las variables recogidas.
Variables demográficas y clínicas (porcentajes/medias e intervalos de confianza al 95%)
| Porcentaje (IC 95%) | |
|---|---|
| Sexo (varones) (n=64) | 80,0 (70,6-89,4) |
| Edad en años (media/desviación típica/IC 95%) | 63,9/9,7/(61,8-66,1) |
| Estudios | |
| Carece (n=2) | 2,5 (0,3-8,7) |
| Primarios (n=48) | 60,0 (48,6-71,4) |
| Secundarios (n=26) | 32,5 (21,6-43,4) |
| Universitarios (n=4) | 5,0 (1,4-12,3) |
| Fumadores activos (n=40) | 50,0 (38,4-61,6) |
| Índice tabáquico en paquetes/año (media; desv.; IC 95%) | 39,4; 19,1; (35,1-43,6) |
| Exposición a biomasa (n=20) | 25,0 (14,9-35,1) |
| Exposición a tóxicos inhalados (n=36)* | 45,0 (33,5-56,5) |
| Antecedentes de infecciones respiratorias (n=21) (bronquitis/neumonía) | 26,3 (16,0-36,5) |
| Antecedentes familiares de EPOC (n=18) | 22,5 (12,7-32,8) |
| BODEX | |
| Leve (n=73) | 91,3 (84,4-98,1) |
| Moderado (n=7) | 8,8 (1,9-15,6) |
| Grave (n=0) | ----- |
| IMC | |
| >21 (n=7) | 95 (87,7-98,6) |
| <21 (n=7) | 5 (1,4-12,3) |
| FEV1 posBD (%) | |
| ≥65 (n=53) | 66, 3 (55,3-77,2) |
| 50-64 (n=16) | 20,0 (10,6-29,4) |
| 36-49 (n=8) | 10 (2,8-17,2) |
| ≤35 (n=3) | 3,8 (0,8-10,6) |
| Disnea (mMRC) | |
| 0 (n=65) | 81,3 (72,1-90,4) |
| 1 (n=13) | 16,3 (7,5-24,9) |
| 2 (n=2) | 2,5 (0,3-8,7) |
| Exacerbaciones graves | |
| 0 (n=78) | 97,5 (91,3-99,7) |
| 1 (n=2) | 2,5 (0,3-8,7) |
BODEX: body mass index, airflow obstruction, dysnea and severe exacerbations; FEV1 posBD: flujo espiratorio máximo por segundo posbroncodilatador; mMRC: modified Medical Research Council (escala de disnea modificada).
Se excluyó la presencia de alelos deficitarios en el 68,75% de la población estudiada. Un 30% era portador de un alelo deficitario en heterocigosis, que en el 80% de ellos se trataba del alelo S, que no tiene repercusión clínica. Se detectó un único caso PiSZ (1,25%) y ninguno PiZZ.
Los resultados detallados del estudio genético se encuentran en la figura 2.
Se detectaron 5 alelos Z y 21 alelos S, lo que representa una frecuencia alélica de 3,1% para el PiZ y 13,1% para el PiS.
DiscusiónLos datos presentados en este trabajo se han obtenido de una población pequeña, en un área geográfica concreta, lo que representa una limitación a la hora de compararlos o extrapolarlos a otras poblaciones, aunque resultan de gran valor a nivel local.
Nuestro estudio ha permitido excluir el déficit grave de alfa-1 antitripsina en el 98,75% de los casos. Además, ha mostrado que la incidencia de DAAT en nuestra población de pacientes con EPOC es inferior a lo esperado. Sin embargo, se observa una elevada frecuencia alélica S y Z: ambos resultados son superiores a la frecuencia alélica descrita previamente para la media de poblaciones españolas (PiZ y PiS es del 1,7% y 10,4% respectivamente) y específicamente en otros trabajos realizados por el grupo del REDAAT utilizando una metodología similar (frecuencia para PiZ entre 1,69% y 1,76%)15,17,18.
En el proyecto IDDEA (estudio nacional de detección de déficit AAT) realizado en los años 2008-2009, en el que se reclutaron 596 pacientes de 25 centros de atención primaria (entre ellos el de Culleredo) y en los que se realizó la prueba de la gota seca, se encontraron 2 casos de déficit grave con genotipo PiZZ (0,34%); uno un caso índice y el otro un caso familiar. Un caso de déficit moderado PiSZ (0,17%) y 16 Pi MZ (2,7%), 10 Pi SS, 80 Pi MS y 487 casos con genotipo normal Pi MM. La frecuencia alélica PiZ fue del 1,76%15. Uno de los casos PiZZ y el caso PiSZ procedían de nuestro centro de salud, pero fueron excluidos del presente estudio.
Nuestros hallazgos corroboran que en el Noroeste de España la prevalencia del alelo Z es superior a la de otras regiones de la Península Ibérica y similar a la de los países nórdicos6.
La prevalencia de EPOC en el municipio de Culleredo es del 3,4%, inferior a la calculada en el estudio EPISCAN para la población española, aunque este estudio ya describió importantes diferencias en función del área geográfica. Este resultado podría ser esperable además por el diferente diseño del estudio: los resultados de EPISCAN se obtuvieron a través de un estudio de prevalencia realizado sobre censo poblacional con búsqueda activa, mientras que el presentado aquí se basa en diagnósticos clínicos.
Los pacientes de nuestro estudio, comparado con el estudio EPISCAN, muestran una edad y un consumo de tabaco definido en paquetes/año similar, una mayor distribución porcentual de hombres y un menor porcentaje de estudios universitarios2.
Llama la atención en nuestros resultados la alta exposición a combustibles de biomasa, 20 pacientes (25%) con respecto al estudio On-Sint realizado en Andalucía, Extremadura, Ceuta y Melilla también en atención primaria, en el que en una cohorte de 257 solo 5 (2%) referían tal exposición. Esto se esperaba, hasta cierto punto, por la utilización de la combustión de biomasa en la preparación de alimentos y calefacción en el medio rural gallego. Sin embargo, la exposición a polvo y sustancias químicas profesionales es aún mayor, 36 casos (45%), que la de la biomasa, que se considera segunda causa de EPOC después del tabaco19.
ConclusionesLa realización de este trabajo ha permitido excluir la presencia de déficit grave de AAT en el 98,75% de la población estudiada, sin necesidad de desplazar a los pacientes fuera de nuestro centro de salud dada la facilidad de la recogida de la muestra con el kit de gota desecada. El caso con genotipo Pi*SZ ha sido diagnosticado en una fase precoz de la enfermedad, y puede ser adecuadamente derivado a atención especializada y puede, además, asesorarse a su familia sobre el riesgo de ser portadores de las mutaciones deficitarias. Este diagnóstico precoz permite hacer un esfuerzo especial en la deshabituación tabáquica, en el control temprano de las infecciones respiratorias, la vacunación de la gripe y del neumococo. Con ello, hemos cumplido con uno de los indicadores de calidad asistencial recomendados por GesEPOC1.
Hemos constatado una elevada frecuencia alélica PiS y PiZ en la población de nuestra área, lo que servirá de referencia para futuros estudios más amplios en la población gallega.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLa Dra. Beatriz Lara ha recibido honorarios de diferentes compan¿i¿as farmacéuticas por la realizacio¿n de ponencias cienti¿ficas no relacionadas con este trabajo. Del resto de las autoras no hay conflicto de intereses.
Los autores agradecen la participación de los pacientes y médicos del CS de Acea da Ma en el estudio, la valiosa revisión del doctor Ignacio Blanco, coordinador del Registro español de pacientes con déficit de alfa-1 antitripsina, y el procesamiento de las muestras de los pacientes participantes a las genetistas Beatriz Martínez Delgado y Nerea Matamala.
El trabajo se ha realizado en colaboracio¿n con el Registro espan¿ol de pacientes con déficit de alfa-1 antitripsina (REDAAT), perteneciente a la Fundacio¿n Espan¿ola de Pulmón, SEPAR. Laboratorios Grifols realiza donaciones a dicha Fundacio¿n con el objetivo de apoyar distintas actividades cienti¿ficas del REDAAT.