INTRODUCCIÓN
La demencia es un síndrome caracterizado por un deterioro global de las funciones cognitivas, de carácter orgánico, que origina una desadaptación social del paciente, sin alteración del nivel de conciencia. Es una entidad anatomoclínica, por lo que la historia y la exploración son los elementos indispensables para un correcto diagnóstico1.
CLASIFICACIÓN ETIOLÓGICA DE LAS DEMENCIAS
Existen más de 100 causas descritas, capaces de producir un síndrome de demencia que quedan resumidas en la tabla 1:
1) Las demencias degenerativas primarias se producen por afectación de las células del cerebro, sin una causa bien conocida (intervienen factores genéticos, ambientales, etc.). La más frecuente es la enfermedad de Alzheimer, que supone el 50-70% de todas las demencias. La demencia con cuerpos de Lewy (DCL) representa el 15-20% de ellas, siendo la segunda forma más frecuente de demencia.
2) Las demencias secundarias pueden estar ocasionadas por patologías diversas, entre las que se encuentran las alteraciones vasculares cerebrales que son la causa más frecuente de demencia de este grupo.
3) Las demencias combinadas están provocadas por la combinación de dos o más enfermedades2.
DIAGNÓSTICO
Ante cualquier paciente con sospecha de una posible demencia, se deberá realizar: historia clínica, exploración física (incluyendo exploración neurológica completa) y neuropsicológica, siendo exploraciones complementarias obligadas las siguientes:
1) Analítica de sangre: hemograma, velocidad de sedimentación globular (VSG), glucosa, perfil lipídico y hepático, urea, creatinina, ácido úrico, fosfatasa alcalina, Na, K, Ca, vitamina B12, ácido fólico, hormona estimulante del tiroides (TSH), T4 libre y serología de lúes.
2) Prueba de neuroimagen estructural (tomografía axial computarizada [TAC] o resonancia magnética [RM]).
La realización sistemática de estas pruebas es importante para detectar posibles causas de demencia reversibles2.
CLÍNICA
Los criterios para el diagnóstico clínico de la DCL tal y como han sido definidos por un panel de expertos internacional (Consenso sobre criterios diagnósticos de la demencia con cuerpos de Lewy)3 está conformado jerárquicamente por rasgos centrales, nucleares y sugestivos, a partir de los cuales se concluyen las formas probables y posibles de DCL (tabla 2). El factor determinante es el número de rasgos nucleares presentes: uno solo ya nos coloca en la categoría de posible y dos o más presentes, en la categoría de DCL probable4.
La DCL es menos probable en presencia de infartos cerebrales y otras enfermedades o alteraciones que puedan explicar el cuadro.
Los diagnósticos de demencia por cuerpos de Lewy y enfermedad de Alzheimer no son mutuamente excluyentes; muchos de los pacientes que cumplen criterios para DCL también pueden cumplir los criterios de enfermedad de Alzheimer4,5.
Rasgo central
Un requerimiento esencial para la DCL es la presencia de demencia, un deterioro adquirido y persistente de memoria y de otros dominios cognitivos que interfieren en la función social o laboral. Comparado con la enfermedad de Alzheimer presentan, en general, una mayor afecta-ción de las tareas atencionales, ejecutivas y visuoespaciales.
La demencia en DCL puede corresponder a una demencia cortical (afectación de la memoria, el lenguaje y las
funciones visuoespaciales), subcortical (bradipsiquia, alteraciones de la memoria, dificultades atencionales y de concentración y alteraciones en la capacidad ejecutiva) o ambas.
La presencia de movimientos anormales y de alteraciones neuropsiquiátricas son frecuentes en la DCL.
Características nucleares
Las fluctuaciones en la atención o el nivel de conciencia se consideran como una de las características fundamentales de la DCL. Las fluctuaciones clínicas pueden cursar de diferentes formas, desde períodos de lucidez, a la presencia de descensos importantes en el nivel de conciencia y períodos prolongados de somnolencia diurna.
Los síntomas psicóticos son frecuentemente un rasgo destacado en la DCL; las alucinaciones visuales son experimentadas con una gran sensación de realidad y son las más características. Son alucinaciones bien formadas y recurrentes e incluyen normalmente animales, niños o gente pequeña, aunque pueden incluir también objetos inanimados o percepciones abstractas. Los factores que determinan la necesidad de tratamiento incluyen el grado de "realidad" de las alucinaciones, lo molestas que resultan para el paciente y si intenta actuar sobre ellas. En la enfermedad de Alzheimer es más frecuente la presencia de ideas delirantes, especialmente de tipo paranoide, que las alucinaciones.
Los signos motores parkinsonianos se encuentran presentes en aproximadamente el 80% de los pacientes con DCL, siendo la rigidez y la bradicinesia las manifestaciones parkinsonianas más frecuentes. Pueden también estar presentes: la expresión facial reducida, el temblor de intención o acción, la postura encorvada y la marcha a pequeños pasos. Los signos extrapiramidales responden de forma variable al tratamiento con L-dopa6.
Características sugestivas
Son manifestaciones clínicas que están presentes de forma variable en estos pacientes. Incluyen pérdidas de conciencia no explicadas, episodios sincopales, incontinencia urinaria, alteraciones de la marcha con tendencia a caer, la sensibilidad a neurolépticos y la presencia de ideas delirantes y alucinaciones no visuales.
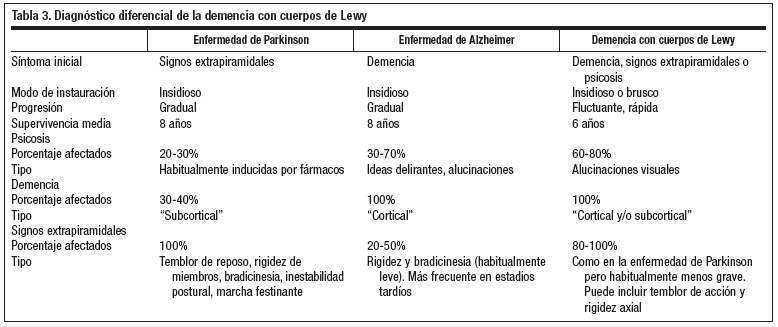
DIAGNÓSTICO DIFERENCIAL
Hay que realizarlo con la enfermedad de Alzheimer y con la enfermedad de Parkinson fundamentalmente (tabla 3).
El mayor problema en el diagnóstico clínico de esta enfermedad es que pueden presentar los mismos signos y síntomas de la enfermedad de Alzheimer pues en la mayoría de los casos estas dos enfermedades coexisten4,7.
La DCL se distingue básicamente de ambas por las formas de presentación variables, las cuales incluyen la presencia de importantes alteraciones neuropsiquiátricas, y por un curso clínico más rápido4,7. En el electroencefalograma (EEG) se objetiva un enlentecimiento generalizado, pudiendo acompañarse de anomalías transitorias en las regiones frontal y temporal.
Hallazgos anatomopatológicos
La DCL se asocia constantemente a la presencia de cuerpos de Lewy en el tronco del encéfalo. El dato anatomopatológico fundamental es la presencia de cuerpos de Lewy corticales, con tendencia a concentrarse en la región frontal y temporal y en áreas paralímbicas (ínsula y circunvolución angular anterior). Las placas de amiloide están presentes con frecuencia y en grado variable en la DCL y los ovillos neurofibrilares ausentes o en una proporción mínima.
TRATAMIENTO DE LA DEMENCIA CON CUERPOS DE LEWY
Tratamiento sintomático y estabilizador
Inhibidores de la acetilcolinesterasa
El sistema neurotransmisor colinérgico junto con la dopamina es uno de los neurotransmisores más afectado en la DCL, por lo que las principales estrategias terapéuticas se encaminan a restaurar la función colinérgica. Sólo los inhibidores de la acetilcolinesterasa (ACE) en estudios a corto plazo (3-6 meses) han demostrado ser eficaces en la mejoría sintomática de estos enfermos. Aunque la respuesta de los pacientes con enfermedad de Alzheimer a este tratamiento es generalmente modesta y variable, se ha sugerido que los pacientes con DCL deberían responder mejor al mismo. Las manifestaciones cardinales neuropsiquiátricas y cognitivas de la DCL (psicosis y déficits atencionales/ejecutivos) están entre los síntomas en la enfermedad de Alzheimer para los que se han obtenido mejor respuesta con este tipo de tratamiento. Los pacientes con DCL son candidatos a beneficiarse de los ACE puesto que tienen un déficit colinérgico mayor que los pacientes con enfermedad de Alzheimer4,6.
Los fármacos comercializados de este grupo son:
Tacrina(Cognex®). Es un inhibidor no selectivo y reversible de la ACE. Ha demostrado una mejoría significativa en los síntomas cognitivos y en las actividades de la vida diaria.
La dosis recomendada de inicio del tratamiento es de 10 mg 4 veces al día durante 6 semanas, con controles de transaminasas semanales. La dosis máxima es de 40 mg 4 veces al día.
El principal efecto secundario es una hepatotoxicidad directa y reversible. Las transaminasas se elevan tres veces por encima de lo normal, en aproximadamente un 30% de los pacientes y vuelven a la normalidad a las 6 semanas tras la supresión del tratamiento8. Este tratamiento sigue en vigencia en la actualidad.
Donepezilo (Aricept®). Es un inhibidor reversible y selectivo de la ACE.
La dosis de inicio es de 5 mg/día, aumentándose a 10 mg/día tras 4-6 semanas de tratamiento. Tiene un metabolismo renal, siendo los efectos secundarios más frecuentes: náuseas, vómitos, diarrea y anorexia y se producen con más frecuencia cuando el aumento de dosis de 5 a 10 mg se realiza en menos tiempo del recomendado9.
Rivastigmina(Exelon®, Prometax®). Es un inhibidor selectivo y pseudorreversible de la ACE, inhibiendo también la butirilcolinesterasa. Tiene un metabolismo hepático.
La dosis de inicio es de 1,5 mg dos veces al día con las comidas, pudiendo aumentarse a 3 mg al día tras 2 semanas con la dosis anterior. Si existe buena tolerancia, se puede administrar 4,5 ó 6 mg dos veces al día tras al menos dos semanas de tratamiento.
Los efectos secundarios más frecuentes son gastrointestinales y ocurren con dosis altas. Otros efectos secundarios son: fatiga, astenia, mareos, somnolencia, sinusitis y dispepsia sobre todo, con dosis de 6-12 mg/día10.
Galantamina(Remynil®). Es un inhibidor de la ACE reversible y selectivo. Tiene una acción moduladora sobre los receptores nicotínicos, favoreciendo la transmisión colinérgica por estimulación presináptica.
La dosis de inicio es de 4 mg dos veces al día. Se debe aumentar a 8 mg dos veces al día tras 4 semanas de tratamiento y posteriormente a 12 mg cada 12 horas. Los distintos ensayos han demostrado eficacia con dosis diarias de 16-24 mg, no con 8 mg/día.
Los efectos adversos más frecuentes son las alteraciones gastrointestinales y ocurren a dosis altas11.
La eficacia de los inhibidores de la ACE es muy similar. Determina la elección de un fármaco u otro, la tolerancia (menos efectos adversos) y la comodidad posológica. Con todos ellos conviene asociar omeprazol al tratamiento, pues tienen como efecto colateral el aumento de la secreción gástrica, lo que aumenta el riesgo de úlcera o sangrado gástrico.
El tratamiento puede mantenerse mientras exista un beneficio terapéutico para el paciente. La observación de una mejoría, por leve que sea, o el retraso en la progresión de la sintomatología es motivo suficiente para mantener el tratamiento siempre que sea bien tolerado por el paciente.
Inhibidor del receptor NMDA de glutamato
En el año 2003 se comercializó un nuevo fármaco inhibidor del receptor N-metilD-aspartato (NMDA) de glutamato: memantina. Está indicado en pacientes con enfermedad de Alzheimer moderadamente grave o grave. En la DCL no estaría indicado porque entre los efectos secundarios más frecuentes se encuentran alucinaciones en un 2% de los casos, con lo que empeoraría la sintomatología de estos pacientes12.
Tratamiento de los síntomas no cognitivos
Los síntomas conductuales en pacientes con DCL pueden agruparse en:
1) Conductas no agresivas: vagabundeo, acciones para llamar la atención, entrometimiento, etc.
2) Conductas agresivas: pegar, empujar, gritar, etc.
Ante la presencia de trastornos del comportamiento en el curso de una demencia lo primero a cuestionarse es la causa de los mismos: problemas orgánicos, efectos secundarios de los fármacos utilizados, etc.
En segundo lugar intentar la aplicación de medidas no farmacológicas dirigidas al paciente y/o a los cuidadores (tranquilizar al enfermo, crear un entorno planificado, ofrecer grupos de ayuda al cuidador, etc.)13,14. Por último y si no hay respuesta a las medidas anteriores, planificar un tratamiento con psicofármacos teniendo en cuenta que: sólo hay datos de eficacia de fármacos sobre agresividad, agitación y síntomas psicóticos y que en los estudios disponibles se ha observado una alta respuesta a placebo.
Si es preciso poner tratamiento farmacológico: iniciar el tratamiento con dosis bajas, realizar incrementos y reducciones de la dosis de forma lenta, evaluar efectos secundarios y mantenerlos el mínimo tiempo posible.
Tratamiento farmacológico de los trastornos del comportamiento
Neurolépticos. Los antipsicóticos son el tratamiento de elección por ser los únicos que han demostrado eficacia en el control de los síntomas psicóticos en la demencia, pero en los pacientes con DCL el uso de neurolépticos debe ser cauteloso. Existen evidencias de que los agentes antipsicóticos atípicos pueden representar un menor riesgo.
La elección del fármaco se basará, por tanto, en el perfil de efectos secundarios.
Por otro lado, en pacientes con demencia los efectos secundarios extrapiramidales por neurolépticos pueden tardar varios meses en desaparecer, pero su persistencia más allá de unas semanas debería hacernos sospechar una DCL.
Los fármacos más utilizados de este grupo son:
1) Haloperidol: no debe utilizarse en estos pacientes con DCL, por los síntomas extrapiramidales asociados al tratamiento que producen15,16.
2) Risperidona (Risperdal®): está autorizado por las autoridades sanitarias para el tratamiento sintomático de episodios graves de agresividad o cuadros psicóticos severos que no respondan a otras medidas, manteniendo el tratamiento durante el menor tiempo posible. Aumenta el riesgo de episodios isquémicos cerebrales (tres veces más frecuente que con placebo) por lo que se debe utilizar, si es necesario, a dosis bajas (0,5-2 mg/día).
3) Olanzapina (Zyprexa®): no está autorizada su indicación en demencias por las autoridades sanitarias.
4) Tioridazina (Meleril®): produce empeoramiento del estado cognitivo, confusión, delirium, etc.
5) Clozapina (Leponex®): tiene un mínimo riesgo de efectos extrapiramidales, por lo que sería de elección en pacientes con DCL con síntomas psicóticos. Exige la rea-lización de recuentos hemáticos periódicos por ser la agranulocitosis su principal efecto secundario. Produce cuadros de hipotensión importante, al igual que la tioridazina17.
Benzodiacepinas. Tienen una alta tasa de efectos secundarios en el anciano: ataxia, confusión, sedación excesiva y reacciones de ansiedad paradójica.
El uso de estos fármacos puede ser útil en pacientes con demencia con síntomas de ansiedad asociados a trastornos de conducta o cuando es preciso controlar el componente ansioso de forma puntual. Son de elección en este caso, las benzodiacepinas (BDZ) de vida media corta (oxazepam, loracepam y alprazolam), a las menores dosis eficaces y durante el menor tiempo posible1,18.
Otros agentes para el tratamiento de la agitación. Existen datos sobre la eficacia de la carbamazepina y el ácido valproico en el tratamiento de la agitación en el paciente con demencia, pero está limitado su uso por los importantes efectos secundarios que tienen (sedación, hepatotoxicidad, alteraciones hematológicas, etc.)19.
La trazodona (Deprax®) a dosis de 50-300 mg ha demostrado también su utilidad. Puede producir hipotensión postural, sedación y sequedad de boca.
Tratamiento de la depresión y de los trastornos del sueño
Es muy frecuente la existencia de síntomas depresivos en el paciente con demencia. Es necesario valorar la gravedad de los síntomas antes de comenzar con el tratamiento farmacológico. Por otra parte, los estudios demuestran que ningún antidepresivo es superior a otro en eficacia, siendo los efectos secundarios los mismos que en pacientes sin demencia. Son de elección los inhibidores selectivos de la recaptación de serotonina (ISRS) a dosis menores que en pacientes sin demencia, por ser mejor tolerados y carecer de acción anticolinérgica20.
Igualmente los trastornos del sueño son frecuentes en la DCL. Es necesario comenzar con tratamiento farmacológico si, tras la instauración de las medidas para una correcta higiene del sueño (regularidad de horarios, evitar siestas diurnas, disminución de la ingesta de líquidos al final del día, etc.) no se obtiene una respuesta adecuada y, si la repercusión de dichos trastornos en el paciente y/o los cuidadores son importantes.
Debido a la hipersensibilidad a neurolépticos que muestran los pacientes con DCL, se deben utilizar BDZ de vida media corta en las alteraciones del sueño puntuales.
El zolpidem en dosis de 5-10 mg antes de acostarse y la trazodona en dosis de 25-100 mg son también útiles para inducir el sueño en estos pacientes21.