La azatioprina (AZA) y la 6-mercaptopurina (6-MP) son los fármacos inmunosupresores de elección en el tratamiento de la enfermedad inflamatoria intestinal. No están exentos de efectos adversos habiéndose comunicado mielotoxicidad en el 7% de los pacientes, que suele aparecer en los primeros meses del tratamiento, aunque se ha comunicado tras tratamientos muy prolongados. La mielotoxicidad suele presentarse sin un motivo clínico detectable, siendo impredecible, aunque en ocasiones puede ser consecuencia de dosis elevadas de los fármacos, niveles bajos de la enzima tiopuril-metiltransferasa (TPMT) o por interacción medicamentosa como en el caso que comunicamos1.
Se presenta el caso de un paciente con enfermedad de Crohn en tratamiento de mantenimiento con AZA que desarrolla mielotoxidad atribuible a la interacción de este fármaco con alopurinol.
Caso clínicoVarón de 73 años, diagnosticado en 1995 de enfermedad de Crohn ileocólica con criterios de corticodependencia que seguía, desde hacía unos 15 años, tratamiento continuo con AZA con dosis de 150mg/día (2,5mg/kg) manteniéndose en remisión clínica, sin efectos adversos al fármaco ni requerir hospitalización ni esteroides.
Consulta en mayo de 2012 por presentar desde hacía 2 semanas astenia progresiva. No refería fiebre, dolor abdominal ni otros síntomas relevantes. En la analítica destacaba: hemoglobina 10,4g/dl y leucocitos 2.000/mm3, con cifra normal de plaquetas 143.000/mm3 y de proteína C reactiva 0,9mg/l. Refería haber iniciado hacía 4 semanas tratamiento con alopurinol, 300mg/día, por hiperuricemia. Las cifras de leucocitos y de hemoglobina, antes de iniciar el tratamiento con estos fármacos, eran respectivamente de 4.300/mm3 y de 12,7g/dl. Se establece el diagnóstico de mielodepresión, inducido por la interacción entre alopurinol y AZA, y se suspende el tratamiento con estos fármacos. La anemia y la leucopenia empeoró en los días sucesivos con cifras de 7,9g/dl de hemoglobina y 1.300 leucocitos/mm3 y se indicó tratamiento con factor estimulante de colonias durante 4 días, y transfusión de 2 concentrados de hematíes. Los niveles de la TPMT eran de 47 U/ml. La analítica al alta hospitalaria mostraba: 6.300 leucocitos/mm3 y 10,1g/dl de hemoglobina. El tratamiento con AZA se reintrodujo al mes del alta hospitalaria sin repercusión clínico-analítica.
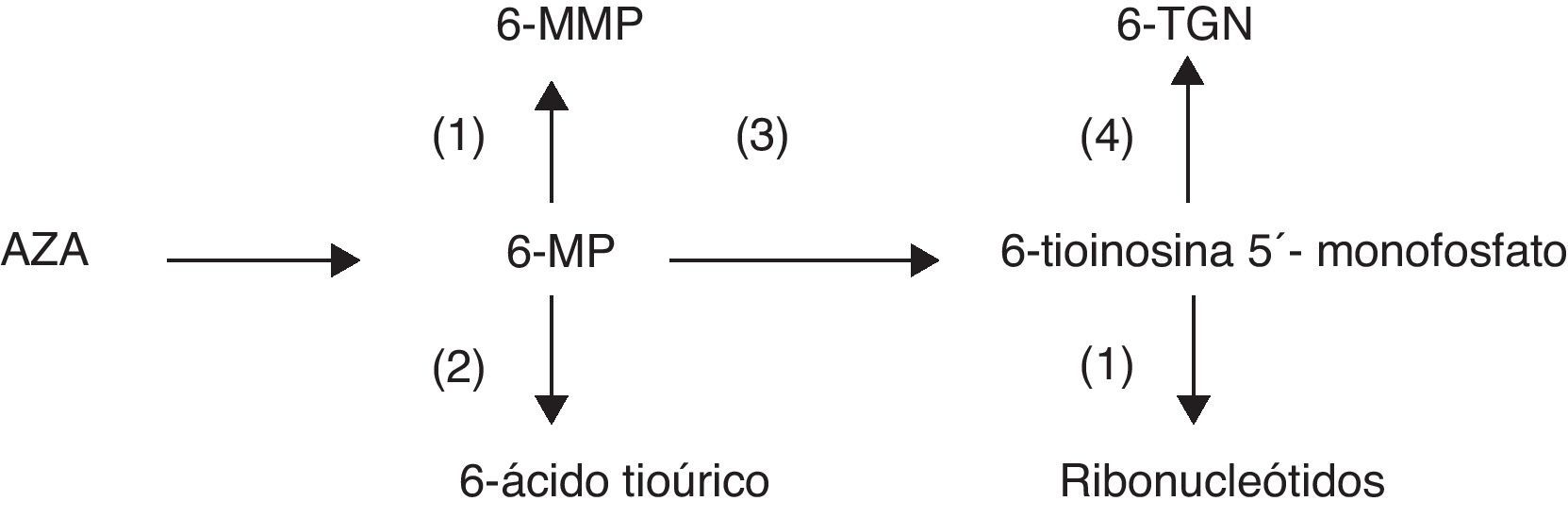
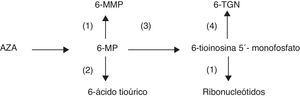
DiscusiónAzatioprina y 6-MP son fármacos, análogos de las purinas, que para ser activos requieren la participación de varios sistemas enzimáticos. Los metabolitos activos responsables de la eficacia del fármaco y también de la mielotoxicidad son los 6-tioguanina nucleótidos (6-TGN) (fig. 1). Niveles muy elevados de 6-TGN se relacionan con un mayor riesgo de toxicidad mientras que niveles bajos se relacionan con una baja eficacia del fármaco.
El alopurinol es un inhibidor de la xantina oxidasa, enzima que metaboliza la 6-MP trasformándola en el 6-ácido tioúrico, metabolito inactivo, y puede favorecer indirectamente un incremento de los niveles de 6-TGN. No es descartable que el alopurinol pueda actuar a otros niveles, inhibiendo incluso la TPMT, favoreciendo también por este mecanismo la elevación y disminución respectivamente de los niveles de 6-TNG y de 6-metilmercaptopurina, metabolito implicado en la hepatotoxicidad de las tiopurinas2–4. Deberíamos evitar, dentro de lo posible, el tratamiento simultáneo con alopurinol y AZA o 6-MP y cuando esto no es posible se recomienda que se reduzca incluso a la cuarta parte la dosis habitual de estos últimos fármacos, y que el paciente reciba una estrecha monitorización analítica.
Algunos autores valoran los potenciales efectos beneficiosos de esta interacción al favorecer que la eficacia de la AZA se incremente o se obtenga con menores dosis de las habituales, favoreciendo la tolerancia gastrointestinal y disminuyendo el riesgo de hepatotoxicidad5–8. El caso que presentamos es una clara demostración de mielotoxicidad por la interacción entre el alopurinol y AZA, condicionada por no reducirse la dosis de este último fármaco. La mielotoxicidad por interacción de estos fármacos es un efecto adverso teóricamente muy conocido pero que probablemente convenga recordar a los especialistas, bien gastroenterólogos, reumatólogos o médicos de atención primaria responsables del tratamiento de pacientes con enfermedad inflamatoria intestinal.