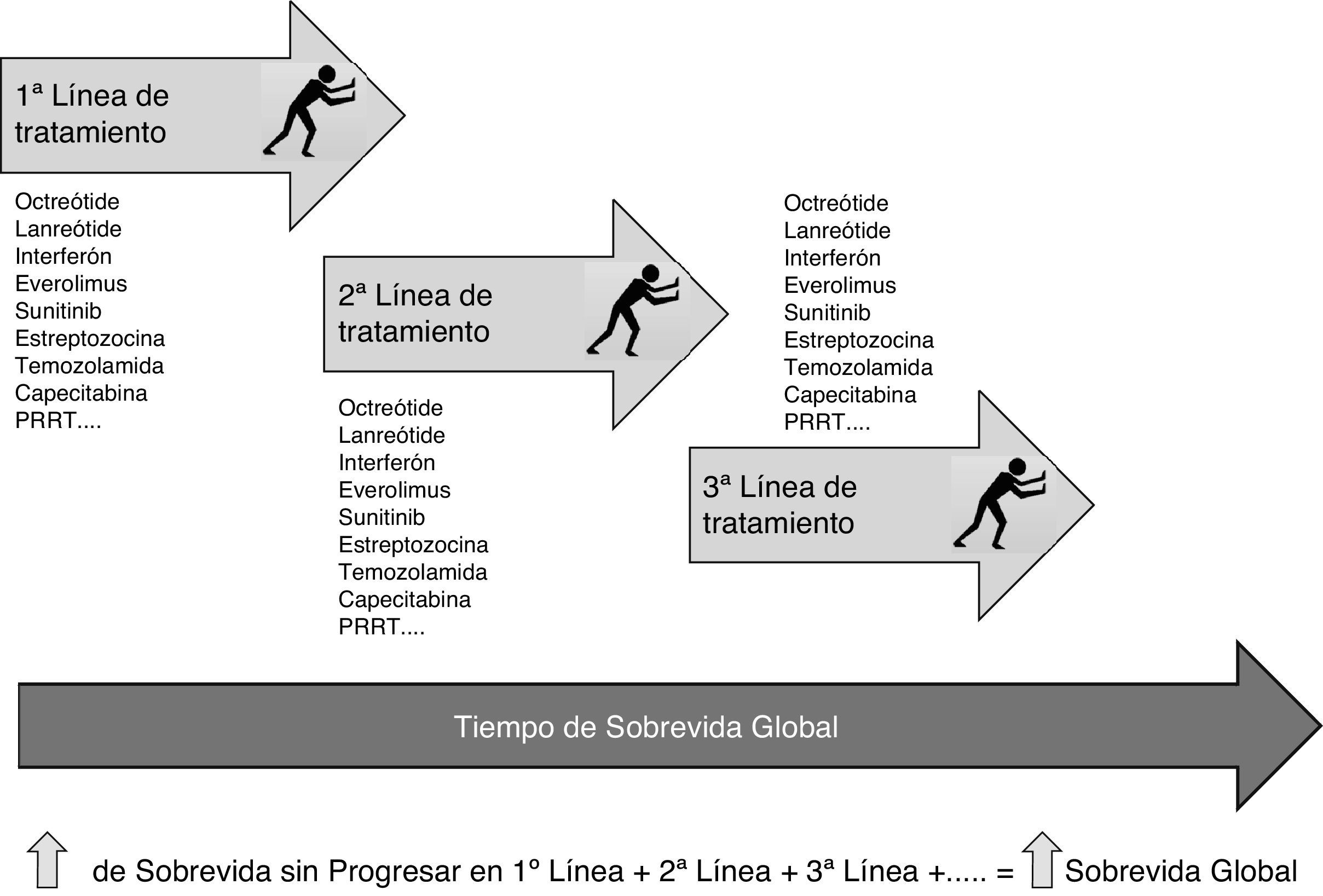
El tratamiento secuencial con distintas opciones sistémicas es algo que se realiza con elevada frecuencia en los tumores sólidos diseminados. Por ejemplo, para el cáncer de mama avanzado disponemos de al menos 9 opciones distintas aprobadas para su empleo de una manera secuencial. Con el empleo de subsecuentes líneas de tratamiento lo que pretendemos conseguir es aumentar los periodos de tiempo en los que el tumor no progresa a la par que mantenemos en la mayoría de los casos una calidad de vida aceptable o al menos retrasamos el deterioro en la calidad de vida inducido por el avance de la enfermedad. El resultado final de la terapéutica secuencial impacta directamente en la supervivencia global de los pacientes resultante de la suma de los sucesivos retrasos en el tiempo a la progresión a lo largo de las distintas líneas de tratamiento (fig. 1).
Para el manejo sistémico de los tumores neuroendocrinos de grado 1 y 2 de diferenciación contamos con la aprobación de los análogos de la somatostatina (octreótido y lancreótido), de interferón alfa, así como de sunitinib y everolimus pero en este caso ceñido a los tumores de origen pancreático. La única quimioterapia que cuenta con la aprobación por parte de las principales agencias reguladoras es la estreptozocina en combinación con 5-fluorouracilo y/o doxorrubicina. Los estudios que han facilitado la aprobación de estos fármacos han incluido a pacientes muy heterogéneos respecto a la carga de enfermedad, grado de diferenciación, tratamientos sistémicos y locorregionales previos y parámetros de evaluación de las respuestas1.
Aunque no se encuentran oficialmente aprobados, en los últimos años se ha extendido el uso, en mayor o en menor medida, en la práctica clínica habitual de otros agentes como la temozolamida, la capecitabina o incluso irinotecan con 5-fluorouracilo. En países y en centros seleccionados es del mismo modo habitual el empleo de radionúclidos como el lutecio marcado como tratamiento sistémico1.
Desafortunadamente, pocos son los datos prospectivos y aleatorizados de los que disponemos acerca de la eficacia de un tratamiento tras el empleo de otros. En un análisis retrospectivo de los datos del estudio RADIANT-3 que dio la aprobación a everolimus en pacientes con tumores neuroendocrinos de páncreas, se objetivó que la mediana de supervivencia libre de progresión en el subgrupo de pacientes tratados previamente con quimioterapia fue superior en el brazo de everolimus que en el brazo de placebo (11 vs. 3.2 meses; hazard ratio, 0.34; intervalo de confianza del 95% [IC95%]: 0.25-0.48; p<0.0001)2. Resultados similares se encontraron en los datos de este mismo estudio de acuerdo a los pacientes que habían recibido previamente tratamiento con análogos de la somatostatina (0.40: IC95%: 0.28-0.57)2.
Aunque con un mecanismo de acción distinto, los datos del estudio de registro de sunitinib muestran una eficacia comparable en términos de supervivencia libre de progresión a los de everolimus en el estudio de registro tanto en los pacientes que habían recibido una terapia sistémica previa (0.33: IC95%: 0.19-0.59) como en los que habían recibido tratamiento con análogos de somatostatina (0.43: IC95%: 0.21-0.89)3. Del mismo modo, y aunque no alcanzó una significación estadística, los pacientes que previamente habían recibido más de 2 líneas de tratamiento sistémico también se beneficiaron del empleo de sunitinib frente a placebo (0.61: IC95% 0.27-1.37)3.
Hasta el momento, no conocemos de la existencia de datos prospectivos que apoyen el uso de sunitinib o de everolimus tras el fracaso del otro. Del mismo modo, tampoco se dispone de evidencia clara en sentido estricto para el empleo de quimioterapia o de análogos de la somatostatina tras el fracaso de alguno de estos nuevos agentes aunque se haga de manera rutinaria en la consulta diaria. El hecho de que sunitinib y everolimus hayan mostrado actividad tras el fracaso a análogos de la somatostatina y/o quimioterapia no significa que necesariamente los debamos emplear en la clínica como «tercera línea» de tratamiento. De hecho, el nivel de evidencia de ambas terapias dirigidas es al menos el mismo si no superior al que puedan disponer los análogos y, sobre todo, al de la quimioterapia.
El Grupo Español de Tumores Neuroendocrinos (GETNE) llevó a cabo un estudio fase ii prospectivo y exploratorio de la actividad de pazopanib, un agente inhibidor de múltiples cinasas relacionadas con la angiogénesis, en pacientes con tumores neuroendocrinos, en la mayoría de los cuales había fracasado al tratamiento previo con everolimus y/o sunitinib (Estudio PAZONET)4. Se reclutaron un total de 44 pacientes, de los cuales 11 (25%) recibieron everolimus previamente, 16 (36.4%) sunitinib y 8 (18.2%) recibieron ambos agentes. La mediana de supervivencia libre de progresión que se alcanzó con pazopanib fue de 9.5 meses (IC95%: 4.8-14.1) en el total de la población del estudio. Sin embargo, la mediana de supervivencia libre de progresión en el subgrupo de pacientes que habían recibido sunitinib o everolimus previamente fue de 12.4 meses (IC95%: 11.3-13.5) y 6.8 meses (IC95%: 0.0-15.3) respectivamente. El tiempo hasta la progresión de la enfermedad fue mucho más inferior cuando pazopanib se ofreció a pacientes que habían sido tratados con las 2 alternativas sistémicas previamente (4 meses: IC95%: 1.3-6.8). De una manera muy significativa, aquellos pacientes que dentro del estudio recibieron pazopanib en combinación con análogos de la somatostatina presentaron una mayor eficacia respecto a aquellos pacientes que recibieron pazopanib como agente único (11.7 meses, IC95%: 9.7-13.7 vs. 4.2 meses, IC95%: 3.3-5.1; p=0.043). Este dato abre la puerta a la posible sinergia existente entre los nuevos agentes antidiana con los análogos de la somatostatina4.
Cómo vamos a poder ordenar de la manera más efectiva las distintas opciones de tratamiento sistémico de las que disponemos para el tratamiento de los tumores neuroendocrinos avanzados para alcanzar la mayor sobrevida global posible preservando al máximo la calidad de vida de los pacientes es nuestro reto en el mundo de los tumores neuroendocrinos. La falta de biomarcadores moleculares existente en este campo que nos ayude a predecir la eficacia de uno u otro tratamiento tampoco nos ayuda en este sentido. Asimismo, y por suerte, nuevos fármacos se van a incorporar próximamente a nuestro armamento tales como los radionúclidos encabezados por lutecio (Lutathera®) como los nuevos inhibidores de la síntesis de la serotonina como telotristat etiprato (Xermelo®) que permitirán un mejor control de los síntomas carcinoides en pacientes refractarios a los análogos de la somatostatina.
Este aumento en la complejidad de los tratamientos disponibles hace muy improbable el desarrollo de ensayos clínicos para evaluar la actividad de las distintas secuencias de tratamiento posible5. El estudio SEQTOR, que actualmente se encuentra reclutando pacientes y que se lleva a cabo entre una colaboración del grupo GETNE con la Sociedad Europea de Tumores Neuroendocrinos (ENETS), es el único que de manera prospectiva y aleatorizada pretende comparar la eficacia de everolimus seguido de quimioterapia basada en estreptozocina frente a la secuencia inversa en pacientes con tumores neuroendocrinos de páncreas (NCT02246127). Por su parte, el grupo GETNE está llevando a cabo un estudio fase ii (PALBONET) de brazo único en el que palbociclib, un inhibidor de las ciclinas cinasas del ciclo celular (CDK4 y 6), se ofrece como agente único en el tratamiento de pacientes con tumores neuroendocrinos de páncreas en los que ha fracasado el tratamiento previo con al menos una de las nuevas dianas.
Actualmente, y para ser prácticos, solemos emplear los criterios clínicos clásicos tales como la funcionalidad o no de los tumores, la presencia de síntomas debidos a la carga tumoral, la tasa de crecimiento de los tumores, el grado de proliferación en términos del índice ki67, el grado histológico de diferenciación, las comorbilidades, etc… para customizar nuestro tratamiento de los pacientes con tumores neuroendocrinos.5 Tras la progresión a una primera línea, debemos realizar de nuevo el mismo esfuerzo teniendo en cuenta todos esos parámetros otra vez. No disponemos de una secuenciación de distintos agentes que haya demostrado ser superior a otras. Del mismo modo que no hay un tratamiento sistémico que haya demostrado ser superior a otros ya que en todos los estudios de registro de los que disponemos los fármacos activos se han comparado frente a placebo con el mejor tratamiento de soporte. Se requiere, por tanto, un mayor nivel de evidencia línea tras línea de nuestros tratamientos. Asimismo, los datos muestran una actividad sinérgica de los distintos agentes en combinación con los análogos de la somatostatina, pero no sabemos si esta sinergia sería superior en cuanto al tiempo total del control del crecimiento tumoral respecto al que conseguiríamos con la secuenciación de los distintos agentes. Probablemente, los avances en el conocimiento de la biología molecular de estos tumores se puedan trasladar más pronto que tarde al manejo sistémico secuencial de nuestros pacientes5.
Conflicto de interesesE.G. ha servido como asesor y ha recibido honorarios por ponencias de Pfizer, Novartis, IPSEN y Lexicon. EG ha recibido becas educacionales para investigación en tumores neuroendocrinos de Pfizer, Merck-Serono y GSK.