La introducción de nuevos fármacos para el tratamiento de los pacientes con cáncer gástrico irresecable, recurrente o metastásico ha reportado un modesto incremento en la supervivencia libre de progresión (SLP) y la supervivencia global (SG).
ObjetivoDeterminar el impacto de la aplicación de los nuevos esquemas de quimioterapia paliativa en la SG de los pacientes con cáncer gástrico del Centro Médico Nacional 20 de noviembre, ISSSTE.
Material y métodosEstudio retrospectivo, descriptivo. Analizamos expedientes de pacientes con cáncer gástrico irresecable o metastásico, tratados con quimioterapia paliativa de enero de 2002 a diciembre de 2012 en el Centro Médico Nacional 20 de noviembre, ISSSTE. Se evaluó la SG, SLP y los esquemas de quimioterapia más frecuentemente utilizados. Se asignaron los casos a 2 cohortes de acuerdo a la fecha de inicio de la quimioterapia, conformando la cohorte A los pacientes tratados de enero de 2002 hasta diciembre de 2006 y la cohorte B de enero de 2007 a diciembre de 2012. Se estableció estos periodos dado que representaba el cambio en los esquemas de tratamiento utilizados; es decir; la introducción de esquemas que incluyen antraciclinas, oxaliplatino, capecitabina y docetaxel.
ResultadosRevisamos los expedientes de 291 pacientes con cáncer gástrico; excluimos a 221 pacientes por estar en etapas tempranas (i, ii o iii) resecables, recibir tratamiento con quimioterapia fuera de la unidad o no ser candidatos a quimioterapia. Finalmente incluimos 70 casos con tratamiento de primera línea. La mediana de SG para pacientes de la cohorte A fue de 11.2 vs. 10.5 meses para los pacientes de la cohorte B. La mediana de SLP en primera línea de tratamiento fue 8.5 vs. 5.2 meses respectivamente. Ambos resultados sin diferencia estadísticamente significativa.
ConclusiónEn nuestro centro, no hay impacto de los nuevos esquemas de tratamiento en SLP o SG. Un tamaño de muestra pequeño y el hecho de que pacientes con pobre estado funcional recibieran quimioterapia podrían ser factores que influyeron en los resultados del estudio, en el cual se observó una tendencia a favor de los nuevos esquemas de quimioterapia, pero sin demostrar significación estadística.
The introduction of new drugs for the treatment of patients with advanced, recurrent or metastatic gastric cancer has resulted in a small benefit in overall survival (OS) and progression free survival (PFS).
ObjectiveTo determine the impact of new chemotherapy schedules on the OS of patients with advanced or metastic gastric cancer treated at the Centro Medico Nacional 20 de noviembre, ISSSTE.
Material and methodologyRetrolective, descriptive study, the clinical files of patients with advanced, recurrent or metastatic gastric cancer treated with chemotherapy at the Centro Medico Nacional 20 de noviembre, ISSSTE, from january 2002 to december 2012, were analyzed. Chemotherapy schedules, OS and PFS were evaluated. Patients were assigned to two cohorts: those treated from january 2002 to december 2006 were included in cohort A and those treated from january 2007 to december 2012 in cohort B. These time periods were determined based on the years when newer chemotherapy agents (anthracyclines, oxaliplatin, capecitabine and docetaxel) were introduced in our institution.
Results291 clinical files were analyzed; 221 patients were excluded for they had clinical stage I, II or resectable III disease, started first line chemotherapy as outpatients of our institution or were not candidates for chemotherapy. 70 cases treated with first line chemotherapy were included. OS for patients in cohort A was 11.2 months vs 10.5 months for patients in cohort B. PFS was 8.5 months vs 5.2, respectively. There was no statistical difference in either comparison.
ConclusionThere was no impact of the introduction of newer chemotherapy agents in OS or PFS in patients treated in our institution. A small sample size and the fact that patients with poor performance status received chemotherapy could have had influenced the results of our study, in which tendency towards a better outcome for patients treated with newer chemotherapy schemes was observed, although a statistically significant benefit was not proven.
El cáncer gástrico es una neoplasia maligna con un importante significado por su incidencia y la mortalidad que conlleva. Se diagnosticaron cerca de un millón de casos nuevos de cáncer gástrico en 2008 (988,000 casos, un 7.8% del total de casos de cáncer), ocupando el cuarto lugar en incidencia y el segundo en mortalidad por neoplasias malignas en el mundo (736,000 muertes, un 9.7% del total de muertes por cáncer). En México, la incidencia estimada es de 7.9/100,000 habitantes (7,859 casos) y la mortalidad de 6.7/100,000 habitantes (6,751 muertes)1.
En la década de los noventa el estándar de tratamiento lo constituía el esquema 5fluorouracilo, adriamicina y metotrexate (denominado FAMtx), que demostró superioridad respecto al tratamiento utilizado en ese momento (5fluorouracilo, adriamicina y mitomicina C [FAM]) con impacto en supervivencia global2. A partir del año 2000, la introducción de nuevos fármacos como los compuestos platinados (cisplatino y oxaliplatino) e irinotecan ha reportado incremento de la supervivencia libre de progresión (SLP) y de la supervivencia global (SG) en estos pacientes3. La SLP con los diferentes esquemas alcanza 5-7 meses y la SG 8.5-11.2 meses, con tasas de respuesta favorable que no superan el 50% de los pacientes4.
La pobre SG asociada al cáncer gástrico en nuestro país está relacionada con el diagnóstico en etapa iv hasta en el 65% de los pacientes5. Se ha demostrado prolongación significativa de la SG con el empleo de terapia combinada, contra monoterapia en pacientes con cáncer gástrico metastásico6.
A pesar de los esfuerzos, los resultados de estos esquemas de tratamiento, con pobre a moderada tasa de respuesta y corta SLP, no han logrado establecer un estándar de tratamiento en la enfermedad metastásica o irresecable.
Se realizó este estudio en donde se evalúa el impacto de la implementación de los diferentes esquemas de quimioterapia en términos de SG de los pacientes con cáncer gástrico metastásico, recurrente o irresecable, tratados en nuestro centro en los últimos 10 años.
Material y métodosEstudio retrospectivo, descriptivo, observacional. Se analizaron los expedientes de 291 pacientes con cáncer gástrico avanzado, irresecable o metastásico, tratados con quimioterapia paliativa de enero de 2002 a diciembre de 2012. Se evaluó la SG, la SLP, esquemas de quimioterapia más frecuentemente utilizados, así como las características de los pacientes que tuvieran un impacto en estos parámetros.
Se incluyeron expedientes de pacientes de ambos sexos, mayores de 18 años, con diagnóstico de adenocarcinoma gástrico avanzado o metastásico con confirmación histopatológica de adenocarcinoma gástrico o de la unión gastroesofágica, que recibieron al menos un ciclo de quimioterapia en esta unidad con objetivo paliativo, y que contaran con expediente físico y electrónico en esta unidad.
Se excluyeron aquellos casos con segundas neoplasias y tratamiento previo con quimioterapia para enfermedad metastásica fuera de la unidad.Se eliminaron del estudio los casos con expediente incompleto o no disponible por cualquier causa.
Se compararon los pacientes en 2 cohortes de acuerdo a la fecha de inicio de la quimioterapia: de enero de 2002 a diciembre de 2006 (cohorte A), y de enero de 2007 a diciembre de 2012 (cohorte B); se establecieron estos periodos dado que representan un cambio en los esquemas de tratamiento utilizados; es decir la introducción de esquemas que incluyen antraciclinas, oxaliplatino, capecitabina y docetaxel.
Una vez seleccionados los pacientes; se analizó la SG en cada una de las cohortes. Determinamos también la SLP, los esquemas de tratamiento más frecuentemente utilizados y el promedio de líneas de tratamiento utilizadas.
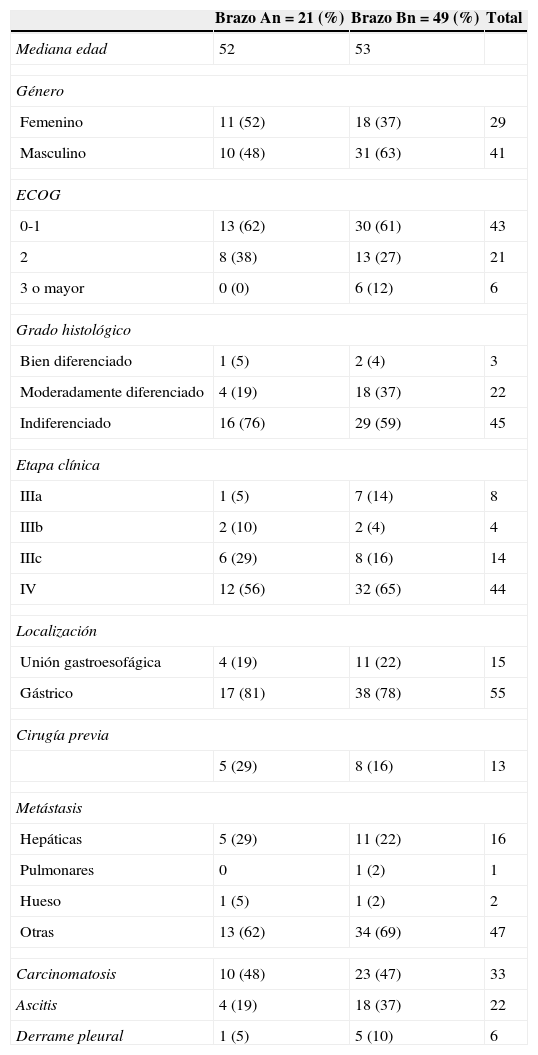
ResultadosSe revisaron los expedientes de 291 pacientes con cáncer gástrico, se excluyeron 164 casos con cáncer gástrico en etapas i y ii; así como etapas iii que fueron resecadas, 21 que no recibieron quimioterapia por decisión del paciente o por no ser candidatos por las comorbilidades; 4 por tener segundas neoplasias, 10 que iniciaron su tratamiento fuera de la unidad, 15 que no contaban con expediente completo en la unidad, 4 con tumores del estroma gastrointestinal y 3 más con tumores neuroendocrinos. Se analizaron finalmente los casos de 70 pacientes, con el programa estadístico SPSS versión 21.0. Las características de los casos incluidos se describen en la tabla 1.
Características de los pacientes
| Brazo An=21 (%) | Brazo Bn=49 (%) | Total | |
|---|---|---|---|
| Mediana edad | 52 | 53 | |
| Género | |||
| Femenino | 11 (52) | 18 (37) | 29 |
| Masculino | 10 (48) | 31 (63) | 41 |
| ECOG | |||
| 0-1 | 13 (62) | 30 (61) | 43 |
| 2 | 8 (38) | 13 (27) | 21 |
| 3 o mayor | 0 (0) | 6 (12) | 6 |
| Grado histológico | |||
| Bien diferenciado | 1 (5) | 2 (4) | 3 |
| Moderadamente diferenciado | 4 (19) | 18 (37) | 22 |
| Indiferenciado | 16 (76) | 29 (59) | 45 |
| Etapa clínica | |||
| IIIa | 1 (5) | 7 (14) | 8 |
| IIIb | 2 (10) | 2 (4) | 4 |
| IIIc | 6 (29) | 8 (16) | 14 |
| IV | 12 (56) | 32 (65) | 44 |
| Localización | |||
| Unión gastroesofágica | 4 (19) | 11 (22) | 15 |
| Gástrico | 17 (81) | 38 (78) | 55 |
| Cirugía previa | |||
| 5 (29) | 8 (16) | 13 | |
| Metástasis | |||
| Hepáticas | 5 (29) | 11 (22) | 16 |
| Pulmonares | 0 | 1 (2) | 1 |
| Hueso | 1 (5) | 1 (2) | 2 |
| Otras | 13 (62) | 34 (69) | 47 |
| Carcinomatosis | 10 (48) | 23 (47) | 33 |
| Ascitis | 4 (19) | 18 (37) | 22 |
| Derrame pleural | 1 (5) | 5 (10) | 6 |
La mediana de SG para pacientes del brazo A fue de 11.2 vs. 10.5 meses para los pacientes del brazo B. La mediana de SLP en primera línea de tratamiento fue 8.5 vs. 5.2 meses respectivamente. Ambos resultados sin diferencia estadísticamente significativa.
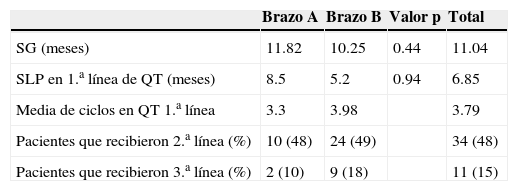
Analizamos también la mediana de ciclos recibidos en primera línea de tratamiento en cada una de las cohortes: 3.3 ciclos para los pacientes tratados en el 2006 o antes, y 3.98 para los tratados en el 2007 o después. El porcentaje de pacientes que recibieron segundas líneas de tratamiento fue similar en ambas cohortes (el 48% del total), mientras que solo el 15% del total de pacientes estuvieron en condiciones de recibir una tercera línea de tratamiento (tabla 2).
Resultados
| Brazo A | Brazo B | Valor p | Total | |
|---|---|---|---|---|
| SG (meses) | 11.82 | 10.25 | 0.44 | 11.04 |
| SLP en 1.a línea de QT (meses) | 8.5 | 5.2 | 0.94 | 6.85 |
| Media de ciclos en QT 1.a línea | 3.3 | 3.98 | 3.79 | |
| Pacientes que recibieron 2.a línea (%) | 10 (48) | 24 (49) | 34 (48) | |
| Pacientes que recibieron 3.a línea (%) | 2 (10) | 9 (18) | 11 (15) |
QT: quimioterapia; SG: supervivencia global; SLP: supervivencia libre de progresión.
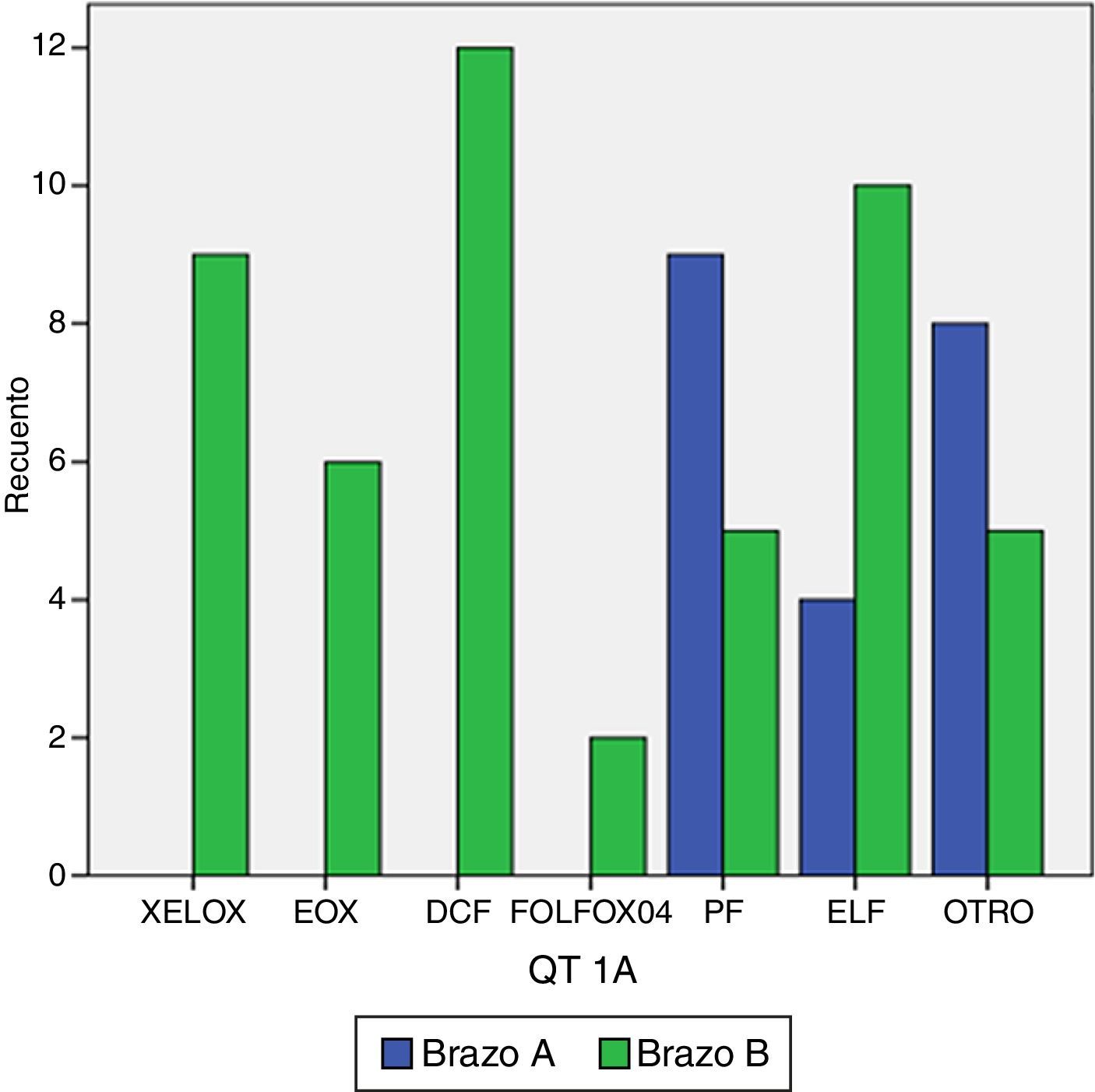
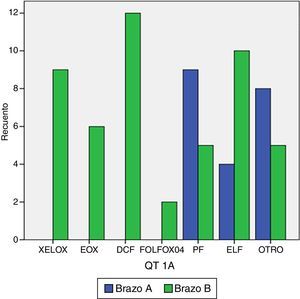
Los esquemas más frecuentemente utilizados en primera línea de tratamiento se describen en la figura 1.
Esquemas de quimioterapia utilizados en primera línea de tratamiento. DCF: docetaxel-cisplatino-5fluorouracilo; ELF: etopósido-leucovorin-5fluorouracilo; EOX: epirrubicina-oxaliplatino-capecitabina; FOLFOX04: 5fluorouracilo-leucovorin-oxaliplatino; PF: cisplatino-5fluorouracilo; XELOX: capecitabina-oxaliplatino. Otros esquemas incluyeron monofármacos como capecitabina, docetaxel, irinotecan, 5flurouracilo-leucovorin. En azul el brazo A y verde el brazo B.
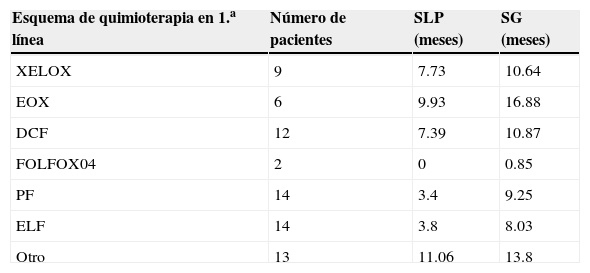
Describimos las medias de SLP y SG de acuerdo a cada esquema de tratamiento destacando mejores resultados con capecitabina-oxaliplatino, epirrubicina-oxaliplatino-capecitabina, docetaxel-cisplatino-5fluorouracilo, las cuales se detallan en la tabla 3.
Supervivencia global y supervivencia libre de progresión de acuerdo al esquema de quimioterapia en 1.a línea
| Esquema de quimioterapia en 1.a línea | Número de pacientes | SLP (meses) | SG (meses) |
|---|---|---|---|
| XELOX | 9 | 7.73 | 10.64 |
| EOX | 6 | 9.93 | 16.88 |
| DCF | 12 | 7.39 | 10.87 |
| FOLFOX04 | 2 | 0 | 0.85 |
| PF | 14 | 3.4 | 9.25 |
| ELF | 14 | 3.8 | 8.03 |
| Otro | 13 | 11.06 | 13.8 |
DCF: docetaxel-cisplatino-5fluorouracilo; ELF: etopósido-leucovorin-5fluorouracilo; EOX: epirrubicina-oxaliplatino-capecitabina; FOLFOX04: 5fluorouracilo-leucovorin-oxaliplatino; PF: cisplatino-5fluorouracilo; SG: supervivencia global; SLP: supervivencia libre de progresión; XELOX: capecitabina-oxaliplatino.
Se compararon los resultados obtenidos en primera línea de tratamiento para esquemas basados en compuestos platinados con los tratados con esquemas que no los contienen, con SG similar en ambos grupos (tabla 4).
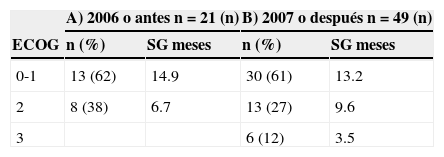
Analizamos también la SG con respecto al estado funcional de ECOG en cada una de las cohortes (tabla 5). Observamos que el porcentaje de pacientes con estado funcional 0-1 fue similar en ambas cohortes. No se incluyeron pacientes con ECOG 3 en la cohorte A.
La SLP de acuerdo a los esquemas de tratamiento nuevos fue 7.38 vs. 5.93 meses para tratamientos previos. La SG 10.14 (nuevos) vs. 10.35 meses (previos). Calculamos también la SG a un año para el brazo A 23.8 vs. 32% para el brazo B.
DiscusiónLa adición de nuevos fármacos al tratamiento del cáncer gástrico recurrente o metastásico ha mostrado un modesto incremento de la SG (disminución del riesgo de mortalidad) de acuerdo a un metaanálisis publicado por el GASTRIC group3.
En nuestro centro, la SG de los pacientes no muestra diferencias en las 2 cohortes estudiadas; alcanzando resultados similares a lo reportado en los estudios a nivel internacional4. Cabe destacar que los pacientes incluidos en los estudios referidos son pacientes seleccionados, mientras que los casos incluidos en el presente estudio pertenecen a la población general de pacientes atendidos en nuestro servicio.
Los esquemas de quimioterapia utilizados en primera línea de tratamiento fueron numerosos; todos incluyen fluoropirimidinas combinadas o no con análogos del platino. Antes de 2007, la mayoría de los pacientes fueron tratados con etopósido-leucovorin-5fluorouracilo, y cisplatino-5fluorouracilo y aquellos pacientes que por las comorbilidades no eran candidatos a recibir uno de estos esquemas fueron tratados principalmente con fluoropirimidinas en monofármaco, ya sea en bolos o en infusiones a diferentes dosis. Del 2007 en adelante se incrementó la variedad de opciones de tratamiento, sin embargo, estos esquemas reportan incremento en SLP y SG pero a expensas de mayor toxicidad, por lo que no todos los pacientes son candidatos a recibirlos por lo que estos pacientes fueron tratados con los esquemas disponibles antes del 2007 y 5 (10%) pacientes fueron tratados con monofármaco (taxanos, fluoropirimidinas). Esto probablemente impactó en los resultados de nuestro estudio, ya que al analizar la SLP y SG de acuerdo a los esquemas de tratamiento, los mejores resultados se obtuvieron con capecitabina-oxaliplatino, epirrubicina-oxaliplatino-capecitabina y docetaxel-cisplatino-5fluorouracilo, tal como se ha reportado en la literatura4,7,8. Los pacientes que pudieron recibir estos esquemas alcanzaron hasta 16.8 meses de SG, pero fueron casos aislados. Al final el uso de estos esquemas no reflejó diferencias dado que la cohorte de pacientes tratados desde el 2007 a la actualidad incluye más del 30% de los pacientes tratados con esquemas similares a los utilizados antes de esa fecha y probablemente el beneficio se dispersa dado que la muestra es pequeña y hay al menos 8 opciones de tratamiento. Debemos destacar que en la cohorte de pacientes del brazo A se reportó una paciente que tiene SLP y SG muy prolongada (105 meses), presentaba enfermedad metastásica confirmada y presentó respuesta completa con la quimioterapia; se trata de un caso aislado pero debido a que el número de pacientes es pequeño modifica de forma importante los resultados ya que si excluimos a esta paciente del análisis la SLP es de 3.2 meses para el brazo A vs. 5.2 meses para el brazo B, y la SG es de 7.3 meses para el brazo A vs. 10.5 meses para el brazo B.
Hicimos también un análisis de la SG de acuerdo al estado funcional de ECOG, en donde observamos que la SG fue similar para los pacientes con ECOG 0-1. Destaca que mientras en la cohorte A no se incluyeron pacientes con ECOG 3, en la cohorte B representan el 12% de los pacientes, reportándose disminución significativa de la SG en estos pacientes comparativamente con aquellos con mejor estado funcional. Es posible que ello haya impactado en los resultados globales de SG en esa cohorte considerando que además estos pacientes recibieron los esquemas de quimioterapia que reportaron menor SG, dado que la toxicidad es uno de los principales limitantes al elegir el esquema de tratamiento a utilizar.No hubo diferencia en los resultados entre esquemas basados o no en platinos.
ConclusionesEn nuestro centro no hay impacto de los nuevos esquemas de tratamiento en SLP o SG.
Conflicto de interesesLos autores declaran no tener conflicto de intereses.