La traqueotomía es una técnica habitual en las Unidades de Cuidados Intensivos (UCI). Es sabido que los cuidados enfermeros durante y posteriores al procedimiento están directamente relacionados con el éxito del mismo, minimizando el riesgo de aparición de complicaciones como la infección del estoma y favoreciendo la adecuada evolución del paciente crítico.
ObjetivosComparar la incidencia de infección en las traqueotomías realizadas en UCI según el antiséptico empleado: cura con polihexanida (PLX) y cura con suero fisiológico+povidona yodada (PY).
Material y métodoEnsayo experimental, aleatorizado y abierto, realizado en una UCI polivalente de 32 camas durante 2 años. El estudio fue aprobado por el Comité Ético de Investigación del Principado de Asturias.
ResultadosLa tasa observada de infecciones por 100 pacientes-día de traqueotomía fue de 1,34 (IC del 95%, 0,81-2,01): 1,46 en PLX y 1,21 PY (p valor 0,685).
ConclusionesA pesar de que el tratamiento experimental (PLX) ha mostrado su eficacia en otro tipo de heridas, en nuestro estudio no se encontraron diferencias significativas entre esta técnica y la estándar. Dado que no existe un registro nacional de incidencia de infección asociada a traqueotomías, no se puede saber si la observada está dentro de los parámetros habituales.
Tracheotomy is a common technique in Intensive Care Units (ICU). It is known that nursing care during and after that procedure is directly related to its success, by reducing the possible complications to a minimum, such as the stoma infection, and contributing to a favourable outcome in critical patients.
ObjectivesTo compare the use of polyhexanide (PLX) versus saline+povidone iodine (PY) as antiseptics and infection incidence in tracheostomies performed in Intensive Care Units.
Material and methodA 2-year, experimental, randomised, open-label trial carried out in a multidiscipline ICU with 32 beds. The study was approved by the Research Ethics Committee of Principality of Asturias.
ResultsThe overall infection rate observed for every hundred patients was 1.34 (95% CI; 0.81-2.01), with 1.46 when using PLX and 1.21 for PY (P=.685).
ConclusionsIn spite of the experimental treatment (PLX) was shown to be effective in other types of wounds in our study. No significant differences were found between this technique and the standard one. Since there is no national registry of tracheotomy- associated infections, it is not possible to know whether the rate observed is within the usual parameters.
La falta de un registro específico de incidencia de infección asociada a las traqueotomías realizadas en las Unidades de Cuidados Intensivos no debe hacernos olvidar su posible y relevante implicación en el aumento de la morbimortalidad asociada. Conocerlos facilita la identificación de los campos de actuación necesarios para posibilitar mejoras en su control y reducción. Implementar protocolos de cuidados basados en la evidencia mejora la atención y seguridad del paciente crítico.
El profesional sanitario debe de tener acceso a aquellos recursos más eficaces y efectivos para su práctica diaria sin olvidarse, por supuesto, que dichos recursos también deberán ser eficientes.
Implicaciones del estudioLa implicación de este estudio trata de dotar a la práctica clínica de la evidencia necesaria para protocolizar las curas y estandarizar los cuidados de la traqueotomía en el paciente crítico, aportando calidad y seguridad durante el proceso asistencial a fin de prevenir la infección, disminuyendo los riesgos asociados a esta, así como las estancias y el gasto sanitario.
La traqueotomía es una técnica habitual en las Unidades de Cuidados Intensivos (UCI)1-4. Consiste en un procedimiento quirúrgico que permite la apertura de la vía aérea mediante la introducción de una cánula, con objeto de mantenerla permeable y garantizar su estabilidad. Este procedimiento no está exento de riesgos, por lo que es necesario conocer cuáles son sus indicaciones y posibles complicaciones.
Con el tiempo, la traqueotomía ha pasado de ser un procedimiento quirúrgico complejo, realizado en quirófano, a una intervención que puede ser realizada en la propia cama del paciente dentro de la UCI. Esta técnica, conocida como traqueotomía percutánea, se ha convertido en una alternativa a la traqueotomía quirúrgica convencional. Con ella se evita el traslado del paciente al quirófano, no se depende de otros servicios y se reducen tiempos y agresiones quirúrgicas, siendo por sus propias características, según distintos estudios, una técnica rápida, sencilla y segura, con una reducción significativa de la tasa de infección del estoma, del sangrado operatorio y del riesgo de muerte2,4-11.
En las UCI, el mayor número de traqueotomías se realizan en pacientes sometidos a ventilación mecánica prolongada (15-20 días), aunque también está indicada en otros casos, como, por ejemplo3,4,9-16:
- –
Intubación dificultosa.
- –
Pacientes con enfermedades respiratorias crónicas y otras entidades patológicas que cursen con insuficiencia respiratoria crónica y precisen ventilación mecánica invasiva.
- –
Pacientes con necesidad de protección de la vía aérea o su acceso para el drenaje de secreciones, que suelen ser pacientes con alguna neuropatía.
- –
Pacientes con obstrucción de la vía aérea superior (tratados por el Servicio de Otorrinolaringología).
Se debe señalar la importancia de los cuidados enfermeros previos, durante y posteriores al propio procedimiento, ya que estas actividades están directamente relacionada con el éxito del mismo, pudiendo evitar muchas de sus complicaciones, tales como4,6,7,9,10,12,16:
- –
Lesiones traqueales: causadas por la presión del balón sobre las paredes de la tráquea con el consiguiente riesgo de isquemia, necrosis y dilatación traqueal.
- –
Fístula traqueoesofágica: especialmente cuando el paciente es portador de SNG durante largos períodos. El roce de los planos duro, la cánula y la SNG, pueden originar una fístula.
- –
Broncoaspiración.
- –
Hipoxemia: falta de oxígeno, fundamentalmente, durante la técnica de aspiración de secreciones.
- –
Hemorragia: debido a una rotura de algún vaso, particularmente en el postoperatorio inmediato y en laringectomías totales.
- –
Infección: sobre todo en el postoperatorio inmediato debido a la herida quirúrgica, ya que el estoma no ha cicatrizado.
La infección puede tener una gran repercusión en la evolución de los pacientes ingresados en la UCI, tal como refleja el informe anual del Estudio nacional de vigilancia de la infección nosocomial en los Servicios de Medicina Intensiva. Los dispositivos invasivos que precisa el paciente crítico (accesos vasculares, tubo endotraqueal o sondaje vesical, por ejemplo) llevan asociado un gran riesgo de infección17-20; esta complicación será el eje principal de este estudio.
Pese a la importancia del cuidado de una traqueotomía en los pacientes de la UCI, no se han elaborado estudios rigurosos ni revisiones sistemáticas al respecto.
Dawson21 realiza una extensa investigación bibliográfica y pone de manifiesto la limitada evidencia científica existente en torno al cuidado del estoma de los pacientes traqueotomizados. Si bien es cierto que se trata de otra especialidad médica, Núñez-Moral et al.22, ante la inexistencia de directrices claras sobre el cuidado del orificio de salida el catéter de diálisis peritoneal, diseñan un estudio prospectivo aleatorizado en el que demuestran la eficacia de la polihexanida (PLX) en la prevención de la infección asociada a este tipo de catéteres.
La PLX se presenta con mayor frecuencia como el producto sanitario de elección en la limpieza y tratamiento de gran variedad de heridas23, lo cual, unido a la falta de evidencia en los cuidados a las personas con traqueotomías y los reveladores resultados del estudio de Núñez-Moral et al.22 en su ámbito, pone de manifiesto la pertinencia del estudio sobre la posible influencia del tipo de cura en la infección de las traqueotomías. El objetivo pues de nuestro trabajo fue comparar la incidencia de infección en las traqueotomías realizadas en UCI sometidas a 2 tipos de cura del estoma: cura local con PLX frente a la cura tradicional con suero fisiológico más povidona yodada (PY).
Material y métodosSe trata de un ensayo experimental, aleatorizado y abierto desarrollado en la UCI I del Hospital Universitario Central de Asturias, unidad polivalente que consta de 24 camas de cuidados intensivos y 8 más de cuidados intermedios.
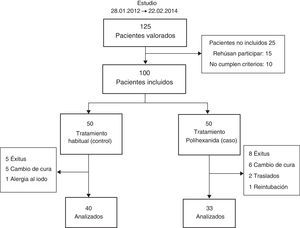
El estudio contó con la aprobación del Comité de Ética de Investigación del Principado de Asturias y con el consentimiento informado de los sujetos participantes. El periodo de inclusión de pacientes se prolongó durante un periodo de 2 años (del 28 de enero del 2012 al 22 de febrero del 2014). Los pacientes finalmente incluidos cumplieron los siguientes criterios:
Criterios de inclusiónPacientes mayores de 18 años a los que se les había realizado una traqueotomía quirúrgica o percutánea entre el 28 de enero del 2012 y el 22 de febrero del 2014, que llevaban más de 48h ingresados en la unidad y que habían firmado el consentimiento informado.
Criterios de exclusiónPacientes con tratamiento antibiótico local (tópico) de la traqueotomía y/o los que presentaban intolerancia a compuestos yodados y/o a la polihexanida. Pacientes a los que se les realizaba una traqueotomía en las 24 primeras horas de su ingreso en UCI y/o los que ya portaban una traqueotomía al ingreso. Pacientes que no firmaron el consentimiento informado.
DefinicionesSe consideró sospecha de infección local del estoma la aparición de al menos 3 de los siguientes signos: inflamación, enrojecimiento, mal olor, exudado purulento y/o expresión de dolor a la palpación en la zona periestomal. Tres o más signos conllevaron a un control microbiológico (cultivo de exudado del estoma) y su positividad condicionó la salida del estudio. Si era negativo, se mantenía en el estudio. El tiempo hasta la infección fue considerado desde la realización de la traqueotomía hasta la confirmación microbiológica de la infección.
El método de muestreoEl método de muestreo empleado fue secuencial; subdividiendo aleatoriamente en 2 grupos a los pacientes incluidos y aplicando a cada grupo un tipo de cura: tratamiento habitual (grupo control) o empleo de polihexanida (grupo experimental).
Se sorteó el grupo de pertenencia del primer paciente reclutado (1: grupo control, 2: grupo experimental). Seguidamente se generó una tabla secuencial de pertenencias, de tal manera que 2 pacientes consecutivos no fueran asignados al mismo grupo. Los pacientes fueron reclutados por los investigadores y, en función de la lista generada, el paciente era incluido en el grupo correspondiente.
La lista de aleatorización fue custodiada por las supervisoras de la unidad, miembros de equipo investigador, en su despacho.
El seguimiento de los pacientes se mantuvo hasta el momento en que fueron dados de alta de la unidad, cumplían los criterios acordados de infección, eran decanulados o fallecían.
Cálculo del tamaño muestralDado que, como se comentó anteriormente, existe una carencia de información en lo que se refiere a la tasa de infección estudiada, basándonos en nuestra experiencia clínica, se estimó que la tasa de infección observada era en torno al 30% y que una mejora del 20% tendría relevancia clínica. Así las cosas, asumiendo que la tasa esperada de infección en el grupo PLX y PY es del 10% y del 30%, respectivamente, y una tasa de pérdida durante el seguimiento del 10%, el tamaño muestral requerido para encontrar significativas diferencias inferiores al 5% (error de tipo i de 0,05) con una potencia del 80% (error de tipo ii de 0,2) es de 52 por grupo (cálculo realizado con el software estadístico Epidat 3.1).
Recogida de datosSe diseñó un registro específico que incluía datos generales de cada paciente y datos relativos a las curas. Se estudiaron las siguientes variables: demográficas (edad, sexo), diagnóstico médico al ingreso (enfermedades del aparato respiratorio, del sistema nervioso, neoplasias, enfermedades infecciosas, politraumatismo y otros), APACHE II, fecha de ingreso en la UCI, hipertensión arterial, diabetes, consumo de alcohol y/o tabaco. Variables relacionadas con el procedimiento: fecha de realización de traqueotomía, tipo, lugar de realización (UCI o quirófano), duración y servicio que la realiza, aparición de complicaciones (sí/no) y en caso afirmativo cuáles eran, fecha del primer cambio de cánula y existencia o no de complicaciones en el mismo, uso simultáneo de antibióticos, ventilación mecánica.
Relacionadas con las curas: se registraron 2 curas al día anotando hasta 5 posibles signos locales de infección. El personal de enfermería responsable del paciente fue el encargado de realizar la cura del estoma anotando en la hoja de registro el estado del mismo según los ítems elegidos (sí/no). La primera cura se hacía a las 24 h para evitar posibles desplazamientos o sangrados. Al personal, junto con la hoja de registro, se les adjuntaba un anexo (anexos 1 y 2), donde se especificaba cómo debía realizarse la cura con cada producto a fin de estandarizar el procedimiento. La aparición de 3 o más signos de infección requería la toma de muestra del estoma, dejándolo reflejado en la hoja de registro de cura, siguiendo con los mismos cuidados hasta la obtención del resultado del cultivo.
Como se ha descrito anteriormente, la aleatorización se realizó mediante la adjudicación secuencial de un código o número según la incorporación del paciente al estudio y mediante el cual se le asignaba alternativamente la cura tradicional o la cura con PLX. Dada la diferente naturaleza de los productos empleados en la cura, el estudio no pudo ser ciego para los investigadores, si bien fue ciego en el procesamiento estadístico de los datos.
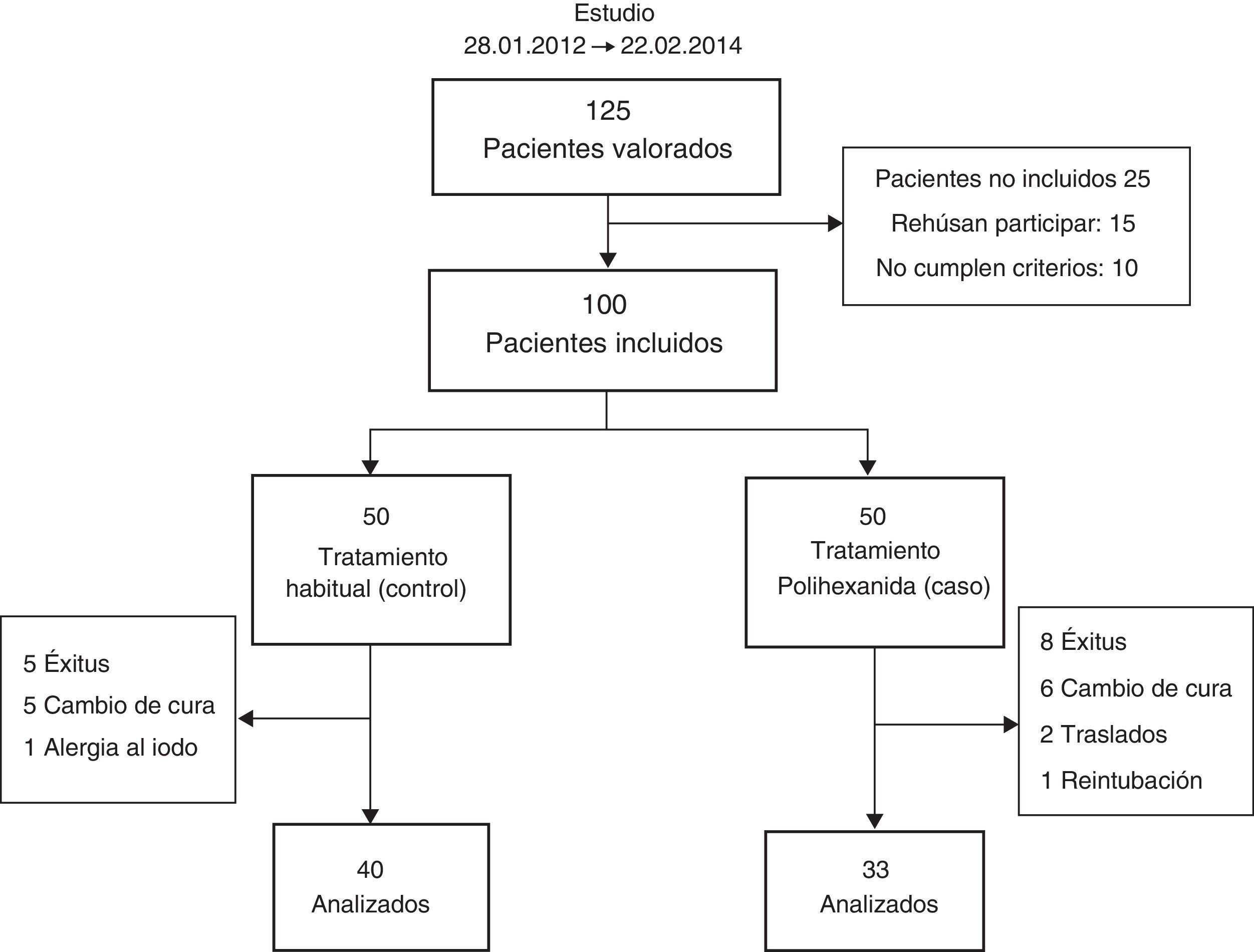
De los 125 pacientes valorados inicialmente, 15 rehusaron participar y 10 fueron desestimados al no cumplir alguno de los criterios de inclusión (fig. 1).
Análisis estadísticoLas variables continuas fueron descritas mediante medias±desviación típica y los variables de tiempo como mediana (valor mínimo, valor máximo) y comparadas mediante la prueba de Student-Welch y el test no paramétrico de Mann-Whitney, respectivamente. Las variables categóricas fueron descritas mediante frecuencias relativas y absolutas, y comparadas mediante el test exacto de Fisher. Las tasas de infección por 100 pacientes-día (100×[n.° infecciones observadas/suma de días computados]) se compararon mediante el método Bootstrap. El estimador de Kaplan-Meier ajustado por riesgos competitivos (muerte sin infección/alta en la UCI) fue utilizado para estudiar la probabilidad de infección en cada momento del tiempo. La comparación de las curvas en PLX y PY se realizó mediante el logrank test y el tamaño del efecto se midió mediante la razón de riesgos (hazard ratio [HR]) cruda y ajustada por covariables. Se reportan intervalos de confianza del 95% para las estimaciones de los principales resultados (tasa de infección global y razones de riesgos). Los p valores inferiores a 0,05 fueron considerados estadísticamente significativos. Los cálculos fueron realizados con el software de libre distribución R 2.1 (www.r-project.org).
Este trabajo ha sido preparado siguiendo los 25 puntos de la guía CONSORT (www.consort-statement.org), si bien, en su momento, no se consideró necesaria la inscripción del mismo en ningún registro.
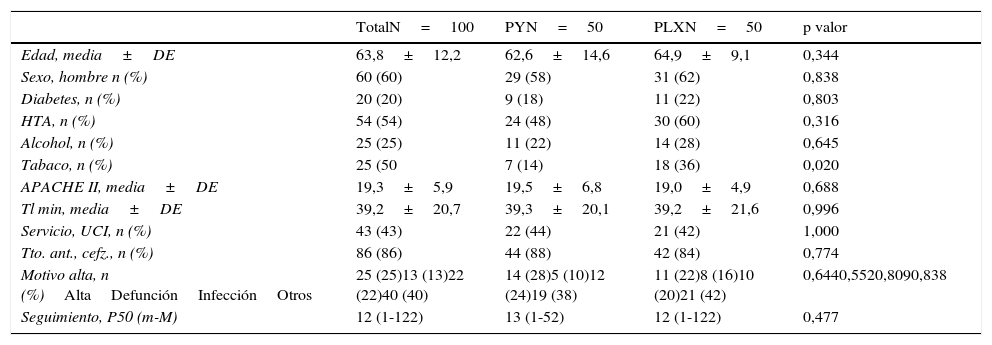
ResultadosDe los 100 pacientes finalmente incluidos en el estudio, el 60% fueron hombres. La edad en el momento del ingreso fue de 64±12 años, oscilando entre los 18 y los 82 años. Como era de esperar, ya que la asignación fue realizada al azar, no se observan diferencias en la mayoría de las variables estudiadas, si bien en el grupo de PLX hubo mayor número de fumadores. El tiempo de seguimiento osciló entre uno y 122 días. Durante este tiempo, hubo un total de 22 infecciones, 12 en el grupo de PLX y 10 en el grupo PY. La tasa de infección por 100 pacientes-día de intubación observada fue de 1,34, 1,46 en controles y 1,21 en tratamientos (p valor de 0,628). La tabla 1 muestra las principales características según el grupo al que fueron asignados (PLX/PY).
Estadísticos descriptivos para las variables incluidas en el estudio
| TotalN=100 | PYN=50 | PLXN=50 | p valor | |
|---|---|---|---|---|
| Edad, media±DE | 63,8±12,2 | 62,6±14,6 | 64,9±9,1 | 0,344 |
| Sexo, hombre n (%) | 60 (60) | 29 (58) | 31 (62) | 0,838 |
| Diabetes, n (%) | 20 (20) | 9 (18) | 11 (22) | 0,803 |
| HTA, n (%) | 54 (54) | 24 (48) | 30 (60) | 0,316 |
| Alcohol, n (%) | 25 (25) | 11 (22) | 14 (28) | 0,645 |
| Tabaco, n (%) | 25 (50 | 7 (14) | 18 (36) | 0,020 |
| APACHE II, media±DE | 19,3±5,9 | 19,5±6,8 | 19,0±4,9 | 0,688 |
| Tl min, media±DE | 39,2±20,7 | 39,3±20,1 | 39,2±21,6 | 0,996 |
| Servicio, UCI, n (%) | 43 (43) | 22 (44) | 21 (42) | 1,000 |
| Tto. ant., cefz., n (%) | 86 (86) | 44 (88) | 42 (84) | 0,774 |
| Motivo alta, n (%)AltaDefunciónInfecciónOtros | 25 (25)13 (13)22 (22)40 (40) | 14 (28)5 (10)12 (24)19 (38) | 11 (22)8 (16)10 (20)21 (42) | 0,6440,5520,8090,838 |
| Seguimiento, P50 (m-M) | 12 (1-122) | 13 (1-52) | 12 (1-122) | 0,477 |
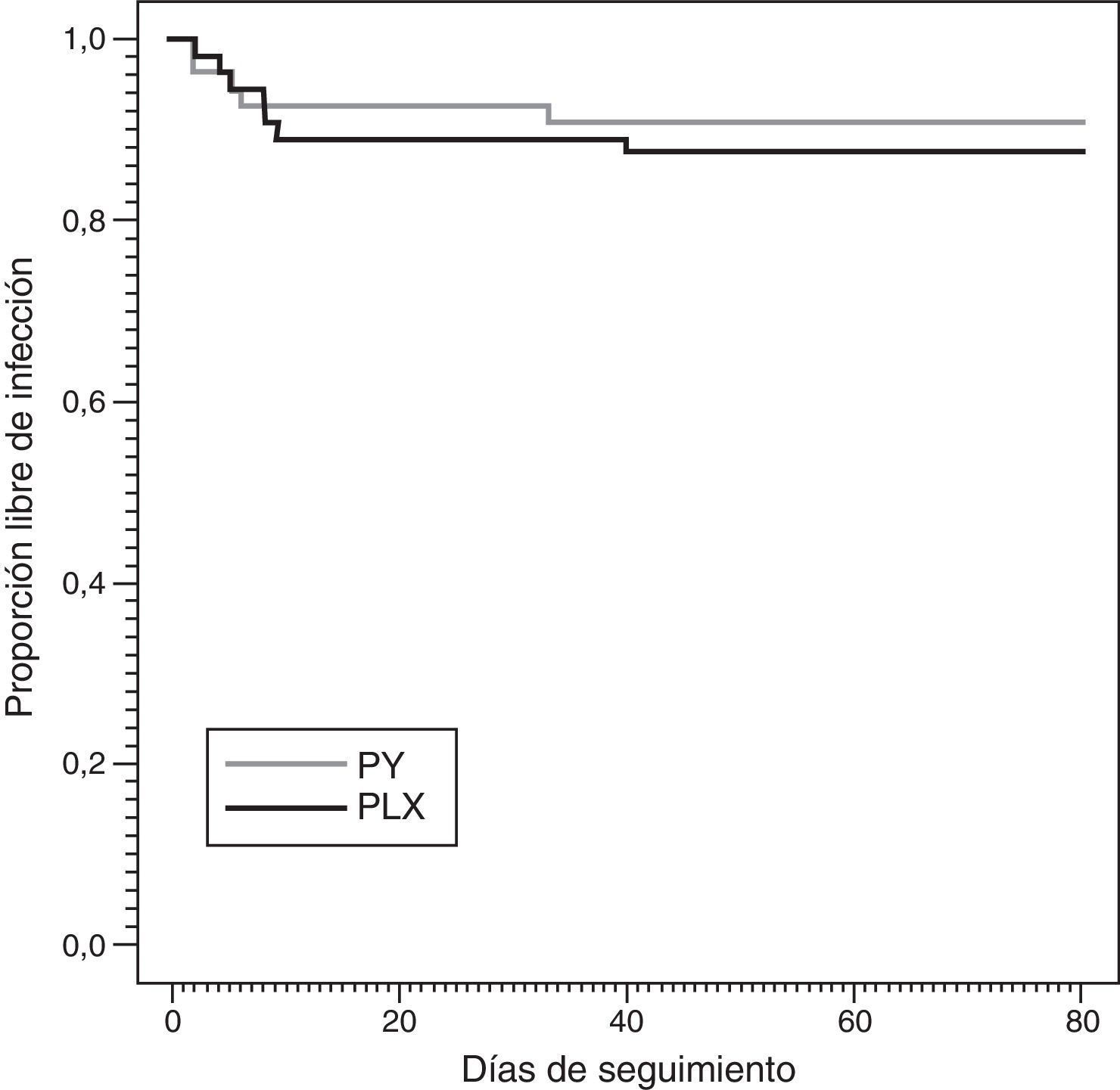
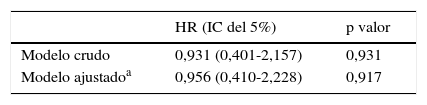
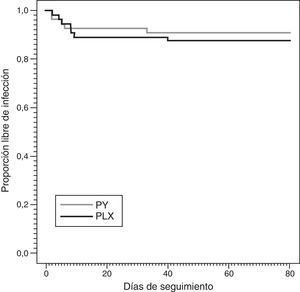
El desenlace final de los 100 pacientes incluidos en el estudio fue: 27 fueron dados de alta sin infección, 23 fueron decanulados, 13 fallecieron antes de tener una infección, 22 tuvieron una infección y 15 tuvieron otro desenlace (reintubación, cambio en el producto usado en la cura, alergias). A pesar de que se observó que el grupo PY tuvo una incidencia ligeramente menor que el grupo PLX, el descenso del riesgo no fue significativo (HR=0,931 [0,401-2,157]; p valor de 0,931) y fue similar cuando se ajustó por posibles confusores: sexo, edad, tabaco, alcohol, APACHE II, tiempo intervención mínimo y servicio (HR=0,956 [0,410-2,228]; p valor de 0,917). La figura 2 muestra el estimador de Kaplan-Meier ajustado por riesgos competitivos (muerte/alta) para el tiempo libre de infección en los pacientes PLX y PY. La tabla 2 muestra las HR con un intervalo de confianza del 95% para los modelos de riesgos proporcionales crudo y ajustado por las covariables anteriormente mencionadas.
Hazard ratios e intervalos de confianza para el efecto del tratamiento (PLX) en la infección. Crudo y ajustado por las principales covariables
| HR (IC del 5%) | p valor | |
|---|---|---|
| Modelo crudo | 0,931 (0,401-2,157) | 0,931 |
| Modelo ajustadoa | 0,956 (0,410-2,228) | 0,917 |
La traqueotomía, por ser una técnica habitual realizada a los pacientes ingresados en las UCI, ha sido objeto de estudio a lo largo de los años y han sido varios los autores que han descrito sus indicaciones, tipos de técnicas quirúrgicas y las complicaciones derivadas de las mismas. Sin embargo, una vez realizada la traqueotomía, son escasas las referencias que encontramos sobre la evolución de esta herida quirúrgica y sus complicaciones; autores como Brook19, Cardone24 Stauffer et al.25 señalan, por ejemplo, que la infección relacionada con este procedimiento es una complicación nada desdeñable.
La PY es un antiséptico altamente efectivo que ha sido utilizado clínicamente en el tratamiento de las heridas desde hace más de 170 años con un amplio espectro de actividad. Existe una evidencia sustancial que apoya el uso del yodo en la cicatrización de las heridas. Barato y fácil de usar, su uso no está exento de controversia debido a problemas de toxicidad, absorción y alergias, entre otros, pero, a pesar de esta controversia, los antimicrobianos yodóforos son eficaces y seguros26.
Sin embargo, numerosos estudios han demostrado la utilidad de otros productos sanitarios como la PLX en el cuidado de las heridas, tanto agudas como crónicas, por su amplio espectro de acción, mínima toxicidad y buena tolerancia tanto en su modalidad en irrigación como en gel27-33.Motta y Triglia18, en un estudio aleatorizado, controlado y prospectivo en el 2005, demostraron una reducción importante de los gérmenes más frecuentemente aislados en los traqueostomas, entre ellos el Staphylococcus aureus resistente a meticilina (SARM) y la Pseudomonas aeruginosa, tratados con PLX, frente a los que no. Varios estudios concluyen que la PLX reduce significativamente el SARM18,34,35. Romanelli et al.36 y Horrocks37, en sus estudios, obtuvieron un menor crecimiento bacteriano en las heridas irrigadas con PLX con respecto a las irrigadas con suero salino (SS). Seipp et al.38 y Adriessen y Eberlein39 obtuvieron similares resultados cuando comparaban PLX con SS y solución ringer. En varios estudios in vitro38,40-42 se obtuvo que PLX era eficiente en la reducción de la carga bacteriana y en la eliminación del biofilm. Lee et al.43 en su estudio concluyeron que el uso de gasas impregnadas con PLX reducía el riesgo de infección del punto de inserción de los clavos del fijador externo. En su estudio, Koburger et al.44 concluyeron que cuando el tiempo de contacto con el antiséptico era prolongado PLX, era el más adecuado además de bien tolerado. Alonso Torres et al.45 demostraron en un estudio cuantitativo la mejora del lecho de la herida posquirúrgica afectada por gangrena de Fournier con el uso de PLX, reduciendo además la estancia hospitalaria y la morbilidad. Núñez-Moral et al.22 concluye en un ensayo clínico prospectivo que la PLX es eficaz en la prevención de las infecciones del orificio de salida del catéter de diálisis peritoneal frente a la realización de los cuidados tradicionales del mismo.
Por otro lado, en un estudio reciente realizado por Ahmadinegad Lashkarizadeh et al.46, no se encontraron diferencias significativas en la prevención de infección tras la realización de la cura tradicional de las traqueotomías frente al cuidado llevado a cabo con un nuevo apósito absorbente.
LimitacionesEl tiempo de recogida de datos se prolongó por encima de lo estimado, llegando a duplicarse, debido al descenso en el número de pacientes/día y al acortamiento en las estancias medias de los mismos durante periodos puntuales que coincidieron en fechas con el estudio.
La ausencia de registros de incidencia de infección de la traqueotomía no nos ha permitido comparar nuestros resultados con los de otros estudios, puesto que los registros de infección en relación con el sitio quirúrgico son generales y no específicos para este procedimiento.
ConclusionesLos resultados de nuestro estudio ponen de manifiesto que la cura realizada con PLX (grupo experimental) no disminuye la tasa de infección frente a la cura realizada con PY (grupo control).
Se constata que hay una ligera tendencia a la disminución de la infección en el grupo sometido a tratamiento con PLX frente al grupo control pero exenta de significación estadística, lo cual puede deberse a un tamaño insuficiente de la muestra.
Aportar calidad a nuestros cuidados, basándonos en evidencia científica, demostraría, a su vez, que los profesionales enfermeros son fundamentales para el control de las infecciones hospitalarias, ya que las medidas básicas cobran gran importancia en su control.
Conflicto de interesesLos autores del trabajo manifiestan que no existe ningún conflicto de interés ni han recibido subvención alguna para la realización del mismo.
Nuestro agradecimiento a los profesionales de enfermería de la UCI 3-4-5-6, que se interesaron y colaboraron en este proyecto con la consecuente carga de trabajo asociada.