La presencia de pacientes con infección en los servicios de urgencias (SU) representa un 15-20% de todos los atendidos diariamente en España1. Además, la gravedad de su presentación clínica y la mortalidad a corto plazo (30 días) se ha incrementado en la última década, especialmente en los pacientes que cumplen criterios de sepsis, presentan comorbilidades relevantes, inmunodeprimidos, ancianos o con bacteriemia significativa confirmada desde el SU. En ellos, la mortalidad se cifra en el doble o triple que en el resto de pacientes con el mismo proceso1.
En este escenario, la administración precoz y adecuada del tratamiento antibiótico (AB), junto con el control del foco de infección, así como la toma inmediata de otras decisiones (solicitar pruebas complementarias, obtener hemocultivos y otras muestras microbiológicas, la intensidad del soporte hemodinámico, entre otras), repercuten directamente en la supervivencia de los enfermos con infección bacteriana grave y bacteriemia2.
En los últimos años, se ha acentuado la búsqueda de herramientas de ayuda para predecir un diagnóstico precoz, el pronóstico y, junto con la posible etiología bacteriana, la sospecha de bacteriemia. Así, los biomarcadores de respuesta inflamatoria e infección (BMRII)3,4 han demostrado su utilidad para predecir y detectar la existencia de bacteriemia verdadera, tanto como predictores independientes3,5,6, como formando parte de modelos predictivos de bacteriemia7–9. Entre todos los BMRII destaca la procalcitonina (PCT), que también es muy sensible y específica para predecir infección bacteriana, orientar hacia el patógeno causante de la infección, su evolución clínica (a sepsis y shock séptico) y la mortalidad3,5.
Recientemente, se ha descrito una nueva prueba basada en la alteración de las concentraciones de distintas proteínas que se producen en la respuesta inmunológica. Este test, denominado LIAISON®MeMed®, obtiene una puntuación en función de un modelo que correlaciona los resultados de tres proteínas solubles del huésped, lo que permite distinguir entre el origen bacteriano frente al viral de una infección10. Pero, hasta ahora, no se han publicado estudios que evalúen la capacidad predictiva de bacteriemia de LIAISON®MeMed®. Esta prueba de diagnóstico incluye una puntuación basada en la combinación de la concentración de 3 proteínas circulantes en sangre de BMRII inducidos tanto por virus como por bacterias: 1) el ligando inductor de apoptosis relacionado con el factor de necrosis tumoral (TRAIL) que se eleva como expresión de infección viral y disminuye en infección bacteriana; 2) la proteína 10 inducida por el interferón gamma(IP-10) que se incrementa más en infecciones virales y en menor medida en bacterianas, y 3) la proteína C reactiva (PCR) que muestra un patrón opuesto a la IP-10. De esta manera, la presencia de proteínas del huésped no relacionadas entre sí que participan en diferentes vías podría mejorar la precisión del diagnóstico10.
En este contexto, con el objetivo de investigar la capacidad de la prueba MeMed® para predecir bacteriemia en los pacientes adultos atendidos con sospecha clínica de infección en el SU y comparar su rendimiento con la PCT, se elaboró este estudio observacional, de cohortes, prospectivo de pacientes adultos atendidos en un SU con el diagnóstico clínico de un proceso infeccioso en los que se obtuvo analítica y pruebas microbiológicas (en todos ellos hemocultivos [HC]). Los casos se incluyeron por oportunidad (cuando los investigadores estuvieron de guardia). Como variable dependiente se consideró el diagnóstico de bacteriemia verdadera (BV) que se definió, según criterios ya publicados por los autores en otros artículos8,9, ante el aislamiento de bacterias habitualmente patógenas en uno o los 2 HC con un cuadro clínico compatible. Y, como HC contaminado el aislamiento en una sola botella de HC de Staphylococcus coagulasa- negativo (ECN), Bacillus spp., Streptococcus del grupo viridans, Micrococcus spp., Propionibacterium spp., Corynebacterium spp., y otros bacilos grampositivos cuando se interpretó la ausencia de significado clínico en estos casos (confirmado según la historia y/o el criterio del médico responsable y el de microbiología).
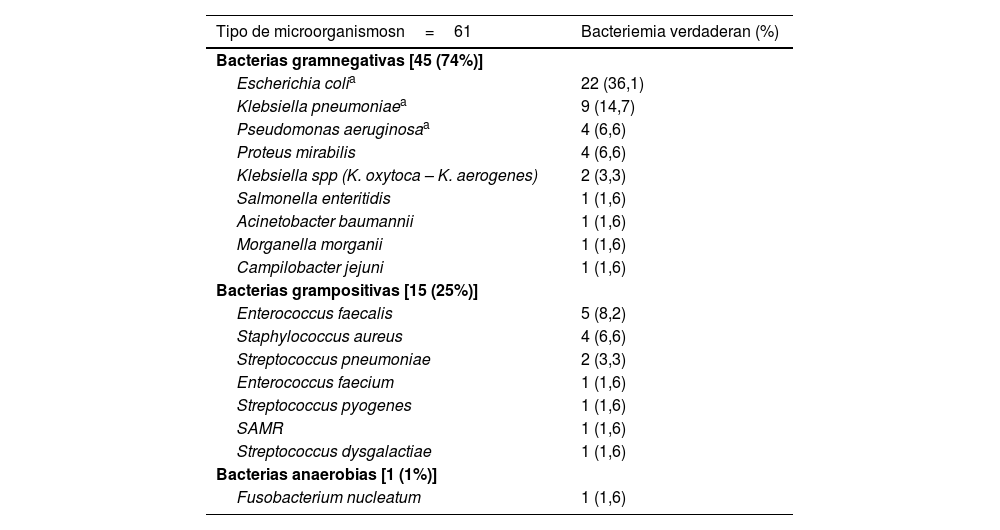
Se analizó la capacidad predictiva con el área bajo la curva (ABC) de la característica operativa del receptor (COR) y los valores de sensibilidad (Se), especificidad (Es), valor predictivo positivo (VPP) y negativo (VPN) de la PCT y el test LIAISON®MeMed®. Se incluyó a 345 pacientes, 61 (17,7%) con BV (en la tabla 1 se muestran los microorganismos aislados considerados como BV o significativa). La edad media fue 66,48 (DE 18,84) años, el 58% eran hombres. El ABC-COR de MeMed® para predecir BV fue de 0,94 (IC 95%: 0,87-1,00; p<0,001); y de la PCT de 0,83 (IC 95%: 0,77-0,89; p<0,001). Con un punto de corte (PC) >65 puntos del test MeMed® se obtiene un ABC-COR de 0,91 (IC 95%: 0,83-0,98; p<0,001), Se: 85%, Es: 93%, VPP: 97% y VPN: 64% y con PC≥0,51ng/ml de PCT un ABC-COR de 0,82 (IC 95%: 0,76-0,88); p<0,001), Se: 74%, Es: 85%, VPP: 93% y VPN: 56%.
Microorganismos aislados en los episodios de bacteriemia verdadera
| Tipo de microorganismosn=61 | Bacteriemia verdaderan (%) |
|---|---|
| Bacterias gramnegativas [45 (74%)] | |
| Escherichia colia | 22 (36,1) |
| Klebsiella pneumoniaea | 9 (14,7) |
| Pseudomonas aeruginosaa | 4 (6,6) |
| Proteus mirabilis | 4 (6,6) |
| Klebsiella spp (K. oxytoca – K. aerogenes) | 2 (3,3) |
| Salmonella enteritidis | 1 (1,6) |
| Acinetobacter baumannii | 1 (1,6) |
| Morganella morganii | 1 (1,6) |
| Campilobacter jejuni | 1 (1,6) |
| Bacterias grampositivas [15 (25%)] | |
| Enterococcus faecalis | 5 (8,2) |
| Staphylococcus aureus | 4 (6,6) |
| Streptococcus pneumoniae | 2 (3,3) |
| Enterococcus faecium | 1 (1,6) |
| Streptococcus pyogenes | 1 (1,6) |
| SAMR | 1 (1,6) |
| Streptococcus dysgalactiae | 1 (1,6) |
| Bacterias anaerobias [1 (1%)] | |
| Fusobacterium nucleatum | 1 (1,6) |
SAMR: Staphylococcus aureus resistente a meticilina.
Como conclusión podemos decir que en los pacientes adultos atendidos con sospecha clínica de infección en el SU, la prueba de LIAISON MeMed® presenta una estimable capacidad para predecir BV y obtiene mejor rendimiento que la PCT.
AutoríaLos cuatro autores declaran ser los responsables del diseño, desarrollo y elaboración del artículo.
Responsabilidades éticasEl estudio fue aprobado por el Comité Ético de Investigación Clínica con medicamentos (CEIm) del Hospital Universitario de Toledo (n.o: 1075/2023).
FinanciaciónLos reactivos para medir LIAISON®MeMed® fueron cedidos por Diasorin. Pero, nadie de la compañía participó en el diseño del estudio ni en la evaluación de sus resultados ni condicionó ninguna fase de su elaboración.
Conflicto de interesesLos autores declaran la ausencia de conflictos de intereses en relación con el presente artículo.