En este trabajo se proporciona una definición de estudio de cohortes y se revisan los principales tipos de estudios de cohortes en el estudio de la infección por el virus de la inmunodeficiencia humana (VIH). Se discute cómo las principales fuentes de introducción de sesgos de selección en los estudios de cohortes son las derivadas de la no observación del episodio que determina el origen y de la no observación del episodio de interés debido a pérdidas en el seguimiento o al desarrollo de un episodio competitivo, y cómo éstos deben valorarse adecuadamente y siguiendo una metodología epidemiológica específica. Finalmente, si bien los estudios de cohortes han tenido un papel fundamental en el estudio de la infección por VIH, éstos son logísticamente complejos y consumen muchos recursos. Por esto, la planificación estratégica sobre la calidad y la cantidad de la información que se recoge debe ir siempre acompañada una asignación de los recursos.
In this paper, we provide a definition of cohort studies and reviews the main types of cohort studies used in the context of HIV infection. We discuss how the main sources of selection biases in cohort studies are those derived from the lack of observation of the event that determines the origin and/or of the event of interest due to losses to follow-up or development of a competing event, and how this bias must be appropriately taken into account following specific epidemiological methods. Although cohort studies play an essential role in the study of HIV infection, they are logistically complex and require considerable resources. Therefore, strategic planning on the quality and quantity of the information collected must always be accompanied by a resource allocation plan.
Los estudios de cohortes han sido fundamentales para describir la historia natural de la infección por el virus de la inmunodeficiencia humana (VIH), determinar los factores y los marcadores biológicos asociados a la progresión de la enfermedad por VIH y evaluar la efectividad de los tratamientos. Los estudios de cohortes son logísticamente complejos y consumen muchos recursos, por lo que se precisa un equilibrio entre la cantidad y la calidad de la información que se recoge.
Los estudios de cohortes son estudios observacionales formados por individuos con un origen común que se siguen en el tiempo para observar la aparición de un episodio resultado de interés (en inglés outcome), en función de que hayan recibido o no una o varias exposiciones, cuya distribución no es aleatoria1,2.
Los estudios de cohorte son, dentro de los diseños epidemiológicos observacionales, los más adecuados para la inferencia causal. El diseño más adecuado para la investigación de efectos causales en biomedicina es el ensayo clínico, debido a que, mediante la asignación aleatoria de la exposición de interés (p. ej: tratamiento antirretroviral), se hace que los sujetos que lo toman y los que no lo toman sólo difieran entre sí en función de la exposición de interés. Los ensayos clínicos tienen, no obstante, un problema de generalizabilidad (también llamada validez externa) debido a que el sujeto que participa en un ensayo clínico es claramente diferente del que no lo hace, lo que se conoce como sesgo del voluntario, caracterizado porque estos individuos son más sanos. En un estudio de cohortes, los sujetos que conforman la muestra son más representativos de la población de origen que los participantes de un ensayo clínico, pero la asignación del tratamiento no es, ni mucho menos, aleatoria, por cuanto son los sujetos más enfermos los que con mayor frecuencia reciben tratamiento.
A continuación se detallan los diferentes tipos de estudios de cohortes de sujetos VIH positivos que existen, se describen las diferentes variables (tanto variables de resultado como variables de exposición) que se manejan en los estudios de cohortes y, finalmente, se detallan los sesgos en los que se puede incurrir en este tipo de diseños.
Clasificación de los estudios de cohortes de personas con virus de la inmunodeficiencia humanaEn función de las características del reclutamiento de los sujetos, se pueden dividir los estudios de cohortes en estudios de cohortes de base poblacional3,4 y estudios de cohortes de base clínica5–12 si los individuos se reclutan en un centro clínico, que puede a su vez ser hospitalario o extrahospitalario. En los estudios de cohortes de base poblacional, los individuos suelen acudir al centro de estudio en visitas regulares programadas (p. ej: cada 6 meses) y se siguen hasta que el episodio de interés ocurre, el estudio finaliza o el individuo decide no seguir participando. En contraste, los estudios de cohortes de base clínica siguen a los pacientes en un centro clínico y los datos se obtienen de la historia clínica de los pacientes o de la base de datos del centro clínico. Como resultado, puede haber más información disponible, aunque las mediciones pueden también ser más esporádicas y la disponibilidad de la información dependiente del episodio de interés. Los pacientes de una cohorte clínica suelen ser representativos de la población que accede al sistema sanitario, siendo, además, su seguimiento más fácil de mantener.
En función del número de centros participantes, los estudios de cohortes pueden ser unicéntricos13,14, si hay un único centro de estudio, o multicéntricos3–12,15, si el reclutamiento y el seguimiento de los individuos se realiza en varios centros. La principal ventaja de los estudios multicéntricos es que permite responder cuestiones sobre la historia natural y el curso clínico del VIH que no pueden responderse mediante cohortes unicéntricas que disponen de un número mas pequeño de sujetos. Además, las cohortes multicéntricas suelen ser más representativas y tener, por tanto, mayor validez externa o potencial de generalización de los resultados. Una iniciativa todavía más ambiciosa a la de una cohorte multicéntrica es la de establecer nuevas colaboraciones entre las colaboraciones de cohortes multicéntricas ya establecidas16–19.
Las cohortes pueden clasificarse como cohortes cerradas o abiertas. Una cohorte cerrada3,6 es aquélla en la que los individuos se reclutan en el mismo período de tiempo y no permite la entrada de nuevos individuos durante el seguimiento. Todos los miembros de una cohorte cerrada tienen períodos de seguimiento que comienzan al mismo tiempo. Por el contrario, una cohorte abierta o dinámica7–19 es aquélla en la que los individuos pueden entrar en la cohorte en diferentes momentos de tiempo durante el período de estudio.
En el caso concreto de la infección por VIH, los estudios de cohortes pueden clasificarse en función de las características de los individuos que forman la cohorte. En primer lugar, los autores de este artículo distinguen entre estudios de cohortes de seroconvertores16,17,20–22 y estudios de cohortes de seroprevalentes5,7–12, dependiendo de si la fecha de seroconversión se conoce o no. Los estudios de cohortes de seroprevalentes están formados por individuos que estaban infectados por VIH antes de su entrada en la cohorte y cuya fecha de seroconversión se desconoce. Por el contrario, los estudios de cohortes de seroconvertores están formados por individuos infectados por VIH cuya fecha de seroconversión se conoce o puede estimarse con fiabilidad. Los estudios de cohortes de seroconvertores se clasifican, a su vez, en cohortes incidentes prospectivas, cohortes incidentes retrospectivas, cohortes prevalentes prospectivas con fechas de seroconversión conocidas y cohortes prevalentes retrospectivas con fechas de seroconversión conocidas. Las cohortes incidentes prospectivas están formadas por una población de individuos sin VIH bien definida en los que se observa la seroconversión durante el seguimiento3,23,24. La baja incidencia de VIH en la mayoría de las poblaciones, requiere el seguimiento de un gran número de individuos para identificar a un grupo de seroconvertores. Este tipo de estudios son los únicos que proporcionan información completa sobre la historia natural de la infección por VIH. Las cohortes incidentes retrospectivas están formadas por individuos procedentes de poblaciones bien definidas, en los que la fecha de seroconversión se identifica retrospectivamente. Este tipo de estudios incluyen cohortes de pacientes hemofílicos25,26 y cohortes de pacientes reclutados en ensayos clínicos para evaluar la vacuna contra el virus de la hepatitis B27. El almacenamiento de las muestras de sangre de estos pacientes, seguidos inicialmente por razones no relacionadas con la infección por VIH, ha permitido determinar retrospectivamente su serología frente a la infección una vez que el test estuvo disponible en 1984. Las cohortes prospectivas prevalentes con fechas de seroconversión conocidas están formadas por individuos con VIH de los que se dispone de un test reciente negativo para VIH y previo al primer test positivo para VIH28,29. Finalmente, las cohortes retrospectivas prevalentes con fechas de seroconversión conocidas están formadas por individuos con VIH y con una fecha de seroconversión identificada retrospectivamente21,30. En esta situación, se debe tener en cuenta la necesidad de utilizar métodos analíticos que incorporen el truncamiento a la izquierda, tal como se detalla en este trabajo.
Variables de interés en los estudios de cohortesLas variables de interés comunes a la mayoría de los estudios epidemiológicos son las variables relativas a la exposición y las relativas al resultado.
Tipos de exposicionesLas variables de exposición que determinan la salud de los individuos pueden ser fijas o cambiantes en el tiempo. Las variables de exposición fijas son variables que no cambian en el tiempo (p. ej. sexo, origen étnico) o que se miden únicamente al inicio del período de observación (p. ej: fumador o no fumador a la entrada en la cohorte). Las variables de exposición cambiantes en el tiempo son variables que presentan diferentes valores en el tiempo. Se puede distinguir entre variables de exposición cambiantes en el tiempo internas, si varían de forma diferente en diferentes individuos (p. ej: linfocitos CD4, tratamiento antirretroviral), o externas, si cambian de la misma forma para todos los individuos (p. ej: períodos calendario).
Tipos de episodios resultados de interésLos episodios resultados de interés más comúnmente estudiados a partir de los datos procedentes de los estudios de cohortes son los episodios en personas-tiempo, los tiempos transcurridos hasta el episodio y el cambio en un marcador medido repetidamente en el tiempo. A continuación se presentan algunas consideraciones sobre los datos, que deben ser tenidas en cuenta en las fases de recogida o análisis de éstos.
Episodios en personas-tiempoEl conocimiento de la incidencia de síndrome de inmunodeficiencia adquirida (sida) o de muerte es fundamental para caracterizar la epidemia. Para su cálculo, es necesario conocer si el individuo experimenta el episodio de interés y el tiempo que cada individuo está a riesgo de desarrollar el evento, es decir, el tiempo transcurrido desde el inicio del período de observación hasta la ocurrencia del episodio o el fin de su período de observación. El análisis del número de episodios en personas-tiempo debe restringirse a los individuos libres del episodio de interés al inicio de su período de observación.
Tiempo a episodioEn investigación en VIH/sida, son numerosas las ocasiones en las que el interés se centra en determinar el tiempo transcurrido entre un origen determinado y la ocurrencia del episodio de interés (p. ej: tiempo a la muerte desde la seroconversión a VIH). Igual que al analizar el número de episodios en personas-tiempo, el análisis del tiempo transcurrido hasta el episodio de interés debe restringirse a los individuos libres del episodio al inicio de su período de observación.
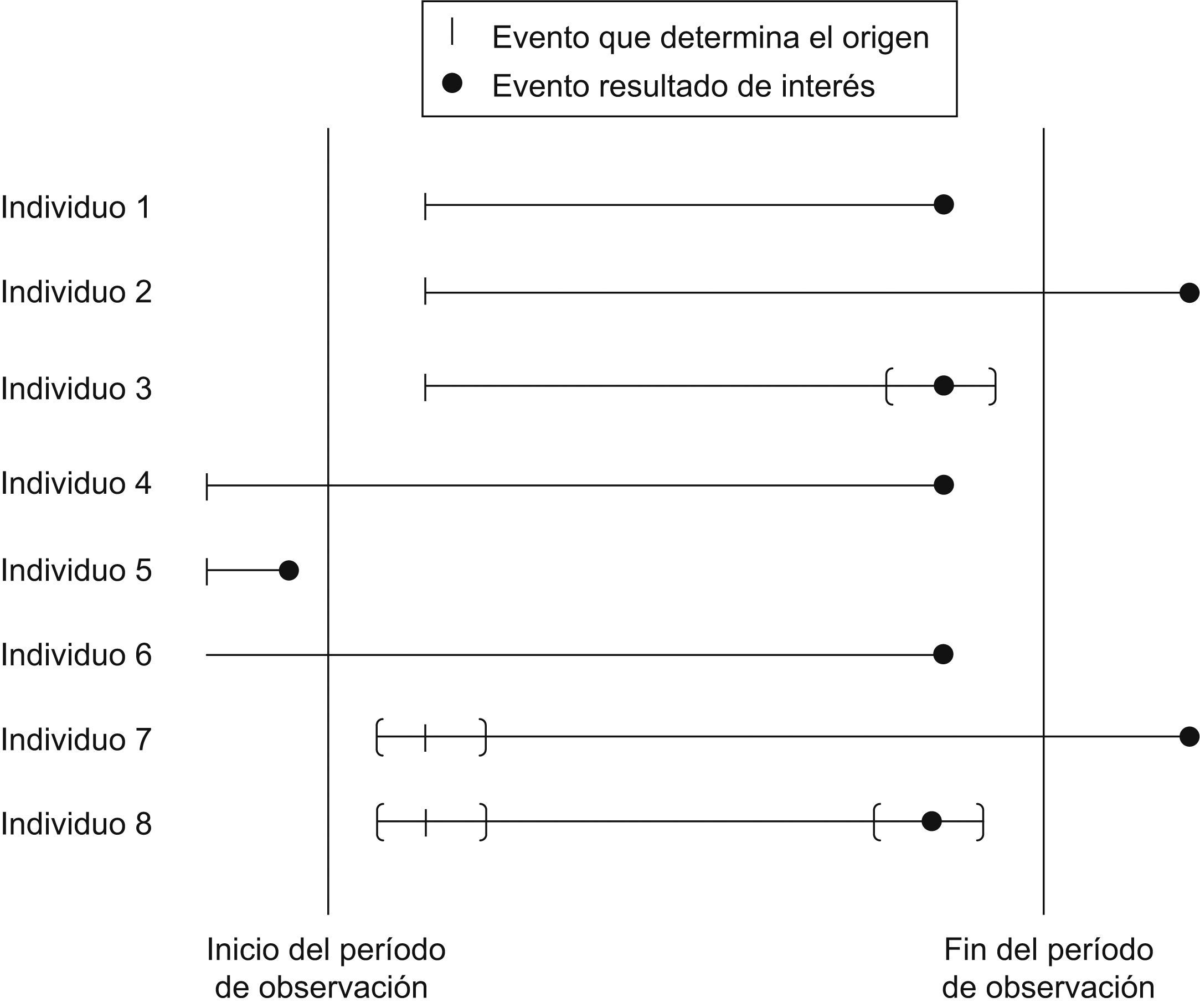
La situación ideal es que el investigador observe con exactitud tanto la ocurrencia del origen como la del episodio de interés (fig. 1, individuo 1). Sin embargo, tanto el origen como el episodio de interés pueden no ser observados por el investigador, dando lugar a observaciones en las que el origen y/o el episodio de interés pueden estar censurados a la derecha, a la izquierda y/o en un intervalo, aspectos clave en el análisis de los datos.
Si el episodio de interés no se observa durante el período de observación, se dice que el episodio está censurado a la derecha (fig. 1, individuo 2). Los principales motivos de censura a la derecha son: fin del estudio (censura administrativa), pérdida en el seguimiento (p. ej: movimientos migratorios o aspectos relacionados con su estado de salud) y ocurrencia de un episodio competitivo que previene la ocurrencia del episodio de interés (p. ej: mortalidad previa a sida cuando el diagnóstico de sida es el episodio de interés). En el ejemplo de la figura 1, el individuo 2 está censurado a la derecha debido a una censura administrativa. Si el episodio de interés ocurre entre 2 fechas consecutivas dentro del período de observación, pero no se sabe exactamente cuándo, se dice que el episodio está censurado en un intervalo (fig. 1, individuo 3). Esta situación es común en la práctica, ya que en determinadas ocasiones se sabe que un sujeto ha muerto pero no se sabe la fecha exacta, aunque sí se puede estimar cuándo ocurrió dentro de un intervalo conocido, ya que el sujeto murió después de su última visita pero antes del día en el que se comunica su muerte.
En algunas ocasiones, el episodio que determina el origen puede haber ocurrido antes de que se inicie el período de observación (fig. 1, individuos 4, 5, 6). Si este origen es desconocido (fig. 1, individuo 6), se dice que el origen está censurado a la izquierda (p. ej: individuos con VIH a la entrada en la cohorte, con fecha de seroconversión desconocida, para el estudio de la supervivencia desde la seroconversión al VIH). Si este origen es conocido (fig. 1, individuos 4, 5), se da lo que se conoce como entradas retardadas o truncamiento a la izquierda (p. ej: individuos con diagnóstico de sida conocido y previo al inicio del período de observación para el estudio de la supervivencia desde sida). Si el origen ocurre entre 2 instantes dentro del período de observación, se dice que el origen está censurado en un intervalo (fig. 1, individuo 7).
En algunas ocasiones, tanto el origen (p. ej: fecha de seroconversión al VIH) como el episodio de interés (ej. diagnóstico de sida) están censurados (fig. 1, individuo 8), lo que da lugar a lo que se conoce como observaciones doblemente censuradas.
Cambio en un marcador medido repetidamente en el tiempoEl estudio de la trayectoria de los marcadores inmunológicos (valores de linfocitos CD4) y virológicos (valores de carga viral) de la infección por VIH tiene un papel fundamental en el conocimiento de la historia natural de la enfermedad y en la evaluación de nuevos tratamientos. Para determinar el cambio en un marcador medido repetidamente en el tiempo deberá disponerse de la medición del marcador de interés medido en diferentes momentos de tiempo.
Principales sesgos de los estudios de cohortes y su aplicación al estudio del virus de la inmunodeficiencia humanaConceptos generales sobre errores sistemáticos y aleatoriosUn sesgo es un error sistemático que resulta en una estimación incorrecta de la frecuencia del episodio de interés (p. ej: cirrosis hepática) y/o de la exposición de interés (p. ej: infección por el virus de la hepatitis C [VHC]) en un estudio descriptivo o de la asociación entre una exposición (p. ej: infección por VHC) y un episodio de interés (p. ej: cirrosis hepática) en un estudio analítico. Los sesgos se pueden producir por cómo se seleccionan los participantes en el estudio (sesgos de selección) y/o por cuáles son los procedimientos de medición y de recogida de información sobre la exposición y/o la enfermedad (sesgos de información). Los sesgos no se pueden solventar con el aumento del tamaño de la muestra, a diferencia de los errores aleatorios, que se atribuyen esencialmente a la variabilidad inherente al proceso de muestreo, y a la propia variabilidad del parámetro que se mide. La ausencia de sesgos o de errores sistemáticos se llama validez interna y la ausencia de errores aleatorizados se llama precisión. La validez externa es la capacidad de hacer extensible la inferencia desde la población estudiada a otras poblaciones y permite generalizar los resultados. Es importante destacar que la mayoría de los estudios de cohortes no suelen tener una selección aleatoria de sus participantes, por lo que su validez externa se ve disminuida y la información que proporcionan no sustituye a la de los registros poblacionales de vigilancia epidemiológica de VIH y sida.
Sesgos de los estudios de cohortesEn el estudio de la historia natural y de la progresión de la infección por VIH es necesario valorar algunos sesgos específicos de la epidemiología del VIH que pueden afectar las estimaciones de interés. En primer lugar, los autores de este artículo se centran en los sesgos comunes a todos los estudios de cohortes y a continuación se presentan los sesgos específicos presentes en las cohortes de seroprevalentes y en las cohortes de seroconvertores.
Las principales fuentes de introducción de sesgos de selección en los estudios de cohortes en los que el episodio resultado de interés es el tiempo transcurrido hasta la ocurrencia del episodio son las derivadas de la no observación del episodio que determina el origen y de la no observación del episodio resultado debido a pérdidas en el seguimiento o a la ocurrencia de un episodio competitivo que previene la ocurrencia del episodio de interés.
La no observación del episodio que determina el origen se refiere a la situación en la que los individuos entran en la cohorte con posterioridad a la ocurrencia del episodio que determina el origen (p. ej: seroconversión al VIH), siendo la fecha de ocurrencia de este evento conocida o pudiéndose estimar con fiabilidad. Este puede ser el caso tanto de cohortes de seroconvertores reconstruidas retrospectivamente para el estudio del tiempo transcurrido desde la seroconversión al VIH hasta la aparición de los diferentes episodios resultado de interés, como de cohortes de seroprevalentes para el estudio del tiempo de sida a muerte con diagnósticos de sida previos a la entrada en la cohorte. En ambas situaciones, la probabilidad de que un individuo se incluya en el análisis depende de su estado vital en el momento de reconstrucción de la cohorte, ya que los individuos que murieron poco después de la seroconversión o del diagnóstico de sida tienen menos posibilidades de ser incluidos en el análisis que aquellos que todavía están vivos, lo que da lugar a un sesgo de supervivencia21,31,32. Para corregir el sesgo de selección derivado de la no observación del episodio que determina el origen es necesario utilizar métodos analíticos que permitan la entrada retardada (o truncamiento a la izquierda) de los individuos en la cohorte, es decir, que sólo consideren la información de los individuos a partir del momento en el que están bajo seguimiento activo en la cohorte. Ignorar la entrada retardada en el análisis produciría una sobrestimación de la mediana del tiempo desde el origen al evento de interés, dado que se está ignorando a los individuos con los tiempos al episodio de interés más cortos33.
Las pérdidas al seguimiento son otra de las principales fuentes de introducción de sesgos de selección en los estudios de cohortes ya que, a menudo, las personas que siguen en el estudio son diferentes de las que no lo hacen; en ocasiones están más sanas y a quienes se pierde es a aquéllos de peor pronóstico, pero en otras ocasiones son las personas más enfermas las que cumplen con las pautas de visitas, y las personas más sanas las que se pierden en el seguimiento. El manejo analítico de los individuos perdidos en el seguimiento puede afectar las estimaciones de interés. Son numerosas las estrategias de censura que se han propuesto para tratar a estos individuos30,34. La aproximación más conservadora consiste en censurar a los individuos perdidos al seguimiento en la fecha en la que fueron vistos por última vez. Si los individuos con mejor pronóstico acuden a las visitas con menor frecuencia que los individuos más enfermos, esta aproximación resultará en una sobrerrepresentación de los individuos que desarrollan el episodio de interés y, por tanto, en una infraestimación del tiempo al episodio de interés. Si, por el contrario, las personas más enfermas o con más riesgo de morir tienden a abandonar el estudio con mayor frecuencia (p. ej: se sienten demasiado enfermas para acudir a las visitas médicas o han muerto por una sobredosis de heroína fuera de la red hospitalaria), esta aproximación resultará en una sobrestimación del tiempo al episodio de interés.
Una posibilidad para minimizar las pérdidas al seguimiento consiste en cruzar los datos de los individuos de la cohorte con información procedente de registros externos como el Registro Nacional de Sida o el Registro de Mortalidad22,35,36. La información proporcionada por los registros externos permite la identificación de casos de sida y/o fallecimientos con posterioridad a la fecha en la que se vio a los individuos por última vez. Sin embargo, debe tenerse en cuenta que si únicamente se actualiza la información de los individuos que aparecen en los registros externos, se producirá una sobrestimación del tiempo al episodio. Para evitar este sesgo, resulta necesaria la actualización adicional de los individuos que no aparecen en los registros externos. Una posibilidad consiste en asumir que los individuos que no aparecen en los registros, permanecen libres del episodio en la fecha de fin del estudio, bajo la asunción de que los registros están perfectamente actualizados. Si la asunción no es cierta, algo probable por los retrasos de notificación de los registros externos, esta aproximación repercutirá en un alargamiento de las personas-tiempo de observación de los individuos sin el episodio, pudiendo producir una infraestimación del tiempo al episodio de interés. Por tanto, resulta necesario conocer el retraso de notificación de los registros (tiempo probable transcurrido entre el diagnóstico y la notificación de un caso al registro) e incorporar esta información en los análisis. Otro de los problemas relacionados con el cruce con registros externos es la posible infranotificación de los registros: conforme aumenta la proporción de casos notificados con respecto al total de casos diagnosticados, mayor es la certeza de que las asunciones realizadas respecto a los casos que no aparecen en los registros sean ciertas. La estimación del período de incubación del sida y de la supervivencia desde la seroconversión es sensible a la estrategia de censura utilizada. Por tanto, es importante que la elección de la estrategia de censura se haga a priori, sobre la base de asunciones razonables sobre la calidad y la exhaustividad de la información de los registros externos.
Otro de los motivos por los que el episodio de interés puede no ser observado durante el seguimiento es porque el individuo experimente un episodio competitivo que prevenga la ocurrencia del episodio de interés. En esta situación, son necesarios métodos alternativos a los métodos de supervivencia estándar, que se presentarán en detalle en otro artículo vinculado a éste, que desarrolla los principales métodos de análisis de datos procedentes de los estudios de cohortes.
Además de los aspectos que se han discutido hasta ahora, hay otros sesgos específicos que hay que valorar en los estudios de cohortes en función de que sean de sujetos seroprevalentes al VIH o de sujetos seroconvertores.
Sesgos en los estudios de cohortes de sujetos seroprevalentes al virus de la inmunodeficiencia humanaEn las cohortes de individuos seroprevalentes se desconoce el tiempo que los individuos llevan infectados por VIH a su entrada en la cohorte. Los principales sesgos en este tipo de estudio son los que resultan de considerar como escala de tiempo en los análisis de supervivencia el tiempo de seguimiento desde la entrada en la cohorte en lugar del tiempo desde la infección por VIH32,37. Cuando la fecha de infección por VIH (p. ej: antes de 1985 en comparación con después de 1985) se asocia tanto al riesgo del episodio de interés (p. ej: muerte por sida) como a la variable bajo estudio (p. ej: ser hemofílico en comparación con ser heterosexual) se puede producir un sesgo por el hecho de que un subgrupo de individuos (hemofílicos) puede aparecer con mayor riesgo del episodio de interés simplemente porque se infectó por VIH antes que el otro subgrupo de comparación. Se ha sugerido que para controlar este sesgo se puede ajustar por el valor basal de un marcador, como el número de células CD4 al inicio del seguimiento. En las cohortes de seroprevalentes con poca dispersión en la intensidad epidémica (p. ej: cohorte de seroprevalentes identificada inmediatamente después del inicio de la epidemia, entre 1979 y 1981), la variación en los tiempos desde la infección por VIH a la entrada en la cohorte es escasa, por lo que se esperaría que el efecto de este sesgo fuera inapreciable.
Sesgos en cohortes de seroconvertoresEl seroconvertor es un individuo peculiar en el sentido de que se percibe con riesgo de infección por VIH. Esta característica hace que los individuos incluidos en una cohorte de seroconvertores puedan no ser representativos de la población con VIH, dando lugar a lo que se conoce como sesgo de selección del seroconvertor. Al principio de la epidemia del VIH en España, las personas infectadas por contacto heterosexual no se percibían con riesgo de infección y no solían realizarse el test para detectar anticuerpos frente al VIH. En consecuencia, los individuos infectados por contacto heterosexual no suelen cumplir el criterio de seroconvertor al no disponer de un test negativo previo al primer test positivo, apareciendo con frecuencia infrarrepresentados en las cohortes de seroconvertores.
Las cohortes de seroconvertores evitan los sesgos derivados del desconocimiento de la duración de la infección presentes en las cohortes de seroprevalentes. Sin embargo, pueden estar sujetos a sesgos derivados de la imputación de la fecha de seroconversion y a sesgos de selección38.
La fecha de seroconversión estimada es una fecha censurada en el intervalo definido por el último test negativo para VIH y el primer test positivo para VIH. Normalmente, se considera como fecha de seroconversión el punto medio de este intervalo, asumiendo que el riesgo de infección por VIH es constante durante todo el intervalo y que los individuos cuyo comportamiento les sitúa a un mayor riesgo de infección se realizan el test para detectar anticuerpos frente al VIH con la misma frecuencia que los individuos con menor riesgo de infección. Esta aproximación proporciona resultados fiables siempre que el tiempo transcurrido entre los sucesivos tests sea inferior a 3 años39. En caso contrario, este método resulta en estimaciones sesgadas del riesgo de progresión a sida y/o a muerte, siendo necesarios métodos alternativos que tengan en cuenta la distribución de la seroincidencia40.
Tal como describe Porter et al38, es fundamental que la fecha de la última prueba negativa para VIH esté documentada. En un análisis comparativo del UK Seroconverter Register, las personas que decían haber tenido una prueba negativa para VIH previa pero que no podían documentarlo tenían una progresión más rápida que aquellos que podían documentarlo. Es muy probable que las personas sin prueba documentada tengan un sesgo de memoria y que hayan infraestimado el tiempo que llevaban infectadas.
Este artículo se ha financiado con ayuda de la Red de Investigación en Sida (RIS) (ISCIII RD06/0006). También ha recibido fondos del CIBERESP y de FIPSE (beca 36491 [A/05]).