Desde la descripción de la infección por el virus de la inmunodeficiencia humana (VIH) se han producido muchos avances en su diagnóstico, seguimiento y tratamiento. Sin embargo, son escasas las aportaciones relacionadas con el área de calidad asistencial.
En este sentido, el Grupo de Estudio de Sida (GESIDA) ha elaborado un documento con 66indicadores de calidad asistencial para la atención de los adultos que viven con el VIH —de los que 22 se consideran relevantes— que recoge con sus estándares de cumplimiento requeridos correspondientes. No disponemos de un documento de estas características para el paciente pediátrico.
MétodosElaboración de indicadores de calidad aplicables a la edad pediátrica a partir del documento de GESIDA y las Guías Españolas para el seguimiento del paciente pediátrico infectado por el VIH. Se analizó cada uno de los indicadores respecto a los estándares requeridos en todos los pacientes <18años controlados en nuestra unidad con el fin de evaluar la asistencia ofrecida.
ResultadosSe obtuvo un total de 61indicadores, 51 adaptados del documento GESIDA para la población adulta y 10adecuados según las guías pediátricas, de los cuales 30 se consideraron relevantes. Se obtuvo un cumplimiento global del 81%, y del 83% en los indicadores relevantes.
ConclusiónLa creación y el cumplimiento de unos estándares de calidad asistencial es imprescindible en la atención del paciente pediátrico infectado por el VIH. La evaluación del seguimiento de nuestros pacientes a partir de estos indicadores ofreció resultados satisfactorios.
Since infection with human immunodeficiency virus (HIV) was first described, there have been many advances in its diagnosis, monitoring and treatment. However, few contributions are related to the area of health care quality.
In this sense, the Spanish Study Group on AIDS (GESIDA) has developed a set of quality care indicators for adult patients living with HIV infection that includes a total of 66indicators, 22 of which are considered to be relevant. Standards were calculated for each of them in order to reflect the level of the quality of care offered to these patients. Similar documents for pediatric patients are currently lacking.
MethodsPreparation of a set of quality care indicators applicable to pediatric patients based on the GESIDA document and the Spanish Guidelines for monitoring of pediatric patients infected with HIV. Each indicator was analysed with respect to the required standards in all patients under 18years of age followed-up in our Unit, with the aim of evaluating the quality of care provided.
ResultsA total of 61indicators were collected (51 from the GESIDA document and 10 from currently available pediatric guidelines), 30 of which were considered to be relevant. An overall compliance of 81%-83% was obtained when assessing the relevant indicators.
ConclusionThe availability of health care quality standards is essential for the care of pediatric HIV-infected patients. The assessment of these indicators in our Unit yielded satisfactory results.
La infección por el virus de la inmunodeficiencia humana (VIH) en la población pediátrica en España se encuentra actualmente en claro descenso debido al mejor manejo y control de la embarazada que vive con el VIH y, como consecuencia, a una disminución de la transmisión vertical del virus1. Según el Registro Nacional de Casos de Sida, la proporción de casos pediátricos en el año 2011 se sitúa, respecto al total de casos, en el 0,2%2.
A pesar de ello, el número de pacientes menores de 18años que viven con el VIH es todavía importante, siendo la transmisión vertical la vía de transmisión más frecuente, representando un 97% de los casos3. La Cohorte Española de Pacientes Pediátricos con VIH (CoRISpe) recoge en la actualidad 838pacientes, controlados en 74centros, de los cuales 536 son actualmente menores de 18años. En nuestra unidad, la atención al paciente pediátrico con VIH se realiza a través del programa multidisciplinar «No estoy solo» (http://www.upiip.com/programa/presentacion.aspx), cuyo objetivo es la educación sanitaria, el apoyo multidisciplinar y, finalmente, la optimización de la calidad de vida de dichos pacientes.
La infección por VIH es una enfermedad crónica y requiere de la participación de distintos profesionales. Del correcto seguimiento, control y calidad de atención sanitaria dependerá, en gran parte, el pronóstico del paciente. Por tanto, la elaboración de indicadores para monitorizar la calidad asistencial es imprescindible. Así, aunque no siempre se ha dispuesto de una metodología que permitiera medir el nivel de calidad en todos y cada uno de los procesos médicos, en los últimos años se ha avanzado notablemente, y en la actualidad existen en nuestro país sistemas de garantía de calidad asistencial en casi todos los campos de la atención sanitaria4-7.
En el campo de la atención al paciente que vive con el VIH, el Grupo de Estudio de Sida (GESIDA) ha presentado recientemente un documento de indicadores de calidad asistencial para personas adultas infectadas por el VIH en el que se recogen las aportaciones de un Comité de profesionales asesorados por el Instituto Universitario Avedis Donabedian y evaluados por un equipo de asesores externos8. En dicho trabajo, el equipo redactor consensuó un estándar para cada indicador que representa el nivel de buena práctica exigible dada la evidencia científica y a la vez alcanzable con los medios disponibles, entendiendo que este no debe reflejar los resultados de la práctica habitual. El documento final recoge 66indicadores (estructura: 5, proceso: 45, resultados: 16), de los que finalmente se seleccionaron 22 como relevantes, y que GESIDA entiende que todas las unidades VIH deben monitorizar para evaluar sus resultados y así poder introducir opciones de mejora.
Ante la ausencia de trabajos en esta línea en el ámbito del paciente VIH pediátrico, los objetivos principales del presente trabajo son: a)revisar la potencial adaptación a la edad pediátrica de los marcadores de calidad y seleccionar los potencialmente aplicables a este grupo de edad; b)incorporar nuevos indicadores para la edad pediátrica, y c)elaborar un documento final donde consten los indicadores aplicables a las unidades VIH pediátricas, definiendo los considerados relevantes en este grupo.
El objetivo secundario es analizar la calidad en la asistencia sanitaria ofrecida a los niños y adolescentes con infección por el VIH atendidos en el proyecto «No estoy solo» mediante los indicadores propuestos para la población pediátrica, para que de esta manera se pueda alcanzar el estándar óptimo de atención que dichos pacientes requieren.
Pacientes y métodosElección de los indicadoresSe evaluaron los 66 indicadores elaborados por GESIDA, y posteriormente el subgrupo de los 22 más relevantes, excluyendo aquellos no aplicables en pediatría —detallando la causa de la exclusión— y se realizó la adaptación de los mismos a la población pediátrica.
Se elaboraron nuevos indicadores a partir de las guías publicadas para el seguimiento del paciente pediátrico infectado por VIH por parte del Grupo Colaborativo Español de VIH Pediátrico (CEVIHP), la Sociedad Española de Infectología Pediátrica (SEIP), la Asociación Española de Pediatría (AEP) y la Secretaría del Plan Nacional sobre el Sida (SPNS)9 y de las recomendaciones para el seguimiento del niño expuesto al VIH y a los antirretrovirales durante la gestación y el periodo neonatal de la SEIP10.
Se consideraron como relevantes los indicadores exigibles a toda unidad que realice el seguimiento de estos pacientes, siguiendo el modelo del documento elaborado por GESIDA para el paciente adulto.
La selección de los indicadores se realizó según la técnica de grupos nominales. Los autores que fueron los encargados de la selección son pediatras con especial dedicación a la infectología pediátrica (P.S.P., A.C.P., A.M.N., M.E. y C.F.) y farmacéuticos (A.F.P.), respectivamente. Además, se contó con la colaboración de una psicóloga (C.R.) y de 2enfermeras (A.A. y M.A.A.) para la selección de los indicadores correspondientes a sus áreas de conocimiento.
Valoración de los estándares de cumplimiento de los indicadoresSe comparó el grado de cumplimiento de cada indicador con respecto a los estándares que representan el nivel de buena práctica exigible según la guía elaborada por GESIDA para la población adulta, por lo cual se extrajo de dicha guía la explicación de términos para realizar la valoración de los cumplidos y los no cumplidos, analizando el porqué en ambos casos y proponiendo acciones de mejora.
En la determinación de los porcentajes necesarios para considerar un buen cumplimiento de cada uno de los indicadores evaluados se tuvo en cuenta el menor tamaño de la muestra que representa la población infantil con infección por el VIH en comparación con la adulta, por lo que se consideró como cumplido todo aquel indicador con un cumplimiento ≥95% del exigido para la población adulta.
Respecto a los indicadores elaborados a partir de las guías pediátricas, se establecieron los estándares correspondientes así como la explicación de términos, obtenida también de datos bibliográficos. Se consideró como cumplido todo aquel indicador con una adecuación ≥95% de la exigida.
Del mismo modo, para los indicadores de hospitalización y mortalidad se usaron comparadores basados en literatura pediátrica reciente para evitar sesgos relacionados con la edad del paciente y factores de riesgo asociados a la misma11.
Análisis de los niveles de evidenciaSe analizaron los niveles de evidencia en 3grupos (según pautas recomendadas de tratamiento antirretroviral [TARV] de GESIDA, y las utilizadas en recomendaciones de TARV en niños y adolescentes infectados por VIH)12.
Nivel A: Estudios y/o ensayos clínicos aleatorizados y controlados.
Nivel B: Estudios de cohortes o de casos y controles.
Nivel C: Opinión de expertos, basada en experiencia clínica o estudios descriptivos.
Cada indicador se evaluó utilizando la medida de frecuencia adecuada a su naturaleza: proporción, en caso de variables cualitativas, y mediana, en caso de variables cuantitativas. Estas mismas medidas se utilizaron para describir la muestra de la que se obtuvo información. Se incluyó el intervalo de confianza al 95% (IC95%) en las proporciones que se consideraron de mayor interés
Pacientes incluidos en la evaluaciónLos resultados obtenidos se utilizaron para la evaluación de los pacientes <18 años infectados por el VIH controlados en el programa «No estoy solo» de la Unitat de Patologia Infecciosa i Immunodeficiències de Pediatria (UPIIP) del Hospital Universitari Vall d’Hebron (Barcelona) hasta el mes de enero de 2011. Dichos pacientes forman parte en su totalidad de CoRISpe, obteniéndose la información basal de la base de datos que la recoge.
No se incluyeron los pacientes >18 años de edad aún en seguimiento en la unidad ni los menores de edad que por algún motivo se habían trasladado a la unidad de adultos de nuestro centro o a otros centros.
En cuanto a los indicadores que evalúan hospitalización y mortalidad, se recogieron los datos de los últimos 5años (2006-2011), por tratarse de población pediátrica —con un menor número de ingresos y menos fallecimientos anuales—.
Consideraciones éticasEl estudio fue aprobado por el Comité Ético de Investigación Clínica del centro.
ResultadosSe definieron un total de 61indicadores del documento final que se recoge en la tabla 1 y se detalla en el anexo 1 disponible online, y que se obtuvo a partir de las siguientes fuentes:
- 1)
Extraídos del documento de GESIDA y adaptados a la población pediátrica: 51indicadores (condiciones estructurales: 4; diagnóstico y evaluación inicial: 7; seguimiento e intervenciones orientadas a la prevención: 16; seguimiento de pacientes en tratamiento: 10; aspectos específicos en la mujer [VIH en la mujer]: 1; comorbilidades: 3; hospitalización: 5; índices de mortalidad: 2, y formación e investigación: 3).
El 86% de estos indicadores no han requerido modificaciones significativas.
En cuanto a los indicadores adaptados, las modificaciones se realizaron siguiendo las recomendaciones para la atención y el seguimiento del paciente pediátrico VIH9. La justificación de la adaptación, así como de los indicadores que fueron rechazados, se encuentra disponible en el material suplementario online.
- 2)
Obtenidos de las Guías Españolas para el Seguimiento del Paciente Pediátrico Infectado por el VIH9 y de las Recomendaciones para el seguimiento del niño expuesto al VIH y a los antirretrovirales durante la gestación y el periodo neonatal de la SEIP10: 10indicadores (diagnóstico y evaluación inicial: 2; seguimiento e intervenciones orientadas a la prevención: 6, y seguimiento de pacientes en tratamiento: 2).
Indicadores elaborados para la edad pediátrica a partir del documento de GESIDA y las Guías de Seguimiento del Paciente Pediátrico con VIH de CEVIHP/SEIP/AEP/SPNS
| Condiciones estructurales |
| 1) Atención por médico especializado |
| 2) Disponibilidad de recursos diagnósticos |
| 3) Farmacia externa para dispensación de fármacos |
| 4) Condiciones de intimidad y confidencialidad estructural |
| Diagnóstico y evaluación inicial |
| 5) Tiempo transcurrido entre diagnóstico VIH y primer control en atención especializada (AE) |
| 6) Diagnóstico tardío de la infección VIH en AE |
| 7) Carga viral (CV) plasmática |
| 8) Determinación de subpoblaciones linfocitarias (linfocitosT CD4+) |
| 9) Educación sanitaria en la valoración inicial |
| 10) Valoración social al inicio |
| 11) Pacientes con <350/mm3linfocitos T CD4+ en ≥6 años o <15% en <6 años de edad, sin TARV |
| Seguimiento e intervenciones orientadas a la prevención |
| 12) Periodicidad de las visitas (seguimiento regular) |
| 13) Estudio renal básico en pacientes VIH |
| 14) Valoración de enfermería |
| 15) Detección de la infección tuberculosa/enfermedad tuberculosa |
| 16) Vacunación frente a hepatitis A |
| 17) Vacunación frente a hepatitis B |
| 18) Vacunación frente a infección neumocócica |
| 19) Profilaxis frente aPneumocystis jiroveciiyToxoplasma gondiien pacientes con <200linfocitos T CD4+/mm3(≥6años) o <15% (<6años) y en todos los menores de 12meses |
| 20) Tratamiento y prevención del tabaquismo |
| 21) Evaluación de la ingesta alcohólica |
| 22) Seguimiento de medidas de prevención de riesgo |
| 23) Tratamiento de la infección tuberculosa latente |
| 24) Pérdidas de seguimiento |
| 25) Recuperación de citas fallidas |
| 26) Informe periódico de consulta |
| 27) Calidad percibida por los pacientes |
| Seguimiento de pacientes en tratamiento |
| 28) Adecuación de las pautas iniciales de TARV a las guías españolas (CEVIHP/SEIP/AEP/SPNS) |
| 29) Inicio de TARV en pacientes con eventos B o C |
| 30) Primera visita tras instauración de un TARV |
| 31) CV indetectable (<50copias/ml) en la semana 48 de tratamiento |
| 32) Tratamiento con abacavir (ABC) sin estudio de HLA-B*5701 previo |
| 33) Cambios de tratamiento durante el primer año |
| 34) Registro de adherencia al tratamiento |
| 35) Estudio de resistencias en el fracaso virológico |
| 36) Respuesta al TARV en situación de fracaso avanzado |
| 37) Gasto medio por paciente en primer tratamiento |
| Aspectos específicos en la mujer (VIH en la mujer) |
| 38) Incidencia de transmisión vertical |
| Comorbilidades |
| 39) Evaluación del paciente coinfectado por VHC |
| 40) Pacientes con HBsAg que reciben tratamiento eficaz |
| 41) Control ecográfico de la hepatopatía |
| Hospitalización |
| 42) Incidencia de ingresos en pacientes en seguimiento |
| 43) Pacientes con informe de alta tras hospitalización |
| 44) Informes de alta en pacientes fallecidos en el hospital |
| 45) Seguimiento en consultas externas tras el alta hospitalaria |
| 46) Autopsias-necropsias en pacientes VIH |
| Índices de mortalidad |
| 47) Tasa mortalidad global en pacientes en seguimiento |
| 48) Tasa de mortalidad por causas relacionadas con sida |
| Formación e investigación |
| 49) Formación continuada |
| 50) Publicaciones y comunicaciones a congresos |
| 51) Participación en proyectos de investigación |
| Indicadores obtenidos a partir de las Guías de Seguimiento del paciente pediátrico que vive con el VIH y Recomendaciones de seguimiento del niño expuesto al VIH y a antirretrovirales durante la gestación y el periodo neonatal |
| Diagnóstico y evaluación inicial |
| 52) Contenidos relevantes de la valoración inicial del niño y adolescente con VIH |
| 53) Pruebas complementarias en la valoración inicial del niño y adolescente con VIH |
| Seguimiento e intervenciones orientadas a la prevención |
| 54) Contenidos relevantes de la valoración inicial en la embarazada con infección VIH |
| 55) Seguimiento del hijo de madre VIH, no infectado |
| 56) Cribado de enfermedades de transmisión sexual en adolescentes con el VIH |
| 57) Monitorización de las concentraciones plasmáticas de antirretrovirales (MCP-ARV) |
| 58) Crecimiento y desarrollo en niños y adolescentes infectados por el VIH |
| 59) Estudio de inmunoprotección frente a antígenos vacunales |
| Seguimiento de pacientes en tratamiento |
| 60) Traspaso coordinado de los adolescentes VIH a la unidad de adultos |
| 61) Valoración neuropsicológica de los pacientes VIH en seguimiento |
En negrita, los 30 indicadores considerados como relevantes.
Finalmente se consideraron como relevantes 30indicadores (tabla 1, resaltados en negrita).
Resultados obtenidos del cumplimiento de los distintos indicadoresSe incluyó, para su evaluación, un total de 32 niños y adolescentes con infección VIH de entre 4 y 18años (mediana 13,2años), sin diferencias entre sexos.
Del total de pacientes evaluados, 22 (68,75% [IC95%: 50-83,9]) presentaban cargas virales (CV) indetectables (<50 copias/ml) en el momento del estudio, con recuentos de linfocitosT CD4+ entre 221 y 1.654/mm3, con una mediana de 770/mm3. Solo 2pacientes (6,25%) presentaban signos de inmunodepresión grave, 4pacientes (12,5%) moderada y la gran mayoría (81,25% [IC95%: 63,6-92,8]) no presentaban signos de inmunosupresión o esta era leve. Ocho pacientes no recibían TARV por tratarse de pacientes naive o haberse sometido a una interrupción estructurada del tratamiento.
Las tablas recogen los resultados obtenidos al aplicar los indicadores de calidad asistencial a nuestra cohorte de pacientes pediátricos con VIH.
Tras la valoración de los diferentes indicadores en el seguimiento de nuestros pacientes se obtuvo un porcentaje global de cumplimiento del 81% (83% en los indicadores relevantes).
Se excluyeron 2indicadores en el cálculo del porcentaje global: uno correspondiente al apartado de comorbilidades (pacientes con HBsAg que reciben tratamiento eficaz, ya que no se incluyó ningún paciente con coinfección VIH-VHB en la muestra) y el otro correspondiente a índices de mortalidad (tasa de mortalidad por causas relacionadas con sida) por no disponer de un estándar establecido. Así pues, dicho cálculo se realizó sobre 59indicadores.
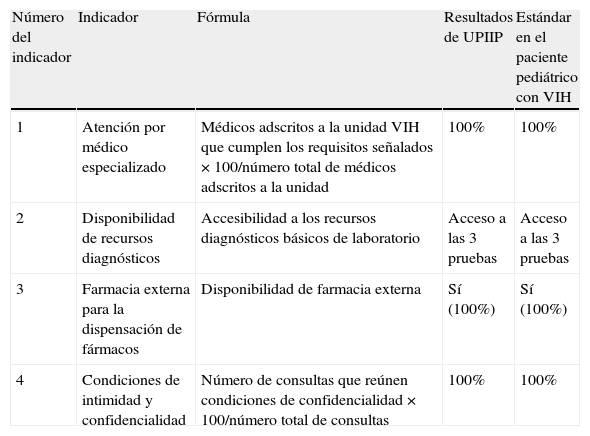
Indicadores adaptados del documento de GESIDA para la población adulta8Condiciones estructuralesSe cumplieron los estándares en los 4indicadores evaluados en este apartado (100%) (tabla 2).
Valoración del cumplimiento de los indicadores correspondientes a condiciones estructurales a partir del documento de GESIDA
| Número del indicador | Indicador | Fórmula | Resultados de UPIIP | Estándar en el paciente pediátrico con VIH |
| 1 | Atención por médico especializado | Médicos adscritos a la unidad VIH que cumplen los requisitos señalados×100/número total de médicos adscritos a la unidad | 100% | 100% |
| 2 | Disponibilidad de recursos diagnósticos | Accesibilidad a los recursos diagnósticos básicos de laboratorio | Acceso a las 3 pruebas | Acceso a las 3 pruebas |
| 3 | Farmacia externa para la dispensación de fármacos | Disponibilidad de farmacia externa | Sí (100%) | Sí (100%) |
| 4 | Condiciones de intimidad y confidencialidad | Número de consultas que reúnen condiciones de confidencialidad×100/número total de consultas | 100% | 100% |
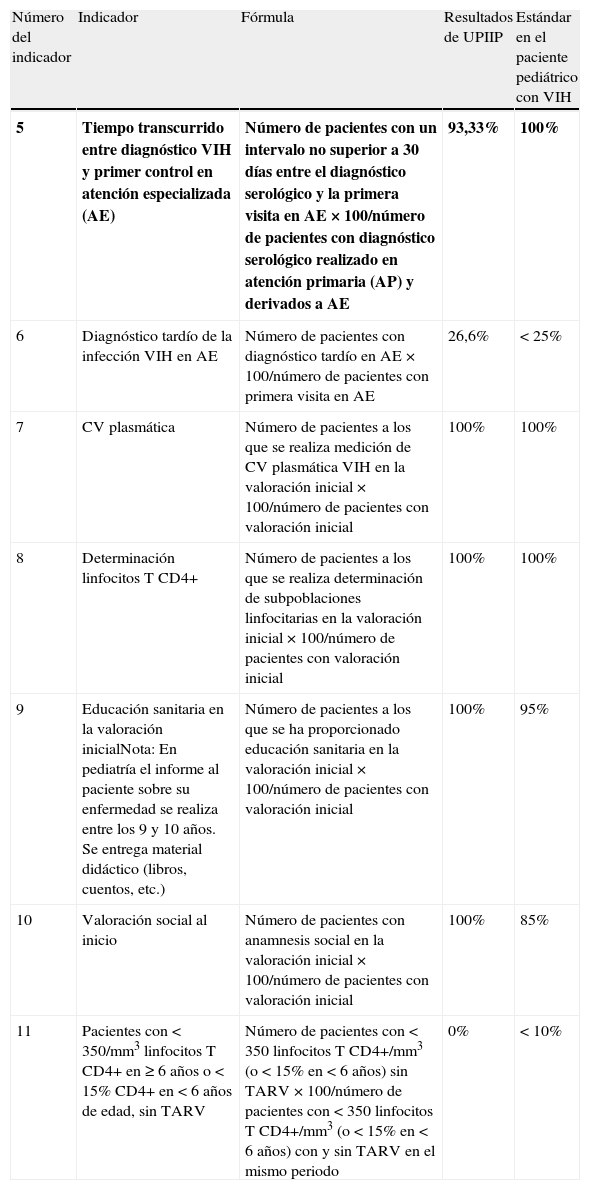
Se cumplieron los estándares en 6 de los 7indicadores (86%) (tabla 3).
Valoración del cumplimiento de los indicadores correspondientes a diagnóstico y evaluación inicial a partir del documento de GESIDA
| Número del indicador | Indicador | Fórmula | Resultados de UPIIP | Estándar en el paciente pediátrico con VIH |
| 5 | Tiempo transcurrido entre diagnóstico VIH y primer control en atención especializada (AE) | Número de pacientes con un intervalo no superior a 30 días entre el diagnóstico serológico y la primera visita en AE×100/número de pacientes con diagnóstico serológico realizado en atención primaria (AP) y derivados a AE | 93,33% | 100% |
| 6 | Diagnóstico tardío de la infección VIH en AE | Número de pacientes con diagnóstico tardío en AE×100/número de pacientes con primera visita en AE | 26,6% | < 25% |
| 7 | CV plasmática | Número de pacientes a los que se realiza medición de CV plasmática VIH en la valoración inicial×100/número de pacientes con valoración inicial | 100% | 100% |
| 8 | Determinación linfocitosT CD4+ | Número de pacientes a los que se realiza determinación de subpoblaciones linfocitarias en la valoración inicial×100/número de pacientes con valoración inicial | 100% | 100% |
| 9 | Educación sanitaria en la valoración inicialNota: En pediatría el informe al paciente sobre su enfermedad se realiza entre los 9 y 10años. Se entrega material didáctico (libros, cuentos, etc.) | Número de pacientes a los que se ha proporcionado educación sanitaria en la valoración inicial×100/número de pacientes con valoración inicial | 100% | 95% |
| 10 | Valoración social al inicio | Número de pacientes con anamnesis social en la valoración inicial×100/número de pacientes con valoración inicial | 100% | 85% |
| 11 | Pacientes con <350/mm3 linfocitosT CD4+ en ≥6años o <15% CD4+ en <6años de edad, sin TARV | Número de pacientes con <350linfocitosT CD4+/mm3 (o <15% en <6años) sin TARV×100/número de pacientes con <350linfocitosT CD4+/mm3 (o <15% en <6años) con y sin TARV en el mismo periodo | 0% | <10% |
En negrita los indicadores que no se cumplieron al evaluar el seguimiento de nuestros pacientes.
Se cumplieron los estándares en 12 de los 16indicadores (75%) (tabla 4).
Valoración del cumplimiento de los indicadores correspondientes a seguimiento e intervenciones orientadas a la prevención a partir del documento de GESIDA
| Número del indicador | Indicador | Fórmula | Resultados de UPIIP | Estándar en el paciente pediátrico con VIH |
| 12 | Periodicidad de las visitas (seguimiento regular) | Número de pacientes con seguimiento adecuado que acuden de forma regular a la consulta×100/número de pacientes en seguimiento | 93,75% | 85% |
| 13 | Estudio renal básico en pacientes VIHNota: en los pacientes tratados con tenofovir se monitoriza la función renal mediante vigilancia clínica, bioquímica y tira de orina cada 6meses en el 100% de los casos | Número de pacientes VIH con estudio renal básico bienal×100/número de pacientes VIH en seguimiento regular | 46,87% | 100% |
| 14 | Valoración de enfermería | Número de pacientes valorados por enfermería×100/número de personas con VIH en seguimiento regular | 90% | 90% |
| 15 | Detección de la infección tuberculosa latente (ITL) | Número de pacientes en los que se ha realizado detección de ITL×100/número de pacientes en seguimiento regular | 100% | 90% |
| 16 | Vacunación frente a la hepatitisA | Número de pacientes a los que se ha realizado indicación expresa de las vacunas frente a VHA×100/número de pacientes en seguimiento regular | 53,86% | 85% |
| 17 | Vacunación frente a la hepatitisB | Número de pacientes a los que se ha realizado indicación expresa de las vacunas frente a VHB×100/número de pacientes en seguimiento regular | 88,46% | 85% |
| 18 | Vacunación frente a la infección neumocócica | Número de pacientes a los que se ha realizado indicación expresa de vacunación antineumocócica×100/número de pacientes en seguimiento regular | 76,92% | 85% |
| 19 | Profilaxis frente a Pneumocystis jirovecii y Toxoplasma gondii en pacientes con <200 linfocitosT CD4+/mm3 (≥6 años) o <15% CD4 (<6años) y en todos los menores de 12meses | Número de pacientes con <200linfocitosT CD4+/mm3 (≥6años) o <15% CD4 (<6años) o menores de 12meses que reciben profilaxis frente a P.jirovecii y T.gondii×100/número de pacientes en seguimiento regular con <200linfocitosT CD4+/mm3 (≥6años) o <15% CD4 (<6años) | 100% | 100% |
| 20 | Tratamiento y prevención del tabaquismo | Número de pacientes con hábito tabáquico activo e intervención anual×100/número de pacientes con hábito tabáquico activo | 100% | 95% |
| 21 | Evaluación de la ingesta de alcohol | Número de pacientes en los que se ha registrado la ingesta alcohólica en el último año×100/número de pacientes en seguimiento | 100% | 95% |
| 22 | Seguimiento de medidas de prevención de riesgos | Número de visitas en las que se han indagado sobre conductas de riesgo, prevención e infecciones de transmisión sexual (ITS)×100/número de visitas de pacientes en seguimiento | 100% | 80% |
| 23 | Tratamiento de la infección tuberculosa latente (ITL) | Número de pacientes con ITL a los que se ha indicado tratamiento (quimioprofilaxis)×100/número de pacientes con enfermedad tuberculosa latente | 100% | 95% |
| 24 | Pérdidas de seguimiento | Número de pacientes VIH perdidos en seguimiento en los últimos 12meses×100/número de pacientes VIH en programa | 6,25% | <5% |
| 25 | Recuperación de citas fallidas | Número de citas fallidas, con nueva citación×100/número de citas fallidas | 100% | 85% |
| 26 | Informe periódico de consulta | Número de pacientes con informe periódico de consulta×100/número de pacientes en seguimiento regular | 90,62% | 90% |
| 27 | Calidad percibida por los pacientes | Realización periódica (cada 2años) de un estudio de opinión de los pacientes | No se realiza | Un estudio de opinión cada 2años |
En negrita los indicadores que no se cumplieron al evaluar el seguimiento de nuestros pacientes.
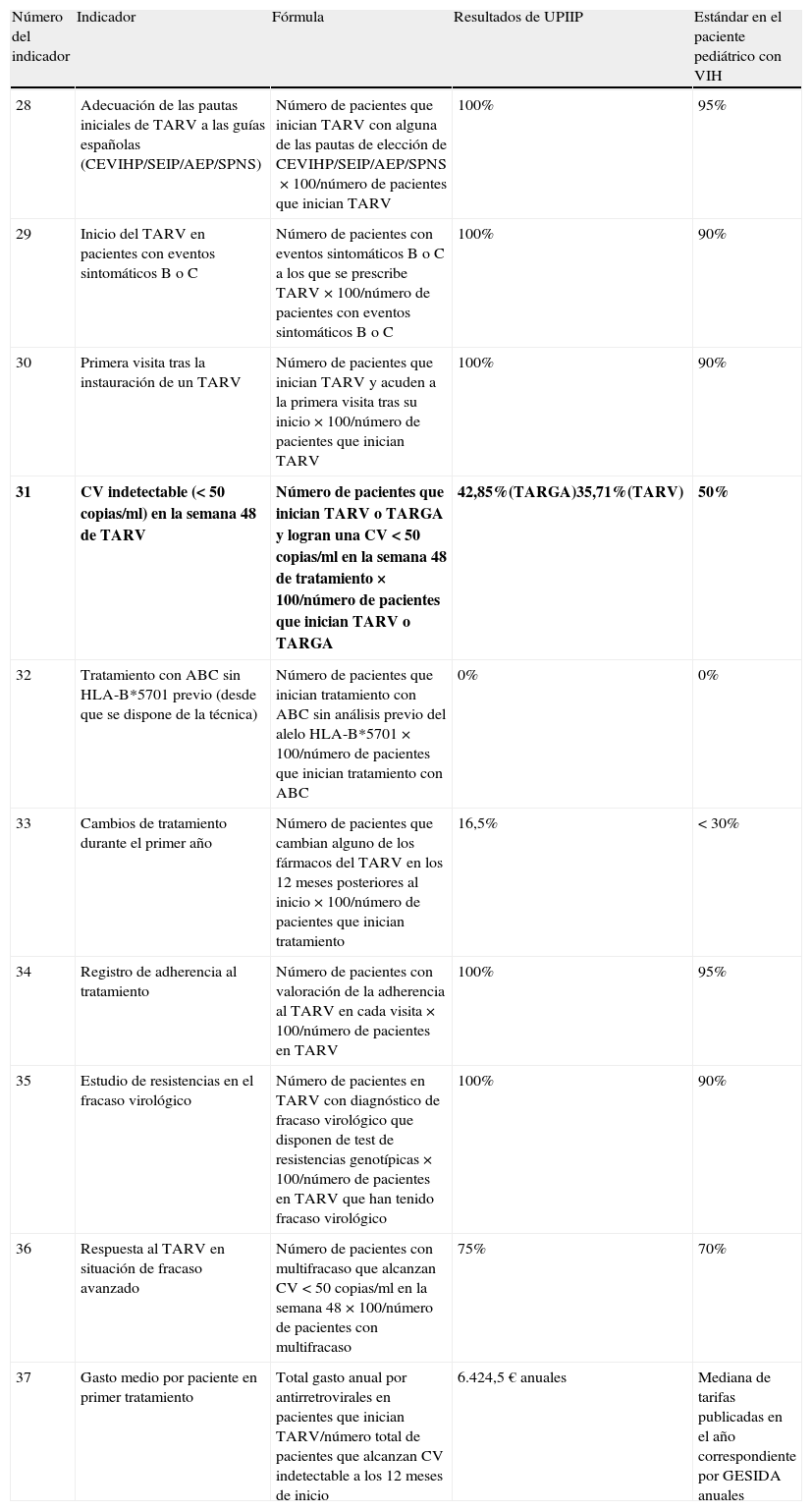
De los 10 indicadores evaluables se cumplieron los estándares en 9 de ellos (90%) (tabla 5).
Valoración del cumplimiento de los indicadores correspondientes a seguimiento de pacientes en tratamiento a partir del documento de GESIDA
| Número del indicador | Indicador | Fórmula | Resultados de UPIIP | Estándar en el paciente pediátrico con VIH |
| 28 | Adecuación de las pautas iniciales de TARV a las guías españolas (CEVIHP/SEIP/AEP/SPNS) | Número de pacientes que inician TARV con alguna de las pautas de elección de CEVIHP/SEIP/AEP/SPNS×100/número de pacientes que inician TARV | 100% | 95% |
| 29 | Inicio del TARV en pacientes con eventos sintomáticos B o C | Número de pacientes con eventos sintomáticos B o C a los que se prescribe TARV×100/número de pacientes con eventos sintomáticos B o C | 100% | 90% |
| 30 | Primera visita tras la instauración de un TARV | Número de pacientes que inician TARV y acuden a la primera visita tras su inicio×100/número de pacientes que inician TARV | 100% | 90% |
| 31 | CV indetectable (<50copias/ml) en la semana 48 de TARV | Número de pacientes que inician TARV o TARGA y logran una CV<50copias/ml en la semana 48 de tratamiento×100/número de pacientes que inician TARV o TARGA | 42,85%(TARGA)35,71%(TARV) | 50% |
| 32 | Tratamiento con ABC sin HLA-B*5701 previo (desde que se dispone de la técnica) | Número de pacientes que inician tratamiento con ABC sin análisis previo del alelo HLA-B*5701×100/número de pacientes que inician tratamiento con ABC | 0% | 0% |
| 33 | Cambios de tratamiento durante el primer año | Número de pacientes que cambian alguno de los fármacos del TARV en los 12meses posteriores al inicio×100/número de pacientes que inician tratamiento | 16,5% | < 30% |
| 34 | Registro de adherencia al tratamiento | Número de pacientes con valoración de la adherencia al TARV en cada visita×100/número de pacientes en TARV | 100% | 95% |
| 35 | Estudio de resistencias en el fracaso virológico | Número de pacientes en TARV con diagnóstico de fracaso virológico que disponen de test de resistencias genotípicas×100/número de pacientes en TARV que han tenido fracaso virológico | 100% | 90% |
| 36 | Respuesta al TARV en situación de fracaso avanzado | Número de pacientes con multifracaso que alcanzan CV<50 copias/ml en la semana 48×100/número de pacientes con multifracaso | 75% | 70% |
| 37 | Gasto medio por paciente en primer tratamiento | Total gasto anual por antirretrovirales en pacientes que inician TARV/número total de pacientes que alcanzan CV indetectable a los 12meses de inicio | 6.424,5€ anuales | Mediana de tarifas publicadas en el año correspondiente por GESIDA anuales |
En negrita los indicadores que no se cumplieron al evaluar el seguimiento de nuestros pacientes.
Aspectos específicos en la mujer (VIH en la mujer): se cumplió el estándar evaluado (100%) (tabla 6).
Valoración del cumplimiento de los indicadores correspondientes a aspectos específicos en la mujer (VIH en la mujer) a partir del documento de GESIDA
| Número del indicador | Indicador | Fórmula | Resultados de UPIIP | Estándar propuesto para TV |
| 38 | Incidencia de transmisión vertical | Número de hijos nacidos infectados por el VIH de madres infectadas por el VIH×100/número de hijos nacidos de madres infectadas por el VIH | 1,5% | <2% |
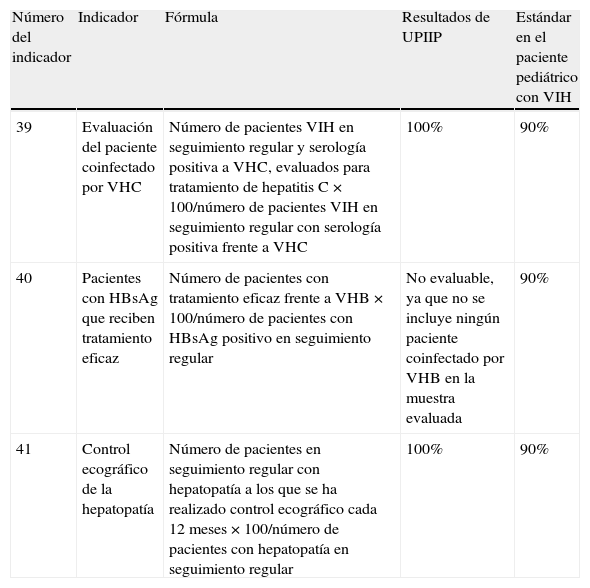
Se cumplieron los estándares en los 2indicadores (100%) (tabla 7). Como se comenta en el apartado correspondiente a la infección por el virus de la hepatitisB, en las tablas este no fue valorado por no incluirse en este estudio pacientes con coinfección por este virus.
Valoración del cumplimiento de los indicadores correspondientes a comorbilidades a partir del documento de GESIDA
| Número del indicador | Indicador | Fórmula | Resultados de UPIIP | Estándar en el paciente pediátrico con VIH |
| 39 | Evaluación del paciente coinfectado por VHC | Número de pacientes VIH en seguimiento regular y serología positiva a VHC, evaluados para tratamiento de hepatitisC×100/número de pacientes VIH en seguimiento regular con serología positiva frente a VHC | 100% | 90% |
| 40 | Pacientes con HBsAg que reciben tratamiento eficaz | Número de pacientes con tratamiento eficaz frente a VHB×100/número de pacientes con HBsAg positivo en seguimiento regular | No evaluable, ya que no se incluye ningún paciente coinfectado por VHB en la muestra evaluada | 90% |
| 41 | Control ecográfico de la hepatopatía | Número de pacientes en seguimiento regular con hepatopatía a los que se ha realizado control ecográfico cada 12meses×100/número de pacientes con hepatopatía en seguimiento regular | 100% | 90% |
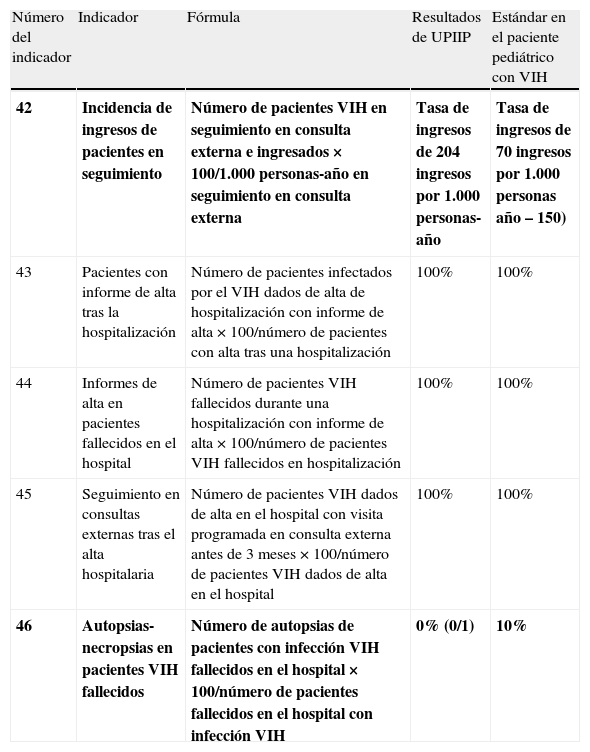
Se cumplieron los estándares en 3 de los 5indicadores (60%) (tabla 8).
Valoración del cumplimiento de los indicadores correspondientes a hospitalización a partir del documento de GESIDA
| Número del indicador | Indicador | Fórmula | Resultados de UPIIP | Estándar en el paciente pediátrico con VIH |
| 42 | Incidencia de ingresos de pacientes en seguimiento | Número de pacientes VIH en seguimiento en consulta externa e ingresados×100/1.000personas-año en seguimiento en consulta externa | Tasa de ingresos de 204ingresos por 1.000personas-año | Tasa de ingresos de 70ingresos por 1.000personas año–150) |
| 43 | Pacientes con informe de alta tras la hospitalización | Número de pacientes infectados por el VIH dados de alta de hospitalización con informe de alta×100/número de pacientes con alta tras una hospitalización | 100% | 100% |
| 44 | Informes de alta en pacientes fallecidos en el hospital | Número de pacientes VIH fallecidos durante una hospitalización con informe de alta×100/número de pacientes VIH fallecidos en hospitalización | 100% | 100% |
| 45 | Seguimiento en consultas externas tras el alta hospitalaria | Número de pacientes VIH dados de alta en el hospital con visita programada en consulta externa antes de 3meses×100/número de pacientes VIH dados de alta en el hospital | 100% | 100% |
| 46 | Autopsias-necropsias en pacientes VIH fallecidos | Número de autopsias de pacientes con infección VIH fallecidos en el hospital×100/número de pacientes fallecidos en el hospital con infección VIH | 0% (0/1) | 10% |
En negrita los indicadores que no se cumplieron al evaluar el seguimiento de nuestros pacientes.
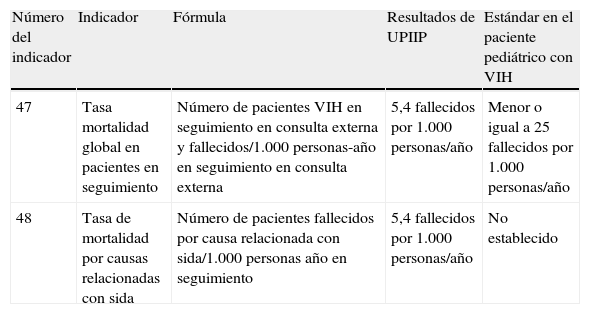
Se cumplió el estándar en el indicador evaluado con datos comparativos de adultos (100%) (tabla 9).
Valoración del cumplimiento de los indicadores correspondientes a índices de mortalidad a partir del documento de GESIDA
| Número del indicador | Indicador | Fórmula | Resultados de UPIIP | Estándar en el paciente pediátrico con VIH |
| 47 | Tasa mortalidad global en pacientes en seguimiento | Número de pacientes VIH en seguimiento en consulta externa y fallecidos/1.000 personas-año en seguimiento en consulta externa | 5,4 fallecidos por 1.000personas/año | Menor o igual a 25fallecidos por 1.000personas/año |
| 48 | Tasa de mortalidad por causas relacionadas con sida | Número de pacientes fallecidos por causa relacionada con sida/1.000personas año en seguimiento | 5,4 fallecidos por 1.000personas/año | No establecido |
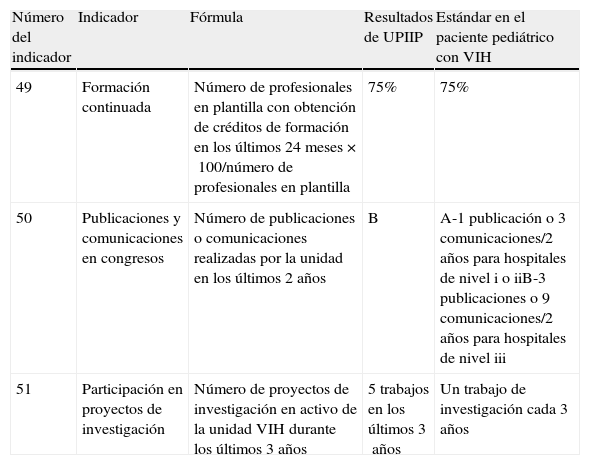
Se cumplieron los estándares en los 3 indicadores (100%) (tabla 10).
Valoración del cumplimiento de los indicadores correspondientes a formación e investigación a partir del documento de GESIDA
| Número del indicador | Indicador | Fórmula | Resultados de UPIIP | Estándar en el paciente pediátrico con VIH |
| 49 | Formación continuada | Número de profesionales en plantilla con obtención de créditos de formación en los últimos 24meses×100/número de profesionales en plantilla | 75% | 75% |
| 50 | Publicaciones y comunicaciones en congresos | Número de publicaciones o comunicaciones realizadas por la unidad en los últimos 2años | B | A-1 publicación o 3comunicaciones/2años para hospitales de nivel i o iiB-3 publicaciones o 9comunicaciones/2años para hospitales de nivel iii |
| 51 | Participación en proyectos de investigación | Número de proyectos de investigación en activo de la unidad VIH durante los últimos 3años | 5trabajos en los últimos 3años | Un trabajo de investigación cada 3años |
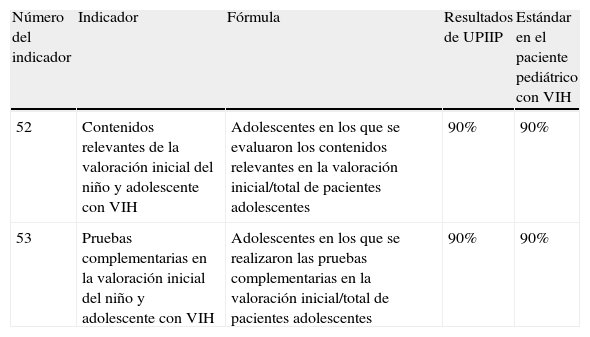
Se cumplieron los estándares establecidos en los 2 indicadores que integran este grupo (100%) (tabla 11).
Valoración del cumplimiento de los indicadores correspondientes a diagnóstico y evaluación inicial elaborados según las Guías pediátricas en infección por VIH/sida
| Número del indicador | Indicador | Fórmula | Resultados de UPIIP | Estándar en el paciente pediátrico con VIH |
| 52 | Contenidos relevantes de la valoración inicial del niño y adolescente con VIH | Adolescentes en los que se evaluaron los contenidos relevantes en la valoración inicial/total de pacientes adolescentes | 90% | 90% |
| 53 | Pruebas complementarias en la valoración inicial del niño y adolescente con VIH | Adolescentes en los que se realizaron las pruebas complementarias en la valoración inicial/total de pacientes adolescentes | 90% | 90% |
Se cumplieron los estándares en 4 de los 6indicadores (66%) (tabla 12).
Valoración del cumplimiento de los indicadores correspondientes a seguimiento e intervenciones orientadas a la prevención elaborados según las Guías pediátricas en infección por VIH/sida
| Número del indicador | Indicador | Fórmula | Resultados de UPIIP | Estándar en el paciente pediátrico con VIH |
| 54 | Contenidos relevantes de la valoración inicial en la embarazada con infección VIH | Número de embarazadas VIH con examen básico en la valoración inicial×100/número de embarazadas con valoración inicial | 90% | 90% |
| 55 | Seguimiento del hijo de madre VIH, no infectado | Número de niños expuestos al VIH en seguimiento ambulatorio×100/número de niños expuestos al VIH | 98% | 90% |
| 56 | Cribado de enfermedades de transmisión sexual (ETS) anual en adolescentes con el VIH | Número de adolescentes a los que se ha realizado el cribado de ETS anual×100/número de adolescentes en seguimiento regular | 0% | 80% |
| 57 | Monitorización de las concentraciones plasmáticas de antirretrovirales (MCP-ARV) | Número de pacientes en los que se ha realizado la MCP-ARV×100/número de pacientes en seguimiento regular | 100% | 85% |
| 58 | Evaluación del crecimiento y desarrollo en niños y adolescentes infectados por el VIH | Número de pacientes en los que se realiza la evaluación del crecimiento y desarrollo×100/número de pacientes en seguimiento regular | 100% | 95% |
| 59 | Estudio de inmunoprotección frente a antígenos vacunales | Número de pacientes en los que se ha realizado estudio de inmunoprotección frente a antígenos vacunales×100/número de pacientes con esquema vacunal completo en seguimiento regular | 30,80% | 95% |
En negrita los indicadores que no se cumplieron al evaluar el seguimiento de nuestros pacientes.
Se cumplió el estándar en uno de los 2indicadores (50%) (tabla 13).
Valoración del cumplimiento de los indicadores correspondientes a seguimiento de pacientes en tratamiento elaborados según las Guías pediátricas en infección por VIH/sida
| Número del indicador | Indicador | Fórmula | Resultados de UPIIP | Estándar en el paciente pediátrico con VIH |
| 60 | Traspaso coordinado de los adolescentes VIH a la unidad de adultos | Número de adolescentes VIH en seguimiento con traspaso coordinado a la unidad de adultos×100/número de adolescentes VIH en seguimiento regular | 100% | 100% |
| 61 | Valoración neuropsicológica de los pacientes VIH en seguimiento | Número de adolescentes en seguimiento en los que se ha realizado valoración neuropsicológica×100/número de pacientes en seguimiento regular | 43,75% | 90% |
En negrita los indicadores que no se cumplieron al evaluar el seguimiento de nuestros pacientes.
El seguimiento de la infección por el VIH en la población pediátrica requiere un abordaje profesional multidisciplinar y de la colaboración del paciente y sus familiares y cuidadores10,12. Este abordaje se basa en protocolos y documentos de consenso elaborados por diferentes grupos y sociedades que definen y orientan el seguimiento de la enfermedad y que han permitido homogeneizar y mejorar la calidad de la asistencia de estos pacientes1,9,10,12,13. Sin embargo, no disponemos de indicadores que nos permitan evaluar la calidad de la atención ofrecida a esta población y, por consiguiente, mejorarla.
Tras la publicación por el GESIDA en el año 2010 de unos estándares muy bien definidos que permiten la valoración del seguimiento en el paciente adulto, creímos oportuno adaptarlos al paciente pediátrico y evaluar con ellos el seguimiento que se les ofrece.
La adaptación de los estándares al paciente pediátrico se ha podido realizar a partir de las recomendaciones recogidas en los protocolos y documentos específicamente pediátricos antes mencionados, suponiendo una modificación de tan solo el 14% de los indicadores valorados en el paciente adulto. No se dispone, a nuestro conocimiento, de ninguna publicación que recoja una herramienta similar, por lo que consideramos que se trata de una aportación importante para la valoración de la calidad de la asistencia al niño que vive con el VIH.
Las adaptaciones se han realizado de acuerdo con las diferencias que presenta la población pediátrica respecto a la adulta en cuanto a vías de transmisión, períodos de incubación, progresión de la enfermedad, manifestaciones clínicas y necesidades diferenciales a la hora de decidir el tratamiento12. Dichas modificaciones se han realizado mayoritariamente en variables que evalúan parámetros inmunovirológicos y adecuación del TARV, siguiendo guías pediátricas, y en el indicador referido al coste del TARV, claramente diferente en los pacientes pediátricos y los adultos. El detalle de las variables adaptadas y su descripción se encuentra disponible en el material suplementario online.
La aplicación de estos indicadores, previamente definidos, para valorar la calidad de la asistencia ofrecida a nuestros pacientes nos permite demostrar que dicha asistencia es globalmente buena, ya que cumple satisfactoriamente el 81% de los indicadores, siendo este cumplimiento del 83% cuando evaluamos exclusivamente los definidos como relevantes. De todos modos, resulta imprescindible evaluar y corregir los puntos de potencial mejora en la calidad asistencial.
Aunque no se demuestran deficiencias significativas en las condiciones estructurales, algo propio de un sistema sanitario de países desarrollados, ni en el seguimiento y en la evaluación inicial (excepto en el indicador de educación sanitaria en la primera visita, probablemente artefactado por la edad del paciente al diagnóstico y la necesidad de «preparar» progresivamente a la familia frente al diagnóstico de la enfermedad), sí aparecen deficiencias en los apartados de intervenciones orientadas a la prevención y al seguimiento de pacientes en tratamiento que merecen ser revisadas.
Así pues, detectamos que no se realiza de forma rutinaria un seguimiento de la función renal básica de los pacientes (indicador13), posiblemente debido a la baja incidencia de la nefropatía por el VIH en el paciente pediátrico que vive en un país desarrollado en la actualidad14,15. De todos modos, consideramos que es imprescindible valorar periódicamente la posibilidad de daño renal asociado a fármacos9,16,17 y también de daño renovascular en el contexto de la enfermedad cardiovascular propia del paciente con infección por el VIH. En este sentido, nuestra unidad ha llevado a cabo estudios específicos de disfunción renal en los pacientes pediátricos que reciben tenofovir como parte de su régimen terapéutico16, por lo que el control semestral de la función glomerular y tubular en estos pacientes se lleva a cabo de manera estricta. Del mismo modo, también se realiza un estudio de síndrome metabólico en todos nuestros pacientes que incluye la medición del perímetro abdominal y la determinación basal de la presión arterial como marcador de daño renovascular (datos no publicados).
En cuanto a la actualización del calendario vacunal según las recomendaciones actuales para el paciente pediátrico infectado por el VIH18, evaluados en los indicadores16, 17 y 18, se ofrece una aceptable cobertura frente al virus de la hepatitisB (por formar parte del calendario vacunal habitual en nuestro medio) y de la infección neumocócica, ya que la relativa incidencia y potencial gravedad de esta infección en la población pediátrica19 lleva al médico responsable a insistir en una cobertura vacunal completa frente a este patógeno. En cambio, la cobertura frente al virus de la hepatitisA es claramente insuficiente, posiblemente debido a la baja incidencia de esta enfermedad en nuestro medio en la actualidad, lo que ha provocado que esta vacunación prácticamente se haya limitado a los pacientes con un elevado grado de inmunosupresión, a los que viajan a zona endémicas y a aquellos con infección por el virus de la hepatitisC, por el elevado riesgo de descompensación hepática en caso de coinfección20,21.
En cuanto a la evaluación del grado de inmunoprotección ofrecido por las diferentes vacunas administradas según las indicaciones de la literatura correspondiente18, es imprescindible mejorar la cobertura ofrecida ya que, según los registros del Servicio de Medicina Preventiva de nuestro centro, esta no supera el 30% del total.
Otro punto de mejora es la implantación de un cuestionario anónimo de calidad en la atención sanitaria percibida por el paciente y su familia en nuestra unidad (indicador27). Se ha demostrado que el feedback entre el sistema sanitario y el paciente permite optimizar los esfuerzos destinados a mejorar la calidad asistencial22-24.
Es importante resaltar los esfuerzos dedicados a una transición progresiva y coordinada a la unidad de adultos y la colaboración de los infectólogos que posteriormente atenderán a estos pacientes, hecho que ocurre en todos los pacientes de nuestra unidad, tal y como reflejan los resultados del indicador60. Sin embargo, el resultado del indicador56 alerta de una baja cobertura del cribado de las enfermedades de transmisión sexual en los adolescentes que viven con el VIH, probablemente por el menor contacto del infectólogo pediátrico respecto al de adultos con este tipo de enfermedades, a pesar de conocerse que se trata de una población activa sexualmente, con prácticas de riesgo habituales y en la que la evolución de estas enfermedades es peor que en la población general25,26.
Por otra parte, a pesar de contar con la colaboración de una psicóloga, que evidentemente permite optimizar el seguimiento psicológico de estos pacientes y facilitar una atención integrada en una misma visita, solo el 50% de nuestros pacientes han sido valorados desde el punto de vista neuropsicológico durante el periodo evaluado (indicador61). Es aún menor el número de pacientes que han sido sometidos a un estudio reglado desde el punto de vista neurocognitivo mediante la aplicación de los tests correspondientes. Esta baja cobertura nos obliga a mejorar el rendimiento de este aspecto, especialmente a través de medidas encaminadas a convencer al paciente y su familia de la necesidad de este seguimiento, como se demuestra en múltiples publicaciones en el paciente adolescente con VIH9,13,27,28.
Respecto a los indicadores de seguimiento del paciente que recibe TARV, los 2puntos de fracaso se relacionan con la idiosincrasia del paciente VIH pediátrico. Así, recientemente 2estudios del colaborativo COHERE demuestran una mayor frecuencia de fracaso virológico precoz en la edad pediátrica29,30, hecho que justificaría los resultados obtenidos en los indicadores de respuesta virológica.
El primero de estos estudios demuestra una tasa global de fracaso en los niños más de 2veces superior a la de los pacientes adultos con transmisión heterosexual del virus29. Del mismo modo, un segundo trabajo en esta línea demuestra que esta respuesta virológica más pobre puede aumentar la probabilidad de aparición de resistencias30.
Respecto al indicador37, el gasto medio por paciente en su primer TARV en nuestra unidad es inferior al valor de referencia publicado de 7.500€/paciente y año31. Analizando los datos en detalle, se observan claramente 2subgrupos de coste: los pacientes con inicio de TARV menores de 3años, con una media de 2.992,5€/paciente y año, y los pacientes que inician TARV con 3años de edad o más, con una media de 8.484,8€/paciente y año. Esta clara diferencia la podemos atribuir a las distintas recomendaciones de combinaciones de fármacos de inicio entre los 2subgrupos de población, al menor consumo anual de fármacos por requerir dosis inferiores debidas al menor peso de los pacientes de menor edad, y por la utilización de especialidades en suspensión oral.
Respecto a la prevención de la transmisión vertical del virus, nuestra unidad cumple los 3indicadores (uno adaptado del documento de GESIDA y 2 creados a partir de las guías pediátricas de VIH y transmisión vertical), de modo que se obtiene un porcentaje de transmisión similar al de la mayoría de cohortes de nuestro medio, y un elevado seguimiento hasta los 5años según las recomendaciones estatales actuales10. Consideramos que la visita de valoración que se ofrece a todas las embarazadas con infección por VIH durante el tercer trimestre de gestación facilita la adherencia de las familias al seguimiento propuesto. Debido a este bajo porcentaje de transmisión vertical de la infección cuando se aplican las medidas oportunas y a la necesidad de un seguimiento a medio-largo plazo de los niños no infectados pero expuestos a VIH y a TARV, se han incorporado 2indicadores de calidad (indicadores54 y 55) por ser un aspecto de gran importancia en la atención al paciente pediátrico.
En cuanto a los indicadores excluidos de los propuestos por GESIDA para el paciente adulto, queremos hacer hincapié en los marcadores de riesgo cardiovascular que no se incluyeron como indicadores evaluables en la población pediátrica. Es evidente que cada vez se dispone de más datos que orientan a la necesidad de incluir la valoración del riesgo de síndrome metabólico en el paciente VIH pediátrico32,33, en especial durante la adolescencia, pero la ausencia de guías claras para definir cómo debe realizarse este seguimiento nos han llevado a su exclusión a la hora de la valoración de la calidad asistencial. A pesar de ello, en la actualidad CoRISpe está llevando a cabo un estudio transversal que pretende establecer la prevalencia del síndrome metabólico en esta población para definir futuros pacientes de riesgo cardiovascular (datos no publicados).
Por todo lo analizado, consideramos que la calidad asistencial ofrecida al paciente pediátrico con infección por el VIH puede evaluarse completamente con la adaptación que hemos realizado de los indicadores definidos por GESIDA y los nuevos indicadores propuestos a partir de las Guías Españolas para el Seguimiento del Paciente Pediátrico Infectado por el VIH9 y las Recomendaciones para el seguimiento del niño expuesto al VIH y a los antirretrovirales durante la gestación y el periodo neonatal de la SEIP10. Su aplicación a nuestros pacientes indica una calidad de asistencia globalmente satisfactoria, poniendo de todos modos en evidencia ciertos aspectos que deben optimizarse.
Es de especial interés la realización de nuevos estudios multicéntricos de validación de estos estándares en otros grupos de pacientes, para su consolidación como indicadores de calidad en la asistencia pediátrica y así poder definir desde la SEIP el nivel recomendable para la capacitación de centros para el control y el seguimiento de estos pacientes.
FinanciaciónNo se ha dispuesto de financiación externa para la realización de este manuscrito.
Conflicto de interesesP.S.P. ha actuado como consultor de Bristol-Myers Squibb y ha participado en ensayos clínicos de Tibotec Laboratories y Abbott Laboratories. A.M.N. y C.F. han participado en ensayos clínicos de Tibotec Laboratories y Abbott Laboratories. El resto de autores de este manuscrito declaran la ausencia de conflicto de intereses.
Los autores quieren expresar su agradecimiento a todos los pacientes y sus familias por su colaboración, al Dr. Xavier Martínez Gómez y Santiago Pérez Hoyos, del Servei de Medicina Preventiva i Epidemiologia de nuestro centro, por su colaboración en la evaluación estadística de los resultados obtenidos, y al personal de enfermería y psicología (Sra. Carolina Rodríguez) por su participación activa en este proyecto de control de calidad asistencial.