Sí. La población de estudio está bien definida e incluye de forma consecutiva a 174 pacientes en 17 centros de Australia y Nueva Zelanda con enfermedad de Crohn intervenidos con resección de todas las áreas macroscópicamente afectadas. La anastomosis tiene que ser endoscópicamente accesible para que un paciente pueda ser incluido en el estudio. Por otro lado, los criterios de exclusión son los habituales en los estudios de recurrencia e incluyen estoma, persistencia de zonas con afectación macroscópica tras la cirugía, comorbilidades que limiten la realización de una colonoscopia o gestación.
La intervención también está claramente definida y es uno de los puntos fuertes del estudio porque compara estrategias clínicas, no tratamientos concretos. En las dos estrategias comparadas los pacientes reciben tratamiento tras la cirugía en función del riesgo de recurrencia, siendo alto cuando están presentes alguno de los siguientes factores: hábito tabáquico, enfermedad penetrante (absceso, fístula o perforación libre) o cirugía previa; en caso contrario se considera al paciente como de bajo riesgo. La azatioprina en dosis de 2mg/kg/día es el fármaco empleado en caso de riesgo de recurrencia elevado aunque si existe intolerancia se emplea en su lugar adalimumab a las dosis habituales. Todos los pacientes reciben durante los tres primeros meses metronidazol 400mg/12 horas; dosis que se reduce a la mitad en caso de intolerancia. Tras este periodo los pacientes con bajo riesgo de recurrencia no reciben ningún tratamiento. La estrategia evaluada denominada «activa» (EA) consiste en realizar una colonoscopia precoz a los 6 meses intensificando el tratamiento en caso de recurrencia. La intensificación consistía en introducir tiopurínicos en pacientes de bajo riesgo, asociar adalimumab si el paciente estaba con azatioprina o aumentar la dosis del biológico en caso de haberlo iniciado tras la cirugía por intolerancia a los tiopurínicos. En la estrategia de tratamiento estándar (EE) no se realiza ninguna intervención hasta la colonoscopia final del estudio en el mes 18. Si algún paciente experimenta recurrencia clínica se retiraba del estudio y se le proponía una colonoscopia no programada. A este respecto, comentar que la estrategia estándar no lo es tanto puesto que las guías recomiendan la realización de una colonoscopia en el primer año1.
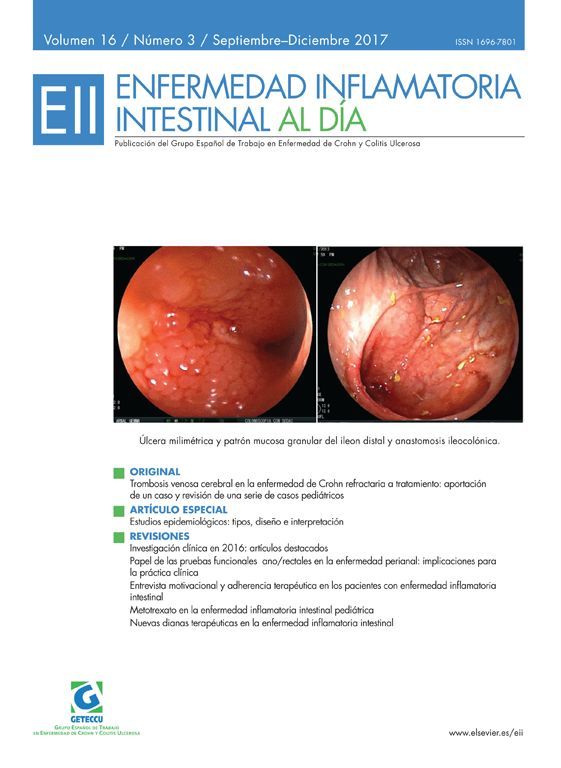
La principal variable de eficacia fue la recurrencia en el mes 18, definida con los criterios habitualmente empleados como es un índice de Rutgeerts igual o superior a i2 (más de 5 aftas en el íleon o lesiones limitadas a la anastomosis). En este sentido, subrayar que las recurrencias catalogadas como i2 limitadas a la anastomosis y sin lesiones en el neoíleon terminal tienen una baja probabilidad de evolucionar a formas más graves de recurrencia2 y esta distinción no se hizo en el estudio. Otras variables consideradas fueron la recurrencia clínica y quirúrgica, la eficacia de los diferentes fármacos, índices endoscópicos (CDEIS y SES-CD) o reactantes como la PCR. No se incorporó la calprotectina fecal a ninguna de las estrategias a pesar de su papel en la detección precoz de recurrencia3.
¿Fue aleatoria la asignación de los pacientes a los tratamientos?Los pacientes fueron aleatorizados a una u otra estrategia en una proporción 2:1. La secuencia de aleatorización fue generada por un ordenador central.
¿Fueron adecuadamente considerados hasta el final del estudio todos los pacientes que entraron en él?Sí. Se analizan detalladamente todos los pacientes que fueron evaluados al inicio del estudio, así como las causas de su exclusión al inicio del mismo o de la retirada prematura. Las pérdidas fueron similares en ambos grupos, 30% en la EA (37/122) y 32% en la EE (19/52). El análisis realizado es doble, por protocolo y por intención de tratamiento modificado (ITm) de forma que los pacientes retirados sin endoscopia se consideran i2 y en aquellos con endoscopia no programada por recurrencia clínica se asumen los hallazgos al final del estudio.
¿Se mantuvieron ciegos al tratamiento los pacientes, los clínicos y el personal del estudio?No. Tanto médicos como pacientes no eran ciegos a la estrategia asignada, únicamente las endoscopias del final del estudio eran valoradas, además de por el endoscopista responsable del paciente, por dos evaluadores ciegos al tratamiento.
¿Fueron similares los grupos al comienzo del ensayo?Sí. Aparte de las diferencias determinadas por el riesgo de recurrencia, no hubo diferencias en las poblaciones incluidas en cada estrategia, salvo, quizá, un mayor número de pacientes con exposición previa a dos anti-TNF en la EE (p=0,09), aunque son pocos pacientes por lo que la repercusión en el resultado final, de existir, es mínima.
¿Al margen de la intervención del estudio, los grupos fueron tratados de igual modo?Sí. Todos los pacientes fueron tratados igual en función del riesgo de recurrencia y seguidos a intervalos bimensuales el primer año y cada 3 meses hasta los 18.
¿Es muy grande el efecto del tratamiento?La recurrencia a los 18 meses de seguimiento tras la cirugía, que fue el objetivo principal del estudio, se observó en el 49% de pacientes asignados a la EA (60/122) y en un 67% (35/52) de la clásica, diferencias que son estadísticamente significativas (p=0,03, ITm). El NNT es de 6; es decir, el beneficio clínico es significativo aunque desde luego no el que cabría esperar. En el análisis por protocolo el NNT es de 4 pero desde luego no es el análisis más correcto porque excluiría a los pacientes retirados de forma prematura por recurrencia clínica. Los índices endoscópicos también fueron significativamente diferentes entre ambos grupos: CDEIS: 13 vs. 16; p<0,0001, SES-CD: 3 vs. 3,5; p=0,005 o el recuento de úlceras: 1 vs. 1,5; p=0,002. De forma llamativa muy pocos pacientes mantenían una endoscopia normal (Rutgeerts i0) al final del estudio, 22% en la EA y 8% en la EE.
La mayor parte de los pacientes presentaba algún factor de riesgo de recurrencia (83% en la EA y 85% en la EE) por lo que la mayoría recibió algún tratamiento preventivo que en un 72% se trató de tiopurinas en la EA (64% en la EE) y en un 28% adalimumab (36% en la EE). Aunque el estudio no está diseñado para evaluar diferencias entre los distintos tratamientos empleados es interesante analizar estos resultados. En la EA podemos valorar la diferente eficacia entre tiopurinas y adalimumab en el mes 6 y en la EE en el mes 18. En el primer intervalo, los pacientes que reciben adalimumab tienen una menor recurrencia (21% 6/28 vs. 45% 33/73; p=0,045) que los tratados con tiopurinas con un NNT de 5. Sin embargo, al final del estudio estas diferencias desaparecen. La exposición previa a tiopurinas (más de 6 meses en los 12 previos a la cirugía) no influye en los resultados pero, la exposición previa a anti-TNF sí se asocia a una mayor recurrencia a los 6 meses (56 vs. 5%; p=0,007).
La intensificación que se realiza en la EA ante la recurrencia en el mes 6 se muestra eficaz aunque de forma limitada porque solo el 38% de los pacientes al final del estudio está en remisión endoscópica (i0-1). No hay diferencias entre los distintos fármacos aunque los números, de nuevo, son pequeños.
La estratificación en bajo y alto riesgo no se acompañó en diferencias de recurrencia ni a los 6 meses ni a los 18 meses, probablemente lo que hace replantearse la necesidad de, por un lado, realizar un tratamiento preventivo en todos los pacientes y, por otro, mejorar la capacidad predictiva incorporando otros factores conocidos4. Por último, el que un paciente se encuentre en remisión endoscópica a los 6 meses no es indicativo de un menor riesgo posterior puesto que se produce recurrencia a los 18 meses en el 41%, sin diferencias entre los distintos tratamientos.
¿Cómo es la precisión de la estimación del efecto del tratamiento?La precisión del efecto es escasa como lo refleja la amplitud del intervalo de confianza de la reducción absoluta de riesgo para el resultado principal (IC95%: -33,7 a -2,6%) y por tanto del NNT (IC95%: 3 a 38).
¿Se tuvieron en cuenta todos los resultados de importancia clínica?Sí. Los resultados mostrados son tremendamente exhaustivos aunque no se aprecian diferencias estadísticamente significativas en la mayoría de las comparaciones realizadas porque el número de pacientes incluido estaba calculado para el objetivo principal del estudio.
¿Pueden aplicarse estos resultados en tu medio o población local?Sí. La principal aplicación del estudio a la práctica habitual es adoptar una actitud activa de seguimiento en los pacientes con EC intervenidos adoptando como momento para realizar la primera endoscopia los 6 meses del estudio. No obstante, en estudios donde se realiza la exploración a los 3 meses la probabilidad de recurrencia afecta hasta a un tercio de los pacientes tratados con tiopurinas5, por lo que este intervalo podría acortarse en un futuro. En la estrategia evaluada no se incorpora la calprotectina fecal que podría disminuir la realización de colonoscopias repetidas o bien seleccionar mejor el momento de su realización3,6.
Los resultados al final del estudio son discretos con una frecuencia elevada de recurrencia (50% en el grupo de alto riesgo tratado, incluyendo intensificados) lo que obliga a replantearse si la estrategia de tratamiento empleada es la más eficaz y si un empleo más precoz con biológicos hubiera mejorado los resultados7 (son pocos los pacientes incluidos con esta pauta).
La estratificación en alto y bajo riesgo no es de gran utilidad en este estudio dada la frecuencia de recurrencia en los pacientes considerados como de bajo riesgo lo que plantea la necesidad de incorporar otros factores conocidos como los marcadores serológicos o historia familiar; o bien, utilizar el tratamiento preventivo de forma más generalizada8.
Aunque la calidad del estudio es baja (Jadad 2) aporta una estrategia de manejo en la que se integran aspectos como la estratificación por riesgo de recurrencia, diferente eficacia de los fármacos, valor de la monitorización endoscópica y una actitud estructurada ante la aparición de recurrencia. Sin embargo, la principal limitación es que se pueden extraer pocas conclusiones más allá de la adopción de una vigilancia intensiva de estos pacientes.
¿Los beneficios a obtener justifican los riesgos y los costes?Salvando comorbilidades, en los pacientes intervenidos se asumen con facilidad los riesgos asociados a los tratamientos dado que la probabilidad de recurrencia es elevada y la eficacia de los mismos limitada precisando una segunda cirugía el 24% de los pacientes en los 5 años siguientes9. En cuanto a los costes, la estrategia evaluada intenta minimizarlos ya que utiliza como primera opción las tiopurinas a pesar de que los anti-TNF son más eficaces en esta indicación10 pero la relación coste-beneficio de estos es más desfavorable11.