Fue Himsworth1 quien, en fecha tan temprana como 1936, hizo referencia explícita a la sensibilidad-insensibilidad (RI) crónica a la insulina de esta forma: "Diabetes mellitus its differentiation into insulin-sensitive and insulin-insensitive types", insistiendo sobre ello en publicaciones posteriores. También se atribuye a Reaven2 la paternidad del síndrome de resistencia a la insulina o síndrome metabólico (SM), al que denominó primeramente "síndrome X". Pero esa mirada hacia atrás que es la investigación (en inglés se entiende mejor lo que queremos decir: research = look back) con frecuencia descubre precursores, y ésta no iba a ser una excepción. Por supuesto que hubiera sido imposible referirse a la RI antes del descubrimiento y aplicación de la hormona, lo que no ocurrió hasta enero de 1922. Esto es así, lo que no obsta para que puedan detectarse antecedentes próximos y aun remotos de autores o escritos colectivos que distinguieron (o al menos intuyeron) la existencia de enfermedades, síndromes o situaciones que hoy día concuerdan con los que catalogamos como sensibles a la insulina (diabetes mellitus [DM] tipo 1) y menos sensibles a la insulina o resistentes a ella (DM tipo 2 y otras condiciones asociadas a la misma: obesidad, "diátesis artrítica o úrica" hiperuricemia y gota, hipertensión arterial hipertonía y apoplejía accidente cerebrovascular hemorrágico), que no dudaríamos en asimilar al síndrome metabólico si no fuera por la ausencia de referencia a la dislipemia.
Así, quizás Himsworth tenga sus antecedentes en los redactores del Charaka Asmita y Sushmita Ayurveda, 100-200 años antes de Cristo (a.C.) cuando leemos que "hay dos tipos de trastornos urinarios (recordemos que el término diabetes atribuido a Demetrio de Apamia3 200 a.C. procede de la palabra griega diá-beétee4, que puede traducirse como "a través de un sifón o tubo". Esto es, lo riñones dejarían pasar la orina como un líquido que fluye por un sifón o por un tubo), uno natural y de orden genético, y otro debido a una vida desordenada o a imprudencias dietéticas. El paciente que sufre del primero es delgado, pálido, come poco y orina mucho. El paciente con el último come mucho, es de hábito sedentario, suele ser obeso y duerme demasiado5. El primer tipo correspondería a la DM tipo 1 (sensible a la insulina) y el segundo tipo de "desorden urinario" correspondería a la DM tipo 2 (resistente a la insulina), y, respectivamente, a la "diabetes magra" y "diabetes grasa" a las que hacía referencia Lancereaux en 1877. La última sería la misma que en la observación de Bouchardat mejoraba y su incidencia disminuía durante el cerco a París por las tropas prusianas de Bismark en 1870. Desde entonces, Bouchardat aconsejaba a sus pacientes: "mangez le moins possible". Ambas observaciones insistían en la asociación de DM tipo 2 y obesidad, unidas en la actualidad en un solo nombre que comienza a abrirse camino: el de diabesity6. En la breve revisión histórica que hace Hanefeld7 nos recuerda que la asociación de obesidad, gota y apoplejía era conocida desde la antigüedad, así como las lesiones ateroscleróticas que serían su consecuencia. Y ya más próximo a nosotros, hemos de referirnos a dos singulares figuras de la medicina española: Marañón y Carrasco Formiguera.
En una excelente revisión, Serrano Ríos e Iancu8 pasan revista a un importante número de intuiciones anticipativas al tema que nos ocupa por parte de Marañón. Así, en 1928, con ocasión de la publicación de un caso mortal de diabetes en un niño, Marañón hacía referencia a la "sensibilidad a la insulina" con la que estaba siendo tratado este niño, sensibilidad que atribuyó a la "adrenalitis" hallada en el estudio necrópsico. Entre los años 1922 y 1930 insiste Marañón sobre la hipersensibilidad a la insulina en diabéticos con insuficiencia adrenal, en la frecuente asociación de obesidad, "diátesis artrítica", diabetes de la madurez (hoy día DM tipo 2), "hipertonía" (hipertensión arterial), así como sobre la importancia de la conjunción de la genética y del ambiente (al que se refiere como las "condiciones de la vida moderna, propicias al desarrollo de diabetes en los países más cultos (...) por el auge de la civilización occidental", según la transcripción de Serrano Ríos e Iancu. ¡Y esto lo escribe Marañón en 1926! Y así sería posible continuar. Baste señalar que consideraba la hipertensión arterial como un estado precursor del desarrollo de diabetes.
También Rossend Carrasco9 se anticipó a nuestro tiempo. En diciembre de 1922 escribió una carta al British Medical Journal referida al original de Cammidge publicado en la misma revista el mes anterior, y en el que éste defendía que en más de la mitad de los diabéticos, el fracaso pancreático no es el factor dominante (hoy día diríamos que más de la mitad de los diabéticos son de tipo 2). Carrasco Formiguera coincidía con él, pero no con la sugerencia de Cammidge de que el tratamiento insulínico sería inefectivo en estos casos (en la actualidad quizá diríamos que porque son resistentes). Argulle Carrasco que también en esos casos la insulina es efectiva. Con esta carta al British Medical Journal se abre el libro referenciado, cuyo texto no es otro que una ampliación de la Ponencia presentada al Congreso de Medicina celebrado en Sevilla en 1924.
Refiere el autor otros casos publicados de refractariedad a la insulina (resistentes a la insulina exógena) en diabéticos obesos, en diabéticos con infecciones dentarias o afectados de tuberculosis. En los últimos 2 casos, la resistencia a la insulina exógena es un hecho bien conocido hoy, así como en otras infecciones. Y, coindicidiendo con la obesidad, la RI (a la insulina endógena y exógena) forma parte del núcleo patogénico y fisiopatológico de ambas condiciones.
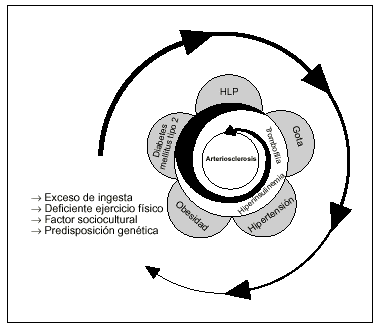
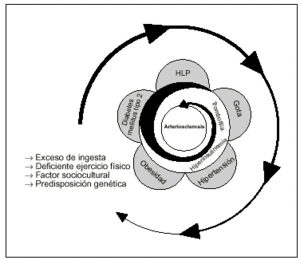
Más próximo a nosotros, Jean Vague10 delimitaba el carácter singular de la obesidad androide (OBA) y la situaba en íntima asociación con la DM del adulto (DM tipo 2), la hiperlipemia, la hiperuricemia y la aterosclerosis. Y no deja de ser curioso que el término hoy día vigente de síndrome metabólico fuera acuñado y dado a conocer por Hanefeld y Leonhardt11 en 1981 y que lo representaran de un modo explícito y muy actual (fig. 1).
Fig. 1. Esquema del "síndrome metabólico", sus condicionantes y consecuencias Modificada de Hanefeld y Leonhardt (1981).HLP: hiperlipoproteimia.
En 2003, el término síndrome metabólico hace referencia a la concurrencia en el mismo individuo de OB/OBA (incluso sobrepeso androide), un diverso grado de alteración del metabolismo de la glucosa (glucemia basal alterada, intolerancia a la glucosa, DM tipo 2), dislipemia (valores elevados de triglicéridos-lipoproteínas de muy baja densidad [TG-VLDL], valores bajos de colesterol unido a lipoproteínas de alta densidad [cHDL], concentraciones altas de colesterol unido a lipoproteínas de baja densidad [cLDL] y valores altos de LDLpd), RI con hiperinsulinemia adaptativa e hipertensión arterial. Su importancia viene dada por su elevada prevalencia (utilizando los criterios diagnósticos del NCEP12, en los EE.UU. más del 20% de la población adulta sería portadora del SM en progresión creciente con la edad y, sobre todo, con un índice de masa corporal [IMC] del 4,6, 22,4 y 59,6% según éste fuera normal, indicativo de sobrepeso o diagnóstico de obesidad, respectivamente)13. En España, el estudio VIVA14 ofrece una prevalencia global del 19,3 y 15,5%, siguiendo los criterios diagnósticos de la OMS o del EGIR15, porque su "componente principal"16 (obesidad/obesidad androide, glucemia basal alterada/intolerancia a la glucosa, dislipemia y RI/HiINS) es un fuerte predictor de DM tipo 217,18, y todo el conjunto indicado con anterioridad un no menos fuerte predictor del desarrollo de enfermedad cardiovascular aterosclerótica19,20.
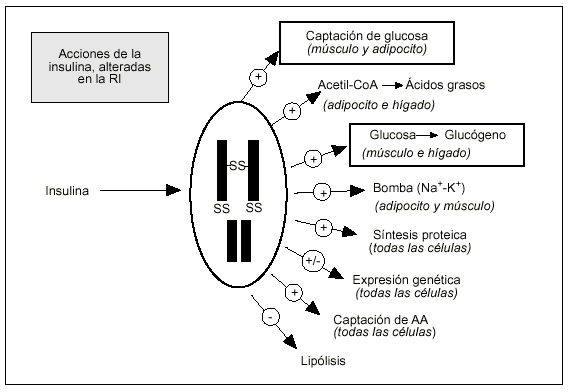
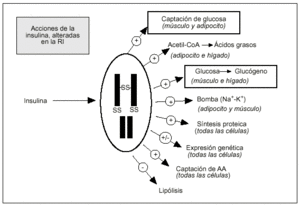
El Grupo de Trabajo "Resistencia a la Insulina" de la Sociedad Española de Diabetes, en su Documento de Trabajo citado15 define la RI como "la disminución de la capacidad de la insulina para ejercer sus acciones biológicas en tejidos diana típicos, como el muscular esquelético, el hígado o el tejido adiposo". Pero debe hacerse constar desde el principio que toda la construcción teórica que se ha hecho acerca de la RI y sus consecuencias metabólicas y cardiovasculares se basa en la alteración de dos de las múltiples acciones de la hormona (fig. 2): la menor captación de glucosa bajo el estímulo de la insulina y la reducida síntesis de glucógeno que ésta promueve. La extensión de sus efectos a otras acciones, aunque evidenciada en algunos aspectos a dosis farmacológicas y/o en estudios in vitro, está por demostrar21.
Fig. 2. Sinopsis de las múltiples acciones de la insulina in vivo. Recuadradas figuran las dos sobre las que descansa, hasta ahora, toda la construcción teórica que sirve de base a los diferentes métodos diseñados para la estimación de la sensibilidad a la insulina o de su inversa, la RI.
El binomio RI/HiINS ocupa un papel central en el desarrollo de ITG y en su conversión a DM tipo 2. También es (entre los sin duda varios existentes) el "factor" fisiopatológico mejor estudiado en el SM y en la DM tipo 2. Pero, además, son otras muchas las situaciones fisiológicas o patológicas en las que la caracterización del grado de RI puede ser de interés, incluso necesaria. Sin embargo, consideramos que bastaría su caracterización en cada una de las etapas evolutivas hacia la DM tipo 2 para justificar su estudio. Esta revisión trata de las diferentes técnicas descritas para la estimación de la RI in vivo.
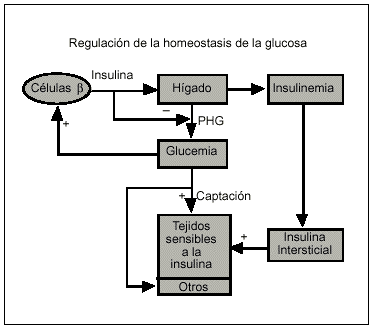
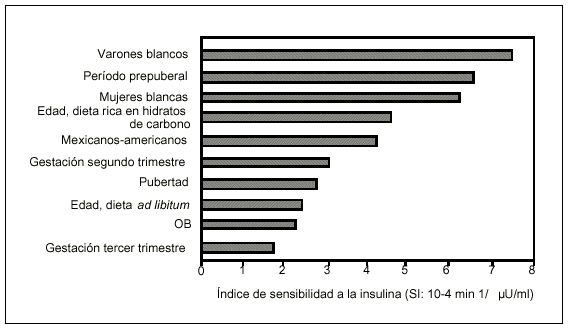
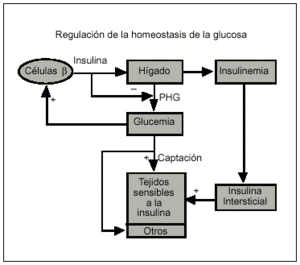
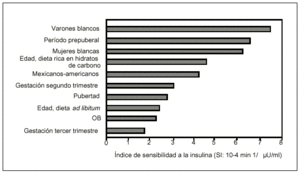
Para comprender mejor lo que sigue, obsérvese (fig. 3) que la homeostasis de la glucosa se mantiene dentro de los parámetros de la normalidad gracias a la estrecha y permanente intercomunicación entre los tejidos sensibles a la insulina (destacan, por orden de importancia cuantitativa, el músculo, el hígado y el tejido adiposo) y la célula ß, de modo que cualquier cambio en la glucemia induce otro adaptativo en la célula ß; luego la insulina inhibe la producción hepática de glucosa al tiempo que estimula su captación por los tejidos diana. Pero es importante que se tenga en cuenta, además, que para que la insulina ejerza estos efectos una vez secretada ha de pasar, vía vena porta, al hígado, difundirse después a la circulación, pasar al intersticio ("compartimiento remoto del plasma" en la ya antigua terminología) para, finalmente, alcanzar su receptor intacto en una célula diana intacta. Al menos, las principales técnicas de determinación de la RI in vivo utilizadas en investigación están basadas en esta regulación y hacen referencia explícita a ella. Otras, las más sencillas, también la contemplan, aunque en su aspecto más simple y último. Se ha de señalar, finalmente, que la sensibilidad a la insulina es muy variable, aun entre los sujetos normales, y depende de la edad, las situaciones fisiológicas (pubertad, gestación y puerperio y envejecimiento), el tipo de dieta, la actividad física, el momento del día y de otros factores desconocidos22 (fig 4).
Fig. 3. Homeostasis de la glucosa, en cuya regulación (a veces en su forma más elemental) se basan las diferentes técnicas de estimación de la RI in vivo. PHG: producción hepática de glucosa.
Fig. 4. Variabilidad de la sensibilidad a la insulina en sujetos normotolerantes a la glucosa. OB: obesidad. (Tomada de Bergman RN22).
TÉCNICAS PARA LA ESTIMACIÓN DE LA RI
Las dividiremos en dos grandes categorías: a) estimación directa de la RI, y b) estimación indirecta de la RI.
Estimación directa
Dada su complejidad, duración y coste, las técnicas de estimación directa quedan relegadas, en la práctica, a la investigación de casos y controles en muestras reducidas y, más dudosamente, al estudio de pacientes aislados.
Clamp euglucémico-hiperinsulinémico
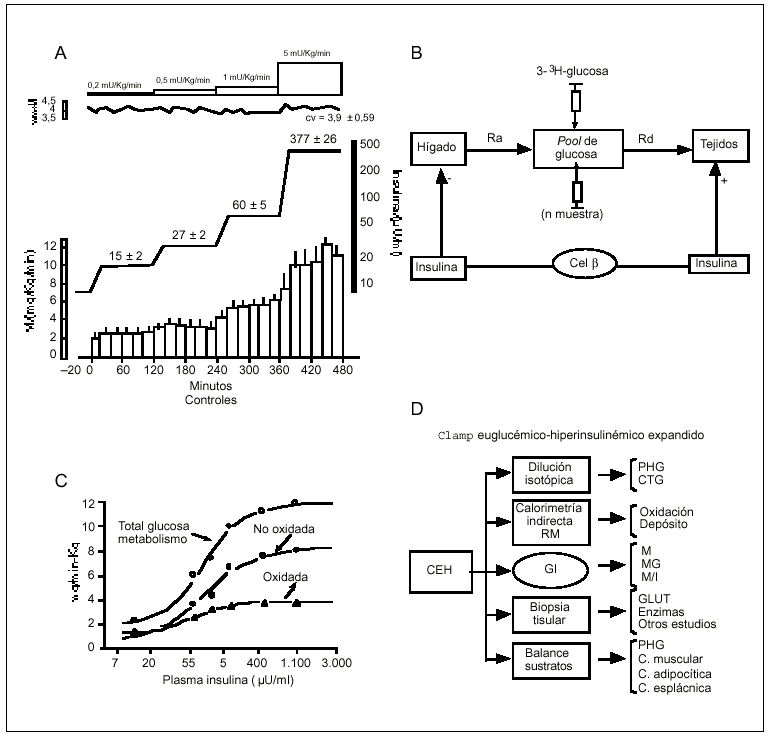
La técnica del clamp euglucémico-hiperinsulinémico (CEH) es considerada el "estándar oro" de los métodos que cuantifican la sensibilidad a la insulina in vivo. Introducida por DeFronzo23, esta técnica se basa en la infusión por vía venosa de una cantidad fija de insulina (previamente estipulada) y una cantidad variable de glucosa con el fin de mantener la glucemia del sujeto en un valor de euglucemia prefijado. La cantidad de glucosa administrada se estima mediante un algoritmo matemático, relativamente sencillo, que tiene en cuenta las concentraciones glucémicas precedentes, utilizando el Biostator (dejó de fabricarse hace años) o un programa sencillo de ordenador. La medida básica del CEH es el denominado valor M, que no es otro que el promedio de glucosa infundida al sujeto en los últimos 20 min de la prueba, una vez alcanzado el estado estacionario. El valor M representa la sensibilidad a la insulina. Cuando la insulina se administra en varias etapas sucesivas y crecientes, se obtiene una curva dosis-respuesta.
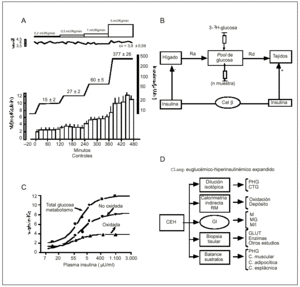
Si a este método básico se le asocia la infusión de glucosa marcada con tritio, se obtienen datos adicionales valiosos, como la medición de la produción hepática de glucosa (PHG) y la de su consumo periférico, con lo que se puede medir el diferente grado de sensibilidad a la insulina que existe normalmente en el hígado, en el músculo y en tejido adiposo (el hígado es particularmente sensible a la insulina; incluso en situaciones de RI, ésta es menor que en el músculo y en tejido adiposo; fig. 5). Es importante (en investigaciones sobre todo fisiológicas) la determinación de la PHG. Pero, además (y es el aspecto concreto del que trata esta minirrevisión), porque si la PHG estuviera elevada, el grado de RI resultaría infraestimado24, aunque los autores no precisen en qué grado.
Fig. 5. A: Clamp euglucémico hiperinsulinémico con cuatro dosis de insulina (control de nuestra unidad metabólica). B: Infusión de glucosa marcada con tritio. Se ilustra el método de dilucción isotópica. Ra: tasa de aparición de glucosa en plasma, que en condiciones basales, de equilibrio, equivale a la producción hepática de glucosa, inhibida por la insulina; Rd: tasa de desaparición, captación por los tejidos diana de la insulina, cuya captación estimula, pero también por otros como el sitema nervioso, células sanguíneas y médula renal. En el sujeto normal, la PHG en "situación de equilibrio" es aproximadamente de 2 mg/kg/min. En condiciones de "no equilibrio", es decir, durante la infusión de insulina, la PHG puede ser infraestimada. Para evitarlo, el método de elección consiste en impedir el descenso de la actividad específica de la glucosa tritiada mediante una infusión, no constante sino variable de la misma (hot-glucose infusión). C: Acoplando la técnica del CEH a la calorimetría indirecta, permite calcular el total de glucosa metabolizada y oxidada y estimar, mediante la diferencia, la glucosa no oxidada y depositada como glucógeno. D: el acoplamiento del CEH con otras técnicas permite expandir considerablemente sus posibilidades en investigación humana y animal in vivo.PHG: producción hepática de glucosa; CTG: captación tisular de glucosa; RM: resonancia magnética; GI: glucosa infundida; M: glucosa captada por los t diana; M/G: aclaramiento de la glucosa; M/I:glucosa captada en relación con la concentración plasmática de insulina; c: captación; GLUT: glucose transporter-4.
Con la utilización simultánea de la calorimetría indirecta es posible la estimación semicuantitativa de la vía preferencialmente afectada por la RI: las vías oxidativa y no oxidativa de la glucosa por igual, si la RI estuviera originada exclusivamente por una alteración en el receptor (molecular o inmunológica), o preferencialmente la vía no oxidativa que conduce a la síntesis y al depósito de glucógeno, si la alteración responsable de la RI se situara en el posreceptor (fig. 5). Así, es posible también conocer cuál de estos tejidos diana para la insulina (hígado o músculo) es el mayor responsable de la RI o si lo son ambos en una situación patológica determinada. Y aún puede ser utilizada la técnica CEH acoplada a la biopsia tisular o a técnicas basadas en el principio de Fick para un mejor estudio de la distribución regional de la glucosa25 (fig. 5).
Supresión pancreática
La prueba de supresión pancreática es un procedimiento para cuantificar la sensibilidad a la insulina que se basa en suprimir la secreción de insulina mediante la administración de fármacos. El protocolo más usado comprende la administración intravenosa de una cantidad fija de glucosa e insulina, así como propranolol y adrenalina26, o bien somatostatina27. Con la célula beta suprimida, aquellos individuos con mayor sensibilidad a la insulina serán los que tengan unas concentraciones de glucemia menores una vez alcanzado el estado estacionario. Esta técnica ha sido mucho menos usada que el CEH y es también compleja, laboriosa y cara. Además, se la considera "menos fisiológica" en la medida en que no se puede asegurar que las sustancias administradas no estén influyendo sobre el metabolismo de la glucosa.
Modelo mínimo del metabolismo de la glucosa
El modelo mínimo del metabolismo de la glucosa (MMg) fue diseñado por Bergman en 197928. De mayor simplicidad experimental que los anteriores, también se basa en una rotura matemática del feedback glucémico-insulinémico. A diferencia de los dos métodos anteriores, la sensibilidad a la insulina se determina en una situación experimental no estacionaria, durante un test de tolerancia intravenosa a la glucosa con muestreo frecuente (TTIVGMF). Esta técnica se basa en la modelización del comportamiento de la glucemia durante el TTIVGMF empleando los mínimos elementos: distribución de la glucosa en un único compartimiento, consumo de glucosa por los tejidos periféricos (sensibles e insensibles a la insulina) y producción/consumo hepático de glucosa. La insulina se asume que actúa desde el espacio intersticial ("compartimiento remoto" en la antigua terminología), y su modelización se ajusta a un modelo farmacocinético de primer orden. La rotura mencionada se basa en utilizar la insulinemia durante el TTIVGMF como una entrada del sistema. El desarrollo matemático del modelo proporciona dos ecuaciones diferenciales de primer orden, con tres variables y cuatro parámetros. La resolución del sistema de ecuaciones diferenciales se realiza mediante un método numérico, de manera que cada sujeto tendrá unos valores particulares de estos parámetros, de los que se obtendrá un índice de sensibilidad a la insulina (SI) y otro de eficacia de la glucosa (SG).
El MMg ha sido comparado con el CEH, con resultados dispares29,30. Cuando se utiliza en sujetos con una buena respuesta pancreática, en un protocolo con la administración de tolbutamida intravenosa en sujetos con una buena respuesta pancreática y sin una excesiva resistencia a la insulina31-37, los resultados obtenidos son equiparables al "estándar oro" (fig. 6). Para obviar los problemas derivados de una respuesta secretora deficiente se han propuesto dos protocolos diferentes38 basados en la administración de tolbutamida o en la administración de insulina durante el TTIVGMF. Con todo ello, y a pesar de necesitar un procedimiento experimental más simple, el MMg no debe entenderse como una técnica de uso sistemático en la práctica clínica ni en estudios epidemiológicos. Requiere tres horas y media de experimento y al menos 27 extracciones de sangre para la determinación de glucosa e insulina, lo cual encarece la prueba. Se han propuesto protocolos experimentales más cortos pero, con ellos, la precisión de los resultados disminuye y el número de fracasos en la convergencia (entre los datos teóricos y experimentales) aumenta (existen dos programas disponibles: el original de Bergman, a la venta, y la modificación al mismo realizada en nuestra unidad metabólica, STELLUM-Mg(CR), que puede solicitar gratuitamente cualquier grupo interesado).
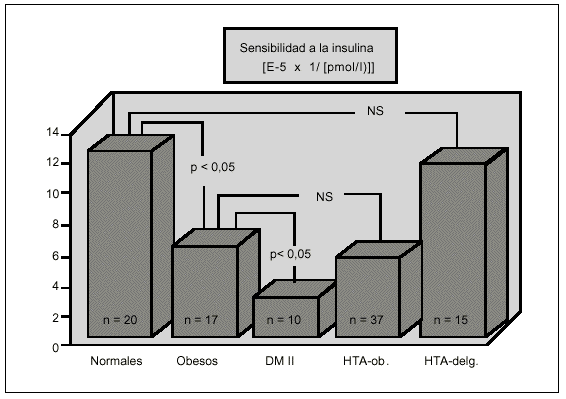
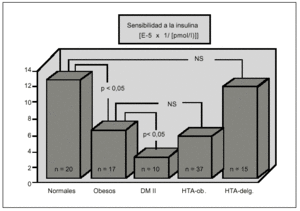
Fig. 6. Resultados obtenidos en nuestra unidad metabólica con el MMg: controles normales, obesos, diabéticos tipo 2, obesos hipertensos e hipertensos con peso normal.
Estimación indirecta
Dada su menor complejidad, duración y coste, los métodos de estimación indirecta comienzan a ser los más utilizados. Sin embargo, debido a su menor precisión, su empleo debiera quedar relegado a estudios epidemiológicos y a investigaciones con muestras amplias, o más pequeñas si existieran desviaciones importantes de la sensibilidad a la insulina39.
Podríamos distinguir entre los métodos que se basan en la determinación de los valores plasmáticos de insulina y glucosa en ayunas, que serían los más atractivos por su simplicidad, y aquéllos basados en algún procedimiento experimental simple (generalmente un TTGO).
HOMA y CIGMA
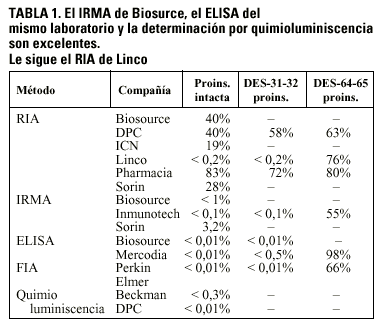
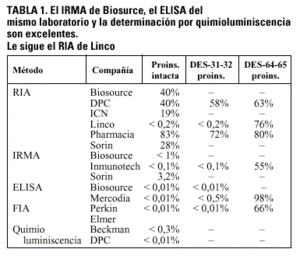
Los métodos HOMA (homeostasis model assessment) y CIGMA (continuous infusion of glucose with model assessment) son los procedimientos más difundidos entre los primeros y fueron diseñados por el grupo de Turner en el Oxford Diabetes Laboratory40,41. Se trata de técnicas basadas en modelos matemáticos denominados "estructurales", término que hace referencia a que las relaciones matemáticas que se establecen entre glucemia e insulinemia están basadas en resultados empíricos obtenidos previamente, y que se relacionan con dos variables: la sensibilidad a la insulina y la función de la célula ß. Ambos proporcionan una medida semicuantitativa de la sensibilidad a la insulina y de la función de la célula ß, de manera que un sujeto joven en su peso y sano tendrá de promedio una sensibilidad a la insulina de 1 y una función de la célula ß del 100%. Los resultados de estos modelos proporcionan nomogramas en los que a cada par de valores de glucemia e insulinemia le corresponden otros dos de sensibilidad a la insulina y de funcionamiento de la célula beta pancreática, y viceversa. En el HOMA, los valores de glucemia e insulinemia (tres determinaciones consecutivas a intervalos de 5 min) se obtienen a las 10-12 h de la última cena, sin olvidar que el método utilizado en la determinación de insulina debe ser lo más específico posible (tabla 1).
En el método CIGMA, el protocolo experimental es algo más complejo y requiere la infusión de una cantidad constante de glucosa durante 1-2 h. En comparación con los resultados obtenidos con el CEH, los hallados por sus autores con este método han sido más que aceptables (r = 0,88 para HOMA y 0,81 para CIGMA). En otro estudio, estos modelos han sido comparados con otros procedimientos sencillos para la cuantificación de la sensibilidad a la insulina (la recíproca de la concentración plasmática basal de insulina [FPI-1] y el test corto de tolerancia a la insulina [ITT]) y con el MMg42, y se ha observado que la reproducibilidad, los coeficientes de correlación y la capacidad discriminativa fueron semejantes en todos ellos, excepto para el test corto de tolerancia a la insulina (véase a continuación). Así, los coeficientes de correlación entre MMg y LogHOMA, LogCIGMA, LogFPI-1 y LogITT fueron, respectivamente, 0,88; 0,86; 0,88 y 0,66. En un estudio de similares características realizado por nuestro grupo no se obtuvieron unos resultados tan buenos (coeficiente de correlación entre SIMMg y logHOMA-1, r = 0,60; y entre logFPI, r = 0,58)37. Ascaso et al43 utilizaron el HOMA en una población normal muy bien seleccionada y aportaron los siguientes valores como referencia de anormalidad en la sensibilidad a la insulina y en la secreción basal de insulina: RI >= 3,8 (percentil 90) e insulinemia en ayunas (promedio de 3 determinaciones) >= 16,7 mU/l; estos valores podrían ser considerados de referencia para nuestro país.
Método de McAuley
El método de McAuley et al44 propone un procedimiento alternativo basado en una ecuación en la que se incluyen los valores basales de insulina y triglicéridos plasmáticos como variables independientes. Este procedimiento se contrastó en 178 sujetos normoglucémicos a los que se les realizó un CEH, y sus autores consideran que es un buen método para el cribado de la resistencia a la insulina en la población general.
Otros métodos
Otros métodos (también basados en las determinaciones basales de glucemia e insulinemia) son el FIRI45 ([Ib * Gb]/25) (prácticamente idéntico al HOMA), el de Raynaud46 (40/Ib), el QUICKI47 (1/[log Ib + log Gb]) y el de Hanson48 (1/[log Ib * log Gb]). Estos índices, incluido el HOMA, han sido evaluados recientemente por Hanley et al49 y correlacionados con el obtenido con el modelo mínimo realizado a 981 sujetos del Insulin Resistance Atherosclerosis Study (IRAS), siendo el coeficiente de correlación inferior a 0,7.
Test corto de tolerancia a la insulina
Se basa en la administración intravenosa de una pequeña dosis de insulina y en la cuantificación del descenso de la glucemia en un período de 15 min50. El índice de sensibilidad a la insulina se obtendría de la pendiente de descenso de la glucemia, que adopta una forma de curva exponencial decreciente. Se trata de una prueba simple, económica y fácil de realizar, y que ha mostrado buena correlación con el CEH. Sin embargo, resulta poco claro qué es lo que realmente se está midiendo. Las concentraciones de insulina alcanzan valores suprafisiológicos, y el descenso de la insulinemia es errático. Es probable que una buena parte del descenso de la glucemia se deba al efecto supresor de la insulina sobre la producción hepática de la glucosa y, al tratarse de un test tan corto, no dé tiempo a cuantificar todo el efecto de la hormona sobre la captación periférica.
Métodos basados en la respuesta glucémica e insulinémica a la sobrecarga oral de glucosa (incluso en respuesta a la ingesta de alimentos)
Uno de ellos es una modificación del MMg que permite la cuantificación de la sensibilidad a la insulina a partir de un test de tolerancia oral a la glucosa o de un test de tolerancia oral a la comida)51. El modelo matemático resulta más sencillo que el MMg original y exige únicamente calcular el área bajo de curva de glucemia e insulinemia. En el trabajo original se analizaron únicamente sujetos sanos y delgados, y se comparó con el MMg modificado con tolbutamida, con buenos resultados. En nuestra unidad metabólica (datos no publicados) lo hemos aplicado a un grupo de 16 sujetos (8 con peso normal y 8 obesos) y lo hemos comparado con los resultados obtenidos con el MMg, observando que el método es capaz de identificar a los sujetos con resistencia a la insulina (r = 0,77; p < 0,05). Su limitación reside en que aún no está adecuadamente validado, en la medida en que no se han comparado sus resultados con los obtenidos con el CEH, y se ha aplicado a un número muy reducido de sujetos, entre los que no se incluyen los más problemáticos, es decir, los diabéticos.
Método de Matsuda et al52. Se basa en datos empíricos. Tiene la ventaja de que permite valorar la sensibilidad hepática a la insulina. En el trabajo original se estudiaron a 153 sujetos, incluyendo individuos con intolerancia a la glucosa y pacientes con diabetes mellitus tipo 2, y la correlación del grupo en conjunto con los resultados obtenidos con el CEH fueron muy buenos (r = 0,73).
Método de Stumvoll et al53. Permite cuantificar no sólo la sensiblidad a la insulina, sino también el MCR y la secreción de la célula beta durante la primera y segunda fase. El método consiste en una ecuación obtenida mediante una regresión lineal múltiple (hay una para cada una de las variables antes indicadas) introduciendo, como variables dependientes, los valores de glucemia e insulinemia durante un TTOG, así como la edad y el IMC. La variable dependiente se obtuvo inicialmente a partir de los resultados de un clamp hiperglucémico y otro hiperinsulinémico euglucémico realizado a un grupo de 104 sujetos no diabéticos. Aunque los resultados obtenidos fueron muy buenos al compararlos con el CEH (r = 0,79), será necesario que estudios independientes validen esta técnica. Posteriomente, los mismos autores publicaron una serie de ecuaciones basadas en la misma metodología en función de los diferentes tiempos de extracción del TTGO54.
El método OGIS55. Se basa en un modelo determinista del comportamiento de la glucemia y la insulinemia durante un TTGO. El método ha sido validado frente al CEH, obteniendo un coeficiente de correlación de 0,77 (que disminuyó cuando se analizaron subgrupos de sujetos: obesos, ITG, DM). La crítica que se puede hacer a este método es que emplea unos valores constantes para los parámetros del mismo que son válidos para el grupo de sujetos de los que se obtuvieron los datos pero que no tienen por qué serlo cuando se aplican a muestras independientes.
Otros métodos. Otros métodos obtenidos de un TTGO son el de Gutt56, el de Avignon57 y el de Belfiore58. La mejor correlación que se obtuvo con el modelo mínimo en los sujetos del estudio IRAS fue con el índice de Avignon (0,77); no obstante, fue el índice de Gutt (que presentó una correlación con el modelo mínimo menor, de 0,68) el que mejor predijo la aparición de diabetes mellitus tipo 2.
El último del que tenemos noticia es el descrito por Soonthornpun et al59, que incluye la determinación de la glucosuria en la orina recogida al final del TTGO. Parte de dos asunciones, la primera es que todos los sujetos absorben la glucosa ingerida en la misma proporción, y la segunda que el consumo de glucosa no mediado por la insulina es igual en todos los sujetos. La glucosa consumida por los tejidos periféricos es la diferencia entre la glucosa absorbida y la glucosa que aparece en plasma y la que se pierde en la orina. A su vez, la glucosa plasmática será el resultado de la que no es consumida por los tejidos periféricos y la producida por el hígado. Este método se ha probado en 33 voluntarios con peso normal y sin ITG y se ha comparado con el clamp euglucémico hiperinsulinémico, siendo el coeficiente de correlación de 0,869. El método fue comparado por los autores con varios de los que hemos analizado, con un resultado claramente superior (tabla 2).
En resumen, de los métodos que se han publicado hasta el momento para cuantificar la sensibilidad a la insulina in vivo, dirigidos a la investigación fisiopatológica, el CEH es, sin duda, el "estándar oro"; y si se acopla a las técnicas que se resumen en la figura 5, sus posibilidades en investigación son extraordinarias. A nuestro juicio, le sigue en fiabilidad el MMg, del que varios grupos de investigación en España (Carmena y Ascaso, Rovira, Ricart y Fernández-Real, y García, además del nuestro) se han servido con resultados notables. En cuanto a los otros métodos que hemos comentado (múltiples ya), que por su sencillez podrían ser utilizados en el estudio de amplias poblaciones (p. ej., epidemiológicos) o en investigación clínica (con muestra numerosa), no parece que haya ninguno que se muestre superior a los otros (sobre todo cuando son comparados con el CEH o MMg por grupos independientes).
De los métodos basados en la cuantificación basal de la glucosa y de la insulina, el HOMA es el que ha superado mejor los controles de fiabilidad. En cuanto a los métodos pertenecientes a la categoría B, los que utilizan valores de la glucosa y de la insulina post-TTGO parecen más robustos que los basados en determinaciones basales, ya que estos últimos valoran fundamentalmente la sensibilidad hepática a la acción de la insulina, pero no la captación muscular. Todos tienen sus ventajas e inconvenientes (contraste con CEH o MMg, número y características de los sujetos estudiados, bases teóricas en las que se sustentan). No deja de llamar la atención (y debe servirnos de advertencia) que, en la gran mayoría de ellos, la correlación obtenida es buena, incluso excelente, cuando la comparación la hacen sus diseñadores, para bajar considerablemente cuando se producen réplicas en otros laboratorios. Deberemos, pues, esperar algún tiempo para que, mediante su aplicación a amplias series de individuos con diversas alteraciones, podamos disponer de los elementos de juicio suficientes para optar por alguno de ellos. Aun así, aplicados a un determinado paciente aislado, la fiabilidad de los métodos pertenecientes a la categoría B es muy dudosa.