Los niños nacidos pequeños para la edad gestacional (PEG) tienen mayor riesgo de presentar anomalías en el neurodesarrollo y la capacidad cognitiva. El objetivo del estudio es determinar el neurodesarrollo de niños PEG durante los primeros 2 años de vida y establecer la influencia de datos antropométricos, la edad gestacional, la gemelaridad y factores perinatales.
Pacientes y métodoEstudio observacional, prospectivo, descriptivo y analítico de la valoración neurocognitiva realizada, con el test de Brunet-Lézine, a niños PEG (n=91) desde los 3 a los 24 meses de edad, comparándola con controles propios.
ResultadosNoventa y un niños PEG, 47% mujeres, 83,5% gestaciones únicas; edad gestacional media 37,7 semanas (desviación estándar [DE] 2,1). Peso al nacimiento 2.053,3g (DE 433,1), longitud 43,9cm (DE 2,6) y perímetro cefálico 31,7cm (DE 1,7). La población PEG presenta un neurodesarrollo significativamente inferior al de la población control, con tendencia a mejorar durante los primeros 2 años de vida. No existen diferencias por sexos. Los niños PEG nacidos de gestaciones múltiples presentan resultados neurocognitivos inferiores únicamente durante el primer año de vida. Existe una correlación directa y positiva entre el peso, la longitud y el perímetro cefálico con el desarrollo neurocognitivo a los 6, 9, 12 y 18 meses. La edad gestacional se correlaciona con un mejor neurodesarrollo a los 3 y 6 meses.
ConclusionesLos niños nacidos PEG presentan un neurodesarrollo inferior al de la población control. Una mayor afectación del peso, la longitud y el perímetro cefálico al nacimiento se correlaciona con peores datos neurocognitivos. La multiparidad no influye significativamente en la evolución del neurodesarrollo.
Children born small for gestational age (SGA) show higher risk of neurodevelopmental and cognitive abnormalities. The objective of this study is to determine in children born SGA the neurodevelopment during the first 2 years of life and to establish the influence of anthropometric data, gestational age, multiple gestation and perinatal factors.
Patients and methodObservational, prospective, descriptive and analytical study of the neurocognitive assessment performed, with Brunet-Lézine test, on SGA children (n=91) from 3 to 24 months of age, comparing with own controls.
ResultsNinety-one SGA children, 47% girls, 83.5% single pregnancies; mean gestational age 37.7 weeks (standard deviation [SD] 2.1). Weight at birth 2,053g (SD 433.1), length 43.9cm (SD 2.6) and head circumference 31.7cm (SD 1.7). The SGA population shows significantly lower neurodevelopment than the control population, with a tendency to improve during the first 2 years of life. There are no differences by sex. SGA children born to multiple gestations have lower neurodevelopment only during the first year of life. There is a direct and positive correlation between weight, length and head circumference with neurocognitive development at 6, 9, 12 and 18 months. Gestational age correlated with better neurodevelopment at 3 and 6 months.
ConclusionsChildren born SGA present lower neurodevelopment than the control population. A greater impact on weight, length, and head circumference at birth is correlated with poorer neurocognitive development. Multiparity does not show significant influence on neurodevelopment evolution.
Se define como pequeño para la edad gestacional (PEG) aquel recién nacido (RN) con peso y/o longitud por debajo de 2 desviaciones estándar (DE) o del percentil 3 para su edad gestacional1,2. Es un concepto estático que utiliza el peso y la longitud en el momento del nacimiento. Esta definición, sin embargo, no distingue entre los RN que son constitucionalmente pequeños de aquellos que durante el embarazo ven restringido su crecimiento, conocido como crecimiento intrauterino restringido (CIR). Se definen como CIR aquellos fetos que durante el embarazo presentan un peso fetal estimado, en este caso mediante ecografía prenatal, menor del percentil 101,3, consecuencia de una noxa o un ambiente intrauterino desfavorable. Se trata, por tanto, de un concepto dinámico que implica un seguimiento ecográfico intrauterino de la velocidad de crecimiento, independientemente de si el peso o la longitud al nacimiento cumplen la definición de PEG. La identificación del niño PEG es importante porque muestra un mayor riesgo de morbimortalidad perinatal y posnatal, pudiendo presentar menor talla durante la infancia, alteraciones del eje adrenal y gonadal, así como de enfermedad cardiovascular, diabetes tipo 2 y síndrome metabólico en la edad adulta2,4.
Nacer PEG podría tener también una influencia negativa sobre el neurodesarrollo, ya que la vida intrauterina y el primer año de vida son periodos críticos para el complejo proceso de desarrollo cerebral5,6. Existen estudios que indican que los niños PEG asocian un deterioro en diversas funciones cognitivas y sensoriales, que en la mayoría de los casos es leve, y puede estar presente desde el periodo neonatal o hacerse evidente en etapas más tardías. Estos niños presentan un volumen cerebral disminuido que podría relacionarse con el deterioro cognitivo7 y que, en estudios morfológicos realizados mediante resonancia magnética, se demuestra ya desde el nacimiento8. El compromiso del crecimiento cerebral afecta sobre todo al volumen del hipocampo, la densidad neuronal, el espesor y la mielinización9.
Estos problemas son objetivables desde la primera infancia, ya que presentan un perímetro cefálico (PC) en percentiles bajos10. Presentan, con mayor frecuencia, problemas neurológicos que afectan a funciones reguladas por la corteza frontal como la atención, la creatividad, el lenguaje, la memoria y las capacidades de aprendizaje, objetivándose en muchos de ellos un trastorno por déficit de atención e hiperactividad10,11.
El deterioro del cociente intelectual (CI) podría ser una de las consecuencias de nacer PEG. Estos niños muestran valores de CI inferiores a los de la población normal, desde los 3 meses hasta los 14 años de edad. Aproximadamente el 22% tendrá valores de CI por debajo de 2 DE, que empeoran progresivamente con la edad e incluso puede determinar retraso mental severo12.
Estos RN podrían tener, por tanto, incrementado el riesgo de anomalías del neurodesarrollo, lo que debería considerarse para diagnosticar precozmente retrasos del desarrollo y para el tratamiento precoz de los mismos13.
No obstante, la evidencia al respecto es débil debido a la heterogeneidad de los estudios, las diferentes medidas de evaluación, el ajuste de los factores de confusión, el pequeño tamaño muestral de los estudios, así como la controvertida definición de PEG. Este estudio pretende analizar de forma prospectiva la relación entre los datos antropométricos al nacimiento, la edad gestacional, la gemelaridad y factores perinatales con el neurodesarrollo durante la primera infancia, en una cohorte de niños nacidos PEG.
Material y métodosSe realiza un estudio observacional, prospectivo, descriptivo y analítico del seguimiento clínico y neurocognitivo de niños PEG nacidos en la maternidad de un hospital terciario, entre los años 2000 y 2015. Estos niños son derivados desde las unidades de Neonatología y Endocrinología Pediátrica, al nacimiento o durante su crecimiento, para realizar de forma voluntaria una evaluación de su desarrollo neurocognitivo desde los 3 hasta los 24 meses. Eran derivados desde estas unidades por cumplir criterios de PEG, independientemente de la evolución neurológica hasta ese momento. A partir de los datos obtenidos sobre neurodesarrollo en los 2 primeros años de vida de esta cohorte, se realiza este estudio.
Se incluyeron como PEG aquellos RN con longitud y/o peso al nacimiento por debajo de 2 DE para su edad gestacional y sexo, según las gráficas del Estudio Español de Crecimiento de 201014. En el caso de RN procedentes de gestaciones múltiples, se utilizaron gráficas específicas para embarazos gemelares (Estudio Español de Crecimiento de 2010), y se incluyeron aquellos que cumplían la definición de PEG14.
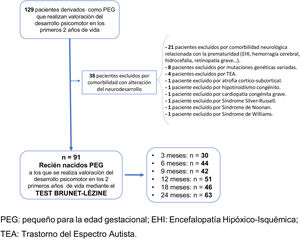
Se excluyeron aquellos RN que presentaban enfermedades con implicaciones en su neurodesarrollo durante la infancia: comorbilidad neonatal derivada fundamentalmente de la prematuridad extrema, deleciones y mutaciones genéticas variadas, síndrome de Silver-Russell, síndrome de Noonan, síndrome de Williams o trastornos del espectro autista.
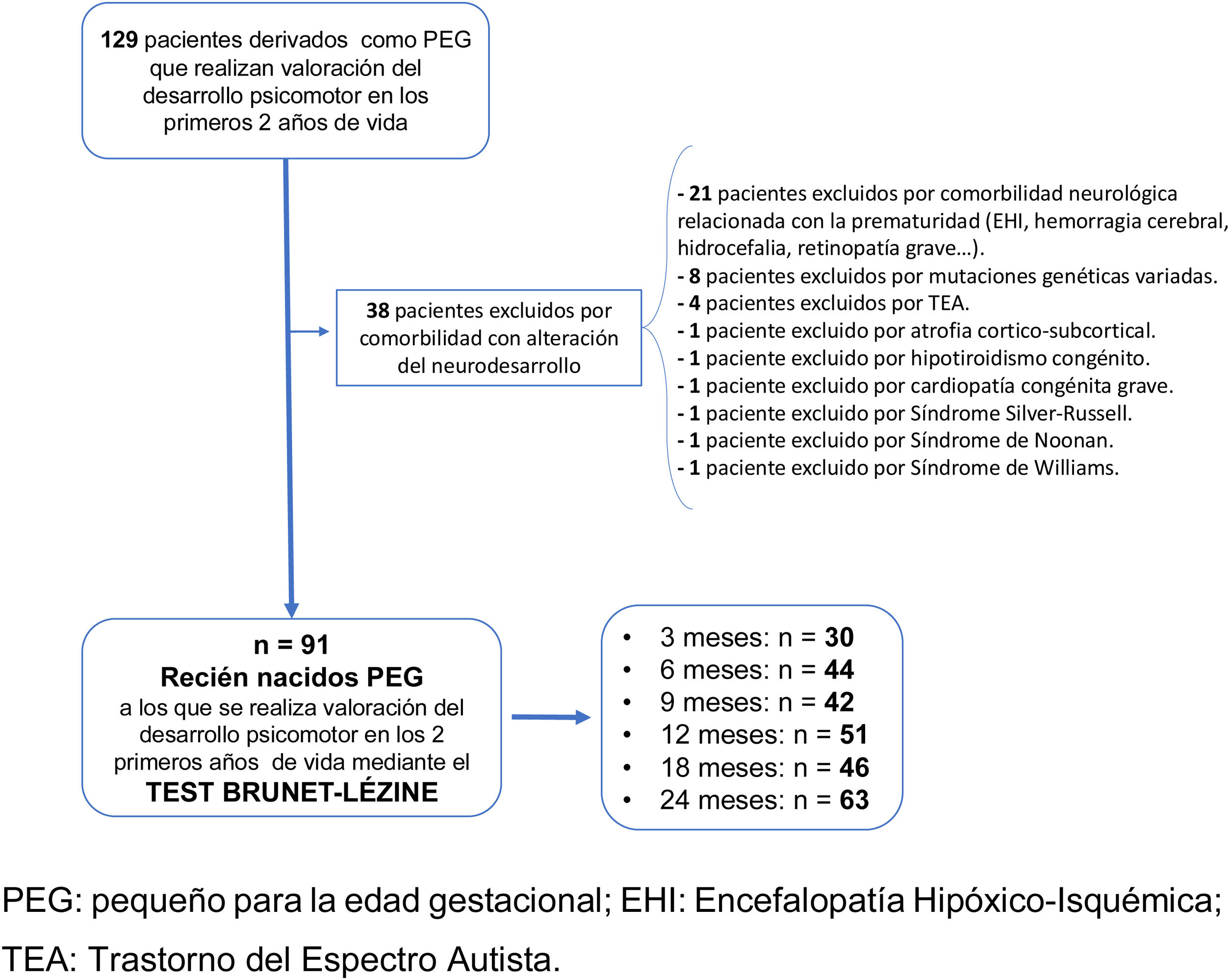
En la figura 1 se muestra el diagrama de flujo de la población a estudio.
La evaluación neurocognitiva se realizó por la misma psicóloga a la edad cronológica de 3 (n=30), 6 (n=44), 9 (n=42), 12 (n=51), 18 (n=46) y 24 meses (n=63). Se aplicó la Escala de Desarrollo Psicomotor de la Primera Infancia de Brunet-Lézine, test validado para conocer el desarrollo psicomotor e intelectual durante los primeros 2 años de vida. Se estandarizaron los resultados con los obtenidos del Estudio Longitudinal del Crecimiento, Desarrollo y Maduración Intelectual15, que sirvieron de grupo control a los 3 (n=233), 6 (n=290), 9 (n=303), 12 (n=299), 18 (n=269) y 24 meses (n=260). La evaluación del desarrollo psicomotor del grupo control fue realizada por la misma psicóloga, mediante el mismo test y en el mismo centro. Los datos referentes a la selección, las características y los resultados de los controles se detallan en el Estudio Longitudinal del Crecimiento, Desarrollo y Maduración Intelectual15.
El test calcula un cociente de desarrollo global (CD), que en la primera infancia reemplaza al CI, a través de los resultados obtenidos en 4 áreas: control postural y motricidad, coordinación oculomotriz, lenguaje/comunicación y sociabilidad/autonomía.
La variable principal fue el Z-score del CD del test de Brunet-Lézine obtenido en cada una de las edades de evaluación. Las variables secundarias fueron Z-score de peso (g), longitud (cm) y PC (cm) al nacimiento, además de sexo, edad gestacional (semanas), gestación única o múltiple y valores del test de Apgar.
Para el análisis y la exposición de resultados se calcularon medidas centrales y de dispersión para variables cuantitativas. Las cualitativas se expresaron como porcentajes con sus respectivos intervalos de confianza al 95%. Se calculó la diferencia de medias y su significación mediante la prueba t-Student para datos independientes, una vez comprobada la normalidad de la distribución. Para el cálculo de correlaciones se utilizó el coeficiente de Pearson o de Spearman según cumplieran o no, respectivamente, el criterio de normalidad de ambas distribuciones.
El umbral de significación estadística se estableció para un valor de p≤0,05.
El proyecto de investigación fue aprobado por el Comité de Ética de la Investigación de la Comunidad de Aragón (CP-CI PI20/293), así como por la Dirección Médica del hospital.
ResultadosSe siguieron 91 niños hasta los 2 años de edad. El 47% fueron mujeres y el 83,5% procedían de gestaciones únicas. El peso medio al nacimiento fue de 2.053,3±433,1g (−2,3 DE), la longitud, de 43,9±2,6cm (−2,6 DE), y el PC, de 31,7±1,7cm (−1,4 DE). La edad gestacional media fue de 37,8±2,1 semanas. La puntuación media del test de Apgar fue de 8,2±1,5 al minuto y de 9,5±0,8 a los 5min.
Por subgrupos, el peso medio al nacimiento de los varones (n=48) fue de 2.096,3±447,6g (−2,3 DE), la longitud, de 44,3±2,5cm (−2,7 DE), y el PC, de 31,9±1,8cm (−1,2 DE). En las mujeres (n=43), 2.005,2±416,3g de peso (−2,4 DE), 43,5±2,7cm de longitud (−2,7 DE) y 31,5±1,5cm de PC (−1,5 DE). Un total de 15 pacientes procedía de gestaciones múltiples, 12 de embarazos gemelares. El peso medio al nacimiento en los PEG procedentes de gestaciones múltiples fue de 1.692,4±355,4g (−2,6 DE), la longitud, de 42,2±2,3cm (−2,8 DE), el PC, de 30,8±2,0cm (−1,3 DE) y la edad gestacional media, de 36,1±1,7 semanas.
Del total de la muestra, 22 PEG eran RN pretérmino, de los cuales 18 fueron prematuros tardíos (≥34 semanas de edad gestacional), con una edad gestacional media de 35,2±1,8 semanas, un peso medio al nacimiento de 1.553,5±375,1g (−2,4 DE), una longitud media de 40,7±2,7cm (−2,8 DE) y un PC de 29,7±1,6cm (−1,6 DE).
En la tabla 1 se muestra la puntuación obtenida del CD global tanto en los niños PEG como en el grupo control15, junto con la diferencia de medias entre ambas. El CD de la población PEG se encuentra significativamente disminuido en comparación con el de los controles.
Comparación de los resultados del cociente de desarrollo en puntuación total de todas las áreas del test de Brunet-Lézine comparadas con el grupo control en las distintas edades de estudio
| PEG | Controles | IC 95% | ||||||
|---|---|---|---|---|---|---|---|---|
| Edad (meses) | CD | n | CD | n | DM | p | Mín | Máx |
| 3 | 99,53 | 30 | 114,6 | 233 | 15,07 | 0,00 | 9,25 | 20,88 |
| 6 | 102,84 | 44 | 108,7 | 290 | 5,86 | 0,00 | 3,40 | 8,32 |
| 9 | 100,07 | 42 | 106,4 | 303 | 6,33 | 0,00 | 4,39 | 8,27 |
| 12 | 96,08 | 51 | 107,1 | 299 | 11,03 | 0,00 | 8,32 | 13,73 |
| 18 | 99,61 | 46 | 104,8 | 269 | 5,19 | 0,00 | 2,80 | 7,58 |
| 24 | 99,89 | 63 | 105,0 | 260 | 5,11 | 0,00 | 2,69 | 7,53 |
CD: cociente de desarrollo; DM: diferencia de medias; IC 95%: intervalo de confianza al 95%; PEG: pequeños para la edad gestacional.
Fuente: Ferrández Longás et al.15.
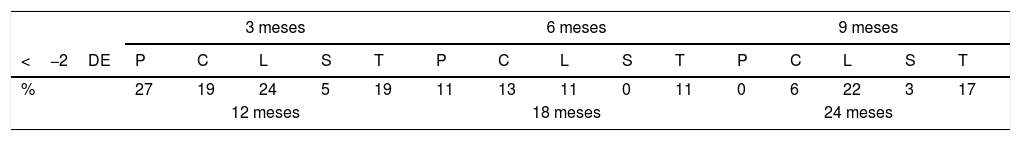
En la tabla 2 se detalla el porcentaje de niños con valores de Z-score por debajo de 2 DE en cada una de las visitas de seguimiento, por cada una de las áreas del test y de forma global.
Distribución expresada en porcentaje de los rangos de desviación estándar del Z-score por debajo de 2 en las distintas visitas de seguimiento por áreas del test de Brunet-Lézine y en total
| 3 meses | 6 meses | 9 meses | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| <−2DE | P | C | L | S | T | P | C | L | S | T | P | C | L | S | T |
| % | 27 | 19 | 24 | 5 | 19 | 11 | 13 | 11 | 0 | 11 | 0 | 6 | 22 | 3 | 17 |
| 12 meses | 18 meses | 24 meses | |||||||||||||
| <−2DE | P | C | L | S | T | P | C | L | S | T | P | C | L | S | T |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| % | 13 | 11 | 26 | 7 | 28 | 13 | 4 | 25 | 9 | 11 | 17 | 5 | 8 | 3 | 10 |
C: coordinación; DE: desviación estándar; L: lenguaje; P: control postural; S: sociabilidad; T: Z-score total.
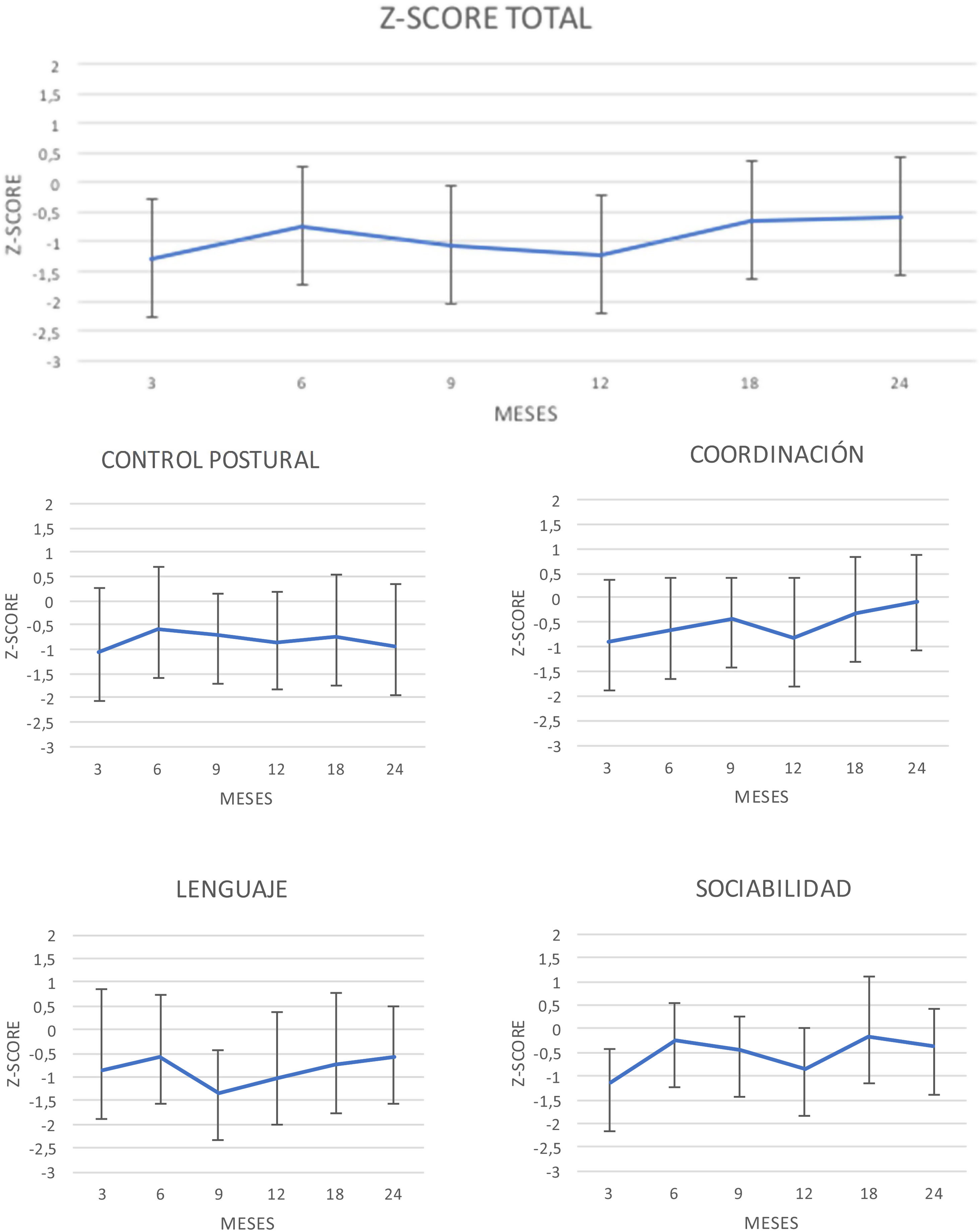
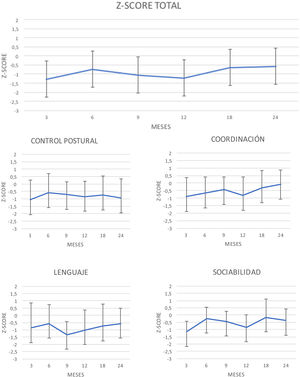
En la figura 2 se observa la evolución en el tiempo de los resultados de la puntuación del CD global y de las puntuaciones de cada área del test.
Se compararon los resultados obtenidos en el CD global y en cada una de las áreas de cada una de las visitas entre sí. Se han encontrado diferencias significativas entre las medias del CD global entre los siguientes momentos: 3 vs. 24 meses (p=0,00); 9 vs. 24 meses (p=0,02), y 12 vs. 24 meses (p=0,02). Por áreas, destacan las diferencias encontradas en el área de coordinación: 3 vs. 24 meses (p=0,00); 6 vs. 24 meses (p=0,00) y 12 vs. 24 meses (p=0,00); en el área del lenguaje: 9 vs. 24 meses (p=0,00), y en el área de sociabilidad: 3 vs. 24 meses (p=0,00) y 12 vs. 24 meses (p=0,00). No se han encontrado diferencias significativas en el control postural.
Al comparar los resultados por sexo, no se encontraron diferencias y únicamente la diferencia de medias fue estadísticamente significativa en coordinación a los 12 meses a favor de las niñas (p=0,01).
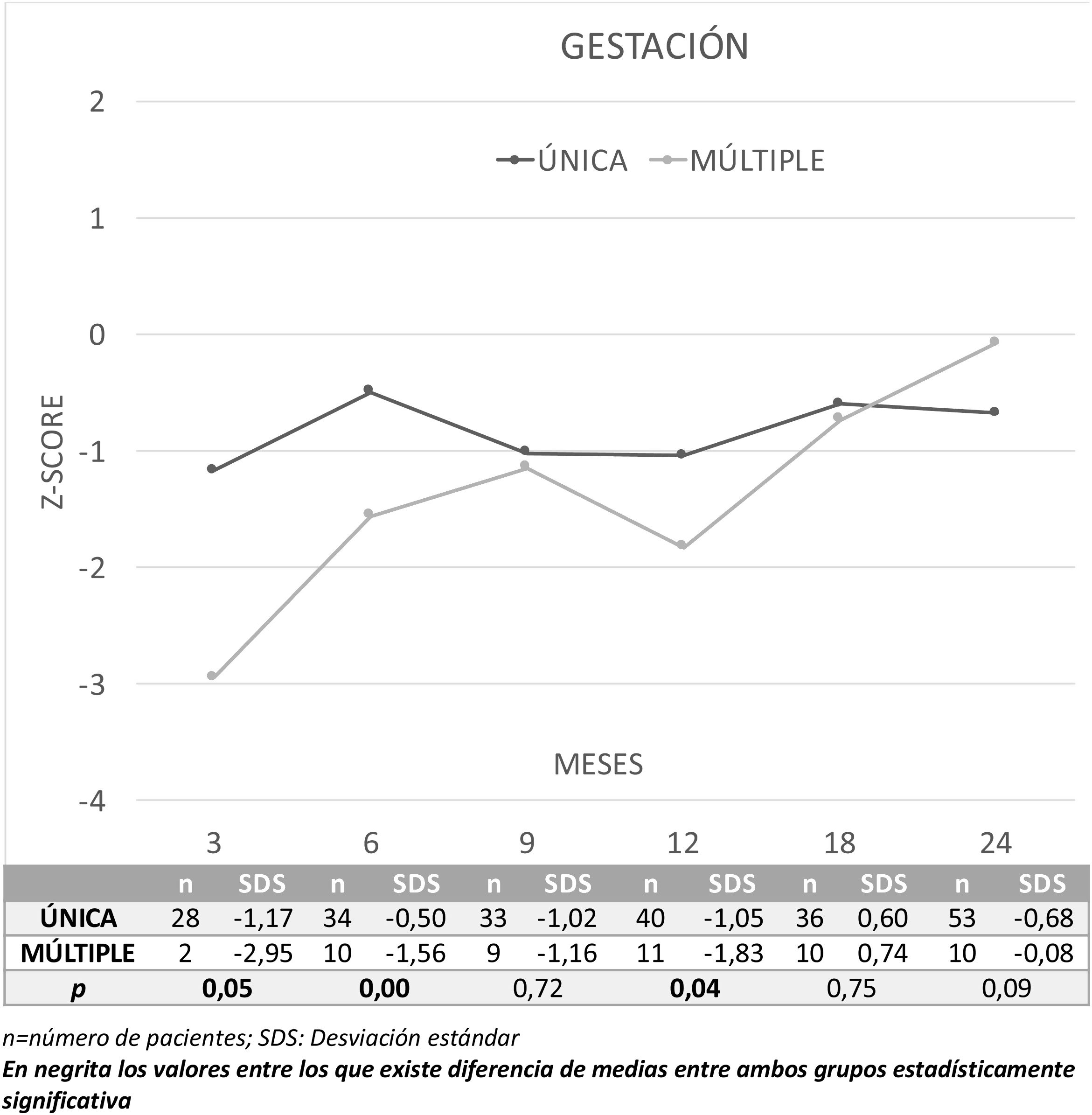
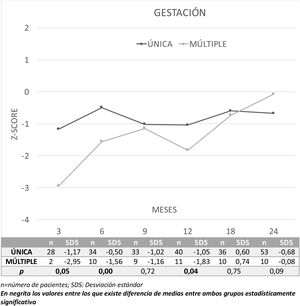
La figura 3 presenta la evolución de los resultados del CD global en Z-score durante los 2 primeros años de vida entre niños nacidos tras gestación única (n=76) o múltiple (n=15) y la comparación entre ambos. Los niños nacidos PEG de gestación única presentan mejor CD a los 3, 6 y 12 meses que los nacidos de gestación múltiple. Por áreas se observan mejores resultados en gestaciones únicas a los 3 meses en las áreas de coordinación (p=0,03) y lenguaje (p=0,04); y a los 6 meses, en coordinación (p=0,00). Por el contrario, el grupo de gestaciones múltiples presenta mejores resultados en el área de coordinación a los 24 meses (p=0,03).
Se calculó la correlación entre los resultados del test y los Z-score de peso, longitud y PC al nacimiento. Se encuentra una correlación positiva entre el Z-score del peso y lenguaje a los 6 meses (r=0,33; p=0,01) y control postural a los 9 (r=0,31; p=0,02). También es positiva entre el Z-score de la longitud y sociabilidad a los 9 meses (r=0,27; p=0,04) y lenguaje a los 12 (r=0,24; p=0,05). Se encontró correlación positiva entre el PC y coordinación (r=0,32; p=0,02) y Z-score total a los 18 meses (r=0,36; p=0,01).
La correlación entre la edad gestacional y las distintas áreas del test fue positiva a los 3 meses en coordinación (rho=0,49; p=0,01) y Z-score total (rho=0,43; p=0,02), y a los 6 meses en control postural (rho=0,41; p=0,01), coordinación (rho=0,35; p=0,02) y Z-score total (rho=0,44; p=0,01).
DiscusiónLos RN PEG presentan peores resultados en el desarrollo neurocognitivo a lo largo de la infancia7,16–19. La mayoría de los estudios se centran en el neurodesarrollo de niños mayores o adultos, siendo escasa la evidencia al respecto en lactantes, objetivo de esta investigación.
En este estudio, centrado en la evaluación del neurodesarrollo precoz, se ha comprobado que las puntuaciones del test son significativamente inferiores a las de la población control nacida adecuada para la edad gestacional.
Históricamente se han utilizado distintas definiciones de PEG. Incluso, en ocasiones, el término CIR se ha utilizado de forma intercambiable con el de PEG20. Von Beckerath et al.21 comparan las diferencias a largo plazo en el neurodesarrollo entre los PEG y los CIR, existiendo un riesgo incrementado de alteraciones en el neurodesarrollo en ambos grupos. Una reciente revisión sistemática22 hace distinción entre los resultados en niños CIR y PEG, obteniendo peores resultados con respecto a los adecuados para la edad gestacional. El presente trabajo considera a estudio solo aquellos RN que cumplen los criterios de PEG, independientemente de si durante el embarazo sufrieron o no un crecimiento restringido.
Se ha valorado la evolución durante los 2 años de seguimiento y parece existir una tendencia a la mejoría, ya que inicialmente se obtienen valores por debajo de 1 DE a los 3, 9 y 12 meses, que mejoran −0,53 y −0,58 DE a los 18 y 24 meses, respectivamente. Los valores de Z-score negativos tanto en el CD global como en las áreas específicas de las que consta el test persistieron en el tiempo, aunque esta evolución no es igual en todas las áreas. Los resultados en el control postural no varían de forma significativa en ninguna de las valoraciones del seguimiento, pero en el área de la coordinación sí existe una evolución positiva, alcanzándose a los 24 meses prácticamente la media poblacional (−0,08 DE). En lenguaje existe un deterioro hasta los 9 meses y una mejoría estadísticamente significativa hasta los 24 meses (desde −1,36 DE a los 9 meses a −0,58 a los 24).
Sobre estos aspectos, Arcangeli et al.23 realizan una revisión sistemática sobre neurodesarrollo en niños PEG, separándolos de los CIR. Los resultados ofrecidos por el metaanálisis muestran que las puntuaciones en Z-score global son significativamente inferiores (−0,32 DE; intervalo de confianza al 95%: −0,38 a −0,25; p=0,00) en los PEG respecto a los controles, tal y como sucede en nuestra serie.
En el análisis por subgrupos, el sexo no parece un factor que condicione el neurodesarrollo, encontrando solo diferencias estadísticamente significativas en coordinación a los 12 meses, a favor de las niñas.
Al tener en cuenta la gemelaridad, se observa que los niños PEG nacidos tras un embarazo múltiple presentan puntuaciones inferiores de manera significativa en el primer año (3, 6 y 12 meses) y estas diferencias desaparecen en el segundo año. Estas diferencias se explicarían probablemente por la necesidad de compartir la nutrición vía placentaria en este tipo de gestaciones.
Se ha encontrado una correlación entre la antropometría neonatal y el desarrollo neurocognitivo. Se observa una correlación positiva y significativa del peso con el área del lenguaje a los 6 y 9 meses en control postural. La longitud al nacimiento se correlaciona de manera positiva y significativa con la sociabilidad a los 9 meses y con el lenguaje a los 12 meses. El PC muestra una correlación positiva significativa a los 18 meses con el CD global y con el área de la coordinación, que a pesar de que la media de PC de la muestra se sitúe por encima de −2 DE (PC 31,7±1,7cm, −1,4 DE), creemos pueda estar justificado por los casos de PEG más pronunciados con valores antropométricos menores. Numerosos estudios son consistentes en que tanto un bajo peso o longitud al nacimiento como una disminución del tamaño cerebral están asociados con un mayor deterioro intraútero y secundariamente con déficits cognitivos más severos. Lee y Houk20, en 2013, establecen el crecimiento cefálico como un importante factor predictor asociado a una reducción de la habilidad cognitiva. Barre et al.24, en 2011, realizan un metaanálisis por el que relacionan un peor desarrollo del lenguaje con el peso muy bajo al nacimiento (<1.500g). De Bie et al.25 justifican que una reducción del volumen cerebral total se correlaciona con el PC, así como con la función cognitiva relativa a la atención.
La edad gestacional ha mostrado una influencia moderada sobre el neurodesarrollo, ya que se ha encontrado una correlación significativa entre peores puntajes del test y menor EG únicamente a los 3 y 6 meses, que se podría explicar porque los test han sido realizados a la edad real y no corregida. Se decidió analizar de forma conjunta RN pretérmino y a término debido a que la gran mayoría eran pretérmino tardíos (18 de los 22 RN pretérmino con una edad gestacional media de 35,2±1,8 semanas), y en estudios previos se ha comprobado una evolución similar en ambos grupos18.
No obstante, en la revisión de De Bie et al.25 se comprueba que el CI en niños pretérmino es inferior tanto en los nacidos con un peso adecuado para la edad gestacional como en los PEG, siendo más bajo en los niños pretérmino nacidos PEG. Por su parte, Graz et al.26 concluyen que nacer PEG y pretérmino parece tener un leve impacto sobre el neurodesarrollo a la edad estudiada, predominando los síntomas de hiperactividad, y recalcan que los predictores de neurodesarrollo más potentes parecen ser la edad gestacional, tener graves lesiones cerebrales, el nivel socioeconómico, experimentar asfixia perinatal y la exposición al tabaco.
Nuestro estudio presenta limitaciones relacionadas con posibles factores de confusión que pueden influir de forma extrínseca en el desarrollo, como el nivel socioeconómico familiar y la clase social. La muestra de pacientes no fue escogida de forma aleatoria, sino que son los padres los que deciden colaborar en el estudio de forma voluntaria y esto ha condicionado que no en todos los controles se obtuviese el mismo número de pacientes. La fortaleza del estudio es su seguimiento longitudinal y que la valoración del desarrollo neurocognitivo ha sido realizada por la misma psicóloga y por la estandarización de los mismos con valores de normalidad propios15.
ConclusionesEl presente trabajo muestra que el desarrollo neurocognitivo de los niños nacidos PEG durante los 2 primeros años de vida, si bien se encuentra dentro de la normalidad, se sitúa significativamente por debajo de la población control. Parece ser que los factores que mayor impacto muestran en dicho desarrollo son la auxología perinatal y, en menor medida, la edad gestacional, siendo destacable la influencia de la multiparidad únicamente en el primer año de vida. Por todo ello, el antecedente perinatal de haber nacido PEG debe ser considerado como un posible factor de riesgo para la evolución neurocognitiva de estos niños, lo que hace, por tanto, recomendable un seguimiento más estrecho con el fin de detectar alteraciones en su neurodesarrollo de forma precoz.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Los resultados preliminares incluidos en este artículo fueron presentados en forma de Comunicación Oral en el XLI Congreso de la Sociedad Española de Endocrinología Pediátrica (SEEP), Madrid 22-24 de mayo de 2019.