La insuficiencia ovárica primaria es una condición en la que las mujeres menores de 40años experimentan oligomenorrea o amenorrea durante 4meses o más; esta pérdida temprana de la función ovárica puede estar relacionada con una serie de etiologías, incluidos trastornos genéticos, autoinmunes, infecciones o causas iatrogénicas; no obstante, del 74 al 90% son idiopáticas. A pesar de ser una alteración poco prevalente, es de gran importancia clínica, ya que afecta en múltiples aspectos de la vida a todas las mujeres. En la actualidad se están desarrollando diferentes estudios con el fin de encontrar nuevos blancos moleculares para establecer nuevas terapias para el tratamiento de esta patología.
Primary ovarian failure is a condition in which women under 40 experience oligomenorrhea or amenorrhea for 4months or longer; this early ovarian function loss may be related to a series of etiologies, including genetic disorders, autoimmune diseases, infections or iatrogenic causes; however 74%-90% are idiopathic. Despite being a less prevalent disorder, it is of great clinical importance since it affects all women in multiple aspects of life. At present, different studies are being developed in order to find new molecular targets to establish new therapies for the treatment of this pathology.
La insuficiencia ovárica primaria (IOP) es una condición en la que las mujeres menores de 40años experimentan oligomenorrea o amenorrea durante 4meses o más, asociado a niveles de hormona foliculoestimulante (FSH) en rangos de la menopausia, en al menos dos ocasiones con un mes de diferencia de acuerdo con las directrices más recientes de la Sociedad Europea de Reproducción Humana y Embriología (European Society of Human Reproduction and Embryology [ESHRE])1,2. Esta pérdida temprana de la función ovárica puede estar relacionada con una serie de etiologías, incluidos trastornos genéticos, trastornos autoinmunes, infecciones o causas iatrogénicas relacionadas con la quimioterapia, la radiación o la cirugía, con alteraciones en el metabolismo y con exposición a toxinas ambientales; pese a esto, actualmente del 74% al 90% son idiopáticas3,4.
Se pueden asociar tres mecanismos potenciales con IOP: disminución congénita de los folículos primordiales, atresia folicular acelerada e incapacidad para reclutar folículos primordiales; dichos mecanismos pueden variar desde la apoptosis de las células foliculares y la atrofia celular hasta el daño en los vasos sanguíneos5,6. Estos mecanismos pueden ser desencadenados por intervenciones médicas como la cirugía ovárica o la terapia del cáncer citotóxico, trastornos metabólicos y de almacenamiento, infecciones, anomalías cromosómicas y enfermedades autoinmunes4. La IOP a menudo tiene una base genética, con más de 50 genes en los que las mutaciones pueden ser directamente causales y muchos otros genes con posible implicación en diferentes procesos, como el desarrollo gonadal, la replicación del ácido desoxirribonucleico (ADN) y la reparación del mismo, la señalización hormonal, la función inmunológica y el metabolismo; sin embargo, no se ha dilucidado por completo la etiología precisa, ni todos los genes asociados a la IOP7.
El espectro clínico de la IOP es generalmente variable, con síntomas como la amenorrea, la disfunción sexual y la infertilidad, mientras que las consecuencias de la enfermedad pueden incluir el aumento del riesgo cardiovascular y la disminución de la densidad ósea, principalmente8,9.
MetodologíaSe realizó la búsqueda de literatura, principalmente artículos de investigaciones originales en MEDLINE, EMBASE, Lilacs y Science Direct durante julio de 2021 y noviembre del mismo año. Se empleó la combinación de palabras clave y términos MeSH relacionados con insuficiencia ovárica primaria, enfermedades del ovario y ginecología.
EpidemiologíaLa IOP afecta a una de cada 10.000 mujeres a los 20años, una de cada 1.000 a los 30años y una de cada 100 a los 40años10,11. Una de cada 130-250 mujeres es portadora de la pre-mutación FMR1, causa genética más común de IOP que afecta al 15-24% de las portadoras de esta pre-mutación12. Por otro lado, la pre-mutación es responsable del 1,6 al 3,2% de la IOP esporádica y del 11,5 al 16% de IOP familiar, que corresponden a una alta prevalencia de IOP asociada a FMR1 en la población general13.
Sin embargo, algunos estudios han mostrado una variación en la prevalencia de la IOP según el origen étnico, que iba desde el 1,4% entre las mujeres de ascendencia afroamericana e hispana hasta el 1,0% entre las mujeres de ascendencia europea, el 0,5% entre las mujeres de ascendencia china y el 0,1% entre las mujeres de ascendencia japonesa14,15.
Aproximadamente el 50% de las pacientes con IOP tienen una función ovárica variable e impredecible, el 25% de estas tienen una ovulación espontánea y cerca del 5 al 10% de las mujeres tienen una concepción espontánea y un embarazo exitoso después de recibir su diagnóstico16,17.
Cerca del 60% de las mujeres con amenorrea primaria presentan alteraciones en el cariotipo, en comparación con el 13% de las pacientes que tienen amenorrea secundaria16.
FisiopatologíaPara comprender mejor la fisiopatología de la IOP se debe tener claro el ciclo ovárico, en el cual, aproximadamente cada 28días por acción de las gonadotropinas liberadas por la adenohipófisis, se genera el inicio de la fase folicular, en donde hay crecimiento de 8 a 12 folículos ováricos, los cuales liberan principalmente estrógenos; de ellos, solo uno madura y se ovula el día 1418. Luego de esto comienza la fase lútea, en la que el cuerpo lúteo secreta principalmente estrógenos y progesterona18. Después de 2semanas el cuerpo lúteo se degenera y ello produce el comienzo de la menstruación18.
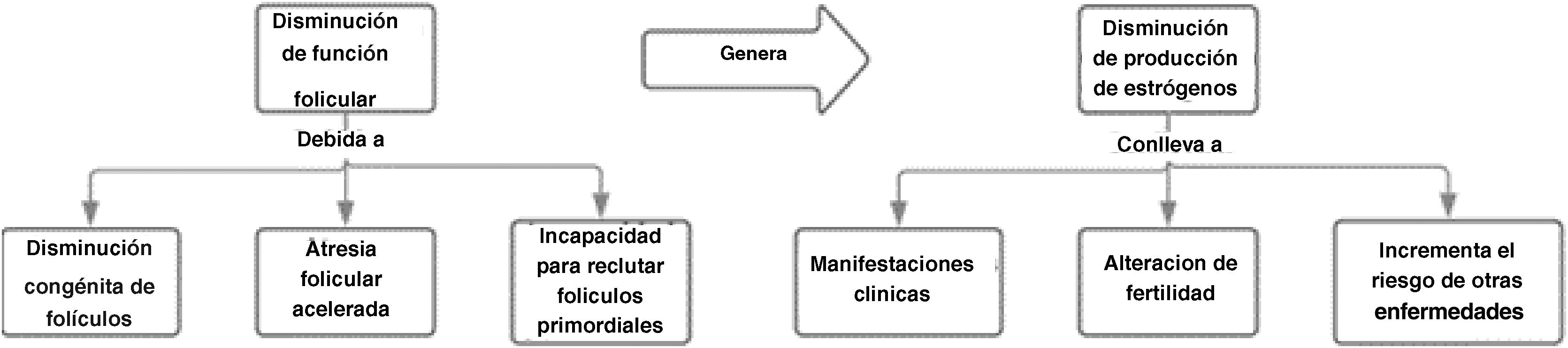
En la IOP, la función de la adenohipófisis se encuentra íntegra, pero existe un compromiso de la función ovárica, específicamente de los folículos, que puede deberse a una disminución congénita de los folículos primordiales, a la atresia folicular acelerada o a la incapacidad para reclutar folículos primordiales, y por tanto los niveles de estrógenos se van a ver reducidos, lo que conlleva la alteración del ciclo ovárico7,19,20 (fig. 1).
Fisiopatología de la insuficiencia ovárica primaria.
Fuente: adaptado de Cox y Liu6.
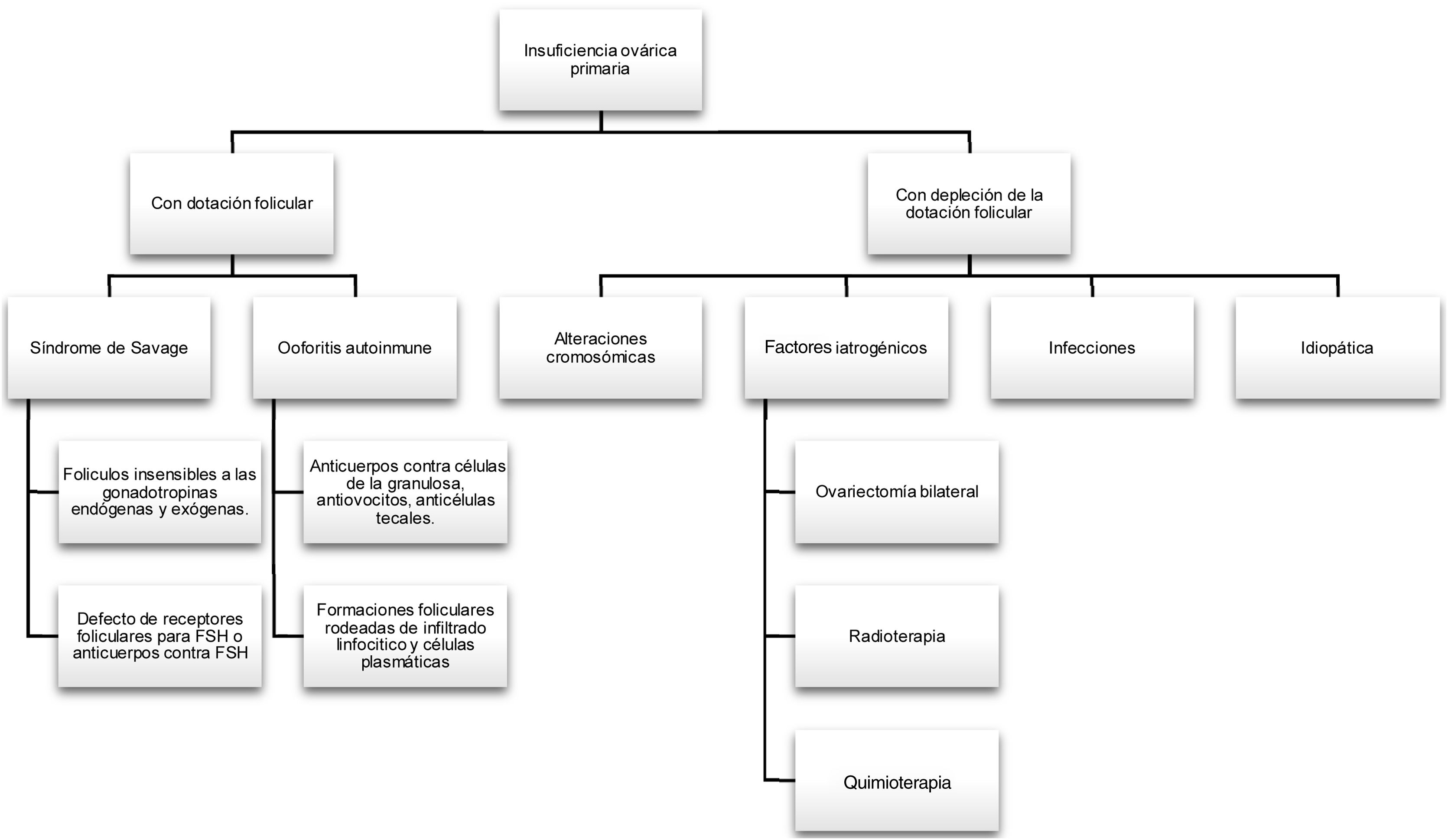
Según la causa, se puede clasificar como IOP con dotación folicular, en las cuales se presentan abundantes folículos primarios y elevación de gonadotropinas, y como insuficiencia ovárica con depleción de la dotación folicular (fig. 2).
Manifestaciones clínicasLa presentación clínica de la IOP puede ser variable, pero el síntoma inicial más frecuente es la alteración menstrual, en particular la oligomenorrea o la amenorrea8. La mayoría de las mujeres que desarrollan IOP experimentan una pubertad normal y establecen un patrón de menstruación regular antes del desarrollo de la enfermedad, por lo que no hay una historia menstrual característica que la anuncie8.
Pese a que la mayoría de las pacientes pueden experimentar una pubertad normal, algunas niñas con IOP pueden presentar retraso en la pubertad o amenorrea primaria, mientras que las adultas jóvenes pueden tener amenorrea secundaria con o sin síntomas vasomotores como sofocos, sudoración nocturna, dispareunia y sequedad vaginal; sin embargo, debido a que la función ovárica intermitente ocurre en aproximadamente del 50 al 75% de las mujeres con IOP, la ausencia de síntomas vasomotores no debe ser un criterio para descartar el diagnóstico de IOP en una mujer que presenta irregularidad menstrual; por otro lado, algunas pacientes adultas pueden presentar infertilidad como único síntoma2,21.
A veces la IOP se manifiesta por primera vez como la ausencia de periodo menstrual después de suspender los anticonceptivos orales o después de un embarazo. En el caso de los anticonceptivos orales, son estos los encargados de enmascarar la mayoría de las características de la IOP, incluido el cambio en los ciclos menstruales, los sofocos y el aumento de las gonadotropinas séricas, por lo que las pacientes desarrollan los síntomas hasta que dejan de tomar los anticonceptivos22,23.
Las pacientes comúnmente exhiben perfiles endocrinos típicos con gonadotropina continuamente elevada, con valores de FSH >40UI/l y niveles de estradiol cercanos a 25pg/ml; alrededor del 50% de las pacientes manifiestan deficiencia de testosterona24,25.
Las consecuencias del hipoestrogenismo temprano que tienen las mujeres con IOP suelen asociarse con un riesgo incrementado de enfermedad cardiovascular y alteraciones óseas como la osteoporosis y la disminución de la densidad ósea, además de otros síntomas, como la pérdida del deseo sexual, alteraciones en el sueño, labilidad emocional, depresión y ansiedad25,26.
Metaanálisis previos, que incluyen estudios en Japón, Corea, Estados Unidos, China, Noruega, Dinamarca y Países Bajos, han hallado una asociación de la IOP con un mayor riesgo de cardiopatía isquémica27-29. Un análisis del estudio Nurse Cohort informó un riesgo 2,1 veces mayor de cardiopatía isquémica en las mujeres que experimentaron la menopausia antes de los 40años en comparación con las mujeres que la desarrollaban luego de los 45años30. Incluso se han notificado cambios en el perfil lipídico aterogénico en estas mujeres coincidiendo con niveles más altos de triglicéridos y HDL marginalmente más bajos, lo que podría contribuir a este aumento del riesgo de enfermedad cerebrovascular31.
La IOP se asocia con un mayor riesgo de depresión y de ansiedad, en gran parte debido al diagnóstico de infertilidad y a la falta de apoyo psicosocial; de manera similar, las mujeres con IOP reportan una menor autoestima, mayor ansiedad y timidez social, y más síntomas de depresión en comparación con las mujeres que no la padecen32. De hecho, la prevalencia de depresión es mayor entre las mujeres con IOP en comparación con las mujeres control, y parece estar asociada a la gravedad de los síntomas vasomotores33.
A través de los años se ha demostrado que los estrógenos son neuroprotectores, e incluso estudios de neuroimagen en humanos sugieren que el estrógeno mejora la actividad cerebral relacionada con el procesamiento de la memoria, por lo que su deficiencia a una edad temprana en teoría aumentaría el riesgo de una mujer de deterioro cognitivo y demencia34.
Las mujeres con IOP padecen el síndrome del ojo seco significativamente más que las mujeres con función ovárica normal34. El síndrome del ojo seco en mujeres con IOP no se asocia con una reducción en la producción de lágrimas, sino con la existencia de receptores de hormonas sexuales en los tejidos de la superficie ocular, lo que proporciona un mecanismo potencial por el cual las hormonas ováricas podrían alterar esta función34.
La presentación de la IOP también puede estar asociada a varios trastornos autoinmunes, como hipotiroidismo autoinmune, insuficiencia suprarrenal, diabetes mellitus tipo1, anemia perniciosa e hipoparatiroidismo, siendo el hipotiroidismo el más común, con una incidencia del 8% en las mujeres que padecen esta condición30. Por ello, en ocasiones se puede encontrar bocio, debido a la tiroiditis de Hashimoto o a la enfermedad de Graves, incremento de la pigmentación de la piel o vitíligo en relación con la insuficiencia suprarrenal primaria autoinmune, pudiéndose presentar también en estos casos hipotensión ortostática30.
Mecanismos moleculares de la insuficiencia ovárica primariaLas causas genéticas, como anomalías cromosómicas y mutaciones puntuales, han sido descritas en la presentación de la enfermedad sindrómica (por ejemplo, Turner, síndromeX frágil y síndrome de blefarofimosis, ptosis y de epicanto inverso [BPES]) y no sindrómica17,35,36. Estas causas se pueden atribuir a una minoría de pacientes, ya que alrededor del 90% de los casos de IOP se consideran idiopáticas, sin vínculo genético aparente ni causa conocida37. Comprender los mecanismos moleculares subyacentes es esencial para desarrollar estrategias de prevención, de diagnóstico temprano y para un mejor manejo de la IOP38.
Estudios genealógicos en familias afectadas han mostrado un modo sugerente de transmisión hereditaria autosómica dominante o recesiva, con expresividad altamente variable o herencia ligada al cromosomaX con penetrancia incompleta38.
Un gran número de proteínas se han relacionado con el desarrollo y los procesos fisiológicos del ovario, además de las variantes en al menos 20 genes que han sido identificados mediante pruebas funcionales en casos de IOP35,39,40. En el estudio realizado por Patiño et al.41 se llevó a cabo la secuenciación del exoma en 69 mujeres caucásicas afectadas por IOP y describieron 55 variantes candidatas, ubicadas en 49 genes potencialmente relacionados con el fenotipo. En las afectadas se pueden presentar al menos dos mutaciones en diferentes genes, por lo que se argumenta que la IOP es de origen poligénico41. Los genes mutados están involucrados en varios procesos biológicos clave, tales como meiosis, desarrollo folicular, diferenciación/proliferación de células granulosas, ovulación, metabolismo celular y regulación de la matriz extracelular42.
Por detección genómica de pequeños reordenamientos genómicos es posible identificar nuevos genes involucrados en el desarrollo ovárico, tanto en el cromosomaX como en los autosomas, y el estudio realizado por Norling et al.43 identificó nuevos genes candidatos para el desarrollo y la función ovárica mediante hibridación genómica comparativa.
El estudio realizado por Wang et al. demostró que la mutación heterocigótica del gen KHDRBS1 (proteína KH que contiene el dominio, unión a ARN, proteína asociada a la transducción de señales1) ejercía un efecto significativo sobre el nivel de expresión del empalme alternativo del ARNm y también podía producir un alto riesgo de susceptibilidad de penetrancia para la IOP al afectar la replicación y la reparación del ADN; este hallazgo proporciona a los investigadores y clínicos una mejor comprensión de la etiología y del mecanismo molecular de la enfermedad44.
DiagnósticoNo existe un consenso sobre los criterios diagnósticos de la IOP, especialmente para las pacientes jóvenes, pero algunos sugieren los siguientes: al menos 4meses de menstruación alterada, FSH elevada, retraso en la pubertad o amenorrea primaria, mientras que los pacientes adultos jóvenes pueden presentar amenorrea secundaria con o sin síntomas vasomotores, como sofocos, sudores nocturnos, dispareunia y sequedad vaginal7,17.
El diagnóstico de la IOP incluye pruebas como el cariotipo, el análisis de la permutación del gen1 de retraso mental del cromosomaX frágil (fragile X messenger ribonucleoprotein1 [FMR1]) y los autoanticuerpos suprarrenales, ya sea por inmunoprecipitación o por inmunofluorescencia. Adicionalmente se recomiendan estudios después de la confirmación del diagnóstico: ecografía pélvica, absorciometría de rayosX de energía dual para medir la densidad ósea y autoanticuerpos tiroideos7,17.
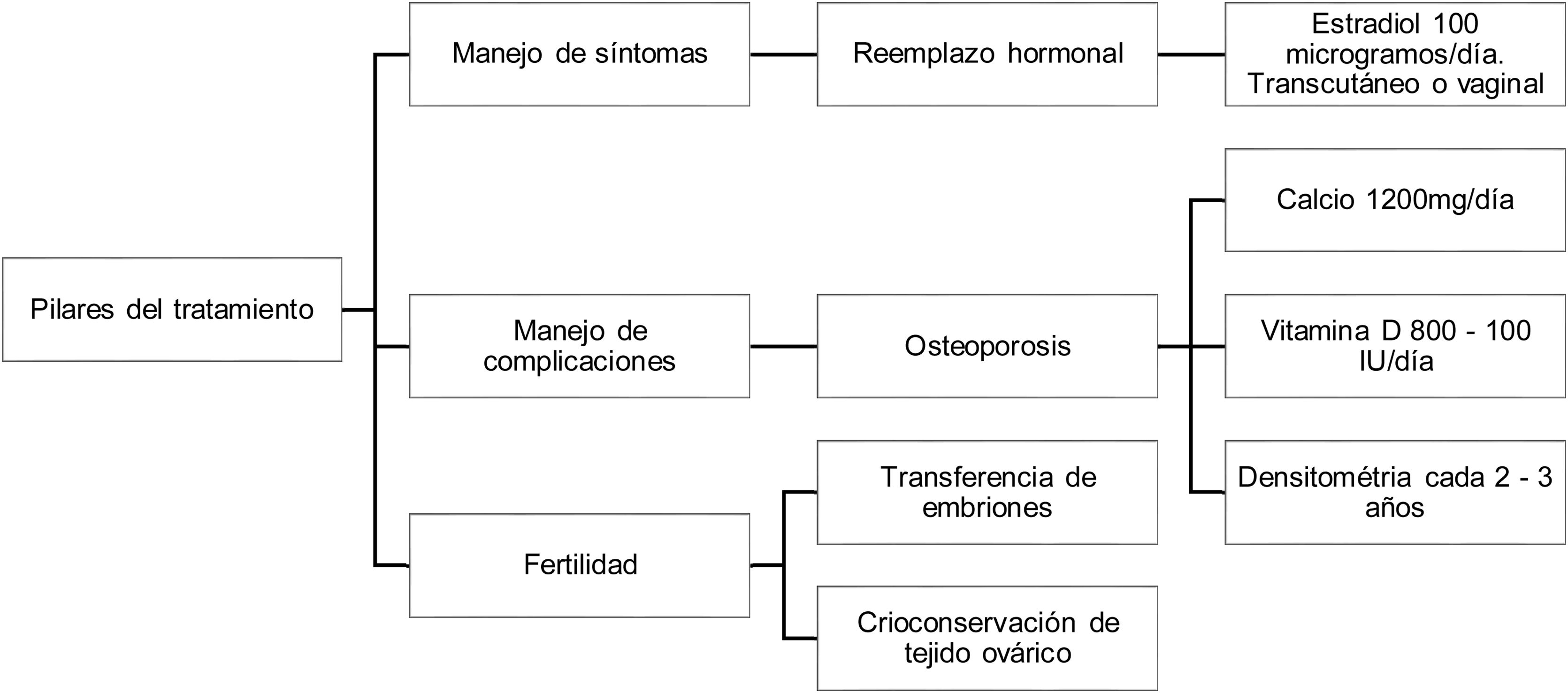
TratamientoEn el tratamiento de la IOP es de vital importancia tener tres pilares fundamentales: manejo de síntomas, conservación de la fertilidad y manejo de complicaciones asociadas a bajos niveles de estrógenos, como osteoporosis y enfermedades cardiovasculares19 (fig. 3).
Pilares del tratamiento de la insuficiencia ovárica primaria.
Fuente: adaptado de Luisi et al.19.
El enfoque terapéutico más frecuente para la infertilidad en la IOP es la transferencia de embriones desde ovocitos donados, aunque las parejas que los requieren deben discutir aspectos médicos, éticos, legales y psicológicos con el médico38.
La crioconservación de tejido ovárico seguida de autotrasplante es un método prometedor para la preservación de la fertilidad en mujeres sometidas a tratamientos gonadotóxicos. En contraste con la congelación de ovocitos, que requiere el almacenamiento de ovocitos maduros aislados a partir de folículos preovulatorios, la crioconservación es adecuada para niñas prepúberes, ya que preserva sus ovocitos inmaduros en folículos ováricos tempranos. Posteriormente se realiza el trasplante ovárico y los folículos tempranos pueden convertirse en folículos preovulatorios y permitir la generación de ovocitos maduros para tratar la infertilidad45.
Los desarrollos tecnológicos recientes con células madre pluripotentes inducidas permiten la reconstitución de la ovogénesis completa, pero solo se ha logrado en modelos murinos38.
ConclusiónLa insuficiencia ovárica primaria es una alteración poco frecuente pero de gran importancia clínica, ya que afecta en múltiples aspectos de la vida a todas las mujeres, que van desde el aumento del riesgo cardiovascular, alteraciones óseas, problemas reproductivos y cognitivos, hasta los trastornos genéticos y emocionales.
Aunque la principal causa de IOP sea idiopática, esta se ha podido asociar a múltiples afecciones comunes, factores que deben ser tenidos en cuenta en el abordaje de las pacientes con el fin de identificar y brindar un adecuado enfoque de tratamiento y, de esta manera, mejorar el pronóstico y la calidad de vida de las mujeres que la padecen.
Responsabilidades éticasProtección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datos. Los autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informado. Los autores declaran que en este artículo no aparecen datos de pacientes.
Consideraciones éticasNo fueron necesarias debido a que es un artículo de revisión de tema.
FinanciaciónNo se dispuso de ninguna fuente de financiación.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.