Valorar si el adelgazamiento del segmento uterino inferior puede aumentar el riesgo de complicaciones obstétricas. Y determinar cuál es el método de elección para su correcta medición.
Material y métodoRevisión bibliográfica de la literatura y exposición de un caso clínico.
Resultados, caso clínicoPresentamos el caso de una gestante con una degeneración quística de la cicatriz uterina que durante la gestación se resuelve: se produce el parto a término y sin complicaciones obstétricas ni neonatales.
Comentario, discusión y revisión de la literaturaLa ecografía se valora como una técnica fácil, reproducible y con una metodología ya definida a la hora de valorar una cicatriz anterior. Aun así, no disponemos de una técnica estandarizada para la medición del segmento uterino inferior. La mayoría de los autores y algunas sociedadesestán de acuerdo en que faltan estudios homogéneos y un punto de corte definitivo. A pesar de los estudios publicados, no hay datos que indiquen que la dehiscencia de la cicatriz uterina requiere reparación para su adecuada cicatrización.
ConclusionesEl mejor método diagnóstico es la histerosonografía. La medición del segmento uterino inferior en el tercer trimestre podría ser útil para decidir la vía de parto. No se puede determinar un punto de corte para predecir el riesgo de rotura uterina o dehiscencia de cicatriz uterina. Se requieren más estudios para establecer una técnica adecuada y un punto de corte mediante el cual se pueda clasificar a las pacientes y tomar decisiones respecto a la vía de parto. El punto de corte más definido en los estudios para el segmento uterino inferior es 3.5-3.2. El factor más importante de las pruebas de imagen es valorar si son capaces o no de predecir las complicaciones obstétricas que pueden suceder, el riesgo de afectación materna o fetal y la opción de la vía vaginal. Faltan estudios para tomar decisiones clínicas conforme a estos resultados.
To assess whether thinning of the lower uterine segment may increase the risk of obstetric complications and to determine the most effective method to study its correct measurement.
Material and methodLiterature review and case report.
Results case reportWe present the case of a pregnant woman with cystic degeneration of a uterine scar during pregnancy. The delivery occurred at term with no obstetric or neonatal complications.
Comment, discussion and literature reviewUltrasound is considered an easy-to-use and reproducible technique with a well-defined methodology to assess a prior caesarean scar. Nevertheless, there is still no standardised technique to measure the lower uterine segment. Although most authors and some societies are in agreement, there is a lack of homogeneous studies and a definitive cut-off value. Despite published studies, there are no data to suggest that uterine scar dehiscence requires repair for proper healing.
ConclusionsThe most effective diagnostic method is hysterosonography. Measurement of the lower uterine segment in the third trimester could be useful to decide the route of delivery. A cut-off cannot be determined to predict the risk of uterine rupture or uterine scar dehiscence. Further studies are required to establish an adequate technique and a cut-off value to classify patients and aid decision-making on the route of delivery. The most clearly defined cut-off for the lower uterine segment is 3.5-3.2. The most important factor in imaging tests is to evaluate whether they are able to predict the obstetric complications that may occur, the risk of maternal or foetal compromise and the option of vaginal delivery. There are no studies on clinical decision-making according to these results.
Nuestro objetivo es valorar si el adelgazamiento del segmento uterino inferior puede aumentar el riesgo de complicaciones obstétricas, entre otras, y la más importante, la rotura uterina. Valorar cuál es el método más eficaz para estudiar la cicatriz de una cesárea, el concepto de dehiscencia de cicatriz, resolver si esta aumenta el riesgo de rotura uterina y si es necesario reparar una dehiscencia para prevenirlo son otros de los objetivos.
Exponemos la evolución y resultado obstétrico de un caso de degeneración quística de la cicatriz uterina y realizamos una revisión bibliográfica de la literatura sobre el riesgo de rotura uterina en caso de dehiscencia de cicatriz anterior.
Material y métodoRevisión bibliográfica de la literatura y exposición de un caso clínico.
ResultadosMujer de 34 sin antecedentes médicos de interés. Como antecedente quirúrgico destaca una cesárea anterior por riesgo de pérdida de bienestar fetal. Esterilidad secundaria de un año de evolución controlada en la Unidad de Reproducción Asistida del Hospital Donostia.
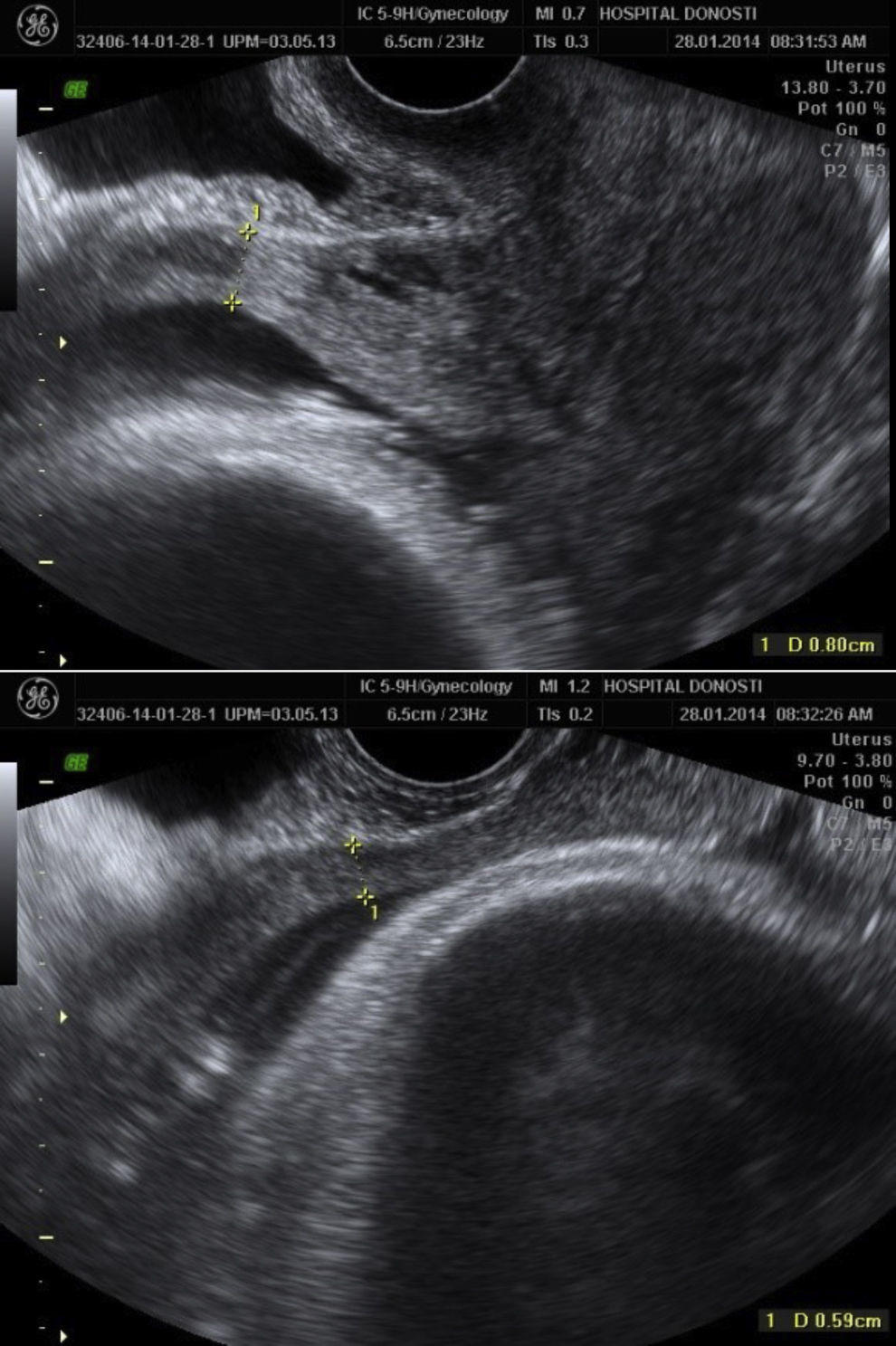
La paciente acude a la Unidad de Reproducción Asistida por esterilidad secundaria de un año de evolución. Durante el estudio, se objetiva en la ecografía un área líquida de 2,5×2cm en zona del istmo uterino, a nivel de la zona de histerotomía, con adelgazamiento de dicha zona.
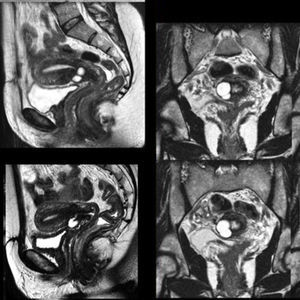
Con sospecha de dehiscencia de la cicatriz uterina se realiza una RMN y una histerosalpingografía para completar el estudio.
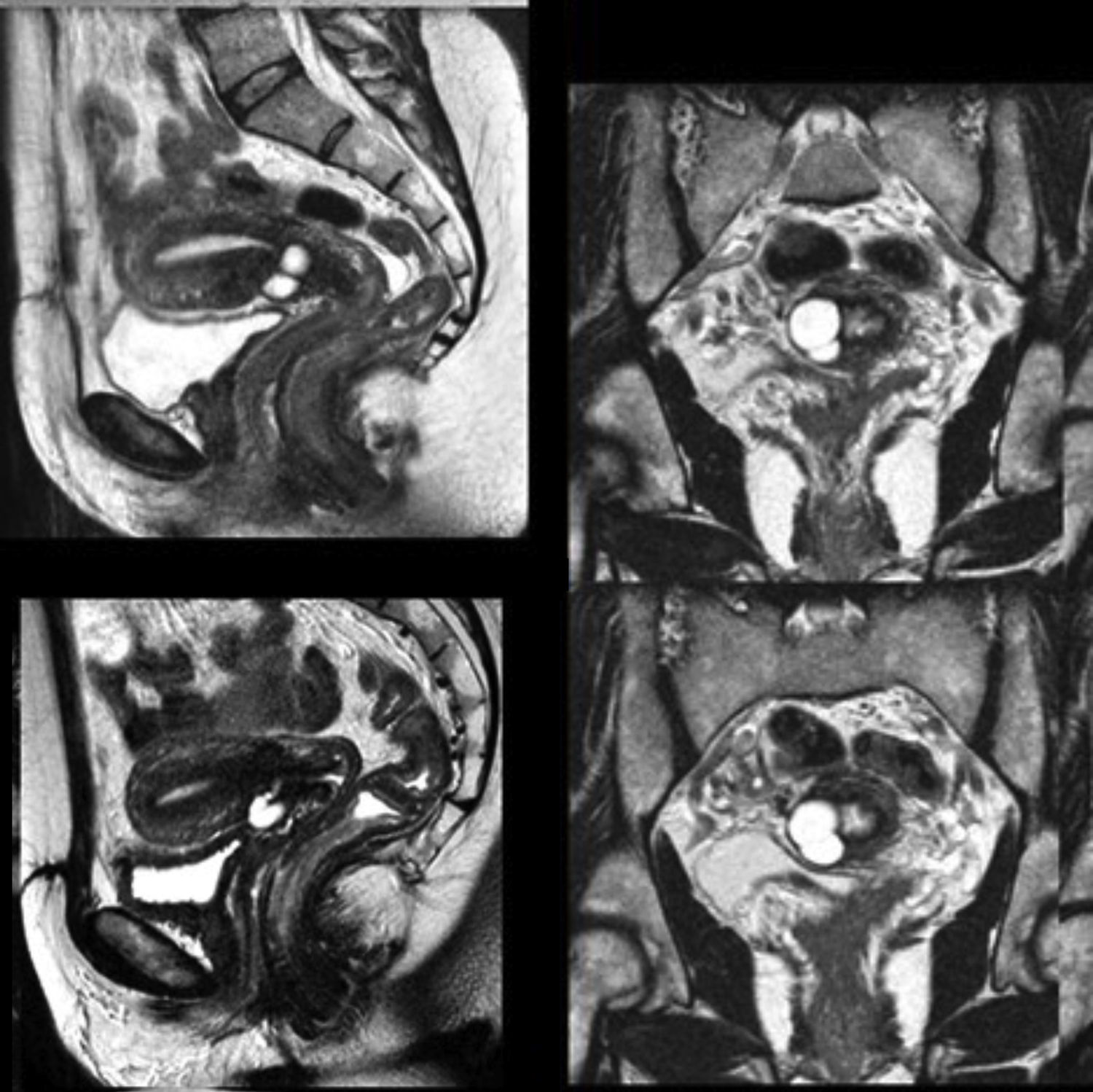
La RMN (ver fig. 1) informa de una área multiquística en la cara anterior del istmo, con comunicaciones filiformes milimétricas a través del estroma cervical de la cavidad. Dados su antecedente y localización, la imagen es sugestiva de degeneración quística cicatricial. Se propone valorar si se completa el estudio mediante histerografía para confirmar la comunicación.
La histerosalpingografia no es informativa, ya que la sonda se queda acodada en el interior del canal cervical, en la cicatriz o lesión quística, sin lograrse el relleno, e informa de permeabilidad tubárica bilateral.
Tras valorar el caso, revisar la literatura y con la conformidad de la paciente, se informa de un riesgo de rotura uterina no incrementado, por lo que se decide realizar una inseminación artificial, con dosis bajas de gonadotrofinas, e intentando un desarrollo monofolicular para evitar una gestación múltiple. Se consigue gestación al segundo ciclo de inseminación.
Durante la gestación se realizan ecografías de control para valorar el grosor del segmento uterino inferior y ver la evolución con respecto a los datos pregestacionales.
En la ecografía del primer trimestre, 10+6 semanas teóricas, se observa una gestación única con morfología fetal normal. A nivel de cara anterior de útero, área ístmica de histerorrafia anterior, se observan varias áreas líquidas anecogénicas de 6mm intercaladas con estroma cervical. No se evidencia «sensación» de discontinuidad ni dehiscencia de cicatriz, por lo que se continúan los controles. En la ecografía del segundo trimestre, a las 20 semanas de gestación: feto de morfología normal, desaparecen las áreas líquidas vistas previamente, el segmento inferior uterino tiene aspecto normal, misma imagen que se observará en la ecografía de la semana 34, cuando la histerotomía tiene un aspecto normal.
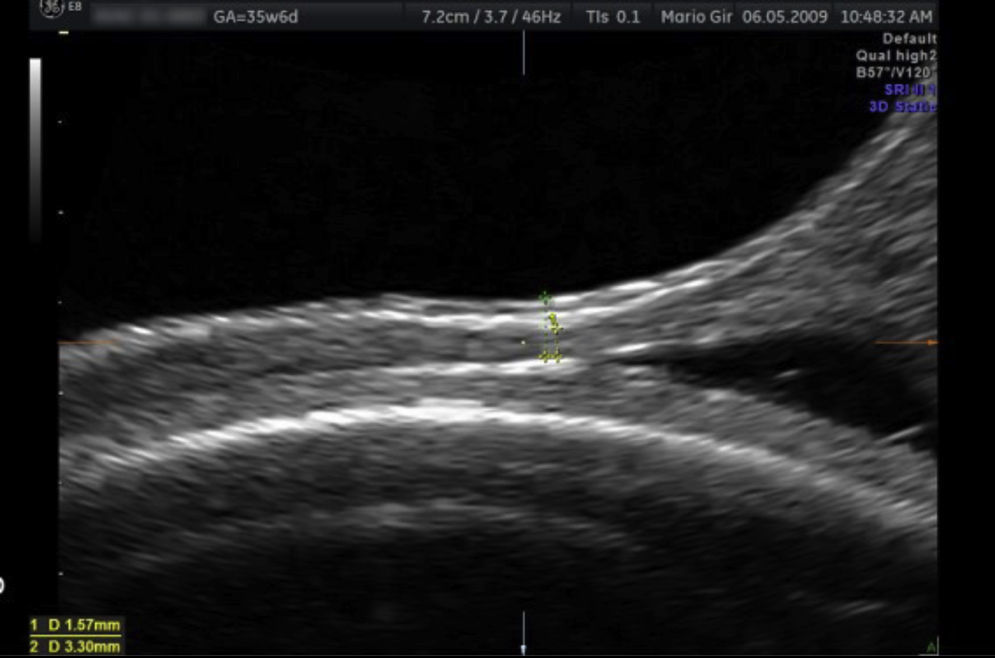
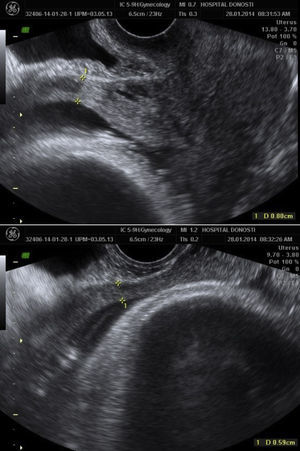
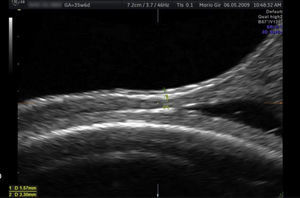
En la semana 38 se comenta el caso en Comité de Perinatología para valorar la vía de parto. En la ecografía en dicha semana de gestación el grosor del segmento por vía vaginal es de 5,5mm (fig. 2), por lo que se decide parto por vía vaginal, con control de presión intrauterina, como en todos los partos con cesárea anterior según protocolo del servicio.
La paciente acude en la semana 40+2 en periodo activo de parto. Se produce el parto vía vaginal de forma eutócica, sin incidencias.
Comentario, discusión y revisión de la literaturaLa cesárea es la intervención quirúrgica más común dentro de la obstetricia. Su incidencia está aumentando, con tasas de hasta un 17-25% según diferentes países. Entre 1990 y 2008 en Reino Unido aumentó la tasa de cesáreas de un 12 a un 29% y en Estados Unidos de un 21,2% a un 30,1%.
El riesgo de rotura uterina, después de una cesárea con un parto vaginal previo, es menor del 1% y el riesgo de rotura sin un parto vaginal previo es mayor: del 1-5%. La tasa de rotura espontánea en países desarrollados es del 0,02-0,08%. En el caso de gestantes sin antecedentes previos de intervención quirúrgica sobre la pared uterina, es de un caso/5.700-20.000 (0,013%).
El 75% de las gestantes que intentan un parto vaginal tras cesárea anterior obtienen resultados favorables. Este porcentaje depende en gran medida de la causa de la cesárea anterior. La tasa de éxito es mayor en el caso de parto vaginal previo a la cesárea, de presentación cefálica y de comienzo espontáneo del parto. En cambio, la tasa de éxito desciende si la cesárea anterior se indicó por fallo de progresión, si no hay antecedente de parto vaginal previo o si se ha realizado inducción del parto en la gestación actual.
La rotura uterina se define como la solución de continuidad no quirúrgica en el útero gravídico. Se excluyen de esta definición las perforaciones uterinas producidas en el curso de un legrado o una histeroscopia. Es una complicación muy grave por la elevada morbimortalidad tanto materna como fetal. Se clasifica según las causas, localización, grado y el momento en el que se produzca y los factores de riesgo a tener en cuenta (tabla 1).
Factores de riesgo para la rotura uterina
| Cirugías que afectan al miometrio |
| - CST anterior |
| - Rotura uterina reparada previamente |
| - Miomectomía |
| Traumatismo uterino |
| - Aborto con legrado posterior (perforación) |
| - Trauma punzante romo |
| Anomalía congénita |
| - Embarazo en cuerno uterino poco desarrollado |
| Antes del parto |
| - DU espontánea persistente e intensa |
| - Estimulación: PG u oxitocina |
| - Perforación por catéter interno de DU |
| - Versión cefálica externa |
| - Hidramnios, embarazo múltiple |
| - Macrosomía fetal |
| - Multiparidad |
| Durante el parto |
| - Pelvis estrecha |
| - Parto instrumentado dificultoso |
| - Situación transversa |
| - Anomalía fetal |
| - Extracción manual de placenta |
| - Maniobra de Kristeller |
| Adquirida |
| - Placenta íncreta o pércreta |
CST: cesárea; DU: dinámica uterina; PG: prostaglandinas.
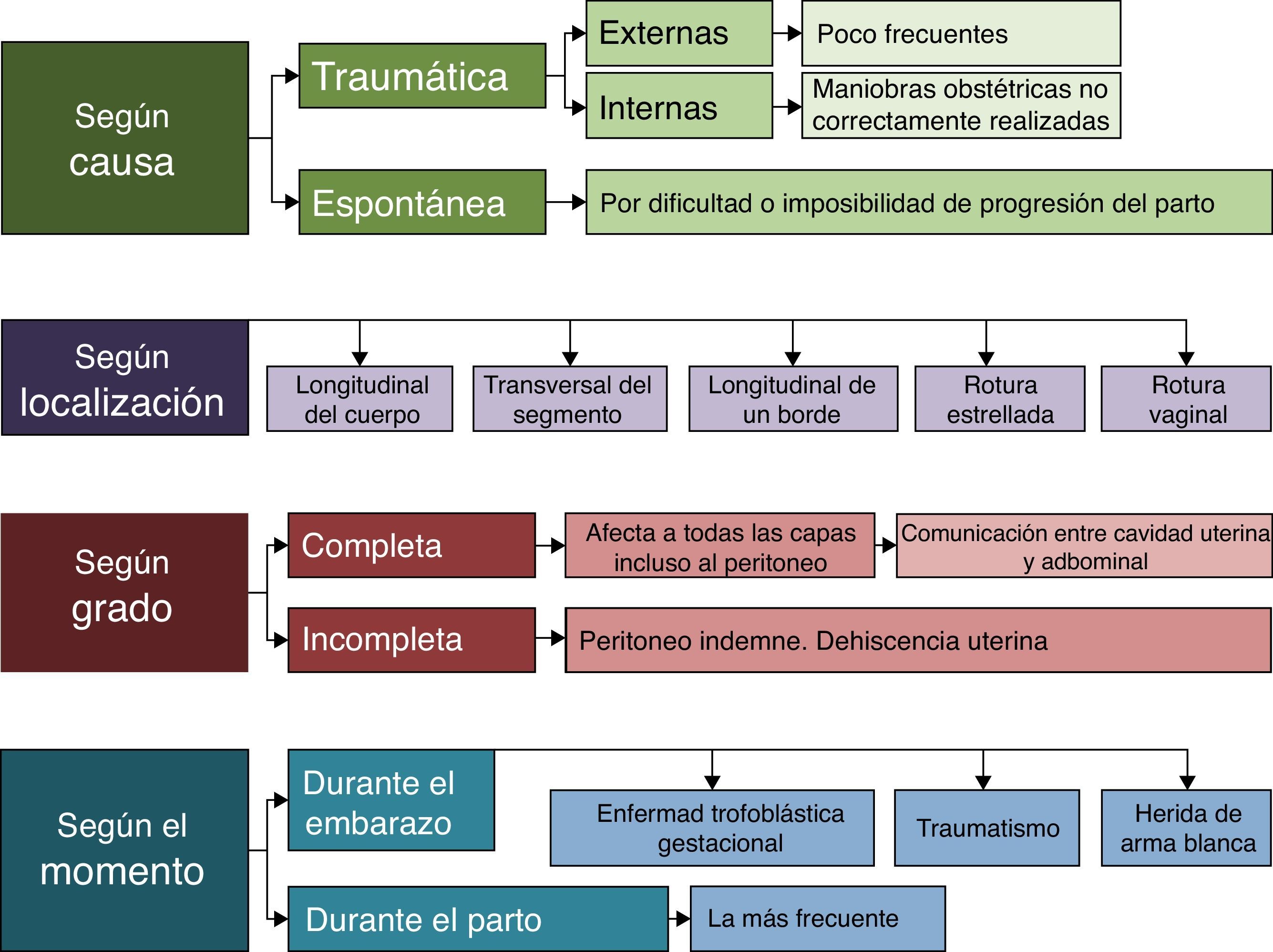
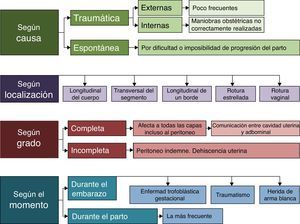
La causa más frecuente de rotura uterina se produce intraparto, secundaria a la apertura de una cicatriz previa por una cesárea anterior. En la figura 3 se expone la clasificación de la rotura uterina según su causa, localización, grado y momento de la lesión ya que cada una de ellas se puede clasificar con una nomenclatura específica.
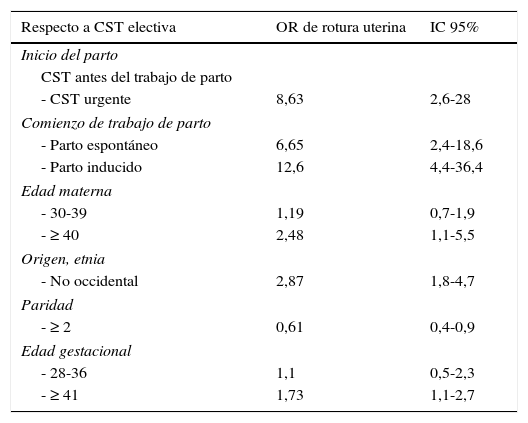
Según el estudio de Valentin14, los siguientes factores parecen aumentar el riesgo de rotura uterina: intergenésico corto, peso fetal > 4.000 g, inducción del parto, altas dosis de oxitocina y cierre en una capa de la histerotomía (tabla 2).En cambio, el antecedente de parto vaginal previo reduce el riesgo de rotura uterina. Aun así, sabemos que únicamente con la presencia de factores de riesgo no se puede predecir el riesgo de rotura uterina.
Intento de parto vaginal en mujeres con cesárea anterior vs. cesárea electiva
| Respecto a CST electiva | OR de rotura uterina | IC 95% |
|---|---|---|
| Inicio del parto | ||
| CST antes del trabajo de parto | ||
| - CST urgente | 8,63 | 2,6-28 |
| Comienzo de trabajo de parto | ||
| - Parto espontáneo | 6,65 | 2,4-18,6 |
| - Parto inducido | 12,6 | 4,4-36,4 |
| Edad materna | ||
| - 30-39 | 1,19 | 0,7-1,9 |
| - ≥ 40 | 2,48 | 1,1-5,5 |
| Origen, etnia | ||
| - No occidental | 2,87 | 1,8-4,7 |
| Paridad | ||
| - ≥ 2 | 0,61 | 0,4-0,9 |
| Edad gestacional | ||
| - 28-36 | 1,1 | 0,5-2,3 |
| - ≥ 41 | 1,73 | 1,1-2,7 |
Según los diversos estudios realizados, se considera que el número necesario a tratar de cesáreas electivas para evitar una rotura uterina es de 370 con un IC del 95%, entre 213 y 1.370. Aun así, la cesárea electiva no garantiza que no vaya a suceder una rotura uterina.
Respecto a las manifestaciones clínicas que se presentan como consecuencia de la rotura uterina destacan las anomalías de la frecuencia cardíaca fetal. Se consideran el signo más frecuente de rotura uterina, que se presenta en el 55-87% de los casos.
Si la causa más frecuente de rotura uterina es la cicatriz uterina, debemos definir qué es una rotura de la cicatriz, y diferenciarla de una dehiscencia o gran defecto, o de un defecto menor y utilizar estos términos con precisión.
Entre las definiciones más consensuadas figuran las siguientes:
- -
Cicatriz de histerotomía: línea hipoecoica o hiperecoica en segmento uterino inferior que observamos en las ecografías.
- -
Defecto de cicatriz uterina: lesión convexa o identación en el segmento inferior o zona de histerotomía que se observa con diferentes métodos de imagen. En algunos casos puede ser un defecto mayor y hacer sospechar una dehiscencia de la cicatriz, es decir, un afinamiento del miometrio en la zona del segmento uterino inferior en mujer con cesárea anterior.
- -
Rotura uterina completa: solución de continuidad que incluye el peritoneo visceral, miometrio y membranas ovulares que conlleva la comunicación entre la cavidad uterina y la abdominal. Consiste en el desgarro hemorrágico de la pared uterina, de bordes anfractuosos y de dirección variable. Se acompaña con frecuencia de hemorragia materna y de graves complicaciones maternas y fetales.
- -
Rotura incompleta: rotura segmentaria que conserva el peritoneo visceral. Las membranas ovulares pueden estar íntegras o rotas. No suele asociarse a hemorragia materna ni a complicaciones neonatales, ya que el feto permanece en la cavidad uterina.
- -
Dehiscencia uterina: disrupción asintomática de la incisión uterina previa, descubierta en el momento de la laparotomía o por examen digital después del parto vaginal, visualizándose la membrana coriónica a través del peritoneo, pero que podemos sospechar previamente por métodos de imagen (defecto mayor).
Teniendo en cuenta que el factor más importante para una rotura uterina es una cesárea anterior, la pregunta clave es si podemos valorar un defecto de cicatriz de la cesárea y, con ello, tomar una actitud obstétrica adecuada, cómo se valora un defecto en la cicatriz de una cesárea y si existe una medida identificable que nos permite prever un resultado obstétrico favorable.
Los estudios son múltiples, han utilizado hasta hoy diferentes definiciones y no está estandarizado cómo se debe diagnosticar, qué es un gran defecto, qué debemos hacer y cuál es su significado. Sin embargo, intentaremos unificar estos conceptos a continuación.
Los defectos de la cicatriz de una cesárea pueden ser diagnosticados por diferentes métodos: por ecografía, histerosonografía, RMN e histerografía. Los defectos de cicatriz de una cesárea están descritos hasta en un 56% de los casos.
Mediante técnicas de imagen se han observado defectos de la cicatriz uterina sospechosas por histerografía, sonohisterografía y ecografía transvaginal en 58% (33-70), 59% (58-85) y 37% (20-65), respectivamente, con diferentes criterios para definir un defecto o dehiscencia de cicatriz, lo que no permite sacar conclusiones6. Además, no realizamos pruebas de imagen tras una cesárea, por lo que muchos defectos no son diagnosticados. A esto se une que las dehiscencias muchas veces cursan de manera asintomática. Si tuviéramos que sospechar un defecto de cicatriz de una cesárea, deberíamos pensar en ello cuando la mujer nos consulte tras una cesárea y asocie un sangrado intermenstrual (en el 63,8% de los casos, es el síntoma más frecuente), una dismenorrea de nueva aparición (en el 53,1%), dolor pélvico crónico (en el 39,6%), dispareunia (18,13%) o infertilidad.
La revisión realizada por Roberge et al.1 en 2012 analiza 21 estudios, de los cuales calculan que la proporción de sospecha de defectos en la cicatriz, con histerografía, sonohisterografía y ecografía, es del 58, 59 y 37%. Hay que señalar que las definiciones de defecto son variables entre estudios, pero se obtienen estas conclusiones:
- •
Si comparamos histerosonografía y ecografía, la sonohisterografia puede detectar mayor número de defectos17.
- •
Un gran defecto en la cicatriz puede estar asociado a un mayor riesgo de rotura en un siguiente embarazo.
- •
Dos estudios continuaron controlando a estas mujeres en un siguiente embarazo y encontraron que una dehiscencia grande y un gran defecto están asociados a un mayor riesgo de rotura uterina; son los estudios de Vikhareva y Osser con 162 mujeres15 y el estudio de Waniorek con 25 mujeres16.
- •
De los factores evaluados, solo el número de cesáreas aumentaba el riesgo de rotura, el resto de factores como tipo de sutura, tiempo entre cesáreas, inducción del parto, no alcanzaron significación estadística, posiblemente por la heterogeneidad entre los estudios.
- •
El control de la cicatriz uterina durante el tercer trimestre en mujeres con una cesárea previa puede ayudar a prevenir una rotura uterina y decidir la vía de parto, y lo demuestran 2 estudios realizados por Osser et al.3 y de Vaate et al.8.
En las últimas publicaciones, la ecografía se considera como una técnica fácil, reproducible y con una metodología ya definida a la hora de valorar una cicatriz anterior. Aun así, no disponemos de una técnica estandarizada, aunque comienzan a aparecer publicaciones que intentan homogenizar las mediciones para que los estudios sean comparables.
En la revisión realizada por Naji et al.9 se intenta estandarizar la medición de la cicatriz uterina mediante la ecografía en 3 dimensiones para que los próximos estudios realizados sean homogéneos. La evaluación se realiza en el primer trimestre o en una revisión ginecológica en la que se medirán las dimensiones del defecto de la cicatriz en anchura, largura y profundidad y el tamaño del miometrio restante tanto en el plano transversal como en el longitudinal (fig. 4). De este modo podríamos clasificar los defectos en leves, moderados y severos.
Se considera gran defecto si la medición del tejido miometrial situado por encima del defecto es<2,2mm por ecografía, < 2,5mm por histerosonografía o cuando el defecto no ocupa más de 2/3 del espesor del miometrio.
Además, en el estudio de Bujold et al.10, los autores concluyen que cuando el segmento uterino inferior es < 2,5mm, la tasa de rotura uterina es mayor al 10% con una especificidad del 90%. Aun así, concluyen que no se han desarrollado ni concluido puntos de corte, por lo que se necesitan técnicas de medición más estandarizadas.
Los diferentes puntos de corte para un defecto mayor según diferentes autores los exponemos en la tabla 3.
Puntos de corte para la dehiscencia uterina según diferentes autores
| Rozenberg et al. (vía abdominal)11 | Gran defecto <3,5mm, límite con alta valor predictivo negativo. Sensibilidad del 88% y especifidad del 73,2% |
| Bujold et al. (vía abdominal)10 | Punto de corte 2,3mm, riesgo de rotura uterina 9,1% |
| Jastrow et al.4 | Punto de corte varía de 3,5 a 2mm cuando se mide el grosor completo del segmento uterino inferior y de 1,4 a 2mm cuando se valora solo el miometrio |
| Brahmalakshmy14 | Un espesor de más de 3,2mm, dentro de una semana antes del parto, se considera seguro, definiendo que la mayoría de las mujeres con un valor superior a este tenían un segmento uterino inferior dentro de la normalidad. Sensibilidad del 92,3% y especifidad del 81,1% |
Quedaría entonces por confirmar si el control ecográfico de la cicatriz uterina durante el tercer trimestre en mujeres con una cesárea previa puede ayudar a prevenir una rotura uterina y a decidir la vía de parto. Hasta ahora, hay 2 estudios que lo demuestran, Osser et al.3 y Vaate et al.8, así como una revisión bibliográfica publicada por Jastrow et al.4 en la que concluyen que el estudio sonográfico del segmento uterino es un buen predictor de defectos en la cicatriz uterina en mujeres con cesárea anterior.
Algunas sociedades también se han pronunciado sobre la importancia de la medición del defecto de la cicatriz uterina.
- -
Según el protocolo de la rotura uterina de la SEGO publicado en 201313: la medición por ECO del segmento uterino inferior al final del embarazo está lejos de ser una herramienta con capacidad predictiva o protectora de rotura uterina.
- -
La sociedad francesa de ginecología y obstetricia18, en el 201319, concluía que todavía la medición del segmento inferior no se puede utilizar como factor para decidir la vía de parto en un siguiente embarazo.
- -
La frase correcta es la siguiente: La sociedad americana de ginecología y obstetricia19 en su última publicación en el 2010, publica los riesgo de cesárea anterior y factores de riesgo para la rotura uterina, sin mencionar conclusiones sobre la medición del segmento inferior
- -
La sociedad canadiense de obstetricia en su guía publicada en el 2005 no hace mención a la medición del segmento inferior como factor a la hora de decidir la vía de parto, pero sí que en el 201020, publicó un artículo de opinión en el que venía a concluir que todavía se necesitan más estudios para su validación.
- -
La RCOG está pendiente de publicar en el 2015 su guía práctica del parto vaginal tras cesárea anterior. En su última publicación del 2007, no hacía mención a este factor.
Por lo tanto, la mayoría de los autores y algunas sociedades12 están de acuerdo en que faltan estudios homogéneos y un punto de corte definitivo. Sin embargo, sí podemos concluir que se ha visto que la asociación es más fuerte entre la estrechez total del segmento uterino inferior y el defecto de la cicatriz que con la capa miometrial únicamente y, por otro lado, las imágenes ecográficas en las no gestantes no son buenas predictoras de riesgo de rotura uterina: en caso de su valoración, debería realizarse en el tercer trimestre y por vía vaginal15.
Otra pregunta que planteamos es si un defecto de cicatriz según los criterios establecidos previamente debería ser corregido.
Según estudios realizados con RMN, el miometrio necesita al menos 3 meses para su correcta involución y formación; la correcta curación no se consigue antes de los 6 meses.
Únicamente hay 2 estudios que realizan una reparación de la cicatriz de la cesárea previamente a un nuevo embarazo por laparoscopia7. Donnez3 en 3 casos, miometrio residual de 1mm en 2 casos y de 2mm en 2 casos. La reparación de los casos descritos en la literatura se realizó por laparoscopia. Defiende la laparoscopia respecto a otras técnicas quirúrgicas ya que permite mayor seguridad y menor riesgo de lesiones a nivel vesical. Por otra parte, tras la práctica de la laparoscopia se ha objetivado en todos los casos la recuperación total de la lesión: proponen que, en caso de miometrio residual menor de 2,5mm o cuando el defecto del segmento uterino inferior es igual o superior al 80%, la reparación laparoscópica se puede realizar con resultados anatómicos favorables. Klemm5 describe 5 casos, 4 de ellos sintomáticos con dolor y sangrado intermenstrual, y con un miometrio residual <2mm en todos los casos. Según este estudio, en los pacientes con antecedente de cesárea anterior se debería realizar ecografía transvaginal de la cicatriz uterina para detectar dehiscencias de la cicatriz latentes asociadas a adelgazamiento de la pared uterina para planificar gestaciones futuras. En los casos sospechosos se podría realizar una técnica combinada vaginal asociada a laparoscopia o únicamente vaginal para reparar el defecto.
A pesar de los estudios publicados, no hay datos que señalen que la dehiscencia de la cicatriz uterina requiera reparación para su adecuada cicatrización. Pero ante la dehiscencia de toda la histerorrafia y una mujer con deseo gestacional, se debe realizar la reparación inmediata de la lesión.
Conclusiones y resumen- •
Para detectar un defecto en la cicatriz o dehiscencia en la cicatriz el mejor método diagnóstico es la histerosonografía.
- •
La medición se puede realizar previamente al embarazo o durante el embarazo, y en el tercer trimestre podría ser útil para decidir la vía de parto, pero no se ha conseguido un acuerdo a la hora de la medición de la cicatriz de una histerotomía en mujeres no gestantes, ni en la medición del segmento uterino inferior en gestantes.
- •
No se puede determinar un punto de corte para predecir el riesgo de rotura uterina o dehiscencia de cicatriz uterina. Aun así, existe una correlación entre el tamaño del defecto del segmento uterino inferior y el riesgo de rotura uterina. Por tanto, se requieren más estudios para establecer una técnica adecuada y un punto de corte mediante el cual se pueda clasificar a las pacientes y tomar decisiones respecto a la vía de parto.
- •
El punto de corte más definido en los estudios para el segmento uterino inferior es 3.5-3.2.
- •
El factor más importante de las pruebas de imagen es valorar si son capaces o no de predecir las complicaciones obstétricas que pueden suceder, el riesgo de afectación materna o fetal y la opción de la vía vaginal. Faltan estudios para tomar decisiones clínicas conforme a estos resultados.
- •
Se deben tener en cuenta otros datos, tales como: intervalo entre embarazos, número de cesáreas, tipo de suturas… Los siguientes factores parecen aumentar el riesgo de rotura uterina: tiempo intergenésico corto, peso fetal>4.000 g, inducción del parto, altas dosis de oxitocina y cierre en una capa de la histerotomía. En cambio, el antecedente de parto vaginal previo reduce el riesgo de rotura uterina.
- •
La aplicación clínica: actualmente podemos valorar mediante ultrasonografía las características del defecto uterino, pero no su asociación con el embarazo ectópico, placentación patológica ni riesgo de rotura uterina. Es importante continuar haciendo estudios y analizar la relación, para que podamos interpretar las imágenes y tomar decisiones respecto al manejo en estas pacientes. Uno de los mayores avances será cuando determinemos la posibilidad de parto vaginal o de realizar cesárea electiva según los hallazgos.
- •
La dehiscencia o rotura uterina no contraindican un embarazo posterior.
- •
En el caso de la dehiscencia asintomática se puede realizar la prueba de parto en el siguiente embarazo.
- •
En caso de rotura uterina, se recomienda que el futuro parto sea mediante cesárea.
Los autores declaran no tener ningún conflicto de intereses.