El desarrollo de enfermedad cardiovascular suele presentarse en sujetos con varios factores de riesgo cardiovascular. Sin embargo, existen otros condicionantes que pueden estar relacionados con la aparición de enfermedad cardiovascular, como pueden ser los fármacos antineoplásicos. Presentamos el caso de un varón de 63 años con muy alto riesgo cardiovascular, con antecedente personal de leucemia mieloide crónica en tratamiento con nilotinib que, a pesar de buen control metabólico, desarrolló una enfermedad arterial periférica grave y acelerada. La enfermedad arterial periférica se ha descrito en el 5-20% de los pacientes bajo tratamiento con nilotinib, siendo más frecuente en los sujetos con varios factores de riesgo cardiovascular.
The development of cardiovascular disease appears in subjects with several cardiovascular risk factors. However, other agents could be related to the appearance of cardiovascular disease, like chemotherapy drugs. We present a 63 years-old man with very high cardiovascular risk and chronic myeloid leukemia under treatment with nilotinib. Despite a good control of cardiovascular risk factors, he development a severe and accelerated peripheral arterial disease. Peripheral arterial disease occurs in 5-20% patients under treatment with nilotinib and it is more frequently in subjects with several cardiovascular risk factors.
El desarrollo de enfermedad coronaria, ictus isquémico y enfermedad arterial periférica (EAP) suele estar relacionado con la presencia de varios factores de riesgo cardiovascular (FRCV). Sin embargo, también existen otros elementos que pueden ser causa de enfermedad cardiovascular (ECV). Entre otros, algunos de los fármacos que se utilizan en el tratamiento de las enfermedades neoplásicas aumentan la incidencia de FRCV y de ECV, por lo que también deben ser tenidos en cuenta como posibles agentes etiopatogénicos.
Caso clínicoPresentamos el caso de un varón con antecedentes de hipertensión arterial, diabetes mellitus tipo 2 e hipercolesterolemia. Nunca fumador. En tratamiento con metformina, candesartán y atorvastatina, con lo que estaba en valores objetivos para sus FRCV. En julio de 2011, a los 63 años, se le diagnosticó leucemia mieloide crónica (LMC), iniciando tratamiento con nilotinib 300mg cada 12h, consiguiendo respuesta molecular y remisión citogenética completa.
En marzo de 2013 ingresó por síndrome coronario agudo sin elevación del segmento ST (SCASEST), realizándose una coronariografía que demostró estenosis severa de la descendente anterior y de la coronaria derecha. Precisó colocación de 2 stents farmacoactivos en la descendente anterior y uno en la coronaria derecha.
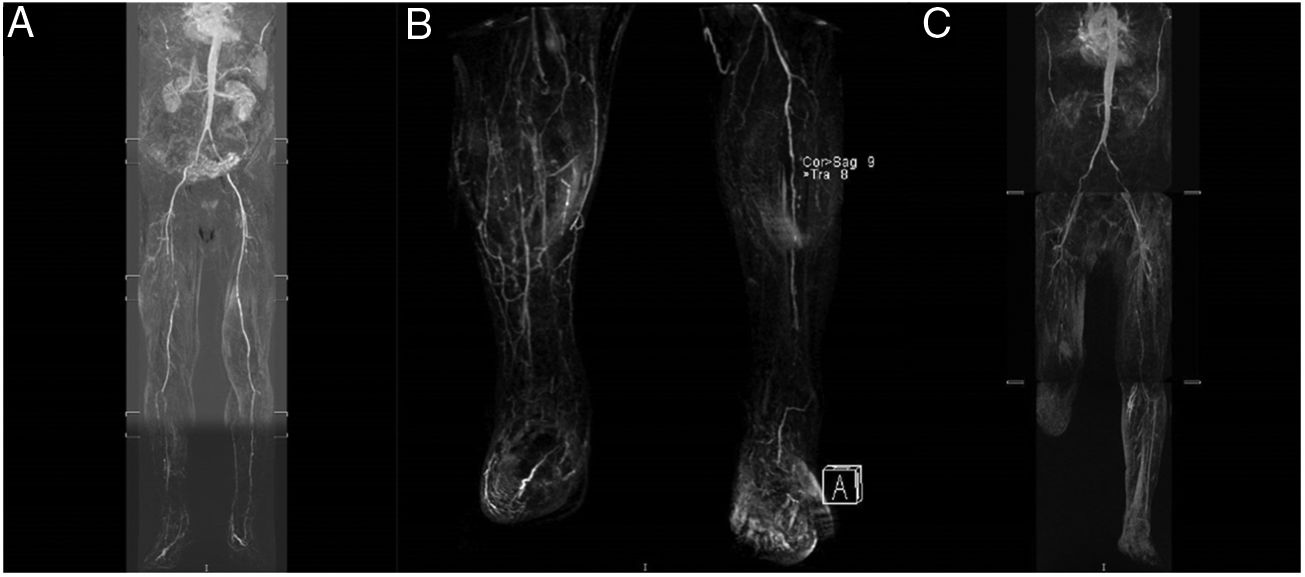
Durante el siguiente año, y a pesar del buen control de los FRCV (HbA1c <6,5mg/dL, cLDL<70mg/dL y presión arterial <140/90mmHg) y del doble tratamiento antiagregante, el paciente desarrolló clínica de claudicación intermitente del miembro inferior derecho (MID) con evolución acelerada, dolor en reposo y lesiones cutáneas de origen vascular incipientes. Se realizó angiorresonancia magnética (fig. 1A), donde se objetivó importante afectación arterial del MID sin afectación vascular del miembro inferior izquierdo (MII). En enero de 2015 se realizó angioplastia de arteria femoral superficial derecha y peronea, así como parche de safena en arteria femoral común.
(A) Agosto 2014: Afectación significativa del territorio femoral superficial y tibioperoneo del MID. (B) Noviembre 2015: MID con arteria poplítea permeable con oclusión completa de tronco tibioperoneo y arteria tibial anterior; MII con oclusión de arteria femoral superficial en su parte proximal y media con reinyección distal. Arteria poplítea permeable en toda su extensión. Oclusión proximal de arteria tibial anterior y posterior. Oclusión de peronea en el tercio proximal y permeabilidad de tibial posterior. (C) Febrero 2016: MII con severas lesiones ateromatosas que producen estenosis críticas en origen de ilíaca tanto común como externa derecha. Oclusión completa de femoral superficial en el tercio medio del muslo.MID: miembro inferior derecho; MII: miembro inferior izquierdo.
En los siguientes meses volvió a ingresar en varias ocasiones en Cirugía Vascular por nueva clínica de isquemia en reposo, tanto del MID como del MII. En marzo de 2015 precisó de forma consecutiva revascularización del MII mediante stent autoexpandible a nivel de arteria ilíaca común y arteria ilíaca externa y arteria femoral superficial del MII y reintervención a nivel del MID por nueva oclusión de la arteria femoral superficial y de la arteria tibial posterior. En septiembre de 2015 desarrolló un nuevo episodio de isquemia en el MID que requirió amputación de los dedos 1.o y 2.o del pie. En noviembre de 2015, por persistencia de la clínica de isquemia y dolor en reposo, con angiorresonancia magnética con oclusión completa de tronco tibioperoneo y arteria tibial anterior (fig. 1B), requirió amputación infracondílea del MID. En febrero de 2016 presentó una nueva revascularización del MII por lesiones oclusivas (fig. 1C). Finalmente, en abril de 2016 reingresó por lesión isquémica del 1.er dedo, con evolución tórpida en planta, obligando finalmente a realizar la amputación infracondílea del MII.
DiscusiónLa arteriosclerosis es una enfermedad sistémica que afecta a las arterias de mediano y gran calibre. Sus manifestaciones pueden afectar a todo el sistema circulatorio, produciendo cardiopatía isquémica, ictus o EAP según la región vascular que se vea afectada.
Los principales factores de riesgo para el desarrollo de EAP son los mismos que para el desarrollo de arteriosclerosis: edad, sexo masculino, hipercolesterolemia, diabetes y tabaquismo. También pueden tener un papel importante en el desarrollo de esta enfermedad los antecedentes familiares de ECV, enfermedad renal crónica, estados inflamatorios crónicos, hiperhomocisteinemia, etc.1. Además, no hay que olvidar el papel fundamental de los efectos adversos de los medicamentos.
Los inhibidores de la tirosina cinasa (ITK) son el tratamiento de la LMC. Inhiben de forma potente la actividad de la proteína tirosina cinasa BCR-ABL causante de esta enfermedad. Tras la introducción de esta terapia en 2001, el pronóstico de la patología cambió radicalmente, pasando de una supervivencia media del 10% a los 10 años en la era previa a los ITK, a una supervivencia similar a la de la población general a día de hoy. Sin embargo, el incremento en la supervivencia de los pacientes con LMC ha llevado consigo un aumento en la incidencia de ECV. Se ha observado que esta incidencia es mayor en los pacientes con LMC bajo tratamiento con ITK que en población con LMC sin tratamiento o en población general2.
Nilotinib es un ITK de segunda generación que induce remisión citogenética completa en una alta proporción de pacientes con resistencia a imatinib. Sin embargo, se ha observado que ejerce efectos proaterogénicos y antiangiogénicos directos sobre las células endoteliales vasculares, que pueden contribuir al desarrollo de EAP hasta en un 5-20% de los pacientes tratados3,4. Este efecto se produce por una regulación al alza sobre proteínas de adhesión proaterogénicas (ICAM-1, E-selectina, VCAM-1), así como suprimiendo la angiogénesis y proliferación de células endoteliales, mediando sobre los receptores de angiopoyetina 1, TEK, ABL-2, JAK-1 y MAP cinasas. Además, se ha observado que puede aumentar los niveles de glucosa y colesterol LDL. La probabilidad de presentar ECV aumenta con el incremento de dosis de nilotinib5.
Como podemos ver en la tabla 1, nilotinib no es el único fármaco que produce efectos secundarios a nivel cardiovascular, estando mediados por distintos biomarcadores6. Se ha observado que la incidencia de eventos cardiovasculares en los pacientes con LMC en tratamiento con ITK es mayor en pacientes con varios FRCV previos7.
Efectos cardiovasculares más frecuentes de los ITK
| Efectos cardiovasculares más frecuentes de los ITK | ||
|---|---|---|
| ITK | Efectos secundarios cardiovasculares | Mecanismo de acción de la ECV |
| Imatinib | No efectos deletéreos a nivel cardiovascular | |
| Nilotinib | Enfermedad arterial periférica | Aterosclerosis acelerada (aumento de proteínas de adhesión proaterogénicas [ICAM-1, E-selectina, VCAM-1]), supresión de angiogénesis y proliferación de células endoteliales (mediado por receptores de angiopoyetina 1, TEK, ABL-2, JAK-1 y MAP cinasas) |
| Aumento de niveles de glucosa y colesterol LDL | ||
| Prolongación del intervalo QT | ||
| Dasatinib | Derrame pleural y pericárdico | Inhibición PDGFRβ |
| Hipertensión pulmonar | Posible alteración de la permeabilidad vascular pulmonar mediada por cinasas Src | |
| Bosutinib | No efectos deletéreos a nivel cardiovascular | |
| Ponatinib | Hipertensión | Angiopatía protrombótica y adhesión plaquetaria mediada por FVW |
| Enfermedad arterial periférica | ||
| Enfermedad coronaria isquémica | ||
| Ictus isquémico | ||
ABL-2: ABL proto-oncogén 2; ECV: enfermedad cardiovascular; FVW: factor Von Willebrand; ICAM: molécula de adhesión intercelular; ITK: inhibidor de la tirosina cinasa; JAK-1: Janus cinasa-1; MAP cinasas: proteín-cinasas activadas por mitógenos; PDGFRβ: receptor beta del factor de crecimiento derivado de plaquetas; TEK: TEK tirosin kinasa receptor; VCAM-1: molécula de citoadhesión vascular-1.
En nuestro caso, aunque se trataba de un paciente con alto riesgo cardiovascular en el momento del IAMSEST, se puede observar que a pesar de un buen control de los FRCV siguió desarrollando ECV, siendo esta grave y de rápida evolución. Solamente se suspendió el ITK tras reconocerlo como posible factor etiopatogénico de la enfermedad. Creemos que el ITK contribuyó al desarrollo de la EAP del paciente, dado que sus FRCV estaban controlados (aunque es cierto que no implica por ello la aparición de nuevos eventos) y los episodios de isquemia no volvieron a aparecer tras su retirada (periodo libre de enfermedad de 30 meses). Es imposible establecer la relación causal, ya que no sería ética la reintroducción del fármaco.
El reconocimiento de los ITK como factor de riesgo para la ECV es tardío con respecto al inicio del tratamiento de la LMC en 2001. Solo a partir del trabajo de Aichberger et al.8 en 2011, donde se objetivó la aparición de 3 individuos con EAP rápidamente progresiva sobre una serie de 24 pacientes, empezaron a señalarse los ITK como causantes de ECV. Posteriormente, numerosos artículos han confirmado la relación entre nilotinib (así como otros ITK) y la aparición precoz de ECV.
Actualmente se ha observado que la única herramienta para la predicción de eventos cardiovasculares en los pacientes con LMC y tratamiento con ITK es el cálculo de riesgo cardiovascular9. La complejidad de estos pacientes, caracterizada por el aumento de supervivencia, aumento de incidencia de ECV y fármacos con efectos secundarios cardiovasculares, hace necesaria la valoración por parte de equipos multidisciplinares compuestos por cardiólogos, internistas y hematólogos.
FinanciaciónLos autores declaran no haber recibido financiación para este artículo.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.