Valorar la utilidad de copeptina (fragmento estable del precursor de vasopresina-arginina) en el diagnóstico diferencial del dolor torácico agudo de posible origen coronario.
Material y métodosSe han incluido en el estudio 82 pacientes que fueron evaluados inicialmente de acuerdo con el protocolo de pacientes con sospecha de síndrome coronario agudo (SCA) de nuestro Servicio de Urgencias, incluyendo la determinación de troponina y copeptina con seriación en admisión y a las 6 h.
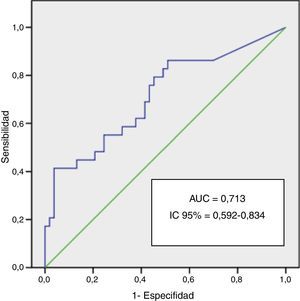
ResultadosObtuvimos diferencias estadísticamente significativas en la concentración de copeptina a tiempo 0 entre los pacientes diagnosticados de SCASEST: 42,1±38,7pmol/L y los pacientes no SCASEST: 15,6±21,2pmol/L (p<0,01). Sin embargo, las diferencias no alcanzaron a ser estadísticamente significativas a las 6 h (p=0,093). El análisis del área bajo la curva ROC para la copeptina en los pacientes SCASEST a tiempo 0 fue de 0,713 con un intervalo de confianza del 95% de 0,592 a 0,834 y un grado de significación de p=0,001.
ConclusionesLa concentración de copeptina representa un valor adicional en la diferenciación entre pacientes SCASEST y pacientes no SCASEST, así como entre pacientes SCA y pacientes con angina estable.
El punto de corte de 10pmol/L proporciona los mejores valores de sensibilidad, valor predictivo negativo (VPN), cociente de probabilidad positivo (CPP) y cociente de probabilidad negativo (CPN) en el diagnóstico de pacientes SCASEST.
This study was conducted in order to evaluate the usefulness of copeptin (a stable fragment of the precursor of arginine vasopressin) in the differential diagnosis of acute chest pain of probable coronary origin.
Material and methodsThe study includes 82 patients who were initially evaluated according to the protocol of a patient with suspected acute coronary syndrome (ACS) in our Emergency Department, including the determination of troponin and copeptin with specimens taken on admission (time 0) and at 6h.
ResultsStatistically significant differences were observed in copeptin concentrations at time 0 among patients diagnosed with non–ST-segment elevation (NTEACS): 42.1±38.7pmol/L and non-NSTEACS patients: 15.6±21.2pmol/L (P<. 01). However, the differences did not reach statistical significance at 6h (P=.093).
The analysis of the area under the ROC curve for Copeptin in NSTEACS patients at time 0 was 0.713, with a confidence interval of 95% from 0.592 to 0.834 and a significance level of P=.001.
ConclusionsThe concentration of copeptin represents an additional value in the differentiation between NSTEACS patients and non-NSTEACS patients, as well as between ACS patients and patients with stable angina. The cut-off point of 10pmol/L provides the best values for sensitivity, negative predictive value (NPV), positive likelihood ratio (LR+), and negative likelihood ratio (LR–) in the diagnosis of NSTEACS patients.
El dolor torácico agudo de posible origen coronario constituye una de las causas más frecuentes de consulta en los servicios de urgencias. Puede representar hasta el 55% de las causas por las que el paciente acude a Urgencias. Esto contrasta con el 11-13% de los pacientes a los que se diagnostica finalmente síndrome coronario agudo (SCA)1,2.
En la actualidad la troponina es el biomarcador de elección para el diagnóstico y estratificación de riesgo en el SCA. Sin embargo, este marcador presenta como principal limitación, con los métodos disponibles en la actualidad, su falta de sensibilidad en las primeras horas del evento.
Esto hace que, en aquellos pacientes con dolor torácico sugestivo de SCA, con inicio del dolor inferior a 12 h y electrocardiograma no diagnóstico, un primer resultado negativo de troponina no excluya el diagnóstico de SCA y obligue a realizar una segunda determinación del marcador transcurridas al menos 3-6 h.
El objetivo de esta segunda determinación es excluir de manera definitiva la presencia de infarto agudo de miocardio (IAM) sin elevación del segmento ST y contribuye a un mayor consumo de recursos sanitarios y a la prolongación de la estancia hospitalaria, pudiendo ser causa incluso de retrasos en la realización de procesos invasivos que mejoren el pronóstico del paciente3.
Por este motivo recientemente se han intentado desarrollar otros biomarcadores en el diagnóstico diferencial del dolor torácico agudo de probable origen coronario. Entre estos nuevos biomarcadores destaca la copeptina, objeto de este estudio.
La copeptina es un fragmento estable (fracción C terminal) del precursor de vasopresina-arginina (regulador clave del balance hídrico). Se secreta por la neurohipófisis en periodos de estrés y desempeña una función crítica en la regulación del eje formado por el hipotálamo, la glándula pituitaria y la glándula suprarrenal4.
Asimismo, se ha correlacionado con el pronóstico de cardiopatía isquémica, fallo cardiaco, sepsis y enfermedades cerebrovasculares5,6.
La medida in vitro del precursor de vasopresina-arginina es muy difícil debido a su corta vida media, inestabilidad y a las dificultades en su determinación, por lo que se mide un marcador subrogado como es la copeptina7,8.
Sin embargo, el papel de la copeptina en el diagnóstico de pacientes SCA todavía no está claramente establecido. Aunque parece que algunos autores encuentran que la combinación de copeptina y troponina negativas aumenta el valor predictivo negativo para la exclusión de forma rápida de IAM hasta en un 99%9,10, otros como Llorens et al.11 o Esteban-Torrella et al.12 encuentran que la determinación de copeptina en pacientes con dolor torácico de menos de 12 h de evolución sugestivo de SCA, electrocardiograma no diagnóstico y primera troponina negativa no permite descartar de forma rápida y segura la presencia de síndrome coronario agudo sin elevación de ST (SCASEST).
Por otro lado, en un metaanálisis llevado a cabo por Lipinski et al.13 se señala que ambas determinaciones mejoran la sensibilidad y el cociente de probabilidad negativo para el diagnóstico de IAM, comparado con la valoración únicamente de troponina.
El objetivo principal de este estudio es comprobar si realmente la determinación de copeptina tiene algún valor en el diagnóstico diferencial del dolor torácico agudo de probable origen coronario y comprobar su utilidad en la diferenciación entre pacientes con SCASEST y pacientes no SCASEST.
Material y métodosDesde septiembre hasta diciembre de 2014 incluimos a todos los pacientes mayores de 18 años de edad atendidos de forma consecutiva en el Departamento de Urgencias por presentar dolor torácico de origen no traumático. Los criterios de exclusión fueron los siguientes: edad inferior a 18 años, cáncer activo, enfermedades avanzadas crónicas (cirrosis, fallo cardiaco o renal), sepsis, shock, dificultades en la comunicación o alteraciones cognitivas.
También se excluyó a los pacientes que llegaron al Departamento de Urgencias 12 h después del comienzo del dolor torácico, puesto que en estos pacientes no se necesitan determinaciones seriadas de troponina, así como a los pacientes cuya primera determinación de troponina fue positiva, debido a que en estos casos el diagnóstico de SCASEST queda ya firmemente establecido.
En cada paciente se recogió la información relativa a datos epidemiológicos: edad, sexo y factores de riesgo para enfermedad cardiovascular tales como: hipertensión arterial (presión sanguínea ≥140/90mmHg o tratamiento con fármacos antihipertensivos), diabetes mellitus, dislipidemia (cuando el paciente está tomando fármacos hipolipidemiantes), hábito tabáquico, historia familiar en primer grado de cardiopatía isquémica y obesidad (IMC>30kg/m2).
De todos los pacientes que participaron se recogió por escrito el consentimiento informado.
La evaluación inicial del paciente se realizó de acuerdo con el protocolo de estudio de paciente con sospecha de SCA de nuestro Servicio de Urgencias, incluyendo la medida de troponina, con seriación en admisión y a las 6 h. Tras 15 min de reposo se extrajeron 20ml de sangre, 10ml en un contenedor con EDTA para la determinación de copeptina y 10ml en un tubo sin aditivos, únicamente con gel separador, para la determinación de los parámetros séricos. El plasma obtenido del tubo con EDTA se separó rápidamente y se congeló a −80°C hasta la determinación de copeptina.
La determinación de copeptina se llevó a cabo mediante un novedoso ensayo comercial de inmunofluorescencia basado en la tecnología TRACE™ (time-resolved amplified cryptate emission), que mide la señal que es emitida desde un inmunocomplejo con retardo de tiempo (BRAHMS AG, Hennigsdorf, Alemania).
La técnica se encuentra totalmente automatizada en un equipo Kryptor Compact Plus System (Thermo Fisher Scientific).
El límite inferior de detección de esta técnica es de 4,8pmol/L y su sensibilidad funcional (valor correspondiente a una imprecisión analítica con un coeficiente de variación interanálisis del 20%) es inferior a 12pmol/L según datos del fabricante.
La mediana en la concentración de copeptina en 200 individuos sanos fue de 3,7pmol/L y los percentiles 95; 97,5 y 99 fueron respectivamente 9,8, 13 y 18,9pmol/L.
Los pacientes del estudio se subdividieron en 5grupos según su diagnóstico final:
- •
Pacientes con SCASEST.
- •
Pacientes con angina inestable.
- •
Pacientes con angina estable.
- •
Pacientes con enfermedad cardiaca diferente a SCA.
- •
Pacientes con dolor no traumático de origen no coronario.
Las variables continuas se expresan como media±desviación estándar o como mediana (rango intercuartílico) según su distribución, y las variables cualitativas como frecuencias. Para la comparación de variables cualitativas se ha utilizado el test de chi cuadrado y para la comparación de variables cuantitativas entre varios grupos se empleó el test no paramétrico de U de Mann-Whitney. Para las comparaciones múltiples se utilizó el método de Bonferroni. Se consideró significativo un valor de p<0,05.
El rendimiento diagnóstico de copeptina se calcula mediante el análisis del área bajo la curva ROC con un intervalo de confianza del 95% (IC 95%). Se calcula asimismo la sensibilidad y especificidad y los valores predictivos VPP, VPN, CPP y CPN.
Para el análisis estadístico de los datos se ha utilizado el programa SPSS versión 20.0 (IBM, EE. UU.).
ResultadosDurante el periodo del estudio se incluyeron a 82 pacientes. La edad media fue de 68±15 años y el 63% eran varones. El 56,8% de los pacientes presentaron una concentración de copeptina inferior a 14pmol/L (uno de los valores de punto de corte de copeptina más frecuentemente utilizado).
Se diagnosticaron de SCASEST el 15,7% de todos los pacientes. Un 19,3% presentaron angina inestable y el 13,2% fueron diagnosticados de angina estable.
El 20,5% de los pacientes presentó alguna enfermedad cardiaca diferente a SCA y el 31,3% fueron diagnosticados de dolor torácico de origen no coronario.
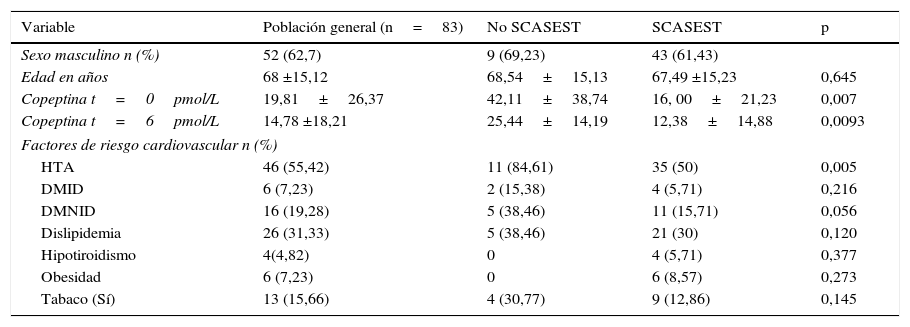
En la tabla 1 se muestran las características generales de la muestra de pacientes estudiada.
Características generales de la población de estudio
| Variable | Población general (n=83) | No SCASEST | SCASEST | p |
|---|---|---|---|---|
| Sexo masculino n (%) | 52 (62,7) | 9 (69,23) | 43 (61,43) | |
| Edad en años | 68 ±15,12 | 68,54±15,13 | 67,49 ±15,23 | 0,645 |
| Copeptina t=0pmol/L | 19,81±26,37 | 42,11±38,74 | 16, 00±21,23 | 0,007 |
| Copeptina t=6pmol/L | 14,78 ±18,21 | 25,44±14,19 | 12,38±14,88 | 0,0093 |
| Factores de riesgo cardiovascular n (%) | ||||
| HTA | 46 (55,42) | 11 (84,61) | 35 (50) | 0,005 |
| DMID | 6 (7,23) | 2 (15,38) | 4 (5,71) | 0,216 |
| DMNID | 16 (19,28) | 5 (38,46) | 11 (15,71) | 0,056 |
| Dislipidemia | 26 (31,33) | 5 (38,46) | 21 (30) | 0,120 |
| Hipotiroidismo | 4(4,82) | 0 | 4 (5,71) | 0,377 |
| Obesidad | 6 (7,23) | 0 | 6 (8,57) | 0,273 |
| Tabaco (Sí) | 13 (15,66) | 4 (30,77) | 9 (12,86) | 0,145 |
DMID: diabetes mellitus indulinodependiente; DMNID: diabetes mellitus no insulinodependiente: HTA: hipertensión arterial.
Entre los pacientes diagnosticados de SCASEST, 5 (38,5%) presentaron concentración de copeptina inferior a 14pmol/L y solamente 3 (23,1%) presentaron una concentración de copeptina inferior a 10pmol/L.
La concentración de copeptina a tiempo 0 (19,8±26,4pmol/L) resultó ser mayor a la obtenida a las 6 h (14,8±18,2pmol/L) en el grupo total de pacientes y las diferencias fueron estadísticamente significativas (p<0,05).
En el grupo de pacientes SCASEST obtuvimos las mayores diferencias entre la concentración de copeptina a tiempo 0 (42,1±38,7pmol/l) y la concentración de copeptina a las 6 h (25,4±27,2pmol/L; p<0,01).
En el grupo de pacientes con angina inestable, así como en los pacientes con enfermedad cardiaca diferente a SCA, el grado de significación fue p<0,05 y en el de pacientes con dolor de origen no traumático y no coronario no obtuvimos significación estadística (p=0,080). Tampoco se obtuvieron diferencias significativas en el grupo de pacientes con angina estable.
Obtuvimos diferencias estadísticamente significativas en los valores de copeptina a tiempo 0 entre los pacientes diagnosticados de SCASEST: 42,1±38,7pmol/L y los pacientes no SCASEST: 16,0±21,2pmol/L (p<0,01), sin diferencias significativas en la concentración de copeptina a las 6 h: 25,4± 14,2pmol/L en pacientes SCASEST vs. 12,4±14,9pmol/L en pacientes no SCASEST (p=0,093).
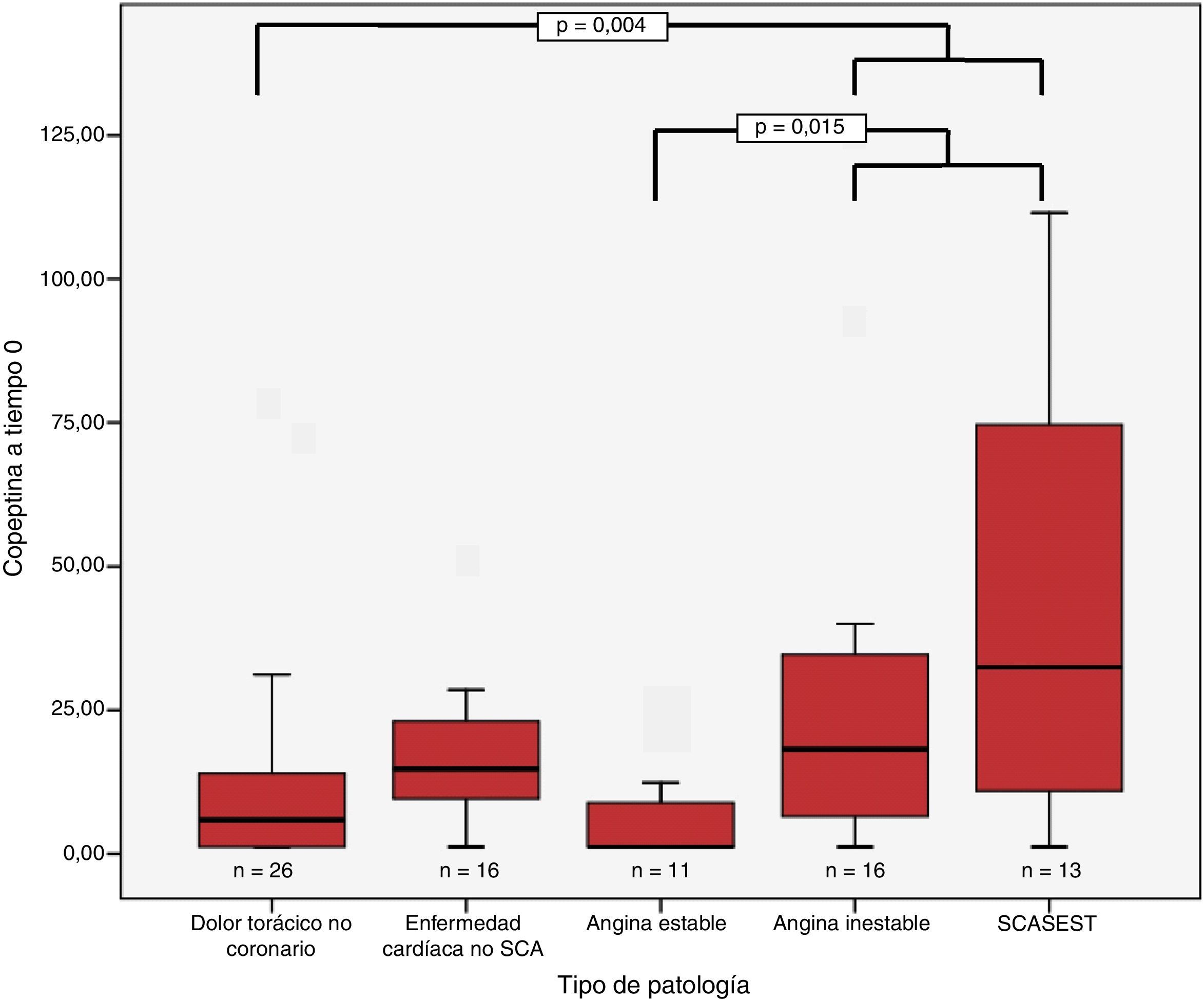
Cuando nos referimos a las diferencias existentes en la concentración de copeptina entre los distintos grupos según la enfermedad, podemos apreciar lo siguiente (fig. 1):
- •
Encontramos diferencias significativas en la concentración de copeptina cuando comparamos el grupo de pacientes SCA (SCASEST+pacientes con angina inestable) con los pacientes con dolor muscular de origen no coronario a tiempo 0: 34,1±36,4 vs. 10,7±15,9pmol/L (p<0,01), pero no a las 6 h: 20,9±23,3 vs. 6,2 ±8,4pmol/L.
- •
No se obtuvieron diferencias estadísticamente significativas en la concentración de copeptina a tiempo 0 entre los pacientes con SCA (SCASEST+pacientes con angina inestable): 34,1±36,4pmol/L y los pacientes con enfermedad cardiaca distinta a SCA, 17,3±11,6pmol/L, ni tampoco hubo diferencias a las 6 h: 20,9±23,3 vs. 14,2±10,2pmol/L.
- •
Obtuvimos, en cambio, diferencias estadísticamente significativas cuando comparamos las concentraciones de pacientes con SCA (SCASEST+pacientes con angina inestable) con los que padecen angina estable a tiempo 0: 34,1±36,4 vs. 7,1±9,1pmol/L, (p<0,05), pero no a las 6 h: 20,9±23,3 vs. 6, 6±6,6pmol/L.
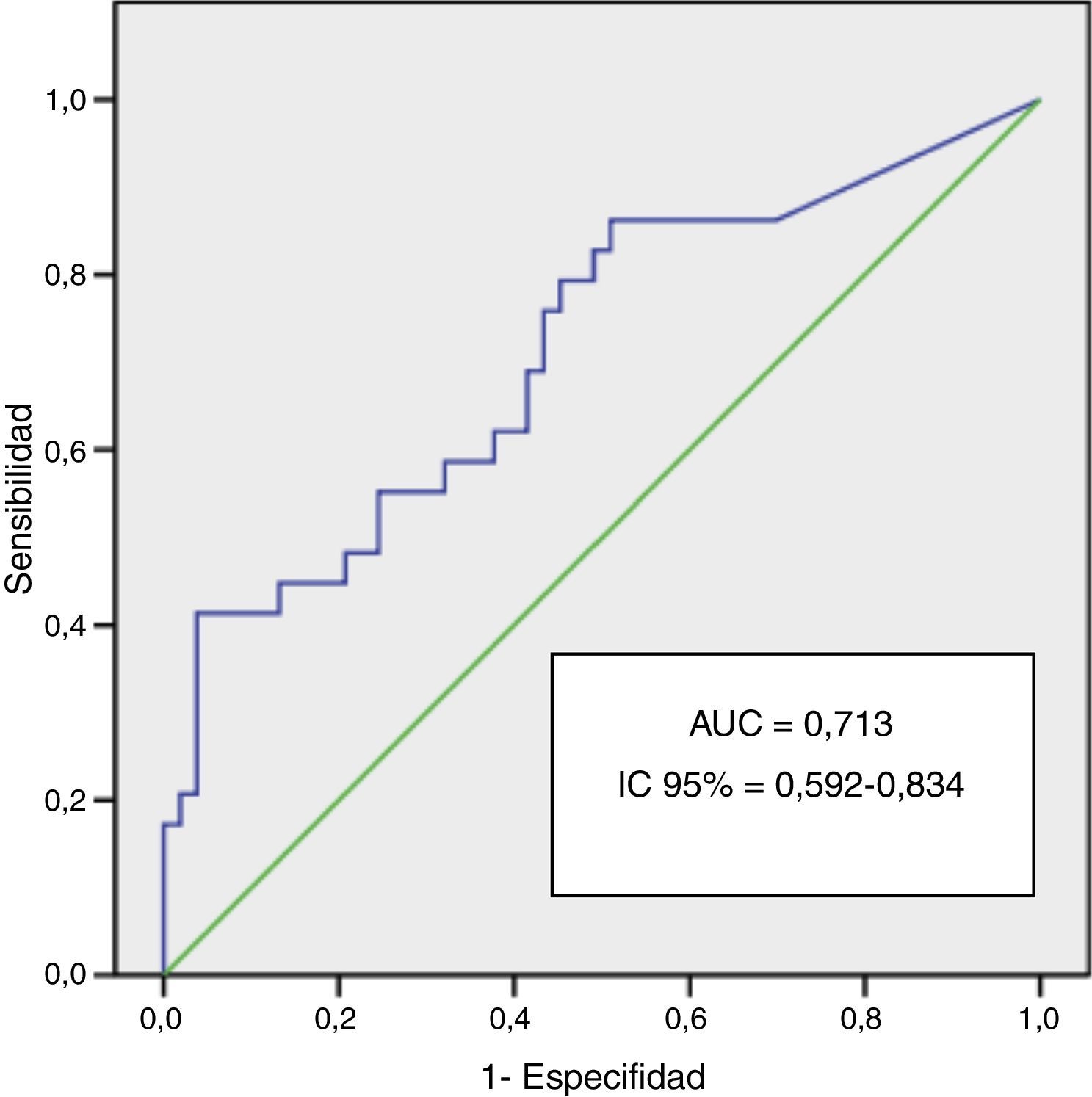
El análisis ROC para la copeptina en los pacientes SCASEST a tiempo 0 fue de 0,713 con un IC 95% de 0,592 a 0,834 y un grado de significación p=0,001 (fig. 2).
Para un punto de corte de 14pmol/L obtuvimos una sensibilidad de 0,615 (61,54%), especificidad de 0,608 (60,87%), VPP de 0,226 (22,6%), VPN de 0,895 (89,50%), CPP de 1,57 y CPN de 0,57.
Cuando se establece un punto de corte de 10pmol/L se obtienen los siguientes valores: sensibilidad: 0,769 (76,9%); especificidad: 0,521 (52,1%); VPP: 0,230 (23,0%); VPN: 0,924 (92,41%); CPP: 1,65 y CPN: 0,44.
DiscusiónCabe destacar el alto porcentaje de pacientes SCASEST que presentan hipertensión arterial (92,3%), frente al 50% en pacientes no SCASEST (p<0,01).
Existe también un mayor porcentaje de pacientes SCASEST que presentan dislipidemia, diabetes mellitus no insulinodependiente y tabaquismo que en el grupo de pacientes no SCASEST, pero las diferencias en ningún caso llegaron a ser significativas, aunque se aproximaron a alcanzar significación en diabetes mellitus no insulinodependiente (p=0,069).
Estos resultados apoyan el concepto de que existe mayor frecuencia de SCASEST entre aquellos pacientes que presentan los factores clásicos de riesgo cardiovascular14.
Nusestro estudio pone de manifiesto que se produce mayor secreción de copeptina ante un evento agudo a tiempo 0 y que disminuye posteriormente su concentración por degradación entre las 4 y las 10 h, sobre todo en los pacientes SCASEST, resultados que concuerdan con los obtenidos por otros autores15,16.
Este es el motivo por el que según nuestros resultados resulta mucho más útil la determinación de copeptina a tiempo 0 frente a la determinación a las 6 h.
A tiempo 0 obtenemos diferencias estadísticamente significativas en la concentración de copeptina entre pacientes SCASEST y no SCASEST, y entre pacientes SCA y pacientes con angina estable (con concentración superior en los primeros), mientras que estas diferencias desaparecen cuando se hace la determinación a las 6 h.
Sin embargo, en el estudio de Marston et al.17 se comprobó que una segunda determinación de copeptina 2 h después de la presentación del dolor torácico puede ser útil en la estratificación de riesgo y en la exclusión de IAM en pacientes con troponina negativa y una primera determinación de copeptina positiva (riesgo intermedio).
El mayor problema que presenta la copeptina como marcador de IAM y SCASEST es su falta de especificidad respecto al tejido cardiaco. De hecho, es un marcador específico de estrés endógeno, por lo que tiene implicaciones clínicas en distintas condiciones tanto no cardiovasculares, neumonía y sepsis18 como cardiovasculares, fallo cardiaco19.
Es por ello por lo que no obtenemos diferencias estadísticamente significativas cuando comparamos la concentración de copeptina entre pacientes con SCA (SCASEST+angina inestable) y pacientes con alguna enfermedad cardiaca diferente a SCA.
Asimismo, la concentración es más elevada en pacientes SCASEST que en pacientes con angina inestable (el estrés producido en la angina inestable es inferior al producido en SCASEST)20.
Los autores del estudio ROMICAT señalan que la copeptina refleja sobre todo la disfunción ventricular, teoría corroborada por Kelly et al. y Narayan et al.21,22, cuyos resultados demuestran que la concentración de copeptina tiene gran valor para predecir efectos adversos y mortalidad en pacientes SCASEST y su valor pronóstico es similar a pro-BNP.
Nuestro valor ROC 0,713 de copeptina para pacientes SCASEST fue similar al obtenido en el estudio de Llorens et al. (0,710)11 y de Raskovalova et al.23 en un metaanálisis en el que se evaluó solamente la efectividad de copeptina en el diagnóstico de IAM, encontrando en este caso un valor ROC de 0,700 (IC 95%: 0,660–0,740).
En nuestro estudio obtuvimos los mejores resultados de sensibilidad, VPN, CPP y CPN para copeptina, con un punto de corte en 10pmol/l, punto de corte propuesto también por Keller et al.24 como óptimo para el diagnóstico de IAM.
Utilizando este punto de corte, solamente 3 de nuestros 13 pacientes diagnosticados de SCASEST quedarían mal clasificados con relación a su concentración de copeptina.
En el estudio de Duchenne et al.25, con un tamaño muestral parecido al nuestro (n=102) obtienen un VPN de 94,2% para un punto de corte de copeptina de 14pmol/L, similar al obtenido por nosotros (92,4%), para un punto de corte de 10pmol/L y. En el estudio de Llorens et al.11 encontraron mayor utilidad a la determinación de copeptina en el subgrupo de pacientes de mayor edad (mayores de 70 años), obteniendo en estos casos un VPN de 95,1% en contraste con el obtenido en pacientes menores de 70 años (VPN = 92,6%).
Recientemente, a partir de los datos de un estudio multicéntrico, se ha indicado la estrategia de medida de copeptina y troponina en pacientes con riesgo de SCA entre bajo e intermedio, en los que un resultado negativo de ambos permitiría dar de alta de forma segura al paciente26.
En este estudio se partía de un total de 902 pacientes de riesgo cardiovascular bajo o intermedio en los que se sospechaba SCA y que presentaban troponina y copeptina negativas, los cuales se distribuyeron aleatoriamente en 2grupos, uno al que se le hicieron determinaciones bioquímicas seriadas de los marcadores bioquímicos y se les mantuvo ingresados el tiempo estipulado según protocolo normal, y otro al que se le siguió de forma ambulatoria, sin diferencias en cuanto a eventos cardiacos mayores adversos entre ambos grupos.
Este grupo de estudio también utilizó como punto de corte de copeptina 10pmol/L, pero no queda muy claro si utilizaron para el diagnóstico la troponina habitual o la troponina ultrasensible.
Nuestros resultados, al igual que los obtenidos por Llorens et al.11 y Esteban-Torrella et al.12, no permiten llegar a la conclusión de que con la medida de copeptina en adición a troponina pueda descartarse la presencia de SCASEST, por lo que es necesaria una segunda determinación de troponina a las 6 h, tal y como se viene haciendo hasta ahora.
La utilización de un nuevo marcador para el diagnóstico de SCASEST requiere al menos una sensibilidad y un VPN tan altos como la determinación seriada de troponina.
Teniendo en cuenta la morbimortalidad de la enfermedad, la determinación de copeptina solo podría evitar una segunda determinación de troponina si su VPN fuese ≥99%, valor que no se ha encontrado en ninguno de estos estudios.
El uso de ensayos de troponina ultrasensible en combinación con la determinación de copeptina probablemente conduzca a la obtención de VPN más altos27,28, pero esto todavía ha de estudiarse en grupos más numerosos de población. En el momento actual la medición seriada de troponina ultrasensible representa el gold standard para el diagnóstico de SCASEST.
Sin embargo, un hallazgo importante en nuestro estudio es que la concentración de copeptina nos permite diferenciar los distintos grupos de pacientes presentados en este estudio.
ConclusionesLa concentración de copeptina representa un valor adicional en la diferenciación de los distintos grupos de pacientes que acuden a Urgencias por dolor torácico sugestivo de origen coronario, y permite diferenciar entre pacientes SCASEST y pacientes no SCASEST, así como entre pacientes SCA y pacientes con angina estable.
El punto de corte de 10pmol/L proporciona los mejores valores de sensibilidad, VPN, CPN y CPP en el diagnóstico de pacientes SCASEST.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.