La Sociedad Española de Arteriosclerosis tiene entre sus objetivos contribuir al mayor y mejor conocimiento de la enfermedad vascular, su prevención y su tratamiento. Es de sobra conocido que las enfermedades cardiovasculares son la primera causa de muerte en nuestro país y conllevan además un elevado grado de discapacidad y gasto sanitario. La arteriosclerosis es una enfermedad de causa multifactorial y es por ello que su prevención exige un abordaje global que contemple los distintos factores de riesgo con los que se asocia. Así, este documento resume el nivel actual de conocimientos e incluye recomendaciones y procedimientos a seguir ante el paciente que presenta enfermedad cardiovascular establecida o se encuentra con elevado riesgo vascular. En concreto, este documento revisa los principales síntomas y signos a evaluar durante la visita clínica, los procedimientos de laboratorio y de imagen a solicitar de forma rutinaria o aquellos en situaciones especiales. Igualmente, incluye la estimación del riesgo vascular, los criterios diagnósticos de las distintas entidades que son factores de riesgo cardiovascular, plantea recomendaciones generales y específicas para el tratamiento de los distintos factores de riesgo cardiovascular y sus objetivos finales. Por último, el documento recoge aspectos habitualmente poco referenciados en la literatura como son la organización de una consulta de riesgo vascular.
One of the objectives of the Spanish Society of Arteriosclerosis is to contribute to better knowledge of vascular disease, its prevention and treatment. It is well known that cardiovascular diseases are the leading cause of death in our country and entail a high degree of disability and health care costs. Arteriosclerosis is a multifactorial disease and therefore its prevention requires a global approach that takes into account the different risk factors with which it is associated. Therefore, this document summarizes the current level of knowledge and includes recommendations and procedures to be followed in patients with established cardiovascular disease or at high vascular risk. Specifically, this document reviews the main symptoms and signs to be evaluated during the clinical visit, the laboratory and imaging procedures to be routinely requested or requested for those in special situations. It also includes vascular risk estimation, the diagnostic criteria of the different entities that are cardiovascular risk factors, and makes general and specific recommendations for the treatment of the different cardiovascular risk factors and their final objectives. Finally, the document includes aspects that are not usually referenced in the literature, such as the organization of a vascular risk consultation.
La medicina es una ciencia en perpetuo cambio. En los últimos años hemos asistido a un continuo avance en el diagnóstico y tratamiento de la enfermedad cardiovascular (CV) y de sus factores de riesgo, por lo que es preciso una actualización permanente de las guías terapéuticas.
En los últimos decenios, el avance en el diagnóstico y tratamiento farmacológico de la hipertensión arterial (HTA), la hipercolesterolemia y la diabetes mellitus de tipo 2 (DM2), ha sido espectacular y se traduce en un mayor grado de control, si bien aún lejos de los niveles óptimos, ensombrecidos por grupos de pacientes con una baja adherencia y colectivos médicos con una elevada inercia terapéutica. Asimismo, se va reduciendo la prevalencia del tabaquismo, en ciertos subgrupos de población, que en gran parte se explica por las restricciones de consumo, legisladas en los últimos años. Sin embargo, otras áreas de la prevención cardiovascular no ofrecen expectativas tan positivas; el incremento de la prevalencia del síndrome metabólico (SM), la obesidad y la diabetes mellitus (DM), cada vez en edades más tempranas, indican que aún existe un largo camino por recorrer, y una oportunidad de mejora en evitar la enfermedad cardiovascular aterosclerótica (ECVA), o al menos retrasarla.
La Sociedad Española de Arteriosclerosis (SEA) tiene entre sus objetivos contribuir al mejor conocimiento y control de los factores de riesgo cardiovascular (FRCV) en nuestro país, en especial de la dislipemia, a través de su red de Unidades de Lípidos. Esto se traduce en fomentar actividades investigadoras y formativas. La ECVA es multifactorial y por ello requiere una estrategia dirigida al control del conjunto de FRCV, incluyendo las dislipemias. Por ello, la SEA ha decidido elaborar unos Estándares para el Control Global del Riesgo Cardiovascular, una forma de resumir la evidencia científica y las recomendaciones nacionales e internacionales sobre los principales factores de riesgo. Estamos convencidos de que este documento aportará claridad y constituirá una puesta al día de los procedimientos diagnósticos, de la utilidad real o de investigación de diversas pruebas bioquímicas o de imagen y de la categorización del riesgo vascular y el tratamiento, tanto en lo que se refiere a los hábitos de vida, especialmente la dieta, como al tratamiento farmacológico.
Como ya se indicó en la primera versión de estos estándares, el documento nació con la intención de ser revisado y actualizado de forma periódica, por lo que se han introducido cambios a raíz de las nuevas evidencias relacionadas con el diagnóstico, la evaluación clínica y tratamiento de los distintos factores de riesgo, así como de las que provienen de las nuevas Guías de Práctica Clínica publicadas recientemente. El objetivo del documento sigue siendo el mismo: ser de utilidad a todos los clínicos que de una u otra forma atendemos pacientes de riesgo vascular, desde la atención primaria a la atención hospitalaria, en prevención primaria o secundaria, y, en general, a todos aquellos miembros que pertenecen a las sociedades que integran el Comité Español Interdisciplinario para la Prevención Vascular (CEIPV). Este documento va también dirigido a los profesionales en formación, no exclusivamente a los de las profesiones sanitarias, y en particular a los investigadores básicos interesados en el proceso de la arteriosclerosis.
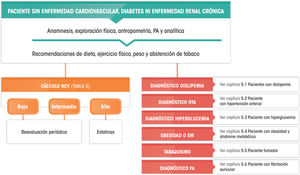
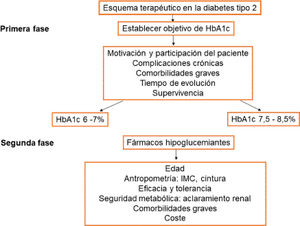
Anamnesis, exploración y pruebas complementarias en consultaLa historia clínica convencional y la recogida ordenada de síntomas y signos del paciente suponen el procedimiento común para acceder al diagnóstico de la patología. En este apartado, nos centraremos en destacar las características más importantes. La tabla 1 muestra de forma resumida los elementos que deben practicarse en una consulta que aborde el riesgo cardiovascular (RCV).
Requerimientos, anamnesis, exploración y pruebas complementarias para la estimación del riesgo vascular
| Imprescindibles | Recomendables | |
|---|---|---|
| Anamnesis | – AF de ECVA precoz o de FRCV.– AP de ECVA (territorio, forma de presentación, fecha o edad del episodio).– AP de FRCV.– Consumo de alcohol y tabaquismo.– Tratamientos, incluyendo tratamiento de los FRCV: diabetes, HTA, dislipemia.– Síntomas por aparatos (cardiológicos, claudicación intermitente, disfunción eréctil). | – Cuestionario de Edimburgo1 (Anexo 1).– Cuestionario de disfunción eréctil (SQUED)2 (Anexo 2).– Test de Fargenström en fumadores3,4 (Anexo 3) |
| Exploración física | – Antropometría: Peso, talla, IMC, perímetro abdominal.– Medida de la presión arterial.– Pulsos centrales y periféricos y soplos vasculares.– Exploración cardíaca.– Exploración abdominal: hepatomegalia y esplenomegalia.– Xantomas, arco corneal. | – Búsqueda de opacidad corneal e hipertrofia de amígdalas.– Fundoscopia. |
| Pruebas complementarias | – ECG.– Perfil lipídico (CT, cHDL, triglicéridos, Colesterol no-HDL y cLDL).– Apo B.– Perfil hepático (bilirrubina, ALT, AST, GGT, FAL).– Glucemia, Na, K, Ca, ácido úrico.– HbA1c– FGe y Albuminuria.– TSH.– CPK.– Lp(a) | – MAPA o AMPA.– Pruebas genéticas para diagnósticos concretos.– Genotipo de Apo E.– Ecografía abdominal.– Test del monofilamento.– Apo A1.– Lipopartículas |
| Cuestionarios de dieta y actividad física | – Valoración genérica del cumplimiento de dieta y ejercicio. | – Puntuación de dieta mediterránea MEDAS5 (Anexo 4).– Cuestionario de ejercicio IPAQ6 (Anexo 5). |
| Estudio de enfermedad cardiovascular subclínica | – ITB.– Ecografía carotídea y femoral.– CAC. |
AF: antecedentes familiares; ALT: alanina aminotransferasa; AMPA: automedida de la presión arterial; AP: antecedentes personales; Apo A1: apolipoproteína A1; Apo B: apolipoproteína B; Apo E: apolipoproteína E; ALT: alanina aminotransferasa; AST: aspartato aminotransferasa; Ca: calcio; CAC: calcio coronario; CPK: creatin-fosfokinasa; cHDL: colesterol de lipoproteínas de alta densidad; ECVA: enfermedad cardiovascular; ECG: electrocardiograma; FAL: fosfatasa alcalina; FGe: filtrado glomerular estimado; FRCV: factores de riesgo cardiovascular; GGT: gamma glutamil transferasa; HbA1c: hemoglobina glucosilada; HTA: hipertensión arterial; IMC: índice de masa corporal; ITB: índice tobillo-brazo; K: potasio; Lp(a): lipoproteína(a); MAPA: medición ambulatoria de PA; Na: sodio; PA: presión arterial; TSH: hormona estimulante de tiroides.
Es necesario el conocimiento de los antecedentes familiares de primer y segundo grado, tanto en lo que se refiere a enfermedades prevalentes relacionadas con la ECVA, como a los factores de riesgo, sobre todo en los casos con sospecha de hipercolesterolemia familiar (HF) o de ECVA prematura. Los antecedentes familiares tienen mayor valor cuando estos aparecen en familiares de primer grado (padre, madre, hijos o hermanos) y a edades tempranas de la vida, por debajo de los 55 años en el varón y por debajo de los 65 años en la mujer.
Antecedentes personalesAdemás de los antecedentes personales (AP) convencionales (alergias, intervenciones quirúrgicas, etc.) se debe indagar específicamente en los antecedentes de ECVA y en los diversos FRCV mayores (DM, HTA, dislipemia, tabaquismo y obesidad). En caso de estar presentes se debe anotar la edad de inicio y los tratamientos que se reciben, independientemente de su indicación. Las reacciones adversas o la intolerancia a los medicamentos y la existencia de embarazo o posibilidad del mismo deben igualmente ser conocidas. Se debe cuantificar la potencia y la cronología de los FRCV (número de cigarrillos al día y años de fumador, niveles máximos de colesterol LDL (cLDL), hemoglobina glucosilada (HbA1c) y presión arterial sistólica (PAS) o peso). Asimismo, debe registrarse la presencia de enfermedades sistémicas con carga inflamatoria de bajo grado, como la psoriasis, la enfermedad por virus de la inmunodeficiencia humana (VIH), la artritis reumatoide o el lupus eritematoso sistémico, y las neoplasias, pues por sí mismas o por su tratamiento aumentan el riesgo vascular. También deben recogerse en las mujeres los antecedentes de HTA o DM gestacional, síndrome de ovario poliquístico, la fecha de inicio de la menopausia y los tratamientos hormonales recibidos.
Anamnesis actual y por aparatosEs necesario indagar sobre el motivo de consulta, que en las consultas de RV suele ser una falta de control de uno o más de los FRCV. Se debe inquirir sobre los síntomas asociados con episodios isquémicos en los tres territorios mayores que hayan podido pasar desapercibidos o no estén diagnosticados aún (déficits neurológicos transitorios, dolor torácico con el esfuerzo, palpitaciones, disnea o claudicación intermitente), síntomas cardinales de la DM, cefalea o mareos asociados con elevación de las cifras de presión arterial (PA), síntomas relacionados con procesos que causan HTA secundaria (tabla 2) y elevaciones asintomáticas de los lípidos, excepcionalmente asociados con xantomas. Si el paciente ha sido instruido, sería aconsejable anotar las automedidas de la PA ambulatoria.
Síntomas y signos sugerentes de HTA secundaria
| – Elevación paroxística de la PA o HTA establecida con crisis añadidas, y la triada clásica de cefalea, sudoración y palpitaciones (feocromocitoma). |
| – Empeoramiento rápidamente progresivo de una HTA preexistente. |
| – Presencia de soplos arteriales como sospecha de HTA vasculorrenal. |
| – Ronquidos e hipersomnia (apnea del sueño). |
| – Síntomas prostáticos (IRC obstructiva). |
| – Calambres musculares, debilidad (hipopotasemia por hiperaldosteronismo). |
| – Edemas, astenia, tenesmo y polaquiuria (enfermedad renal). |
| – Obesidad central, facies luna llena, equimosis, estrías (síndrome de Cushing). |
| – Fármacos o drogas de abuso (alcohol, AINE, cocaína, anfetamina, regaliz, corticoides tópicos, etc.). |
| – Ausencia de historia familiar de HTA. |
| – Aparición de HTA en sujetos jóvenes (< 35 años). |
| – HTA resistente / refractaria: requiere más de tres o cinco fármacos, respectivamente, para su control. |
| – Respuesta paradójica a betabloqueantes. |
Debe registrarse el peso, la talla, el perímetro abdominal y calcularse el índice de masa corporal (IMC). La PA debe medirse de acuerdo con las recomendaciones de la tabla 3. La exploración cardiocirculatoria básica es obligada, en especial la presencia de soplos y la magnitud de los pulsos arteriales; la interpretación de los hallazgos dependerá del contexto: una ausencia de pulsos pedios puede indicar en un anciano claudicante una enfermedad arterial periférica (EAP), mientras que una asimetría de pulsos en un joven hipertenso puede indicar coartación de la aorta. Debe recogerse el hallazgo de hepatomegalia y/o esplenomegalia La presencia de xantomas, su morfología y su localización en muchos casos constituyen un factor diagnóstico de primer nivel. Como ejemplo orientativo, los xantomas tendinosos sugieren HF, los tubero-eruptivos indican quilomicronemia y los xantomas estriados palmares son característicos de la disbetalipoproteinemia. La presencia de xantomas de consistencia pétrea adheridos a superficies óseas son sugestivos de xantomatosis cerebro-tendinosa.
Recomendaciones para la medida de la PA y diagnóstico de HTA
| Medida de la PA |
| – Paciente sentado durante 3-5 minutos antes de iniciar las medidas de la PA. |
| – Realizar al menos dos medidas, en posición sentado y sin cruzar las piernas, separadas 1-2 minutos, y hacer medidas adicionales si las dos primeras son muy diferentes. Registre la media de las dos últimas medidas. |
| – Realizar un mayor número de medidas si el paciente presenta arritmia (por ejemplo, fibrilación auricular). |
| – Utilizar un manguito estandarizado: 12-13cm de ancho y 35cm de largo, pero disponer de uno más ancho cuando la circunferencia del brazo sea > 32cm. |
| – El manguito debe situarse a la altura del corazón; el dorso de la mano y el brazo apoyados sobre una mesa para evitar el efecto de la contracción muscular isométrica sobre la PA. |
| – Se recomienda realizar una medida bilateral (simultánea de la PA en los dos brazos en la primera visita, especialmente en los pacientes de alto riesgo vascular. En posteriores visitas, utilizar como referencia el brazo con los valores más altos de PA: Una diferencia entre las dos extremidades superiores > 10-15mmHg, se asocia con un incremento del RCV. Cuando la diferencia es importante (≥ 20 mmHg), se ha de sospechar una estenosis de la arteria subclavia. |
| – Tras cinco minutos de reposo en decúbito supino, medir la PA y después de 1 y 3 minutos en bipedestación: Se debe hacer en la primera visita o cuando se sospecha clínicamente una hipotensión ortostática, especialmente en pacientes mayores, diabéticos, o pacientes neurológicos con trastornos neurodegenerativos. Si el descenso de PAS / PAD es ≥ 20 / 10mmHg, se aconseja medir adicionalmente la PA tras cinco minutos en decúbito supino para descartar HTA supina asociada. |
| Diagnóstico de HTA |
| – El diagnóstico de HTA (especialmente en la HTA grado 1) se establecerá después de la comprobación de los valores de PA en dos o más medidas tomadas en cada una de dos o más ocasiones separadas varias semanas. Se recomienda confirmar el diagnóstico mediante medidas ambulatorias de la PA: AMPA o MAPA durante 24 horas. |
Una parte importante en la evaluación del riesgo vascular y en el diagnóstico de las dislipemias requiere de una analítica de sangre. Las condiciones óptimas para su extracción, su procesamiento y su evaluación han sido publicadas en forma de consenso por las sociedades europeas de arteriosclerosis y medicina del laboratorio11 y pueden consultarse en el Anexo 7.
Se debe contar con un perfil lipídico completo (colesterol total (CT), triglicéridos (TGS), colesterol HDL (cHDL), colesterol de lipoproteínas de baja densidad (cLDL) [estimado por la fórmula de Friedewald o por método directo] y el cálculo del colesterol no HDL si los TGS están elevados). Si están disponibles en el centro, es útil la determinación de Apolipoproteína B (Apo B) porque puede contribuir al cribado de disbetalipoproteinemia y a diferenciarla de la forma más común que es la hiperlipemia familiar combinada12. La elevación de la lipoproteína(a) [Lp(a)] tiene un papel relevante en el incremento del riesgo vascular que presentan algunos pacientes con HF, y en sujetos con enfermedad isquémica prematura, o recurrente, a pesar de que presenten un buen control del resto de FRCV. Se aconseja la determinación de los niveles de Lp(a) al menos en la primera analítica del paciente, en especial en casos de ateroclerosis prematura.
En la primera visita debe solicitarse un hemograma convencional y pruebas de bioquímica en sangre que incluyan el perfil glucémico (glucemia en ayunas, HbA1c), la función renal y hepática, así como los niveles de creatina-fosfoquinasa (CPK), Na, K, Ca, ácido úrico y thyroid-stimulating hormone (TSH). En la orina, preferentemente de primera hora de la mañana, se debe solicitar la determinación del cociente albuminuria/creatinina urinaria. La medición de proteínas en orina es necesaria para descartar síndrome nefrótico. Puesto que el riesgo de hepatotoxicidad por los tratamientos es excepcional13, no se recomienda el control sistemático de transaminasas durante el tratamiento con estatinas, excepto cuando hay un aumento de dosis14 (EAS/ESC 2019). Un electrocardiograma (ECG) en reposo aporta información de valor en pacientes que son evaluados por HTA.
Anamnesis, exploración y pruebas complementarias en consulta: recomendablesAnamnesis: Cuestionario de Edimburgo y cuestionario de disfunción eréctilDebe realizarse una anamnesis específica sobre hábito de fumar, incluyendo test de Fargeström en los fumadores (Anexo 3), (ver Paciente fumador). Ante la sospecha de claudicación intermitente, el cuestionario de Edimburgo, validado en nuestro país (Anexo 1), permite reforzar el diagnóstico clínico de la EAP1. El cuestionario para la valoración de disfunción eréctil (SQUED) se muestra en el Anexo 2.
Exploración físicaEn los pacientes con colesterol de lipoproteínas de alta densidad (cHDL) muy bajo, deberá buscarse de forma específica la presencia de opacidad corneal (déficit de lecitina-colesterol aciltransferasa [LCAT]) o la hipertrofia amigdalar (enfermedad de Tangier). La fundoscopia aporta información valiosa en el examen del paciente con DM, en las hiperquilomicronemias primarias (lipemia retinalis) y en las lesiones de órgano diana de la HTA, siendo imprescindible en la HTA de grado 3 (PAS ≥ 180 mmHg y/o presión arterial diastólica (PAD) ≥ 110 mmHg).
Pruebas complementarias adicionalesAnte la sospecha de HF15 debe utilizarse la escala clínica y bioquímica Diagnostic criteria for the clinical diagnosis of HeFH according to MedPed and WHO1 (Anexo 6) y confirmarse con el diagnóstico genético. La existencia de procedimientos de secuenciación masiva y la comercialización de paneles genéticos para hipercolesterolemia permite el diagnóstico de la misma, la diferenciación entre formas heterocigotas, heterocigotas compuestas, dobles heterocigotas y homocigotas (entre las cuales puede haber solapamiento clínico y analítico) o el hallazgo de otras enfermedades con las que puede compartir fenotipo (déficit de lipasa ácida lisosomal). El genotipo de apolipoproteína E (Apo E) se debe solicitar cuando existe sospecha de disbetalipoproteinemia. La cuantificación Beta (mediante ultracentrifugación) podría ser de interés para la confirmación de la disbetalipoproteinemia (cociente colesterol de lipoproteínas de muy baja densidad (cVLDL)/TGS en mg/dL > 0,3) y para conocer la composición de las lipoproteínas plasmáticas, pero dado su elevado coste y complejidad, su uso está limitado. Una concentración de Apo B baja en presencia de hiperlipemia combinada es sospechosa de disbetalipoproteinemia. La determinación de la apolipoproteína A1 (Apo A1) se recomienda en el estudio de la hipercolesterolemia en la infancia. Un índice ApoB/ApoA1 superior a 0,82 ha mostrado mayor sensibilidad y especificidad en la detección de los portadores de una mutación genética para HF16.
La SEA entiende aconsejable medir las lipopartículas cuando exista: a) Sospecha de desajuste entre la concentración de lípidos y el número de partículas, situación común en la DM, obesidad y en el SM; b) ECVA precoz o recurrente, sin FRCV que la justifiquen; c) Trastornos lipídicos raros o complejos, como concentraciones extremas de cHDL y d) Situaciones clínicas en las que no se pueden aplicar técnicas analíticas clásicas, como cuando existen concentraciones muy bajas de cLDL17.
Entre las pruebas complementarias adicionales, la medición ambulatoria de la presión arterial (MAPA) durante 24 horas, está especialmente indicada cuando hay discordancia entre las tomas de PA en consulta y fuera del contexto clínico, existe una elevada variabilidad, cuando se sospecha HTA nocturna (apneas del sueño) y en casos de HTA resistente18. La automedida estandarizada de la PA en domicilio (AMPA) durante cinco a sete días, puede reemplazar a la MAPA, en especial durante el seguimiento, si se comprueba una buena concordancia entre ambas.
Estudio de la enfermedad vascular subclínicaLas pruebas que comentamos en este apartado se efectúan con la única intención de re-estratificar el RCV de un sujeto, ya que conciernen a un paciente sin ECVA establecida ni síntomas que hagan sospechar ECVA. Se refieren a un periodo de la historia natural del proceso aterosclerótico durante el cual, en ausencia de síntomas y signos, existen alteraciones estructurales demostrables en los vasos. Por definición, solo puede conocerse su existencia mediante pruebas diagnósticas específicas. Tanto los FRCV, como la enfermedad ateromatosa, tienen carácter sistémico, por lo que el hallazgo de afectación vascular en un territorio también aporta información sobre el estado de la enfermedad en los demás territorios. Las técnicas exploratorias disponibles deben ser no invasivas y su utilización se plantea para la obtención de información complementaria en la estimación del RCV, para redefinir los objetivos lipídicos y para orientar las decisiones terapéuticas19. También se ha propuesto la utilización de alguna de estas exploraciones para el cribado sistemático. Las exploraciones más habituales para diagnosticar la ECVA subclínica son las siguientes:
Índice tobillo/brazoEl índice tobillo/brazo (ITB) es el cociente de las presiones sistólicas de tobillo/brazo para cada miembro inferior. Un valor inferior a 0,9 indica la existencia de una estenosis mayor del 50% entre la aorta y las arterias distales de la pierna, con alta especificidad (90%) y una sensibilidad aceptable (79%); lo que permite identificar EAP significativa que puede cursar de modo silente o con síntomas mal definidos. Valores ≥1,4 suelen indicar la presencia de calcificación arterial, una situación que también se asocia con un incremento del riesgo de complicaciones cardiovasculares, especialmente frecuente en pacientes diabéticos. Por su sencillez, el ITB puede realizarse de forma sistemática en la evaluación del estado vascular del paciente, siempre que se disponga de un mini-doppler portátil y de 15 minutos para su determinación.
La medición del ITB no está justificada en pacientes de bajo riesgo por su escasa rentabilidad20, mientras que su rentabilidad es máxima cuando se efectúa en sujetos con los dos principales factores de riesgo asociados con EAP, como son la DM y el hábito de fumar. En series españolas, hasta un 25% de pacientes con DM2 sin claudicación, tienen ITB < 0,921. En los pacientes con DM de larga evolución y alta probabilidad de microangiopatía (que pueden identificarse con el test de monofilamento), el ITB tiene escasa sensibilidad para detectar casos de EAP debido a la elevada frecuencia de calcificación arterial que enmascara su medida.
Placas de ateroma en carótidasAunque la cuantificación del grosor íntima-media (GIM) carotideo medido por ecografía ha sido ampliamente utilizado para evaluar la evolución del proceso arteriosclerótico e incluso del beneficio del tratamiento de la hipercolesterolemia, en la actualidad su uso no está recomendado para la re-estratificación del RCV. No así la existencia de una placa carotídea19.
Se considera placa carotidea al engrosamiento focal mayor del 50% de la pared del vaso que lo rodea, o a un GIM mayor a 1,5 mm que protruye en la luz adyacente22. No solo se valora su presencia sino también el número, el tamaño, la irregularidad y la ecodensidad, características que se asocian también con el riesgo de complicaciones cardiovasculares en los territorios cerebral y coronario.
Presencia de calcio coronarioEl TAC (tomografía axial computarizada) torácico permite la cuantificación del calcio coronario (CAC) que se expresa en unidades Agatston23. La presencia de CAC indica una fase avanzada de arteriosclerosis coronaria y es un mejor predictor de episodios isquémicos que la presencia de placa carotidea y femoral24,25. Una puntuación igual o superior a 300 u Agatston superior al percentil 75 para la edad, sexo y raza, es el umbral que se utiliza para considerar un RCV alto, información complementaria que reclasifica el riesgo de los pacientes, en especial de los pacientes en riesgo intermedio26. Cuando no existe calcificación alguna (Agatston = 0), la probabilidad de lesión obstructiva coronaria es casi nula; mientras que el riesgo de complicaciones cardiovasculares es tanto mayor cuanto mayor es el grado de calcificación26. La puntuación aumenta inexorablemente con la edad, y aunque la repetición de la medición tras unos años aporta una actualización del riesgo, que es el correspondiente a la exploración más reciente, los cambios observados raramente contribuyen a modificar la actitud preventiva o terapéutica27. Las guías europeas19 consideran la presencia de CAC como un modificador del riesgo cuando su nivel supera los 100 u Agatston. Su mayor limitación es el coste y clásicamente el riesgo asociado con la radiación, aunque en la actualidad las nuevas exploraciones rápidas de baja radiación han minimizado dicho riesgo28. La angiografía por tomografía computarizada muestra enfermedad coronaria estenótica subclínica, capaz de aportar información adicional a los factores de riesgo clásicos, en especial en diabéticos y pacientes con HF de larga evolución29,30. La información que aporta es independiente de la suministrada por el CAC, que continúa identificando a pacientes con un riesgo superior aún en ausencia de estenosis31.
Cuestionarios de dieta y actividad física: escalas recomendadasMás allá de averiguar sobre datos generales de la dieta, como si ésta es rica en carbohidratos o grasas saturadas o de alteraciones del patrón alimentario, la dieta puede ser evaluada con un simple cuestionario de 14 preguntas, mediterranean diet adherence screener (MEDAS) sobre adherencia a la dieta mediterránea (Anexo 4), que ha sido validado en el ensayo prevención con dieta mediterránea (PREDIMED) y se asocia con la presencia de FRCV y con el RCV32. Debe cuantificarse el consumo de alcohol, que puede hacerse anotando el número (volumen en mL) de cervezas, vino y/o de licor a la semana y cuantificando los gramos del alcohol ingeridos por semana, estimando una graduación de 6, 12 y 40 grados, respectivamente, mediante la fórmula [volumen en mL x graduación x 0,8]/100.
La actividad física puede evaluarse de una forma semicuantitativa tanto durante el trabajo (1=no trabaja o sedentario; 2 = camina regularmente durante el trabajo; 3 = camina regularmente y levanta pesos y 4 = importante actividad física) como durante el tiempo de ocio (1 = no realiza ejercicio; 2 = camina al menos cuatro horas en semana; 3 = camina > cuatro horas en semana y 4 = entrenamiento vigoroso)33. Por último, es posible cuantificar de forma simple la actividad física usando el cuestionario international physical activity questionnaire (IPAQ), también validado6 y disponible online34 (Anexo 5).
Indicación de pruebas especialesAlgunos biomarcadores han sido ampliamente investigados como predictores del RCV (homocisteína, fosfolipasa A2 asociada con lipoproteína, factores trombogénicos) y no han sido incorporados a la rutina clínica por no aportar información adicional relevante del RCV en un paciente concreto. En su conjunto, estos biomarcadores no tienen justificación clínica ya que no aumentan la capacidad predictora de episodios respecto del systematic coronary risk evaluation (SCORE) europeo18. Más controvertido es el papel del más estudiado de todos ellos, la proteína C reactiva (PCR) ultrasensible, que en diversos estudios ha mostrado su capacidad predictiva de RCV. Su determinación en estudios epidemiológicos permite detectar pacientes que pueden presentar un riesgo residual independiente de los parámetros lipídicos, si bien presenta el inconveniente de una elevada variabilidad intraindividual que dificulta su utilización en la práctica clínica35.
En presencia de síntomas o signos sugestivos o ante la sospecha de enfermedad se deben solicitar las pruebas complementarias pertinentes, ergometría en caso de dolor torácico, o pruebas de imagen ante sospecha de HTA secundaria, test hormonales, etc.
Diagnóstico del riesgo cardiovascularRecogida de diagnósticos en la historia clínica: criterios diagnósticosTodo paciente atendido en una unidad de lípidos debe tener en su historia clínica un listado de diagnósticos estandarizados, que incluyen los referidos en la tabla 4. Además, deben añadirse todos los diagnósticos derivados de las enfermedades que pudiera tener, tanto cardiovasculares como no cardiovasculares8,36–44.
Criterios diagnósticos
| Diagnóstico | Definición |
|---|---|
| HipercolesterolemiaNo existe una cifra óptima de colesterol total o cLDL dado que cuanto más baja su concentración mejor. Se consideraría colesterol elevado, aquellos valores a partir de los cuales se recomiende tratamiento hipolipemiante, los cuales dependen del riesgo basal de cada persona (tabla 5). El C-no-HDL se utilizaría en pacientes con TGS > 400 mg/dL o en pacientes con diabetes. | – En prevención secundaria (enfermedad coronaria, cerebrovascular o arterial periférica) o si existen placas obstructivas en carótidas o coronarias: cLDL > 55 mg/dL o C-no-HDL > 85 mg/dL.– En diabetes tipo 2, con LOD, EVS o con 3 o más factores de riesgo: cLDL > 55 mg/dL o C-no-HDL 85 mg/dL.– En diabetes tipo 2, sin LOD, sin EVS y con menos de 3 factores de riesgo: cLDL > 70 mg/dl o C-no-HDL > 100 mg/dL.– En pacientes con ERC grado 3, sin LOD ni EVS: cLDL > 70 mg/dL o C-no-HDL > 100 mg/dL.– En pacientes con ERC grado 3, con LOD o EVS: cLDL > 55 mg/dL o C-no-HDL > 85 mg/dL.– En pacientes con ERC grados 4 o 5: cLDL > 55 mg/dL o C-no-HDL > 85 mg/dL.– En pacientes sin enfermedad cardiovascular, DM ni ERC cLDL > 100-116 mg/dL en función de si el riesgo es bajo o moderado de acuerdo con SCORE. |
| Hipertrigliceridemia | – TGS deseables < 150 mg/dL– Hipertrigliceridemia:– Leve: 150-499 mg/dL– Moderada 500-1.000 mg/dL– Grave: > 1.000 mg/dL |
| Hiperlipemia mixta | Concentraciones elevadas tanto de cLDL o C-no-HDL, como de TGS. |
| Hipercolesterolemia familiar | Utilización de las tablas de la Diagnostic criteria for the clinical diagnosis of HeFH according to MedPed and WHO1 (Anexo 6). |
| Hiperlipemia familiar combinada | ApoB > 120 mg/dL y TGS > 150 mg/dL en al menos dos miembros de la familia e historia familiar de ECVA sintomática prematura. Ausencia de xantomas. Se deben excluir causas de dislipemia secundaria. |
| Dislipemia aterogénica | Hipertrigliceridemia (TGS > 150 mg/dL) y cHDL bajo (< 40 mg/dL en varones y < 45 mg/dL en mujeres). Aumento del número de partículas LDL pequeñas y densas |
| Hipoalfalipoproteinemia | – cHDL inferior al percentil 10 según edad, raza y sexo. |
| Hiperlipoproteinemia (a) | Lp(a) ≥ 50 mg/dL. |
| HTA (medidas en consulta) | – PA óptima < 120 y < 80 mmHg– Normal 120-129 y 80-84 mmHg– Normal-alta 130-139 y/o 85-89 mmHg– HTA grado I: PAS 140-159 y/o PAD 90-99 mmHg– HTA grado II: PAS 160-179 y/o PAD 100-109 mmHg– HTA grado III: PAS ≥ 180 y/o PAD ≥ 110 mmHg– HTA sistólica aislada: PAS ≥ 140 y PAD < 90 mmHgEl diagnóstico se establece tras comprobar los valores de PA en al menos dos medidas en dos o más visitas separadas varias semanas.Cuando la PAS y la PAD se ubiquen en distintas categorías se aplicará la categoría superior.La HTA sistólica aislada se clasifica en grados (1, 2 o 3) según el valor de la PA sistólica. |
| Diabetes | Glucemia en ayunas de al menos 8 horas ≥ 126 mg/dL (7,0 mmol/L)*, oGlucemia 2 horas tras una SOG de 75g ≥ 200 mg/dL (11,1 mmol/L)*, oHbA1C ≥ 6,5% (48 mmol/mol), opaciente con síntomas clásicos de hiperglucemia con un valor de glucemia ≥ 200 mg/dL independientemente de la situación de ayuno (11,1 mmol/L)*.* En ausencia de hiperglucemia inequívoca los resultados deben repetirse con un segundo análisis. |
| Prediabetes | Presencia de:– Glucemia en ayunas alterada: Glucemia en ayunas entre 100 mg/dL (5,6 mmol/L) y 125 mg/dL (6,9 mmol/L), o– Intolerancia a la glucosa: Glucemia 2 horas tras SOG de 75g, entre 140 mg/dL (7,8 mmol/L) y 199 mg/dL (11,0 mmol/L), o– HbA1c entre 5,7 y 6,4% (39–47 mmol/mol). |
| Obesidad | IMC ≥ 30,0 kg/m2Obesidad grado I 30,0-34,9 kg/m2Obesidad grado II 35,0-39,9 kg/m2Obesidad grado III ≥ 40 kg/m2 |
| Sobrepeso | IMC ≥ 25,0 kg/m2 y < 30,0 kg/m2Grado I 25,1-27,5 kg/m2Grado II 27,6-30,0 kg/m2 |
| Normopeso | IMC 18,50-24,9 kg/m2 |
| Bajo peso | IMC < 18,5 kg/m2– Delgadez extrema < 16,0 kg/m2– Delgadez moderada 16,0-16,9 kg/m2– Delgadez leve 17,0-18,4 kg/m2 |
| Síndrome metabólico | Se requieren 3 de los siguientes 5 criterios:1. Perímetro abdominal elevado (≥ 94cm en varones y ≥80cm en mujeres de origen europeo).2. TGS ≥ 150 mg/dL (1,7 mmol/L) o en tratamiento con fármacos que reduzcan los TGS.3. cHDL < 40 mg/dL (1,0 mmol/L) en varones o < 50 mg/dL (1,3 mmol/L) en mujeres o en tratamiento con fármacos dirigidos a aumentar el cHDL.4. PA ≥ 130/85mmHg o en tratamiento con fármacos dirigidos a reducir la PA.5. Glucemia en ayunas ≥ 100 mg/dL o en tratamiento con fármacos antidiabéticos. |
| Fumador actual42 | Es la persona que ha fumado por lo menos un cigarrillo en los últimos seis meses. Dentro de este grupo se puede diferenciar:– Fumador diario: es la persona que ha fumado por lo menos un cigarrillo al día, durante los últimos seis meses.– Fumador ocasional: es la persona que ha fumado menos de un cigarrillo al día.Cuantificación del consumo de tabaco (índice paquetes / año): (N.° cigarrillos fumados al día x N.° años de fumador)/20. |
| Ex fumador | Es la persona que habiendo sido fumador se ha mantenido en abstinencia completa al menos los últimos seis meses. |
| Nunca fumador | Es la persona que nunca ha fumado o ha fumado menos de 100 cigarrillos en toda su vida. |
| Fumador pasivo | Es la persona que no fuma, pero que respira habitualmente el humo de tabaco ajeno o humo de segunda mano o humo de tabaco ambiental. |
| Lesión de órgano diana | – Rigidez arterial: Presión de pulso (en el anciano) ≥ 60mmHg o Velocidad de Onda de Pulso > 10 m/s.– Hipertrofia ventricular izquierda:- en el ECG (Índice Sokolow–Lyon > 3,5 mV; RaVL > 1,1 mV; producto voltaje por duración Cornell > 2440 mV*ms), o- ecocardiográfica (masa de ventrículo izquierdo > 115 g/m2 en varones o > 95 g/m2 en mujeres por área de superficie corporal).– Microalbuminuria (30–300 mg/24 h) o cociente albuminuria/creatinina (30–300 mg/g) o macroalbuminuria (> 300 mg/24 h). |
| Enfermedad vascular subclínica | Presencia de:– ITB < 0,9 (para algunos autores un valor > 1,4 es también patológico), o– Al menos una placa en arteria coronaria epicárdica, carótida o femoral, o– cuantificación de CAC: Agatston ≥ 300 unidades. |
| FG (ml/min/1,73 m2) en la ERC | Grado | FG | Definición |
| G1 | ≥ 90 | Normal. | |
| G2 | 60-89 | Ligero descenso del FG. | |
| G3a | 45-59 | Descenso ligero-moderado del FG. | |
| G3b | 30-44 | Descenso moderado del FG. | |
| G4 | 15-29 | Descenso grave del FG. | |
| G5 | < 15 | Fallo renal (prediálisis). | |
| Categorías de albuminuria (cociente albuminuria/ creatinina en mg/g) en la ERC | A1 | < 30 | Normal |
| A2 | 30-300 | Moderadamente elevada. | |
| A3 | > 300 | Muy elevada. |
Apo B: apolipoproteína B; CAC: calcio coronario; cLDL: colesterol-LDL; cHDL: colesterol-HDL; C-no-HDL: colesterol-no-HDL; DM: diabetes mellitus; ECG: electrocardiograma; ECVA: enfermedad cardiovascular aterosclerótica; ERC: enfermedad renal crónica; EVS: enfermedad vascular subclínica; FG: filtrado glomerular; GIM: grosor íntima-media; HbA1c: hemoglobina glucosilada; HDL: lipoproteínas de alta densidad; HTA: hipertensión arterial; IMC: índice de masa corporal; ITB: índice tobillo-brazo; LDL: lipoproteínas de baja densidad; LOD: lesión de órganos diana; PA: presión arterial; PAD: presión arterial diastólica; PAS: presión arterial sistólica; RaVL: voltaje de la onda R en la derivación aVL; SOG: sobrecarga oral de glucosa; TGS: triglicéridos.
Nota: Definición adaptada de las Sociedades Europeas de HTA y de Cardiología.
* En ausencia de hiperglucemia inequívoca los resultados deben repetirse con un segundo análisis.
Uno de los primeros pasos que hay que realizar al evaluar a pacientes con factores de riesgo es el cálculo del RCV, ya que hay determinadas decisiones que se tomarán en un sentido u otro según el nivel o valor del RCV, como, por ejemplo, el momento de iniciar tratamiento hipocolesterolemiante y su objetivo terapéutico.
El riesgo (absoluto) cardiovascular es la probabilidad de que ocurra un determinado episodio vascular en un periodo de tiempo definido en base a los FRCV que tiene el paciente que pertenece a un determinado grupo poblacional. Por lo tanto, no hay un sistema universal de cálculo del RCV. Las guías europeas de prevención cardiovascular18 y las de control de la dislipemia19, a las que se adhiere la SEA a través del CEIPV, recomiendan el uso del sistema SCORE45 para valorar el RCV en su versión para países de bajo RCV, en situación de prevención primaria, es decir, para individuos que aún no han tenido episodios cardiovasculares. Este sistema calcula el riesgo de muerte cardiovascular de causa aterosclerótica en un plazo de 10 años considerando los siguientes factores de riesgo: sexo, edad, tabaquismo, PAS y CT o c-noHDL.
Sistemas de cálculo de riesgo cardiovascularEn España se han utilizado mayoritariamente tres sistemas de estimación del RCV: uno cualitativo-ordinal (de la Guía Europea de Hipertensión8) y dos cuantitativos: el registre gironí del cor (REGICOR)46 y el SCORE45.
La guía de HTA utiliza un sistema que no cuantifica numéricamente el RCV, sino que identifica la categoría de riesgo: bajo, moderado, alto o muy alto.
El sistema REGICOR está derivado de una muestra de población de Girona mediante un modelo matemático procedente del estudio Framingham y validado en un conjunto de muestras españolas. Es un sistema cuantitativo como también lo es el SCORE, pero a diferencia de éste, valora el riesgo coronario fatal y no fatal.
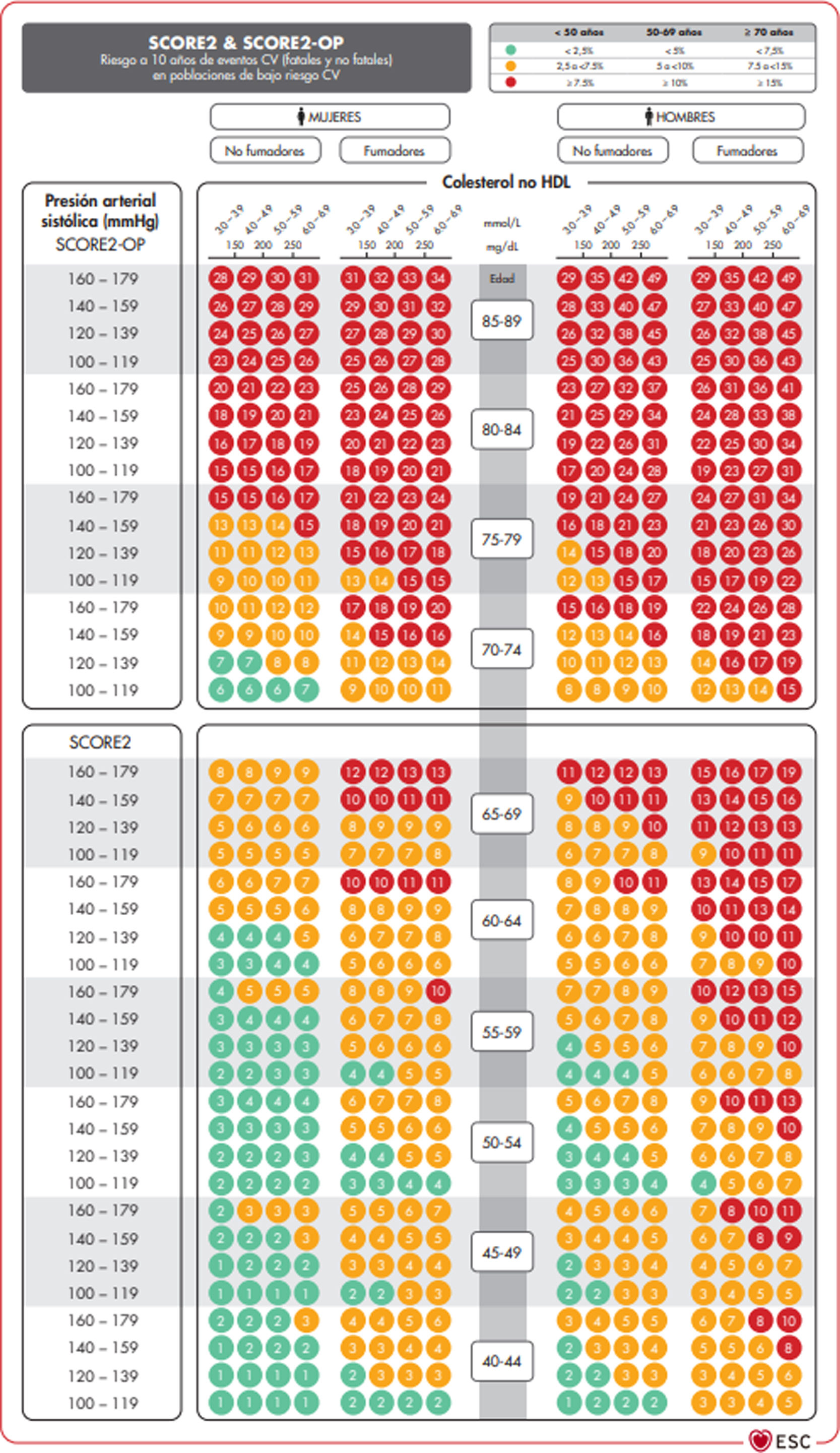
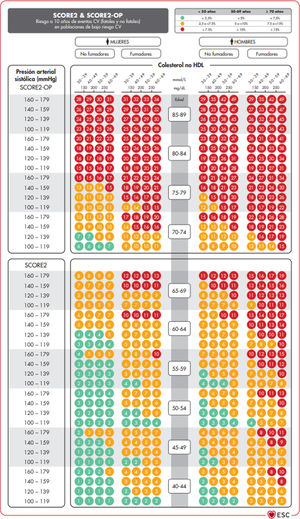
Proyecto SCORE y SCORE2En el marco del proyecto SCORE (Systematic COronary Risk Evaluation)45, se ha publicado recientemente una actualización de los índices de cálculo de riesgo (SCORE2)47,48. Dicha actualización introduce diferentes variaciones sobre el índice SCORE original: Se ha calculado el riesgo no tan solo de mortalidad cardiovascular sino de desarrollar un evento; el análisis se ha basado en el estudio de 45 cohortes de 43 países, incluyendo 677684 personas y 30121 episodios CV. Las variables que predicen el riesgo son sexo, edad, tabaquismo (dicotómica), PAS, y en este nuevo índice el parámetro lipídico incluido es el colesterol no HDL. No se incluye la DM dado que se considera «a priori» una condición de alto riesgo. La ecuación de riesgo está modulada por la incidencia de eventos cardiovasculares de cada país por lo que los índices finales están distribuidos en cuatro zonas: Riesgo bajo (en la que se incluye España); moderado; alto y muy alto; mostrando un claro gradiente este-oeste. Los valores son aplicables hasta los 70 años, habiéndose desarrollado por separado unas tablas específicas para personas de edad superior que alcanza hasta los 89 años (SCORE2-OP) (fig. 1).
Sistema SCORE2 y SCORE2-OP para países de bajo riesgo cardiovascular.
CV: Cardiovascular; SCORE2: Systematic Coronary Risk Estimation 2; SCORE2-OP: Systematic Coronary Risk Estimation 2-Older Persons.
Visseren et al.18. Reproduced by permission of Oxford University Press on behalf of the European Society of Cardiology. Material translated with their permission.
Con base en estos nuevos índices SCORE2 y SCORE2-OP el riesgo cardiovascular a 10 años se distribuye en tres categorías en tres franjas de edad:
Cálculo integral del riesgo cardiovascularEl cálculo general del RCV debe realizarse mediante una valoración integral del paciente que incluya no exclusivamente el valor del riesgo calculado con SCORE, sino integrando factores modificadores del riesgo, datos de lesión de órganos diana y la presencia de ECVA (tabla 5)8,14,18.
Estimación del riesgo cardiovascular
| Sin LOD1, EVS1 u otros factores moduladores del riesgo2 | Con LOD1, EVS1 u otros factores moduladores del riesgo2 | Presión arterial ≥ 180/110mmHg ocLDL ≥ 190 mg/dL (especialmente hipercolesterolemia familiar) | |
|---|---|---|---|
| – Sin ECVA, DM ni ERC | El estimado según SCORE | Incrementar en un escalón la categoría obtenida con el SCORE | Alto |
| – ERC grado 3 o– DM tipo 1 o 23 | Alto | Muy alto | Muy alto |
| – Enfermedad cardiovascular clínica o equivalente4– ERC grados 4 o 5– DM con 3 o más factores de riesgo; tipo 1 de más de 20 años de evolución | Muy alto | Muy alto | Muy alto |
| 1 Ir a tabla 4: Criterios diagnósticos. | |||
| 2 El incremento del riesgo depende del número e intensidad de los factores moduladores. En general se precisa de varios de ellos o de una extrema gravedad de los mismos para elevar la categoría de riesgo al mismo nivel que lo hacen la presencia de EVS o LOD:– Obesidad o sedentarismo– Individuos en situación de exclusión social– Intolerancia a la glucosa o glucemia en ayunas alterada.– Elevación de TGS, Apo B, Lp(a)– Antecedentes familiares de ECVA precoz.– Enfermedades que supongan aumento de estrés inflamatorio-metabólico: enfermedades autoinmunes, síndrome de apnea/hipopnea del sueño, síndrome metabólico, lupus eritematoso sistémico, psoriasis, cáncer, VIH.– Enfermedades psiquiátricas graves– Hígado graso no alcohólico | |||
| 3 Los pacientes con diabetes tipo 1 menores de 35 años o tipo 2 menores de 50 años, y con menos de 10 años de evolución, pueden tener un riesgo cardiovascular moderado. | |||
| 4 Se considera ECVA o equivalente a las siguientes condiciones:– ECVA clínica establecida:– Episodio coronario (infarto de miocardio, síndrome coronario agudo, angina estable, procedimiento de revascularización).– Episodio cerebrovascular: ictus o AIT.– EAP sintomática– Aneurisma de aorta abdominal– Insuficiencia cardiaca (IC) independiente de la FE.– ECVA evidente por técnicas de imagen, es decir, presencia de placa de ateroma significativa:– Mediante angiografía o TAC coronario (enfermedad multivaso con obstrucción > 50% de dos arterias epicárdicas)– Mediante ecografía carotidea o femoral (estenosis > 50%). | |||
AIT: ataque isquémico transitorio; Apo B: apolipoproteína B; cLDL: colesterol de lipoproteínas de baja densidad; DM: diabetes mellitus; EAP: enfermedad arterial periférica; ECVA: enfermedad cardiovascular aterosclerótica; ERC: enfermedad renal crónica; EVS: enfermedad vascular subclínica; FE: fracción de eyección; FRCV: factores de riesgo cardiovascular; HTA: hipertensión arterial; LOD: lesión del órgano diana; Lp(a): lipoproteína (a); TGS: triglicéridos.
Se aconseja seguir la estrategia de las guías europeas de prevención cardiovascular y de control de dislipemia, así como las de HTA, que clasifican a los sujetos en cuatro categorías de riesgo: bajo, moderado, alto y muy alto.
Hay situaciones que cualifican un riesgo alto o muy alto: HTA de grado 3, hipercolesterolemia con cLDL > 190 mg/dL, DM, lesión de órgano diana, enfermedad renal crónica (ERC) estadio 3 o mayor o ECVA establecida. En el resto de las situaciones nos manejaremos con el sistema SCORE. Si utilizamos la escala SCORE2 utilizaremos los puntos de corte indicados en el apartado anterior. La presencia de modificadores de riesgo supone incrementar una categoría de riesgo en caso de valores de riesgo próximos a una categoría superior.
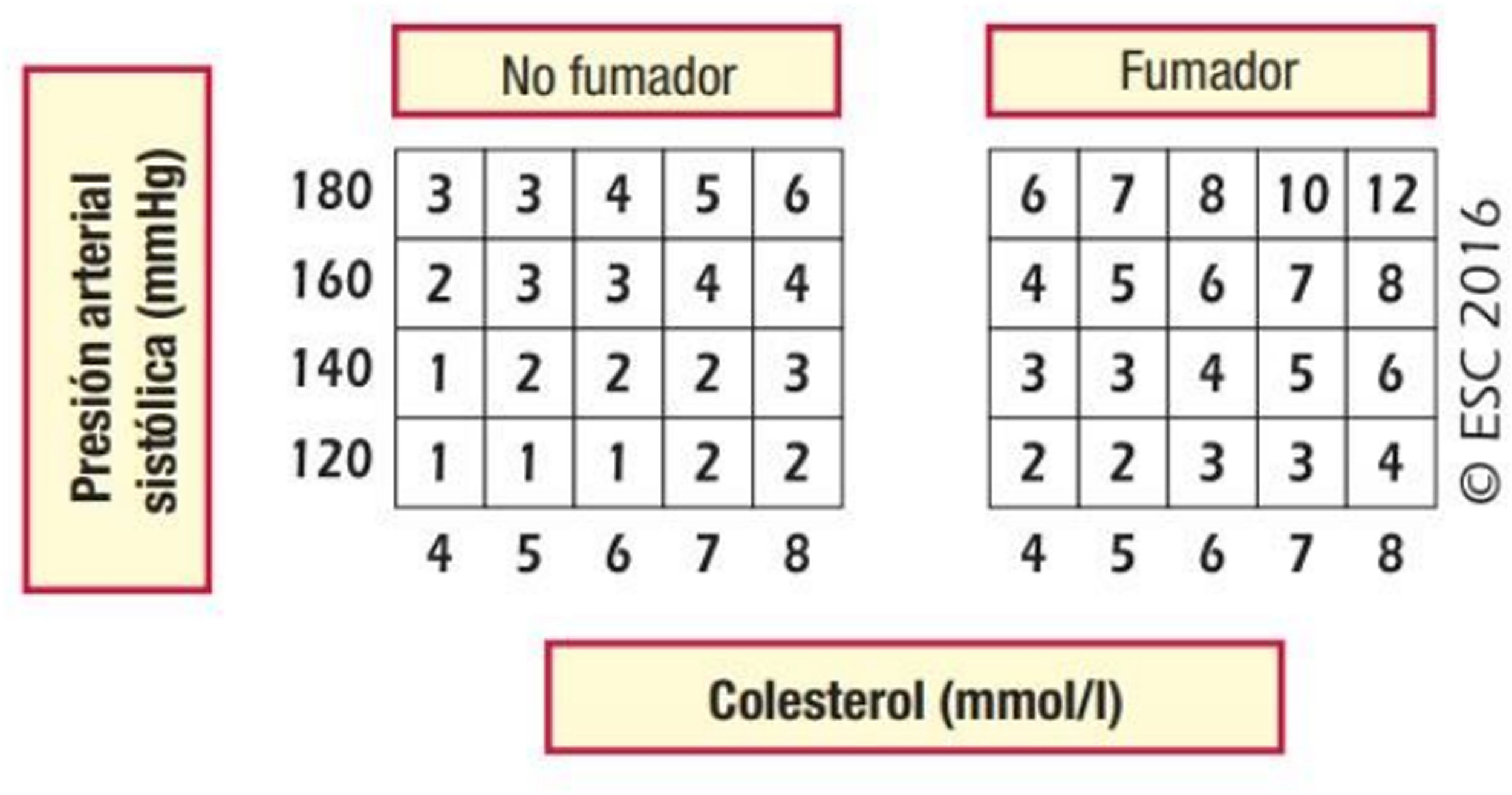
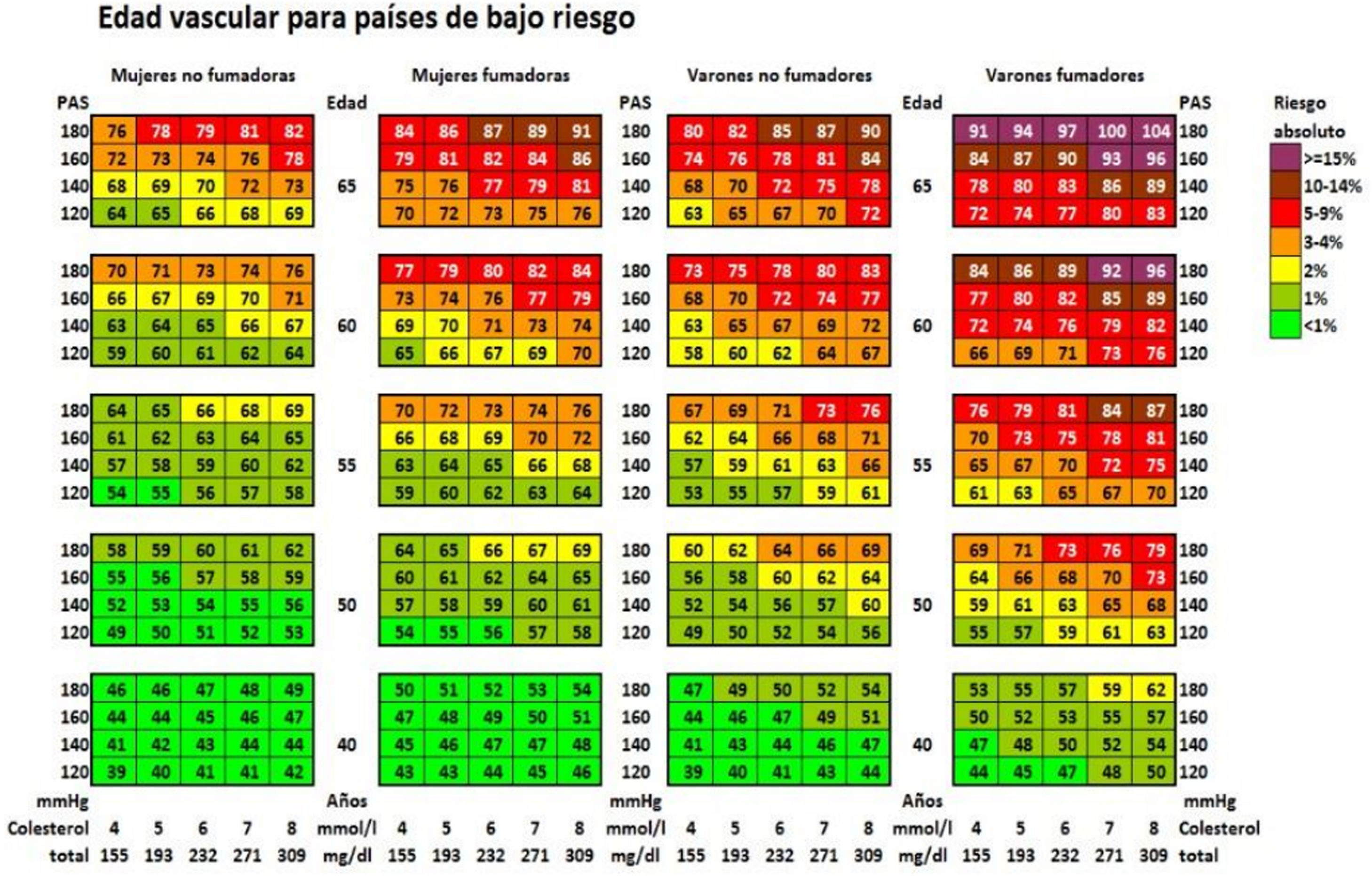
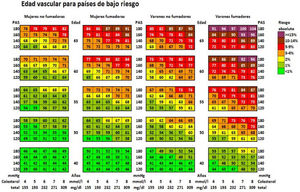
Edad cardiovascular y riesgo relativoEn los adultos jóvenes con elevación importante de múltiples FRCV se puede calcular el riesgo relativo (fig. 2) y la edad vascular49 (fig. 3). Comunicar al paciente su edad vascular es una forma de transmitir la información de su estado de RCV que se puede entender mejor que el valor matemático del riesgo absoluto. Los pacientes deben ser conscientes de su estado de riesgo para que adopten las medidas terapéuticas de estilos de vida y, si es el caso, farmacológicas.
Tabla de riesgo relativo.
PAS: Presión arterial sistólica.
Piepoli MF, Hoes AW, Agewall S et al., 2016 European Guidelines on cardiovascular disease prevention in clinical practice: The Sixth Joint Task Force of the European Society of Cardiology and Other Societies on Cardiovascular Disease Prevention in Clinical Practice (constituted by representatives of 10 societies and by invited experts) Developed with the special contribution of the European Association for Cardiovascular Prevention & Rehabilitation (EACPR), European Heart Journal 2016; 37 (29): 2315–2381 doi:10.1093/eurheartj/ehw106.
Reproduced by permission of Oxford University Press on behalf of the European Society of Cardiology. Material was translated with their permission.
Tabla de la edad vascular según SCORE para países de bajo riesgo cardiovascular.
PAS: Presión arterial sistólica; SCORE: Systematic Coronary Risk Estimation.
Cuende et al.49. Translated and reproduced by permission of Oxford University Press on behalf of the European Society of Cardiology.
Mediante la tabla de edad vascular derivada del SCORE se puede informar del riesgo absoluto y de la edad vascular. El cálculo de la edad vascular no precisa calibración por lo que puede ser aplicado a cualquier población general, no existiendo diferencias territoriales.
Tanto la edad vascular como el riesgo relativo se pueden aplicar a cualquier edad, y tienen más utilidad clínica para sujetos sin riesgo alto.
Derivado del concepto de edad vascular está la velocidad de envejecimiento vascular50, que relaciona la edad vascular y la cronológica.
Para pacientes con HF, que no aplican para las tablas habituales de cálculo del RCV, se han creado varias herramientas específicas. Una de ellas está basada en los datos de seguimiento de la Cohorte española SAFEHEART51. Esta ecuación tiene en cuenta diversos factores como la edad, tabaquismo, los niveles de cLDL en tratamiento, el IMC, la PA y los niveles de Lp(a) y permite discernir las diferencias en el riesgo en esta población específica tan importante en nuestras consultas. El registro de la SEA aporta otro instrumento de estratificación del RV en pacientes con HF en tratamiento con estatinas basado en la presencia de otros FRCV (sexo masculino, obesidad, HTA, diabetes), niveles máximos de cLDL y test genético positivo para HF52. Por último, en pacientes con fenotipo de HF, se ha desarrollado una herramienta para el cálculo de riesgo: el SIDIAP-FH con mejor capacidad predictiva tanto en prevención primaria como en secundaria53.
Recomendaciones generales para el control del riesgo cardiovascularRecomendaciones generales a la población para reducir su riesgo cardiovascularEl grupo de trabajo de Nutrición y Estilo de Vida de la SEA dispone de un detallado documento de consenso54, que aporta evidencias útiles y jerarquizadas, que sirven de herramienta a los profesionales de la salud para ayudar a sus pacientes, partiendo del concepto de que las recomendaciones saludables deben ser las mismas para el control de cualquier factor de riesgo y para la prevención primaria y secundaria de las ECVA. En él se resume la evidencia acumulada sobre componentes del estilo de vida como la dieta y el ejercicio físico54. Además, se hace un especial hincapié, no en el consumo de nutrientes aislados, sino en el de alimentos y, sobre todo, en el de los patrones alimentarios más importantes para la prevención cardiovascular. Este concepto de patrón alimentario se ha afianzado en los últimos años, como modelo para examinar la relación entre nutrición y salud y para servir de herramienta educativa para la población, modificando el paradigma tradicional de que la unidad nutricional básica de la dieta no son los nutrientes (por ejemplo los ácidos grasos), sino los alimentos que los contienen (aceites, frutos secos, carnes rojas, productos lácteos, etc.), ya que en sus matrices existen multitud de componentes capaces de interaccionar sinérgicamente o de modo antagónico sobre vías metabólicas determinantes para la salud cardiovascular. En esta guía recopilamos las principales recomendaciones del referido documento54.
Las diferentes dietas saludables tienen muchos componentes en común, algunos de ellos recomendables, como las frutas, las verduras, los frutos secos, las legumbres y el pescado, mientras que otros se deben restringir, como algunos alimentos ricos en grasa saturada, los que tienen azúcar añadido, abundante sal o han sido procesados. Hay una fuerte evidencia de que los patrones alimentarios de base vegetal, bajos en ácidos grasos saturados, colesterol y sodio, con un alto contenido en fibra, potasio y ácidos grasos insaturados, son beneficiosos y reducen la expresión de los FRCV. En este contexto destacan la dieta mediterránea, la dieta dietary approaches to stop hypertension (DASH), la dieta vegano-vegetariana y el Índice de Alimentación Saludable Alternativo, todos de base vegetal y con abundantes hidratos de carbono complejos. Los datos de grandes estudios de cohortes y, en el caso de la dieta mediterránea, el estudio clínico aleatorizado PREDIMED, indican que la adherencia a estos patrones de alimentación confiere un claro beneficio cardiovascular55. Por el contrario, la dieta baja en grasas está actualmente en entredicho por su escaso potencial de protección cardiovascular. Con relación a las grasas comestibles, el aceite de oliva virgen es la grasa culinaria más eficaz en la prevención de las ECVA56. La intervención nutricional durante unos cinco años, en el estudio PREDIMED, demostró que los participantes asignados a la dieta mediterránea suplementada con aceite de oliva virgen extra o con frutos secos experimentaron una reducción media del 30% de episodios cardiovasculares mayores55, aparte de otros efectos beneficiosos, entre ellos la reducción del riesgo de DM2 y de fibrilación auricular (FA)57. Es importante destacar que las margarinas actuales carecen en su mayoría de ácidos grasos trans y aportan ácidos grasos poliinsaturados n-6 y n-3.
El consumo de pescado o marisco al menos tres veces por semana, dos de ellas en forma de pescado azul, reduce el RCV. Por ello, incentivar su consumo es un importante componente de las modificaciones de estilo de vida para la prevención de la ECVA. Un beneficio nada desdeñable podría obtenerse cuando sustituye a la carne como plato principal en las comidas. Aun así, el documento antes indicado destaca que, por su riqueza en contaminantes marinos, los niños y mujeres en edad fértil no deben consumir pescado graso de gran tamaño (atún rojo, pez espada, tiburón), o la caballa porque contienen más contaminantes que especies más pequeñas. Las evidencias sobre las carnes indican que el consumo de carne blanca o carne magra (sin grasa visible), tres a cuatro raciones por semana, no incrementa el RCV, a diferencia del consumo de carnes procesadas (beicon, salchichas, embutidos) que contienen aditivos perjudiciales, como sal y nitratos, que incrementa la mortalidad total y el desarrollo de DM2 y ECVA.
Con relación a los lácteos, es deseable consumir al menos dos raciones diarias (leche, leche fermentada, queso, yogur, etc.), por su importante papel nutricional en el metabolismo del calcio y por su riqueza en proteínas de alta calidad biológica. La restricción de lácteos enteros no parece ser una estrategia adecuada para la reducción del RCV, aunque sí se desaconseja el consumo habitual de lácteos con azúcares añadidos. Para la prevención cardiovascular es recomendable reducir el consumo de grasa láctea concentrada, como la mantequilla y la nata. En la última década las recomendaciones sobre el consumo de huevos y la salud han sido discrepantes, en gran medida por falta de evidencia. Sin embargo, la evidencia científica actual sugiere que su consumo no es perjudicial en el contexto de una dieta saludable. Tanto la población general sana, como las personas con FRCV, ECVA previa o DM2, pueden consumir hasta un huevo al día sin temor por su salud cardiometabólica. En los pacientes con DM2 tampoco parece haber suficientes argumentos para restringir su consumo con el objeto de reducir el RCV o mejorar el control metabólico, aunque algunas series que limitan su ingesta a un máximo de tres a la semana58.
Las legumbres y cereales de grano completo son semillas que contienen múltiples nutrientes saludables y su consumo frecuente se asocia con reducción de factores de riesgo y de ECVA. Para promover la salud cardiovascular y disminuir la colesterolemia es recomendable consumir una ración de legumbres al menos cuatro veces por semana. El consumo recomendado de cereales integrales es de unas cuatro raciones/día, incluyendo pan en todas las comidas del día, pasta doa a tres veces/semana y arroz dos a tres veces/semana. En cuanto al consumo de frutas y verduras, con las evidencias existentes, se recomienda el consumo de cuatro a cinco raciones diarias entre frutas y verduras dado que reduce la mortalidad global y cardiovascular. Además, el efecto beneficioso de frutas y verduras es dosis dependiente y es más evidente sobre la enfermedad cerebrovascular que sobre la enfermedad coronaria. El consumo de tubérculos (sobre todo, patatas) no se asocia con un aumento del RCV excepto si son fritas en aceites no recomendables y saladas.
El consumo frecuente de frutos secos se asocia con la reducción de ECVA, sobre todo enfermedad coronaria, y mortalidad por cualquier causa55. Consumir con frecuencia (a diario o al menos tres veces por semana) un puñado de frutos secos (equivalente a una ración de 30 g) es muy recomendable para el control del colesterol y la salud en general. Se aconseja consumirlos crudos y sin pelar (no tostados ni salados) si es factible, ya que la mayor parte de los antioxidantes están en la piel. Para mantener el efecto saciante y evitar ganar peso, deben consumirse durante el día, no como postre después de cenar. Entre los frutos secos que se recomienda consumir se incluyen las avellanas, nueces, almendras, pistachos, anacardos, macadamias, piñones, etc. Si bien los cacahuetes no son realmente frutos de un árbol sino legumbres, su composición general y alto contenido en ácidos grasos insaturados los asimila a los frutos secos, tanto desde el punto de vista nutricional como por sus efectos biológicos.
El cacao es una semilla con abundantes nutrientes y el consumo de su principal derivado, el chocolate, mejora los factores de riesgo y se asocia con reducción de ECVA, accidente cerebrovascular (ACV) y DM2. Hay información que indica que tiene efectos hipocolesterolemiantes y antihipertensivos, mejorando la resistencia a la insulina, de forma que puede consumirse chocolate negro ≥ 70% sin azúcar añadido en el contexto de una dieta saludable. Además, se aconseja hacerlo durante el día y no por la noche después de cenar, cuando el efecto saciante no se puede compensar ingiriendo menos alimentos en la comida siguiente.
Las bebidas azucaradas forman parte de la dieta habitual de muchas personas y pueden suponer hasta un 20% del consumo calórico diario, favoreciendo un aumento de ECVA, de obesidad y de DM2. La sustitución de este tipo de bebidas por agua sería muy importante para reducir el consumo energético y el riesgo de estas patologías y sus complicaciones. Si el paciente no acepta dicha sustitución, podemos recurrir a las bebidas con edulcorantes artificiales mientras no tengamos una evidencia científica de primer nivel sobre su inocuidad. El consumo de bebidas alcohólicas de cualquier tipo aumenta el cHDL y su ingesta moderada (de bebidas fermentadas no destiladas), en comparación con la abstención o el consumo excesivo, se asocia con una reducción de ECVA y mortalidad cardiovascular. Se puede permitir su consumo moderado siempre con las comidas y en el marco de una dieta saludable como la dieta mediterránea, siendo diferentes las recomendaciones para hombres y mujeres, ya que éstas son más sensibles a los efectos del alcohol. No se debe promover el consumo de alcohol en las personas que habitualmente no lo hacen. El café (tanto el normal como el descafeinado) y el té son ricos en polifenoles y hay evidencias de alto nivel de que su consumo habitual se asocia con reducción de ECVA.
Existen numerosos alimentos funcionales (nutracéuticos) dirigidos a reducir el RCV, principalmente por reducción de la colesterolemia. La eficacia hipocolesterolemiante de los esteroles vegetales y los preparados de fibra soluble, a nivel intestinal, ha sido ampliamente demostrada. La monacolina es un componente presente en la levadura roja de arroz que también reduce el colesterol pues tiene la misma estructura química que la forma activa de la lovastatina. Así mismo, existen evidencias consistentes de que los ácidos grasos omega-3 a dosis farmacológicas disminuyen los TGS plasmáticos.
El consumo excesivo de sal se asocia con ECVA y mortalidad de causas cardiometabólicas. Debe recomendarse una dieta baja en sal (< 5 g/día) a nivel poblacional y con mayor justificación en pacientes hipertensos y sus familiares, recordando que para calcular la cantidad de sal total hay que multiplicar por 2,5 el contenido de sodio de los alimentos. Medidas especialmente eficaces para este fin son limitar el consumo de alimentos ricos en sal, como precocinados, enlatados, salazones, embutidos y bebidas carbónicas. Una alternativa a la sal es utilizar zumo de limón, ajo o hierbas aromáticas.
La actividad física es, según la Organización Mundial de la Salud (OMS), cualquier movimiento corporal producido por los músculos esqueléticos y que exija gasto de energía. Cuando se realiza de forma regular y mantenida protege del RCV y mejora sus factores de riesgo. Su práctica debe adaptarse a las particularidades propias de cada individuo, partiendo del principio de que poco es mejor que nada y considerando que abarca actividades como las que se realizan durante el trabajo, las formas de transporte activas, las tareas domésticas o de actividades recreativas. A su vez el ejercicio físico es una variedad de la actividad física pero que se realiza de forma planificada, estructurada, repetitiva y realizada con un objetivo relacionado con la mejora o el mantenimiento de la aptitud física. Ambos se deben hacer de forma pausada y moderada, más que intensa y concentrada.
Es razonable pensar, y así lo muestran evidencias recientes, que no exista un modelo estándar de dieta saludable, sino que la respuesta biológica varía entre las personas, especialmente por diferencias individuales en el genoma y en el microbioma. En los próximos años, la nutrición personalizada y de precisión, junto con otras ciencias como la cronobiología, en la que cada uno adopte la dieta que le sea personalmente más beneficiosa serán un reto de la comunidad científica59. Finalmente, uno de los problemas más complejos de la relación entre las personas y su dieta es la adherencia, que depende de factores muy diferentes, como los propios del paciente, la familia, el equipo de salud que le acompaña y el propio sistema sanitario. Por ello, es fundamental poner en marcha las estrategias para conseguirlo.
La tabla 6, recogida de dicho documento54, incluye de forma práctica la frecuencia en la forma y en la cantidad de consumo de alimentos.
Frecuencia en la forma y en la cantidad de consumo de alimentos
| Frecuencia de consumo | Diario | Tres veces por semanamáximo | Desaconsejado u ocasional |
|---|---|---|---|
| Grasas comestibles | Aceite de oliva, preferentemente virgen | Margarina | Freír con aceites de semillas |
| Huevos | No se desaconsejan los huevos enteros | Pacientes con diabetes | |
| Pescadoa | Azul o blanco | Marisco | Pescado en salazón, ahumados. |
| Carnesb | Volatería y conejo | Carnes rojas magras | Carnes procesadas y embutidos |
| Productos lácteos | Leche y yogur semidesnatados o desnatados (sin azúcar).Quesos frescos | Leche y yogur enteros (sin azúcar)Quesos curados | Mantequilla, nataQuesos curados en pacientes hipertensos |
| Legumbres y cereales | Cereales integrales, legumbres | Arroz, pasta | Cereales de harina refinada |
| Frutos secos y cacahuetes | Crudos (30 a 45 g) | Tostados | Salados |
| Chocolate | Negro con cacao ≥ 70% | Negro con cacao< 70% | Chocolate con leche y blanco |
| Café y té | Té sin limitación. Café hasta cinco diarios, sin azúcar. | ||
| Frutas, verduras, féculas | 4-5 raciones combinando los distintos tipos de frutas y verduras | Alimentos ricos en féculas (patatas) | Zumos de fruta comerciales y patatas fritas comerciales |
| Bebidas alcohólicas | Limitar a 30g de alcohol en hombres bebedores y 15g en mujeres. Preferentemente bebidas fermentadas (vino, cerveza) con las comidas. | No aconsejable en los no bebedores | |
| Productos conazúcares añadidos | Evitar cualquier alimento con azúcar añadido | ||
| Preparación de los alimentosc | Preferiblemente cocidos, a la plancha o rehogados. | Alimentos fritos en aceite de oliva virgen | Evitar ahumados, procesados y fritos con aceites refinados |
| Sal | Entre 2,5 y 4g diarios | Salazones |
Las carnes, fuente importante de proteínas animales, deben alternarse con el pescado consumiendo una de estas opciones al día. Es preferible la carne blanca que la carne roja
El consumo de platos aderezados con salsa de tomate, ajo, cebolla o puerro elaborada a fuego lento con aceite de oliva virgen (sofrito) puede realizarse a diario
Publicado con permiso del editor. Fuente original: Pérez-Jiménez et al.54.
Una manera de evaluar la adherencia a la dieta mediterránea se puede obtener utilizando el cuestionario MEDAS (Anexo 4).
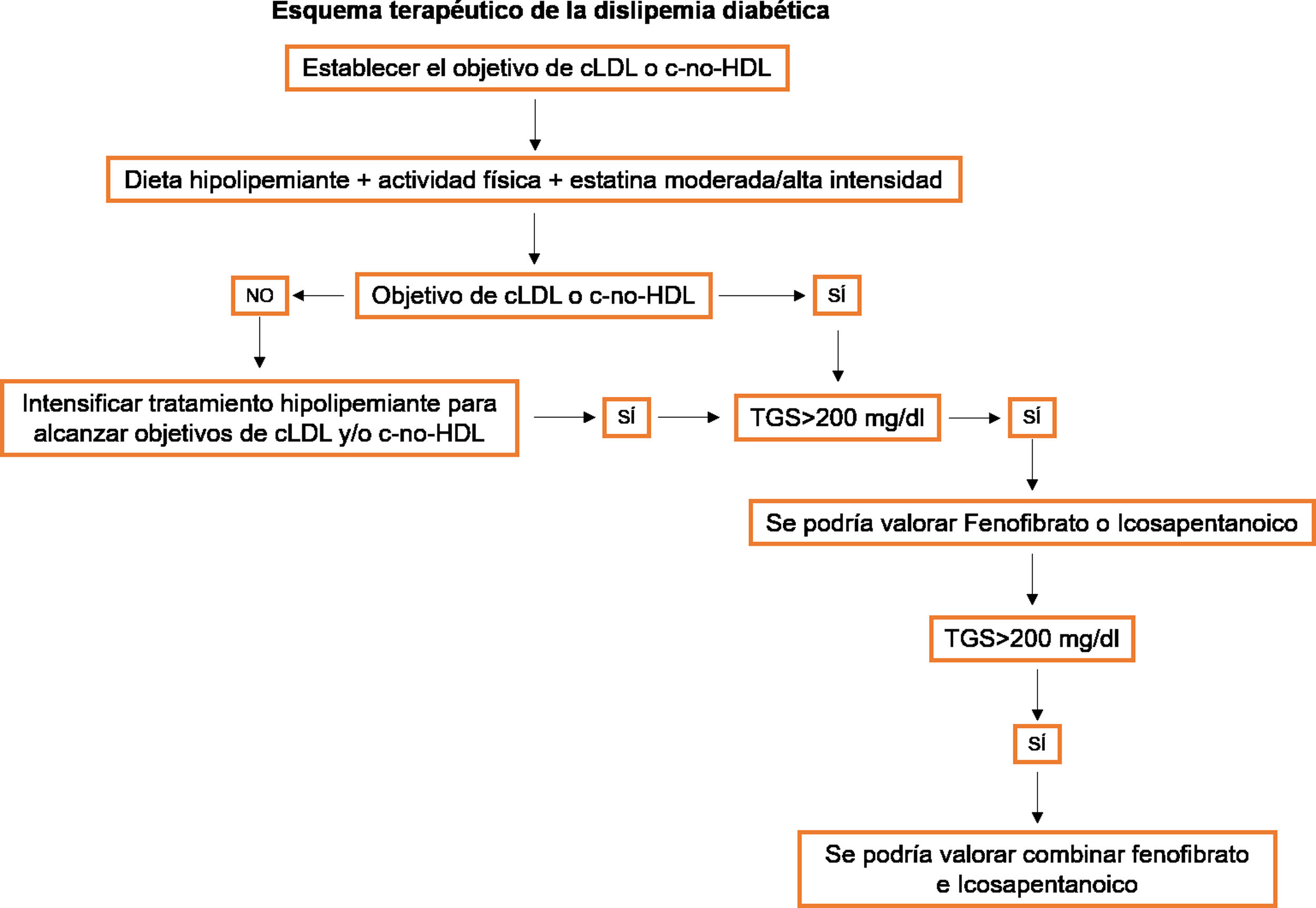
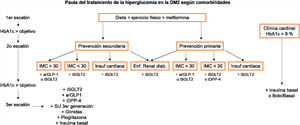
Recomendaciones farmacológicas generales en pacientes en prevención primariaLas recomendaciones de manejo clínico del RCV en pacientes sin ECVA, DM ni insuficiencia renal crónica (IRC) se recogen en la figura 4.
Antiagregantes plaquetariosSe ha demostrado que el tratamiento con dosis bajas de ácido acetilsalicílico reduce el riesgo de complicaciones vasculares, principalmente en personas de mediana edad, a expensas de la reducción de los infartos de miocardio no fatales, sin afectar al riesgo de ictus ni a la mortalidad. Sin embargo, parte del beneficio del ácido acetilsalicílico puede perderse por sus efectos adversos, sobre todo los relacionados con su potencial hemorrágico, de ahí que el balance de riesgos y beneficios de las dosis bajas de ácido acetilsalicílico no estén claramente establecidos en prevención primaria.
Las guías norteamericanas de la US preventive service task force (USPSTF)60 recomiendan iniciar el uso de ácido acetilsalicílico a dosis bajas (dosis de 100 mg/día o inferior) para la prevención primaria de la ECVA en adultos de 50 a 59 años que tengan un riesgo de morbi-mortalidad cardiovascular mayor o igual a 10% a 10 años, que no tengan aumentado el riesgo de hemorragia, que tengan una expectativa de vida de al menos 10 años, y que estén dispuestos a tomar este tratamiento diariamente durante al menos 10 años. La decisión de iniciar tratamiento en adultos de entre 60 y 69 años con un RCV mayor o igual a 10% a 10 años debe ser individualizada60.
Sin embargo, las guías europeas para la prevención cardiovascular de 202118 no recomiendan sistemáticamente el tratamiento antiagregante para pacientes sin ECVA, debido al aumento del riesgo de sangrado mayor. En este sentido, recientemente se han publicado varios ensayos clínicos con ácido acetilsalicílico en prevención primaria, tanto en diabéticos como en no diabéticos, no encontrando un beneficio claro en su utilización en la prevención primaria de la enfermedad cardiovascular61–63, y en especial cuando se controlan adecuadamente los FRCV presentes.
Tratamiento hipolipemianteEn numerosos ensayos clínicos y metaanálisis64, las estatinas han demostrado reducir los episodios cardiovasculares en pacientes sin ECVA, incluso con concentraciones no elevadas de colesterol. La reducción del riesgo relativo de ECVA con las estatinas es independiente del RCV basal, pero para que el tratamiento sea eficiente es importante seleccionar a los pacientes con un alto RCV basal para que la reducción absoluta del RCV sea mayor (tabla 5).
Las indicaciones de tratamiento hipolipemiante en prevención primaria se exponen en el apartado de Recomendaciones terapéuticas específicas.
Suplementos vitamínicosMuchos estudios observacionales prospectivos de casos y controles han observado asociaciones inversas entre la ingesta o las concentraciones séricas de vitaminas (A, grupo B, C, D y E) y el riesgo de ECVA. Sin embargo, los datos de estudios prospectivos y los ensayos clínicos de intervención con suplementos vitamínicos y minerales no han demostrado ningún beneficio cardiovascular65. Por lo tanto, no está indicado el empleo de suplementos vitamínicos para la prevención de la ECVA.
Recomendaciones generales en pacientes con enfermedad vascular subclínica y en prevención secundariaLos pacientes con enfermedad vascular subclínica diagnosticada mediante la presencia de placas en arteria carótida o femoral o mediante la determinación de CAC, tienen un riesgo de complicaciones cardiovasculares intermedio entre los sujetos en prevención primaria y secundaria, si bien en numerosas guías los clasifican como prevención secundaria. En estas circunstancias, su manejo no diferiría del de los sujetos en prevención secundaria, si bien las evidencias de eficacia del tratamiento con antiagregantes son limitadas. Por ejemplo, en pacientes con ITB bajo, pero sin claudicación intermitente, el tratamiento con antiagregantes no ha demostrado ser eficaz66. En cualquier caso, su nivel de riesgo debe estimarse en función de lo recogido en la tabla 5.
En los pacientes en prevención secundaria, además de las medidas higiénico-dietéticas previamente comentadas (ver Recomendaciones generales a la población para reducir su riesgo cardiovascular) y de los tratamientos indicados para el control de los FRCV, existen una serie de tratamientos que han demostrado reducir el riesgo de nuevos episodios cardiovasculares (tabla 7).
Medidas farmacológicas que han demostrado reducir la tasa de complicaciones cardiovasculares en sujetos en prevención secundaria
| Tratamiento | Indicaciones potenciales |
|---|---|
| Antiagregantes | – Aspirina a dosis bajas o clopidogrel en pacientes con enfermedad coronaria, cerebrovascular o arterial periférica.– Aspirina más clopidogrel tras un AIT o ictus leve67,68.– Aspirina y dipiridamol estaría también indicado en sujetos con ictus o AIT previos.– Aspirina más un inhibidor de P2Y12 en sujetos con síndrome coronario agudo o con colocación de stent, mantenido al menos 12 meses. |
| Hipolipemiantes | – Estatinas asociadas o no a ezetimiba para reducir el cLDL por debajo de 55 mg/dL o, al menos, un 50% su concentración.– iPCSK9 si no se consiguen las reducciones adecuadas con el tratamiento hipolipemiante previo, y de acuerdo con los criterios de la tabla 10.– Fibratos si triglicéridos > 200 mg/dL y cHDL reducido, una vez controlado el cLDL con estatinas en pacientes de muy alto RCV.– Ácidos grasos omega-3 (EPA purificado 4 g/día) a dosis elevadas en hipertrigliceridemias > 200 mg/dl que persisten a pesar del tratamiento con estatinas en pacientes de alto RCV69. |
| Suplementos vitamínicos o nutricionales | – Sin indicación |
| Bloqueo SRA | Si cardiopatía isquémica y:– FE ≤ 40% o– Insuficiencia cardiaca o– DM o– Hipertensión arterial |
| Beta bloqueantes | – FE ≤ 40% |
| Inhibidores de la aldosterona | – FE ≤ 40% |
| Inhibidores de la neprilisina | – Insuficiente control de la disfunción del ventrículo izquierdo |
AIT: ataque isquémico transitorio; cLDL: colesterol-LDL; DM: diabetes mellitus; EPA: ácido eicosapentanoico; FE: fracción de eyección; iPCSK9: inhibidor de la convertasa de proteínas subtilisina/kexina 9; P2Y12: quimiorreceptor para adenosín difosfato; SRA: sistema renina-angiotensina
El ácido acetilsalicílico es el antiagregante plaquetario más estudiado en la prevención cardiovascular a largo plazo en pacientes con infarto agudo de miocardio, ictus isquémico o EAP. En un metaanálisis de 16 estudios clínicos que incluían a más de 17.000 pacientes, el tratamiento con ácido acetilsalicílico redujo significativamente los episodios cardiovasculares mayores (coronarios y cerebrovasculares) y la mortalidad total70. Asimismo, el tratamiento con ácido acetilsalicílico se asoció con un exceso significativo de sangrados mayores; no obstante, los beneficios cardiovasculares del ácido acetilsalicílico superaron claramente el riesgo de sangrado.
El clopidogrel tiene un efecto similar al ácido acetilsalicílico en pacientes con infarto de miocardio o ictus isquémicos, pero puede ser superior a esta en sujetos con EAP. La asociación de ácido acetilsalicílico y clopidogrel en prevención secundaria disminuye significativamente los episodios cardiovasculares graves en comparación con el ácido acetilsalicílico solo, pero también incrementa significativamente el riesgo de sangrado.
En pacientes con ACV isquémico no cardioembólico o AIT, el ácido acetilsalicílico se puede usar en monoterapia o asociada a dipiridamol, y también se puede utilizar el clopidogrel en solitario. En pacientes con un AIT o ictus menor, el beneficio del doble tratamiento antiagregante durante un máximo de 90 días supera los riesgos de aumento de sangrado67,68. La protección ocurre durante los primeros 21 días, por lo que ésta sería la duración recomendable para el doble tratamiento71.
El tratamiento estándar para un paciente que ha sufrido un síndrome coronario agudo, con o sin la colocación de stents, es la doble antiagregación plaquetaria (ácido acetilsalicílico con un inhibidor de quimiorreceptor para adenosín difosfato [P2Y12]) durante 12 meses. En pacientes con alto riesgo de sangrado, el tiempo con la doble antiagregación se puede reducir hasta uno a tres meses.
HipolipemiantesNumerosos ensayos clínicos y metaanálisis64 han demostrado que el tratamiento con fármacos hipolipemiantes (resinas, estatinas, ezetimiba, inhibidores de convertasa de proteínas subtilisina/kexina 9 [iPCSK9]) en pacientes con ECVA establecida disminuye los episodios cardiovasculares graves y la mortalidad.
Los datos de las guías19 indican que los pacientes con enfermedad cardiovascular subclínica establecida (enfermedad coronaria multivaso demostrada mediante la obstrucción > 50% en al menos dos arterias epicárdicas en TAC coronario o angiografía, o mediante la presencia de placas carotídeas) deben considerarse de muy alto RCV y ser tratados como si hubieran tenido previamente un episodio cardiovascular. Las recomendaciones de tratamiento hipolipemiante en estos sujetos se recogen en el apartado de Recomendaciones terapéuticas específicas.
Otros fármacosLos suplementos de ácidos grasos omega-3 pueden reducir la mortalidad cardiovascular, a través de la reducción de las muertes súbitas cardiacas en pacientes con enfermedad coronaria previa. Por ello, su utilización puede ser razonable en la prevención secundaria de la cardiopatía isquémica, en particular en los pacientes con un consumo insuficiente de pescado72. En pacientes en prevención secundaria o diabéticos de alto riesgo en tratamiento con estatinas (cLDL medio de 75 mg/dL y TGS entre 150-499 mg/dL), el tratamiento con 4 g de EPA redujo un 25% el riesgo de episodios cardiovasculares graves69.
En pacientes con cardiopatía isquémica y disfunción del ventrículo izquierdo (fracción de eyección ventricular izquierda (FEVI) ≤ 40%), insuficiencia cardiaca (IC), DM o HTA, estaría indicado el tratamiento con un inhibidor de la enzima convertidora de la angiotensina (IECA), o con un bloqueador del receptor de la angiotesina II si hubiera intolerancia.
En pacientes con cardiopatía isquémica y disfunción del ventrículo izquierdo (FEVI ≤ 40%) estaría también indicado el tratamiento con betabloqueadores y con antagonistas del receptor mineralocorticoide, siempre que no haya contraindicación.
Así mismo, en casos seleccionados, si no se consigue un control suficiente de la disfunción del ventrículo izquierdo, puede utilizarse sacubitrilo-valsartán, en el que el sacubitrilo, un inhibidor de la neprilisina, que aumenta la actividad de los péptidos natriuréticos, está asociado a un bloqueador del receptor de la angiotensina II, ya que ésta aumenta por efecto de aquel compuesto73.
No existen evidencias de que el descenso de la homocisteína con suplementos de ácido fólico o vitamina B12 disminuya el riesgo de ECVA en prevención secundaria.
La utilización en un mismo comprimido de ácido acetilsalicílico, una estatina y un inhibidor del enzima convertidor de la angiotensina facilita la adherencia al tratamiento en pacientes en prevención secundaria74.
Recientemente, se ha valorado la intervención sobre el estado inflamatorio. El uso de un anticuerpo monoclonal anti-IL-1β, canakinumab, redujo significativamente la tasa de recurrencia de ECVA, mostrando beneficio pese al ligero incremento de infecciones severas y fatales75. Sin embargo, no ha sido aprobado por la administración norteamericana porque en el estudio CANTOS75 no se enfrentó a terapia máxima que incluyese ezetimiba o iPCSK9 y se asociaba a un aumento del riesgo de infecciones graves. La colchicina es un fármaco con acciones anti-inflamatorias que a dosis de 0,5 mg al día o cada 12 horas, ha demostrado reducir en un 32% la tasa de complicaciones cardiovasculares, sin diferencias significativas en los efectos secundarios76.
Recomendaciones terapéuticas específicasPacientes con dislipemiaPacientes con hipercolesterolemiaTodo paciente con hipercolesterolemia debe recibir una dieta baja en grasas de origen animal, de tipo mediterráneo, de acuerdo con las recomendaciones sobre alimentación de la SEA (tabla 6). La indicación de tratamiento hipolipemiante se basa en la concentración de cLDL y el RCV global basal. Recomendamos el uso de tratamiento hipolipemiante orientado a obtener al menos los objetivos cLDL, por ello hacemos énfasis en el uso de terapias hipocolesterolemiantes de alta intensidad, en las que las estatinas deben estar incluidas, según la tabla 8.
Terapias hipolipemiantes clasificadas según su intensidad hipocolesterolemiante
| Baja intensidadcLDL <- 30% | Moderada intensidadcLDL > 30% < 50% | Alta intensidadcLDL > 50% < 60% | Muy alta intensidadcLDL > 60% < 80% | Extremadamente alta intensidadcLDL > 80% < 85% | |
|---|---|---|---|---|---|
| Monoterapia oral | Simvastatina 10Pravastatina 10-20Lovastatina 10-20Fluvastatina 40Pitavastatina 1Ezetimiba 10 | Atorvastatina 10-20Rosuvastatina 5-10Simvastatina 20-40Pravastatina 40Lovastatina 40Fluvastatina 80Pitavastatina 2-4 | Atorvastatina 40-80Rosuvastatina 20-40 | ||
| Terapia combinada oral | Simvastatina 10 + Ezetimiba 10Pravastatina 20 + Ezetimiba 10Lovastatina 20 +Ezetimiba 10Fluvastatina 40 + Ezetimiba 10Pitavastatina 1 +Ezetimiba 10 | Atorvastatina 10-20 + Ezetimiba 10Rosuvastatina 5-10 + Ezetimiba 10Simvastatina 20-40 + Ezetimiba 10Pravastatina 40 + Ezetimiba 10Lovastatina 40 +Ezetimiba 10Fluvastatina 80 + Ezetimiba 10Pitavastatina 2-4 + Ezetimiba 10 | Atorvastatina 40-80 + Ezetimiba 10Rosuvastatina 20-40 + Ezetimiba 10 | ||
| Terapia combinada oral + subcutánea | Alirocumab 75 | Alirocumab 150Evolocumab 140Atorvastatina 10-20 + Alirocumab/EvolocumabRosuvastatina 5-10 + Alirocumab/ EvolocumabSimvastatina 40 +Alirocumab/Evolocumab | Atorvastatina 40-80 +Alirocumab/EvolocumabRosuvastatina 20-40 +Alirocumab/EvolocumabAtorvastatina 40-80 + Ezetimiba 10 +Alirocumab/EvolocumabRosuvastatina 20-40 + Ezetimiba 10 +Alirocumab/Evolocumab |
Masana et al., 202077.
La eficacia de los fibratos para reducir el colesterol suele ser moderada (tabla 9).
Paciente de riesgo cardiovascular bajo-moderadocLDL entre 115 y 190 mg/dLHace referencia a pacientes en prevención primaria, no diabéticos, con función renal preservada y un RCV según las tablas de SCORE inferior al 5% en 10 años sin que coexistan factores moduladores del riesgo ni lesión de órganos diana (tabla 5). La concentración de cLDL recomendada es cLDL < 115 mg/dL.
El tratamiento se basará en cambios terapéuticos del estilo de vida (CTEV) que incluye: alimentación según los estándares de la dieta mediterránea. Podría estar indicado el uso de alimentos funcionales enriquecidos en fitosteroles y fibra para descender el colesterol junto a incremento de la actividad física, abstención tabáquica y pérdida de peso si fuera necesaria. La prescripción de fármacos para disminuir el colesterol no está universalmente indicada y deberá considerarse de forma individualizada si un paciente presenta dos de los siguientes factores: edad (hombres > 45 años; mujeres > 50 años); IMC > 30 kg/m2; tabaquismo; HTA; antecedentes familiares de ECVA precoz; dislipemia aterogénica; SM; o Lp(a) > 50 mg/dL.
Paciente de alto riesgo cardiovascularEl objetivo terapéutico es reducir el cLDL < 70 mg/dL y al menos un 50% de descenso de los valores basales de cLDL.
El tratamiento inicial se basará en la aplicación de CTEV. Si persisten cifras de cLDL > 70 mg/dL, se recomienda tratamiento hipocolesterolemiante de alta intensidad que teóricamente garantice un descenso de cLDL de al menos un 50% (tabla 8). El tratamiento inicial debe ser con estatinas y en caso de no alcanzar objetivos asociado, con ezetimiba. La combinación debe valorarse de inicio en pacientes con cifras basales de cLDL superiores a 140 mg/dL.
Paciente de muy alto riesgo cardiovascularEl objetivo terapéutico es un cLDL < 55 mg/dL y un descenso de al menos el 50% de los valores basales.
El tratamiento inicial se basará en la aplicación de CTEV y simultáneamente tratamiento hipocolesterolemiante de alta intensidad que teóricamente garantice un descenso de cLDL de al menos un 50% y permita alcanzar el objetivo (tabla 8). El tratamiento inicial debe ser con estatinas y en caso de no alcanzar objetivos, asociadas con ezetimiba. La combinación debe valorarse de inicio en pacientes con cifras basales de cLDL superiores a 110 mg/dL. La utilización de iPCSK9 estaría recomendada según las indicaciones que se enumeran en la tabla 10.
Criterios de la SEA para la utilización de iPCSK9
| Situaciones clínicas | Condicionantes adicionales | cLDL |
| Hipercolesterolemia familiar homocigota | - | >100 |
| Hipercolesterolemia familiar heterocigota | <4 factores de riesgo asociados | >160 |
| ≥4 factores de riesgo asociados | >130 | |
| Con diabetes | >100 | |
| Con enfermedad vascular arteriosclerótica | >70 | |
| Prevención secundaria | Estable | >130 |
| Síndrome coronario agudo (<1 año) | >100 | |
| Diabetes + Factor de riesgo adicional | >100 | |
| Más de dos factores de riesgo adicionales no controlados | >100 | |
| Lp(a) > 50 mg/dL | >70 | |
| Enfermedad coronaria recurrente o multivaso no revascularizable | >70 | |
| EAP sintomática aislada o enfermedad polivascular | >70 | |
| Síndrome coronario agudo < 1 año + diabetes | >70 | |
| IRC estadio ≥3 + 1FR | >70 | |
| Prevención primaria con riesgo muy alto | IRC ≥ 3b (no en diálisis) + DM | >130 |
Adaptado de Ascaso et al., 201978.
Un resumen de las indicaciones del tratamiento con fármacos hipolipemiantes de acuerdo con el riesgo obtenido en la tabla 5 puede verse en la tabla 11.
Indicaciones de tratamiento hipolipemiante según riesgo cardiovascular y concentración de cLDL
| Riesgo vascular | Colesterol LDL | ||||
|---|---|---|---|---|---|
| 55-70 mg/dL | < 70 mg/dL | 70-115 mg/dL | 116-190 mg/dL | > 190 mg/dL | |
| Bajo o moderado | Recomendaciones de hábitos de vida. No precisa tratamiento | Recomendaciones de hábitos de vida. No precisa tratamiento | Modificación de hábitos de vida y alimentos funcionales.Valorar tratamiento hipolipemiante | Riesgo alto por definiciónModificación de hábitos de vida y alimentos funcionales.Iniciar tratamiento hipolipemiante de alta intensidad | |
| Objetivo cLDL < 115 mg/dL | Objetivo cLDL < 70 mg/dL | ||||
| Alto | Recomendaciones de hábitos de vida. No precisa tratamiento | Modificación de hábitos de vida y alimentos funcionales.Iniciar tratamiento hipolipemiante si no se alcanzan objetivos | Modificación de hábitos de vida y alimentos funcionales.Iniciar tratamiento hipolipemiante de alta intensidad | Modificación de hábitos de vida y alimentos funcionales.Iniciar tratamiento hipolipemiante de alta intensidad | |
| Objetivo cLDL < 70 mg/dL | Objetivo cLDL < 70 mg/dL | Objetivo cLDL < 70 mg/dL | |||
| Muy alto | Modificación de hábitos de vida y alimentos funcionales.Valorar tratamiento hipolipemiante | Modificación de hábitos de vida y alimentos funcionales.Iniciar tratamiento hipolipemiante | Modificación de hábitos de vida y alimentos funcionales.Iniciar tratamiento hipolipemiante de alta intensidad | Modificación de hábitos de vida y alimentos funcionales.Iniciar tratamiento hipolipemiante de alta intensidad | Modificación de hábitos de vida y alimentos funcionales.Iniciar tratamiento hipolipemiante de alta intensidad |
| Objetivo cLDL < 55 mg/dL | Objetivo cLDL < 55 mg/dL | Objetivo cLDL < 55 mg/dL | Objetivo cLDL < 55 mg/dL | Objetivo cLDL < 55 mg/dL | |
En pacientes con dislipemia aterogénica, el objetivo principal es conseguir un cLDL o un colesterol no-HDL en objetivos terapéuticos según el nivel de riesgo, utilizando tratamiento con estatinas o combinaciones terapéuticas de alta intensidad (fig. 5). Una vez conseguido, en pacientes en prevención secundaria que, a pesar de un tratamiento hipolipemiante óptimo, mantengan una concentración de TGS > 200 mg/dL y cHDL bajo (< 40 mg/dL en varones o < 50 mg/dL en mujeres), se podría recomendar la utilización de fenofibrato o de ácidos grasos omega-3 (eicosapentaenoico etilo 4 g/día)79.
Pacientes con hipertrigliceridemiaTriglicéridos entre 200 y 500 mg/dLActuar según lo mencionado anteriormente para su nivel de RCV y sus cifras de cLDL. Según las recomendaciones de la European Atherosclerosis Society (EAS), en los pacientes de alto riesgo, en los que después de controlar el cLDL con estatinas persiste una concentración de TGS > 200 mg/dL, se puede considerar el uso de fenofibrato o de ácidos grasos omega-319. Asimismo, las guías de la EAS/ESC de 2019, en base a los resultados del estudio REDUCE-IT, recomiendan dosis elevadas de eicosapentaenoico etilo asociadas a estatinas en pacientes en prevención secundaria o DM con un factor de riesgo asociado y TGS de 150 mg/dL o superiores69.
Triglicéridos entre 500 y 1.000 mg/dLActuar según lo mencionado anteriormente para su nivel de RCV y sus cifras de colesterol no-HDL (aplicando los mismos criterios que los del cLDL más 30 mg/dL).
Si tras la aplicación de las medidas terapéuticas recomendadas persisten cifras de TGS > 500 mg/dl, valorar la asociación de fenofibrato y/o ácidos grasos omega-380.
Triglicéridos > 1.000 mg/dLEs prioritario disminuir los TGS con dieta para prevenir una pancreatitis reduciendo la cantidad total de grasa a menos de 30 g diarios y valorar, en los casos graves y persistentes, la introducción de aceite TGS de cadena media (TCM).
Iniciar tratamiento con fenofibrato y/o ácidos grasos omega-3 (> 3 g al día) y valorar su asociación ante un inadecuado control.
Pacientes con dislipemias genéticasHipercolesterolemia familiarLos pacientes con HF se consideran por definición de riesgo alto y deben alcanzar un cLDL < 70 mg/dL o < 55 mg/dL en caso de ECVA asociada. Además de la dieta y el estilo vida saludable, la mayor parte de los pacientes deben recibir una combinación de estatinas de alta potencia con ezetimiba81. De acuerdo con su riesgo basal, que como ya se ha comentado previamente, debe estratificarse, estos pacientes pueden ser tratados con iPCSK9 (tabla 10). Es necesario proceder a un tratamiento precoz para evitar el desarrollo de complicaciones cardiovasculares futuras. Los pacientes con la forma homocigota de la enfermedad pueden recibir, además de la terapia hipolipemiante convencional (estatinas altas dosis y ezetimiba), iPCSK9 y, en algunas circunstancias, lomitapida y/o aféresis de LDL82. Las guías sugieren que los niños con HF pueden iniciar tratamiento a los ocho a 10 años, comenzando con dosis bajas y escalando hasta alcanzar los niveles recomendables14. El objetivo de cLDL recomendado en los niños es < 135 mg/dL.
Hiperlipemia familiar combinadaNo existen recomendaciones específicas para el tratamiento de esta entidad. Esta dislipemia eleva el RCV y debe ser tratada inicialmente con dieta y cambios del estilo de vida; el fármaco de primera elección son las estatinas, ya que estas reducen igualmente el RCV en paciente con hipertrigliceridemia concomitante; los objetivos del cLDL y del colesterol no HDL son los recomendados según el nivel de riesgo. Con frecuencia es preciso para alcanzar los objetivos terapéuticos recomendados asociar un fibrato a la terapia con estatinas. En estos casos, el fibrato de elección es el fenofibrato.
DisbetalipoproteinemiaEsta es una rara hiperlipemia caracterizada por elevación de partículas lipoproteicas de densidad intermedia, que se traduce en una hiperlipemia mixta grave, la presencia de xantomas estriados palmares y un elevado riesgo de ECVA precoz, con una especial predilección por la enfermedad arterial periférica. Suele estar causada por la combinación de un genotipo E2/E2 en el gen de la Apo E y uno o varios factores ambientales (hipotiroidismo, obesidad, etc.). Debe ser sospechada en cualquier hiperlipemia mixta con niveles bajos de Apo B (< 120 mg/dL)83. El tratamiento va dirigido a controlar el factor ambiental coexistente, en especial la obesidad, y a utilizar estatinas combinadas o no con ezetimiba y/o fibratos. Dadas las características de la dislipemia, el objetivo principal es controlar el colesterol no-HDL84.
Síndrome de quilomicronemiaConsiste en un acumulo de quilomicrones en el torrente sanguíneo debido a una falta de actividad de la lipoproteína lipasa (LPL) lo que conduce a un insuficiente catabolismo de los TGS con un aumento severo de la concentración de éstos85. Existe un grupo de quilomicronemias de base genética grave, el síndrome de quilomicronemia familiar (SQF)86,87, y otro mucho más frecuente, debido a la asociación de variantes genéticas menos patogénicas con factores agravantes, el síndrome de quilomicronemia multifactorial (SQM)88. El SQF es raro, ya que afecta a 1/1.000.000 de la población mundial. Se debe a mutaciones recesivas con pérdida de función, de carácter homocigoto o heterocigoto compuesto, de los genes de la LPL, de la Apo C2, la Apo A5, el factor 1 de maduración de la lipasa (LMF1), la proteína 1 de unión a las lipoproteínas de alta densidad anclada en el glicosilfosfatidilinositol (GPIHBP1) y la glicerol 3-fosfato deshidrogenasa 1 (G3PDH1)89,90. La quilomicronemia aparece aún sin factores agravantes y las concentraciones de TGS se mantienen muy altas de forma crónica, en general > 10 mmol/L (885 mg/dL)91. La complicación más grave es la pancreatitis aguda, que es tanto más frecuente y recidivante, cuanto mayor es la concentración de TGS, y puede aparecer en los primeros años de la vida92. La pancreatitis puede evolucionar a pancreatitis crónica con insuficiencia pancreática y DM pancreopriva. También pueden aparecer xantomas eruptivos que afectan a la superficie de extensión de las extremidades y al tronco, hepatoesplenomegalia y lipemia retinalis93.
El SQM es debido a la asociación de distintos factores genéticos de menor patogenicidad, asociado a entidades responsables de hipertrigliceridemia secundaria94. Existe un riesgo de pancreatitis, pero es menor que en el SQF por el menor grado de severidad y persistencia de la hipertrigliceridemia95. La respuesta a la dieta, la actividad física y a los fármacos hipotrigliceridemiantes suele ser buena. El SQM suelen aparecer en la edad adulta o media de la vida.
En ambas situaciones el tratamiento se basa en una dieta con importante restricción de la cantidad total de grasa (< 30 g al día), utilización de aceite TCM, fibratos y ácidos grasos n-3 a dosis superiores a los 3 g al día.
HipoalfalipoproteinemiaLas causas más comunes de hipoalfalipoproteinemia son las ligadas a la hipertrigliceridemia y a la denominada dislipemia aterogénica. Las causas primarias son excepcionales y comprenden la Enfermedad de Tangier, el déficit de LCAT y variantes genéticas a nivel del gen de Apo A196. No existen tratamientos específicos para estas entidades, y el tratamiento de estos sujetos debe ir encaminado al control de los restantes factores de RCV97.
Paciente con hipertensión arterialAntes de iniciar el tratamiento antihipertensivo, se recomienda una medida adecuada de la PA para confirmar el diagnóstico de HTA (tabla 3), especialmente en la HTA de grado 1: PAS 140-159 mmHg y/o PAS 90-99 mmHg8 (tabla 4).
La MAPA durante 24 horas o la AMPA se correlacionan más estrechamente con el pronóstico y la lesión de órganos diana que la medida clínica, por lo que su uso es altamente recomendado. Además de su valor en el diagnóstico en sujetos no tratados, y la identificación de sujetos con HTA de bata blanca (PA clínica elevada, con valores de PA en la MAPA normales), es también un instrumento útil para monitorizar los efectos del tratamiento, evaluar la adherencia y detectar sujetos con HTA enmascarada (sujetos con PA normal en la consulta y valores elevados durante la MAPA). La tabla 12 muestra la definición de HTA según los valores de PA clínica, ambulatoria o automedida en el domicilio.
Definiciones de hipertensión según los valores de PA clínica, ambulatoria o automedida en domicilio
| Categoría | PAS (mmHg) | PAD (mmHg) |
|---|---|---|
| PA en la consulta | ≥ 140 | ≥ 90 |
| PA ambulatoria | ||
| Diurna (o en vigilia) | ≥ 135 | ≥ 85 |
| Nocturna (o durmiendo) | ≥ 120 | ≥ 70 |
| 24 horas | ≥ 130 | ≥ 80 |
| PA en el domicilio | ≥ 135 | ≥ 85 |
PA: presión arterial; PAD: presión arterial diastólica; PAS: presión arterial sistólica
Adaptado de Williams et al., 20188.
La decisión de iniciar el tratamiento farmacológico dependerá no solo del nivel de PA, sino también del RCV global en función de otros FRCV asociados, de la presencia de lesión subclínica de órganos diana (tabla 4), la cual predice la mortalidad cardiovascular de forma independiente a la puntuación del SCORE8,18, especialmente en el grupo de riesgo moderado, o bien de la presencia de una ECVA o enfermedad renal establecida.
El tratamiento inicial debe incluir siempre los cambios de estilo de vida, como único tratamiento inicial en los sujetos con HTA grado 1 y riesgo bajo o moderado98,99. En los sujetos con HTA de grado 1 pero de alto riesgo o con lesión de órgano diana, se debería iniciar el tratamiento farmacológico precozmente, una vez confirmado el diagnóstico de HTA en varias visitas, y preferiblemente mediante la MAPA o AMPA.
En los sujetos con HTA de grado 2 (PAS entre 160-179 mmHg y/o PAD de 100-109 mmHg) y en los sujetos con HTA de grado 3, debe añadirse el tratamiento farmacológico desde el inicio, y la mayoría de ellos requerirán tratamiento antihipertensivo combinado con al menos dos antihipertensivos. Aproximadamente el 10-12% de los hipertensos tratados requerirán más de 3 antihipertensivos100.
El principal beneficio del tratamiento antihipertensivo deriva de la reducción de la PA99, independientemente del fármaco utilizado, pudiendo iniciarse el tratamiento con diuréticos tiazídicos, o similares (indapamida, clortalidona), IECAs o antagonistas de los receptores AT1 de la angiotensina II (ARA-II), antagonistas del calcio o betabloqueadores. La posición de estos últimos como fármacos de primera línea ha sido cuestionada, debido a su menor efectividad en la prevención del ictus o sus posibles efectos metabólicos desfavorables (aunque esto puede no ser aplicable a todos los betabloqueadores), excepto en las situaciones clínicas con indicación específica para estos agentes (enfermedad coronaria, IC con fracción de eyección (FE) reducida, etc.). También pueden estar indicados como tratamiento inicial en hipertensos jóvenes con un patrón hipercinético y tendencia a la taquicardia, o en mujeres en edad fértil, en las que el uso de inhibidores del sistema renina-angiotensina (SRA) debe emplearse con precaución por su contraindicación desde las fases iniciales de la gestación.
Un reciente metaanálisis ha mostrado que una reducción de 5 mmHg de la PA sistólica reduce los eventos cardiovasculares mayores aproximadamente en un 10%, tanto en prevención primaria como en prevención secundaria101.
Objetivo terapéutico del tratamiento antihipertensivoEl primer objetivo es reducir la PAS < 140 mmHg en todos los pacientes. A partir de los resultados del estudio SPRINT7,102 y de los más recientes metaanálisis103, las nuevas guías8 aconsejan que, si el tratamiento antihipertensivo es bien tolerado, la meta terapéutica sería una PAS ≥ 130 mmHg y < 140 mmHg en la mayoría de los pacientes, y una PAS 120-129 mm Hg en algunas situaciones concretas. Respecto a la PAD, un valor < 80 mmHg debería ser considerado en todos los hipertensos, independientemente del nivel previo, riesgo basal o comorbilidades (tabla 13).
Objetivos terapéuticos de la PAS clínica en algunos subgrupos de hipertensos
| Condiciones clínicas | Presión arterial sistólica |
|---|---|
| Edad < 65 años | 120 < 130 mmHg |
| Edad ≥ 65 años | 130 < 140mmHga |
| Diabetes | 130mmHg o inferiorb |
| Enfermedad coronaria | 130mmHg o inferior |
| Enfermedad renal crónica | 130 < 140 mmHg |
| Post Ictus /AIT | 120 < 130 mmHg |
La prevalencia de HTA en los pacientes con DM es de hasta el 80%, siendo el doble de la observada en población no diabética de la misma edad y características. La coexistencia de HTA y DM incrementa el riesgo de desarrollar ECVA con una mayor incidencia de enfermedad coronaria, IC, EAP, ictus y mortalidad cardiovascular.
Se recomienda iniciar el tratamiento con una combinación de un inhibidor del SRA más un antagonista del calcio o un diurético tiazídico o tiazida-like, excepto cuando el filtrado glomerular estimado (FGe) sea < 30 mL/min/1,73 m2, en cuyo caso estaría indicado el diurético de asa. No se recomienda el uso de una combinación de dos inhibidores del SRA.
Se aconseja iniciar el tratamiento antihipertensivo cuando la PA clínica sea ≥140/90 mmHg, y el objetivo terapéutico será una PA sistólica de 130 mmHg o menor si es tolerada, pero no inferior a 120 mmHg, con una PAD < 80 mmHg, pero no < 70 mmHg, si proteinuria. En los sujetos de 65 años o más, se recomienda un objetivo terapéutico para la PAS de 130 a < 140 mmHg80,104.
HTA y enfermedad renal crónicaLa prevalencia de HTA en estos pacientes es del 67-92%, y representa su comorbilidad más frecuente. Por otra parte, la presencia de la HTA puede acelerar el daño renal, además de incrementar el RCV. Como en todos los sujetos con HTA el tratamiento farmacológico debe acompañarse de cambios de estilo de vida, haciendo especial énfasis en la reducción en la ingesta de Na. Los diuréticos de asa deben sustituir a los diuréticos tipo tiazida o tiazida-like cuando el FGe sea < 30 mL/min/1,73 m2. Debido a que el descenso de la PA disminuye la presión de perfusión, no es infrecuente una reducción del FGe entre el 10-20% al inicio del tratamiento. Se debe hacer una cuidadosa monitorización de los electrolitos.
Se recomienda iniciar el tratamiento cuando la PA sea ≥ 140/90 mmHg con un objetivo terapéutico para la PAS (tanto en el paciente diabético como en el no diabético) en el rango de 130 a < 140 mmHg. En algunos casos, y de forma individualizada, se puede reducir más la PA en función de la tolerancia y de su impacto sobre la función renal y electrolitos. En los pacientes con proteinuria > 1 g/día es beneficiosa una reducción mayor de la PA.
Se recomienda como tratamiento inicial un inhibidor del SRA más un antagonista del calcio o un diurético. No se recomienda el uso simultáneo de IECAs y ARA-II.
HTA y enfermedad coronaria estableLa HTA es un factor de riesgo mayor de enfermedad coronaria. Numerosos ensayos clínicos han demostrado los beneficios del tratamiento antihipertensivo en la reducción de la incidencia de enfermedad coronaria, tanto en prevención primaria como en prevención secundaria.
Excepto en algunos casos, como ancianos mayores de 80 años o ancianos frágiles, en general se recomienda como tratamiento inicial la terapia doble con un inhibidor del SRA (IECA o ARA-II) más un betabloqueante o antagonista del calcio, aunque pueden ser utilizadas otras combinaciones como antagonista del calcio dihidropiridínico más betabloqueante. En un segundo escalón, si no se controla la HTA, el paciente debe ser tratado con triple terapia, en general añadiendo un diurético a alguna de las combinaciones anteriores.
Si presentan angina sintomática, se recomienda una combinación de betabloqueadores y antagonistas del calcio dihidripiridínicos.
El objetivo terapéutico sería una PAS de 130 mmHg o inferior si es tolerado, pero no < 120 mmHg, y una PAD < 80 mmHg, pero no < 70 mmHg. En sujetos de 65 o más años, un objetivo terapéutico de PAS entre 130-140 mmHg puede ser adecuado.
HTA e Insuficiencia cardiaca o hipertrofia ventricular izquierdaEl antecedente de HTA está presente en el 75% de los pacientes con IC crónica. Se recomienda el tratamiento antihipertensivo cuando la PA clínica es ≥ 140/90 mmHg, tanto en pacientes con IC con FE reducida como en los que presentan IC con FE preservada. En los pacientes con IC y FE reducida, se recomienda el tratamiento con un inhibidor del SRA (IECA o ARA-II), un betabloqueante y un diurético, asociado o no a un antagonista de los receptores mineralcorticoides. Si no se logra el control de la HTA a pesar del tratamiento anterior, se podría añadir un antagonista del calcio dihidropiridínico.
En los pacientes con IC y FE preservada, no hay fármacos específicos que hayan demostrado su eficacia en la morbimortalidad más allá del control de la HTA, pero en caso de hipertrofia ventricular izquierda (HVI), muy frecuente en estos pacientes, se recomienda el uso de un inhibidor del SRA en combinación con un antagonista del calcio o un diurético. En los pacientes con HVI se recomienda un objetivo terapéutico de PAS entre 120-130 mmHg.
HTA e ictusEl ictus es una causa mayor de mortalidad, incapacidad y demencia, y está asociado de forma independiente con el incremento de eventos cardiovasculares mayores en ambos sexos105. Dado que el ictus es un grupo heterogéneo, en cuanto a causas y hemodinámica subyacente, el control de la HTA en estos pacientes es complejo y supone un auténtico reto. El objetivo terapéutico es una PA < 140/90 mmHg, si bien un objetivo de PAS entre 120-130 mmHg puede ser adecuado en muchos casos. Un reciente metaanálisis106 confirma el beneficio de reducir la PA por debajo de 130/80 mmHg en la prevención secundaria del ictus.
HTA resistente e HTA refractariaExisten diversas causas del mal control de la HTA en la práctica clínica, que deberían ser tenidas en cuenta antes de etiquetar a una paciente de HTA resistente (fig. 6)107.
La HTA resistente representa aproximadamente un 10-12% de los hipertensos tratados100. Una HTA se considera resistente cuando no se ha conseguido reducir la PA < 140/90 mmHg a pesar de dosis óptimas (o las dosis máximas toleradas) de tres fármacos y un plan terapéutico que incluya un diurético (típicamente IECA o ARA-II más un antagonista del calcio y un diurético).
Se debe confirmar el mal control mediante MAPA (preferible) o AMPA y se han de excluir las causas de pseudorresistencia (mala adherencia) y la HTA secundaria.
En los últimos años se ha descrito un nuevo fenotipo HTA refractaria, cuando no se alcanza una PA < 140/90 mmHg a pesar del uso de ≥ 5 antihipertensivos108,109. Es poco frecuente (1,4%), y también precisa de la realización de una MAPA de 24 horas para su confirmación, así como descartar las causas de pseudorresistencia, como se ha mencionado anteriormente en la HTA resistente. Un reciente estudio prospectivo110 ha mostrado que los pacientes con HTA refractaria, confirmada por MAPA-24 h, presentan un riesgo más elevado de eventos cardiovasculares mayores y de mortalidad, En la figura 7 se expone una propuesta práctica para el manejo clínico de los sujetos con HTA resistente o HTA refractaria111.
Seguimiento del paciente hipertensoTras el inicio del tratamiento farmacológico antihipertensivo, es importante efectuar un seguimiento del mismo al menos una vez dentro de los dos primeros meses, para evaluar el efecto sobre la PA, detectar los posibles efectos adversos y descubrir una posible mala adherencia. Posteriormente, se recomienda una visita de seguimiento entre tres a seis meses para verificar el control de la PA y evaluar la adherencia.
La mala adherencia es una causa frecuente de falta de control de la PA. Para su evaluación y detección, juegan un papel fundamental las enfermeras, farmacéuticos comunitarios y otros profesionales sanitarios, que son también de gran ayuda para la educación, apoyo y seguimiento a largo plazo de los pacientes hipertensos, por lo que han de formar parte de la estrategia global para la mejora del control de la PA. La simplificación del tratamiento y la reducción del número de comprimidos, ayudarán sin duda a una mejor adherencia y a un mejor control de la PA a mediano y largo plazo.
En los sujetos con PA normal-alta, aunque no sean tratados, se recomiendan cambios de estilo de vida, y un seguimiento periódico (al menos una visita anual) para medir la PA clínica y ambulatoria, así como para reevaluar su RCV.
Paciente con hiperglucemia (prediabetes y diabetes)Clasificación y pruebas diagnósticasSe considera hiperglucemia a unas cifras de glucosa plasmática en ayunas ≥ 100 mg/dL y DM a cifras de glucemia plasmática en ayunas ≥ 126 mg/dL. Además del criterio de glucemia en ayunas, la de prediabetes y DM pueden diagnosticarse si se cumple al menos uno de los criterios de HbA1c, los valores al azar de glucemia, o los valores de glucemia plasmática a las dos horas de la prueba de la sobrecarga oral de glucosa (SOG) descritos en la tabla 1439.
Criterios de diagnóstico según la American Diabetes Association (ADA)39
| Diagnóstico de prediabetes y diabetes | |||
|---|---|---|---|
| Normal | Prediabetes | Diabetes | |
| HbA1c (%) o | <5,7 | 5,7-6,4 | ≥6,5 |
| Glucemia plasmática basal (mg/dL) o | <100 | 100-125 | ≥126 |
| Glucemia 2h SOG con 75g (mg/dL) o | <140 | 140-199 | ≥200 |
| Glucemia al azar con clínica hiperglucémica (mg/dL) | ≥200 | ||
La prueba de SOG se realiza administrando 75 g de glucosa en un adulto o 1,75 g/kg de peso (máximo 75 g) en niños en condiciones estandarizadas. Es una prueba muy útil para confirmar el diagnóstico en pacientes de alto riesgo (tabla 15)41 asintomáticos, si por los valores de glucemia en ayuno o de HbA1c no quedan diagnosticados39,41. La medición de los valores de HbA1c debe realizarse utilizando un método estandarizado con el estudio DTCC y de referencia39.
Despistaje de diabetes41
| Edad ≥ 45 años | Edad < 45 años |
|---|---|
| En todos los casos | Prediabetes (antecedentes de intolerancia oral a la glucosa o glucemia basal alterada o HbA1c ≥ 5,7%) |
| Antecedentes de diabetes gestacional. Realizar nuevos controles cada tres años. | |
| Si IMC ≥ 25 kg/m2, en asiáticos ≥ 23 kg/m2, con al menos uno de los siguientes: | |
| - Perímetro de cintura: hombres ≥ 102cm y mujeres ≥ 88 cm | |
| - Diabetes en familiares de primer grado | |
| - Pertenencia a un grupo étnico de alto riesgo de diabetes (afroamericanos, latinos, etc.) | |
| - Historia de enfermedad cardiovascular | |
| - Hipertensión arterial (≥ 140/90mmHg o en tratamiento) | |
| - cHDL < 35 mg/dL, TGS > 250 mg/dL, o ambos | |
| - Síndrome de ovario poliquístico | |
| - Vida sedentaria | |
| - Otras condiciones asociadas a resistencia a la insulina (acantosis nigricans, hígado graso no alcohólico, hiperlipemia familiar combinada, etc.) |
Es obligatorio realizar despistajes de DM en sujetos asintomáticos de alto RCV (tabla 15) con el fin de hacer un diagnóstico precoz.
Objetivos de control en la prediabetes y diabetesLos objetivos generales de control se presentan en la tabla 16.
Objetivos de control de la prediabetes y diabetes
| 1 Establecer y mantener un buen control metabólico. |
| 2 Prevenir las complicaciones de la diabetes. |
| 3 Preservar la vida del paciente y aliviar los síntomas de la hiperglucemia. |
| 4 Capacitar al paciente para conseguir una buena calidad de vida (personal, familiar, laboral y social). |
| Individualizar el valor de HbA1c |
Para obtener un buen control glucémico es necesario individualizar el objetivo de HbA1c39. Para fijar el valor de HbA1c a alcanzar, tendremos en cuenta el grado de motivación, la presencia de complicaciones crónicas o de comorbilidades graves, edad del paciente, supervivencia y el tiempo de evolución (fig. 8). En pacientes jóvenes, sin complicaciones crónicas, ni comorbilidades, con tiempos de evolución cortos y larga supervivencia buscaremos intensificar el tratamiento para alcanzar HbA1c de entre el 6-7%39.
Los objetivos globales del tratamiento de la DM vienen recogidos en la tabla 17.
Objetivos globales del tratamiento en el adulto diabético
| Óptimo | Aceptable | No deseable | |
|---|---|---|---|
| GB mg/dL | 70-130 | 130-179 | ≥180 |
| GP 2h mg/dL | < 180 | 180-199 | ≥200 |
| HbA1c % | < 7,0 | 7,0-7,9 | ≥8,0 |
| cLDL mg/dL* | Variable | Variable | Variable |
| IMC | < 25 | 25-26,9 | ≥27 |
| PA mmHg | < 130/< 80 | 130-139/80-89 | ≥140/≥90 |
| Tabaco | NO FUMAR | ||
| IMC | Ideal <25 kg/m2 en obesos <30 kg/m2 | ||
LDLc: en función del riesgo; CV: DM de muy alto riesgo LDLc<55 mg/dL, DM de alto riesgo <70 mg/dL, DM de moderado riesgo LDLc<115 mg/dL (ver tabla 23).
GB: glucemia basal, GP: glucemia postprandial, PA: presión arterial
Para manejar adecuadamente el tratamiento de la DM, es necesario no sólo controlar la glucemia y buscar un valor individualizado de HbA1c, sino que debemos controlar los valores de PA, lípidos, dejar de fumar y buscar un peso óptimo. Es lo que se conoce como tratamiento global de la DM. Este tratamiento siempre será individualizado y precoz.
Tratamiento de la prediabetes y la diabetesDieta y cambios en el estilo de vidaEl tratamiento debe ir orientado a cumplir con todos los objetivos globales expuestos. El pilar del tratamiento de la prediabetes y de la DM2 es la dieta, los cambios en el estilo de vida y actividad física19,39,112. Como la mayor parte de los afectados presenta obesidad, el tratamiento dietético es similar al presentado en el apartado del paciente obeso.
Las modificaciones del estilo de vida del paciente con DM2 son una intervención esencial para mejorar no solo el control glucémico, sino también las comorbilidades asociadas, como la dislipemia, la obesidad y la HTA. Los cambios hacia un estilo de vida saludable deben incluir los siguientes aspectos: cese del tabaquismo y moderación de la ingesta alcohólica, gestión intensiva de pérdida de peso (> 5%) en caso de sobrepeso u obesidad, asesoramiento nutricional, actividad física y cambio de hábitos con supervisión continua. Se recomienda la ingesta de hidratos de carbono procedentes de las verduras, frutas, cereales integrales, legumbres y productos lácteos sobre otras fuentes19,112. Limitar especialmente los alimentos procesados que contienen grasas añadidas, azúcares o sodio. Recomendamos el consumo de ácidos grasos poliinsaturados n-3 presentes en el pescado, especialmente en el azul (sardina, salmón, atún, caballa, jurel, etc.). En resumen, una dieta tipo mediterránea rica en ácidos grasos monoinsaturados (aceite de oliva virgen y frutos secos) puede ser útil para el control global del RCV en estos pacientes19,112.
Diferentes metaanálisis sobre los efectos de intervenciones en los estilos de vida en personas con prediabetes encontraron reducciones en torno al 50% del riesgo de desarrollar DM239. Las características generales de la dieta y del ejercicio físico en la prevención cardiovascular han sido previamente descritas19,112 y avalan la idoneidad de una dieta tipo mediterránea, con restricción calórica si existe sobrepeso u obesidad en sujetos con prediabetes113.
Las recomendaciones generales de la actividad física en personas con prediabetes o DM vienen recogidas en la siguiente tabla 18.
Recomendaciones generales de la actividad física en personas con prediabetes y diabetes
| Realizar como mínimo 150 minutos por semana de actividad aeróbica moderada a intensa, repartidos en al menos tres días a la semana. Evitar pasar más de dos días sin actividad física. |
| Realizar de 2 a 3 sesiones por semana de ejercicios de resistencia en días no consecutivos |
| Disminuir el tiempo diario dedicado a actividades sedentarias |
| Para los adultos mayores, realizar de 2 a 3 veces por semana ejercicios de flexibilidad y equilibrio |
En sujetos con prediabetes, la ADA recomienda el tratamiento con metformina, especialmente en aquellos con IMC > 35 kg/m2, edad < 60 años, en mujeres con antecedentes de DM gestacional y se debe valorar en los casos que presenten glucemia en ayunas ≥ 110 mg/dL, HbA1c ≥ 6,1% y obesidad de predominio visceral39.
Los objetivos del tratamiento del paciente con DM son: prevenir y retardar las complicaciones macrovasculares y microvasculares, y reducir la elevada morbimortalidad cardiovascular. El máximo beneficio en la prevención cardiovascular del paciente con DM se obtiene interviniendo de forma simultánea en todos los FRCV: tabaco, dislipemia, HTA e hiperglucemia19,39.
Centrándonos en el tratamiento farmacológico de la hiperglucemia, una vez establecido el valor objetivo de HbA1c, la elección de los fármacos dependerá de la edad, grado y tipo de obesidad, eficacia y tolerancia de los fármacos, coste, comorbilidades (prevención secundaria, IC o nefropatía diabética) (fig. 8).
En la tabla 19 presentamos los principales fármacos utilizados para el tratamiento de la hiperglucemia en la DM y su indicación.
Principales fármacos utilizados en el tratamiento de la diabetes
| Fármaco | Dosis | Indicación |
|---|---|---|
| Metformina | 850mg x 3Titular de forma gradual | DM2DM1 obesoDiabetes gestacionalDM insuf. cardiaca |
| Pioglitazona | 30-45 mg/día | DM2DM2 e hígado graso |
| IDPP-4 | Sitagliptina 100 mg/díaVidagliptina 50mg x 2Saxagliptina 5 mg/díaLinagliptina 5 mg/díaAlogliptina 25 mg/día | DM2 |
| arGLP-1 | Exenatide 5μg sc x 2 1er mes, 10μg sc x 2 2.° mesLiraglutide 0,6 mg/día, 1,2 mg/día 2ª semana y si es necesario 1,8 mg/díaExenatide LAR, 2 mg/semanaLixisenatide, 10μg/día 2 semanas, aumentar hasta 20μg/díaDulaglutide 0,75 mg/semana aumentar 1,5 mg/semanaSemaglutide 0,25 mg/semana durante 4 semanas y subir a 0,5 mg/semana Máximo 1 mg/semana | DM2 obeso en prevención secundariaDM2 con IMC≥30 kg/m2 |
| Inhibidores de SGLT-2 | Dapagliflozina 10 mg/díaEmpagliflozina 10 y 25 mg/díaCanagliflozina 100 y 300 mg/díaErtugliflozina 5 y 15 mg/día | DM2DM2 con ICDM2 en prevención secundariaDM2 nefropatía diabética |
| Meglitinidas | Repaglinida 0,5-4mg antes de las 3 comidas principalesNateglinida 120mg, en las 3 comidas principales. | DM2 con ERC |
| Sulfonilureas2ª o 3ª generación | Iniciar con dosis bajas e ir incrementado la dosis. | DM2 |
| Inhibidores de alfa- glucosidasa | Acarbosa o miglitol 50mg x 3/ día, al inicio de la comida. Máximo 100mg x 3/día | DM2 |
arGLP-1: agonistas del receptor de GLP-1.
En la tabla 20, resumimos los principales beneficios, contraindicaciones, efectos adversos y capacidad de prevención cardiovascular independiente de su efecto hipoglucemiante.
Beneficios, contraindicaciones, principales efectos adversos y prevención cardiovascular de los principales fármacos utilizados en el tratamiento de la diabetes
| Fármaco | Beneficios | Contraindicación | Desventajas/Efectos adversos | Prevención CV |
|---|---|---|---|---|
| Metformina | ↓ HbA1c 1%↓ peso (1,5-2 kg)↓ costeNo hipoglucemias | FGe<30 mL/min/1,73 m2Insuf hepática grave24 h antes de cirugías | Náuseas, vómitos dolor abdominalExcepcionales: Déficit vitamina B12 y acidosis láctica | Sí39 |
| Pioglitazona | ↓ HbA1c 0,5-1%↓ TGS y ↑ cHDL | Insuficiencia cardiaca | ↑ peso↑ costeEdemasICFracturas en postmenopáusicas | Sí, en prevención primariaIctus39 |
| IDPP-4 | ↓ HbA1c 0,8%Peso =No hipoglucemias | FG <60 mL/min/1,73 m2 ajustar dosis sitagliptina 25 y 50 mg/día, alogliptina 6,25 y 12,5 mg/díaNo requiere linagliptina | ↑ costeLesiones cutáneas (penfigoide ampolloso)No combinar con arGLP-1 | NoSaxagliptina ↑ ingresos por Insuf. cardiaca |
| arGLP-1 | ↓ HbA1c 1%↓↓ pesoNo hipoglucemias | Embarazo | Náuseas, vómitos↑ coste | SíLiraglutide y semaglutide en prevención secundaria114,115. Dulaglutide prevención primaria y secundaria116 |
| Inhibidores de SGLT-2 | ↓ HbA1c 1%↓ peso↓ presión arterialNo hipoglucemias | Embarazo | Infecciones urinariasMicosis genitalesRaro hipotensión ortostática, deshidratación y cetoacidosis euglucémica | SíEmpagliflozina y Canagliflozina en prevención secundaria117,118Empagliflozina mortalidad117Dapagliflozina mortalidad CV119Empagliflozina, Canagliflozina, Dapagliflozina Ertugliflozina ingresos por Insuficiencia cardiaca117–119 Canagliflozina y Dapagliflozina preservación función renal y ↓ progresión nefropatía diabética120,121 |
| Meglitinidas | ↓ HbA1c 0,8%↑ PesoUso en Enf. Renal crónica | Embarazo y lactancia | Hipoglucemias | No |
| Sulfonilureas | ↓ HbA1c 1%↑ Peso (2-4 kg) | Embarazo y lactanciaPaciente ingresado | HipoglucemiasNo usar si ERC, insuficiencia hepática e Inf. cardiaca | No |
| Inhibidores de alpha- glucosidasa | ↓ HbA1c 0,5%Peso = | DM1Gestación y lactanciaEnf. gastrointestinal | Gastrointestinales: flatulencia, distensión, dolor | No |
En la figura 9 se presentan las pautas terapéuticas. El fármaco de primera elección en pacientes con DM2 es la metformina39. Como segundo escalón terapéutico, elegiremos el fármaco atendiendo a si el paciente está en prevención cardiovascular primaria o secundaria, presencia de obesidad, nefropatía diabética o IC39. Existen numerosos estudios de intervención que demuestran la capacidad de los inhibidores de SGLT2117–119 o los agonistas del receptor de GLP-1 en la prevención cardiovascular114–116 y progresión de la nefropatía diabética en las personas con DM120,121 y deben constituir los fármacos de uso prioritario en segundo escalón terapéutico.
Pautas terapéuticas y escalonamiento en el tratamiento farmacológico de la diabetes atendiendo a las principales comorbilidades.
arGLP1: agonistas del receptor del péptido similar al glucagón 1; IMC: body mass index; DM2: diabetes mellitus tipo 2; HbA1c: hemoglobina glucosilada; iSGLT2: inhibidores del cotransportador de sodio y glucosa tipo 2; IDPP-4: inhibidores de la dipeptidil peptidasa 4.
La insulinización en la DM2 con una insulina de acción prolongada o basal estará indicada si falla la triple asociación (tercer escalón terapéutico, fig. 9), siempre después de haber ensayado los arGLP-1, o si inicialmente existe clara clínica de hiperglucemia con HbA1c elevada (fig. 9). La dosis total diaria para comenzar la insulinización es de 0,1-0,3 U/kg de peso, con modificación de la dosis cada tres días hasta conseguir objetivos. Hemos de valorar en cada ocasión la necesidad real de aumentar la dosis, ya que en sujetos con obesidad e insulinorresistencia dosis elevadas pueden aumentar el peso y, con ello, la resistencia a la insulina, sin mejoría del control glucémico39.
Prevención cardiovascular en la diabetesTratamiento y prevención de la ECVA en la persona con diabetesLa prevención cardiovascular en la DM requiere una intervención precoz, intensiva y mantenida sobre todos los FRCV: dislipemia, PA, tabaquismo y obesidad abdominal19,39,112tabla 21.
Tratamiento y prevención de la enfermedad cardiovascular en la persona con diabetes
| Objetivo | Tratamiento | |
|---|---|---|
| Control de la hiperglucemia | HbA1c <7%. | Dieta hipoglucemiante–SGLT2 o arGLP-1 |
| Hipertensión arterial | PA <140-130/80-90mmHg Si albuminuria PA <130/80mmHg. | Reducción ingesta de sal < 3 g/24 hSi macroalbuminuria o insuficiencia renal, restringir el consumo de proteínas a 0,6-0,8 g/kg/24 hReducir el alcohol (máximo tolerado 30 g/día)Consumo moderado de café (2 tazas/24 h).IECA o ARA-II |
| Tabaco | No fumar ni activa, ni pasivamente | |
| Obesidad | IMC<30 kg/m2 | Estrategia dietoterapia |
| Dislipemia | Primario: descenso de cLDL según el riesgo del paciente (ver tabla 23).Secundario TGS < 150 mg/dL | Estatinas asociadas o no a ezetimiba para alcanzar objetivos terapéuticos, - iPCSK9 en prevención 2ª según recomendaciones de la SEA (tabla 10).Fibratos u omega 3 (EPA) |
tabla 22 En general, las personas con DM2 son consideradas como de alto RCV19,122. Las personas con DM2 y múltiples FRCV (dislipemia, HTA, tabaquismo) o lesión de órgano diana (nefropatía diabética) o que estén en prevención secundaria, son pacientes de muy alto RCV19. El objetivo primario para la prevención CV es obtener un valor de cLDL o de c-no-HDL recogido en la tabla 23, según la clasificación de riesgo del paciente19.
Objetivo primario de cLDL o c-no-HDL para la prevención cardiovascular en las personas con diabetes19
| Riesgo moderadoDM2<50 años o DM1<35 años con menos de 10 años de evolución y sin otros FRCV | Alto riesgoLos no incluidos en moderado o muy alto riesgo | Muy alto riesgoDM con ECVA o más de 3 FRCV o afectación de órgano dianaDM1 con más de 20 años de evolución | |
|---|---|---|---|
| LDLc (mg/dL) | <100 | <70 | <55 |
| c-no-HDL (mg/dL) | <130 | <100 | <85 |
| TGS mg/dL | <200 | <200 | <200 |
| cHDL (mg/dL) (hombre/mujer) | >40 / >50 | >40 / >50 | >40 / >50 |
Criterios diagnósticos del síndrome metabólico
| Criterios diagnósticos del síndrome metabólico. Diagnóstico si ≥3 criterios | |
|---|---|
| Obesidad abdominal | Perímetro de cintura (por encima de las crestas iliacas) elevado según sexo y etnia (≥ 94 H y ≥ 80M caucásicos) |
| Glucemia en ayunas (mg/dL) | ≥100 mg/dL o tratamiento previo específico |
| Triglicéridos plasmáticos (mg/dL) | ≥150 mg/dL o tratamiento previo específico |
| Colesterol HDL (mg/dL) | <40 mg/dL en H o <50 mg/dL en M o en tratamiento específico |
| Presión arterial (mmHg) | Sistólica ≥130 o diastólica ≥85 o con tratamiento antihipertensivo |
Para obtener estos objetivos será necesario utilizar estatinas de alta intensidad, en la mayor parte de los casos asociadas a ezetimiba. En la figura 5 queda recogido la estrategia y el esquema del tratamiento de la dislipemia en la persona con DM con el fin de conseguir una prevención cardiovascular efectiva. Una vez obtenido el valor de cLDL o c-no-HDL debemos buscar un objetivo secundario de TGS < 200 mg/dL en los pacientes con DM y SM19,41,79.
Paciente con obesidad y síndrome metabólicoPaciente con síndrome metabólicoEn la tabla 24 se define el SM41.
Tratamiento del síndrome metabólico
| Cambios en estilo de vida | |
| Dieta | De tipo mediterránea (saturadas <7% del aporte calórico total, colesterol <200 mg/día, evitar grasas trans)Rica en fibraLimitar consumo de sodio (5-6 g/día)Alimentos con índice glucémico bajo. Evitar azúcares simples.Aumentar frutas, vegetales y cereales integrales.Aceite de oliva como grasa culinaria principalEvitar alimentos procesados |
| Actividad física | Moderada-intensa30 minutos/día (preferible 45-60 min)Continua/intermitenteAl menos 5 días/semanaAdaptada a edad y estado cardiovascular del paciente. |
Entre las alteraciones metabólicas relacionadas con el SM destacan41:
Dislipemia, fundamentalmente hipertrigliceridemia, descenso del cHDL y presencia de partículas cLDL pequeñas y densas, con aumento plasmático de los ácidos grasos libres. A este conjunto de alteraciones se le conoce como dislipemia aterogénica.
Hiperglucemia o DMHTAEstas alteraciones, junto con la obesidad abdominal, son los parámetros que se han establecido para el diagnóstico de SM. Además, otras muchas alteraciones no utilizadas para establecer el diagnóstico tienen un gran interés, entre las que cabe citar, entre otras, la hiperuricemia o la gota, la hipercoagulabilidad y los defectos de la fibrinólisis que con frecuencia cursan con una elevación del inhibidor del activador del plasminógeno-1 (PAI-1), la esteatosis hepática no alcohólica y el hiperandrogenismo. La relevancia clínica del SM se relaciona con su prevalencia, un 20-40% de la población general y un 80-85% de los sujetos con DM2. Los pacientes con SM tienen un riesgo elevado de desarrollar ECVA y DM2.
Datos de diferentes metaanálisis indican que las personas con SM tienen un aumento doble del riesgo de episodios cardiovasculares y un incremento de 1,5 veces en la mortalidad por todas las causas, comparado con aquellos sin SM41. Estudios recientes encuentran un incremento en el riesgo relativo de desarrollar DM2 de entre cinco a 10 veces. Otras complicaciones no menos importantes relacionadas con el SM son: apnea del sueño, insuficiencia respiratoria o síndrome de hipoventilación alveolar idiopática y diversas formas de cáncer (mama, útero, colon, esófago, páncreas, riñón, próstata, etc.).
El tratamiento del SM debe buscar controlar todos los componentes del síndrome (tabla 25 y tabla 26). En la tabla 25 exponemos el tratamiento del SM. El pilar del tratamiento se basa en el cambio del estilo de vida buscando una reducción ponderal y un control de la dislipidemia aterogénica41,112,123.
Tratamiento de otros componentes del síndrome metabólico
| Tratamiento | |||
|---|---|---|---|
| Objetivo | Objetivos secundarios | Tratamiento | |
| Dislipemia | cLDL en función de los FRCV asociados*Si hipertrigliceridemia --> c-no-HDL (30 mg/dL superior al objetivo de LDL) o apoB | cHDL mg/dL>40 H y >50 MTGS <150 mg/dL. | Medidas higiénico-dietéticasEstatinas, ezetimiba y/o fibratos si precisa |
| Hipertensión y microalbuminuria | PA < 140/90mmHg. | Medidas higiénico-dietéticasIECA o ARA-II ± otros fármacos | |
| Otros FRCV | Abandono tabacoValorar antiagregación en sujetos de muy alto riesgo (aspirina) | ||
El SM no es un equivalente coronario pero sí es un modulador del riesgo (tabla 5) en la valoración del riesgo para establecer el objetivo de LDL.
Clasificación de las personas según el índice de masa corporal. Definición de delgadez y obesidad
| IMC | |
|---|---|
| Peso insuficiente | < 18,5 kg/m2 |
| Normopeso | 18,5-24,9 kg/m2 |
| Sobrepeso grado 1 | 25-26,9 kg/m2 |
| Sobrepeso grado 2 | 27-29,9 kg/m2 |
| Obesidad grado 1 | 30-34,9kg/m2 |
| Obesidad grado 2 | 35-39,9 kg/m2 |
| Obesidad grado 3 o mórbida | 40-49,9 kg/m2 |
| Obesidad grado 4 o extrema | ≥ 50 kg/m2 |
La obesidad se define como un IMC ≥ 30 kg/m2124. La clasificación de los pacientes en función de su valor de IMC viene recogida en la tabla 27.
Indicaciones de dietas de muy bajo contenido calórico
| Indicaciones | Contraindicaciones |
|---|---|
| Pacientes con IMC >35 kg/m2 en los que ha fracasado el tratamiento convencional y además presentan:Necesidad de una pérdida de peso rápida. Ej: insuficiencia respiratoria severa o cirugía ortopédicaPatología grave asociada a la obesidad que responde a la reducción ponderal, como la DM tipo 2, HTA, dislipemia o SAHS | IMC <30 kg/m2Embarazo y lactanciaPatología severa sistémica o de órgano, salvo en situaciones que se vean francamente agravadas por el sobrepeso, en las que se recomienda valoración individual de la relación riesgo-beneficioDM tipo 1Alteraciones psiquiátricas: trastorno de la conducta alimentaria, depresión grave, psicosis, adicción a drogas o alcoholTrastornos hidroelectrolíticos e hipotensión ortostáticaEnfermedades con pérdidas proteicas: enfermedad de Cushing, lupus eritematoso sistémico, proteinuria, neoplasias, malabsorción, enfermedad inflamatoria intestinal, etc.Enfermedades agudas cardiovasculares, arritmias cardíacas, ictusCirugía mayor o trauma en los últimos tres meses |
La obesidad es muy prevalente en nuestro país estimándose en el 14%, y en el 24% la de sobrepeso. La obesidad es el principal factor de riesgo para desarrollar DM2 y tiene, especialmente la obesidad abdominal, un alto RCV124.
El tratamiento de la obesidad es complejo y debe ser individualizado124,125. Se basa en estrategias de dietoterapia (fig. 10)126, cambios de estilo de vida, psicoterapia y fármacos (tabla 28 y tabla 29)124,125.
Tratamiento farmacológico de la obesidad
| Liraglutida |
| Posología |
| Saxenda® 6 mg/mL solución inyectable en pluma precargada. |
| Efectos clínicos |
| Pérdida de peso del 8% mantenido a 3 años. |
| Disminución progresión prediabetes a diabetes. |
| Efectos adversos |
| Náuseas y vómitos |
| Contraindicaciones |
| Embarazo y lactancia |
| Neoplasia endocrina múltiple (MEN-2) |
| Carcinoma medular tiroides |
| Enfermedad renal avanzada |
| Enfermedad hepática avanzada |
| Orlistat |
| Posología |
| Orlistat 120 mg/ 2-3 veces día en las comidas principales (requiere prescripción médica). |
| Orlistat 60 mg/ 2-3 veces día en las comidas principales (no requiere prescripción médica). |
| Efectos clínicos |
| ↓ 37% progresión a DM2 |
| Dosis 120 mg/3 veces día ↓ 3,1% peso inicial al año |
| ↓ PAS, PAD, Colesterol total, cLDL |
| Efectos adversos |
| 15-25% gastrointestinales |
| Puede ↓ absorción de vitaminas liposolubles |
| Nefrolitiasis por oxalatos (Orlistat ↑ niveles de oxalato en orina y debe usarse con precaución en pacientes con historia de nefrolitiasis por oxalatos) |
| Contraindicaciones |
| Síndrome de malabsorción crónica |
| Colestasis |
| Embarazo Lactancia |
| Naltrexona/Bupropión |
| Posología |
| Naltrexona/Bupropión 8 mg/90mg comprimidos de liberación prolongada |
| Al iniciar el tratamiento, la dosis se debe aumentar durante 4 semanas: |
| - Semana 1: un comprimido por la mañana |
| - Semana 2: un comprimido por la mañana y otro por la noche |
| - Semana 3: dos comprimidos por la mañana y uno por la noche |
| - Semana 4 y posteriores: dos comprimidos por la mañana y dos por la noche |
| La última dosis se recomienda que se tome por la tarde para evitar la aparición de insomnio si se ingiere a la hora de cenar |
| Efectos clínicos |
| 50% de los pacientes pierden ≥ 5% del peso |
| Efectos adversos |
| Náuseas |
| Contraindicaciones |
| Embarazo y lactancia |
| HTA no controlada |
| Pacientes que padezcan en la actualidad trastornos convulsivos o presenten antecedentes de convulsiones |
| Neoplasia conocida en el sistema nervioso central |
| Síndrome de abstinencia de alcohol o benzodiacepinas |
| Antecedentes de trastorno bipolar |
| Cualquier tratamiento simultáneo que contenga bupropión o naltrexona |
| Diagnóstico actual o previo de bulimia o anorexia nerviosas |
| Dependencia a los opiáceos de administración prolongada o a los agonistas opiáceos (p. ej., metadona) o con un síndrome agudo de abstinencia a los opiáceos |
| Tratamiento simultáneo con inhibidores de la monoaminoxidasa (IMAO). Entre la interrupción de la administración de IMAO y el inicio del tratamiento con Naltrexona/Bupropión deben haber transcurrido un mínimo de 14 días |
| Insuficiencia hepática grave |
| Insuficiencia renal terminal |
Tratamiento quirúrgico de la obesidad
| Indicaciones de cirugía bariátrica | • IMC ≥ 40 kg/m2• IMC ≥ 35 kg/m2 con una o más comorbilidades graves– Se consideran comorbilidades graves:– DM tipo 2– Hipertensión arterial– Dislipemia– Trastornos respiratorios secundarios a obesidad– Hígado graso no alcohólico– Artrosis– Incontinencia urinaria |
| Requisitos | – Edad 18 a 60 años. En mayores, se deberán individualizar casos concretos.– Descartar endocrinopatías.– Historia de obesidad mórbida de al menos cinco años– Fracaso o respuesta insuficiente del tratamiento médico - nutricional– Capacidad de adherencia a las recomendaciones y cambios en el estilo de vida posteriores a la cirugía.– El paciente debe entender el tratamiento al que va a ser sometido y las consecuencias a largo plazo.– Valoración psiquiátrica en caso de antecedente relevante o sospecha de enfermedad mental. |
| Contraindicaciones | – Patología psiquiátrica grave: esquizofrenia, depresión mayor, retraso mental.– Inestabilidad psiquiátrica.– Trastornos de la conducta alimentaria. Test BITE para descartar bulimia– Abuso de alcohol u otras drogas |
Las dietas habitualmente utilizadas son de 1.200 (mujeres) -1.700 kcal/día (hombres). Pueden utilizarse dietas más hipocalóricas, pero a largo plazo pueden producir déficit de minerales y vitaminas. Como un objetivo posible, el hecho de reducir el peso corporal en un 10% produce un importante beneficio para la salud, con cambios metabólicos significativos. Además, es importante el ejercicio físico adecuado a cada paciente y el soporte psicológico con modificación de la conducta alimentaria.
El tratamiento farmacológico en la obesidad debe ser individualizado. La selección de los fármacos dependerá de la edad, presencia o no de DM y contraindicaciones (tabla 29).
El tratamiento quirúrgico de la obesidad se reserva para un grupo de pacientes tras el fracaso terapéutico de otras opciones conservadoras127. La cirugía bariátrica (tabla 30) está indicada en la obesidad mórbida o en obesidad grave con múltiples complicaciones no controladas médicamente y que han fracasado con otras estrategias terapéuticas. Es un tratamiento efectivo no exento de complicaciones. Las indicaciones y contraindicaciones quedan recogidas en la tabla 30.
Recomendaciones sobre las estrategias para tratar el tabaquismo
| Recomendación | Clase | Nivel |
|---|---|---|
| Cualquier consumo de tabaco debe ser interrumpido, dado que el uso de tabaco se asocia de forma intensa e independiente con el desarrollo de enfermedad cardiovascular | I | A |
| Se debe ayudar a los fumadores a abandonar el tabaco, ofreciéndoles sustitutos de nicotina y fármacos (vareniclina y bupropion solos o en combinación), cuando sea necesario. | IIa | A |
| El cese del tabaquismo es recomendable a pesar de la ganancia de peso, dado que dicha ganancia no reduce el beneficio cardiovascular derivado de su abandono | I | B |
| Debe evitarse el tabaquismo pasivo. | I | B |
Adaptado de Visseren et al. 202118.
El tabaquismo es una adicción letal y la primera causa de mortalidad evitable, ya que duplica el riesgo de muerte por ECVA y la multiplica por 5 en los menores de 50 años. Fumar tabaco favorece la formación y la rotura de las placas de ateroma, además, promueve la inflamación, la oxidación y la disfunción del endotelio arterial que predispone al espasmo arterial, a la trombosis y a la obstrucción vascular. El fumar tabaco es perjudicial en todas sus formas, de una forma proporcional a la cantidad fumada128,129. Dejar de fumar es entre todas las medidas preventivas, la más rentable en cuanto a la disminución del RCV. El beneficio se observa en los primeros meses de la abstinencia. En España, en el periodo 2009-2012 la población fumadora disminuyó un 3,13% y en el periodo 2009-2017 un 4,81%130. Sin embargo, el tabaco se sigue promocionando y una vez adquirido el hábito de fumar, su interrupción es compleja, ya que el número de intentos fallidos antes del abandono del tabaco oscila según distintos informes entre 5 y 14131. En todos los fumadores y en cualquier interacción con los profesionales sanitarios se debe aconsejar el abandono del tabaco, lo cual aumenta en más de un 50% la probabilidad de que el paciente abandone el tabaco. Se considera que una persona ha dejado de fumar cuando ha transcurrido 1 año desde que se fumó el último cigarrillo.
En la tabla 31 se muestran las recomendaciones sobre las estrategias para tratar el tabaquismo contenidas en las guías europeas de prevención cardiovascular18.
Escala de riesgo trombótico CHADS2-VASc en fibrilación auricular
| Factor de riesgo | Valor ponderal |
|---|---|
| Insuficiencia cardiaca congestiva | 1 |
| Hipertensión | 1 |
| Edad ≥ 75 años | 2 |
| Diabetes | 1 |
| Ictus/AIT/embolismo periférico previo | 2 |
| Enfermedad vascular (arteriopatía periférica, cardiopatía isquémica, placa aórtica) | 1 |
| Edad entre 65 y 74 años | 1 |
| Sexo femenino | 1 |
| Puntuación máxima | 9 |
| Interpretación: Bajo riesgo=0; Riesgo moderado=1; Riesgo alto≥2 |
Toda visita médica de control del RCV debería incluir los siguientes apartados:
- –
Anamnesis sobre el hábito de fumar:
- ∘
¿Ha sido fumador en algún periodo de su vida (ha fumado con regularidad al menos 1 cigarrillo al mes)? (No/ Sí)
- ∘
¿Cuántos cigarrillos fuma al día?
- ∘
Si ha dejado de fumar, ¿cuántos meses han transcurrido desde que lo dejó?:
- ∘
¿Cuántos intentos serios de dejar de fumar ha realizado a lo largo de su vida?
- –
Aconsejar con convencimiento de la necesidad de dejar de fumar. Información sobre los beneficios de dejar de fumar y las estrategias facilitadoras. También sobre el potencial incremento de peso (3-5 kg de promedio) y su importancia menor a la del beneficio preventivo cardiovascular y de mejora del estado de salud general.
- –
Valoración del grado de adicción mediante el test de Fagerström132,133 (Anexo 3) para orientar sobre la necesidad de utilizar medidas farmacológicas y de sustitución de la nicotina.
- –
Valoración de la actitud del paciente frente al tabaquismo. Se pueden realizar tres preguntas clave:
- ∘
¿Cree que el tabaco le perjudica?
- ∘
¿Le gustaría dejar de fumar?
- ∘
¿Cree que podrá dejarlo?
- –
Si el paciente ha respondido afirmativamente a las tres preguntas anteriores hay que asistirlo mediante una estrategia planificada, incluyendo la fijación de la fecha, terapia conductual/motivacional y apoyo farmacológico o de consultas de tabaco específicas. Si no lo ha hecho habrá que informarlo, motivarlo e insistir.
- –
Establecer un programa de seguimiento.
Además de las terapias mediadas por la comunicación en la visita médica, incluyendo el consejo y la entrevista motivacional, pueden utilizarse los sustitutos de nicotina y distintos fármacos134. Los sustitutos de nicotina, tanto en forma de chicles, parches, espráis nasales o inhaladores, son eficaces y aumentan la probabilidad de abandono del tabaquismo4. El bupropión es un antidepresivo sobre el que existe una amplia base de ensayos clínicos que han demostrado su eficacia para dejar de fumar, ya que incrementa en más de un 50% las posibilidades de éxito. Su principal inconveniente es un riesgo pequeño (1/1.000) de convulsiones, sin aumentar el riesgo de ECVA o enfermedad neuropsiquiátrica. La vareniclina es un agonista parcial de los receptores de la nicotina sobre el que también existe una amplia base de ensayos clínicos que han demostrado que su uso incrementa en más de dos veces la probabilidad de abandonar el tabaco con éxito. Su principal efecto secundario es la aparición de nauseas, que puede mitigarse con un aumento progresivo de las dosis y evitando las dosis más altas135,136. Sin embargo, con fecha 6 de julio de 2021 la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) recomendó que no se iniciasen nuevos tratamientos con este fármaco, ya que se había detectado una impureza en los comprimidos de vareniclina que había obligado a retirar 3 lotes de este medicamento, y que no se podía garantizar a los pacientes la continuidad de este tratamiento.
Existe todavía una información insuficiente sobre el uso de cigarrillos electrónicos y los productos de calentamiento de tabaco. El uso de estos últimos se está incrementando137, por encima del uso de los cigarrillos electrónicos, y en ello parece haber influido la aprobación de la U.S. Food and Drug Administration (FDA) como un producto del tabaco de riesgo modificado en 2020138. Sin embargo, existen aún muchas cuestiones por resolver sobre estos productos y entre ellos, el más importante, sus efectos sobre la salud a largo plazo.
Paciente con fibrilación auricularLa FA es la arritmia más frecuente en la población, afectando a más de 33 millones de personas en el mundo139. Debido al aumento de la longevidad y a la intensificación en el diagnóstico, se estima que su prevalencia global será de 15.9 millones para el año 2050, siendo más de la mitad de ellos pacientes ≥80 años140.
Factores de riesgo cardiovascular que facilitan la presencia o recurrencia de la fibrilación auricularEl riesgo de la FA a lo largo de la vida aumenta con el incremento de la carga de FRCV. Identificarlos, prevenirlos y tratarlos es importante en aras de aminorar la prevalencia de la FA y su carga de morbilidad.
Hipertensión arterialUna PA alta e incontrolada puede modificar la estructura de la pared miocárdica, favoreciendo así el desarrollo de una FA e incrementando la posibilidad de hacerla recurrente. Por otra parte, la HTA aumenta el riesgo de ACV y de episodios de sangrado intracerebrales. Por lo tanto, el control de la PA debería ser una parte integral del tratamiento de pacientes con FA141.
Diabetes mellitusAunque se conoce la influencia de la DM en el remodelado miocárdico y su predisposición al desarrollo de una FA, el control glucémico intensivo no disminuye la tasa de FA de nueva aparición. Por el contrario, una DM de larga evolución predispone a un mayor riesgo de ACV y de fenómenos tromboembólicos en pacientes con FA. No obstante, el tratamiento con metformina en pacientes diabéticos parece estar asociado con un menor riesgo a largo plazo de FA142.
ObesidadLa obesidad incrementa la probabilidad de desarrollar una FA de forma paralela al aumento del IMC143. La reducción de peso, del orden de 10-15 kg, disminuye la recurrencia de la FA144. Asimismo, la mejora de la capacidad cardiorrespiratoria puede disminuir aún más la carga de FA en pacientes obesos con FA145.
Diagnóstico de la fibrilación auricular y estrategias de cribadoEl diagnóstico de FA se realiza tras objetivar irregularidad en los intervalos RR con ausencias de ondas P durante al menos durante 30 segundos en un ECG. Se distinguen 5 patrones temporales basados en la presentación, duración y la resolución espontánea de los episodios de FA: 1) FA diagnosticada por primera vez. 2) FA paroxística: Aquella que revierte espontáneamente/con intervención en < siete días. 3) FA persistente: Se mantiene durante > siete días. 4) FA persistente de larga duración: Continúa > 1 año tras adoptar una estrategia de control de ritmo 5) FA permanente: Aquella FA asumida por paciente y médico, no adoptándose nuevas médicas para restaurar o mantener el ritmo sinusal. Los términos «FA aislada» (en cada paciente existe una causa para FA), «FA valvular/no valvular» (puede crear confusión) y «FA crónica» (definición contradictoria) se encuentran en desuso en cuanto a su clasificación146. Según su componente clínico, la FA puede ser sintomática o asintomática o, recomendándose la realización de cribado a pacientes con HTA, apnea obstructiva del sueño, IC o mayores de 65 años mediante la palpación de pulso o ECG de 12 derivaciones146.
Manejo integral del paciente con fibrilación auricularEl manejo integral del paciente con FA incluye la información, la educación y el autocuidado del paciente, así como el control de los FRCV y de los posibles condicionantes arritmogénicos subyacentes, la regulación del ritmo o de la frecuencia cardiaca (FC) y la prevención del ictus mediante el empleo de anticoagulantes. No obstante, hay situaciones que requieren que un paciente con FA sea derivado a un servicio de urgencias hospitalario especializado, como son la inestabilidad hemodinámica, la FC elevada e incontrolable, la bradicardia sintomática, la angina severa, la disnea intensa e irreversible o la presencia de AIT o ACV. Para la evaluación inicial y el tratamiento de todos los pacientes con FA se recomienda la realización de ecocardiografía transtorácica, donde podemos evaluar la función y estructura cardiaca.
Control del ritmo o de la frecuencia cardiaca. Fármacos antiarrítmicos, ablación por catéter y cirugía de la fibrilación auricular.La terapia temprana de control del ritmo se asocia a un menor riesgo de eventos en pacientes con FA temprana y en aquellos pacientes con riesgo elevado147, mientras que en la FA de larga duración el control de frecuencia es la terapia más recomendada148. La elección de la terapia de control de ritmo dependerá de las características del paciente, los síntomas y la FEVI. Los betabloqueadores son los fármacos de primera línea para el control de frecuencia, sobre todo en aquellos pacientes con FEVI deprimida, mientras que los calcioantagonistas no dihidropiridinicos son una alternativa eficaz en ausencia de la misma. La digoxina debe ser usada con precaución debido a su posible asociación con un aumento de mortalidad concentración dependiente149. La amiodarona es útil en combinación tras el fracaso de la terapia previa, debiendo evitarse en aquellos con patología tiroidea.
Se recomienda el tratamiento para el control del ritmo con objetivo de mejorar los síntomas y calidad de vida en pacientes sintomáticos con FA146. Mientras que la cardioversión eléctrica directa sincronizada es el método preferido para pacientes con FA y deterioro hemodinámico, en pacientes estables su uso y el de la cardioversión farmacológica es indistinto. La flecainida y propafenona están indicadas en pacientes sin cardiopatía isquémica, hipertrofia o disfunción sistólica del ventrículo izquierdo. La elección de amiodarona intravenosa se realiza en pacientes con IC. El vernakalant intravenoso posee un efecto cardioversor más rápido que la amiodarona146. Pese a que la dronederona puede ser un fármaco utilizado para el control de ritmo se asocia con un aumento de la mortalidad de los pacientes con IC reciente descompensada, clase funcional III-IV de la NYHA, FA permanente ni en concomitancia con dabigatran150. El sotalol, está contraindicado en HVI, IC y alargamiento del QT por su riesgo de arritmias ventriculares y torsades de pointes. La dronederona y el sotalol no deben administrarse con aclaramientos de creatinina inferiores a 30 mL/min. El uso de «pastilla en el bolsillo» o «poket pill» con flecainida o propafenona es seguro y recomendado en aquellos pacientes con FA paroxística tras entrenamiento151.
Del mismo modo, se puede emplear la cirugía para el control del ritmo. Ésta se basa en la creación de cicatrices de aislamiento en las aurículas con el propósito de evitar los fenómenos de reentrada que inician y perpetúan la arritmia, permitiendo la reconducción del estímulo normal desde el nodo sinusal hasta el nodo auriculoventricular. Las técnicas actuales, basadas en dispositivos de transmisión de energía, permiten realizarla mediante toracoscopia con incisión mínima. En algunos estudios se muestra más efectiva que la ablación por catéter, aunque con mayor probabilidad de efectos secundarios y, en ocasiones, precisa de la implantación posterior de un marcapasos152. En la FA persistente sintomática podría indicarse la cirugía si la ablación por catéter ha fallado. También puede considerarse su empleo en pacientes con FA que vayan a ser sometidos a cirugía cardiaca.
Tratamiento anticoagulante para la prevención del ictusLa anticoagulación es el tratamiento de elección para la prevención del ictus isquémico, teniendo en cuenta que el riesgo es similar en la FA persistente y en la paroxística147. Clásicamente los fármacos antivitamina K (AVK), en un rango de international normalized ratio (INR) de 2-3, han sido los de elección, ya que producen una reducción en la tasa de ictus del 60-80%. La indicación de anticoagulación oral viene establecida por modelos pronósticos que han incorporado la edad y comorbilidades del paciente, siendo la escala más utilizada CHA2DS2-VASc (tabla 32), de tal forma que los pacientes con una puntuación de 0 (1 en caso de mujeres) no precisan de terapia anticoagulante oral. La anticoagulación estaría indicada en varones con CHA2DS2-VASc ≥ 1 o mujeres ≥ 2. Esta recomendación se aplica a pacientes con FA no valvular, siempre que no exista un riesgo elevado de complicaciones hemorrágicas, estimado según la escala HAS-BLED (tabla 33).
Escala HAS-BLED de riesgo hemorrágico en fibrilación auricular
| Factor de riesgo | Valor ponderal |
|---|---|
| Hipertensión, presión arterial mal controlada | 1 |
| Función renal/hepática anormal | 1 o 2 |
| Ictus | 1 |
| Tendencia o predisposición al sangrado | 1 |
| INR inestable | 1 |
| Edad avanzada (>65 años, condición frágil) | 1 |
| Medicamentos (aspirina o AINE), o consumo excesivo de alcohol | 1 o 2 |
| Puntuación máxima | 9 |
AINE: fármacos antiinflamatorios no esteroideos; INR: international normalized ratio.
Recursos de una consulta hospitalaria para el control global de los principales factores de riesgo vascular
| Arquitectura | Recursos materiales | Recursos informáticos |
|---|---|---|
| Consulta para cada profesional sanitario y por turno de trabajo.Espacio para enfermería para la medida de la PA, educación sanitaria y revisión de la adherencia al tratamiento.Sistema de climatización en el centro y los consultorios | Mobiliario completo en la consulta: mesa de despacho y camilla de exploración.Fonendoscopio, oftalmoscopio, linterna, báscula, tallímetro y cinta métrica.Dispositivos de medida de la PA validados170Aconsejable disponer de:1. Dispositivo de medida de PA semiautomático para que de forma programada se puedan hacer varias medidas automáticas (en general tres) sin presencia de observador. Se aconseja que en la primera visita las tres medidas automáticas se hagan de forma simultánea en ambos brazos.2. Acceso a la medición ambulatoria de la PA.3. Doppler portátil para la determinación del ITB.4. Electrocardiógrafo | Historia clínica, digital o no, según modelo del servicio de salud, accesible al área sanitaria de referencia.Acceso online a escalas de riesgo y cuestionarios.Prescripción electrónica, según modelo del servicio de saludPosibilidad de consulta online por Atención Primaria. |
ITB: índice tobillo-brazo; PA: presión arterial.
Adaptado de Felip Benach, 2009169.
En la última década, se han realizado cuatro grandes estudios aleatorizados con anticoagulantes orales de acción directa (ACOD): dabigatrán (RELY), rivaroxabán (ROCKET-AF), apixabán (ARISTOTLE) y edoxabán (ENGAGE-AF) y metaanálisis, que han demostrado una eficacia igual o superior a la de los AVK, con menor incidencia de complicaciones hemorrágicas, especialmente hemorragia intracraneal, por lo que en la actualidad constituyen la alternativa de elección en el tratamiento inicial de la FA (fig. 11)153. Los estudios en «vida real» confirman, asimismo, un menor riesgo hemorrágico de los ACOD en comparación con los AVK154. Además, los ACOD, en combinación con monoterapia antiagregante, pueden ser una alternativa segura y eficaz a la triple terapia en pacientes con FA sometidos a intervencionismo coronario percutáneo155. Por todo ello, las guías clínicas más recientes consideran los ACOD como la opción preferente para la prevención del ictus en pacientes con FA156,157.
Aunque las guías europeas sitúan a los ACOD por encima de los AVK, su utilización está restringida en nuestro país. Según un informe de posicionamiento terapéutico, solo se autoriza el uso de estos fármacos, en términos generales, en los pacientes con mal control terapéutico, con antecedentes de hemorragia intracraneal o con riesgo de ella158.
En todo caso, es importante involucrar al paciente en el proceso de decisión sobre las diferentes opciones de anticoagulación y considerar polimedicación y comorbilidades que pueden favorecer la aparición de hemorragias. Es siempre importante tener en cuenta la edad, fragilidad, peso y función renal que pueden influenciar el tipo de anticoagulante.
Anticoagulación en pacientes que requieren cardioversiónEs importante iniciar precozmente la anticoagulación de pacientes programados para cardioversión, dado que este procedimiento está asociado con un riesgo de tromboembolismo. Los pacientes que se han mantenido en FA durante más de 48 horas deben comenzar la anticoagulación al menos 3 semanas antes de la cardioversión, y después, continuar durante 4 semanas (siempre que no requieran anticoagulación indefinida). Las directrices actuales recomiendan una anticoagulación adecuada con un AVK o con dabigatrán (tanto antes como después del procedimiento). Otros ACOD están siendo estudiados en ensayos clínicos prospectivos159.
Organización y funcionamiento de la consulta de riesgo cardiovascular: profesionales y dispositivos. Criterios de calidadDiferentes e importantes estudios a nivel nacional e internacional publicados en los últimos años han mostrado un nivel bajo de control global de los FRCV incluso en prevención secundaria tanto en pacientes coronarios como con ictus o EAP160–167. Ello puede ser debido a diversos factores, entre los que destacarían la insuficiente adherencia al tratamiento, la inercia terapéutica y también los modelos organizativos que, en general, se muestran poco capaces de mejorar estos resultados.
El control multidisciplinar del RCV tiene unas claras ventajas168:
- –
Homogeneizar entre los diferentes niveles asistenciales el abordaje y el tratamiento de los FRCV, y así dar continuidad asistencial en la prevención del riesgo vascular.
- –
Mejorar la detección de todos los FRCV en pacientes de alto RCV que facilite la intervención terapéutica más adecuada y precoz para cada paciente.
- –
Optimizar los recursos sanitarios, evitando duplicidades de visitas y exploraciones complementarias.
- –
Definir y consensuar criterios de derivación, para generar un flujo bidireccional que facilite, en la mayoría de los casos, el retorno del paciente a nivel de atención primaria tras efectuar las evaluaciones e intervenciones que requirieron la derivación a la atención especializada. Así se garantiza que esta información llegue al médico de atención primaria y que el paciente reciba mensajes sanitarios unificados desde ambos niveles asistenciales.
- –
Promover la docencia e investigación en RCV.
Una consulta de Riesgo Vascular, como una unidad organizativa dentro del ámbito de atención programada, precisa de:
- –
Profesionales de distintas especialidades (Medicina Interna, Endocrinología, Cardiología, Nefrología, Bioquímica Clínica, Medicina de Familia, etc.), en coordinación con atención primaria, nutricionistas y enfermería, con capacidad para poder abordar de forma global los principales factores de riesgo.
- –
Protocolos unificados basados en las guías de práctica clínica para el control global de los principales FRCV.
- –
Unos requisitos estructurales básicos169. Ello incluye la posibilidad de realizar una adecuada medida de la PA con dispositivos validados (tabla 34).
Tabla 34.Indicadores para medir la calidad asistencial en el control global del paciente con alto riesgo cardiovascular
Indicadores Estructura o actividad Proceso o calidad Resultado – Número total de pacientes derivados a consulta de riesgo cardiovascular– Número de sesiones del equipo de riesgo cardiovascular– Número de sesiones de consultoría realizadas con atención primaria.– Número de visitas telemáticas realizadas por los integrantes de la consulta de riesgo cardiovascular: Consulta virtual, sesiones de consultoría, telemedicina.– Producción científica: comunicaciones y publicaciones compartidas por varios miembros del grupo – Número derivaciones a consulta de riesgo cardiovascular que cumplen criterios derivación previamente definidos y consensuados / número total de derivaciones.– Número pacientes con primera visita en la consulta de riesgo cardiovascular con tiempo de respuesta dentro de márgenes establecidos / número total de primeras visitas.– Número pacientes visitados con codificación de diagnósticos (según CIE10 / número total de pacientes visitados).– Número de pacientes en prevención primaria y no diabetes que tienen estimado su riesgo por alguna escala. – Número pacientes visitados que cumplen objetivos de control de FRCV según su categoría de riesgo / número total de pacientes visitados.– Adecuación consumo de recursos (exploraciones complementarias) / número total de pacientes visitados.– Número episodios de consulta de riesgo cardiovascular cerrados por alta a atención primaria con informe asistencia consensuado / número altas consulta de riesgo cardiovascular. CIE-10: Clasificación Internacional de Enfermedades, 10ª revisión; FRCV: factores de riesgo cardiovascular.
Adaptado de Armario et al., 2017168.
Como herramienta básica para medir la calidad asistencial se han de establecer unos indicadores (tabla 35) que han de permitir detectar cuáles son los aspectos de posible mejora para optimizar el control global de los factores de riesgo, y que han de ser utilizados como un sistema de autoevaluación.
Criterios de elección del tipo de consulta
| Preferencia consulta presencial | Preferencia consulta telemática |
|---|---|
| Sospecha de problemas potencialmente graves o urgentes, tener que dar malas noticias. Cambios clínicos, descompensación o empeoramiento del paciente, necesidad de entrevista con acompañantes, primera visita. | Situación clínica estable |
| Dificultades en la comunicación con el paciente (idioma, hipoacusia, problemas cognitivos) | Sin dificultades en la comunicación |
| Requiere exploración física | No requiere exploración física |
| Requiere adiestramiento en auto examen físico:PesoMedida de presión arterialAMPA | Está adiestrado en auto examen físico |
| Requiere pruebas complementarias a corto plazo:AnalíticaElectrocardiogramaRadiologíaÍndice tobillo brazoVelocidad onda del pulso (VOP)MAPA | Requiere pruebas complementarias a medio o largo plazo.(gestionar las peticiones vía administrativa) |
| Requiere adiestramiento en educación sanitaria más personalizada o cambios de tratamientos importantes o titulación de los mismos | No va a requerir a priori cambios de tratamiento |
| Enfermedad cardiovascular descontrolada | No enfermedad cardiovascular o en situación estable |
| Presencia de múltiples comorbilidades | No comorbilidades importantes |
AMPA: automedida de la presión arterial; MAPA: monitorización ambulatoria de la presión arterial.
Elaborado de Gijón-Conde et al., 2021171.
Las consultas donde se atiende a pacientes de RCV deben adecuarse al sistema organizativo del servicio de salud correspondiente, bien público o privado. La digitalización de las historias clínicas, la opción de la prescripción electrónica (y el conocimiento del grado de adherencia que ello permite) y las opciones de telemedicina (tanto para la interacción entre paciente-médico como médico-médico) pueden facilitar el acceso a la información clínica del paciente y al mejor control de los FRCV.
La pandemia COVID-19 ha provocado cambios importantes en la atención médica para reducir el riesgo de contagios de pacientes y personal sanitario en las consultas presenciales, con el consiguiente protagonismo de las consultas telemáticas. Estas consultas se han implantado de una forma muy heterogénea, y proponemos que en algunas situaciones clínicas concretas podrían seguir incorporadas en las agendas de atención al RCV, pero de una manera previamente estructurada, y con unos criterios de elección preestablecidos de situaciones en las que sería preferente una consulta presencial y otros en los que se podría preferir la consulta telemática (tabla 36)171.
Causas de derivación de pacientes con diabetes o HTA
| Diabetes mellitus | Hipertensión arterial |
|---|---|
| – Tipo 1. | – HTA resistente. |
| – Gestacional. | – HTA maligna y otras emergencias hipertensivas. |
| – Diabetes no filiada correctamente. | – Sospecha de causa secundaria. |
| – Mal control glucémico, diabetes inestable, hipoglucemias. | – Embarazo; antecedente de HTA gestacional. |
| – Comorbilidades (p. ej., obesidad mórbida). | – Infancia, adolescencia. |
| – Enfermedad microvascular grave (polineuropatía pie diabético, IRC, retinopatía avanzada). | – Comorbilidades (insuficiencia cardiaca o renal, enfermedad cerebrovascular, coronaria o arterial periférica). |
| – Solicitud de MAPA de 24 horas cuando no se dispone de recursos para realizarla e interpretarla. |
HTA: hipertensión arterial; IRC: insuficiencia renal crónica; MAPA: medida ambulatoria de la presión arterial.
Los pacientes con RCV elevado son remitidos a consultas por norma general para el control de alguno de los FRCV, fundamentalmente la HTA, la DM y la dislipemia; ya sea en el ámbito de la prevención primaria o en el de la secundaria. En este sentido, es frecuente que se deriven a nuestras consultas de riesgo vascular a pacientes con ECVA establecida (coronaria, cerebrovascular o arterial periférica), a veces jóvenes, en los que no se identifican FRCV (para el estudio diagnóstico de trombofilia), o bien que desconocían o no controlaban adecuadamente los FRCV detectados durante la valoración hospitalaria.
No es habitual recibir pacientes para deshabituación del tabaco, aun siendo este un factor de riesgo mayor. Algunas áreas de atención primaria o de neumología cuentan con unidades específicas. En cualquier caso, cada Servicio Público de Salud suele establecer sus propios criterios de derivación a unidades especializadas, en función de sus propias agendas, de la disponibilidad de recursos y del nivel asistencial (hospitales comarcales frente a hospitales de referencia de tercer nivel).
Las principales causas de derivación para pacientes con HTA y DM quedan reflejadas en la tabla 37, siendo los pacientes remitidos a la Unidad de HTA y Riesgo Vascular o a la Unidad de Endocrinología. La SEA ha publicado los criterios de derivación de pacientes dislipémicos a sus unidades de lípidos172 (tabla 38).
Criterios de derivación de pacientes con diabetes o HTA
| Diabetes mellitus | Hipertensión arterial |
|---|---|
| -–→Tipo 1-–→Gestacional-–→Diabetes no filiada correctamente-–→Mal control glucémico, diabetes inestable, hipoglucemias-–→Comorbilidades (p. ej., obesidad mórbida)-–→Enfermedad microvascular grave (polineuropatía pie diabético, IRC, retinopatía avanzada) | -–→HTA resistente-–→HTA maligna y otras emergencias hipertensivas-–→Sospecha de causa secundaria-–→Embarazo; antecedente de HTA gestacional-–→Infancia, adolescencia-–→Comorbilidades (insuficiencia cardiaca o renal, enfermedad cerebrovascular, coronaria o arterial periférica)-–→Solicitud de MAPA de 24 horas cuando no se dispone de recursos para realizarla e interpretarla |
HTA: hipertensión arterial; MAPA: medida ambulatoria de la presión arterial.
Criterios de derivación a unidades de lípidos de la Sociedad Española de Arteriosclerosis
| Dislipemia | Dinteles | Contexto clínico | Diagnóstico | Tratamiento |
|---|---|---|---|---|
| Hipercolesterolemia | CT > 300 mg/dlcLDL > 200 mg/dlLp(a) > 50 mg/dl | Xantomas tendinososArco corneal < 45 añosAntecedentes familiares +++CI o EAP prematuraCI recurrenteEnfermedad vascular sin FRCV evidentesSospecha de HFEsteatosis y/o cirrosis | Cribado en cascada de HFTest genéticosTécnicas de imagen para detectar EVS | Triple terapiaNuevos tratamientos (anti-PCSK9)Intolerancia farmacológicaRefractariedad al tratamientoAféresis |
| Hipertrigliceridemia | TGS en ayunas > 1.000 mg/dLTGS > 500 mg/dL pese a tratamientoHipertrigliceridemia y CT > 350 mg/dL | XantomasHepatomegaliaEsplenomegaliaLipemia retinalisDebut en la infanciaPancreatitis | Análisis de causas secundariasTest bioquímicos.Diagnóstico molecular | Excluir causa secundariaTratamiento ineficazDietas especiales |
| cHDL | cHDL < 20 mg/dLcHDL > 100 mg/dL | HepatomegaliaEsplenomegaliaHipertrofia amigdalarOpacidad cornealInsuficiencia renal | Excluir causas secundariasTest bioquímicosDiagnóstico molecular | Control causas secundarias |
| Hipocolesterolemia | cLDL < 50 mg/dL sin tratamiento | MalabsorciónEsteatosis | Excluir causas secundariasTests bioquímicosDiagnóstico molecular |
cHDL: colesterol-HDL; CI: cardiopatía isquémica; cLDL: colesterol-LDL; CT: colesterol total; EAP: enfermedad arterial periférica; HF: hipercolesterolemia familiar; Lp(a): Lipoproteína (a); TGS: triglicéridos. +++ Positivos
Adaptado de Sánchez-Chaparro MA et al.172
En el contexto del RCV, el principal tipo de DM a considerar es la de tipo 2, asociada con la dislipemia, obesidad, HTA y SM; por ello, la causa más habitual va a ser la falta de un control glucémico adecuado, a pesar de que en los últimos años el arsenal terapéutico en el campo de la DM2 es enorme173.
En el caso de la HTA, en nuestro país el motivo más común de remitir pacientes a una unidad de HTA es descartar la causa de HTA secundaria, seguido de mal control terapéutico e HTA resistente174, definiendo esta última como la incapacidad de controlar la PA (< 140/90 mmHg) pese a tres fármacos, uno de ellos un diurético175.
Para el caso de la dislipemia, las causas más comunes de remitir a los pacientes son el mal control en los niveles de colesterol o TGS séricos, el tratamiento y diagnóstico de la HF, los efectos adversos de la medicación, en especial la intolerancia a las estatinas (fundamentalmente por toxicidad muscular) o la necesidad de tratamientos combinados, especialmente con iPCSK9172.
Criterios de alta del paciente con riesgo cardiovascularEs obvio que, una vez alcanzado el diagnóstico definitivo y controlado el factor de riesgo que motivó la consulta, los pacientes deben ser remitidos desde la unidad especializada para su seguimiento por atención primaria. Sin embargo, no es infrecuente que los pacientes sean revisados en las consultas por diversos motivos, entre otros, no alcanzar los objetivos terapéuticos, la necesidad de procedimientos no convencionales (cirugía bariátrica, aféresis de cLDL o perfusión en hospitales de día de terapia lisosomal sustitutiva), la necesidad de prescribir y dispensar determinados fármacos por la farmacia hospitalaria (como es el caso de los fármacos iPCSK9), la polimedicación con elevado riesgo de interacciones farmacológicas (p.ej., en sujetos con infección por VIH y trasplantados) y aquellos que sufran efectos adversos derivados de la medicación, como por ejemplo las hipoglucemias. Algunos pacientes con HTA secundaria se mantienen hipertensos pese al tratamiento etiológico de su enfermedad, lo que sugiere el efecto prolongado de la HTA sobre el árbol vascular (remodelado) o bien que alguno de ellos pueda tener además una HTA esencial176.
FinanciaciónLaboratorios Ferrer ha proporcionado apoyo para la realización de la edición y soporte administrativo con relación a la actualización del documento «Estándares SEA 2022 para el control del riesgo cardiovascular». Los autores del documento son responsables del contenido del mismo. Laboratorios Ferrer no ha intervenido ni en su redacción, ni en su contenido.
Los autores no tienen otras afiliaciones relevantes o participación financiera con ninguna organización o entidad con un interés o conflicto financiero con el tema o los materiales discutidos en el manuscrito, aparte de los divulgados.
Conflicto de interesesLaboratorios Ferrer ha proporcionado apoyo para la realización de la edición y soporte administrativo con relación a la actualización del documento «Estándares SEA 2022 para el control del riesgo cardiovascular». Laboratorios Ferrer no ha intervenido ni en su redacción, ni en su contenido.
Algunos autores han recibido honorarios de diferentes laboratorios farmacéuticos incluyendo a Laboratorios Ferrer por su participación en conferencias y asesorías, que se detallan en el apartado correspondiente. Los autores no han recibido ninguna remuneración para realizar este informe ni declaran otros conflictos de interés directos de acuerdo con este trabajo.
Declaraciones de conflicto de intereses de los autoresMasanaL ha recibido honorarios de consultoría por Amgen; Sanofi; Amarin; Daiichi; Novartis, por conferencias, presentaciones, manuscrito o eventos educativos y reuniones por Amgen; Sanofi; Mylan; Sevier; Amarin; Amryt; Daiichi; Novartis.
ValdivielsoP ha recibido honorarios de consultoría, por experto testimonio, por conferencias, Advisory Boards, presentaciones, manuscrito o eventos educativos, soporte para reuniones por Amarin; Amgen; Novartis; Ferrer; MSD; Akcea; Ionis; Daiichi-Sankyo; Sanofiy Mylan y subvenciones o contratos de Ferrer; Akcea.
Arrobas-Velilla T ha recibido honorarios por conferencias, presentaciones, manuscrito o eventos educativos por Sanofi; Amgen; Novartis.
Cebollada J ha recibido honorarios por conferencias por Daiichi-Sankyo; Servier; Chiesi.
Díaz-Díaz JL ha recibido honorarios por conferencias, presentaciones, manuscrito o eventos educativos de Sanofi; MSD; Amgen; Viatris, soporte para reuniones de Viatris; Sanofi; Amgen; MSD y participación en Advisory Boards de Amgen; Sanofi.
Fernández Pardo J ha participado en la redacción de Textbook of Emergency Medicine y Manual of medical diagnosis and therapy por Menarini; MSD, honorarios por presentaciones de Ferrer Internacional y soporte para congresos de Menarini.
Guijarro C ha recibido apoyo administrativo y de reuniones para la preparación de este manuscrito de Laboratorios Ferrer, honorarios de consultoría de Sanofi; Amgen y Daiichi Sankyo, honorarios por conferencias, presentaciones, manuscrito o eventos educativos de Rubio, Sanofi; Amgen; Daiichi Sankyo, participación en Advisory Boards de Sanofi; Amgen; Daiichi Sankyo.
Jericó C ha recibido honorarios por conferencias, presentaciones, manuscrito o eventos educativos de Amgen; Boehringer; Mylan; Novo Nordisk; Rovi; Sanofi y soporte para reuniones de Sanofi.
López-Miranda J ha recibido honorarios por conferencias y actividades educativas de Amgen; Sanofi; MSD; Ferrer y Laboratorios Esteve, honorarios por consultoría o Advisory Boards y soporte a reuniones de Amgen y Sanofi.
Pedro-Botet J ha recibido honorarios por Advisory Boards de Amgen; Daiichi-Sankyo; Ferrer; Mylan (Viatris); Sanofi y conferencias de Amarin Pharma; Amgen; Daiichi-Sankyo; Esteve; Ferrer; Merck Sharp & Dohme; Mylan (Viatris); Rovi; Sanofi; Servier.
Puzo J ha recibido honorarios de consultoría de Beckman-coulter, por conferencias, presentaciones, manuscrito o eventos educativos de Sanofi y Amgen y liderazgo en junta, sociedad, comité o grupos de defensa por SEQC.
A los compañeros que dedicaron parte de su tiempo para responder la encuesta y la inestimable colaboración de la Gerencia de AP de Burgos, posibilitando este trabajo para todos.