La secreción endocrina pancreática está regulada por el sistema nervioso autónomo. El sistema parasimpático estimula la producción de insulina por las células beta e inhibe la liberación adrenérgica por el sistema nervioso simpático. El objetivo del presente estudio es evaluar el efecto de la neuroestimulación percutánea (PENS) del dermatoma T7, creándose un reflejo somato-autonómico, cuya vía eferente serán las ramas del nervio vago que estimulan específicamente el páncreas. Se analizará el efecto de este tratamiento sobre la glucemia, la secreción de insulina y la resistencia a la acción de la insulina.
MétodosEstudio prospectivo aleatorizado en el que se incluyeron pacientes con Índice Masa Corporal>30kg/m2 y diagnóstico de diabetes mellitus en tratamiento con metformina. Los pacientes fueron aleatorizados en 2 grupos: pacientes sometidos a PENS del dermatoma T7 (12 sesiones de 30min semanales) asociado a dieta de 1.200Kcal/día (grupo 1) y pacientes que seguían una dieta de 1.200Kcal/día exclusivamente (grupo 2). A todos los pacientes se les realizó una analítica sanguínea en ayunas antes de empezar el tratamiento y a los 7 días de finalizarlo.
ResultadosSe incluyeron 60 pacientes: 30 pacientes en cada grupo. Al finalizar el tratamiento en el grupo 1 se observa un descenso significativo en la glucemia (descenso medio de 62,1mg/dl; p=0,024) y en el HOMA (descenso medio 1,37; p=0,014). En el grupo 2 no se observan diferencias significativas en los valores pre y postratamiento.
ConclusiónLa PENS del dermatoma T7 asociada a dieta de 1.200Kcal/día produce una mayor reducción de la glucemia y de la resistencia insulínica que la obtenida solo mediante dieta tras 3 meses de tratamiento.
Endocrine pancreatic segregation is regulated by the autonomic nervous system. The parasympathetic system stimulates insulin production by the beta cells and inhibits the adrenergic discharge by the sympathetic nervous system. The aim of this study was to evaluate the effect of percutaneous neurostimulation (PENS) of dermatome T7, generating a somato-autonomic reflex, whose efferent pathway are the vagal branches that specifically stimulate the pancreas. The effect of this treatment on glycemia, insulin secretion and insulin resistance was investigated.
MethodsA prospective randomized clinical trial was performed. Patients with Body Mass Index>30kg/m2 and diagnosis of diabetes mellitus treated with Metformin were included. Patients were divided into 2 groups: Patients undergoing PENS of dermatome T7 (12 sessions of 30minutes weekly) associated with a 1,200 Kcal/day diet (Group 1) and patients following only a 1,200Kcal/day diet (Group 2). All the patients underwent a blood sample extraction before the treatment and 7 days after finishing it.
Results60 patients were included: 30 in each group. After finishing the treatment, in Group 1 a significant decrease in glycemia (Mean decrease of 62,1mg/dl; P=.024) and HOMA (Mean decrease 1.37; P=.014) was observed. In Group 2, no significant differences between pre and post-treatment values were observed.
ConclusionPENS of dermatome T7 associated with a 1,200Kcal/day diet achieves a greater reduction in glycemia and insulin resistance than with diet exclusively after 3 months of treatment.
Está ampliamente demostrado que la obesidad es un factor de riesgo para el desarrollo de diabetes mellitus tipo 2 (DM2). En las últimas décadas ha aumentado la prevalencia de diabetes mellitus de forma paralela al aumento de la obesidad. Algunos trabajos han estimado que el riesgo de desarrollar DM2 aumenta un 4,5% por cada kg, aumentado por encima del límite de la normalidad. Esto hace que en pacientes con obesidad severa u obesidad mórbida la probabilidad de desarrollar DM2 en algún momento de la vida sea prácticamente del 100%1–3. La resistencia a la acción de la insulina se ha convertido en el mayor determinante para el desarrollo de DM2, que se pone de manifiesto cuando la célula beta pancreática es incapaz de producir mayor cantidad de insulina para vencer la resistencia insulínica perférica4.
Se ha demostrado que la pérdida de peso consigue una mejoría del perfil glucémico. La pérdida de peso secundaria a cirugía bariátrica ha demostrado aumentar la secreción de insulina a nivel del páncreas, así como reducir la resistencia periférica a la acción de la misma, contribuyendo ambos mecanismos a la mejoría e incluso desaparición de la DM2 en pacientes obesos mórbidos4,5.
La secreción endocrina pancreática está regulada por el sistema nervioso autónomo. El sistema parasimpático estimula la producción de insulina por las células beta. La administración de acetilcolina exógena también aumenta la liberación de insulina. Por otra parte, la activación parasimpática inhibe la liberación adrenérgica por el sistema nervioso simpático6.
El objetivo del presente estudio es evaluar el efecto de la neuroestimulación percutánea (PENS) del dermatoma T7 y la consiguiente creación de un reflejo somato-autonómico, cuya vía aferente serán las terminaciones nerviosas sensitivas del dermatoma T7 y la vía eferente serán las ramas del nervio vago que irán a estimular específicamente el páncreas. Se analizará el efecto de este tratamiento sobre la glucemia, la secreción de insulina y la resistencia a la acción de la insulina.
MétodosRealizamos un estudio prospectivo aleatorizado en la Unidad de Obesidad del Hospital General Universitario de Elche y las Unidades de Neuroestimulación para el Tratamiento de la Obesidad de la Clínica Garcilaso (Madrid) y la Clínica Maisonnave (Alicante) entre enero de 2013 y enero de 2014. El cálculo del tamaño muestral se basó en una reducción de la resistencia insulínica según la fórmula Homeostasis model assessment (HOMA) de 0,5 en el grupo control y del doble (1) en el grupo experimental. El cálculo en el grupo control se basó en datos históricos obtenidos en el Hospital General Universitario de Elche en pacientes obesos y diabéticos tipo 2 tras 12 semanas de tratamiento dietético siguiendo una dieta de 1.200kcal/día. Con un 80% de potencia estadística y un nivel de significación p<0,05 se calculó que era necesario incluir 30 pacientes en cada brazo de estudio. Los criterios de inclusión fueron pacientes con Índice de Masa Corporal (IMC)>30kg/m2 y con diagnóstico de DM no insulinodependiente en tratamiento con metformina. Los criterios de exclusión fueron pacientes con otras enfermedades endocrinológicas causantes de su obesidad o de la DM, pacientes con DM insulinodependiente o pacientes en tratamiento con antidiabéticos orales diferentes a metformina.
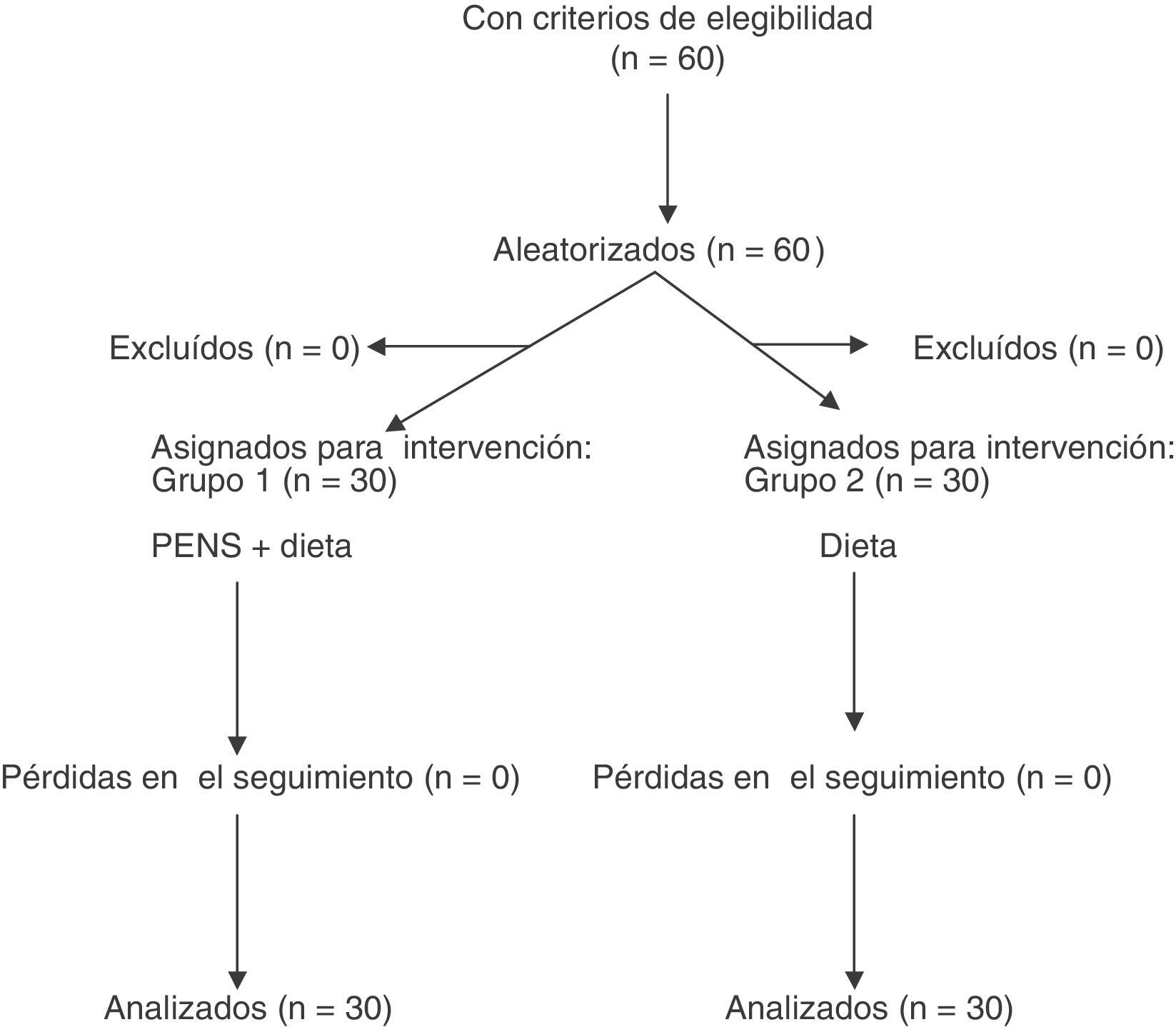
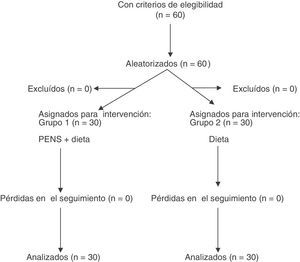
Los pacientes fueron aleatorizados en 2 grupos mediante un modelo de aleatorización extraído de Internet: pacientes sometidos a neuroestimulación percutánea del dermatoma T7 (PENS) asociado a dieta de 1.200kcal/día (grupo 1) y pacientes que seguían una dieta de 1.200kcal/día exclusivamente (grupo 2) (fig. 1).
Todos los pacientes se encontraban en tratamiento con metformina 850mg cada 12h. La dieta prescrita de 1.200kcal/día se expone en la tabla 1. A los pacientes de ambos grupos se les explicó la importancia de la pérdida de peso con la dieta para mejorar su diabetes y evitar el desarrollo de complicaciones asociadas a la misma. A los pacientes sometidos a PENS del dermatoma T7 se les explicó que esta terapia iba orientada a reducirles el apetito y facilitar así el cumplimiento de la dieta, como ocurrió en un estudio previo de nuestro grupo, en los que se estimuló el dermatoma T67.
Dieta 1.200kcal/día
| Valores medios de hidratos de carbono 51%; proteínas 23%; grasas 26% |
| Desayuno |
| Leche desnatada 200cc o 2 yogures desnatados naturales |
| Pan 50g o 2 tostadas de pan tipo «biscotes» |
| Media mañana |
| Fruta (una pieza de 100g de manzana, pera, naranja, melocotón o kiwi) |
| Comida y cena |
| Primer plato a elegir entre: |
| Verduras 200gr: espinacas, acelgas, berenjenas, berros, endivias, lechuga, coliflor, champiñón, puerros, espárragos, escarola, repollo, pepino, pimientos, tomates, alternando cocinadas o en ensalada, o 150g de judías verdes, remolacha, zanahoria, alcachofa o coles de Bruselas |
| Sopa de verduras |
| Consomé desgrasado (consumo libre) |
| Gazpacho andaluz, siempre que en su elaboración no se use pan y escasa cantidad de aceite, recordando que hay que respetar la cantidad de aceite indicada para todo el día |
| Sopa de pasta, sémola, arroz o tapioca (15g en seco) |
| Segundo plato a elegir entre: |
| Pescado blanco 120gr |
| Carne de pollo, pavo, conejo, ternera 100gr |
| Huevos una unidad |
| Ensalada de tomate y lechuga (o cualquier otra verdura cruda) 150gr una sola vez al día |
| Postre, a elegir entre: |
| Fruta (una pieza de 100g de manzana, pera, naranja, melocotón, kiwi, melocotón o 200g de sandía) |
| Pan 25gr |
| Merienda |
| 200cc de leche desnatada sola o con café o té |
| Aceite para todo el día: 30cc (2 cucharadas soperas) |
A todos los pacientes se les realizó una analítica sanguínea en ayunas antes de empezar el tratamiento y otra a los 7 días de finalizarlo (el intervalo entre ambas analíticas fue de 13 semanas). Identificador ClinicalTrials.gov: NCT02122874.
Metodología de la neuroestimulación percutánea del dermatoma T7La PENS fue realizada por cirujanos de los centros participantes en el estudio. Se empleó el dispositivo Urgent PC 200 Neuromodulation System® (Uroplasty, Minnetonka, MN, EE. UU.). Los pacientes fueron sometidos a sesiones semanales de 30min de duración durante 12 semanas consecutivas. El paciente se colocaba en posición de decúbito supino y sin necesidad de anestesia local, se insertaba una aguja en el cuadrante superior izquierdo del abdomen en línea medioclavicular, 4cm por debajo del reborde costal (coincidiendo con el dermatoma T7). A pesar de que podía haberse elegido cualquier lado para la estimulación, la elección del lado izquierdo se debió a cuestiones logísticas del mobiliario en las consultas, que permitía la ubicación del neuroestimulador sobre una mesita auxiliar adyacente a la camilla. La aguja se introducía perpendicular al plano de la pared abdominal con una profundidad de 0,5-1cm Se confirmaba la correcta colocación cuando el paciente notaba una sensación de «hormigueo eléctrico» al menos 5cm lateral al punto de inserción de la aguja, dentro del territorio del dermatoma T7. La PENS se aplicó a una frecuencia de 20Hz y con la máxima amplitud (0-20mA) antes de causar dolor.
VariablesAl comienzo y al final del tratamiento se evaluó el peso, el IMC, la pérdida de peso, la glucemia, la hemoglobina glucosilada, la insulina y el HOMA. Se solicitó a los pacientes sometidos a PENS del dermatoma T7 que cuantificaran su percepción de apetito antes y después del tratamiento mediante una escala visual analógica (EVA) con puntuación desde 0 (ausencia de apetito) hasta 10 (sensación de apetito incontrolable).
EstadísticaTodos los análisis estadísticos fueron realizados con el programa SPSS 17.0 (SPSS Inc., Chicago, IL). Las variables cuantitativas que seguían una distribución normal fueron definidas por media y desviación típica; en las variables no gaussianas se emplearon la mediana y el rango. Las variables cualitativas fueron definidas por número de casos y porcentaje. La comparación entre variables se realizó con los test «t» de Student y correlación de Pearson para variables cuantitativas con distribución gaussiana, y los test de Mann Whitney, Friedman y Spearman para variables no gaussianas. Se consideraron significativos valores de p<0,05.
ResultadosSe incluyeron 60 pacientes en el estudio: 30 pacientes en cada grupo. La muestra estaba formada por un 80% de mujeres y un 20% de hombres con una edad media de 48,9+13,8 años (intervalo 29-72 años). No hubo diferencias significativas en edad y sexo entre grupos.
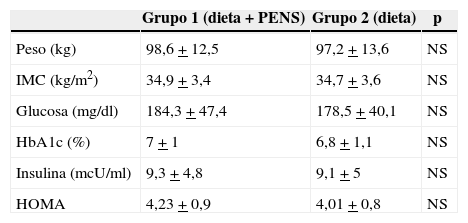
Los valores de peso, IMC, glucosa, hemoglobina glucosilada, insulina y HOMA preoperatorios en ambos grupos se muestran en la tabla 2. No se observaron diferencias significativas entre grupos.
Valores antropométricos y analíticos antes de comenzar el tratamiento en ambos grupos
| Grupo 1 (dieta+PENS) | Grupo 2 (dieta) | p | |
|---|---|---|---|
| Peso (kg) | 98,6+12,5 | 97,2+13,6 | NS |
| IMC (kg/m2) | 34,9+3,4 | 34,7+3,6 | NS |
| Glucosa (mg/dl) | 184,3+47,4 | 178,5+40,1 | NS |
| HbA1c (%) | 7+1 | 6,8+1,1 | NS |
| Insulina (mcU/ml) | 9,3+4,8 | 9,1+5 | NS |
| HOMA | 4,23+0,9 | 4,01+0,8 | NS |
HbA1c: Hemoglobina glicosilada; HOMA se calcula según la fórmula glucosa × insulina/405; IMC: Índice de Masa Corporal.
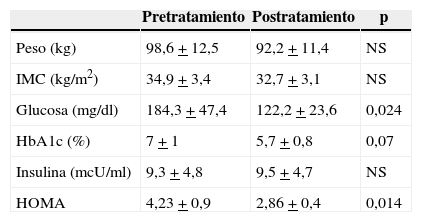
Al finalizar el tratamiento en el grupo 1 se observa un descenso significativo en la glucemia (descenso medio de 62,1mg/dl; IC 95%: 41,6-82,6; p=0,024) y en el HOMA (descenso medio 1,37; IC 95%: 0,63-2,11; p=0,014). Se aprecia una tendencia al descenso en los valores de hemoglobina glucosilada, sin alcanzar la significación estadística (p=0,014) (tabla 3).
Valores pre y postratamiento en el grupo 1
| Pretratamiento | Postratamiento | p | |
|---|---|---|---|
| Peso (kg) | 98,6+12,5 | 92,2+11,4 | NS |
| IMC (kg/m2) | 34,9+3,4 | 32,7+3,1 | NS |
| Glucosa (mg/dl) | 184,3+47,4 | 122,2+23,6 | 0,024 |
| HbA1c (%) | 7+1 | 5,7+0,8 | 0,07 |
| Insulina (mcU/ml) | 9,3+4,8 | 9,5+4,7 | NS |
| HOMA | 4,23+0,9 | 2,86+0,4 | 0,014 |
HbA1c: Hemoglobina glicosilada; HOMA se calcula según la fórmula glucosa × insulina/405; IMC: Índice de Masa Corporal.
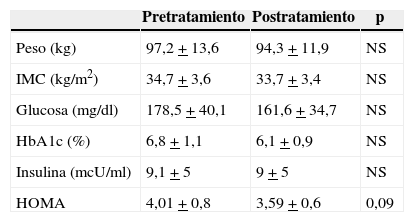
En el grupo 2 no se observan diferencias significativas en los valores pre y postratamiento en ninguno de los parámetros analizados (tabla 4). Solo se aprecia una tendencia al descenso de los valores de HOMA (p=0,09).
Valores pre y postratamiento en el grupo 2
| Pretratamiento | Postratamiento | p | |
|---|---|---|---|
| Peso (kg) | 97,2+13,6 | 94,3+11,9 | NS |
| IMC (kg/m2) | 34,7+3,6 | 33,7+3,4 | NS |
| Glucosa (mg/dl) | 178,5+40,1 | 161,6+34,7 | NS |
| HbA1c (%) | 6,8+1,1 | 6,1+0,9 | NS |
| Insulina (mcU/ml) | 9,1+5 | 9+5 | NS |
| HOMA | 4,01+0,8 | 3,59+0,6 | 0,09 |
HbA1c: Hemoglobina glicosilada; HOMA se calcula según la fórmula glucosa × insulina/405; IMC: Índice de Masa Corporal.
Se aprecia una tendencia a mayor pérdida de peso en el grupo 1 (6,4+1,4kg frente a 2,5+0,8kg; p=0,08).
En el grupo 2 se observó una correlación directa entre la pérdida de peso y el descenso del HOMA (Pearson 0,345; p=0,043). En el grupo 1 no pudo determinarse esa correlación (p=0,258).
Cuantificación del apetito en el grupo 1La mediana de apetito antes del tratamiento fue 6 (rango 4-10) y la mediana tras finalizar el mismo fue 4 (rango 3-7) (p=0,215).
DiscusiónEl efecto de la PENS ha sido ampliamente demostrado en la neuroestimulación del nervio tibial posterior para el tratamiento de la incontinencia anal y urinaria, al crear un reflejo somato-somático8,9. Recientemente, nuestro grupo ha publicado el primer estudio acerca del uso de la PENS del dermatoma T6 para reducir el apetito y, como resultado de ello, obtener una pérdida de peso significativa. En este caso se crea un reflejo somato-autonómico cuya vía eferente son las ramas del nervio vago que van a inervar de forma específica el estómago. Como consecuencia de esta estimulación parasimpática el estómago enlentece su vaciamiento y aumenta la sensación de plenitud, lo que se traduce en una reducción de la sensación de apetito7. El presente estudio se basa en el mismo fundamento que este último trabajo mencionado, al crearse también un reflejo somato-autonómico, cuya vía aferente son las terminaciones nerviosas sensitivas del dermatoma T7 y la vía eferente son las ramas parasimpáticas del nervio vago que van a estimular la glándula pancreática. A pesar de que se aprecia una tendencia a mayor pérdida de peso en el grupo sometido a PENS del dermatoma T7, esta no alcanza la obtenida en nuestro estudio previo con PENS del dermatoma T6. A la hora de evaluar la cuantificación la percepción de apetito, el descenso tras finalizar el tratamiento no es estadísticamente significativo. No obstante, esa tendencia a mayor pérdida de peso y esa leve reducción del apetito tras PENS del dermatoma T7 posiblemente pueda deberse a una leve estimulación colateral de terminaciones nerviosas del dermatoma T6, por su proximidad al dermatoma T7.
Está ampliamente demostrado que la pérdida de peso mejora la glucemia, fundamentalmente por reducción de la resistencia a la acción de la insulina en tejidos periféricos. Esto también suele determinar un descenso del hiperinsulinismo10,11. En los pacientes del grupo 2 de nuestro estudio (sometidos a tratamiento dietético exclusivamente) no se observa un descenso significativo de la glucemia, pero sí una tendencia al descenso de los valores de HOMA tras el tratamiento dietético (p=0,09), manteniéndose los valores de insulina prácticamente inalterados (9,1mcU/ml pretratamiento y 9mcU/ml postratamiento). En este caso no se observa un descenso significativo en los niveles de insulina, si bien estos se encuentran dentro del rango de la normalidad tanto antes como después del tratamiento (rango normal 5-20mcU/ml). Por tanto, al no haber hiperinsulinismo no se produce una reducción significativa en la secreción pancreática de insulina.
En el grupo de pacientes sometidos a PENS del dermatoma T7, asociada a dieta, se obtiene una reducción significativa de la glucemia (p=0,024) y de los valores de HOMA (p=0,014) y una tendencia al descenso de la hemoglobina glucosilada. Aquí se aprecia un ascenso no significativo de los valores de insulina (9,3mcU/ml pretratamiento y 9,5mcU/ml tras finalizar el mismo). Por tanto, podríamos deducir que la estimulación pancreática mediante PENS del dermatoma T7 no produce un aumento significativo de la secreción pancreática de insulina. Lo lógico sería pensar entonces que el mayor descenso en la glucemia se debe a la reducción de la resistencia insulínica como consecuencia de la pérdida de peso. En nuestro grupo de pacientes sometidos solo a dieta la pérdida de peso muestra una correlación directa con el descenso del HOMA. Sin embargo, en los pacientes sometidos a PENS, además de la dieta, se pierde esta correlación directa, por lo que la mayor pérdida de peso en este grupo de pacientes no justifica completamente el mayor descenso en la resistencia insulínica.
La estimulación parasimpática de la glándula pancreática, además de sus efectos propios sobre la glándula, produce una inhibición del sistema nervioso simpático, lo que supone un descenso en la liberación de hormonas contrarreguladoras (adrenalina, hormona de crecimiento y cortisol). Estas hormonas producen un aumento de la síntesis de glucosa endógena y suprimen su utilización en tejidos periféricos, fundamentalmente en el músculo, condicionando así la resistencia a la acción de la insulina12. Por tanto, la inhibición del sistema nervioso simpático por estimulación parasimpática del páncreas podría justificar, al menos en parte, el descenso en la resistencia insulínica tras PENS del dermatoma T7. En nuestra opinión, posiblemente sea este el principal mecanismo fisiopatolágico que justifique los efectos de la neuromodulación sobre la homeostasis de la glucemia.
Como hemos mencionado anteriormente, durante la PENS del dermatoma T7, posiblemente también se active parcialmente el reflejo del dermatoma T6. El retraso en el vaciamiento gástrico que produce inhibe la liberación de grelina por el fundus gástrico13,14. La inhibición de la grelina ha demostrado que aumenta la secreción pancreática de insulina y reduce la resistencia a su acción periférica, especialmente en el tejido adiposo, por lo que esta acción resulta más llamativa en pacientes obesos15. Por esto, un cierto grado de inhibición de la grelina puede también favorecer el descenso del HOMA. En nuestro estudio previo sobre PENS del dermatoma T6 no objetivamos un descenso significativo de la glucemia tras el tratamiento y no analizamos el HOMA. No obstante, la mayoría de pacientes incluidos en ese estudio previo no eran diabéticos, por lo que no se pueden extraer datos concluyentes de ese análisis7. Serían necesarios nuevos estudios sobre PENS del dermatoma T6 en pacientes diabéticos y su efecto sobre la glucemia y la resistencia insulínica.
Las principales limitaciones de este estudio son que se trata de un ensayo clínico no ciego y la posible temporalidad de los resultados, dado que se incluyen solo los resultados tras finalizar el tratamiento. Deben realizarse nuevos estudios evaluando la duración en el tiempo del beneficio obtenido sobre la homeostasis de la glucosa, así como analizar el efecto de la neuroestimulación del dermatoma T6 sobre los niveles de hormonas (adrenalina, hormona de crecimiento, cortisol, grelina, etc.).
ConclusiónLa neuroestimulación percutánea del dermatoma T7 asociada a dieta de 1.200Kcal/día produce una mayor reducción de la glucemia y de la resistencia insulínica que la obtenida solo mediante dieta tras 3 meses de tratamiento.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.