La rehabilitación multimodal (RMM) consiste en la combinación de varios métodos para el manejo del paciente quirúrgico encaminados a disminuir la respuesta al estrés quirúrgico y una recuperación más cómoda y precoz.
ObjetivoValorar la implantación de un protocolo de RMM en una unidad de cirugía colorrectal y comparar los resultados con el modelo tradicional, valorando su eficacia en cuanto a recuperación y estancia.
Material y métodosSe analizó prospectiva y aleatorizadamente a 119 pacientes intervenidos de forma electiva por enfermedad colorrectal entre 2009 y 2010. Se asignó a 58 pacientes al grupo tradicional y 61 al grupo RMM. La RMM consistió en educación preoperatoria, alimentación y movilización precoz.
ResultadosAmbos grupos eran homogéneos en cuanto a variables preoperatorias valoradas, el tipo de enfermedad y los procedimientos realizados. La sonda nasogástrica se mantuvo en el grupo tradicional 4 (1-9) días frente a 1 (0-2) días en el grupo RMM, sin diferencias en la reinserción de la sonda. Se encontraron diferencias significativas en el inicio de la dieta líquida —3 (1-5) días tradicional, frente a 0 (0-2) con RMM (p<0,001)— y expulsión de la primera ventosidad —3 (1-6) días tradicional, frente a 1 (1-3) con RMM (p<0,001)—. Los pacientes en el grupo RMM tuvieron una estancia postoperatoria de 4,15±2,18, frente a 9,23±6,97 días del grupo tradicional (p<0,001). No se encontraron diferencias significativas en las complicaciones o reingresos.
ConclusionesLa RMM en cirugía colorrectal en el sistema sanitario público español es factible y permite una más rápida recuperación de los pacientes operados sin aumentar las complicaciones, permitiendo un alta hospitalaria precoz.
Multimodal rehabilitation (MMR) consists of a combination of several methods for management of the surgical patient, designed to reduce the response to surgical stress and a more comfortable and earlier recovery.
ObjectiveTo assess the implementation of an MMR protocol in a Colorectal Surgery Unit, and to compare the results with the traditional model, as well as assessing its efficacy as regards recovery and hospital stay.
Material and methodsA total of 119 patients who received elective surgery for colorectal diseases in a period during 2009-2010 were prospectively and randomly analysed. The patients were divided into 2 groups: 58 patients were assigned to the traditional group and 61 to the MMR group. The MMR group protocol consisted of, preoperative education, early feeding and mobilisation.
ResultsBoth groups were homogeneous as regards the preoperative variables evaluated, the type of disease and the procedures carried out. The nasogastric tube was kept in place for 4 (1-9) days compared to 1 day (0-2) in the MMR group, with no differences in the number of re-insertions. Significant differences were found in the introduction of a liquid diet (3 [1-5] days traditional versus 0 [0-2] MMR) (P<.001), and passing of first flatulence (3 [1-6] days traditional versus 1 [1-3] MMR) (P<.001). The MMR group had a postoperative stay of 4.15±2.18 versus 9.23±6.97 days in the traditional group (P<.001). No significant differences were found in complications or readmissions.
ConclusionsMMR in colorectal surgery in the Spanish public health system is feasible and enables surgical patients to have a faster recovery without increasing complications, leading to an earlier hospital discharge.
El fast-track en cirugía o rehabilitación multimodal consiste en la combinación de varios métodos para el manejo del paciente quirúrgico antes y durante la intervención y en el postoperatorio inmediato, encaminados a disminuir la respuesta al estrés quirúrgico y la disfunción orgánica ocasionada por este, con el fin de lograr que la recuperación de los pacientes sea más cómoda y precoz1. Se han publicado en la última década muchos trabajos que se muestran a favor de un cambio en las costumbres del manejo del enfermo operado2 y que, basándose en la evidencia científica actual, proponen unas medidas controvertidas por algunos profesionales de la cirugía española. Por este motivo se ideó poner en práctica estos conceptos en el ámbito en el que nos movemos3,4.
El principal objetivo del trabajo clínico es valorar si es posible aplicar un protocolo de manejo multimodal para mejorar la recuperación postoperatoria en una unidad de cirugía colorrectal dentro del Sistema Público de Salud español, comparándolo con el manejo tradicional, evaluando a su vez su eficacia en cuanto a una recuperación postoperatoria precoz, una disminución de la morbilidad y una estancia hospitalaria más breve.
Material y métodosSe ha realizado un estudio prospectivo y aleatorizado entre junio de 2009 y febrero de 2010. Se reclutó a los pacientes del área del Hospital Clínico Universitario de Valencia operados por el mismo equipo de seis cirujanos que componen la Unidad de Coloproctología en el Servicio de Cirugía General. El Comité de Ética del hospital aprobó previamente el estudio.
Criterios de inclusiónPacientes mayores de 18 años. American Society of Anesthesiologists (ASA) score del 1 a 4. Cirugía electiva abdominal que requiera resección de colon/recto (incluidas reoperaciones) por laparotomía o laparoscopia. Consentimiento informado firmado. Residentes en Valencia (área metropolitana).
Criterios de exclusiónPacientes que no fueran independientes para el desarrollo de las actividades de su vida diaria (pacientes incapaces de caminar, lavarse o comer solos). Cirugía realizada de urgencias como perforaciones con peritonitis, oclusión intestinal o hemorragia digestiva baja masiva.
Protocolo del estudioSe reclutó a los pacientes en las consultas externas de coloproctología, donde se les proponía participar en el estudio tras proporcionarles información detallada. Una vez firmado el consentimiento informado, se los aleatorizó mediante «sobres cerrados» a cualquiera de los siguientes grupos: un grupo con manejo postoperatorio tradicional y otro grupo con rehabilitación multimodal (RMM).
Grupo RMMPreoperatorioSe citó a los pacientes incluidos en el grupo RMM a una segunda consulta con una enfermera becada para el estudio, en la que se informaba a ellos y sus acompañantes, de forma verbal y escrita, de cuáles serían las recomendaciones y actuaciones que se irían tomando en el periodo posterior a la intervención, tanto por el personal sanitario como por ellos mismos. Los pacientes ingresaron el día previo a la cirugía. Se les administró heparina de bajo peso molecular subcutánea en función del peso del paciente y profilaxis antibiótica según las recomendaciones actuales. Tomaban una dieta normal hasta la noche anterior a la cirugía, sin preparación del colon. Dentro de este grupo, se hizo una preparación mecánica anterograda del colon con Fosfosoda® tan sólo a los pacientes en que se planeó una colonoscopia intraoperatoria o se preveía la realización de una ileostomía en asa.
Postoperatorio inmediato (día 0)Se retiró la sonda nasogástrica antes de la extubación y se administró en el grupo de RMM oxígeno a concentraciones elevadas (80%), intraoperatoriamente y durante 2 h en el postoperatorio. A los pacientes del grupo RMM se les animó a beber agua ad libitum a las 6 h y levantarse de la cama si les era posible, y se pautó ondansetrón i.v. 4 mg/8h.
Día 1 postoperatorioEl primer día postoperatorio iniciaron tolerancia a dieta pastosa si habían tolerado los líquidos, sin necesidad de esperar signos de inicio de la motilidad intestinal. Se les recomendó andar y realizar fisioterapia respiratoria. Se retiró la sonda vesical.
Día 2 postoperatorioSe retiraron perfusiones y se inició dieta normal si ha presentado una adecuada tolerancia a la dieta pastosa. Se retiraron drenajes si procedía.
Día 3 postoperatorioSe les dio el alta si cumplían los criterios descritos en la tabla 1 (que son los mismos para los dos grupos de pacientes).
Criterios de alta hospitalaria
| No presentar ningún tipo de complicación postoperatoria |
| Expulsión de gases y/o heces |
| Analgesia oral suficiente |
| Independencia para actividades vida diaria (deambulación, alimentación, aseo, etc.) |
| Haber tolerado tres o más comidas sólidas |
| Mostrarse de acuerdo con el alta |
| En pacientes portadores de estoma, débito controlado |
Los pacientes ingresaron el día previo a la cirugía sin la consulta con la enfermera becada descrita anteriormente. Se les administró heparina de bajo peso molecular subcutánea en función del peso del paciente y profilaxis antibiótica según las recomendaciones actuales. La preparación del colon para la cirugía se hizo mediante dieta líquida los 2 días previos a la cirugía y preparación anterograda del colon con Fosfosoda®.
Postoperatorio inmediato (día 0)Se mantuvo la sonda nasogástrica y se administró oxígeno por gafas nasales a 2 l/min. No se pautó un antiemético, al portar la sonda nasogástrica.
Día 1 postoperatorioLos enfermos del grupo tradicional permanecieron el primer día aún con la sonda nasogástrica puesta y a dieta absoluta, sin iniciar tolerancia hasta que hubiera signos de recuperación del tránsito intestinal, como ruidos hidroaéreos o expulsión de gases.
Día 2 postoperatorioEn el grupo tradicional se retiró la sonda vesical y los drenajes, y se inició tolerancia al agua si había alguno de los signos de recuperación del tránsito intestinal descritos en el apartado anterior.
Día 3 postoperatorio y posterioresSe inició dieta líquida si procedía y se progresó según tolerancia y si había signos de recuperación del tránsito intestinal. Se comenzó la movilización del paciente. Se les dio el alta si cumplían los criterios descritos en la tabla 1 (que son los mismos para los dos grupos de pacientes).
El reingreso se define como el paciente al que se ha dado de alta y ha vuelto a ingresar con estancia intrahospitalaria de al menos 1 día. No se considera reingresos a los pacientes que acuden puntualmente para consulta a urgencias.
El seguimiento fue de 30 días postoperatorios.
Los gastos económicos se calculan según el coste de los días de estancia hospitalarios. Estos datos se obtienen de datos oficiales emitidos por la dirección económica del Hospital Clínico Universitario, Valencia. El coste de la estancia actualmente es de 341,70 euros por día.
Protocolo anestésicoEl anestesiólogo fue el mismo para todos los enfermos del estudio. La inducción se realiza con 5mg/kg de tiopental sódico, 0,5mg/kg de besilato de atracurio y 0,1μg/kg de fentanilo, y la anestesia se mantiene con 1,4-2,5% de sevoflurano, con dosis según la edad del paciente. El fentanilo adicional se administra a demanda. Durante el acto quirúrgico se administran fluidos a 15ml/kg/h con el objeto de mantener una presión sistólica por encima de 90 mmHg y una diuresis de al menos 80ml/h. Las pérdidas sanguíneas en principio se reponen con coloides o cristaloides. La temperatura corporal se mantiene mediante una cubierta neumática. Tras la extubación, el paciente se traslada a la sala de recuperación postanestésica. La selección del tipo de analgesia postoperatoria es a criterio del anestesiológo. En ambos grupos el control postoperatorio del dolor se realizó mediante una bomba de infusión intravenosa controlada por el paciente (bomba Hospira®) con morfina 0,5mg/ml, en perfusión continua de 1 ml/h y con bolos de 2 ml/h y un tiempo de cierre de 15 min, según las «pautas analgésicas generales de control del dolor postoperatorio» aceptado en octubre de 2006 por el Servicio de Anestesiología del Hospital Clínico de Valencia, o un catéter epidural con bupivacaína al 0,125% a una velocidad de 10ml/h en perfusión continua. Para el estudio y la evaluación del dolor postoperatorio, a todos los pacientes se les solicitó que rellenaran, desde el primer día postoperatorio y hasta el día del alta, una escala visual analógica para registrar el nivel de dolor de cada enfermo. El segundo día postoperatorio, en ambos grupos se retiró la PCA intravenosa o la epidural, pautando paracetamol i.v. 1 g/8 h alternando cada 4 h con metamizol magnésico i.v. 2 g/8 h.
Estudio estadísticoSe realizó un análisis de los resultados con intención de tratar. El tamaño muestral se calculó con base en estudios previamente publicados5. Asumiendo una diferencia esperada entre un grupo y otro en cuanto a estancia hospitalaria de 2,5 días y una desviación estándar de 4,8 días, se obtiene un tamaño muestral de 58 pacientes en cada brazo del estudio, con una potencia del 80%. Se utilizaron los tests de la U de Mann-Whitney, Kruskall-Wallis, test exacto de Fisher con la razón de verosimilitud o con el test de χ2 de Pearson, según correspondiera. El análisis estadístico se realizó con el programa SPSS® versión 15.0 para Windows (SPSS, Inc.; Chicago, Illinois, Estados Unidos).
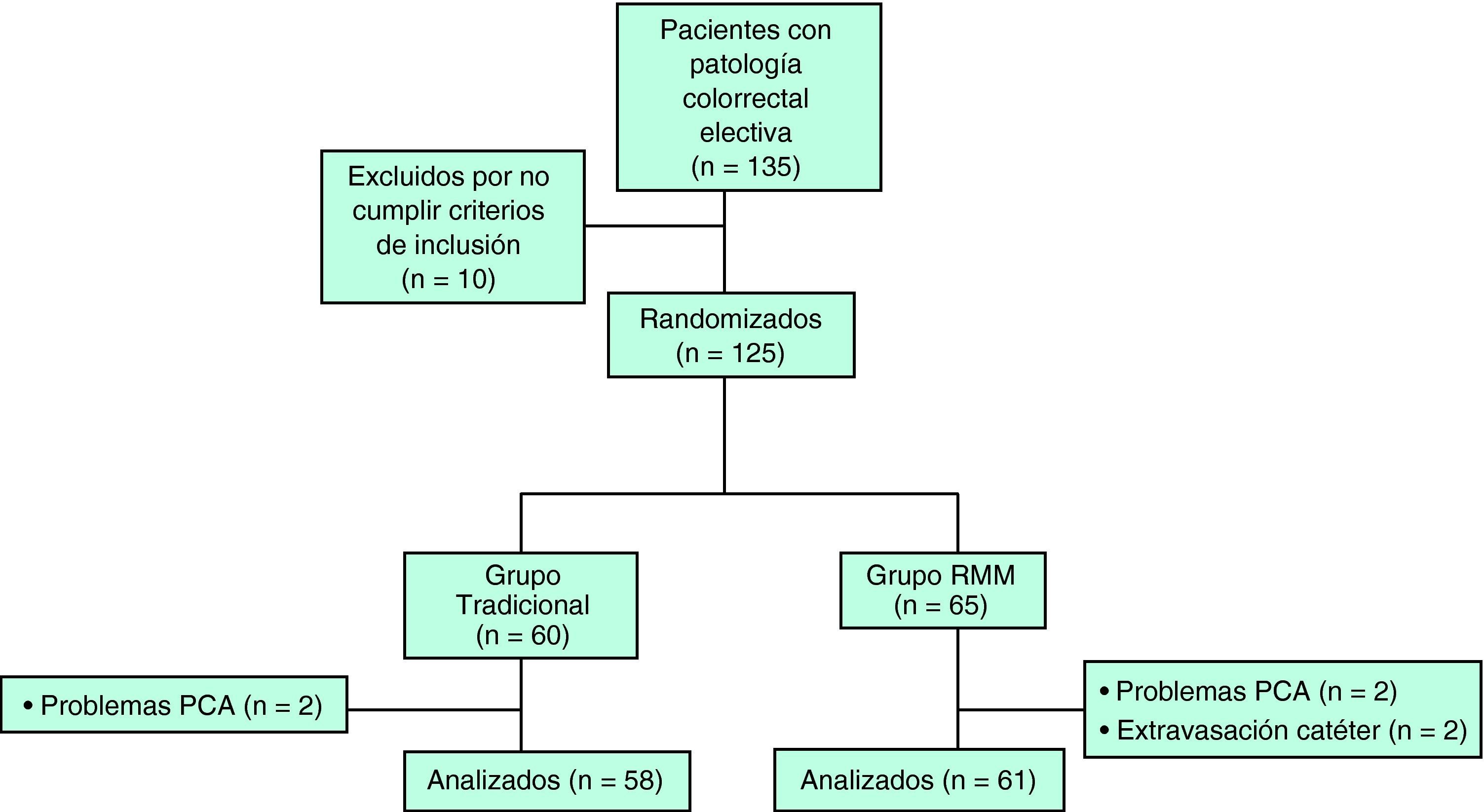
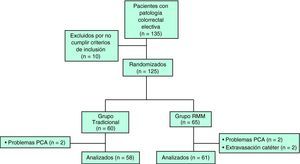
ResultadosSe incluyó a 135 pacientes consecutivos según el perfil del estudio de la figura 1. Se excluyó a 10 pacientes por no cumplir los criterios de inclusión (1 paciente encamado y 9 urgencias, 2 sigmoiditis perforadas, 4 neoplasias de colon en oclusión, 1 colitis isquémica, 1 vólvulo de sigma y 1 paciente no dio su consentimiento para participar en el estudio). Se excluyó a 2 pacientes del grupo tradicional y 2 del grupo RMM por fallo de la bomba de la PCA, y a 2 pacientes del grupo RMM por extravasación del catéter epidural. Finalmente, se analizaron los datos de 58 pacientes adjudicados al brazo tradicional y 61 del brazo RMM. Ambos grupos eran homogéneos en cuanto a las variables demográficas y preoperatorias de los pacientes (tabla 2). Las características de los grupos relacionadas con la intervención se muestran en la tabla 3. No se encontraron diferencias significativas entre los grupos en cuanto a la tasa de reinserción de la sonda nasogástrica, vómitos o íleo postoperatorio. Aunque los pacientes del grupo RMM sí presentaron mayor incidencia de náuseas postoperatorias, no hubo que recolocar la sonda ni se retrasó el inicio de la tolerancia oral. Se aprecia una disminución significativa en la estancia hospitalaria media entre los pacientes del grupo tradicional y los enfermos del grupo con manejo multimodal (p<0,001). No se evidenciaron diferencias significativas en la tasa de reingresos entre uno y otro grupo. Tampoco se evidenciaron diferencias en la tasa de complicaciones. Las complicaciones de herida se definen como evisceración o infección de la herida. Las complicaciones de la sonda urinaria se definen como retención aguda de orina o infección urinaria. Se encontraron significativamente más complicaciones de la sonda urinaria en el grupo tradicional (tabla 4). Como complicaciones de la vía periférica, se tiene en cuenta la extravasación o flebitis; por último, como complicaciones respiratorias, se consideran la infección respiratoria y la tromboembolia pulmonar (tabla 4).
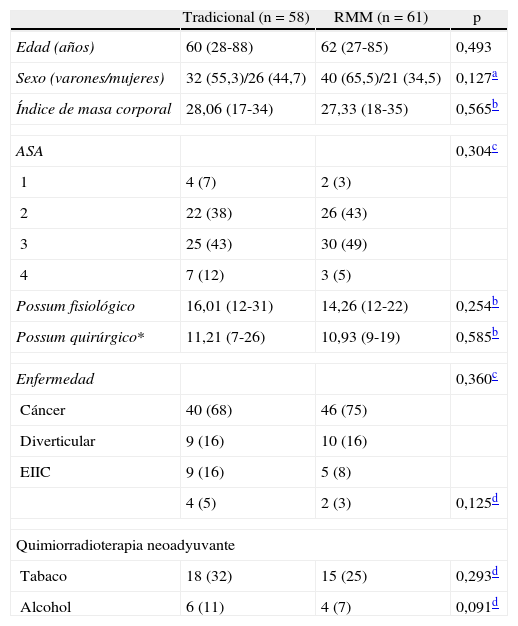
Características de los dos grupos
| Tradicional (n=58) | RMM (n=61) | p | |
| Edad (años) | 60 (28-88) | 62 (27-85) | 0,493 |
| Sexo (varones/mujeres) | 32 (55,3)/26 (44,7) | 40 (65,5)/21 (34,5) | 0,127a |
| Índice de masa corporal | 28,06 (17-34) | 27,33 (18-35) | 0,565b |
| ASA | 0,304c | ||
| 1 | 4 (7) | 2 (3) | |
| 2 | 22 (38) | 26 (43) | |
| 3 | 25 (43) | 30 (49) | |
| 4 | 7 (12) | 3 (5) | |
| Possum fisiológico | 16,01 (12-31) | 14,26 (12-22) | 0,254b |
| Possum quirúrgico* | 11,21 (7-26) | 10,93 (9-19) | 0,585b |
| Enfermedad | 0,360c | ||
| Cáncer | 40 (68) | 46 (75) | |
| Diverticular | 9 (16) | 10 (16) | |
| EIIC | 9 (16) | 5 (8) | |
| 4 (5) | 2 (3) | 0,125d | |
| Quimiorradioterapia neoadyuvante | |||
| Tabaco | 18 (32) | 15 (25) | 0,293d |
| Alcohol | 6 (11) | 4 (7) | 0,091d |
ASA: American Society Anesthesiology score; EIIC: enfermedad inflamatoria intestinal crónica.
Los valores expresan n (%) o mediana (intervalo).
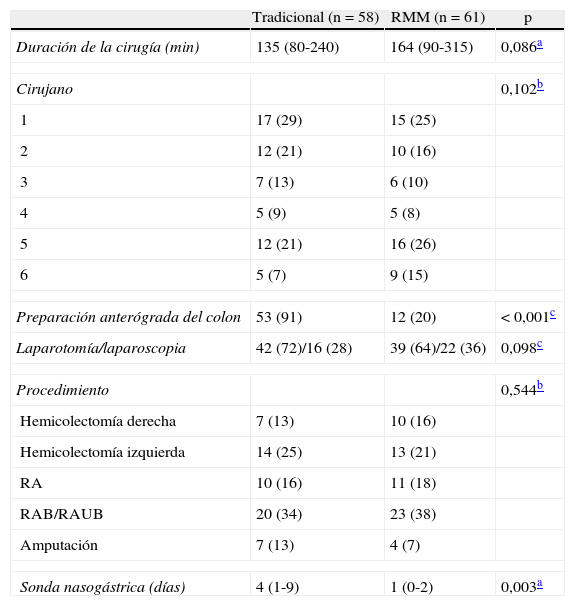
Datos operatorios
| Tradicional (n=58) | RMM (n=61) | p | |
| Duración de la cirugía (min) | 135 (80-240) | 164 (90-315) | 0,086a |
| Cirujano | 0,102b | ||
| 1 | 17 (29) | 15 (25) | |
| 2 | 12 (21) | 10 (16) | |
| 3 | 7 (13) | 6 (10) | |
| 4 | 5 (9) | 5 (8) | |
| 5 | 12 (21) | 16 (26) | |
| 6 | 5 (7) | 9 (15) | |
| Preparación anterógrada del colon | 53 (91) | 12 (20) | < 0,001c |
| Laparotomía/laparoscopia | 42 (72)/16 (28) | 39 (64)/22 (36) | 0,098c |
| Procedimiento | 0,544b | ||
| Hemicolectomía derecha | 7 (13) | 10 (16) | |
| Hemicolectomía izquierda | 14 (25) | 13 (21) | |
| RA | 10 (16) | 11 (18) | |
| RAB/RAUB | 20 (34) | 23 (38) | |
| Amputación | 7 (13) | 4 (7) | |
| Sonda nasogástrica (días) | 4 (1-9) | 1 (0-2) | 0,003a |
RA: resección anterior de sigma; RAB: resección anterior baja; RAUB: resección anterior ultrabaja.
Los valores expresan n (%) o mediana (intervalo).
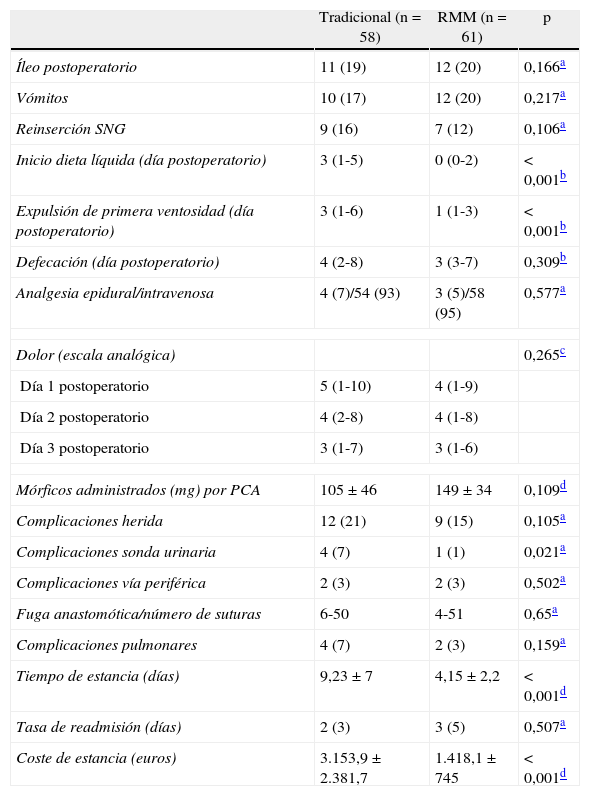
Resultados tras el análisis de ambos grupos
| Tradicional (n=58) | RMM (n=61) | p | |
| Íleo postoperatorio | 11 (19) | 12 (20) | 0,166a |
| Vómitos | 10 (17) | 12 (20) | 0,217a |
| Reinserción SNG | 9 (16) | 7 (12) | 0,106a |
| Inicio dieta líquida (día postoperatorio) | 3 (1-5) | 0 (0-2) | < 0,001b |
| Expulsión de primera ventosidad (día postoperatorio) | 3 (1-6) | 1 (1-3) | < 0,001b |
| Defecación (día postoperatorio) | 4 (2-8) | 3 (3-7) | 0,309b |
| Analgesia epidural/intravenosa | 4 (7)/54 (93) | 3 (5)/58 (95) | 0,577a |
| Dolor (escala analógica) | 0,265c | ||
| Día 1 postoperatorio | 5 (1-10) | 4 (1-9) | |
| Día 2 postoperatorio | 4 (2-8) | 4 (1-8) | |
| Día 3 postoperatorio | 3 (1-7) | 3 (1-6) | |
| Mórficos administrados (mg) por PCA | 105±46 | 149±34 | 0,109d |
| Complicaciones herida | 12 (21) | 9 (15) | 0,105a |
| Complicaciones sonda urinaria | 4 (7) | 1 (1) | 0,021a |
| Complicaciones vía periférica | 2 (3) | 2 (3) | 0,502a |
| Fuga anastomótica/número de suturas | 6-50 | 4-51 | 0,65a |
| Complicaciones pulmonares | 4 (7) | 2 (3) | 0,159a |
| Tiempo de estancia (días) | 9,23±7 | 4,15±2,2 | < 0,001d |
| Tasa de readmisión (días) | 2 (3) | 3 (5) | 0,507a |
| Coste de estancia (euros) | 3.153,9±2.381,7 | 1.418,1±745 | < 0,001d |
PCA: analgesia controlada por el paciente.
Los valores expresan n (%), mediana (intervalo) o media±desviación estándar.
Este trabajo se ha diseñado para comprobar si la aplicación de RMM en cirugía colorrectal permite una mejor y más rápida recuperación de los pacientes. La evidencia científica actual parece indicar que estos regímenes mejoran los síntomas secundarios a la agresión quirúrgica y podrían permitir un descenso en la morbilidad y de los costes sanitarios, un alta precoz y una más rápida reincorporación a las actividades habituales.
La estancia hospitalaria después de una cirugía colorrectal sigue siendo demasiado larga. Una revisión multicéntrica demostró una estancia postoperatoria de 11,8 días6. Hace ya más de 10 años, en pacientes operados por vía laparoscópica se planteó la posibilidad de disminuir de forma significativa la estancia postoperatoria aplicando un abordaje multimodal7. Kehlet et al publicaron una vía clínica que conseguía una mediana de estancias de 2 días y un retorno a la función gastrointestinal en 2-3 días en más del 90% de los pacientes, sin complicaciones cardiopulmonares y con una tasa de readmisiones del 15% en un grupo de 60 pacientes8. En 2005 publicaron otro estudio en el que se recogen las características de los cuidados preoperatorios de 295 hospitales europeos9. En más del 85% de los pacientes se utilizó preparación mecánica del colon. La sonda nasogástrica se retiró en el 78% de los pacientes sometidos a laparoscopia el mismo día de la intervención quirúrgica, mientras que esto sólo se produjo en el 33% de los pacientes sometidos a laparotomía. La utilización de analgesia epidural se utilizó tan sólo en el 8% de los hospitales en Francia, en el 12% de Italia y España, en el 27% en Estados Unidos y Alemania, y en el 67% en Reino Unido. En España la media para el inicio de la tolerancia a líquidos fue de 5,3 días, y de 6,9 días para la ingesta normal. A los 5 días en el 82% de los pacientes sometidos a cirugía laparoscópica se había recuperado la función intestinal, frente al 53% de los pacientes de cirugía abierta. En Europa la mayoría de los pacientes (media del 53%) caminaban con normalidad el tercer día postoperatorio, mientras que en Estados Unidos el 71% caminaban el segundo día y el 85%, en el tercero. En Europa los pacientes sometidos a cirugía laparoscópica tuvieron una estancia hospitalaria menor que los sometidos a laparotomía (8,7 frente a 11,9 días), con una estancia de 11,8 días en los pacientes en que se produjo conversión a cirugía abierta9.
Los resultados de este estudio reflejan la posibilidad de implementar un protocolo de RMM en España con éxito y resultados comparables a los que describen otros autores. Tanto la estancia media como la tasa de reingresos y morbilidad postoperatoria están en los límites inferiores que se describen en la literatura tanto en el grupo RMM como en el tradicional. En el grupo RMM la estancia media postoperatoria se sitúa en 4,23 para el Hospital Clínico Universitario de Valencia (HCUV), frente 3,3-6,6 días por otros autores, y la tasa de reingresos en 4,91 días para HCUV, frente a 3,1-21,3 días en la literatura5,8,10–13. Asimismo la morbilidad postoperatoria no se vio incrementada en este estudio. Sólo a un 6% de los pacientes de este estudio se les administró analgesia postoperatoria por vía epidural, lo cual está por debajo incluso del 12% reflejado en le encuesta de Kehlet et al9. Estas cifras reflejan la dificultad o la resistencia a la introducción de analgesia epidural para el control del dolor postoperatorio habitual en nuestro ámbito. Actualmente la presión asistencial y la falta de quirófanos limitan el tiempo del anestesista para poder colocar un catéter epidural. También la percepción, tanto de los cirujanos como de los anestesistas, de que esto no es del todo necesario es una realidad. Aun así, siendo el uso de la analgesia epidural el patrón de referencia para el control del dolor postoperatorio, nuestros resultados no se han visto perjudicados por el uso de analgesia intravenosa en la mayoría de nuestros pacientes. Estos resultados son similares a los descritos por Delaney et al en su estudio de analgesia epidural frente intravenosa en el contexto de un protocolo de RMM5. Se encontraron significativamente más complicaciones de la sonda urinaria en el grupo tradicional. Esto podría justificar por qué se mantuvo la sonda urinaria más tiempo en el grupo tradicional que en el grupo RMM. Avances en fisiopatología perioperatoria demuestran que son diversos los factores que contribuyen a aumentar la morbilidad postoperatoria y prolongar la estancia y la convalecencia del enfermo operado14. Aún están por definirse claramente cuáles son las pautas clave de un protocolo de RMM y cuáles son secundarias.
Una de las principales preocupaciones acerca del alta hospitalaria temprana es si es seguro dar de alta a los pacientes a los 3-5 días de la cirugía. La experiencia publicada indica que la fuga anastomótica ocurre raramente en pacientes manejados con RMM y, además, hasta la fecha no se han publicado efectos adversos cuando se ha instruido a los pacientes para acudir al hospital si presentan síntomas sospechosos en su domicilio7,12. Nosotros no creemos que sea inapropiado o inseguro, debido a que la proximidad al hospital (criterio de inclusión) y un seguimiento ambulatorio del paciente ajustado en la primera semana tras el alta permiten la readmisión en pocas horas en caso de que aparezca algún signo de complicación. Puede discutirse si la cirugía de colon con un manejo RMM puede conllevar una mayor tasa de readmisiones según la literatura, pero más del 65% de estas readmisiones ocurren después del quinto día postoperatorio y, por lo tanto, no podrían prevenirse con una estancia hospitalaria mayor15. Según nuestro estudio, la tasa de readmisiones no muestra diferencias entre uno y otro grupo.
Los criterios de alta en este protocolo de actuación son los mismos que los clásicos, aunque se consiguen antes. Además, el coste de la estancia incluidos los reingresos es significativamente menor si se aplica el RMM10–12, lo que es fundamental para generar servicios de calidad pero de modo eficiente. La puesta en marcha de estos programas requiere un esfuerzo coordinado de todo el personal sanitario, no sólo de los médicos y los profesionales de enfermería. También existe una curva de aprendizaje, y los resultados y el cumplimiento de la RMM mejoran con la mayor experiencia de los profesionales implicados en la aplicación de dichos programas16. La evidencia científica parece indicar que estos regímenes mejoran la función biológica del individuo ante la cirugía reduciendo las complicaciones postoperatorias, permitiendo un descenso en la morbilidad y un postoperatorio más cómodo para el paciente. Además, la introducción de la rehabilitación multimodal reduce el coste y la estancia de los pacientes sometidos a procedimientos quirúrgicos generales. Así, estos programas son del interés de la administración hospitalaria, que suele poner restricciones económicas a los cuidados de los pacientes. No debemos olvidar, sin embargo, que lo primero y el objetivo más importante es proporcionar el mayor estándar de calidad en los cuidados a todos y cada uno de los pacientes17.
La aplicación de RMM en cirugía colorrectal en el sistema sanitario público español es factible y permite una mejor y más rápida recuperación de los pacientes operados sin aumentar las complicaciones que puedan presentarse y permitiendo un alta hospitalaria precoz.
FinanciaciónBeca EVES (Escuela Valenciana de Estudios de Salud) de la Generalitat Valenciana Conselleria de Sanitat 2007. Beca FIS (Instituto de Salud Carlos III) del Ministerio de Ciencia e Innovación, 2008.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
A la Sra. Lorena Cholvi, por su ayuda en la elaboración del trabajo y la recogida de datos.
Registro: el estudio se ha registrado en Clinical Trials.gov con número de registro: NCT01148394.