El GIST (gastrointestinal stromal tumor) es la neoplasia mesenquimal más frecuente del tubo digestivo. Suele presentarse en mayores de 50 años, independientemente del sexo, con una incidencia de unos 5.000 casos anuales en EE. UU.1. Se origina a partir de las células de Cajal estromales y la localización más frecuente es el estómago (60%), seguida de yeyuno e íleon (30%). Si bien frecuentemente se extiende a hígado y peritoneo, los GIST rara vez metastatizan en linfáticos, pulmón o lugares extraintestinales. Su característica principal es que presentan mutaciones en el protoncogén KIT o en el receptor alfa del factor de crecimiento derivado de las plaquetas (platelet-derived growth factor receptor alpha [PDGRF]), dianas contra las que han sido desarrolladas terapias antitumorales basadas en el bloqueo de tirosinquinasas, tales como imatinib y sunitinib, habiéndose convertido en el paradigma de la terapia molecular dirigida contra el cáncer. Alrededor del 80% de pacientes responden a imatinib, frente al 5% a quimioterapia convencional, hecho que ha permitido aumentar la mediana de supervivencia de pacientes con enfermedad metastásica desde los 15 meses hasta casi los 5 años1,2.
En el manejo del GIST primario, imatinib puede ser utilizado como terapia neoadyuvante en aquellos casos irresecables de inicio, así como adyuvante tras el tratamiento quirúrgico. En casos de GIST recurrentes, localmente avanzados o metastásicos es donde tiene su mayor indicación la asociación de imatinib con cirugías de citorreducción más agresivas, dejando las terapias farmacológicas de segunda línea, como sunitinib, para los casos resistentes a imatinib2.
En tumores localmente avanzados, esta citorreducción radical podría necesitar incluir los procedimientos de peritonectomía descritos en 1995 por Sugarbaker3, asociados o no a quimioterapia perioperatoria intraperitoneal, dados los excelentes resultados obtenidos en el tratamiento de la enfermedad maligna peritoneal de diferentes orígenes4. No obstante, en el caso del GIST con diseminación peritoneal (denominado GISTosis peritoneal por Sugarbaker), la indicación de estos procedimientos es actualmente discutida4.
A razón de un caso de estas características, nos planteamos valorar el papel de la cirugía de citorreducción y la quimioterapia intraperitoneal hipertérmica (hyperthermic intraperitoneal chemotherapy [HIPEC]) en estos pacientes.
Se trató de una mujer de 45 años, diagnosticada e intervenida de GIST yeyunal (c-KIT +) con riesgo alto, que recibió adyuvancia con imatinib durante un año. Tres meses después de finalizar el tratamiento presentó una recidiva siendo intervenida nuevamente. Dada la edad de la paciente, el tipo de enfermedad, la cirugía realizada y la recaída al año, se propuso reiniciar imatinib 400mg/día de forma continuada. No obstante, la paciente presentó progresión a nivel peritoneal por lo que se modificó el esquema terapéutico a sunitinib 37,5mg/24h, consiguiendo una respuesta parcial durante los primeros meses y una estabilización al año del tratamiento con este fármaco. En esta situación, y ante la potencial resecabilidad del tumor mediante procedimientos de peritonectomía, se derivó a nuestra unidad para intervención quirúrgica.
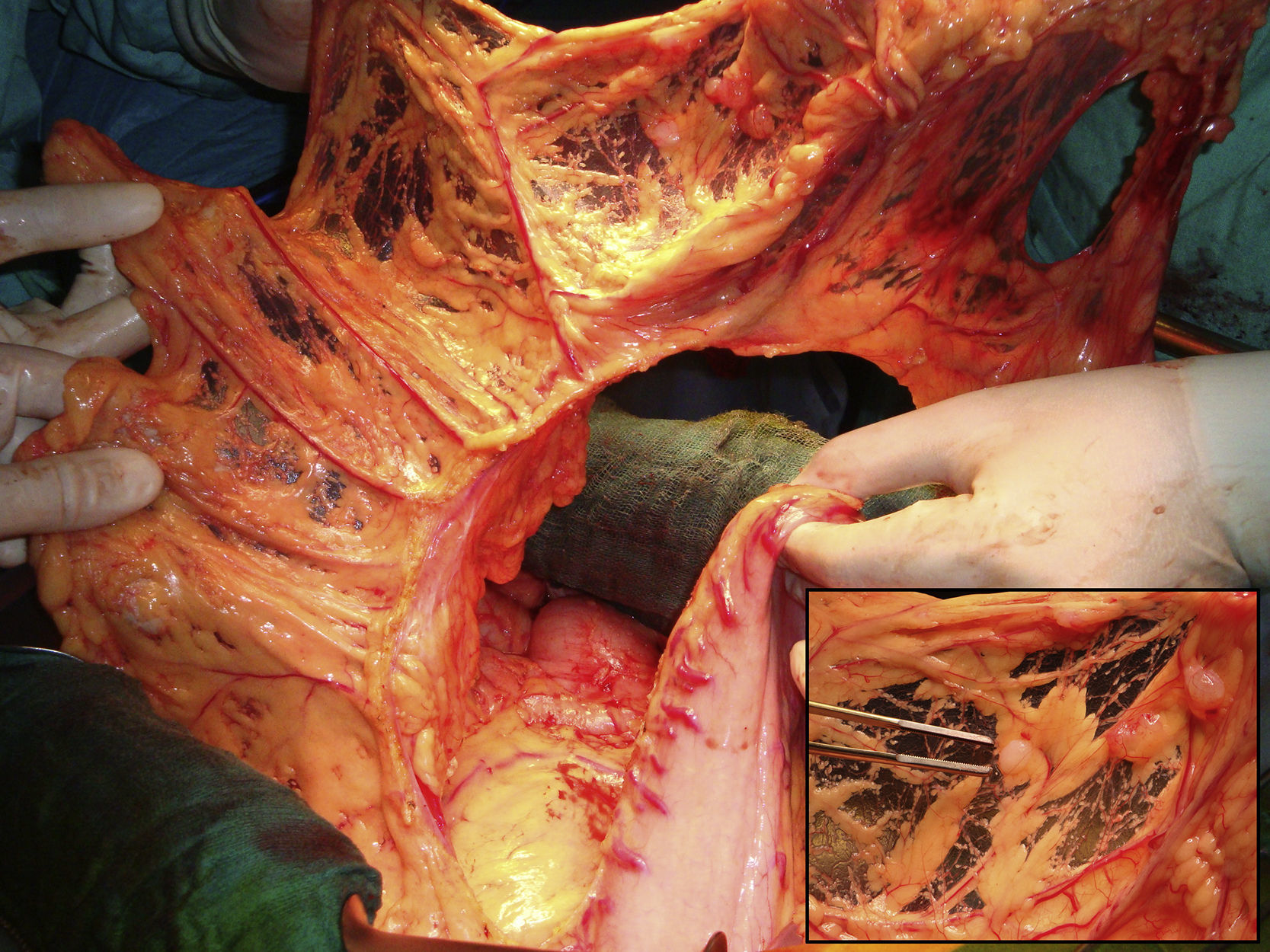
Los hallazgos operatorios demostraron varias masas tumorales mayores de 5cm, así como múltiples implantes centimétricos y subcentimétricos diseminados en cavidad abdominal (peritoneal cancer index [PCI] 23/39) (fig. 1), lográndose cirugía de citorreducción óptima (CC-0) tras peritonectomía diafragmática derecha, parietocólica bilateral y pélvica completa; resección de recto-sigma, útero, trompas, ovarios, vesícula biliar y omento mayor (fig. 2). Además se realizó exéresis-electrofulguración de lesiones mesentéricas aisladas. Previamente a la anastomosis colorrectal, la paciente recibió una hora de HIPEC con cisplatino y doxorrubicina. El postoperatorio transcurrió sin incidencias y, en el momento de la redacción de este artículo, 6 meses después de la cirugía, se encuentra asintomática y libre de enfermedad.
Nos encontramos, por tanto, ante un caso de GIST localmente avanzado, resistente a tratamiento con imatininb y con respuesta parcial a sunitinib. Ante la opción de quimioterapia paliativa exclusivamente, mostramos la posibilidad de una cirugía radical potencialmente curativa a través de los procedimientos preconizados por Sugarbaker3. La sistematización de las técnicas quirúrgicas de peritonectomía ha permitido conseguir cifras de baja morbimortalidad en centros con experiencia y, de esta forma, expandir sus indicaciones. En este sentido, respecto a los GIST, al igual que el tratamiento intensivo de la enfermedad metastásica hepática5,6, lograr citorreducciones óptimas (CC-0) permitiría mejorar la supervivencia7–10, sobre todo en aquellos pacientes respondedores a quimioterapia.
Por otro lado, el uso de HIPEC con cisplatino y doxorrubicina en este tipo tumor es más controvertido debido a la baja sensibilidad del GIST frente a estos citostáticos. La realización de ensayos clínicos al respecto permitirá conocer la verdadera influencia de HIPEC en la secuencia evolutiva de esta neoplasia. En nuestra opinión, y de acuerdo con las recomendaciones de Sugarbaker4, los procedimientos de peritonectomía con múltiples resecciones viscerales estarían indicados en aquellos pacientes en los que se puedan alcanzar citorreducciones completas, dejando la opción de HIPEC para aquellos casos en los que, además, exista un bajo riesgo de dehiscencia anastomótica o fístula. De igual manera, se aconseja su realización en centros con experiencia y siempre bajo la perspectiva de estudios clínicos.