Castleman's disease is an uncommon entity that often mimics the clinical and radiological features of a neoplasm. We present a case of plasma cell type Castleman's disease, located in the juxtarenal retroperitoneal region, that was initially thought to be a retroperitoneal sarcoma. We review the various subtypes of this disease, with their different presentations and diagnostic and therapeutic approaches.
Introducción
La enfermedad de Castleman ha recibido diversas denominaciones desde su descripción original. En relación a su etiología, todavía no aclarada, se han planteado varias hipótesis, considerándose en la actualidad como un proceso proliferativo ganglionar no neoplásico de etiología desconocida. Existen dos formas de presentación clínica (forma localizada y forma multicéntrica), con un pronóstico a largo plazo diferente, pero que comparten una histología similar.
Pretendemos con este trabajo aportar un caso de esta enfermedad poco frecuente y alertar sobre la presentación ocasional en forma de masa que asemeja una neoplasia retroperitoneal, pudiendo provocar dificultades en el abordaje, tanto diagnóstico como terapéutico.
Caso clínico
Varón de 66 años que ingresó para estudio de un síndrome constitucional con aumento de la velocidad de sedimentación globular (VSG). Entre sus antecedentes personales destacaba cardiopatía hipertensiva con insuficiencia aórtica y mitral leves, sin insuficiencia cardíaca, espondilitis tuberculosa en 1995 de D12-L1 con absceso paravertebral, que requirió drenaje y fijación quirúrgica con osteosíntesis. Dos meses antes del ingreso presentó astenia, anorexia, pérdida de 8 kg de peso, sudación profusa vespertina y fiebre de hasta 38 °C. La exploración física fue anodina. La analítica puso de manifiesto anemia normocítica normocrómica VSG de 150 en la primera hora, LDH de 209, y el resto de parámetros dentro de la normalidad. La radiografía de tórax y la función tiroidea eran normales, y la baciloscopia de esputo, los hemocultivos, la serología de Brucella y la sangre oculta en heces negativos. En la eco-TAC abdominal se apreció una masa sólida, homogénea, retroperitoneal, de más de 10 cm de diámetro, en la región yuxtarrenal izquierda, con desplazamiento anterior del riñón que contactaba con el flanco izquierdo, datos que indicaban sarcoma retroperitoneal. No se evidenciaban otras lesiones ocupantes de espacio, adenopatías retroperitoneales ni carcinomatosis peritoneal. Se practicó punción con aguja fina dirigida por TAC sin que se pudiera obtener material suficiente para establecer un diagnóstico citológico definitivo.
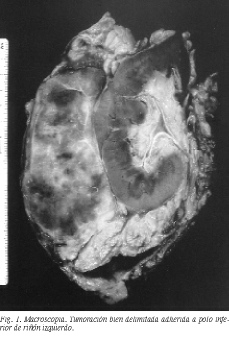
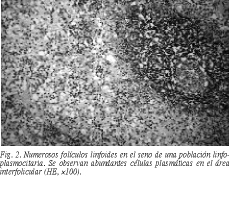
Con el diagnóstico de sospecha de sarcoma retroperitoneal se realizó una laparotomía media, hallando una tumoración retroperitoneal en el flanco izquierdo, bien delimitada, con aparente infiltración del polo renal inferior izquierdo y con la presencia de adenopatías alrededor de la vena renal izquierda y sin diseminación retroperitoneal. No había evidencia de extensión extratumoral ni ascitis. Se realizó tumorectomía, con nefrectomía y extirpación del uréter. La histología puso de manifiesto una tumoración bien delimitada, de 10,5 cm de diámetro, adherida a la cápsula renal, sin infiltración del parénquima renal (fig. 1). El diagnóstico fue enfermedad de Castleman de tipo plasmocelular (fig. 2). El paciente fue dado de alta sin complicaciones. La respuesta a la extirpación de la masa fue favorable, con normalización de la clínica y de la analítica.
Discusión
La enfermedad de Castleman ha recibido numerosas denominaciones, como hiperplasia angiofolicular linfoide, hiperplasia de ganglios linfáticos gigante, hamartoma linfoide, linfoma benigno y linforreticuloma folicular1,2. Se trata de un proceso proliferativo ganglionar no neoplásico de etiología desconocida1,3,4,10,13. Se han propuesto varias hipótesis etiológicas, sin que se haya podido demostrar ninguna de ellas1,5. La mayoría de los autores coinciden en considerarla como una hiperplasia linfoide reactiva. Está relacionada con procesos inflamatorios crónicos y con alteraciones de la inmunorregulación1,2,6,7, a veces en el seno de enfermedades autoinmunes. Otros autores la consideran como una neoplasia benigna (hamartoma), e incluso se ha apuntado la posibilidad de que se trate de un proceso con un componente hereditario. Recientemente ha sido relacionada con la infección por el herpesvirus tipo 82,8.
Existen dos formas de presentación clínica muy diferente, pero que comparten una histología similar2,9. La forma clásica de presentación es en forma de una masa solitaria (enfermedad de Castleman localizada) de crecimiento lento, que generalmente se diagnostica de forma incidental o en el estudio de un síndrome constitucional. La otra forma de presentación es la afectación sistémica del sistema linfático (enfermedad de Castleman multisistémica)2, con una clínica similar a la linfadenopatía angioinmunoblástica y asociación con linfomas, sarcoma de Kaposi2,11,12 y otras enfermedades del sistema inmunitario. Se ha sugerido por ello la participación de una inmunodeficiencia celular en la génesis de este proceso. El curso clínico es mucho más agresivo y comporta peor pronóstico1,2,7.
Hay dos variedades histológicas con localización y sintomatología diferentes:
1. La variedad hialinovascular es la más frecuente (90%)1,5,6,10,13. Se caracteriza por presentarse en pacientes jóvenes1,6, con localización normalmente mediastínica y ausencia de sintomatología acompañante, por lo que su diagnóstico suele ser incidental1. Histológicamente se comporta como una hiperplasia folicular distribuida por todo el ganglio de forma regular, con folículos pequeños y centros germinales rodeados por tejido colágeno o material hialino, presentando centros claros rodeados por un anillo periférico de linfocitos maduros, con disposición en "capas de cebolla". Los vasos penetran en el centro de los folículos y muestran una pared hialina con células endoteliales prominentes. El área interfolicular tiene una marcada vascularización, con masas hialinas de localización perivascular, células plasmáticas, eosinófilos y linfocitos en diferentes estadios de maduración1.
2. El tipo plasmocelular (7%) afecta con más frecuencia a los ganglios mesentéricos y retroperitoneales1,2, y en el 50% de los casos producen manifestaciones sistémicas que mimetizan un proceso neoplásico. La clínica más frecuente es astenia, anorexia, pérdida de peso, fiebre, sudación y artralgias. Los datos de laboratorio son los habituales de los procesos inflamatorios crónicos, con anemia normocítica normocrómica que se debe a la secreción de factores antieritropoyéticos5,14, aumento de VSG, hipoalbuminemia, hipergammaglobulinemia policlonal y trombopenia1,2,3,13,15. La histología se diferencia de la anterior en que los centros germinales son más grandes y con más celularidad, y por tener áreas interfoliculares formadas por células plasmáticas, con una hialinización menos llamativa. Este tipo es el más frecuente en la forma multisistémica2.
3. Se han descrito formas mixtas, lo que sugiere la posibilidad de dos estadios evolutivos del mismo proceso9.
Abordaje diagnóstico y terapéutico del tipo plasmocelular
Desde el punto de vista quirúrgico, la diferencia más importante en relación con el tipo hialinovascular es su frecuente localización retroperitoneal, lo que le hace, mediante las técnicas radiológicas disponibles, difícil de diferenciar de otros tumores retroperitoneales, en especial de los sarcomas13,16,. Por otro lado, su diagnóstico es complicado, ya que se comporta como una masa que mimetiza una neoplasia17 debido a su sintomatología sistémica. Los signos radiológicos son inespecíficos, encontrando una masa homogénea, en ocasiones calcificada, que con el contraste intravenoso se realza en el tipo hialino (debido a su gran vascularización), pero no en el tipo plasmocelular. En la resonancia magnética se visualiza como una masa de baja intensidad, hipercaptante en T1 y homogénea en T2, a diferencia de los sarcomas, en los que se manifiesta como una señal hipercaptante heterogénea en T213,18,19.
Otros factores que añaden confusión son las descripciones de casos de enfermedad de Castleman retroperitoneales adheridos a las glándulas suprarrenales, hilio renal o en contacto con alguno de los polos renales20. En estos casos se plantea el diagnóstico diferencial entre un tumor renal con extensión retroperitoneal, un tumor retroperitoneal que invade secundariamente el riñón o una tumoración benigna. En estos pacientes, la única forma de conseguir un diagnóstico exacto es la obtención directa de la histología1,3. Sin embargo, algunos autores desaconsejan, al menos de forma relativa, la punción de los tumores retroperitoneales, ante la posibilidad de extensión local del tumor. Por otra parte, la PAAF no siempre permite obtener el material adecuado, por lo que la opción más razonable es la biopsia intraoperatoria13,21.
El tratamiento de elección es la extirpación quirúrgica2,3,15 de toda la masa y de las adenopatías adyacentes, con preservación de los tejidos circundantes13. En caso de no poder realizar la resección completa, se recomienda la radioterapia adyuvante para reducir al máximo el riesgo de recidiva local1,2. Dado que se han descrito casos de recidivas locales2,22 y mayor riesgo de desarrollo de neoplasias hematológicas, como leucemia y linfomas2,6,23, es preciso realizar controles anuales tras la cirugía22.