Introducción
La carcinomatosis peritoneal es el principal problema del tratamiento de los pacientes con cáncer avanzado, por cuanto además de no haber ningún tratamiento con eficacia demostrada, conlleva indefectiblemente la muerte en breve tiempo desde el diagnóstico1.
Desde 1982, el Dr. Sugarbaker2 planteó la diseminación peritoneal como un estadio locorregional de la enfermedad y desarrolló una nueva alternativa terapéutica basada en el tratamiento de la enfermedad macroscópica mediante cirugía citorreductora radical oncológica merced a las peritonectomías por él desarrolladas3, seguido del tratamiento de la enfermedad residual microscópica con la aplicación directa de quimioterapia de intensificación locorregional modulada por hipertermia.
Pues bien, la consideración de la enfermedad como un estadio locorregional, frente a la contemplación de una fase terminal clásica, ha permitido que se planteen nuevas opciones terapéuticas en determinados pacientes; con este nuevo esquema terapéutico se obtienen supervivencias a 5 años en carcinomatosis originadas por varias enfermedades4-6, y en grupos selectos incluso curaciones de enfermos hasta ahora erróneamente considerados terminales7-10.
La base racional de la superioridad de este tratamiento, unido a la comunicación repetida de mejores resultados que los tratamientos convencionales, justifica que esté siendo motivo de renovado interés en muchos centros y grupos de tratamiento.
La implantación y el desarrollo en España de esta estrategia completa de tratamiento desde 1997 han permitido obtener, en la experiencia del autor, los primeros beneficios en algunos pacientes con supervivencias, a medio y largo plazo, hasta ahora impensables con ningún otro tratamiento alternativo conocido en el momento actual.
Material y método
Presentamos un estudio prospectivo, no aleatorizado de fase II, de todos los pacientes atendidos consecutivamente desde el 14 de febrero de 1997 al 14 de febrero de 2007 por el mismo cirujano (A.G.P.), siguiendo los mismos criterios del protocolo del triple tratamiento combinado, sin ningún paciente perdido en el seguimiento posterior prospectivo.
Selección de pacientes
Los criterios de inclusión, reflejados en la tabla 1, fueron: edad entre 18 y 75 años; buen estado general, ECOG 1 o 2; sin comorbilidades limitantes, entendiendo por ello una correcta función cardiorrespiratoria, hepática y renal; diagnóstico de certeza de la enfermedad abdominal confirmado por estudio histológico; sin enfermedad extraabdominal; que no recibieran radioterapia o quimioterapia los 30 días anteriores a la citorreducción, y consentimiento informado firmado. Desde el año 2003, se solicita además a todos los pacientes la autorización de uso compasivo del Ministerio de Sanidad.
Cirugía citorreductora
Hemos realizado 110 citorreducciones en 71 pacientes afectos de carcinomatosis peritoneal difusa de diverso origen, que constituyen el objeto de estudio del presente trabajo. El volumen y extensión de la carcinomatosis se determinó siempre con el índice de carcinomatosis peritoneal (ICP)11,12. El mismo cirujano trató a todos los pacientes, siguiendo los mismos criterios de tratamiento, siempre con intención de conseguir una citorreducción completa potencialmente curativa, cuando fuera posible por la enfermedad y no pusiera en riesgo la integridad de la vida del paciente. La citorreducción se obtuvo mediante la técnica de peritonectomías descritas por Sugarbaker et al3,4; se realizaron cuantas peritonectomías y resecciones viscerales fueron necesarias, siempre limitadas exclusivamente a zonas afectas por tumor evidente. El grado de citorreducción alcanzado al final de la cirugía quedó también registrado prospectivamente acorde con el índice de citorreducción conseguida (ICC)13.
Quimioterapia intraperitoneal intraoperatoria hipertérmica (QIIH)
Finalizada la extirpación del tumor macroscópico y antes de proceder a cualquier reconstrucción del tránsito intestinal, se procedió a la colocación de un circuito de quimioterapia intraperitoneal mediante un catéter de Tenckoff® como vía de inyección y 3 drenajes de Jackson Pratt® como vías de extracción; con la ayuda de un sistema de circulación extracorpórea y un intercambiador de calor, se aplicó la QIIH según el esquema correspondiente al tipo de carcinomatosis tratada, según esquemas de protocolos reflejados en la tabla 2, con un flujo de perfusión continua de 1,5 l/min, para mantener la modulación de la hipertermia durante el tiempo de exposición al citostático; la técnica abierta o "técnica de coliseo"14, que empleamos siempre, permite la manipulación del abdomen para evitar lesiones por quemadura de contacto directo continuado y asegurar durante el procedimiento la distribución homogénea del citostático en toda la cavidad.
El ritmo de orina se optimiza hasta conseguir una diuresis > 200 ml/h durante el tiempo que dura la administración de la quimioterapia intraoperatoria, mediante hidratación con fármacos presores si se precisa para conseguir presión venosa central > 12 mmHg.
Quimioterapia intraperitoneal postoperatoria precoz (QIPP)
Nuestros pacientes, atendidos según los protocolos de Sugarbaker et al2,15,16, recibieron QIPP los días 1 a 5 del postoperatorio inmediato, mediante la administración del citostático del esquema correspondiente, según esquemas de protocolos reflejados en la tabla 2, a través del drenaje de Tenckoff y mantenido el citostático dentro de la cavidad durante 23 h mediante el cierre de todos los drenajes abdominales; esta operación se repitió por 5 días consecutivos.
Desde enero de 2005, iniciado el protocolo de oxaliplatino según Elias et al17-19, para el tratamiento de carcinomatosis de origen colorrectal y seudomixoma peritoneal apendicular, los pacientes que reciben este esquema de tratamiento no reciben QIPP postoperatoria inmediata.
Variables clínicas
Hemos estudiado la serie atendiendo al sexo, la edad, el tipo de carcinomatosis según su tumor primario, el intervalo entre la cirugía del tumor primario y la citorreducción, el número y tipo de cirugía previa acorde con el PSS (previous surgical score)13, la administración previa de quimioterapia sistémica adyuvante tras la resección del tumor primario y el número de líneas recibidas, el ICP observado durante la citorreducción, el grado de citorreducción alcanzado, el número de peritonectomías parietales practicadas, el número de resecciones viscerales, el número de anastomosis, el tiempo quirúrgico, las transfusiones y fluidoterapia usadas en la intervención, complicaciones postoperatorias, reintervenciones, estancia hospitalaria, práctica de una segunda o siguientes citorreducciones y supervivencia hasta la fecha de fallecimiento o cierre del estudio el 14 de febrero de 2007.
Análisis estadístico
El estudio estadístico de todos los parámetros clinicopatológicos relacionados con el tratamiento practicado se realizó usando como punto final la supervivencia total desde el inicio del tratamiento en nuestro programa. Se ha utilizado el test de Fisher corregido para el estudio de las variables categóricas y el test de Wilcoxon para los estudios comparativos de las diferencias de medianas de los factores estudiados. Se ha utilizado el método de Kaplan-Meier para el estudio de la supervivencia actuarial. Para estos estudios estadísticos se ha utilizado SPSS para Windows (versión 14 en castellano). Se estimó una diferencia significativa para p > 0,05.
Resultados
En esta serie personal, iniciada en Valencia (Hospital Clínico Universitario) el 14 de febrero de 1997 y continuada posteriormente desde julio de 1998 en Vitoria (Hospital Santiago Apóstol y Policlínica San José), hemos realizado 110 citorreducciones en 71 pacientes, 41 mujeres y 30 varones.
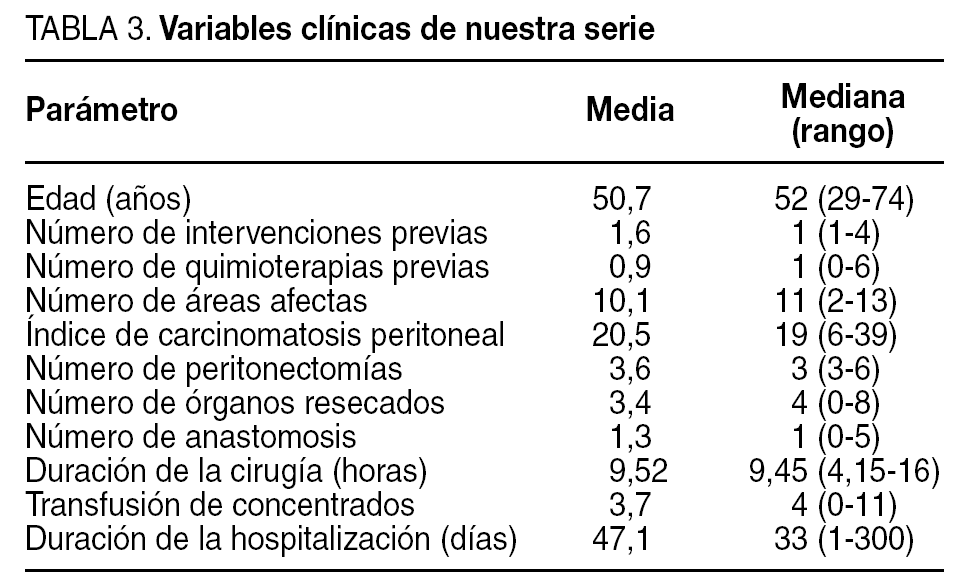
Las características de las variables clínicas de nuestra serie quedan reflejadas en la tabla 3.
Si bien en nuestra serie inicial los pacientes correspondían al Servicio Valenciano de Salud, en Vitoria, a pesar de ser un centro hospitalario privado, hemos atendido también a pacientes remitidos y financiados por los servicios públicos de salud de 11 comunidades autónomas y Portugal.
El origen de las carcinomatosis de los pacientes fue, en 29 ocasiones, por seudomixoma peritoneal; 21, por carcinomatosis difusa de colon; 7, por mesoteliomas primarios; 7, carcinomatosis por cáncer gástrico; 6, por carcinomatosis de origen ovárico, y un caso, por sarcomatosis difusa.
Todos los pacientes, salvo 5 (7%), habían sido intervenidos previamente, entre 1 y 4 veces; media, 1,6 intervenciones previas por paciente, y en el 60% de las ocasiones habían recibido tratamiento citostático sistémico con una o más líneas de tratamiento (rango, 1-6).
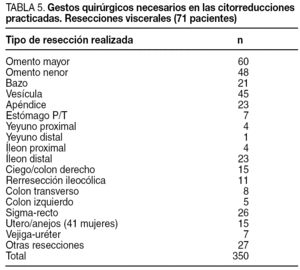
El ICP medio de los pacientes fue 20,5, lo que justifica que el tiempo operatorio medio fuera de 9,50 h, y que se precisaran 264 peritonectomías parietales (media, 3,6 peritonectomías parietales por paciente), junto con 350 resecciones viscerales (media, 3,4 órganos por paciente) y la práctica de 90 anastomosis digestivas (media, 1,3 por paciente), tal y como se refleja en las tablas 3-5.
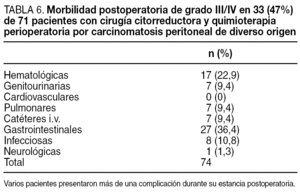
A pesar de lo avanzado de la enfermedad, fuimos capaces de conseguir una citorreducción completa CC0-CC1 en el 83% de las ocasiones, si bien conllevó una mortalidad del 9,8% (7 pacientes) y una morbilidad grado 3-4 en el 47% de los pacientes, motivo por el que la mediana de estancia hospitalaria es de 33 (rango, 1-300) días. El tipo de complicación, y las causas de mortalidad se muestran en las tablas 6 y 7.
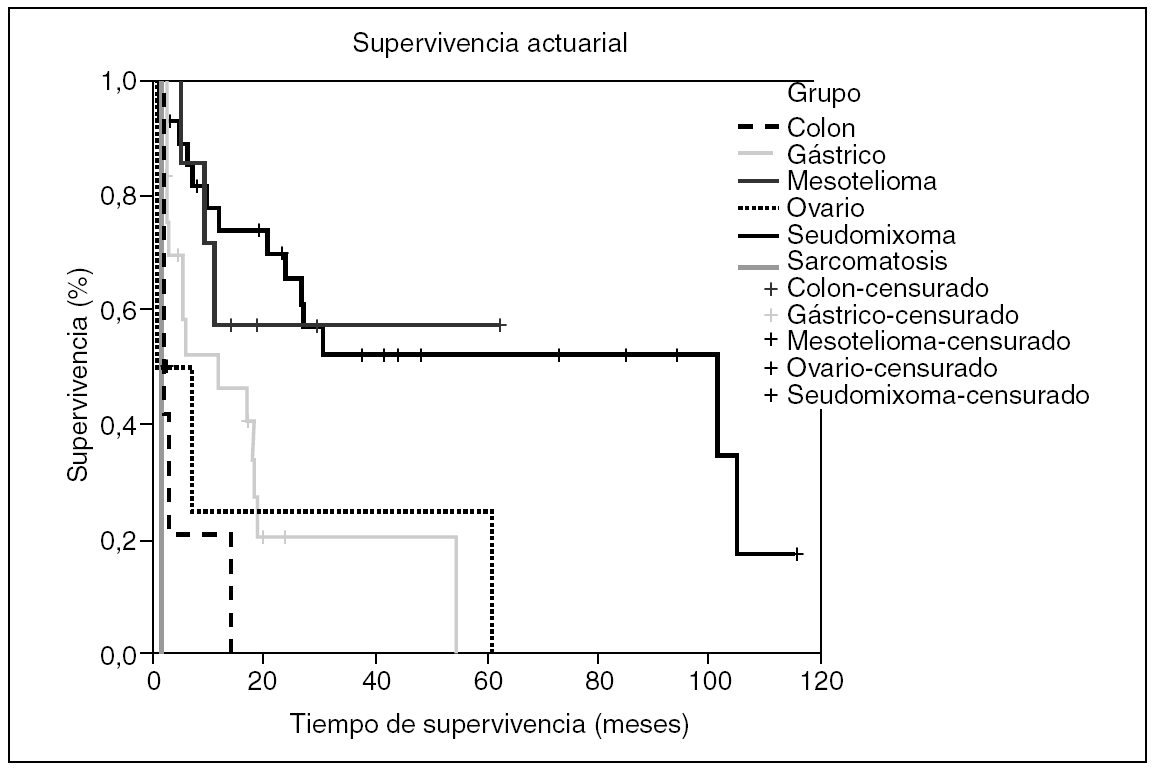
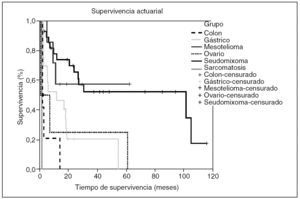
En esta serie con una mediana de seguimiento de 42 meses, la curva de supervivencia queda reflejada en la figura 1, el 42% de los pacientes ha superado los 18 meses; el 37%, más de 2 años; el 20%, 3 años, y el 12,6% ha superado los 5 años. Pacientes atendidos por carcinomatosis por seudomixoma peritoneal, carcinomatosis de ovario y mesoteliomas peritoneales malignos han superado los 5 años.
Fig. 1. Curva de supervivencia actuarial de la serie, atendiendo al tipo de carcinomatosis tratada.
Discusión
En este estudio, no aleatorizado y retrospectivo, se demuestra la reproducibilidad del protocolo de tratamiento de los pacientes afectos de carcinomatosis de diverso origen, en el que se pudo implantar con éxito tanto el protocolo de Sugarbaker2,15,16 como el de Elias17-21, ambos con aplicación de quimiohipertermia intraperitoneal intraoperatoria, sin problemas técnicos, y siempre se usó la técnica abierta conocida como técnica del coliseo14.
En nuestra serie los pacientes atendidos tenían una enfermedad diseminada abdominal de alto volumen, lo que justifica tanto la duración de las cirugías como el elevado número de gestos quirúrgicos necesarios para el control de la enfermedad, peritonectomías, resecciones viscerales orgánicas y anastomosis digestivas, muy superior a la experiencia del grupo del Instituto Nacional del Cáncer de Holanda22,23.
A pesar de la magnitud de la enfermedad, fuimos capaces de conseguir una citorredución completa CC0-CC1, en el 83% de nuestra serie, cifra que duplica la obtenida por el grupo holandés, si bien ese esfuerzo quirúrgico se ha visto traducido en mayores mortalidad (9,8%) y morbilidad (47%), cifras en el rango alto de las principales series mundiales del estudio de morbimortalidad tras aplicación de este triple tratamiento combinado24-26.
En nuestra serie con una mediana de seguimiento de 42 meses, al igual que en la experiencia de Sugarbaker27, hemos conseguido supervivencias a largo plazo en pacientes afectos de carcinomatosis por seudomixoma peritoneal, carcinomatosis de colon, carcinomatosis de ovario y mesoteliomas peritoneales malignos.
Conclusiones
Tal y como establece Sugarbaker, podemos afirmar que la aplicación de la nueva triple terapia combinada, en la que se suman los esfuerzos de la máxima cirugía, mediante la cirugía citorreductora para el tratamiento de la enfermedad macroscópica, unido a la aplicación de la máxima quimioterapia de intensificación regional modulada por la hipertermia como tratamiento de la enfermedad microscópica residual, constituye una alternativa terapéutica factible y reproducible en nuestro medio, y se ha aplicado con seguridad en 110 ocasiones consecutivas en los últimos 10 años en 71 pacientes afectos de carcinomatosis peritoneal de diversa índole.
En nuestra serie hemos constatado que hemos atendido a pacientes con un ICP elevado (mediana, 20,5), lo que se considera pacientes con alta carga tumoral abdominal y, por tanto, con mayor dificultad para conseguir un control quirúrgico de la enfermedad. Sin embargo, en el 83% de los casos hemos sido capaces de conseguir una citorreducción óptima (CC0-CC1), lo que ha permitido que, a pesar de lo avanzado de la enfermedad, el 42% de los pacientes disfrutaran al menos de 18 meses de sobrevida, e incluso se ha conseguido una supervivencia a 3 años del 20%, y supervivencias a largo plazo en 4 de las enfermedades atendidas.
En conclusión, en nuestra experiencia, la aplicación de la nueva triple terapia combinada es la mejor alternativa para estos desafortunados pacientes.
Correspondencia: Dr. A. Gómez Portilla.
Programa de Carcinomatosis Peritoneal. Policlínica San José.
Beato Tomás de Zumárraga, 10. 01008 Vitoria-Gasteiz. Álava.
España.
Correo electrónico: agomezpor@teleline.es
Manuscrito recibido el 11-5-2007 y aceptado el 4-9-2007.