La utilidad de la biopsia selectiva del ganglio centinela (BSGC) en pacientes con cáncer de mama que precisan quimioterapia neoadyuvante (QTN) es controvertida. Nuestro objetivo es analizar la tasa de detección (TD) y de falsos negativos (FN) de la BSGC tras QTN así como la influencia de la afectación ganglionar inicial y de los protocolos aplicados.
MétodosEstudio prospectivo observacional multicéntrico con mujeres con cáncer de mama tratadas con QTN y a las que se les realizó BSGC tras recibir la QTN y linfadenectomía posterior. Se calcularon las TD y las tasas de FN, tanto globales como dependientes de la afectación ganglionar inicial o del uso de protocolos de diagnóstico pre-BSGC.
ResultadosNo se demostraron diferencias en la TD entre los casos sin afectación ganglionar inicial y los que sí la tuvieron (89,8 vs. 84,4%; p=0,437). Sí se encontraron diferencias significativas (94,1 vs. 56,5%; p=0,002) en el valor predictivo negativo, menor cuando existía afectación ganglionar inicial, y mayor tasa de FN, aunque no de forma significativa (18,2 vs. 43,5%; p=0,252) en ese mismo supuesto. Un estudio de la axila antes de indicar la BSGC y tras la QTN disminuyó significativamente la tasa de FN en los casos en los que existía afectación inicial (55,6 vs. 12,5; p=0,009).
ConclusionesLa QTN da lugar a una menor TD y a una mayor tasa de FN en la BSGC posterior, sobre todo si hay afectación ganglionar inicial. Los protocolos para la evaluación axilar después de administrar la QTN y antes de la BSGC disminuyen la tasa de FN en estas pacientes.
A controversial aspect of breast cancer management is the use of sentinel lymph node biopsy (SLNB) in patients requiring neoadjuvant chemotherapy (NCT). This paper discusses the detection rate (DT) and false negatives (FN) of SLNB after NCT to investigate the influence of initial nodal disease and the protocols applied.
MethodsProspective observational multicenter study in women with breast cancer, treated with NCT and SLNB post-NCT with subsequent lymphadenectomy. DT and FN rates were calculated, both overall and depending on the initial nodal status or the use of diagnostic protocols pre-SLNB.
ResultsNo differences in DT between initial node-negative cases and positive cases were found (89.8 vs. 84.4%, P=.437). Significant differences were found (94.1 vs. 56.5%, P=0,002) in the negative predictive value, which was lower when there was initial lymph node positivity, and a higher rate of FN, not significant (18.2 vs. 43.5%, P=.252) in the same cases. The axillary study before SLNB and after the NCT, significantly decreased the rate of FN in patients with initial involvement (55.6 vs 12.5, P=0,009).
ConclusionsNCT means less DT and a higher rate of FN in subsequent SLNB, especially if there is initial nodal involvement. The use of protocols in axillary evaluation after administering the NCT and before BSGC, decreases the FN rate in these patients.
En el estudio de extensión del cáncer de mama, la biopsia selectiva del ganglio centinela (BSGC) es en la actualidad el método diagnóstico estándar. Mediante este procedimiento se logra demostrar la afectación ganglionar y, de este modo, evitar la morbilidad asociada a la linfadenectomía axilar que se realizaba sistemáticamente. En la actualidad, incluso, se considera la posibilidad de no realizar esta linfadenectomía en casos seleccionados con afectación ganglionar limitada1,2.
No obstante, en todas estas series se considera contraindicada su realización cuando se administra terapia sistémica primaria (TSP). La quimioterapia se ha considerado como un factor que puede llegar a interferir en la detección y correcta identificación del ganglio centinela debido a las modificaciones que produce en la estructura del sistema de drenaje linfático, especialmente, cuando provoca una respuesta efectiva3,4.
Un aspecto controvertido es, ahora, conocer si las pacientes que reciben TSP, cada vez más frecuente, se beneficiarían de la BSGC y cuál sería el momento más apropiado para aplicarla5–8.
En este estudio se plantean 2 objetivos: 1) analizar la tasa de detección (TD) y falsos negativos (FN) de la BSGC realizada tras administrar quimioterapia neoadyuvante y 2) conocer si existen diferencias cuando se detecta enfermedad ganglionar inicial y cuando se aplican protocolos asistenciales.
Pacientes y métodosEstudio clínico prospectivo observacional multicéntrico (GEICAM 2005-07) que incluyó a pacientes con cáncer invasivo de mama en las que se indicaron TSP y se realizó BSGC después de administrarla, con linfadenectomía axilar posterior.
Se excluyó a las pacientes con antecedentes de cirugía axilar previa, carcinoma inflamatorio o contraindicación para la BSGC. También se excluyó a aquellas pacientes en las que, por cualquier circunstancia, no se realizaba la BSGC de forma estandarizada siguiendo los protocolos asistenciales habituales. El estudio fue aprobado por el Comité de Ética de la Investigación de los centros participantes. Todas las pacientes fueron informadas y se obtuvo consentimiento informado específico para participar en el estudio.
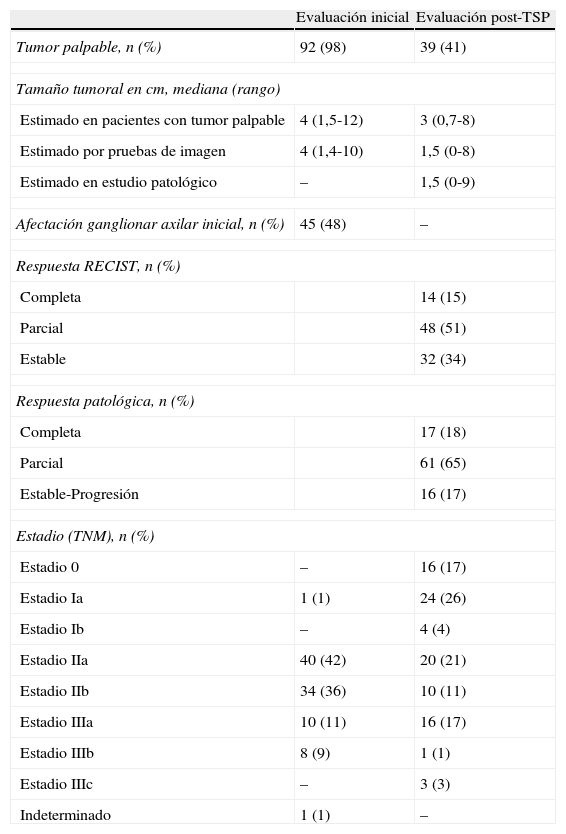
Las características generales de la serie se muestran en la tabla 1, y la tabla 2 muestra los principales cambios pre- y post-TSP.
Características generales de la serie
| n=94 | |
| Edad en años; mediana (rango) | 45 (28-79) |
| Tipo histológico, n (%) | |
| Ductal | 83 (88) |
| Lobulillar | 10 (11) |
| Mixto | 1 (1) |
| Grado histológico, n (%) | |
| I | 3 (3) |
| II | 33 (35) |
| III | 24 (26) |
| No disponible | 34 (36) |
| Características IHQ, n (%) | |
| RE+ | 53 (56) |
| RP+ | 40 (43) |
| Her2neu+ | 11 (12) |
| Régimen de TSP administrada, n (%) | |
| Quimioterapia | 94 (100) |
| Antraciclinas+docetaxel | 65 (69) |
| Antraciclinas+paclitaxel | 18 (19) |
| QT+trastuzumab | 10 (11) |
| Paclitaxel | 1 (1) |
| Hormonoterapia | 0 (0) |
| Número de ciclos administrados, mediana (rango) | 8 (4-16) |
IHQ: inmunohistoquímica; RE: receptores estrogénicos; RP: receptores progesterónicos; TSP: terapia sistémica primaria.
Características antes y después de la terapia sistémica primaria
| Evaluación inicial | Evaluación post-TSP | |
| Tumor palpable, n (%) | 92 (98) | 39 (41) |
| Tamaño tumoral en cm, mediana (rango) | ||
| Estimado en pacientes con tumor palpable | 4 (1,5-12) | 3 (0,7-8) |
| Estimado por pruebas de imagen | 4 (1,4-10) | 1,5 (0-8) |
| Estimado en estudio patológico | – | 1,5 (0-9) |
| Afectación ganglionar axilar inicial, n (%) | 45 (48) | – |
| Respuesta RECIST, n (%) | ||
| Completa | 14 (15) | |
| Parcial | 48 (51) | |
| Estable | 32 (34) | |
| Respuesta patológica, n (%) | ||
| Completa | 17 (18) | |
| Parcial | 61 (65) | |
| Estable-Progresión | 16 (17) | |
| Estadio (TNM), n (%) | ||
| Estadio 0 | – | 16 (17) |
| Estadio Ia | 1 (1) | 24 (26) |
| Estadio Ib | – | 4 (4) |
| Estadio IIa | 40 (42) | 20 (21) |
| Estadio IIb | 34 (36) | 10 (11) |
| Estadio IIIa | 10 (11) | 16 (17) |
| Estadio IIIb | 8 (9) | 1 (1) |
| Estadio IIIc | – | 3 (3) |
| Indeterminado | 1 (1) | – |
TSP: terapia sistémica primaria.
El estudio pre-TSP de las pacientes incluyó una valoración axilar clínico-ecográfica que, en caso de sugerirlo, se acompañó de punción aspiración con aguja fina (PAAF) para confirmar la presencia de enfermedad ganglionar y su clasificación como estadio N+pre-TSP. En caso de no obtenerse estos hallazgos, las pacientes se clasificaron como estadio N0 pre-TSP. Los centros hospitalarios fueron clasificados según el tipo de tratamiento realizado tras la TSP, teniendo en cuenta si fue aplicado un protocolo específico que incluía una nueva valoración con ecografía, y PAAF-BAG en caso de que fuera necesario, después de administrar la TSP y antes de realizar la BSGC.
La metodología para la realización de la BSGC se realizó siguiendo la de los protocolos de la Sociedad Española de Senología y Patología Mamaria9. En todos los casos se realizó linfadenectomía axilar y se registró el número de ganglios aislados y el número de ganglios afectados.
La TD o identificación positiva fue considerada cuando se detectó al menos un ganglio centinela durante la intervención quirúrgica, ya fuera con el trazador isotópico o con un método mixto con isótopo y colorante. Si en la gammagrafía preoperatoria o durante la cirugía no se producía la detección, esta fue considerada negativa.
Se definió como verdadero positivo (VP) aquel caso con BSGC positiva y afectación de algún ganglio no centinela aislado en la linfadenectomía y como verdadero negativo (VN) aquel caso de ganglio centinela negativo sin afectación en ningún ganglio de los aislados en la linfadenectomía. Se definió como FN el caso en el que, siendo el ganglio centinela negativo, se identificaron ganglios no centinelas afectados en la linfadenectomía. La tasa de falsos negativos (TFN) se calculó dividiendo el número de falsos negativos entre la suma de falsos negativos y verdaderos positivos.
Se estudiaron la TD y la TFN global, así como en los casos según que se demostrara afectación ganglionar inicial (cN+) o no (cN0), y se compararon las TD y TFN entre ellas.
Se realizó un subanálisis, inicialmente no planificado, que evaluó los centros hospitalarios según sus protocolos aplicados antes de la realización de la BSGC. Se compararon aquellos centros en los que se realizaba de forma sistemática por radiólogos con dedicación exclusiva a la enfermedad mamaria el estudio axilar con ecografía tras acabar la quimioterapia neoadyuvante y antes de realizar la BSGC, que era excluido en caso de manifiesta afectación, con los centros hospitalarios en los que no se realizaba este estudio o el estudio radiológico era practicado por radiólogos sin dedicación exclusiva.
Análisis estadísticoSe realizó un estudio descriptivo de las variables demográficas, anatomopatológicas y de evolución clínico-radiológica tanto previas como tras TSP. Para las variables cualitativas se calculó su distribución de frecuencias, mientras que para las cuantitativas se utilizaron medidas de tendencia central, como la media y la mediana. Se han aportado tanto los estimadores puntuales de las TD, VPP, VPN, TFN como sus intervalos de confianza (IC) al 95%. En caso de tratarse de muestras pequeñas se ha calculado el IC de manera exacta utilizando la fórmula propuesta por Clopper y Pearson10.
Se han comparado las diversas tasas (TD, PVp, PVn, TFN) entre los distintos subconjuntos de pacientes. Para ello se ha utilizado el test chi-cuadrado o el test exacto de Fisher si la frecuencia esperada era menor de 5.
Se evaluó la validez de la clasificación realizada por la técnica del ganglio centinela frente a la linfadenectomía (gold standard), utilizando la curva ROC. Para ello se calculó la sensibilidad, la especificidad y el área bajo la curva. Estos cálculos se realizaron tanto de forma global como separando los casos con afectación axilar inicial y los que no la tuvieron.
Los cálculos estadísticos se realizaron utilizando el software PASW v18. Se consideró significativo un nivel de p<0,05.
ResultadosDel total de 100 casos, se estudiaron finalmente 94. Se descartó un caso que resultó ser un carcinoma inflamatorio y otros 5 en los que, por distintas causas, no se realizó finalmente la BSGC.
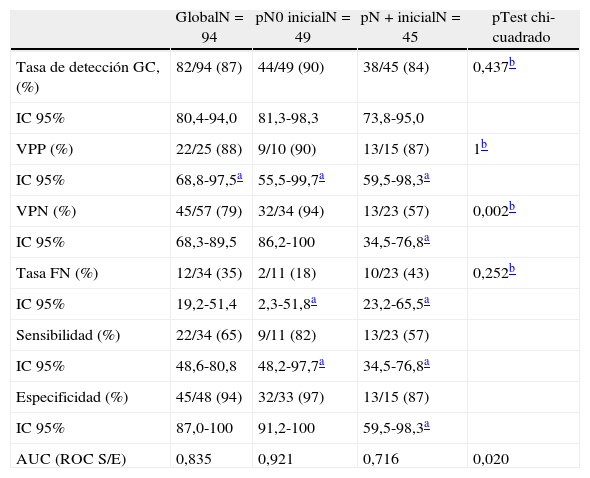
De las 94 BSGC, se detectó al menos un ganglio centinela en 82 casos (87%), y no se demostraron diferencias al considerar los casos con afectación ganglionar inicial frente a los que sí la tuvieron (90 vs. 84%; p=0,437). La tabla 3 muestra los valores de sensibilidad, especificidad, valores predictivos y TFN tanto en la serie global como en los grupos con y sin afectación ganglionar inicial. Puede observarse como existen diferencias significativas (94 vs. 57%; p=0,002) en el VPN, menor cuando existe afectación ganglionar de inicio, así como una mayor TFN, aunque no de forma significativa (18 vs. 44%; p=0,252) en ese mismo supuesto.
Resultados de la serie en función de la afectación ganglionar inicial
| GlobalN=94 | pN0 inicialN=49 | pN+inicialN=45 | pTest chi-cuadrado | |
| Tasa de detección GC, (%) | 82/94 (87) | 44/49 (90) | 38/45 (84) | 0,437b |
| IC 95% | 80,4-94,0 | 81,3-98,3 | 73,8-95,0 | |
| VPP (%) | 22/25 (88) | 9/10 (90) | 13/15 (87) | 1b |
| IC 95% | 68,8-97,5a | 55,5-99,7a | 59,5-98,3a | |
| VPN (%) | 45/57 (79) | 32/34 (94) | 13/23 (57) | 0,002b |
| IC 95% | 68,3-89,5 | 86,2-100 | 34,5-76,8a | |
| Tasa FN (%) | 12/34 (35) | 2/11 (18) | 10/23 (43) | 0,252b |
| IC 95% | 19,2-51,4 | 2,3-51,8a | 23,2-65,5a | |
| Sensibilidad (%) | 22/34 (65) | 9/11 (82) | 13/23 (57) | |
| IC 95% | 48,6-80,8 | 48,2-97,7a | 34,5-76,8a | |
| Especificidad (%) | 45/48 (94) | 32/33 (97) | 13/15 (87) | |
| IC 95% | 87,0-100 | 91,2-100 | 59,5-98,3a | |
| AUC (ROC S/E) | 0,835 | 0,921 | 0,716 | 0,020 |
AUC (ROC S/E): área bajo la curva ROC de sensibilidad/especificidad; FN: falsos negativos; GC: ganglio centinela; IC: intervalo de confianza; VPN: valor predictivo negativo; VPP: valor predictivo positivo.
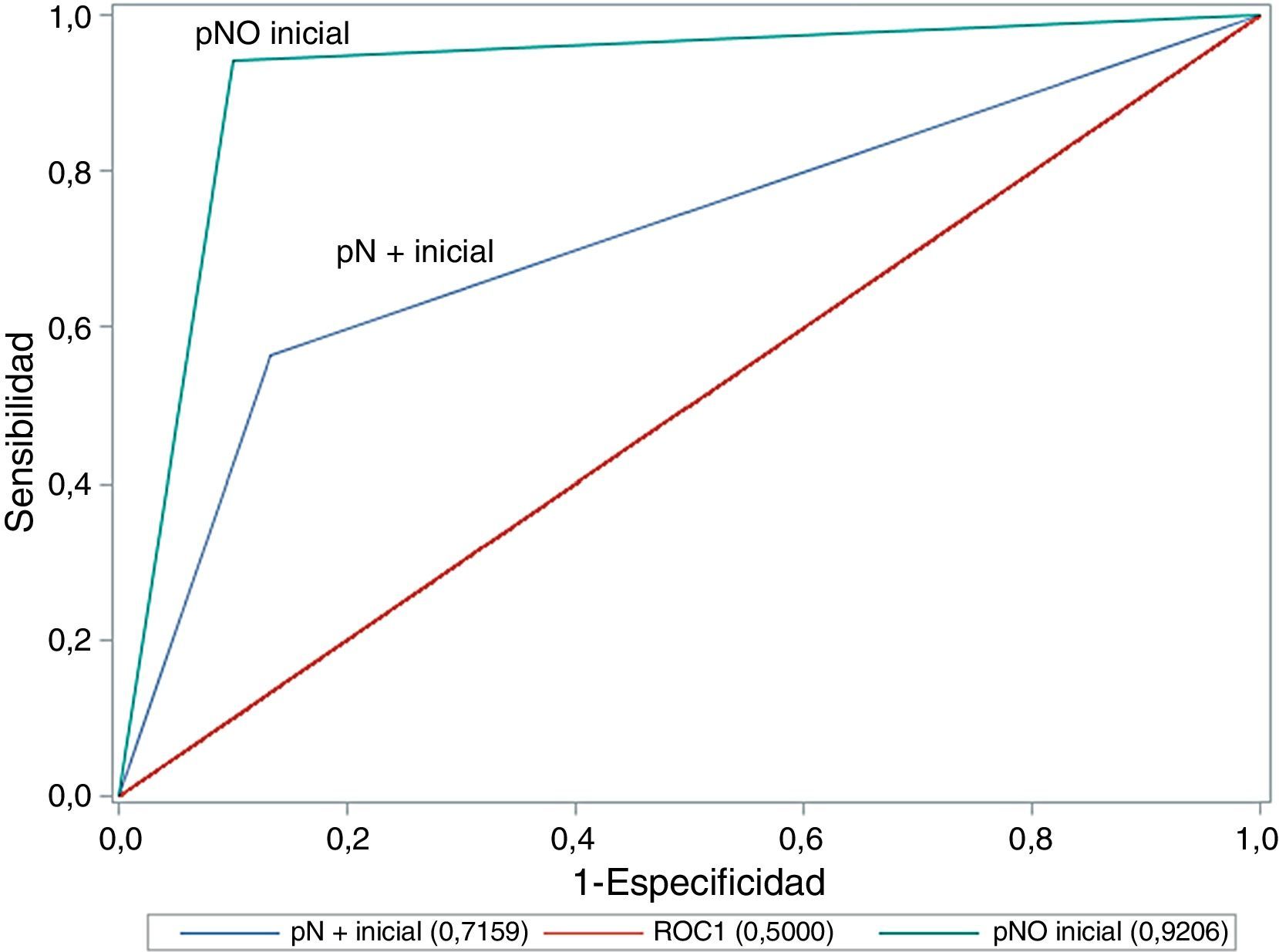
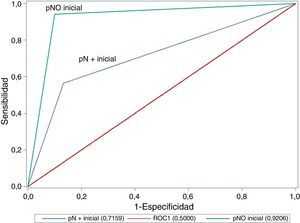
La comparación del área bajo la curva ROC entre los casos con y sin afectación ganglionar (fig. 1) muestra como existen diferencias significativas entre ellas, siendo mucho mejor la precisión cuando no existe afectación ganglionar de inicio (0,921 en cN0 vs. 0,716 en cN+; p=0,020; test chi-cuadrado).
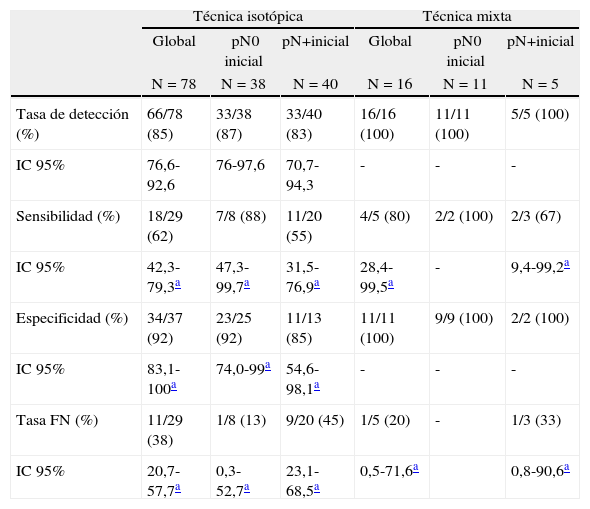
En cuanto a la técnica utilizada, se realizó el marcaje con isótopo en 78 casos (83%) y la técnica mixta con colorante e isótopo en los 16 restantes (17%). Si consideramos la técnica utilizada para realizar la BSGC (tabla 4), observamos que, aunque el uso de la técnica mixta mejora los valores de la TFN respecto a la técnica con isótopo solo (33 vs. 45%), continúan siendo cifras elevadas cuando se comparan con el grupo que no tiene afectación ganglionar antes de administrar la TSP, aunque hay que tener en cuenta el tamaño de la muestra, especialmente en el grupo de técnica mixta.
Resultados en función de la técnica de la biopsia del ganglio centinela
| Técnica isotópica | Técnica mixta | |||||
| Global | pN0 inicial | pN+inicial | Global | pN0 inicial | pN+inicial | |
| N=78 | N=38 | N=40 | N=16 | N=11 | N=5 | |
| Tasa de detección (%) | 66/78 (85) | 33/38 (87) | 33/40 (83) | 16/16 (100) | 11/11 (100) | 5/5 (100) |
| IC 95% | 76,6-92,6 | 76-97,6 | 70,7-94,3 | - | - | - |
| Sensibilidad (%) | 18/29 (62) | 7/8 (88) | 11/20 (55) | 4/5 (80) | 2/2 (100) | 2/3 (67) |
| IC 95% | 42,3-79,3a | 47,3-99,7a | 31,5-76,9a | 28,4-99,5a | - | 9,4-99,2a |
| Especificidad (%) | 34/37 (92) | 23/25 (92) | 11/13 (85) | 11/11 (100) | 9/9 (100) | 2/2 (100) |
| IC 95% | 83,1-100a | 74,0-99a | 54,6-98,1a | - | - | - |
| Tasa FN (%) | 11/29 (38) | 1/8 (13) | 9/20 (45) | 1/5 (20) | - | 1/3 (33) |
| IC 95% | 20,7-57,7a | 0,3-52,7a | 23,1-68,5a | 0,5-71,6a | 0,8-90,6a | |
FN: falso negativo; IC: intervalo de confianza.
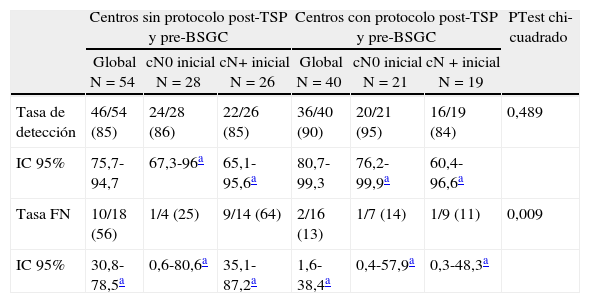
Por último, la tabla 5 muestra los resultados cuando se compara el uso de un protocolo que estudie la axila antes de indicar la BSGC y después de administrar la TSP, mediante ecografía y, en función de los hallazgos, consigue descartar una afectación ganglionar mediante PAAF o BAG de los ganglios sospechosos. En la tabla 5 destacamos como la aplicación de este tipo de protocolos disminuye significativamente la tasa de FN en los casos con afectación inicial (56 vs 13; p=0,009), aunque a expensas de una menor tasa de detección en ese grupo de pacientes.
Resultados en función de la existencia de valoración axilar después de la terapia sistémica primaria
| Centros sin protocolo post-TSP y pre-BSGC | Centros con protocolo post-TSP y pre-BSGC | PTest chi-cuadrado | |||||
| Global N=54 | cN0 inicial N=28 | cN+ inicial N=26 | Global N=40 | cN0 inicial N=21 | cN+inicial N=19 | ||
| Tasa de detección | 46/54 (85) | 24/28 (86) | 22/26 (85) | 36/40 (90) | 20/21 (95) | 16/19 (84) | 0,489 |
| IC 95% | 75,7-94,7 | 67,3-96a | 65,1-95,6a | 80,7-99,3 | 76,2-99,9a | 60,4-96,6a | |
| Tasa FN | 10/18 (56) | 1/4 (25) | 9/14 (64) | 2/16 (13) | 1/7 (14) | 1/9 (11) | 0,009 |
| IC 95% | 30,8-78,5a | 0,6-80,6a | 35,1-87,2a | 1,6-38,4a | 0,4-57,9a | 0,3-48,3a | |
BSGC: biopsia selectiva del ganglio centinela; FN: falsos negativos; IC: intervalo de confianza; TSP: terapia sistémica primaria.
Los resultados encontrados muestran que la BSGC tras tratamiento neoadyuvante presenta una TD menor que la que se describe en la literatura tras cirugía primaria o cuando se hace previamente al tratamiento neoadyuvante, así como una TFN significativamente alta. Además, y como dato relevante de este trabajo, se comprueba que estas cifras dependen no solo de la existencia de afectación ganglionar inicial, sino de los protocolos asistenciales aplicados por los diferentes centros.
En este sentido, la aplicación de vías clínicas con valoración del estado ganglionar axilar tras la quimioterapia primaria utilizando la ecografía y, en caso de ser necesario, mediante la PAAF o BAG guiada por ecografía, y la dedicación exclusiva de los radiólogos en este campo de actuación, hacen que las cifras de FN disminuyan de forma importante, aunque sin alcanzar las de la BSGC realizada previamente a la quimioterapia o en el contexto de cirugía primaria.
En un reciente estudio retrospectivo sobre 178 pacientes con afectación ganglionar, tratadas con quimioterapia neoadyuvante y a las que se les realizó la BSGC11, se encontraron TD aceptables, del 94,9%, aunque con una TFN del 22% que desaconseja claramente su uso. De todas formas, esta serie describe subgrupos inmunofenotípicos, concretamente los triples negativos, en los que esta llega a ser del 7% y en los que podría considerarse este procedimiento diagnóstico en los casos con respuesta ganglionar a la quimioterapia primaria.
En el metaanálisis realizado por Tan et al.12 sobre 10 series publicadas en lengua inglesa entre 2000 y 2008, que recogían 499 casos de cáncer de mama con axila clínicamente negativa tras recibir quimioterapia neoadyuvante y a los que se realizó BSGC, se concluye que esta es una herramienta adecuada para el estudio de extensión, al encontrar una muy buena tasa de identificación de hasta el 94,3% y una TFN del 7,4%. Desafortunadamente, aunque realizan subanálisis sobre la metodología de la BSGC tanto en los trazadores utilizados como en el uso o no de inmunohistoquímica, en su estudio no se analiza la diferencia entre las series que incluyen casos con afectación inicial ganglionar y los que no. De hecho, en 5 de los 10 trabajos revisados, los criterios de inclusión eran N0-2, sin conocer el porcentaje de afectación real en ellos, y en uno no se especificaba.
Otra revisión sistemática13 analiza 40 estudios que incluyen a 3.328 pacientes y en los que sí diferencia los casos con afectación ganglionar inicial de los que no la tenían. Describen una infraestadificación axilar tras la neoadyuvancia de entre el 20 y el 44%, y de forma global, los trabajos N0 preneoadyuvancia arrojan una tasa de identificación del 95% con una TFN del 11,4%, mientras que los que incluían pacientes N+pre-TSP mostraban una tasa de detección del 86,5% y una TFN del 10,3%. No obstante, los autores concluyen que es necesario ajustar la indicación de la linfadenectomía en función del resultado de la BSGC y de la respuesta a la quimioterapia neoadyuvante para beneficiar a aquellas pacientes con respuesta ganglionar al evitar la linfadenectomía.
Recientemente se ha comunicado el resultado del SENTINA trial14, un estudio alemán de cohortes a 4 brazos en el que se considera tanto la existencia de afectación ganglionar previa a la administración de quimioterapia como el momento de realizar la BSGC. En los casos en los que la biopsia se realizó después de haber objetivado la respuesta clínica ganglionar, la TFN era inaceptablemente alta y no se recomienda su utilización para el estudio de extensión del cáncer de mama. Las diferencias significativas entre el AUC que encontramos al comparar el procedimiento entre casos con y sin afectación ganglionar inicial concuerdan con las diferencias encontradas entre los brazos correspondientes en el estudio alemán.
Otro estudio relacionado es el ACOSOG Z107115, en el que se analizó la utilidad de la BSGC en casos con enfermedad ganglionar conocida previa a la administración de la quimioterapia. La tasa de respuesta ganglionar fue del 40% y, en esos casos, se encontró una TFN de más del 12%.
A la hora de aceptar o justificar las cifras encontradas en estos trabajos, para su aplicación en la práctica clínica, habría que tener en consideración que los criterios de validación para la técnica de la BSGC en los diferentes consensos9,16 a la hora de estadificar los casos de cirugía primaria en cánceres de mama precoz, definían como aceptables los valores de TD superiores al 95% y TFN menores del 5%, superiores e inferiores respectivamente a los encontrados cuando existe afectación ganglionar inicial.
El otro aspecto reseñable es que la mejor selección de aquellos casos que realmente no presentan enfermedad ganglionar tras el tratamiento, mediante una adecuada valoración después de terminar la quimioterapia neoadyuvante, con una evaluación ecográfica y una biopsia en caso de ser necesario, hechas por radiólogos con dedicación preferencial o exclusiva, son hechos que podrían mejorar la eficacia y eficiencia de este método17.
A modo de conclusiones del presente estudio se puede decir que la administración de TSP supone una menor TD y una mayor TFN en los casos con afectación ganglionar inicial, con cifras inferiores y superiores, respectivamente, a las recomendadas en la validación del procedimiento de la BSGC para el cáncer de mama precoz con cirugía primaria. Además, la protocolización en la evaluación axilar, con el examen clínico y ecográfico, después de administrar la quimioterapia y antes de la BSGC, disminuye la TFN en estas pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.