El empleo de doble mamaria se ha asociado con un aumento de complicaciones esternales, especialmente en pacientes diabéticos y obesos.
El objetivo de este trabajo es revisar los factores de riesgo de aquellos pacientes en los que se ha usado doble mamaria y la tasa de complicación esternal en este grupo.
MétodosDe nuestra base de datos se ha seleccionado a 526 pacientes revascularizados quirúrgicamente con uso de doble arteria mamaria.
La edad media de los pacientes fue de 59 años, con un EuroScore logístico-1 medio de 2,7%.
ResultadosPresentaron dehiscencia esternal 3 pacientes (0,57%), no se correlacionó con ningún factor de riesgo.
Problemas de herida tanto superficial como profunda 31 pacientes (5.9%), (2 mediastinitis-0.38%).
Con respecto a los pacientes que presentaron infección superficial de la herida quirúrgica (29 pacientes, 5,513%), se obtuvo mayor incidencia en mujeres, pacientes con insuficiencia renal y aquellos a los que se les realizó transfusión de concentrado de hematíes en quirófano, Siendo estas diferencias estadísticamente significativas (p<0,05).
También hubo mayor incidencia de infección superficial en pacientes diabéticos, enfermedad pulmonar obstructiva crónica, obesos, fumadores y a aquellos a los que se les realizó revascularización miocárdica incompleta, siendo estas diferencias no significativas.
ConclusionesEn nuestra experiencia, la utilización de doble mamaria no se acompañó de mayor incidencia de dehiscencia esternal, pero si con problemas de infección superficial de la herida, sobre todo en el grupo de pacientes mujeres, con insuficiencia renal y transfundidos en quirófano. Para mantener el beneficio de la doble mamaria en estos pacientes, deberíamos ser especialmente cuidadosos e implementar nuevas estrategias de cierre esternal.
The use of double internal mammary artery in coronary artery bypass grafting has been associated with increased sternal complications, especially in diabetic and obese patients.
The aim of this article is to review the risk factors for those patients who underwent coronary artery bypass grafting with the use of double internal mammary artery and to analyse the sternal complication rate in this group.
MethodsA total 526 patients revascularized with use of double internal mammary artery were selected from our database.
The mean age of the patients was 59 years, with a mean logistics EuroScore I of 2.7%.
ResultsThere were a total of 3 (0.57%) cases with sternal instability, which did not correspond with any risk factor.
A sternal associated infection was observed in 31 (5.9%) patients, but only 2 of them developed deep infection/mediastinitis (0.38%).
Of the patients who had superficial infection of the surgical wound (29 patients, 5.5%), there was a higher incidence in women, patients with renal failure, and those who received a transfusion of packed red blood cells during the surgery. These findings were statistically significant (P<.05).
There was also a higher incidence (with no statistically significant differences) of superficial infection in patients with diabetes, COPD, obese, smokers, and those who underwent incomplete myocardial revascularisation.
ConclusionsIn our experience, the use of double internal mammary artery was not accompanied by an increased incidence of sternal instability, but it was associated with superficial infections, in the group of female patients, renal disease, and those who needed red blood cells during the surgery. To maintain the benefit of the double internal mammary artery bypass grafting in these patients, special care should be taken, and new strategies for sternal closure should be implemented.
El uso de arteria mamaria interna para revascularizar la arteria descendente anterior es considerado como tratamiento de elección en cirugía de revascularización miocárdica, ya que muestra los mejores resultados a medio y largo plazo1-4. El uso de doble arteria mamaria se ha vuelto muy popular por este motivo5-9, pero, no obstante, está asociado a un aumento de riesgo de complicaciones esternales, tales como: dehiscencia esternal, mediastinitis y/o problemas de herida quirúrgica10,11.
Con este estudio hemos querido analizar la frecuencia de estos problemas de herida y esternón en pacientes intervenidos en nuestro centro con uso de doble arteria mamaria y los factores de riesgo que pudieran favorecer problemas esternales.
MétodosEstudio descriptivo retrospectivo, seleccionando de nuestra base de datos a 526 pacientes a los cuales se les realizó cirugía de revascularización miocárdica aislada («coronarios puros»), utilizando ambas arterias mamarias internas, con o sin otros injertos concomitantes. La muestra recogida incluye a pacientes intervenidos en nuestro centro desde enero del 2001 hasta diciembre del 2015.
Se ha realizado un análisis de los siguientes factores en la muestra: edad, sexo, hipertensión arterial (HTA), diabetes mellitus (DM), obesidad, dislipidemia (DL), tabaquismo, enfermedad pulmonar obstructiva crónica (EPOC), accidente cerebrovascular agudo (ACV), insuficiencia renal (IR), fracción de eyección de ventrículo izquierdo (FEVI), vasculopatía periférica, tiempo de circulación extracorpórea (CEC), tiempo de pinzamiento aórtico, transfusión de concentrados de hematíes en quirófano y durante el ingreso, reintervención por sangrado excesivo en las primeras 24h posquirúrgicas y número de derivaciones coronarias realizadas. También se ha analizado el EuroScore logístico i medio de la muestra y comparado con la mortalidad obtenida.
Se han analizado los datos del grupo de manera conjunta y separados por técnica quirúrgica (arteria mamaria interna esqueletizada o pediculada), encontrándose muestras comparables de ambos grupos y sin encontrarse diferencias estadísticamente significativas en cuanto a resultados.
Estudiando la morbilidad esternal hemos buscado la relación de los factores antes descritos en aquellos pacientes que han presentado algún tipo de complicación, ya sea dehiscencia esternal, como infección superficial de la herida quirúrgica (afectación de piel y/o tejido celular subcutáneo) o infección profunda (mediastinitis).
El diagnóstico de dehiscencia esternal se realizó mediante criterios clínicos: dolor, disnea e inestabilidad esternal palpable, y se confirmó mediante hallazgos quirúrgicos, encontrándose unión inadecuada de ambos bordes esternales.
El diagnóstico de infección superficial de herida quirúrgica se basa en criterios clínicos (problemas locales: calor, rubor, dolor, exudado, dehiscencia cutánea) y criterios de laboratorio: leucocitosis y cultivo recogido de la herida positivo. Con o sin hemocultivos positivos, pero sin llegar a tener afectación más allá del tejido celular subcutáneo.
Entre las dehiscencias esternales se encontraron 2 mediastinitis, consideradas infecciones de herida profunda, ya que presentaron una colección retroesternal, con olor fétido y cultivos positivos de la misma, además de dehiscencia esternal y leucocitosis como hallazgo de laboratorio.
Técnica quirúrgicaLa revascularización miocárdica se realizó mediante esternotomía media completa en el 100% de los casos y con el uso de CEC en 448 pacientes (85,2%). Canulación central arterial en aorta ascendente y venosa con cánula única cavo-atrial. Heparinización completa mediante 3mg/kg de peso. Con hipotermia ligera (34°C) y protección miocárdica vía anterógrada en todos los casos.
Se realizó disección esqueletizada, sin ningún tipo de tejido acompañante, de ambas arterias mamarias internas en 421 pacientes (80,04%), mientras que en el 19,96% (105 pacientes) se obtuvieron los injertos de manera pediculada (junto con sus venas satélite, la parte adjunta de los músculos intercostales y la fascia intratorácica).
Ambas arterias mamarias se utilizaron para revascularizar el árbol arterial izquierdo. Se completó la revascularización del árbol arterial derecho, en aquellos pacientes que fuera necesario, mediante el uso de otros injertos (vena safena y/o arteria radial).
La arteria mamaria interna derecha se utilizó tanto como injerto in situ (a través del seno transverso de manera retroaórtica, conservando su origen en la arteria subclavia), como injerto libre (desconectada de la arteria subclavia y anastomosada a la aorta) y, en la mayoría de los casos, como injerto en T o Y desde la arteria mamaria izquierda.
Profilaxis antibiótica intravenosa con cefazolina 2g, 30 min antes de la intervención y posteriormente cada 8h hasta completar 3 dosis, y para aquellos pacientes alérgicos, vancomicina 1g por vía intravenosa cada 12h hasta completar 2 dosis.
Análisis estadísticoEl programa estadístico SPSS versión 22.0 (IBM/SPSS Inc., Chicago, IL, EE. UU.) fue utilizado para el análisis. Las variables continuas con distribución normal fueron expresadas como media±desviación típica. Las variables continuas con distribución no normal fueron expresadas como mediana y el rango intercuartílico. Las variables categóricas fueron expresadas como proporciones. Se realizó un análisis preliminar univariante de las variables perioperatorias para determinar los posibles factores de riesgo de dehiscencia esternal, mediastinitis y/o problemas de herida quirúrgica, con un grado de significación estadística p<0,05. Completado con regresión logística univariante y pruebas multivariantes para esclarecer posibles factores favorecedores de problemas de herida superficial.
ResultadosLa edad media de los pacientes fue 59±9 años. En su mayoría varones (88%).
La mayoría de los pacientes eran hipertensos (59%), diabéticos (61%) y dislipidémicos (71%), tan solo un 12% de ellos eran obesos (índice de masa corporal>30) y un 39% fumadores.
En su mayoría se intervino a pacientes con una FEVI normal (52%), seguido de aquellos pacientes con FEVI ligera (23%) o moderadamente deprimida (21,3%).
Un 7,4% de los pacientes presentaban IR previa a la intervención entre sus antecedentes (creatinina > 200mmol/l o >2,26mg/dl). Mientras que un 8,6% presentaba EPOC.
La incidencia de arteriopatía periférica entre los pacientes fue de un 17,5% y antecedente de ACV previo en un 3,6%.
En su mayoría (83,2%) se realizaron 2-3 derivaciones coronarias por paciente.
Se utilizó la mamaria derecha como injerto libre en un 4,4% de los pacientes (23 pacientes), mamaria derecha de mamaria izquierda en el 77% (405 pacientes) y mamaria derecha in situ en el 23,6% (124 pacientes).
El tiempo medio de CEC fue de 66,76±17,42 min y de pinzamiento aórtico medio de 44,82±13,42 min.
Se reintervino por sangrado excesivo en las primeras 24 h a 10 pacientes (1,9%), sin encontrarse diferencias estadísticamente significativas en la incidencia de dehiscencia esternal o problemas de herida quirúrgica en estos pacientes.
Necesitaron transfusión un 38% de los pacientes.
De los 526 pacientes, fallecieron 5 (mortalidad de 1%), inferior a la mortalidad esperada (EuroScore medio 2,7±2,44/EuroScore logístico i %: 2,73±3,27).
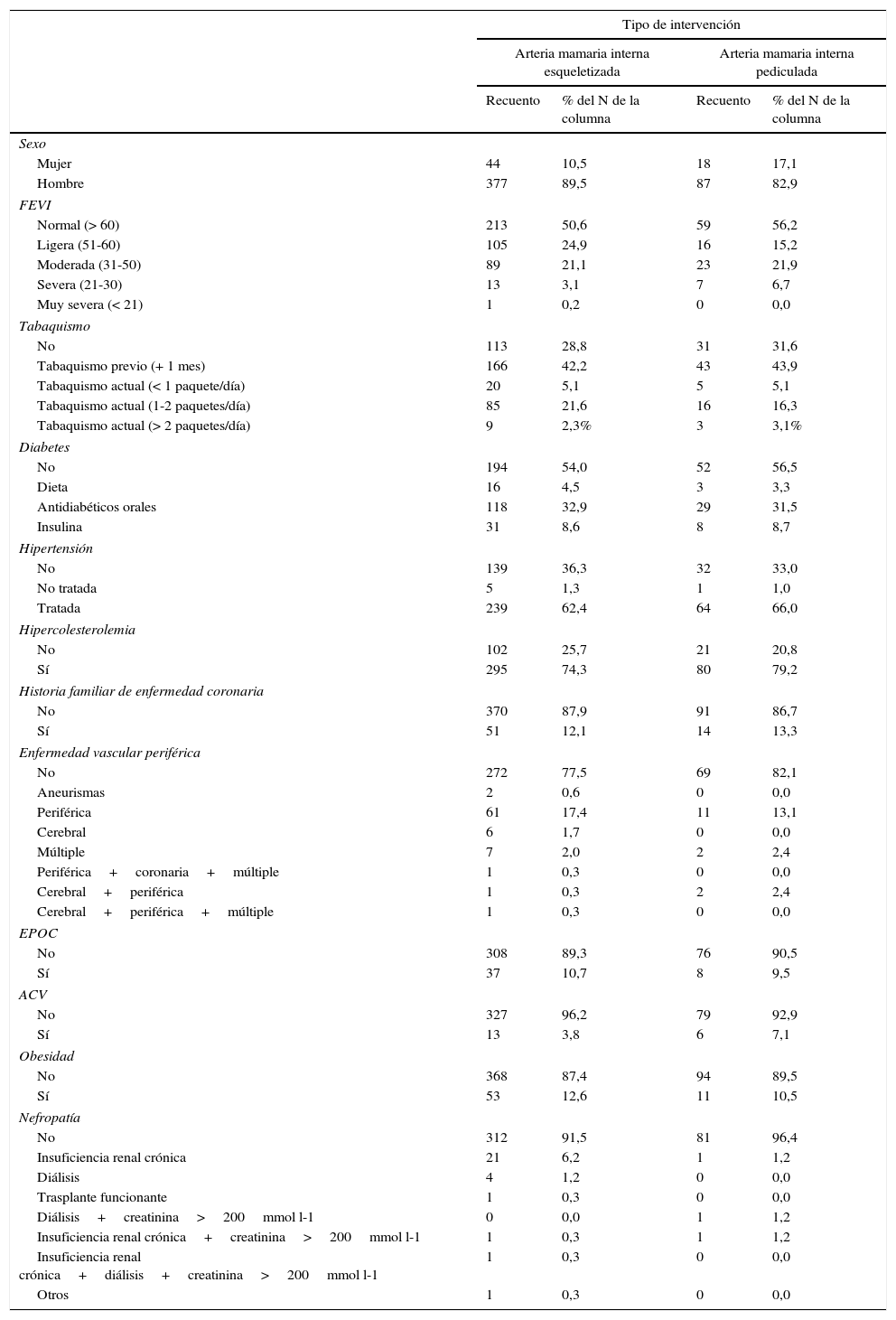
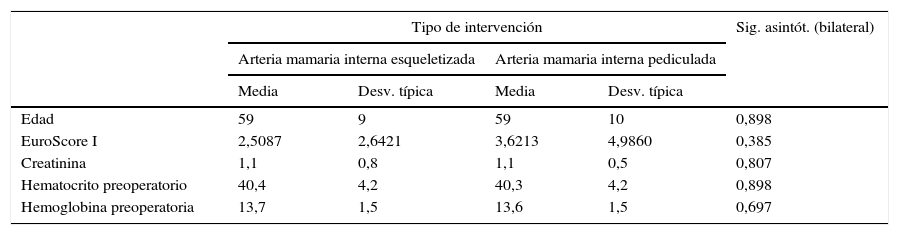
Las tablas 1 y 2 muestra los datos demográficos separando la muestra en 2 grupos según la técnica de obtención del injerto mamario (esqueletizada vs. pediculada), encontrándose muestras comparables sin apenas diferencias en cuanto a factores de riesgo.
Datos demográficos divididos según técnica de obtención arteria mamaria interna. Variables cualitativas
| Tipo de intervención | ||||
|---|---|---|---|---|
| Arteria mamaria interna esqueletizada | Arteria mamaria interna pediculada | |||
| Recuento | % del N de la columna | Recuento | % del N de la columna | |
| Sexo | ||||
| Mujer | 44 | 10,5 | 18 | 17,1 |
| Hombre | 377 | 89,5 | 87 | 82,9 |
| FEVI | ||||
| Normal (> 60) | 213 | 50,6 | 59 | 56,2 |
| Ligera (51-60) | 105 | 24,9 | 16 | 15,2 |
| Moderada (31-50) | 89 | 21,1 | 23 | 21,9 |
| Severa (21-30) | 13 | 3,1 | 7 | 6,7 |
| Muy severa (< 21) | 1 | 0,2 | 0 | 0,0 |
| Tabaquismo | ||||
| No | 113 | 28,8 | 31 | 31,6 |
| Tabaquismo previo (+ 1 mes) | 166 | 42,2 | 43 | 43,9 |
| Tabaquismo actual (< 1 paquete/día) | 20 | 5,1 | 5 | 5,1 |
| Tabaquismo actual (1-2 paquetes/día) | 85 | 21,6 | 16 | 16,3 |
| Tabaquismo actual (> 2 paquetes/día) | 9 | 2,3% | 3 | 3,1% |
| Diabetes | ||||
| No | 194 | 54,0 | 52 | 56,5 |
| Dieta | 16 | 4,5 | 3 | 3,3 |
| Antidiabéticos orales | 118 | 32,9 | 29 | 31,5 |
| Insulina | 31 | 8,6 | 8 | 8,7 |
| Hipertensión | ||||
| No | 139 | 36,3 | 32 | 33,0 |
| No tratada | 5 | 1,3 | 1 | 1,0 |
| Tratada | 239 | 62,4 | 64 | 66,0 |
| Hipercolesterolemia | ||||
| No | 102 | 25,7 | 21 | 20,8 |
| Sí | 295 | 74,3 | 80 | 79,2 |
| Historia familiar de enfermedad coronaria | ||||
| No | 370 | 87,9 | 91 | 86,7 |
| Sí | 51 | 12,1 | 14 | 13,3 |
| Enfermedad vascular periférica | ||||
| No | 272 | 77,5 | 69 | 82,1 |
| Aneurismas | 2 | 0,6 | 0 | 0,0 |
| Periférica | 61 | 17,4 | 11 | 13,1 |
| Cerebral | 6 | 1,7 | 0 | 0,0 |
| Múltiple | 7 | 2,0 | 2 | 2,4 |
| Periférica+coronaria+múltiple | 1 | 0,3 | 0 | 0,0 |
| Cerebral+periférica | 1 | 0,3 | 2 | 2,4 |
| Cerebral+periférica+múltiple | 1 | 0,3 | 0 | 0,0 |
| EPOC | ||||
| No | 308 | 89,3 | 76 | 90,5 |
| Sí | 37 | 10,7 | 8 | 9,5 |
| ACV | ||||
| No | 327 | 96,2 | 79 | 92,9 |
| Sí | 13 | 3,8 | 6 | 7,1 |
| Obesidad | ||||
| No | 368 | 87,4 | 94 | 89,5 |
| Sí | 53 | 12,6 | 11 | 10,5 |
| Nefropatía | ||||
| No | 312 | 91,5 | 81 | 96,4 |
| Insuficiencia renal crónica | 21 | 6,2 | 1 | 1,2 |
| Diálisis | 4 | 1,2 | 0 | 0,0 |
| Trasplante funcionante | 1 | 0,3 | 0 | 0,0 |
| Diálisis+creatinina>200mmol l-1 | 0 | 0,0 | 1 | 1,2 |
| Insuficiencia renal crónica+creatinina>200mmol l-1 | 1 | 0,3 | 1 | 1,2 |
| Insuficiencia renal crónica+diálisis+creatinina>200mmol l-1 | 1 | 0,3 | 0 | 0,0 |
| Otros | 1 | 0,3 | 0 | 0,0 |
Datos demográficos divididos según técnica de obtención arteria mamaria interna. Variables cuantitativas
| Tipo de intervención | Sig. asintót. (bilateral) | ||||
|---|---|---|---|---|---|
| Arteria mamaria interna esqueletizada | Arteria mamaria interna pediculada | ||||
| Media | Desv. típica | Media | Desv. típica | ||
| Edad | 59 | 9 | 59 | 10 | 0,898 |
| EuroScore I | 2,5087 | 2,6421 | 3,6213 | 4,9860 | 0,385 |
| Creatinina | 1,1 | 0,8 | 1,1 | 0,5 | 0,807 |
| Hematocrito preoperatorio | 40,4 | 4,2 | 40,3 | 4,2 | 0,898 |
| Hemoglobina preoperatoria | 13,7 | 1,5 | 13,6 | 1,5 | 0,697 |
Durante el postoperatorio presentaron dehiscencia esternal 3 pacientes (0,57%), sin encontrarse relación estadísticamente significativa con ninguno de los factores analizados. Uno de los pacientes presentó dehiscencia esternal aséptica, mientras que los otros 2 habían desarrollado mediastinitis (0,38%).
No hay suficientes casos de dehiscencia esternal ni de mediastinitis como para poder extraer conclusiones estadísticamente significativas y/o valorables.
Centrándonos en aquellos pacientes que presentaron problemas de herida superficial, se encontraron 29 pacientes (5,52%), 2 de ellos con hemocultivos positivos.
El análisis preliminar evidenció como factores de riesgo para desarrollar infección superficial de la herida quirúrgica:
- –
El sexo, ya que un 17,7% de las mujeres frente a un 5,4% de los hombres presentaron esta complicación, con un nivel de significación p < 0,000.
- –
Insuficiencia renal, con una diferencia fuertemente significativa p<0,001 en la incidencia de infección superficial entre los que presentan IR (18,6%) y los que no (5,8%).
- –
Transfusión de concentrado de hematíes en quirófano: presenta una clara diferencia significativa (18,3% de infecciones en aquellos transfundidos frente a 5,1% los no transfundidos, p < 0,000).
Así mismo se encontró relación con los siguientes factores, aunque sin llegar a la significación estadística:
- –
Hay mayor incidencia de infección superficial de la herida quirúrgica entre los pacientes diabéticos (9,8%) frente a los no diabéticos (5,3%), no llegando a ser esta diferencia estadísticamente significativa (p=0,069). Al desglosarlo por tipos de tratamiento, aquellos con antidiabéticos orales presentan mayor incidencia (10,9%) frente a los insulinodependientes (7,7%), siendo esta diferencia no significativa (p=0,223).
- –
Parece haber diferencias entre los pacientes con EPOC, 13,3% de infecciones frente a un 6,8% en aquellos que no presentan EPOC, pero esta diferencia no es significativa (p=0,113).
- –
Lo mismo ocurre con los pacientes obesos: un 10,9% de infecciones en obesos frente a un 6,3% en no obesos, con una p=0,166.
- –
Aquellos pacientes a los que se les realizó una revascularización incompleta (ya sea por malos vasos, lecho distal afectado o tamaño de la arteria<1mm) parecen tener mayor incidencia de infección (11,6% frente a 5,9% en los que se consiguió realizar revascularización completa). Está al límite de la significación p=0,058. Esto puede ser debido a que esta arteriopatía de pequeño vaso afecte también a la circulación del tejido celular subcutáneo.
- –
Un dato curioso es la menor incidencia de infección en aquellos pacientes exfumadores (4,8%) frente a los no fumadores (9,7%), aunque la mayor incidencia es en aquellos pacientes fumadores (16,7%) independientemente del número de paquetes/año, aunque estas diferencias no son significativas (p=0,3).
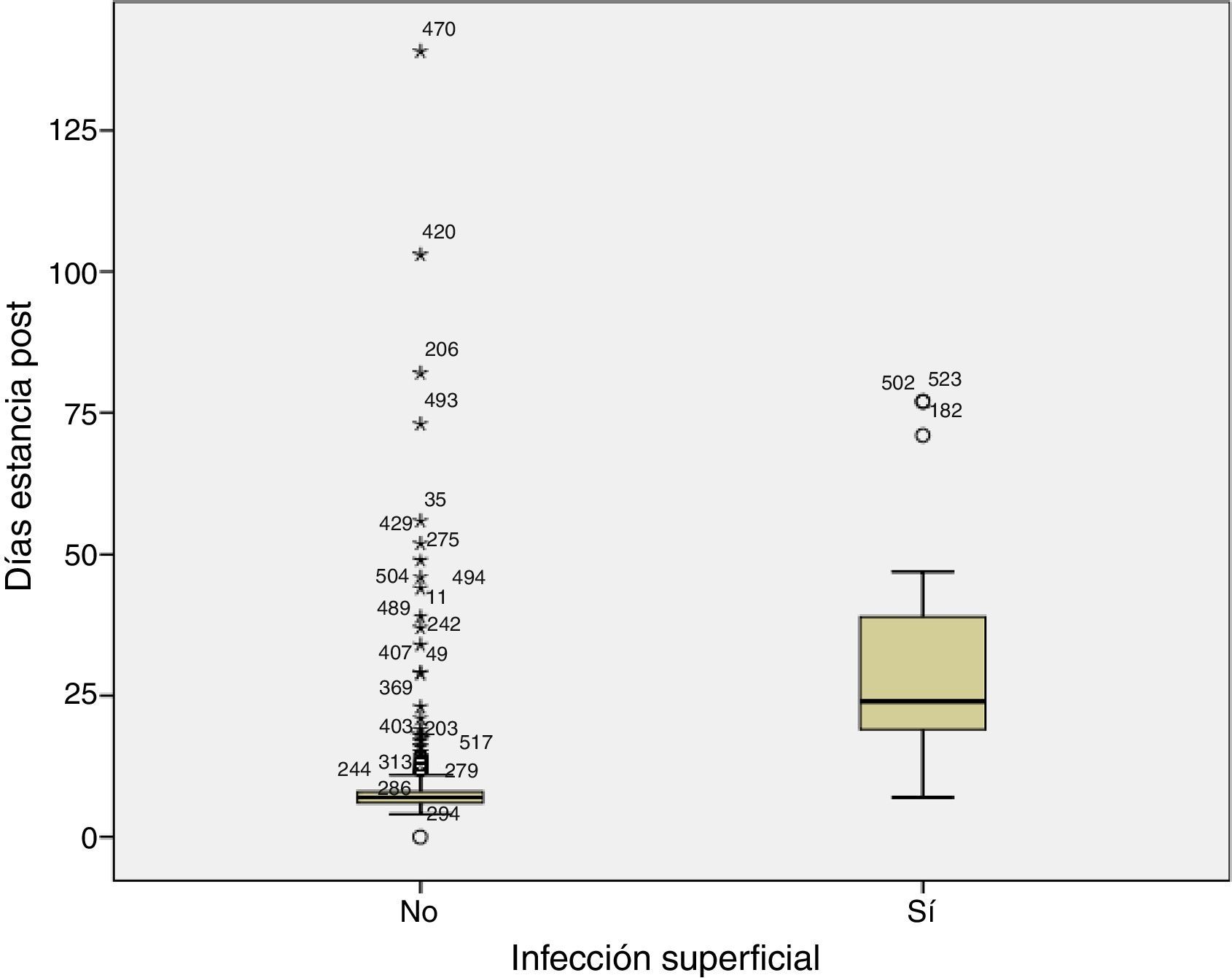
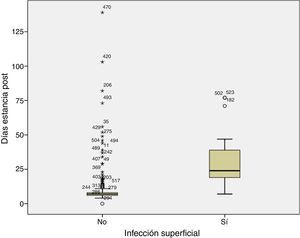
El hecho de desarrollar infección superficial de la herida provoca un aumento de estancia hospitalaria estadísticamente significativo p<0,000, siendo la media de estancia de los que no desarrollaron infección de 10 días frente a 30 días en los que si la desarrollaron (fig. 1).
En los contrastes no paramétricos de variables que no siguen una ley normal, la comparación de medias de las variables cuantitativas dividiendo a los pacientes en 2 grupos, grupo 1: infección superficial sí y grupo 2: infección superficial no, no muestran diferencias significativas en las variables analizadas (edad, nivel de creatinina, tiempo de CEC, tiempo de pinzamiento aórtico, número de injertos, EuroScore logístico i, hematocrito (Hto) postoperatorio, hemoglobina (Hb) postoperatoria, duración de la intervención), con nivel de significación p<0,05 y tampoco subiendo la significación a p<0,10.
Según los resultados de regresión logística univariante, usando como variable dependiente la infección superficial y como variables independientes las variables cuantitativas y cualitativas a analizar, se observan asociaciones en las siguientes:
- –
Confirmación de asociación con el sexo, encontrándose ser hombre como factor protector (intervalo de confianza [IC] del 95%: 0,123-0,568; p=0,001), con una odds ratio (OR) para mujer de 3,78, lo que significa que ser mujer aumenta casi 4 veces el riesgo de presentar infección respecto a ser hombre.
- –
La IR aumenta 3,7 veces el riesgo de desarrollar infección superficial de la herida (IC del 95%: 1,575-8,757; p=0,03).
- –
La transfusión de concentrados de hematíes en quirófano aumenta el riesgo en 4,2 veces respecto a los que no se transfundieron en quirófano (aunque estos requirieran posteriormente en unidad de cuidados intensivos o planta hospitalaria de alguna transfusión) (IC del 95%: 2,022-8,764; p=0,000).
Otros factores con clara tendencia sin llegar a ser significativos son los siguientes:
- –
Revascularización incompleta: parece tener 2 veces más riesgo de presentar infección que aquellos en los que es posible realizar una revascularización completa (OR 2,084), estando esta asociación al límite de la significación (p=0,063).
- –
Tabaquismo: se observa mayor incidencia (sin ser estadísticamente significativa) de infección superficial en aquellos fumadores de más de 2 paquetes al día, con una OR según Propensity score de 1,9.
- –
Diabéticos en tratamiento con antidiabéticos orales presentan 2,2 veces más riesgo de infección frente a los no diabéticos, mientras que aquellos en tratamiento con insulina presentan un riesgo ligeramente menor (OR de 1,5). Diferencias estadísticamente no significativas.
- –
Se ha encontrado como factor protector el tratamiento previo a la intervención con nitratos; pudiera explicarse por el efecto vasodilatador que podría tener repercusión a nivel cutáneo y subcutáneo (OR=0,307) (p=0,054).
No se han encontrado diferencias estadísticamente significativas en cuanto a desarrollo de infección según los tiempos de CEC y de pinzamiento aórtico, ni en aquellos pacientes con función de ventrículo izquierdo deprimida.
Factores como la edad, HTA, DL, vasculopatía periférica, ACV previo y reintervención por sangrado las primeras 24h no han añadido riesgo de problemas de herida esternal. Así mismo, el riesgo medido por EuroScore I tampoco se asocia a riesgo de infección superficial obtenido en nuestra serie de pacientes.
No se han encontrado diferencias estadísticamente significativas en cuanto a incidencia de infección según los diferentes tipos de técnicas quirúrgicas (arteria mamaria interna pediculada frente a esqueletizada), ni de los factores de riesgo influyentes en los 2 grupos por separado. Cabe destacar que la muestra de pacientes con técnica pediculada es mucho menor y esto pudiera tener repercusión estadística (tablas 3 y 4).
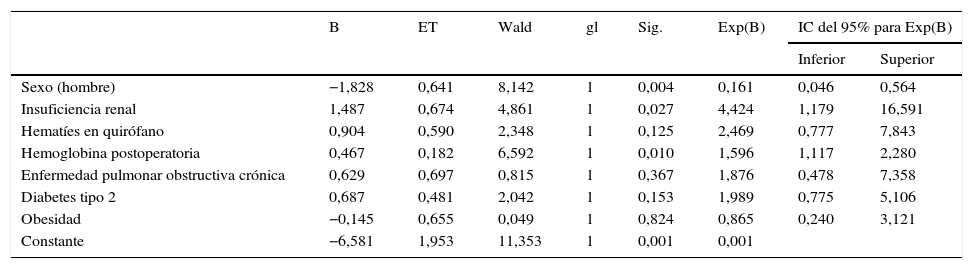
Multivariante. Esqueletizada
| B | ET | Wald | gl | Sig. | Exp(B) | IC del 95% para Exp(B) | ||
|---|---|---|---|---|---|---|---|---|
| Inferior | Superior | |||||||
| Sexo (hombre) | −1,828 | 0,641 | 8,142 | 1 | 0,004 | 0,161 | 0,046 | 0,564 |
| Insuficiencia renal | 1,487 | 0,674 | 4,861 | 1 | 0,027 | 4,424 | 1,179 | 16,591 |
| Hematíes en quirófano | 0,904 | 0,590 | 2,348 | 1 | 0,125 | 2,469 | 0,777 | 7,843 |
| Hemoglobina postoperatoria | 0,467 | 0,182 | 6,592 | 1 | 0,010 | 1,596 | 1,117 | 2,280 |
| Enfermedad pulmonar obstructiva crónica | 0,629 | 0,697 | 0,815 | 1 | 0,367 | 1,876 | 0,478 | 7,358 |
| Diabetes tipo 2 | 0,687 | 0,481 | 2,042 | 1 | 0,153 | 1,989 | 0,775 | 5,106 |
| Obesidad | −0,145 | 0,655 | 0,049 | 1 | 0,824 | 0,865 | 0,240 | 3,121 |
| Constante | −6,581 | 1,953 | 11,353 | 1 | 0,001 | 0,001 | ||
ET: error típico; Exp(B): odds ratio.
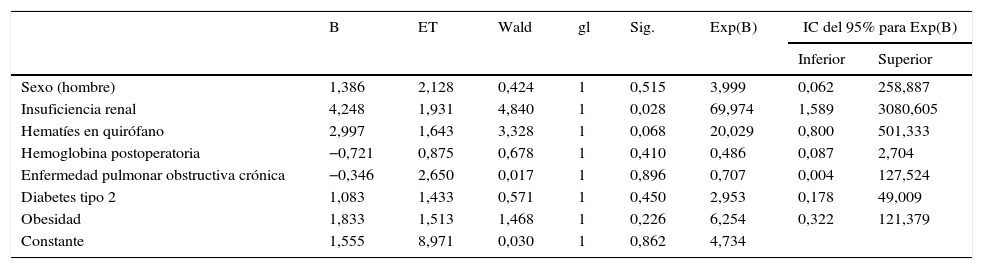
Multivariante arteria mamaria interna pediculada
| B | ET | Wald | gl | Sig. | Exp(B) | IC del 95% para Exp(B) | ||
|---|---|---|---|---|---|---|---|---|
| Inferior | Superior | |||||||
| Sexo (hombre) | 1,386 | 2,128 | 0,424 | 1 | 0,515 | 3,999 | 0,062 | 258,887 |
| Insuficiencia renal | 4,248 | 1,931 | 4,840 | 1 | 0,028 | 69,974 | 1,589 | 3080,605 |
| Hematíes en quirófano | 2,997 | 1,643 | 3,328 | 1 | 0,068 | 20,029 | 0,800 | 501,333 |
| Hemoglobina postoperatoria | −0,721 | 0,875 | 0,678 | 1 | 0,410 | 0,486 | 0,087 | 2,704 |
| Enfermedad pulmonar obstructiva crónica | −0,346 | 2,650 | 0,017 | 1 | 0,896 | 0,707 | 0,004 | 127,524 |
| Diabetes tipo 2 | 1,083 | 1,433 | 0,571 | 1 | 0,450 | 2,953 | 0,178 | 49,009 |
| Obesidad | 1,833 | 1,513 | 1,468 | 1 | 0,226 | 6,254 | 0,322 | 121,379 |
| Constante | 1,555 | 8,971 | 0,030 | 1 | 0,862 | 4,734 | ||
ET: error típico; Exp(B): odds ratio.
En el análisis multivariante se confirma como único parámetro significativo el sexo, siendo factor protector ser hombre (IC del 95%: 0,060-0,743; p=0,015). Otros factores tienen clara tendencia a favorecer la infección, como son la Hb postoperatoria (cada gramo de aumento de Hb supone un aumento de riesgo de 1,466 veces, IC del 95%: 0,965-2,228; p=0,073). Aquellos pacientes que presentan EPOC tendrían un riesgo aumentado 3,475 veces (IC del 95%: 0,9-13,417; p=0,071).
No se han encontrado asociaciones con el resto de interacciones entre variables.
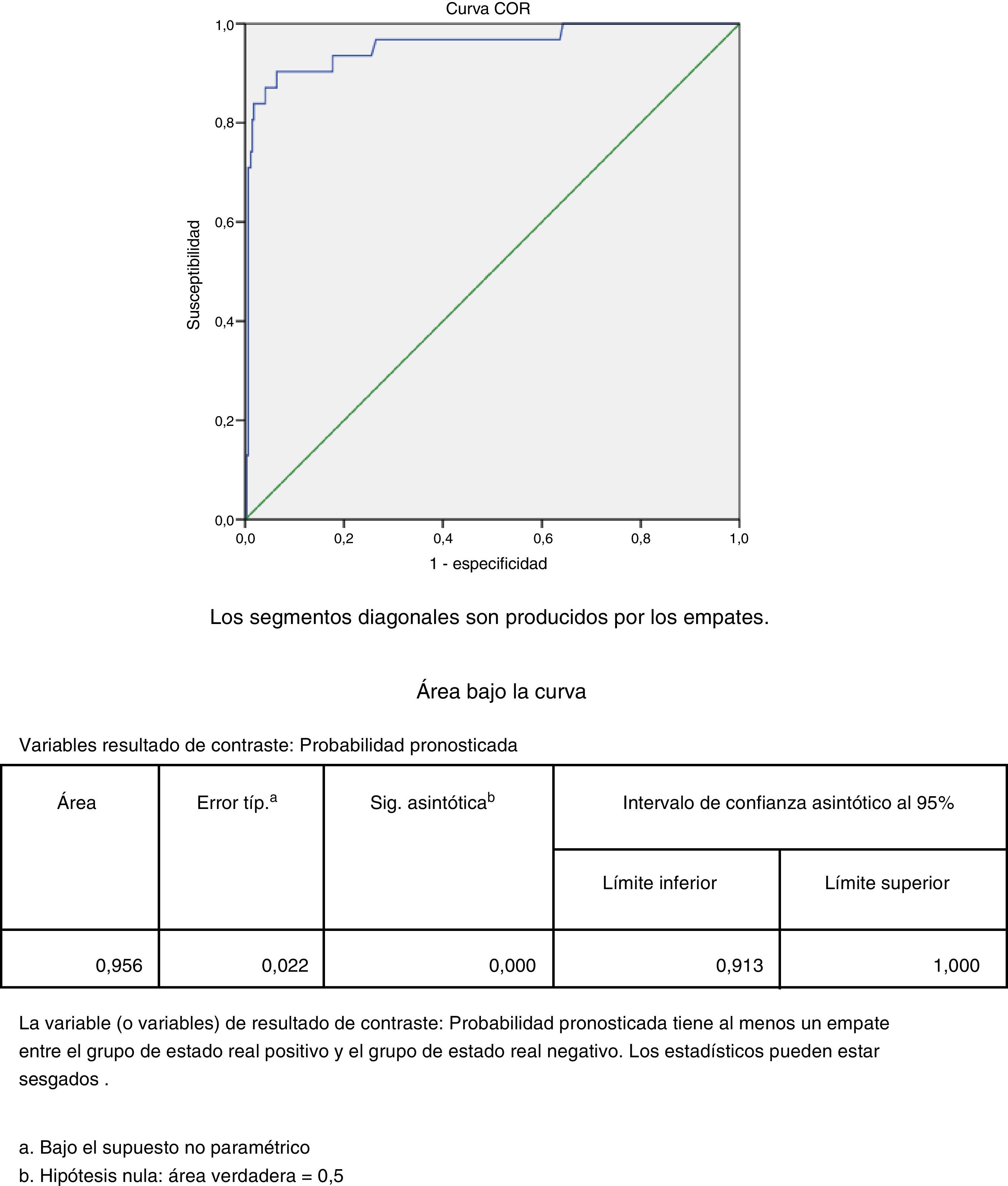
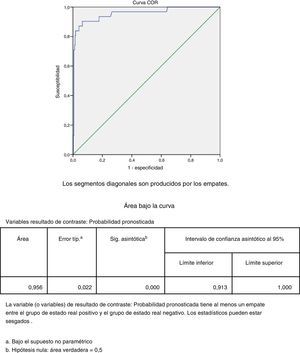
Como prueba de bondad de ajuste del modelo obtuvimos una curva características operativas del receptor (COR) comparando las probabilidades de tener infección superficial que pronostica el modelo de la curva de probabilidad 0,5, con un área bajo la curva recogido como contraste de hipótesis según la figura 2.
DiscusiónEn cirugía de revascularización miocárdica, el uso de arteria mamaria interna como injerto arterial está considerado como patrón de oro1-4; sin embargo, el uso doble de arteria mamaria, que debería mejorar estos resultados, se ha asociado a una mayor incidencia de dehiscencia esternal y/o problemas de herida quirúrgica10,12-22.
De manera tradicional se ha considerado que la cirugía de revascularización miocárdica con el uso de injertos arteriales es superior a aquella realizada con venas. Dicho abordaje aporta unos excelentes resultados de permeabilidad a largo plazo minimizando la necesidad de reintervenciones. Esto es especialmente importante en pacientes jóvenes y/o con enfermedad multivaso. Sin embargo, la revascularización arterial ha recorrido un largo camino antes de ser ampliamente apreciada, con algunos debates aún sin resolver, como la relación entre el uso de doble arteria mamaria y la infección esternal.
La disección de la arteria mamaria interna de manera pediculada para su utilización como injerto implica la disección de la pleura parietal circundante, venas, músculo y fascia acompañante, dejando el pecho devascularizado, especialmente con el uso de ambas arterias mamarias23. Esto, según autores como de Paulis et al.24, podría traducirse en disminución significativa del aporte de sangre esternal, lo que perjudica la cicatrización de heridas y conduce posteriormente a la infección esternal.
Debido a ello, algunos autores recomiendan el uso de arteria esqueletizada para evitar infecciones esternales25. En nuestro estudio no se encuentran diferencias significativas en cuanto a técnica quirúrgica utilizada, pero el número de pacientes realizado mediante técnica pediculada es menor.
Los pacientes con heridas inicialmente comprometidas por la capacidad de curación (p. ej., pacientes con DM) están en mayor riesgo para desarrollar mediastinitis posquirúrgica, especialmente en pacientes sometidos a arteria mamaria interna bilateral (AMIB)26,27. Esto queda respaldado por publicaciones antiguas, como las de Loop et al., gran estudio retrospectivo de 1990, con pacientes diabéticos que recibían AMIB; se concluyó que eran 5 veces más propensos a presentar mediastinitis28. Otro estudio, de Borger et al., compuesto por más de 12.000 pacientes, informó de que el riesgo de mediastinitis en los pacientes diabéticos aumentó del 1,3 al 14,3% con el uso de AMIB29. En nuestra serie, los diabéticos tienen mayor incidencia de infección superficial (p=0.069) sin llegar a ser significativa; esto queda apoyado por numerosos estudios más recientes, que muestran las ventajas del uso de doble arteria mamaria frente a mamaria única. Un ejemplo de ello son los trabajos de Puskas et al. y Stevens et al., y la revisión de Raja, los cuales demuestran el beneficio del uso de doble arteria mamaria incluso en pacientes diabéticos, sin encontrar diferencias estadísticamente significativas en cuanto a incidencia de infección esternal profunda (mediastinitis) en aquellos casos en los que se usó una mamaria con respecto a los de doble arteria mamaria, y con mejor supervivencia a largo plazo de estos últimos26,30,31.
O Galbut et al., con un estudio multivariante, el cual observa ventajas de uso de AMIB con mayor supervivencia a largo plazo en pacientes revascularizados con AMIB con respecto a arteria mamaria interna unilateral (AMIU), sin encontrar más infecciones esternales tanto en pacientes con función ventricular normal, como aquellos con función ventricular disminuida32, hallazgo coincidente en nuestra serie.
Incluso autores como Hashimoto et al. obtienen beneficios a largo plazo en pacientes octogenarios en términos de supervivencia y ausencia de eventos cardiacos, o cerebrovasculares en aquellos pacientes revascularizados con ambas arterias mamarias respecto a los de mamaria única, sin incrementar con ello la tasa de infección esternal33.
El metaanálisis de Smith et al. apoya la teoría del aumento de supervivencia de aquellos pacientes con doble mamaria respecto a mamaria única34. Así mismo, hay estudios que objetivan este beneficio en supervivencia en pacientes obesos35,36; sin embargo, otros estudios encuentran mayor tasa de infección esternal en obesos sin el aumento de supervivencia con el uso de AMIB respecto a AMIU37.
Otro estudio reciente de Kurlansky et al. informó de los resultados que comparan los beneficios de supervivencia a 30 años de seguimiento de AMIU vs. AMIB38. A los 15 años, la supervivencia fue del 39% para AMIU y el 53,5% para AMIB, mientras que a los 25 años la supervivencia fue de 16,5%±2,1% para AMIU y 28,5%±2,2% para AMIB (p=0,001).
A la luz de estas contradicciones, este artículo intenta esclarecer los resultados de esta técnica quirúrgica y su éxito clínico, según la experiencia de un centro de territorio nacional con años de experiencia y diferentes cirujanos, así como un breve comparativo entre ambas técnicas quirúrgicas (arteria mamaria interna pediculada vs. arteria mamaria esqueletizada).
ConclusionesEl uso de doble arteria mamaria para revascularización miocárdica es una técnica segura y reproducible.
La incidencia de dehiscencia esternal según nuestra casuística fue del 0,58%. No obstante, analizando esta incidencia en nuestros pacientes, hemos visto que no hay una mayor proporción de dehiscencia esternal; sin embargo, sí encontramos pacientes que desarrollaron problemas de herida, encontrándose una asociación con parte de los factores de riesgo analizados.
Tan solo 2 pacientes (0,38%) presentaron mediastinitis; esto nos indica que en su mayoría desarrollaron problemas superficiales de la herida quirúrgica. En mujeres, pacientes nefrópatas, diabéticos, con EPOC y obesos, habría que extremar las precauciones y los cuidados de la herida, ya que presentan una mayor incidencia, siendo esta diferencia estadísticamente significativa tan solo en mujeres y pacientes con nefropatía.
Un dato curioso es el aumento de incidencia estadísticamente significativa en aquellos pacientes que requirieron transfusión de concentrado de hematíes en quirófano; esta asociación no se encuentra con los parámetros de HB y/o Hto prequirúrgico ni prealta, ni con la necesidad de transfundir en el resto del tiempo de ingreso, por lo que habría que plantearse ser más estrictos con el punto de corte a partir del cual transfundir a nuestros pacientes durante la intervención.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.