La revascularización coronaria de la arteria descendente anterior (DA) mediante derivación aortocoronaria mínimamente invasiva (MIDCAB) mantiene los beneficios del uso de la arteria mamaria interna izquierda y evita las complicaciones asociadas a la esternotomía media y a la circulación extracorpórea. El objetivo es presentar nuestra experiencia inicial en el MIDCAB.
Material y métodoSe incluyeron todos los pacientes intervenidos mediante MIDCAB de marzo 2019 a junio del 2020. En todos los pacientes se realizó un puente coronario de arteria mamaria interna izquierda a la descendente anterior mediante minitoracotomía anterolateral izquierda sin circulación extracorpórea.
ResultadosSe intervinieron 22 pacientes. La mediana de edad era de 70 años (IQR 63-77) y el 90,9% (n = 20) eran varones. En dos pacientes con estenosis aórtica severa se realizó simultáneamente implante de una prótesis aórtica transcatéter por vía transapical y en ocho (36,4%) pacientes se realizó un procedimiento híbrido con revascularización percutánea al resto de lesiones. No hubo mortalidad hospitalaria, infarto agudo de miocardio, accidente cerebrovascular, ni fracaso renal agudo postoperatorio. La mediana de estancia hospitalaria fue de cuatro días (IQR 3-5).
ConclusionesEl MIDCAB es una técnica segura y eficaz para la revascularización coronaria en el territorio de la descendente anterior que combina las ventajas de un abordaje mínimamente invasivo sin circulación extracorpórea y el uso de la arteria mamaria interna izquierda para la realización de un puente coronario.
Coronary revascularization of the anterior descending artery (DA) using MIDCAB (Minimally Invasive Direct Coronary Artery Bypass) maintains the benefits of the use of the left internal mammary artery (AMII) and avoids the complications associated with middle sternotomy and extracorporeal circulation. The objective is to present our initial experience at MIDCAB.
Material and methodAll patients who underwent MIDCAB from March 2019 to June 2020 were included. In all patients, a left internal mammary artery bypass was performed to the anterior descending artery using a left anterolateral minithoracotomy without extracorporeal circulation.
Results22 patients. The median age was 70 years (IQR 63-77) and 90.9% (n = 20) were male. Transapical aortic valve implantation was performed simultaneously in two patients with severe aortic stenosis and in 8 (36.4%) patients a hybrid procedure with percutaneous coronay intervention was performed for the rest of the lesions. There were no hospital mortality, miocardial infarction, stroke, or postoperative acute renal failure. The median hospital stay was 4 days (IQR 3-5).
ConclusionsMIDCAB is a safe and effective technique for coronary revascularization in the left anterior descending coronary artery that combines the advantages of a minimally invasive approach without extracorporeal circulation and the use of the left internal mammary artery bypass.
La revascularización miocárdica quirúrgica es la técnica de elección en pacientes con enfermedad coronaria multivaso1,2. La derivación coronaria de arteria mamaria interna izquierda (AMII) a la descendente anterior (DA) presenta una tasa de permeabilidad de hasta el 98% a los 10 años y se asocia con un menor riesgo de muerte, infarto agudo de miocardio y recurrencia de la angina al compararlo con injertos venosos y/o tratamiento percutáneo3,4.
La cirugía coronaria mediante derivación aortocoronaria mínimamente invasiva (MIDCAB) combina los beneficios de la derivación coronaria de AMII a la DA con una menor invasividad del procedimiento, lo que se traduce en una menor morbimortalidad, estancia hospitalaria y coste3–9. Además, en pacientes seleccionados con enfermedad coronaria multivaso se puede realizar un procedimiento híbrido en el que se combina el MIDCAB para la DA con la revascularización percutánea del resto de las lesiones1.
El objetivo de este estudio es presentar nuestra experiencia inicial en el MIDCAB.
Material y métodosSe revisaron retrospectivamente todos los pacientes intervenidos mediante MIDCAB desde que se comenzó a realizar el procedimiento en nuestro centro en marzo del 2019 a junio del 2020. Todas las intervenciones fueron realizadas por el mismo cirujano. La información se extrajo de la base de datos del servicio de cirugía cardiaca. El estudio fue aprobado por el comité ético de nuestro centro.
En todos los pacientes se realizaron como pruebas preoperatorias analítica de sangre, electrocardiograma, radiografía de tórax, ecocardiograma transtorácico y coronariografía. Se registraron las variables preoperatorias, perioperatorias y postoperatorias, así como los resultados a corto plazo.
La mortalidad hospitalaria se definió como muerte durante el ingreso o durante los primeros 30 días tras la cirugía. La mortalidad durante el seguimiento se realizó mediante el cruce de nuestra base de datos con el registro del Índice Nacional de Defunciones (INDEF) (fig. 1).
La intervención se realizó bajo anestesia general y sin circulación extracorpórea. El paciente se posicionó en cúbito supino con inclinación lateral derecha. Se utilizó un tubo de doble luz para intubación pulmonar selectiva.
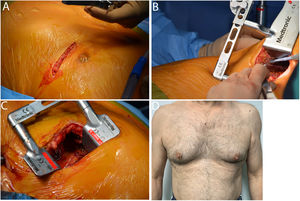
Se realizó una minitoracotomía anterolateral izquierda de unos 5-6 cm de longitud en el 5° espacio intercostal. Utilizamos el separador ThoraTrack® (Medtronic, Minneapolis, Minn.) y el dispositivo de tracción Rultract® skyhook retractor system (Rultract Cleveland, Ohio), especialmente diseñados para este procedimiento. La AMII se disecó esqueletizada bajo visión directa, desde la vena subclavia hasta el sexto espacio intercostal. Tras la heparinización (1,5 mg/kg, ACT > 250 s), introducimos el estabilizador Octopus Nuvo® (Medtronic, Minneapolis, Minn.) a través del 6° espacio intercostal. La anastomosis se realizó con sutura continua de polipropileno de 7/0. Sólo se utilizó shunt intracoronario si al ocluir la DA se produjeron cambios eléctricos y/o inestabilidad hemodinámica.
Utilizamos ecografía epicárdica 2 D y doppler para seleccionar la zona más adecuada para la anastomosis, y flujometría por tiempo de tránsito para confirmar el funcionamiento del bypass (MiraQ Cardiac®, Medistim AS, Oslo, Noruega). Se consideró que el puente coronario es normofuncionante si el índice de pulsatilidad es menor a 3, el flujo medio mayor de 15 mL/min, el porcentaje de llenado diastólico mayor del 50% y el retorno sistólico o insuficiencia menor del 3%10.
Posteriormente se realizó la hemostasia de la pared torácica, se dejó un drenaje pleural curvo de 32F y se cerró la incisión por planos, dejando en el subcutáneo un catéter multiperforado conectado a una bomba elastomérica para la administración de analgesia durante las primeras 48 horas.
El video 1 resume brevemente la técnica quirúrgicaEl implante de una prótesis aórtica transcatéter (TAVI) se realizó por vía transapical según la técnica descrita previamente11.
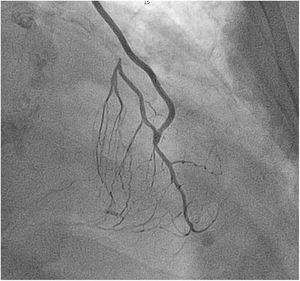
En los pacientes sometidos a un procedimiento híbrido la revascularización percutánea se realizó en dos tiempos a las 48-72 h tras la intervención durante el mismo ingreso. Siempre se realizó previamente una pontografía para verificar la permeabilidad del puente coronario de AMII (fig. 2).
Análisis estadísticoLas variables continuas fueron expresadas con la media y desviación estándar, o mediana e intervalo intercuartil si no seguían una distribución normal. Las variables categóricas se expresaron en frecuencias absolutas y relativas (porcentajes). El análisis estadístico fue realizado con STATA 15 (StataCorp 2015. College Statio, TX).
ResultadosFueron intervenidos 22 pacientes mediante MIDCAB. Las características preoperatorias se describen en la tabla 1.
Características preoperatorias
| N = 22 | |
|---|---|
| Edad (años) | 70 (IQR 63 – 77) |
| Sexo masculino | 20 (90,9%) |
| HTA | 14 (63,6%) |
| Dislipemia | 12 (54,6%) |
| Fumador | 6 (27,3%) |
| Diabetes | 14 (63,6%) |
| Enf. arterial periférica | 5 (22,7%) |
| ACV | 1 (4,6%) |
| EPOC | 3 (13,6%) |
| ERC (FG < 60ml/min) | 7 (31,8%) |
| NYHA | |
| I | 10 (45,5%) |
| II | 9 (40,9%) |
| III | 2 (9,1%) |
| IV | 1 (4,6%) |
| Ritmo sinusal | 19 (86,4%) |
| FEVI % | 56,7 (± 9,8) |
| Normal (>60%) | 13 (59,1%) |
| Disfunción ligera (51-60%) | 3 (13,6%) |
| Disfunción moderada (31-50%) | 6 (27,3%) |
| ES I | 4,8 (IQR 1,8-7,9) |
| ES II | 2,1 (IQR 1,4-7,8) |
HTA: Hipertensión arterial. ACV: Accidente cerebrovascular; EPOC: Enfermedad pulmonar obstructiva crónica; ERC: Enfermedad renal crónica; NYHA: New York Heart Association; FEVI: Fracción de eyección del ventrículo izquierdo; ES: EuroSCORE.
La mediana de edad fue de 70 años (IQR: 63-77) y el 90,9% (n = 20) eran varones. El 86,4% (n = 19) de los pacientes se encontraban en una clase funcional NYHA I-II. La clínica predominante fue angina estable en el 59% (n = 13). El 22,7% (n = 5) presentaba una fracción de eyección del ventrículo izquierdo moderadamente deprimida y dos pacientes presentaban una estenosis aórtica severa.
En la coronariografía preoperatoria un paciente presentaba lesión aislada severa del tronco coronario, seis pacientes lesión aislada de la DA, siete pacientes enfermedad coronaria de dos vasos y ocho pacientes enfermedad de tres vasos.
La mediana del EuroSCORE II fue de 2,1 (IQR 1,4-7,8).
En todos los pacientes se realizó un puente de AMII a la DA. En dos pacientes con estenosis aórtica severa preoperatoria se realizó simultáneamente un implante de TAVI transapical, por tratarse de pacientes con riesgo quirúrgico elevado y patología vascular periférica. Se realizó un abordaje híbrido mediante revascularización percutánea tras la intervención en ocho (36.4%) pacientes en dos tiempos. En dos pacientes se revascularizó la arteria coronaria derecha y en seis pacientes la arteria circunfleja. En los ocho pacientes el puente coronario de AMII estaba permeable sin estenosis.
Un paciente tuvo que convertirse a esternotomía media debido a que la DA era intramiocárdica en todo su trayecto. Se realizó el puente de AMII a la DA sin CEC y el postoperatorio transcurrió sin incidencias.
Todos los pacientes fueron extubados en el quirófano.
No hubo mortalidad hospitalaria, infarto agudo de miocardio, accidente cerebrovascular o fracaso renal postoperatorio. Un paciente (4,5%) fue reoperado por sangrado y cuatro pacientes (18,2%) presentaron fibrilación auricular postquirúrgica cardiovertida a ritmo sinusal con tratamiento médico.
La mediana de estancia en la Unidad de Cuidados Intensivos (UCI) fue de un día (IQR 1–2) y la de estancia hospitalaria de cuatro días (IQR 3-5).
La mediana de seguimiento es de 6,5 meses (IQR 4,5-11,1). Un paciente falleció a los seis meses tras la intervención por un accidente cerebrovascular no relacionado con el procedimiento.
DiscusiónEn pacientes con enfermedad coronaria multivaso la cirugía coronaria mediante esternotomía media es la técnica quirúrgica de elección2. La permeabilidad del puente coronario de arteria mamaria interna izquierda a la descendente anterior es mayor del 90% a los 10 años y se asocia a un menor riesgo de muerte, infarto agudo de miocardio, recurrencia de la angina y a una mayor supervivencia a largo plazo en comparación con otros injertos utilizados y/o con la revascularización percutánea3–5.
La cirugía coronaria mínimamente invasiva es una opción terapéutica en pacientes seleccionados que añade al beneficio a largo plazo del puente de AMII a la DA una menor morbilidad al evitar la esternotomía media y la circulación extracorpórea (accidente cerebrovascular, fracaso renal agudo, infección de herida quirúrgica), una menor estancia hospitalaria y menores costes6–9. Esto se traduce en un menor tiempo de recuperación postoperatorio y una incorporación más temprana a las actividades de la vida diaria, con una mejor calidad de vida durante el seguimiento12.
El MIDCAB está indicado principalmente en pacientes con enfermedad aislada de la DA o en determinados pacientes con enfermedad coronaria de dos o tres vasos en combinación con el tratamiento coronario percutáneo mediante un abordaje híbrido13.
Raja et al.6 en una serie de 668 pacientes sometidos a cirugía de revascularización de la DA mediante MIDCAB o esternotomía sin circulación extracorpórea, no encontraron diferencias significativas en la mortalidad hospitalaria ni en la supervivencia a largo plazo. Xu5 et al. en su estudio de 300 pacientes que comparaba MIDCAB frente a cirugía coronaria convencional, obtuvo un menor tiempo quirúrgico, menor necesidad de transfusión, menor tiempo de intubación y menor estancia hospitalaria y en la unidad de cuidados intensivos para el grupo MIDCAB. Aunque se trata de un procedimiento más demandante desde el punto de vista técnico, las tasas de permeabilidad de los puentes realizados mediante MIDCAB son comparables a las de la cirugía de revascularización coronaria convencional14.
El riesgo de conversión a esternotomía media está entre el 0% al 6%14. Uno de nuestros pacientes tuvo que ser convertido al presentar una DA intramiocárdica que no se sospechó en la coronariografía preoperatoria. Es clave la selección adecuada de los pacientes candidatos para esta técnica con el fin de evitar la morbimortalidad relacionada sobre todo con el fracaso respiratorio postoperatorio, la conversión a esternotomía media y la oclusión precoz o tardía de la AMII. Se consideran buenos candidatos aquellos pacientes que presentan un IMC inferior a 30 kg/m2, con una fracción de eyección por encima del 45%, con afectación asilada de la DA o con lesiones en otras arterias no revascularizables. Por otro lado, pacientes con DA intramiocárdica, enfermedad pulmonar obstructiva crónica (EPOC) severa, deformidades en la cavidad torácica o con indicación de revascularización quirúrgica urgente no son buenos candidatos para esta técnica15.
La revascularización coronaria híbrida permite la revascularización completa mínimamente invasiva en pacientes con enfermedad coronaria multivaso donde la arteria circunfleja o derecha tienen malos lechos para la cirugía o presentan comorbilidades que elevan el riesgo de la esternotomía media, aunque debe tenerse en cuenta que la necesidad de nuevas revascularizaciones es mayor16–19.
Ocho pacientes en nuestra serie (36,4%) se sometieron a revascularización percutánea tras la intervención como parte de un procedimiento híbrido planificado. El resto de los pacientes que presentaban afectación de territorios no dependientes de la descendente anterior tenían lechos no revascularizables quirúrgica ni percutáneamente.
Dos de nuestros pacientes presentaban además una estenosis aórtica severa. Tras realizar el puente a la DA, se realizó el implante de una TAVI vía transapical. Se trata de una alternativa para tener en cuenta en pacientes con riesgo quirúrgico elevado, vasculopatía periférica y/o lesión severa en la DA no revascularizable percutáneamente20–23.
ConclusiónEl MIDCAB es una técnica quirúrgica segura y eficaz para la revascularización del territorio de la descendente anterior que combina las ventajas de un abordaje mínimamente invasivo sin circulación extracorpórea y el uso del puente coronario de arteria mamaria interna izquierda.
LimitacionesSe trata de un estudio retrospectivo, de un único centro, de pacientes seleccionados y con un seguimiento corto.
FinanciaciónEste trabajo no ha recibido ningún tipo de financiación.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Presentado en el XXV Congreso de la SECCE de Octubre 2020.