Desarrollar un modelo predictivo multivariante del accidente cerebrovascular (ACV) intrahospitalario tras cirugía de bypass coronario.
MétodosVeintiséis mil trescientos cuarenta y siete pacientes incluidos en el estudio procedentes de 21 bases de datos de hospitales españoles. El análisis de regresión logística fue utilizado para predecir el riesgo de ACV perioperatorio (ictus o accidente isquémico transitorio). El modelo predictivo fue desarrollado a partir de un subgrupo de datos «de prueba» y validado en otro subgrupo independiente, ambos seleccionados aleatoriamente del total de la muestra. La capacidad predictiva del modelo se relacionó con el área bajo la curva ROC (ABC). Las variables consideradas fueron: preoperatorias (edad, sexo, diabetes mellitus, hipertensión arterial, ACV previo, insuficiencia cardiaca y/o fracción de eyección del ventrículo izquierdo <40%, prioridad de la intervención no electiva, arteriopatía extracardiaca, insuficiencia renal crónica y/o creatininemia≥2mg/dl y fibrilación auricular) e intraoperatorias (cirugía coronaria con/sin circulación extracorpórea).
ResultadosIncidencia global de ACV perioperatorio 1,38%. La prioridad no electiva de la cirugía (priority; OR=2,32), arteriopatía extracardiaca (arteriopathy; OR=1,37), insuficiencia cardiaca (cardiac; OR=3.64) e insuficiencia renal crónica (kidney; OR=6,78) fueron identificados como factores de riesgo independientes de ACV perioperatorio en los modelos uni y multivariante en el subgrupo de prueba; p<0,0001; ABC=0,77, IC del 95%, 0,73-0,82. El modelo PACK2 de ACV perioperatorio tras cirugía de bypass coronario se estableció con 1 punto para cada ítem, excepto para la insuficiencia renal crónica que se le otorgaron 2 puntos (rango 0-5 puntos); ABC=0,76, IC del 95%, 0,72-0,80. En pacientes con puntuación PACK2≥2 puntos, la cirugía coronaria sin circulación extracorpórea redujo la incidencia de ACV en un 2,3% cuando se comparó con el grupo con cirugía realizada con circulación extracorpórea.
ConclusionesLa escala de riesgo PACK2 muestra una buena capacidad predictiva en los datos analizados y podría ser útil en la toma de decisiones y selección de pacientes de la práctica clínica.
To develop a multivariate predictive risk score of perioperative in-hospital stroke after coronary artery bypass grafting (CABG) surgery.
MethodsA total of 26,347 patients were enrolled from 21 Spanish hospital databases. Logistic regression analysis was used to predict the risk of perioperative stroke (stroke or transient ischaemic attack). The predictive scale was developed from a training set of data and validated by an independent test set, both selected randomly from the global sample. The assessment of the accuracy of prediction was related to the area under the ROC curve (AUC). The variables considered were: preoperative (age, gender, diabetes mellitus, arterial hypertension, previous stroke, cardiac failure and/or left ventricular ejection fraction<40%, non-elective priority of surgery, extracardiac arteriopathy, chronic kidney failure and/or serum creatinine ≥2mg/dl, and atrial fibrillation) and intra-operative (on/off-pump).
ResultsThe overall perioperative stroke incidence was 1.38%. Non-elective priority of surgery (priority; OR=2.32), vascular disease (arteriopathy; OR=1.37), heart failure (cardiac; OR=3.64), and chronic kidney failure (kidney; OR=6.78) were found to be independent risk factors for perioperative stroke in uni- and multivariate models in the training set of data; P<.0001; AUC=0.77, 95% CI 0.73–0.82. The PACK2 stroke CABG score was established with 1 point for each item, except for chronic kidney failure with 2 points (range 0–5 points); AUC=0.76, 95% CI 0.72–0.80. In patients with PACK2 score ≥2 points, off-pump reduced perioperative stoke incidence by 2.3% when compared with on-pump CABG.
ConclusionsPACK2 risk scale shows good predictive accuracy in the data analysed and could be useful in clinical practice for decision making and patient selection.
Aunque la mortalidad en cirugía cardiaca ha disminuido en las décadas más recientes1, la morbilidad se ha incrementado fundamentalmente en relación con que los pacientes intervenidos tienen mayor edad y presentan mayor fragilidad debido a su morbilidad preoperatoria2. El accidente cerebrovascular (ACV) es una complicación grave de la cirugía de bypass coronario (CBPC) y su prevención es particularmente importante ya que los pacientes afectados presentan estancias más prolongadas en las unidades de cuidados intensivos, así como tasas marcadamente superiores de morbilidad hospitalaria. El riesgo de desarrollar un ACV tras CBPC no está homogéneamente establecido y diferentes factores clínicos y ecocardiográficos han sido identificados para contribuir a la estratificación de dicho riesgo. Derivado de ello, diversos modelos de predicción han sido desarrollados para identificar preoperatoriamente el subgrupo de pacientes con un riesgo incrementado de desarrollar un ACV perioperatorio; sin embargo, ninguno ha sido aplicado de forma extensiva en la práctica clínica3. La escala de riesgo NNECDSG4 fue desarrollada basándose en 33.062 pacientes consecutivos sometidos a CBPC en la región de Nueva Inglaterra (EE. UU.) entre 1992 y 2001, mostrando una adecuada capacidad predictiva con un área bajo la curva ROC (ABC) de 0,70 (intervalo de confianza del 95% [IC de 95%], 0,67-0,72). Sin embargo, sin lugar a dudas, hoy en día no se dispone de una herramienta aplicable, sencilla y ampliamente aceptada para establecer el riesgo de ACV perioperatorio, presentando cualesquiera de las desarrolladas sus propias limitaciones. El propósito de este estudio es definir una escala de riesgo clínica para estratificar el riesgo perioperatorio en la población de pacientes sometidos a CBPC, utilizando factores preoperatorios predictivos del ACV perioperatorio en un procedimiento rápido y eficiente que podría ser llevado a cabo incluso momentos previos a la intervención quirúrgica.
MetodologíaDiseño del estudio: cohortes de pacientes y recolección de datos.
Diseñamos un estudio retrospectivo, multicéntrico, observacional con pacientes adultos (≥ 18 años) sometidos CBPC aislado, reclutados de 21 hospitales del territorio nacional español (véase el apéndice 1). Los datos de los pacientes fueron obtenidos a partir de las bases de datos hospitalarias de los Servicios de Cirugía Cardiaca/Cardiovascular en orden cronológico inverso, comenzando a partir del 31 de diciembre del 2011. De acuerdo con los criterios de inclusión establecidos, solo fueron considerados pacientes sometidos a CBPC como procedimiento quirúrgico único. Los pacientes sometidos a más de un procedimiento quirúrgico de cirugía cardiaca mayor durante el periodo de estudio fueron solo considerados para el análisis exclusivamente en el primer procedimiento. Todos los pacientes sometidos a CBPC asociada a procedimientos quirúrgicos concomitantes fueron excluidos. Utilizando tablas estandarizadas de recogida de datos, fueron obtenidas selectivamente las variables de los pacientes estudiados a fin de contrarrestar la codificación heterogénea en cada una de las instituciones. Las variables consideradas fueron asimismo introducidas en una base de datos computarizada única de cara a su análisis estadístico una vez depuradas. Todas las variables clínicas recogidas habían mostrado en la literatura presentar un impacto estadísticamente significativo sobre el riesgo de ACV perioperatorio de acuerdo con el modelo predictivo NNECDSG4.
VariablesEl ACV perioperatorio fue definido como cualquier déficit temporal o permanente, focal o global; durante la intervención quirúrgica, en el periodo de los 30 días siguientes a la misma o posterior, si el paciente permanecía todavía ingresado, de acuerdo con las guías clínicas publicadas5. El ACV perioperatorio temporal incluyó el accidente isquémico transitorio, definido como aquel déficit neurológico completamente reversible y con duración <24 h. Los déficits neurológicos prolongados reversibles fueron definidos como episodios de duración >24 h y <3 semanas. Todos los ACV incluidos en el estudio fueron diagnosticados por un neurólogo y, en la mayoría de los casos, tomografía computarizada cerebral o resonancia magnética fueron utilizados para la objetivación de la lesión neurológica. El estudio excluyó a los pacientes con encefalopatía postoperatoria difusa presentada como delirium, estado confusional o agitación psicomotriz en el periodo postoperatorio inmediato, los cuales podrían estar relacionados con la utilización de circulación extracorpórea (CEC), aunque también podrían reflejar exposición prolongada a fármacos anestésicos6.
Las variables incluidas relacionadas con el riesgo de ACV perioperatorio fueron las 13 propuestas por el modelo predictivo NNECDSG, agrupadas en 9 factores mayores: edad, sexo femenino, diabetes mellitus, hipertensión arterial, enfermedad vascular periférica (incluyendo todas las formas de la enfermedad arterial extracardiaca como la claudicación intermitente, amputación, ausencia de pulsos distales y/o úlceras isquémicas en miembros inferiores; cirugía previa y/o intervencionismo percutáneo sobre aorta torácica-abdominal, miembro inferiores y/o troncos supraaórticos), insuficiencia renal crónica (tasa de filtrado glomerular conocida <60ml/min/1,73 m2, diálisis y/o creatininemia preoperatoria ≥2mg/dl), insuficiencia cardiaca preoperatoria (fracción de eyección del ventrículo izquierdo <40% por ecocardiografía o ventriculografía y/o clase funcional preoperatoria NYHA III-IV/IV), y prioridad de la cirugía no-electiva (urgencia: operación requerida dentro de las 24 h para minimizar el riesgo de deterioro clínico, o urgencia: intervención quirúrgica que no admite retraso en su ejecución). La presencia de fibrilación auricular preoperatoria fue asimismo considerada. La puntuación del modelo NNECDSG fue calculada para cada uno de los pacientes y fue utilizada en la validación del estudio multicéntrico. En su determinación, la variable de enfermedad vascular periférica fue computada por la combinación de la definición anterior más la presencia de ACV previo a la intervención como se define en [4]. La variable intraoperatoria considerada fue la realización de la CBPC con CEC o sin CEC.
Análisis estadísticoLas variables continuas fueron presentadas como media±desviación estándar y las variables categóricas fueron expresadas como porcentaje (%). El contraste de hipótesis fue realizado para las variables continuas mediante el test t de Student y para las categóricas el test de la χ2 o el test exacto de Fisher, según conveniencia. Una significación estadística de p<0,05 fue considerada como significativa.
El conjunto global de datos fue dividido aleatoriamente en un subgrupo de datos «de prueba» para desarrollar el modelo clínico predictivo de desarrollo de ACV perioperatorio y otro subgrupo independiente que fue utilizado para validar el modelo obtenido sobre un conjunto de datos diferente del que se utilizó para su desarrollo. Inicialmente, fue llevado a cabo un análisis univariante, incluyendo todas las variables preoperatorias y la realización de la CBPC con o sin CEC. Considerando los resultados neurológicos perioperatorios, las variables con un nivel de significación p<0,05 en el análisis univariante fueron incluidas en un modelo multivariante de regresión logística por pasos sucesivos, para determinar los predictores independientes de desarrollo de ACV perioperatorio. El modelo predictivo fue desarrollado incluyendo los anteriores factores de riesgo independiente, ponderando su fuerza de asociación con el resultado neurológico perioperatorio para obtener una escala de riesgo simple e intuitiva. Las capacidades predictivas del modelo multivariante de regresión logística, del modelo NNECDSG y del sistema desarrollado fueron establecidas por medio del ABC. La bondad de ajuste fue establecida por el test de Hosmer-Lemeshow (H-L) y fue aplicada para la calibración de los anteriores modelos.
Un test estadístico de estrés para probar el sistema de puntuación desarrollado fue obtenido seleccionando aleatoriamente 50 grupos de 1.000 pacientes del conjunto global de datos global y aplicando en cada uno de ellos el modelo predictivo. El ABC fue calculada para cada uno de los grupos individuales de 1.000 pacientes.
El análisis estadístico fue llevado a cabo mediante el pack estadístico de Estudios Sociológicos (IBM® SPSS® 19.0; SPSS Inc., Chicago, EE. UU.). El protocolo del estudio fue aprobado por el Comité de Investigación Científica en Sujetos Humanos de cada una de las instituciones participantes.
ResultadosCohorte de pacientesUn total de 28.296 pacientes fueron incluidos en el estudio. La contribución individual de cada una de las instituciones participantes fue variable (rango 157-3.060 pacientes). De ellos, 1.949 (6,89%) presentaron algún defecto en las variables perioperatorias requeridas, por lo que fueron excluidos del análisis. Las variables requeridas estuvieron completas para 26.347 (93,11%) pacientes. El conjunto total de datos fue dividido aleatoriamente en 2 subgrupos denominados «de prueba» (n=13.096, 49,7%) e independiente (n=13.246, 50,27%) para desarrollar y validar el modelo predictivo, respectivamente.
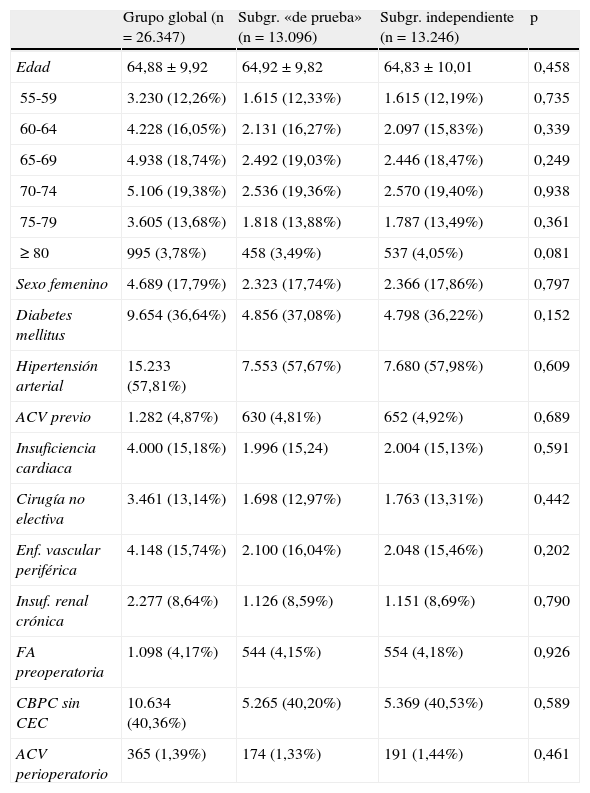
La incidencia global de ACV perioperatorio fue del 1,38%, cuyos valores oscilaron entre 0,3 y 2,5% entre los centros participantes. Las características de los pacientes estudiados quedan resumidas en la tabla 1. La puntuación NNECDSG mostró una buena capacidad predictiva del ACV perioperatorio en nuestra cohorte de estudio (ABC=0,69 [IC del 95%, 0,67-0,72], p<0,0001; test H-L: χ2=8,32, p=0,40).
Características preliminares de los grupos global y de los subgrupos «de prueba» e independiente
| Grupo global (n=26.347) | Subgr. «de prueba» (n=13.096) | Subgr. independiente (n=13.246) | p | |
| Edad | 64,88±9,92 | 64,92±9,82 | 64,83±10,01 | 0,458 |
| 55-59 | 3.230 (12,26%) | 1.615 (12,33%) | 1.615 (12,19%) | 0,735 |
| 60-64 | 4.228 (16,05%) | 2.131 (16,27%) | 2.097 (15,83%) | 0,339 |
| 65-69 | 4.938 (18,74%) | 2.492 (19,03%) | 2.446 (18,47%) | 0,249 |
| 70-74 | 5.106 (19,38%) | 2.536 (19,36%) | 2.570 (19,40%) | 0,938 |
| 75-79 | 3.605 (13,68%) | 1.818 (13,88%) | 1.787 (13,49%) | 0,361 |
| ≥ 80 | 995 (3,78%) | 458 (3,49%) | 537 (4,05%) | 0,081 |
| Sexo femenino | 4.689 (17,79%) | 2.323 (17,74%) | 2.366 (17,86%) | 0,797 |
| Diabetes mellitus | 9.654 (36,64%) | 4.856 (37,08%) | 4.798 (36,22%) | 0,152 |
| Hipertensión arterial | 15.233 (57,81%) | 7.553 (57,67%) | 7.680 (57,98%) | 0,609 |
| ACV previo | 1.282 (4,87%) | 630 (4,81%) | 652 (4,92%) | 0,689 |
| Insuficiencia cardiaca | 4.000 (15,18%) | 1.996 (15,24) | 2.004 (15,13%) | 0,591 |
| Cirugía no electiva | 3.461 (13,14%) | 1.698 (12,97%) | 1.763 (13,31%) | 0,442 |
| Enf. vascular periférica | 4.148 (15,74%) | 2.100 (16,04%) | 2.048 (15,46%) | 0,202 |
| Insuf. renal crónica | 2.277 (8,64%) | 1.126 (8,59%) | 1.151 (8,69%) | 0,790 |
| FA preoperatoria | 1.098 (4,17%) | 544 (4,15%) | 554 (4,18%) | 0,926 |
| CBPC sin CEC | 10.634 (40,36%) | 5.265 (40,20%) | 5.369 (40,53%) | 0,589 |
| ACV perioperatorio | 365 (1,39%) | 174 (1,33%) | 191 (1,44%) | 0,461 |
ACV: accidente cerebrovascular; CBPC: cirugía de bypass coronario; CEC: circulación extracorpórea; FA: fibrilación auricular.
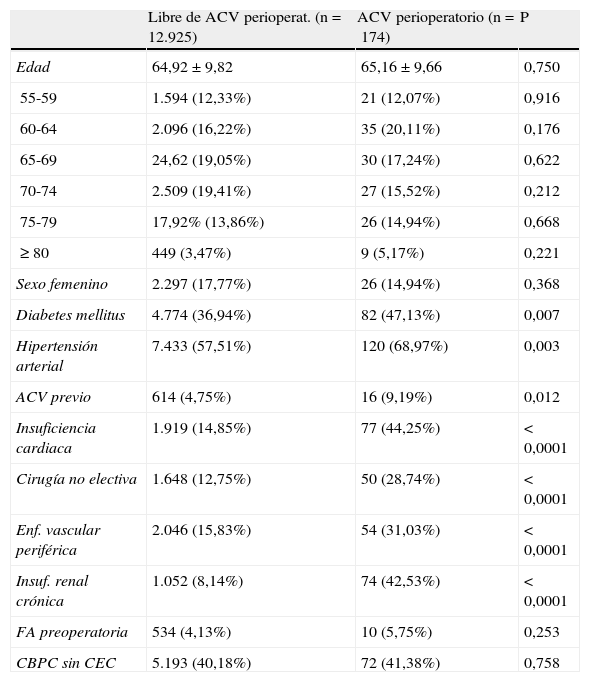
El análisis univariante fue realizado con el subgrupo «de prueba» (tabla 2.). La CBPC sin CEC no se relacionó con una tasa de ACV perioperatorio menor (1,31% CBPC con CEC vs. 1,38% CBPC sin CEC, p>0,05). El análisis multivariante mostró la insuficiencia cardiaca (OR=3,64, p<0,0001), la cirugía no electiva (OR=2,32, p<0,0001), la enfermedad vascular periférica (OR=1,37, p=0,007) y la insuficiencia renal crónica (OR=6,78, p<0,0001) como factores de riesgo independientes para el desarrollo de ACV perioperatorio tras CBPC (tabla 3). La bondad de ajuste por el test de H-L del modelo multivariante mostró buen ajuste (χ2=1,93, p=0,93) y una capacidad predictiva con ABC de 0,77 (IC del 95%, 0,73-0,82), p<0,0001.
Análisis univariante realizado en el subgrupo «de prueba»
| Libre de ACV perioperat. (n=12.925) | ACV perioperatorio (n=174) | P | |
| Edad | 64,92±9,82 | 65,16±9,66 | 0,750 |
| 55-59 | 1.594 (12,33%) | 21 (12,07%) | 0,916 |
| 60-64 | 2.096 (16,22%) | 35 (20,11%) | 0,176 |
| 65-69 | 24,62 (19,05%) | 30 (17,24%) | 0,622 |
| 70-74 | 2.509 (19,41%) | 27 (15,52%) | 0,212 |
| 75-79 | 17,92% (13,86%) | 26 (14,94%) | 0,668 |
| ≥ 80 | 449 (3,47%) | 9 (5,17%) | 0,221 |
| Sexo femenino | 2.297 (17,77%) | 26 (14,94%) | 0,368 |
| Diabetes mellitus | 4.774 (36,94%) | 82 (47,13%) | 0,007 |
| Hipertensión arterial | 7.433 (57,51%) | 120 (68,97%) | 0,003 |
| ACV previo | 614 (4,75%) | 16 (9,19%) | 0,012 |
| Insuficiencia cardiaca | 1.919 (14,85%) | 77 (44,25%) | <0,0001 |
| Cirugía no electiva | 1.648 (12,75%) | 50 (28,74%) | <0,0001 |
| Enf. vascular periférica | 2.046 (15,83%) | 54 (31,03%) | <0,0001 |
| Insuf. renal crónica | 1.052 (8,14%) | 74 (42,53%) | <0,0001 |
| FA preoperatoria | 534 (4,13%) | 10 (5,75%) | 0,253 |
| CBPC sin CEC | 5.193 (40,18%) | 72 (41,38%) | 0,758 |
ACV: accidente cerebrovascular; FA: fibrilación auricular; CBPC: cirugía de bypass coronario; CEC: circulación extracorpórea.
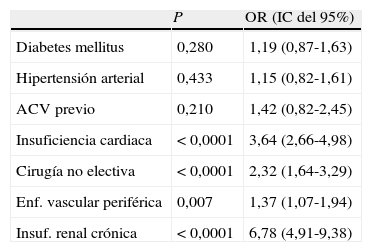
Análisis multivariante realizado en el subgrupo «de prueba»
| P | OR (IC del 95%) | |
| Diabetes mellitus | 0,280 | 1,19 (0,87-1,63) |
| Hipertensión arterial | 0,433 | 1,15 (0,82-1,61) |
| ACV previo | 0,210 | 1,42 (0,82-2,45) |
| Insuficiencia cardiaca | <0,0001 | 3,64 (2,66-4,98) |
| Cirugía no electiva | <0,0001 | 2,32 (1,64-3,29) |
| Enf. vascular periférica | 0,007 | 1,37 (1,07-1,94) |
| Insuf. renal crónica | <0,0001 | 6,78 (4,91-9,38) |
ACV: accidente cerebrovascular; IC del 95%: intervalo de confianza del 95%; OR: odds ratio.
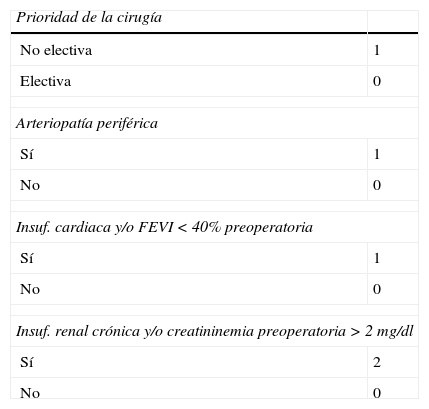
La escala de riesgo fue del resultado neurológico tras CBPC fue desarrollada a partir del modelo de regresión logística. La tabla 4 indica las asignaciones de puntuación específica para cada un de las variables en el cálculo del modelo PACK2.
Cálculo de la puntuación en el modelo PACK2
| Prioridad de la cirugía | |
| No electiva | 1 |
| Electiva | 0 |
| Arteriopatía periférica | |
| Sí | 1 |
| No | 0 |
| Insuf. cardiaca y/o FEVI <40% preoperatoria | |
| Sí | 1 |
| No | 0 |
| Insuf. renal crónica y/o creatininemia preoperatoria >2 mg/dl | |
| Sí | 2 |
| No | 0 |
| Puntuación PACK2total | 0 - 5 |
FEVI: fracción de eyección del ventrículo izquierdo.
En el subgrupo de prueba, la capacidad predictiva para el modelo NNECDSG fue ABC=0,70 (IC del 95%, 0,67-0,74), p<0,0001; test H-L: χ2=8,11, p=0,42. Para PACK2 los resultados fueron ABC=0,77 (IC del 95%, 0,73-0,80), p<0,0001; test H-L: χ2=1,39, p=0,24.
El test estadístico de estrés confirmó buena capacidad predictiva para el modelo PACK2, siendo el ABC>0,8 en el 36%, >0,7 en el 84% y no significativo en el 8% de los subgrupos de 1.000 pacientes seleccionados.
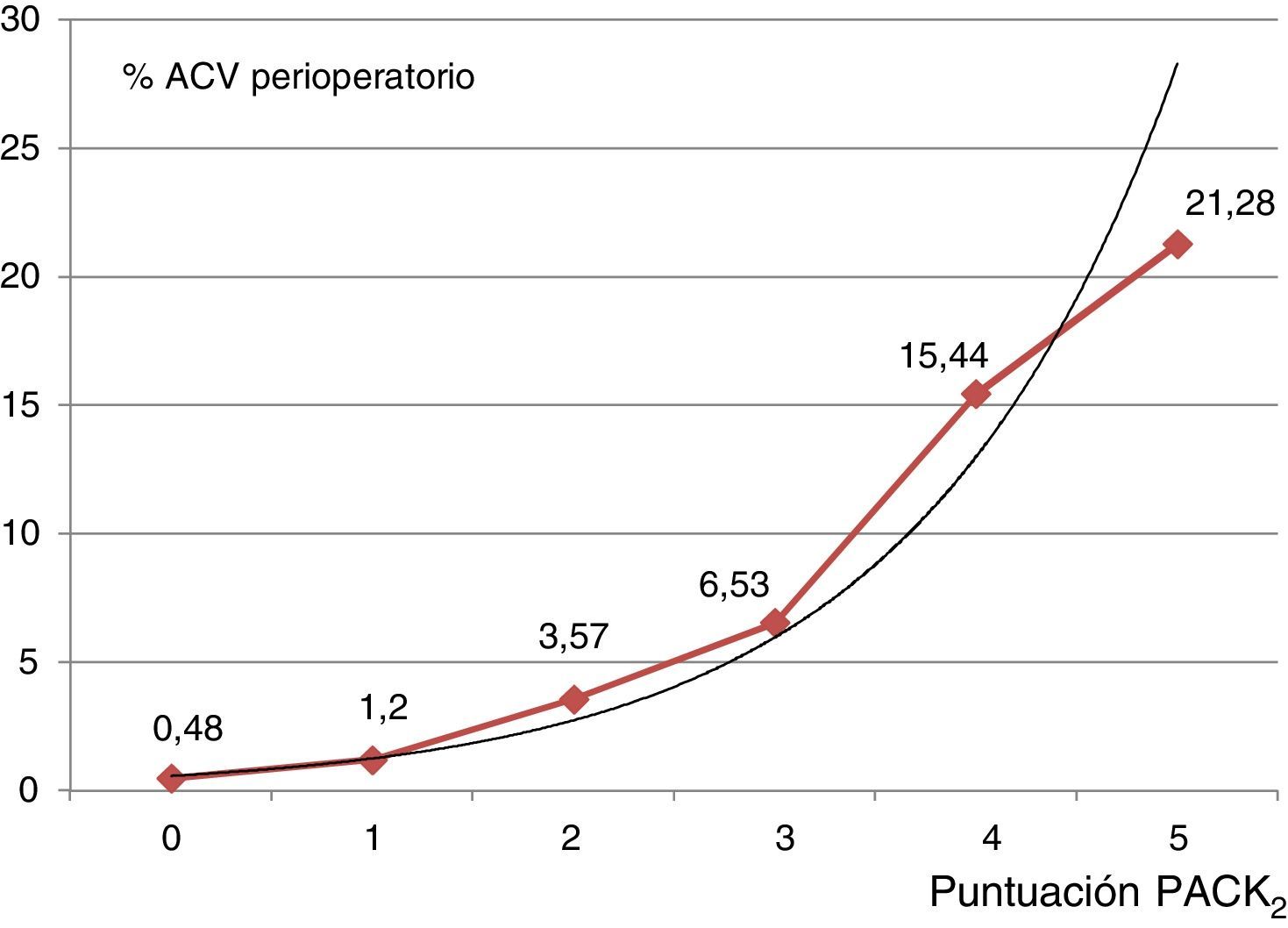
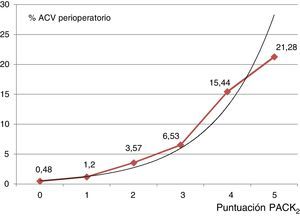
Aplicación clínica del modelo PACK2Es reseñable que el 59,66% de los pacientes fueron clasificados con puntuación 0 puntos (n=15.719), el 25,54% (n=6.728) con 1 punto, 9,99% (n=2.631) con 2 puntos, 3,61% (n=950) con 3 puntos, 1,03% (n=272) con 4 puntos y 0,18% (n=47) con 5 puntos. Las tasas de ACV fueron del 0,48, el 1,20, el 3,57, el 6,53, el 15,44 y el 21,28%, respectivamente, p<0,0001 (fig. 1).
Distribución gráfica del porcentaje de ACV perioperatorio de acuerdo con el rango de puntuaciones del modelo PACK2. La línea representa la tendencia exponencial de una incidencia creciente de la tasa de ACV perioperatorio con el incremento progresivo de la puntuación (y=0,266 e0,78; R2=0,978).ACV: accidente cerebrovascular.
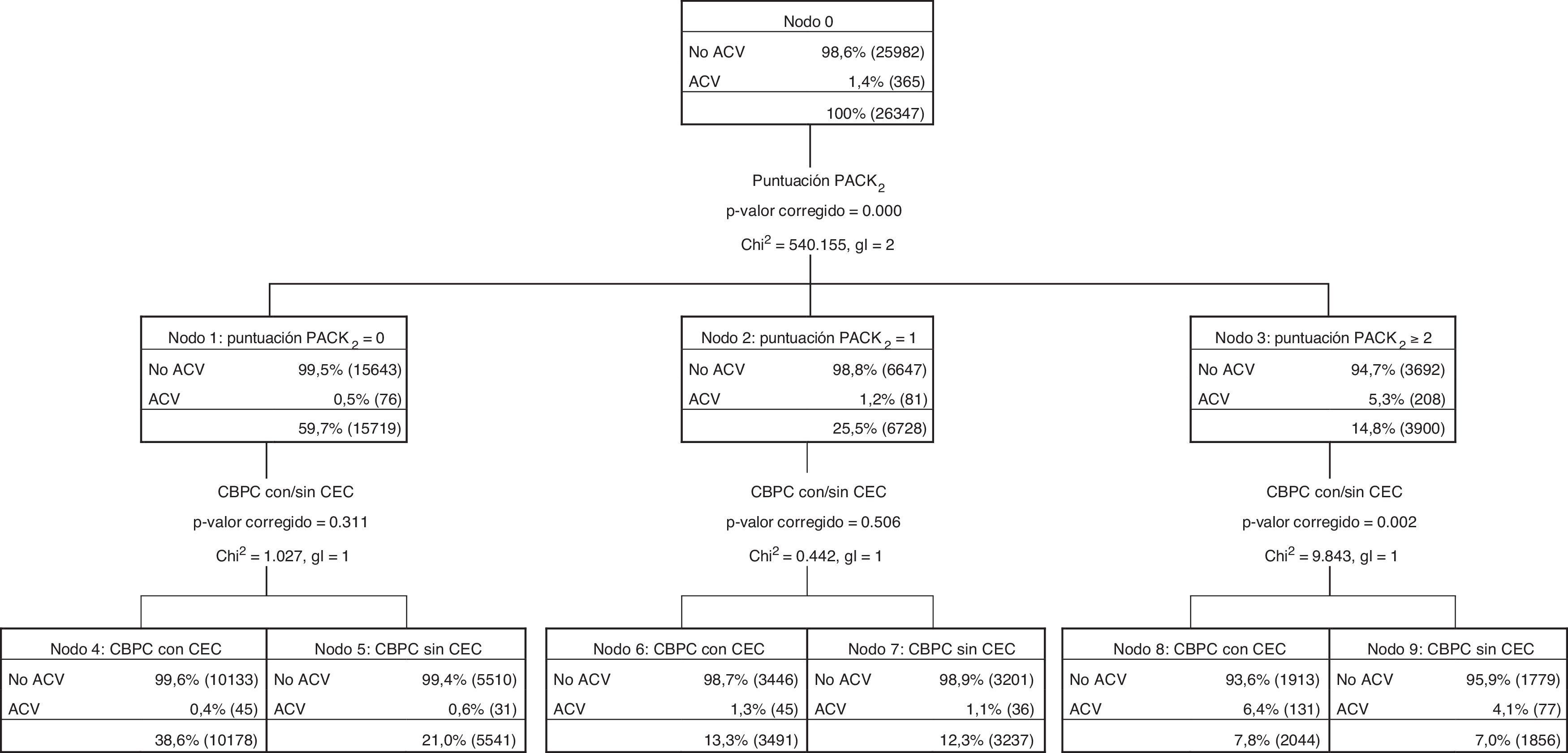
Un árbol de decisión basado en el análisis CHAID (fig. 2) fue obtenido aplicando la puntuación PACK2 para estratificar el riesgo perioperatorio de desarrollar ACV tras CBPC, a fin de determinar el potencial beneficio de llevarla a cabo con o sin CEC. Las puntuaciones 0 y 1 fueron analizadas independientemente, no mostrando diferencias estadísticamente significativas en las tasas de ACV perioperatorio entre los grupos con y sin CEC (0 puntos: 0,6% vs. 0,4%, p=0,311; 1 punto: 1,3% vs. 1,1%; p=0,505). Sin embargo, la CPBC sin CEC redujo significativamente la incidencia de ACV perioperatorio en pacientes con puntuación PACK2 ≥ 2 puntos (4,1% vs. 6,4%, p=0,002).
Árbol de decisión para estratificar el riesgo perioperatorio de desarrollo de ACV en la serie global de CBPC (n=26.347), de acuerdo con la puntuación PACK2 y con la realización del procedimiento con/sin CEC.ACV: accidente cerebrovascular; CBPC: cirugía de bypass coronario; CEC: circulación extracorpórea; gl: grados de libertad.
Este estudio multicéntrico realizado en nuestro medio ha permitido desarrollar una escala de graduación clínica, el modelo PACK2, que permite predecir el riesgo de desarrollar un ACV perioperatorio en el contexto de CBPC aislada. Nuestros resultados sugieren que el modelo PACK2: a) tiene buena precisión y capacidad discriminatoria, con un ABC=0,77 (IC del 95%, 0,74-0,79), p<0,0001, comparable con la de otros modelos específicos como el NNECDSG, y b) constituye un modelo los suficientemente sencillo para tener aplicabilidad práctica directa constando exclusivamente de 4 variables preoperatorias.
Diferentes modelos predictivos de ACV perioperatorio han sido desarrollados y validados con anterioridad2 por lo que, habiendo demostrado adecuadas capacidades predictivas del resultado neurológico postoperatorio, se ha optado por incluir las variables clínicas computadas en los mismos en el desarrollo del estudio realizado. Sin embargo, varios de ellos utilizan complejas/extensas escalas de variables y/o sistemas de puntuación o ecuaciones complejas en la predicción de los resultados neurológicos postoperatorios, lo cual ha conllevado una limitación en su aplicabilidad a la práctica clínica cotidiana. PACK2 contiene solamente 4 variables preoperatorias y, por lo tanto, permite un adecuado balance entre sencillez y capacidad predictiva, dirigido a constituir una herramienta útil en la toma de decisiones sobre el manejo terapéutico más adecuado y la toma de decisiones en pacientes sometidos a CBPC aislada, que podría llevarse a cabo prácticamente momentos antes de proceder al acto quirúrgico.
Por tanto, ¿cómo debe ser utilizado el modelo PACK2? El riesgo de desarrollar ACV perioperatorio en pacientes sometidos a CBPC es una cuestión fundamental que debe ser evitada a toda costa y que, a tal fin, diferentes modelos han sido desarrollados con anterioridad para intentar aportar información preoperatoria7,8. Mientras que la posibilidad de pronosticar dicha grave complicación sería indudablemente importante para estratificar los beneficios y los riesgos de la intervención, cualquier intento de predecir con precisión dicho resultado postoperatorio no conllevaría más que en la incursión en errores sistemáticos al, por ejemplo, no poder ser comparables los medios donde se desarrolló el modelo y donde es aplicado. Por ello, escalas tales como PACK2 deberían solamente ser incorporadas como parte de una planificación del riesgo perioperatorio de la CBPC de cara al adecuado manejo clínico del paciente, pero no como modelos predictivos precisos de los resultados postoperatorios. Nuestro propósito es, por tanto, mostrar su utilidad como herramienta clínica en el establecimiento del riesgo de la intervención de CBPC aislada. En este estudio, los casos con puntuación ≥ 2 puntos mostraron una incidencia reducida de ACV perioperatorio cuando la CBPC fue realizada sin CEC vs. con CEC (p=0,002).
Diversas limitaciones han sido identificadas en la realización del presente trabajo. Primero, los hallazgos obtenidos se ven limitados por su dependencia de un diseño observacional retrospectivo, cuyas conclusiones derivadas limitan su aplicabilidad. Sin embargo, ha tratado de paliarse esta limitación por medio de la inclusión de pacientes de múltiples instituciones de nuestro medio, minimizando así cualquier distorsión debida a diferentes procederes quirúrgicos, anestésicos, relacionados con la perfusión o prácticas médicas específicas llevadas a cabo en los diferentes centros participantes. Segundo, la realización de la CBPC sin CEC no fue establecida en el presente estudio si fue llevada cabo bajo esquemas de «tocar o no tocar» la aorta. Así, los esquemas técnicos que actúan sobre la aorta para la realización de las anastomosis proximales podrían limitar la apreciación del beneficio de la técnica sin CEC sobre la con CEC en términos de incidencia perioperatoria de ACV. Sin embargo, las diferencias estadísticamente significativas encontradas en el subgrupo de pacientes de alto riesgo son suficientes para reforzar la tesis de la potencial capacidad reductora de la incidencia de ACV por la CBPC sin CEC. Tercero, los eventos neurológicos en el perioperatorio fueron evaluados por un neurólogo que llevó a cabo un examen clínico en el perioperatorio inmediato durante el cual tuvieron lugar. Sin embargo, pueden existir significativas variaciones en la práctica clínica y, por ende, en el diagnóstico entre los 21 centros incluidos. Finalmente, la encefalopatía difusa perioperatoria fue excluida como evento neurológico, por lo que potencialmente podrían haber sido infraestimada la incidencia real de pequeños ACV perioperatorios. Sin embargo, otros estudios han comunicado que la encefalopatía difusa perioperatoria podría estar relacionada con factores intraoperatorios como la CEC, pero también en relación con la exposición a la anestesia general durante periodos prolongados6.
ConclusionesSobre base de los datos procedentes de 21 hospitales españoles con 26.347 pacientes incluidos, concluimos que el modelo PACK2 constituye un esquema de estratificación del riesgo perioperatorio de desarrollo de ACV tras CBPC aislada con adecuada capacidad predictiva y útil en la práctica clínica debido a su sencillez. Futuras validaciones tras su aplicación en otros medios/centros serían necesarias antes de que esta escala pudiese ser aplicada como una herramienta útil de cara a planificar el pronóstico de los pacientes o diseñar estrategias terapéuticas que permitiesen prevenir el desarrollo de ACV perioperatorio.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Investigadores e instituciones participantes adscritas al Grupo de Trabajo en Cirugía de las Arritmias y Estimulación Cardiaca de la Sociedad Española de Cirugía Torácica y Cardiovascular (SECTCV): Hospital Vall d’Hebron de Barcelona, Rodríguez R; Hospital Clínic i Provincial de Barcelona, Castellà M; Hospital Clínico Universitario Virgen de la Victoria de Málaga, Porras C; Hospital Germans Trias i Pujol de Badalona, Romero B; Hospital Clínico San Carlos de Madrid, Maroto L; Hospital 12 de Octubre de Madrid, Pérez de la Sota E; Hospital Clínico Universitario de Valladolid, Echevarría M; Hospital Universitario de Salamanca, Dalmau MJ; Hospital Marqués de Valdecilla de Santander, Díez L; Complejo Hospitalario de Toledo, Buendía J; Hospital Son Espases de Palma de Mallorca, Enríquez F; Complejo Asistencial Hospital de León, Castaño M, Martín E; Hospital de La Princesa de Madrid, Reyes G; Hospital de la Santa Creu i Sant Pau de Barcelona, Ginel A; Hospital Universitari i Politècnic La Fe de Valencia, Pérez M; Hospital Universitario Virgen Macarena de Sevilla, García R, Barquero J; Hospital Fundación Jiménez Díaz de Madrid, Heredero A, Jiménez A; Hospital Universitario Puerta de Hierro de Majadahonda, Castedo E; Hospital Xeral de Vigo, Lugo J, Pradas G; Hospital Universitario Puerta del Mar de Cádiz, Gómez M; Hospital General Universitario de Valencia, Hornero F, Mena AV, y análisis estadístico, Martín E, Rieta JJ.