La cirugía de preservación valvular aórtica mediante técnicas como el reimplante valvular (David) y el remodelado de raíz aórtica (Yacoub) se ha consolidado como una alternativa eficaz a la sustitución valvular en pacientes seleccionados. La endocarditis infecciosa tras estas técnicas representa una complicación poco frecuente y con un pronóstico aún no definido. Esta revisión explora la incidencia de endocarditis infecciosa reportada en las principales series publicadas, comparándola con la observada en pacientes portadores de prótesis valvulares aórticas.
Aortic valve preservation techniques such as valve reimplantation (David) and aortic root remodeling (Yacoub) has established itself as an effective alternative to valve replacement in selected patients. Infective endocarditis after these techniques represents a rare complication with an undefined prognosis. This review explores the incidence of infective endocarditis reported in major published series, comparing it with that observed in patients with prosthetic aortic valves.
La preservación de la válvula aórtica en pacientes con insuficiencia valvular o aneurismas de raíz aórtica ha cobrado gran relevancia en la cirugía cardiovascular en las últimas décadas, especialmente en pacientes jóvenes con válvulas morfológicamente normales1,2. Los procedimientos de David y de Yacoub permiten mantener la válvula nativa, disminuyendo los riesgos asociados al uso de las prótesis valvulares. Los beneficios hemodinámicos y la durabilidad de estas técnicas están bien documentados, pero existen aún dudas sobre el impacto en la reducción de la endocarditis infecciosa (EI) en comparación con las prótesis valvulares. El objetivo de esta revisión integradora es analizar en profundidad la incidencia de esta complicación en las principales series publicadas.
Fundamentos técnicos de la preservación valvular aórticaEl procedimiento de David consiste en la reimplantación de los velos valvulares dentro de un tubo de Dacron® (DuPont, Delaware, EE. UU.) estabilizando el anillo aórtico y garantizando una coaptación efectiva3,4. El procedimiento de Yacoub, por otro lado, implica la reconstrucción de los senos de Valsalva, logrando una fisiología más natural pero con mayor riesgo de dilatación futura del anillo5, por lo que actualmente a esta técnica se asocia casi siempre una anuloplastia aórtica6–8. Ambos procedimientos han mostrado excelentes resultados a largo plazo en series con seguimientos de más de 10 años3,9–12. El preservar la válvula nativa y eliminar el material protésico supuestamente disminuye el riesgo de colonización bacteriana y la probabilidad de sufrir una EI.
Incidencia de EI en técnicas de preservación valvular aórticaLos reportes de EI en pacientes en los que se han realizado técnicas de preservación valvular se limitan a los resultados de las principales series, donde la incidencia acumulada de EI es baja. A continuación, describiremos dichos resultados, que presentamos resumidos en la tabla 1.
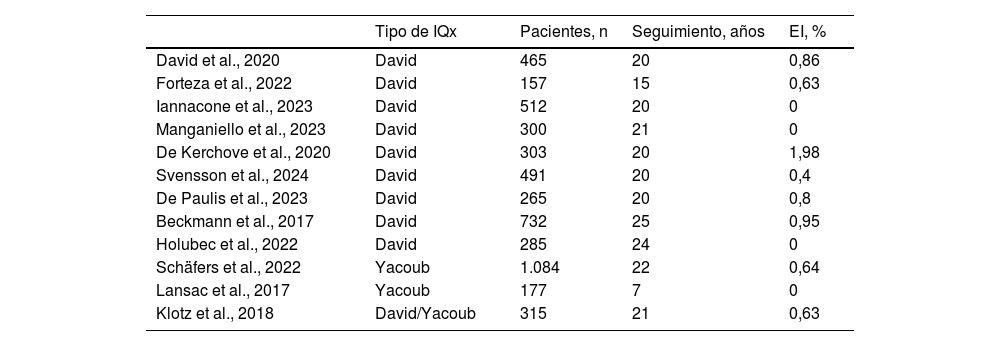
Resumen de estudios en técnicas de preservación valvular aórtica
| Tipo de IQx | Pacientes, n | Seguimiento, años | EI, % | |
|---|---|---|---|---|
| David et al., 2020 | David | 465 | 20 | 0,86 |
| Forteza et al., 2022 | David | 157 | 15 | 0,63 |
| Iannacone et al., 2023 | David | 512 | 20 | 0 |
| Manganiello et al., 2023 | David | 300 | 21 | 0 |
| De Kerchove et al., 2020 | David | 303 | 20 | 1,98 |
| Svensson et al., 2024 | David | 491 | 20 | 0,4 |
| De Paulis et al., 2023 | David | 265 | 20 | 0,8 |
| Beckmann et al., 2017 | David | 732 | 25 | 0,95 |
| Holubec et al., 2022 | David | 285 | 24 | 0 |
| Schäfers et al., 2022 | Yacoub | 1.084 | 22 | 0,64 |
| Lansac et al., 2017 | Yacoub | 177 | 7 | 0 |
| Klotz et al., 2018 | David/Yacoub | 315 | 21 | 0,63 |
EI: endocarditis infecciosa; IQx: intervención quirúrgica se encuentran en la bibliografía.
David et al.4,9,13,14 presentan 4 casos de EI en una cohorte de 465 pacientes tras un seguimiento de 20 años, resultando un riesgo acumulado del 0,86%. En 3 pacientes se evidenció un absceso en el tracto de salida del ventrículo izquierdo, y en el cuarto, la infección se produjo en el injerto de Dacron®. La libertad de reoperación a 20 años fue del 93%, y en el subgrupo de pacientes que requirió una reintervención, la causa más frecuente fue por insuficiencia aórtica (84%), seguida de EI (16%). Cabe resaltar que los casos de EI se produjeron a partir de los 10 años de seguimiento, demostrando que se trata de una complicación de aparición muy tardía. Al tener una incidencia tan baja, no hacen un análisis de factores microbiológicos o predisponentes para desarrollar EI.
Tamer et al.15 reportan 6 casos de EI en una cohorte de 303 pacientes a los que se les realizó un reimplante valvular aórtico, tras un seguimiento de 20 años. Calculan un riesgo acumulado de EI del 1,98% y una tasa de incidencia de 0,32% pacientes-año. Cinco de estos pacientes requirieron una sustitución valvular y en uno fue suficiente el tratamiento antibiótico.
La experiencia de la Cleveland Clinic la presentan Svensson et al.16 con una serie de 491 pacientes intervenidos con la técnica de reimplante valvular. Tras un seguimiento de 20 años, describen 2 pacientes con EI, lo que supone un riesgo acumulado del 0,41%. En ambos se remplazó la válvula aórtica.
El grupo de Martens et al., con una experiencia de 25 años en técnicas de reimplante valvular y una serie de 732 pacientes, describen 7 casos de EI con un riesgo acumulado del 0,95%. En todos los pacientes hubo que remplazar la válvula aórtica17.
El estudio de Forteza et al. en Madrid analiza una cohorte de 157 pacientes con síndrome de Marfan en los que se realizó un reimplante valvular aórtico. Hubo un paciente con EI (mediana de seguimiento de 7 años), lo que supone un riesgo acumulado del 0,63% y una incidencia anual de 0,09 pacientes-año3,18. En el grupo de Manganiello et al., con una serie de 300 intervenciones de David y un seguimiento medio de 7 años, no reportaron ningún caso de EI11.
Chirichilli et al. describen su serie de reimplante valvular aórtico en 265 pacientes, con 20 años de seguimiento. Reportan un riesgo acumulado de EI del 0,8%, detallando los tiempos de presentación, que fueron a los 6 y 10 meses desde la intervención, respectivamente. En su serie calculan una libertad de EI del 99,2±0,5% a 5, 10 y 15 años19.
Con respecto a la técnica del remodelado, las series más representativas son las descritas por el grupo de Giebels y el grupo de Lansac. Giebels et al. presentan su experiencia en 1.084 pacientes intervenidos mediante la técnica de remodelado con un seguimiento de 22 años. Hubo 7 casos de EI que requirieron reintervención sobre la válvula aórtica, lo cual supone un riesgo acumulado del 0,64%20. Lansac et al., con 177 casos de remodelado de la raíz aórtica asociado a técnicas de anuloplastia externa rígida, no describen ningún caso de EI, con un seguimiento de 7 años8.
Finalmente, Klotz et al. reportan 315 pacientes, en los cuales se realizó una intervención de David a 214 y remodelado a 101, con un seguimiento de 21 años21. Describen un caso de EI en cada grupo (riesgo acumulado de 0,46 y 0,99%, respectivamente).
La mayoría de los casos de EI descritos en estas series ocurren tardíamente y se relacionan más con bacteriemias que con aspectos quirúrgicos. En general, las tasas anuales de EI tras técnicas de preservación valvular oscilan entre el 0,15 y el 0,25% por año, datos notablemente inferiores a los observados en los pacientes portadores de prótesis valvulares1,22.
Comparación con la incidencia de EI en prótesis valvulares aórticasEs bien conocido que una de las limitaciones de las prótesis valvulares son las complicaciones a largo plazo relacionadas con el implante. De Meester et al. demostraron una incidencia de complicaciones protésicas (trombosis, sangrado, EI y/o deterioro estructural valvular) del 2-7% por año23, y en el estudio clásico de Hammermeister et al. se describe un riesgo acumulado de complicaciones relacionadas con las prótesis valvulares a 10 años del 50%24. Cabe resaltar que en los registros español y europeo de EI (GAMES y EURO-ENDO), las prótesis valvulares representaron más del 30% de los casos de EI25,26.
Según algunos autores, las tasas anuales de EI reportadas tras el implante de prótesis biológicas y mecánicas son del 0,61 y 0,45%, respectivamente27,28. Comparativamente, las técnicas de preservación muestran tasas acumuladas<2% a 10 años, lo que las posiciona favorablemente en cuanto a riesgo de EI, especialmente en pacientes jóvenes. En la base de datos AVIATOR se realizó un propensity score comparando la preservación valvular aórtica según la técnica de David con la intervención de Bentall-De Bono. Tras esto pudieron extrapolar una incidencia compuesta de EI, tromboembolia y sangrado de 0,39% pacientes-año en el grupo de preservación valvular, comparado con 1,80% pacientes-año tras la cirugía de sustitución de raíz y válvula aórtica (p=0,02)29. A su vez, en el metaanálisis de Wu et al., que compara los resultados de la intervención de David versus la intervención de Bentall-De Bono tras una disección aórtica, reportaron una tasa acumulada de EI de 0,0% pacientes-año (IC 95% 0,0-0,3%, I2=0%) versus 0,2% pacientes-año (IC 95% 0,0-0,5%, I2=0%) en el grupo en el que se realizó la intervención de Bentall-De Bono30.
Sin embargo, aún hay controversia sobre la incidencia de EI con ambas estrategias. En estudios como el de Ouzounian et al., la incidencia de EI fue inferior tras técnicas de reimplante valvular (0,8%) en comparación con el implante de prótesis biológicas (2,8%) o mecánicas (2,2%)31. Por el contrario, Leontyev et al., al comparar estas 2 mismas técnicas, obtuvieron una incidencia similar de EI (4 casos tras la intervención de David y 6 tras la intervención de Bentall-De Bono; p=0,53)32. De forma similar, el grupo de Price et al. comparó la intervención de David versus Bentall-De Bono en 150 pacientes con síndrome de Marfan, y tampoco obtuvo diferencias en la incidencia de EI (2,98% EI en Bentall-De Bono versus 1,02% EI en David)33.
Manejo terapéuticoEl tratamiento médico incluye antibióticos dirigidos por antibiograma durante al menos 6 semanas, sin diferencias con respecto al manejo de otras EI, y las indicaciones quirúrgicas también son similares a las de las válvulas nativas o protésicas, siguiendo las recomendaciones actuales34.
Como principio quirúrgico y al igual que en otras EI, la reintervención quirúrgica debe tener como objetivo la eliminación completa de todos los tejidos afectados por la infección. En la literatura, las técnicas descritas son variables, aunque lo más habitual es el remplazo de la válvula aórtica nativa por una prótesis biológica o mecánica. Esto supone una ventaja sobre las EI que afectan a prótesis valvulares, donde las bacterias con relativa frecuencia originan importantes abscesos que obligan a realizar cirugías muy complejas. Realmente, a pesar de ser una reintervención, la técnica quirúrgica se aproxima a una primera intervención por una EI sobre una válvula nativa. En los casos en los que la afectación se extiende al tracto de salida del ventrículo izquierdo, es obligado realizar un remplazo completo de la raíz de la aorta con un tubo valvulado. La afectación aislada del tubo protésico es muy poco frecuente tras el reimplante o remodelado, con solo un caso descrito en la literatura13. En estos casos, los homoinjertos podrían ser de utilidad para el manejo de estas infecciones complejas.
Resultados postoperatorios y pronósticoDebido al número reducido de series amplias y a la baja frecuencia de esta complicación, no disponemos de datos objetivos para determinar resultados de morbimortalidad tras la EI en pacientes en los que se realizan técnicas de preservación valvular aórtica. Sin embargo, es interesante destacar que en la mayoría de las series presentadas en este artículo, el tratamiento quirúrgico se limitó al remplazo de la válvula nativa por una prótesis, con un resultado favorable.
ConclusionesLa EI tras técnicas de preservación valvular aórtica es una complicación poco frecuente y con un pronóstico favorable, ya que habitualmente solo afecta la válvula nativa. A falta de importantes estudios comparativos, su incidencia en las principales series es menor que la observada en pacientes con prótesis valvulares.
La cirugía de preservación continúa siendo una opción valiosa, particularmente en pacientes jóvenes, no solo por su durabilidad hemodinámica, sino también por su bajo riesgo de infección.
Fuente de financiaciónNinguna.
Consideraciones éticasSe renunció al consentimiento informado debido a que el manuscrito es una revisión integradora de la literatura. No requiere aprobación del Comité de Ética ya que es una revisión de la literatura.
Conflicto de interesesNinguno.