La hiperlipidemia familiar combinada (HFC) es un trastorno muy frecuente asociado a enfermedad coronaria prematura. Se transmite de forma autosómica dominante, aunque no existe un gen único asociado al trastorno. El diagnóstico se realiza mediante criterios clínicos, y son importantes la variabilidad del fenotipo lipídico y la historia familiar de hiperlipidemia.
Es frecuente la asociación con diabetes mellitus tipo2, hipertensión arterial y obesidad central. Los pacientes con HFC se consideran de riesgo cardiovascular alto y el objetivo terapéutico es un colesterol-LDL <100mg/dl, y <70mg/dl en presencia de enfermedad cardiovascular establecida o diabetes mellitus. Los pacientes con HFC requieren tratamiento con estatinas potentes y, a veces, tratamiento combinado. La identificación y el manejo de otros factores de riesgo cardiovascular, como la diabetes y la hipertensión, son fundamentales para reducir la carga de enfermedad cardiovascular. Este documento proporciona recomendaciones para el diagnóstico y el tratamiento integral de los pacientes con HFC especialmente dirigidas a médicos de atención primaria.
Familial combined hyperlipidemia (FCH) is a frequent disorder associated with premature coronary artery disease. It is transmitted in an autosomal dominant manner, although there is not a unique gene involved. The diagnosis is performed using clinical criteria, and variability in lipid phenotype and family history of hyperlipidemia are necessaries.
Frequently, the disorder is associated with type2 diabetes mellitus, arterial hypertension and central obesity. Patients with FCH are considered as high cardiovascular risk and the lipid target is an LDL-cholesterol <100mg/dL, and <70mg/dL if cardiovascular disease or type 2 diabetes are present. Patients with FCH require lipid lowering treatment using potent statins and sometimes, combined lipid-lowering treatment. Identification and management of other cardiovascular risk factors as type 2 diabetes and hypertension are fundamental to reduce cardiovascular disease burden. This document gives recommendations for the diagnosis and global treatment of patients with FCH directed to specialists and general practitioners.
La hiperlipidemia familiar combinada (HFC) es el trastorno heredado más frecuente del metabolismo lipídico asociado con hiperlipidemia mixta y enfermedad cardiovascular (ECV) prematura. Fue descrita por Goldstein en 1973 al estudiar familias de supervivientes de infarto de miocardio (IM)1. Aunque se puede presentar en los niños, habitualmente se expresa a partir de la segunda década de la vida con hipercolesterolemia y/o hipertrigliceridemia, con una gran variación fenotípica intraindividual e interindividual, como respuesta a la interacción entre factores genéticos y ambientales como la alimentación, el aumento del peso corporal, el consumo de alcohol y el tiempo de evolución2,3.
Se estima una prevalencia del 1-2% de la población general1, lo que significa que entre 500.000 y 900.000 personas en España pueden presentar este trastorno. La prevalencia de la HFC es hasta el 20% en los supervivientes de un IM menores de 60años y alcanza el 38% en los que sobreviven a un IM antes de los 40años4,5. Frecuentemente se asocia con numerosas anormalidades metabólicas, como hipertensión arterial (HTA), resistencia a la insulina, diabetes mellitus (DM) tipo2, obesidad central, esteatosis hepática y síndrome metabólico6,7.
La HFC constituye un reto para el manejo integral del riesgo cardiovascular debido a su elevada prevalencia y a su asociación con numerosos factores de riesgo cardiovascular (FRCV). Dada su posición en el sistema sanitario, el médico de atención primaria debe desempeñar un papel fundamental en la detección y el manejo global de los pacientes con HFC, así como en sus familiares.
Con el fin de mejorar el diagnóstico y el manejo de esta población, se ha elaborado este Documento de Consenso, cuyo objetivo es revisar la información actualmente disponible acerca del diagnóstico y tratamiento de la HFC, y consensuar con un grupo de expertos recomendaciones que ayuden a los médicos de diversas especialidades y ámbitos de atención a realizar un adecuado diagnóstico y tratamiento con el fin de prevenir el desarrollo de la ECV prematura.
MetodologíaLa Fundación Hipercolesterolemia Familiar promovió la creación de un panel de expertos formado por 4 especialistas en Medicina Familiar y Comunitaria y 8 especialistas en Endocrinología, Medicina Interna y Cardiología, de los que 4 trabajan en Unidades de Lípidos. El panel realizó una revisión exhaustiva en Medline, PubMed y Cochrane sobre el manejo diagnóstico y terapéutico de la HFC. Se realizaron 3 reuniones de trabajo presenciales y una videoconferencia durante el segundo semestre de 2013. Después de la revisión, se discutieron y consensuaron las recomendaciones basadas en la mejor evidencia disponible, en la opinión de expertos y en la buena práctica clínica.
Para la elaboración de este Documento de Consenso se siguieron las recomendaciones AGREE (Appraisal of Guidelines Research & Evaluation)8. Se empleó la metodología GRADE (Grading of Recommendations Assessment, Development, and Evaluation) en la formulación de mensajes clave calificados con clase o fuerza de la recomendación (CdR), nivel de calidad de la evidencia (NdE), y la categorización GRADE (fuerte, moderada y débil) de la recomendación9.
EtiopatogeniaLa HFC es un trastorno hereditario autosómico dominante con elevada penetrancia y afecta aproximadamente al 50% de la descendencia. Es una enfermedad oligogénica en la que subyacen bases genéticas heterogéneas que se asocian de forma diversa entre las familias con HFC10. Distintas regiones cromosómicas se han asociado a la HFC. Entre ellas, la región 11q-23-24, que codifica las Apo AI-CIII-AIV, se ha asociado a hipertrigliceridemia, la región 1q21-23 se asocia con DM tipo2. También, el gen USF1 (Upstream Stimulatory Factor 1) desempeña una función clave en la regulación de los procesos que están alterados como dislipidemia o la resistencia a la insulina. Como consecuencia de estas alteraciones genéticas, los pacientes con HFC tienen una captación reducida de los ácidos grasos libres (AGL) procedente de la lipólisis de los triglicéridos (TG) en el tejido adiposo. Esto ocasiona un mayor flujo de AGL hacia el hígado, lo que facilita la sobreproducción hepática de apolipoproteína B (apoB) y la síntesis de TG en forma de lipoproteínas de muy baja densidad (VLDL). Por otra parte, las lipoproteínas ricas en triglicéridos de origen intestinal y hepático permanecen más tiempo en plasma3. Además, hay un predominio de partículas LDL pequeñas y densas, pobres en colesterol y con una tasa elevada de apo B/colesterol, conocidas como LDL aterógenas.
Diagnóstico clínicoDebido a su heterogeneidad, complejidad y falta de defectos genéticos específicos, clínicos o bioquímicos que la definan, no hay unanimidad en los criterios diagnósticos. Para establecer el diagnóstico es necesario el estudio de los antecedentes familiares tanto lipídicos como cardiovasculares, así como la exclusión de otras causas de hiperlipidemias secundarias3. Los pacientes con HFC suelen presentar hipercolesterolemia y/o hipertrigliceridemia moderada, con variabilidad en la expresión lipídica tanto en el propio individuo como en sus familiares de primer grado y ECV prematura en la familia3,11,12. Una característica es que los niveles de colesterol y TG son muy variables en el tiempo. También suelen estar elevados los niveles de apoB (>120mg/dl) y con frecuencia existe un colesterol transportado en las lipoproteínas de alta densidad (c-HDL) inferior a 40mg/dl3,12,13. En la HFC no se observan xantomas tendinosos, aunque pueden presentar arco corneal y xantelasmas.
Si bien algunos estudios han demostrado el valor de la apoB en el diagnóstico y como predictor de riesgo cardiovascular en esta población13, la determinación de esta apolipoproteína no es homogénea ni está estandarizada en los distintos laboratorios, y habitualmente no está disponible su determinación en la atención primaria, por lo que este panel considera que su medición no es útil en la práctica clínica habitual.
El antecedente de ECV prematura en los familiares ha sido utilizado como un factor adicional a los criterios lipídicos por algunos autores7,13; sin embargo, no se considera un criterio estricto para el diagnóstico3.
Los criterios clínicos diagnósticos utilizados actualmente son los propuestos por la Red Temática de Investigación Cardiovascular en Hiperlipidemias Genéticas (Instituto de Salud CarlosIII) en 2003, y que están de acuerdo con otros utilizados a nivel internacional (tabla 1).
Criterios diagnósticos de la hiperlipidemia familiar combinada
| 1. Persona afectada |
| • En adultos: colesterol total >240mg/dl (o c-LDL >160mg/dl) y/o triglicéridos >200mg/dl |
| • En menores de 20 años: colesterol total >200mg/dl (o c-LDL >130mg/dl) y/o triglicéridos >120mg/dl |
| • Descartar causas secundarias: índice de masa corporal >35kg/m2, HbA1c >10%, hipotiroidismo no controlado y/o etilismo (>40g alcohol/día) |
| 2. Familia afectada |
| • Dos o más miembros de primer grado (padres, hermanos, hijos) afectados de hiperlipidemia mixta, o de combinaciones de fenotipos, entre hipercolesterolemia pura (IIa), hiperlipidemia mixta (IIb) o hipertrigliceridemia (IV) |
| • Se excluyen familias con xantomas tendinosos y/o cifras de c-LDL >300mg/dl en 2 o más familiares de primer grado con fenotipo IIa |
| • Historia familiar de enfermedad cardiovascular ateroesclerótica prematura (<60años)a |
Adaptado de Red temática en hiperlipidemias genéticas G03/108 del ISCIII.
La HFC frecuentemente se solapa con el síndrome metabólico (SM), que coexiste hasta en el 65% de los pacientes con HFC. Los pacientes con HFC comparten características clínicas y metabólicas similares a las del SM; sin embargo, la HFC se distingue del SM por su carácter fundamentalmente hereditario, niveles de apoB y c-LDL elevados, la variabilidad en el fenotipo, y ser una entidad más grave con mayor carga de enfermedad ateroesclerótica prematura. Además, el SM es más dependiente de la alimentación y del sobrepeso3.
Riesgo cardiovascular y objetivos de control lipídicoDebido a su carácter genético y a su elevada aterogenicidad, la estratificación del riesgo cardiovascular (RCV) mediante las tablas de Framingham o el SCORE puede estar infraestimado en estos pacientes. Las guías europeas para el manejo de las dislipidemias14 y de prevención de la ECV15 clasifican a los pacientes con hiperlipidemias familiares de RCV alto, por lo que el objetivo de control lipídico es un c-LDL <100mg/dl (CdR I, NdE A, GRADE fuerte). El RCV es muy alto cuando los pacientes con HFC tienen además ECV documentada, enfermedad renal crónica moderada o grave, DM, o lesión de órgano diana (CdR I, NdE A, GRADE fuerte). En estas situaciones el objetivo de control lipídico es un c-LDL <70mg/dl, o una reducción >50% de los niveles iniciales, cuando no se pueda alcanzar este objetivo.
En situaciones de hipertrigliceridemia >400mg/dl, la determinación del c-LDL mediante la fórmula de Friedewald no es precisa, por lo que se usa como objetivo subrogado (CdR II, NdE B, GRADE fuerte) el colesterol no-HDL (colesterol total menos c-HDL). El nivel objetivo de colesterol no-HDL se calcula añadiendo 30mg/dl al nivel objetivo previsto de c-LDL.
Si la determinación de apoB está disponible (CdR II, NdE C, GRADE moderado), en los pacientes con RCV alto y muy alto se podrían fijar como objetivo secundario unos niveles <100mg/dl y <80mg/dl, respectivamente.
Tratamiento hipolipemiante en adultosLas modificaciones en el estilo de vida de los pacientes con HFC constituyen una medida fundamental para la mejora del perfil lipídico y la reducción del riesgo CV14-16. Esta reducción se puede conseguir mediante el abandono del tabaco, el mantenimiento de un peso corporal adecuado, la práctica regular de ejercicio y la adopción de una dieta saludable tipo mediterránea (CdR I, NdE A, GRADE fuerte).
Debido a su alto riesgo cardiovascular, el tratamiento farmacológico hipolipemiante debe comenzarse en el momento del diagnóstico13,14 si no se han conseguido los objetivos terapéuticos (CdR I, NdE A, GRADE fuerte). Se deben evaluar otras causas secundarias de hiperlipidemia que pueden coexistir, como hipotiroidismo, diabetes, enfermedad renal crónica, gestación, ingesta de alcohol o grasas saturadas, o la administración de fármacos como estrógenos, glucocorticoides, diuréticos, bloqueadores beta y ácido retinoico.
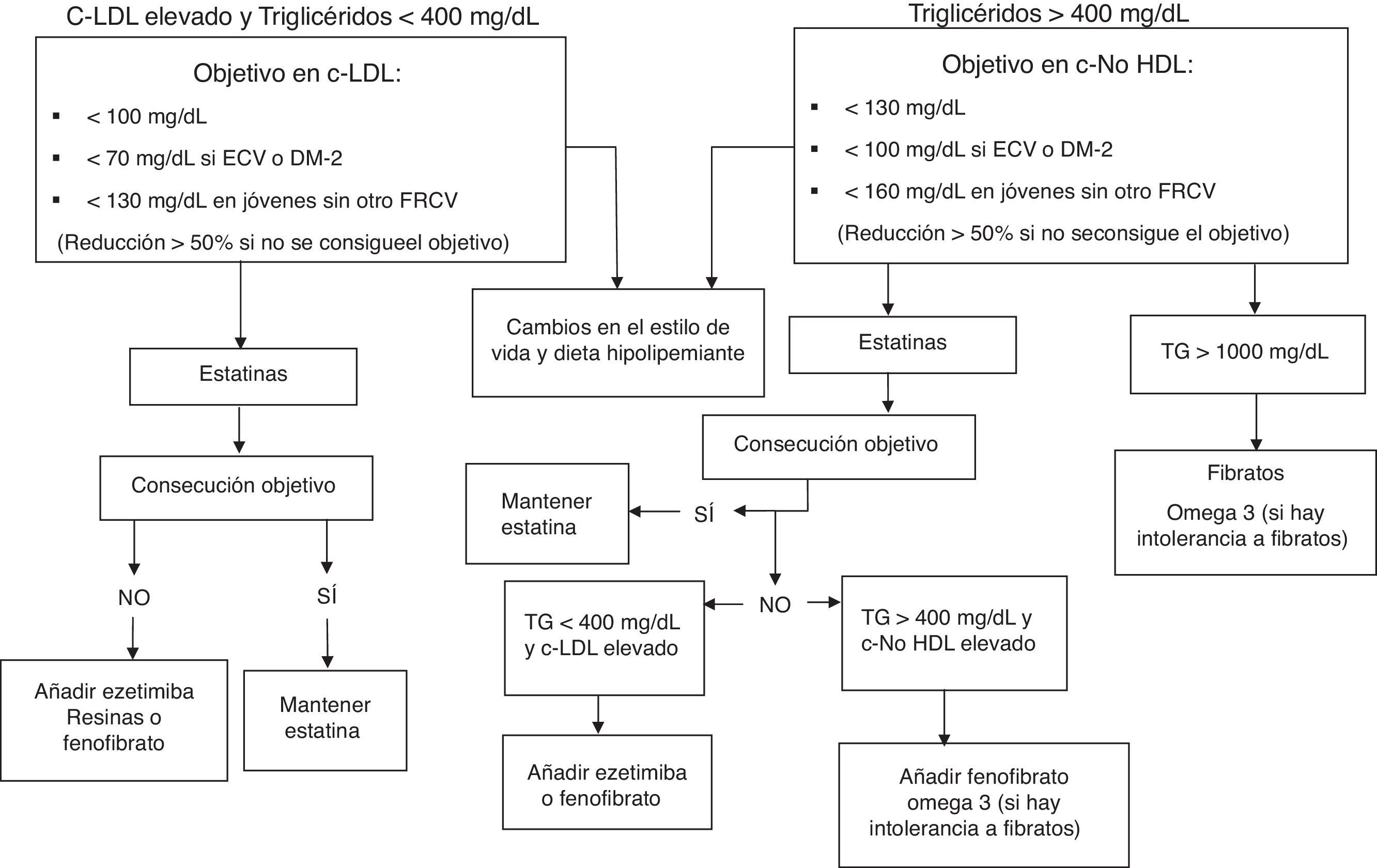
En los pacientes con HFC, el manejo terapéutico con fármacos hipolipemiantes varía según sea el RCV alto o muy alto, y según se asocie o no con hipertrigliceridemia (fig. 1). Se deben medir los niveles de transaminasas y de creatincinasa (CK) antes de iniciar el tratamiento con estatinas. Posteriormente es recomendable realizar un control analítico a las 8-12 semanas con el fin de valorar la eficacia, la tolerancia y la seguridad del tratamiento. Durante el tratamiento con estatinas es razonable medir la función hepática si se presentan síntomas que sugieran hepatotoxicidad o bien al aumentar la dosis de estatina, cambiar de estatina o al combinar tratamientos. De igual manera, hay que determinar la CK si se presentan síntomas musculares.
Algoritmo terapéutico en adultos con HFC.
c-LDL: colesterol transportado por las lipoproteínas de baja densidad; c-no HDL: colesterol transportado por lipoproteínas distintas a las lipoproteínas de alta densidad; DM2: diabetes mellitus tipo2; ECV: enfermedad cardiovascular; FRCV: factores de riesgo cardiovascular; TG: triglicéridos.
Constituyen el tratamiento de elección en la HFC, por haber demostrado14,15,17 una disminución de la morbimortalidad cardiovascular en sujetos con distinto riesgo cardiovascular (CdR I, NdE A, GRADE fuerte). La mayoría de los pacientes con HFC requieren estatinas potentes para alcanzar reducciones ≥50% de c-LDL. Si esto no se consigue, se puede valorar la combinación de estatinas con un inhibidor de la absorción del colesterol, como ezetimiba, o con resinas secuestradoras de ácidos biliares (CdR II, NdE C, GRADE moderado).
FibratosLos fibratos (gemfibrozilo, bezafibrato y fenofibrato) producen reducciones significativas de TG (del 20-50%) y de lipoproteínas ricas en TG. Su efecto sobre el c-LDL es discreto (reducción hasta un 10%) y pueden aumentar el c-HDL hasta un 20%. Algunos pacientes con HFC pueden tener niveles de triglicéridos >500mg/dl que es preciso tratar (CdR I, NdE B, GRADE fuerte) para disminuir el riesgo de pancreatitis. En el caso de requerir tratamiento combinado, el gemfibrozilo está contraindicado por el mayor riesgo de aparición de miopatía severa. El fenofibrato es una buena opción al no compartir las vías metabólicas del gemfibrozilo14.
EzetimibaInhibe la absorción intestinal del colesterol. Al añadir ezetimiba, se produce una reducción adicional del 15-20% en el c-LDL sobre el obtenido en monoterapia con estatinas, y también una ligera reducción de los TG18. La ezetimiba puede administrarse en monoterapia en pacientes intolerantes a las estatinas, o en combinación con estas si no se alcanzan los niveles objetivo14(CdR II, NdE C, GRADE moderado). Aunque no está la indicación aprobada, se ha demostrado la eficacia del tratamiento combinado de ezetimiba con fenofibrato en pacientes con hiperlipidemia mixta19.
Resinas secuestradoras de ácidos biliaresLas resinas ejercen su mecanismo de acción a nivel intestinal ligando a los ácidos biliares, principal fuente de colesterol intestinal. Las resinas producen una reducción adicional del c-LDL del 15-20%. En caso de intolerancia a las estatinas puede considerarse el uso de resinas14(CdR II, NdE B, GRADE fuerte), aunque en general son poco toleradas ya que pueden producir flatulencia, dispepsia y estreñimiento. Elevan ligeramente los TG, por lo que son de menor utilidad en los pacientes con HFC e hipertrigliceridemia. Recientemente se ha comercializado el colesevelam, que se tolera mejor.
Ácidos grasos ω-3Los ácidos eicosapentaenoico (EPA) y docosahexanoico (DHA), a dosis >2g/día, reducen los niveles de TG hasta un 25%; sin embargo, la evidencia disponible sobre su beneficio en prevención cardiovascular no ha sido concluyente. En pacientes con hipertrigliceridemia se pueden considerar ácidos grasos ω-3 (CdR II, NdE B, GRADE débil), en combinación con fármacos hipolipemiantes, o solos si no toleran los fibratos.
Tratamiento de los trastornos del metabolismo de los hidratos de carbonoLos pacientes con HFC tienen mayor mortalidad y 3 veces más episodios cardiovasculares cuando presentan DM. La prevalencia de HFC en pacientes con DM es del 12%, y es conocido que la HTA, la hiperlipidemia y la obesidad coexisten frecuentemente con la DM tipo220,21.
Desde el momento del diagnóstico de HFC, se recomienda detectar de forma activa las alteraciones en el metabolismo glucídico, mediante el cribado anual de DM. Una vez realizado el diagnóstico de DM, es razonable monitorizar el seguimiento cada 3-6meses y evaluar la presencia de macro y microangiopatía22.
El manejo terapéutico de la DM incluye el control de todos los FRCV. Debe ser proactivo, evitando la inercia terapéutica y combinando fármacos antes de alcanzar la dosis máxima en monoterapia, para evitar mayores efectos adversos22. El objetivo de control glucémico debe ser un nivel de HbA1c <7% (CdR I, NdE A, GRADE fuerte), siendo más estricto (<6,5%) en la población joven y sin complicaciones vasculares, y menos estricto (<8%) en pacientes ancianos, diabéticos de larga evolución con comorbilidad, complicaciones microvasculares o ECV establecida o con frecuentes hipoglucemias22,23. Un control demasiado estricto de la glucemia puede conllevar un aumento de mortalidad sin un claro beneficio sobre las complicaciones macroangiopáticas24.
Se recomienda el inicio precoz de metformina (CdR II, NdE B, GRADE fuerte) junto con las modificaciones del estilo de vida, como una dieta saludable y la actividad física regular. El estudio PREDIMED demostró que la dieta mediterránea tiene beneficios en la prevención primaria de episodios cardiovasculares y en la reducción de progresión a diabetes25. La metformina es el único hipoglucemiante que ha demostrado reducción de la morbimortalidad cardiovascular y de la mortalidad total26. Se debe reducir la dosis al 50% si el filtrado glomerular estimado es <45ml/min/1,73m2, y está contraindicada si es <30ml/min/1,73m2.
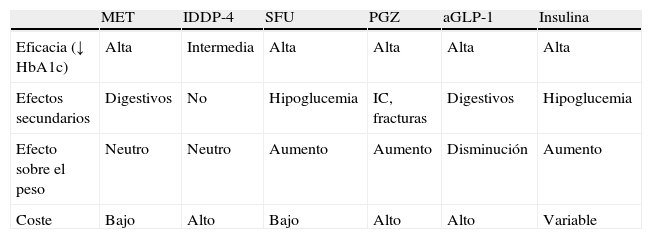
Cuando la metformina es insuficiente para un control glucémico adecuado, es preciso añadir un segundo fármaco27. Además de la insulina, los hipoglucemiantes más utilizados son los secretagogos (sulfonilureas y glinidas), los inhibidores de la dipeptidil-peptidasa-4 (IDPP-4), los análogos de GLP-1 (glucagon-like-peptide-1) y la pioglitazona. Las características principales de cada uno de ellos se muestran en la tabla 2.
Características de los fármacos en el tratamiento de la diabetes tipo 2
| MET | IDDP-4 | SFU | PGZ | aGLP-1 | Insulina | |
| Eficacia (↓ HbA1c) | Alta | Intermedia | Alta | Alta | Alta | Alta |
| Efectos secundarios | Digestivos | No | Hipoglucemia | IC, fracturas | Digestivos | Hipoglucemia |
| Efecto sobre el peso | Neutro | Neutro | Aumento | Aumento | Disminución | Aumento |
| Coste | Bajo | Alto | Bajo | Alto | Alto | Variable |
aGLP-1: agonistas receptor péptido similar al glucagón tipo 1; IC: insuficiencia cardiaca; IDPP-4: inhibidores de la dipeptidilpeptidasa-4; MET: metformina; PGZ: pioglitazona; SFU: sulfonilureas.
La elección del segundo fármaco se debe individualizar atendiendo a las características del paciente y a la comorbilidad. Para ello hay que evaluar no solo la eficacia del hipoglucemiante en el descenso de la HbA1c, sino también el riesgo de hipoglucemia, el efecto sobre el peso, otros efectos secundarios, la seguridad cardiovascular y el coste22,23. La pioglitazona se asocia a aumento de peso, edemas y a un mayor riesgo de insuficiencia cardiaca. Las sulfonilureas se asocian a incremento de peso, mayor riesgo de hipoglucemia y menor seguridad cardiovascular28. Sin embargo, los estudios con los IDPP-4 han demostrado un efecto neutro sobre el peso sin incrementar el RCV29,30.
Tratamiento de la hipertensión arterial en la hiperlipidemia familiar combinadaLa HTA se asocia frecuentemente a la HFC y es un predictor independiente del aumento de morbimortalidad en estos pacientes. Tras confirmar la HTA, se debe ampliar el estudio y evaluar la posible afectación de los órganos diana, detectar posibles causas de HTA secundaria y comprobar la existencia de otras enfermedades asociadas31.
El objetivo terapéutico del paciente hipertenso es conseguir cifras de PAS/PAD<140/90mmHg (CdR II, NdE A, GRADE fuerte). En los pacientes con DM el objetivo de PAD es 80-85mmHg, no existiendo beneficio añadido con cifras de PAS <130mmHg. En los pacientes ancianos con PAS>160mmHg el objetivo es conseguir PAS entre 140-150mmHg, debiendo individualizar los objetivos en el anciano frágil31.
Debido a que los pacientes con HFC son pacientes de alto o muy alto RCV, se debe considerar el tratamiento farmacológico desde el momento del diagnóstico en todos los pacientes con HTA grado1 o 2, independientemente de la implementación de la modificación de estilos de vida. El tratamiento farmacológico se debe implementar de forma inmediata en los pacientes con HTA grado3 (CdR I, NdE C, GRADE fuerte).
Se recomienda iniciar el tratamiento con dosis bajas del fármaco o fármacos, planificando una reducción gradual de la presión arterial (PA). Se deben usar fármacos de acción prolongada que permitan en lo posible dosis única diaria. El control de la PA con monoterapia solo se consigue en el 30%, por lo que generalmente habrá que usar terapia combinada. Es recomendable el uso de fármacos asociados para mejorar el cumplimiento terapéutico31. En general, la disminución de PA es similar en todos los fármacos antihipertensivos, solos o en combinación (CdR I, NdE A, GRADE fuerte). Sin embargo, en los pacientes con HFC son más recomendables, por su perfil metabólico neutro, los inhibidores de la enzima convertidora de angiotensina (IECA), los antagonistas de los receptores de angiotensina ii (ARA-II) si no se toleran los IECA (CdR I, NdE A, GRADE fuerte), y los antagonistas del calcio31,32.
Resumen de recomendaciones- -
La HFC se diagnóstica mediante criterios clínicos. No hay una prueba genética de certeza.
- -
Para el diagnóstico de la HFC se requiere la presencia de al menos 2 familiares directos con hiperlipidemia (colesterol y/o triglicéridos elevados).
- -
Se recomienda confirmar la variabilidad fenotípica en el individuo y sus familiares mediante análisis de lípidos repetidos.
- -
Se debe sospechar la HFC en un sujeto con hiperlipidemia primaria (c-LDL>160mg/dl y/o triglicéridos >200mg/dl).
- -
Si está disponible, la determinación de una apoB>120mg/dl apoya el diagnóstico clínico.
- -
No se deben aplicar los criterios de Framingham y SCORE para la valoración del RCV.
- -
Los pacientes con HFC se deben considerar de alto RCV, y el objetivo en c-LDL debe ser <100mg/dl.
- -
En los pacientes con HFC y ECV o DM tipo2, el objetivo en c-LDL debe ser <70mg/dl.
- -
El tratamiento farmacológico hipolipemiante se debe comenzar en el momento del diagnóstico, y la mayoría de estos pacientes requieren estatinas potentes o tratamiento combinado con ezetimiba o fibratos.
- -
En el tratamiento combinado de estatinas y fibratos está contraindicado el uso del gemfibrozilo.
- -
Si existe un aumento en las transaminasas, se debe realizar una ecografía hepática para descartar esteatosis hepática.
- -
El objetivo de control glucémico en la HFC es una HbA1c<7%, siendo menos estricto en pacientes ancianos, con riesgo de hipoglucemias o con enfermedad aterosclerótica muy avanzada (HbA1c 8-8,5%).
- -
En los pacientes con DM tipo2, el tratamiento inicial es metformina, y en caso necesario se pueden asociar otros fármacos, como IDDP-4 y análogos GLP-1, dado su perfil de seguridad y beneficio sobre el peso.
- -
En los pacientes con HTA, el objetivo es una PA<140/90mmHg.
- -
En los pacientes con DM, el objetivo de PAD es 80-85mmHg, no existiendo beneficio añadido con cifras de PAS<130mmHg.
- -
En la HTA se deben utilizar fármacos de acción prolongada, siendo los IECA, los ARA II y/o los antagonistas del calcio los recomendables por su efecto neutro sobre el perfil lipídico y glucémico.
Los autores declaran no tener ningún conflicto de intereses.
De acuerdo con los autores y los editores, este artículo se publica simultáneamente y de forma íntegra en la revista Semergen http://dx.doi.org/10.1016/j.semerg.2014.07.007