Evaluar la efectividad de los agonistas del receptor GLP-1 (arGLP-1) en pacientes con diabetes mellitus tipo 2 y describir sus características clínicas.
DiseñoEstudio retrospectivo observacional basado en registros electrónicos de salud en atención primaria.
EmplazamientoCentros de salud de la Gerencia de Atención Primaria y a la Comunidad (GAPiC) Camp de Tarragona.
ParticipantesPacientes de edad ≥18 años con diagnóstico de diabetes mellitus tipo 2 en tratamiento con un arGLP-1.
Mediciones principalesSe recogieron variables demográficas, la hemoglobina glicosilada (HbA1c) y el peso/IMC para valorar la efectividad; y el registro de variables clínicas para valorar la seguridad.
ResultadosSe incluyeron 1.227 pacientes (50,2% hombres). Se observó una reducción media de 0,50% en la HbA1c (p<0,001), de 3,08kg de peso (p<0,001) y de 0,99kg/m2 en el IMC (p<0,001) tras 472 días de tratamiento medio.
ConclusionesLos arGLP-1 presentan una efectividad modesta en el control glucémico y la reducción ponderal en pacientes diabéticos de tipo 2 en la práctica clínica. Los resultados son consistentes con estudios internacionales, aunque algo inferiores a los de ensayos clínicos pivotales.
To evaluate the effectiveness of GLP-1 receptor agonists (GLP-1 RAs) in patients with type 2 diabetes mellitus and to describe their clinical characteristics.
DesignRetrospective cohort study based on electronic health records.
SiteHealth centres of the Primary and Community Care Management (GAPiC) Camp de Tarragona.
ParticipantsPatients aged ≥18 years with a diagnosis of type 2 diabetes mellitus on treatment with an GLP-1 RA.
Main measurementsDemographic variables, glycosylated haemoglobin (HbA1c) and weight/BMI were collected to assess effectiveness; and clinical variables were recorded to assess safety.
ResultsA total of 1227 patients (50.2% male) were included. A mean average HbA1c% reduction of 0.50% in HbA1c (p<0.001), weight reduction of 3.08kg weight (p<0.001) and BMI reduction of 0.99kg/m2 (p<0,001) were observed after 472 days of average treatment.
ConclusionsGLP-1 RAs are effective in glycemic control and weight reduction in clinical practice. The results are consistent with international studies, although somewhat lower than pivotal trials.
La diabetes mellitus tipo 2 (DM2) es un problema de salud pública. Según la Organización Mundial de la Salud (OMS), el número de diabéticos ha aumentado en las últimas décadas, especialmente en países de renta baja y media1. Se espera que su prevalencia aumente debido al envejecimiento poblacional, el aumento de la obesidad y los hábitos poco saludables2.
La obesidad se ha duplicado mundialmente desde 1980. Junto al sobrepeso representa una carga significativa para la salud pública, suponiendo el 44% de la carga en el caso de la diabetes, el 23% en el de las enfermedades coronarias y entre el 7 y el 41% para ciertos tipos de cáncer2,3. La resistencia insulínica, común en la obesidad, provoca disfunciones metabólicas que afectan la regulación de glucosa y lípidos, aumentando el riesgo de complicaciones cardiovasculares, que representan el 80% de las macrovasculares y son exacerbadas por factores de riesgo adicionales como la HTA, la dislipidemia y la obesidad4.
El tratamiento de la DM2 implica cambios de estilo de vida y uso de medicación. La primera línea terapéutica incluye una dieta saludable, ejercicio regular y control de peso. La elección farmacológica se basa en el objetivo de control glicémico y las condiciones clínicas del paciente, como enfermedades cardiovasculares, enfermedad renal crónica, fragilidad y obesidad. Los fármacos usados en DM2 son biguanidas, sulfonilureas, inhibidores de la dipeptidil-peptidasa 4 (IDPP-4), agonistas del receptor GLP-1 (arGLP-1), inhibidores del cotransportador de sodio-glucosa tipo 2 (iSGLT2), tiazolidindionas, meglitinidas, inhibidores de la alfa-glucosidasa e insulina3.
Los arGLP-1 se han introducido recientemente en terapéutica en el manejo de la DM2 y de la obesidad5–10. Para el tratamiento de la DM2 actualmente este grupo lo integran liraglutida, dulaglutida y semaglutida. Tienen efectos adicionales como retraso del vaciado gástrico, disminución del apetito y aumento de la sensación de saciedad2,11. En España están autorizados para el tratamiento de la DM2 y de la obesidad, pero solo están financiados en terapia combinada con otros antidiabéticos para el tratamiento de la DM2 en pacientes obesos con un control glicémico inadecuado12.
En ensayos clínicos los arGLP-1 han demostrado reducciones de la hemoglobina glicosilada (HbA1c) del 0,4 al 1,8% y del peso entre 0,7 y 7kg comparado con placebo. Por otra parte, se asocian a un aumento de efectos adversos graves como alteraciones biliares y pancreatitis, trastornos renales, aumento del riesgo de retinopatía diabética y un posible aumento del riesgo de tumores tiroideos y pancreáticos13–18. Aunque diversos estudios han valorado su efecto en condiciones reales, son estudios con pocos pacientes y centrados en subgrupos poblacionales específicos1,2,11,19.
Material y métodosEl objetivo del presente estudio es evaluar la efectividad de los arGLP-1 en vida real y describir las características de los pacientes con DM2 de la Gerencia de Atención Primaria y a la Comunidad (GAPiC) Camp de Tarragona tratados con estos fármacos.
Se realizó un estudio de cohortes retrospectivas que incluyó todos los pacientes adscritos a los equipos de atención primaria de las comarcas del Tarragonès, Alt Camp y Conca de Barberà (12 equipos en total), con diagnóstico de DM2 (CIE-10 E008-E13) y en tratamiento activo con un fármaco arGLP-1 (clasificación ATC A10BJ) a fecha 20 de diciembre de 2023, sin considerarse criterios de exclusión. Se estableció una ventana temporal entre la fecha de la primera prescripción de un arGLP-1 y la fecha de identificación de los pacientes para el seguimiento. Se recogieron variables demográficas de edad y sexo, variables clínicas (peso, índice de masa corporal [IMC], HTA, obesidad, tabaquismo, insuficiencia renal, cardiopatía isquémica, accidente vascular cerebral, enfermedad arterial periférica), variables analíticas (HbA1c y perfil lipídico) y variables relacionadas con el tratamiento antidiabético (tipo de arGLP-1 y fármacos hipoglicemiantes adicionales) para describir las características clínicas de los pacientes y evaluar el cumplimiento de los criterios de financiación de los arGLP-1 (DM2 en obesos con IMC igual o mayor de 30kg/m2 y en terapia combinada con otros antidiabéticos, incluyendo insulina, cuando estos, junto con la dieta y el ejercicio, no proporcionan un control glicémico adecuado)12. Según el IMC, los pacientes se clasificaron como normopeso (IMC <25kg/m2), sobrepeso (IMC 25 a <30kg/m2), obesidad clase 1 (IMC 30 a <35kg/m2), obesidad clase 2 (IMC 35 a <40kg/m2), y obesidad clase 3 (IMC ≥40kg/m2)20. Para evaluar la efectividad del tratamiento con arGLP-1 se consideró la variación de la HbA1c mediante la diferencia de su valor porcentual, y la variación en el peso mediante la diferencia de su valor absoluto en kilogramos, así como la diferencia en el valor del IMC. Las tres variables se evaluaron en aquellos pacientes con un registro previo al inicio del tratamiento con un arGLP-1 y otro adicional después de ≥90 días de tratamiento con el arGLP-1. Se consideraron los objetivos de control glicémico de acuerdo con las recomendaciones de la American Diabetes Association21. La adherencia al tratamiento farmacológico se calculó de forma indirecta mediante la tasa de posesión de medicación, a partir del número de envases del medicamento dispensados desde la farmacia entre el número de envases totales del medicamento prescritos durante el año previo a la fecha de extracción de los datos22; y se consideró como adherencia alta un valor ≥80%23, media entre 40-79% y baja para un valor <40%. Para evaluar la seguridad se recogieron los diagnósticos de pancreatitis, litiasis biliar, colecistitis, neoplasia de vía biliar, cáncer de páncreas y de tiroides con registro posterior al inicio del tratamiento con arGLP-1.
La extracción de los datos la realizó la secretaría técnica de la GAPiC Camp de Tarragona en un fichero anonimizado.
Análisis estadísticoLos datos se analizaron con el programa estadístico R versión 4.3.3. Para las variables categóricas se calculó el valor absoluto y porcentaje, y para las cuantitativas se calculó la media y la desviación estándar. El análisis de la efectividad se realizó mediante la prueba paramétrica de la t de Student para datos apareados, y se realizó un análisis multivariante que incluyó el arGLP-1 utilizado, la adherencia al tratamiento, el sexo, los factores de riesgo cardiovascular (FRCV), la enfermedad cardiovascular establecida y el número de antidiabéticos no insulínicos asociados. Se consideró estadísticamente significativo un valor de p<0,05.
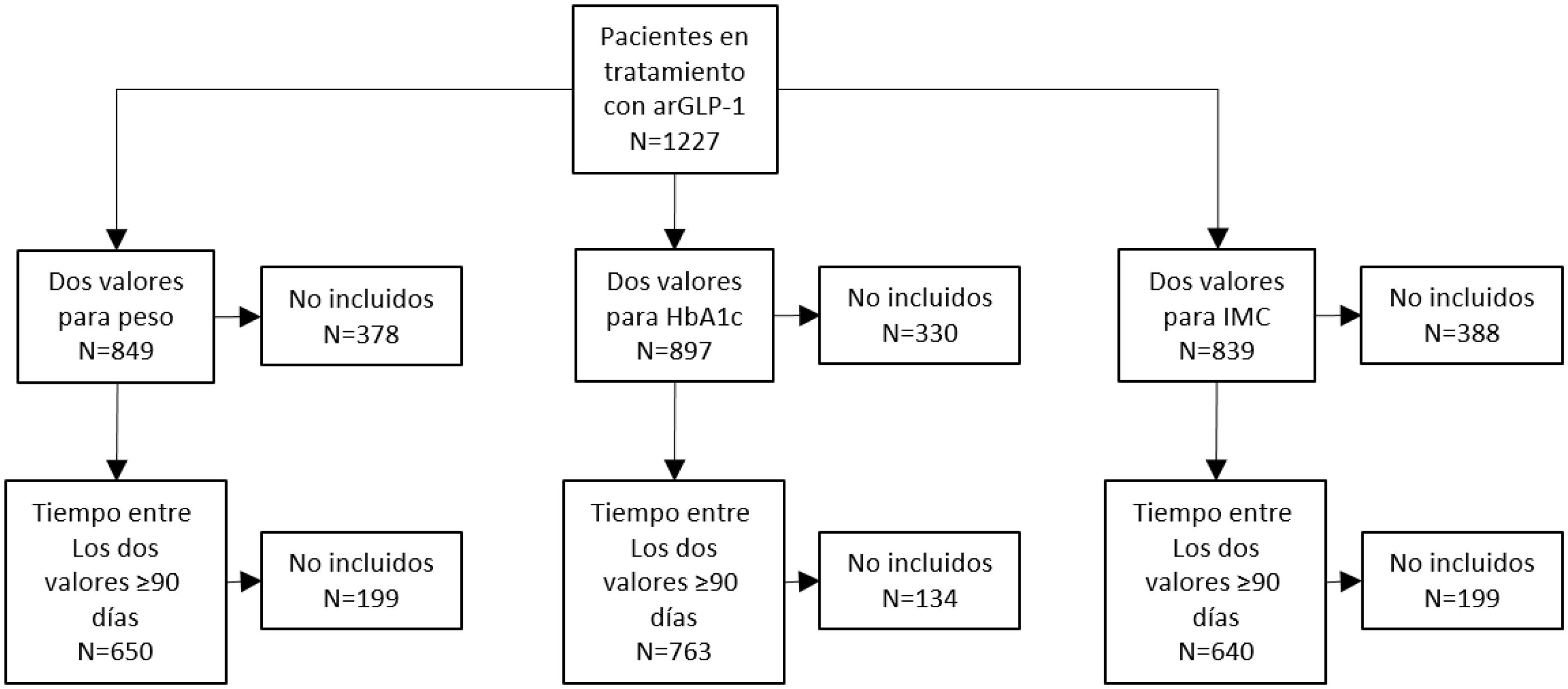
ResultadosLa figura 1 muestra el esquema del estudio. Para los análisis de efectividad de los arGLP-1 sobre la HbA1c, el peso y el IMC se incluyeron los pacientes con registro de un valor basal y otro ≥90 días tras el inicio del tratamiento.
Características basalesSe incluyeron 1.227 pacientes tratados con arGLP-1. La tabla 1 muestra las características basales. El 50,2% eran hombres y la edad media era de 62,7 (DE 11,1). La media de comorbilidades fue de 3,7 (DE 1,2), sin diferencias entre sexos. El 34,8% de los pacientes presentaban 4 comorbilidades relacionadas con el riesgo cardiovascular (DM2, obesidad, dislipemia, insuficiencia renal, HTA, tabaquismo, accidente cerebrovascular, cardiopatía isquémica, enfermedad arterial periférica). El 92,5% tenía obesidad.
Características basales
| Hombres(N=616) | Mujeres(N=611) | Total(N=1227) | |
|---|---|---|---|
| Edad | 62,9 (10,3) | 62,6 (11,9) | 62,7 (11,1) |
| Duración de DM2 (años) | 15,6 (20,3) | 22,1 (31,1) | 18,7 (26,4) |
| HbA1c | 7,7 (1,6) | 7,5 (1,6) | 7,6 (1,6) |
| Peso (kg) | 102,3 (18,8) | 90,2 (17,4) | 96,2 (19,1) |
| IMC (kg/m2) | 34,5 (6) | 36,1 (6,1) | 35,3 (6,1) |
| <25 | 4 (0,6) | 6 (1) | 10 (0,8) |
| 25-<30 | 113 (18,3) | 72 (11,8) | 185 (15,1) |
| 30-<35 | 258 (41,9) | 211 (34,5) | 469 (38,2) |
| 35-<40 | 146 (23,7) | 173 (28,3) | 319 (26) |
| ≥40 | 81 (13,1) | 140 (22,9) | 221 (18) |
| HTA | 462 (75) | 436 (71,4) | 898 (73,2) |
| Dislipemia | 362 (58,8) | 349 (57,1) | 711 (57,9) |
| Tabaquismo | 109 (17,7) | 85 (13,9) | 194 (15,8) |
| Cardiopatía isquémica | 125 (20,3) | 67 (11) | 192 (15,6) |
| Accidente cerebral vascular | 27 (4,4) | 22 (3,6) | 49 (4) |
| Enfermedad arterial periférica | 5 (0,8) | 4 (0,7) | 9 (0,7) |
| Antidiabéticos asociados | 519 (84,3) | 446 (73) | 965 (78,6) |
| No insulínicos | 239 (38,8) | 176 (28,8) | 415 (33,8) |
| Insulina | 143 (23,2) | 126 (20,6) | 269 (21,9) |
| No insulínico+insulina | 137 (22,2) | 144 (23,6) | 281 (22,9) |
| Metformina | 329 (53,4) | 265 (43,4) | 594 (48,4) |
| iSGLT-2 | 262 (42,5) | 154 (25,2) | 416 (33,9) |
| Sulfonilurea | 70 (11,4) | 78 (12,8) | 148 (12,1) |
| Meglitinida | 28 (4,5) | 20 (3,3) | 48 (3,9) |
| IDPP-4 | 24 (3,9) | 15 (2,5) | 39 (3,2) |
| Tiazolidindiona | 21 (3,4) | 13 (1,1) | 34 (2,8) |
Las variables categóricas se muestran con la n y el %, y las variables continuas con la media y desviación estándar.
El tiempo medio de uso de arGLP-1 fue de 440 (DE 397,3) días y los fármacos más utilizados fueron dulaglutida, semaglutida s.c. y liraglutida (tabla 2).
Distribución de especialidades farmacéuticas de arGLP-1
| N pacientes (%) | |
|---|---|
| Dulaglutida 0,75-1,5mg/semana s.c. | 752 (61,3%) |
| Semaglutida 0,25- 1mg/semana s.c. | 200 (16,3%) |
| Liraglutida 0,6-1,8mg/día s.c. | 167 (13,6%) |
| Semaglutida 3-14mg/día v.o. | 105 (8,6%) |
| Exenatida 2mg/semana s.c. | 2 (8,6%) |
| Lixisenatida 10-20μg/día s.c. | 1 (0,1%) |
s.c.: subcutánea; v.o.: vía oral.
El 56,7% de los pacientes tenían asociado otro antidiabético no insulínico, de los cuales la metformina representaba el 46,4%. El 46,1% de los pacientes estaban en tratamiento con insulina.
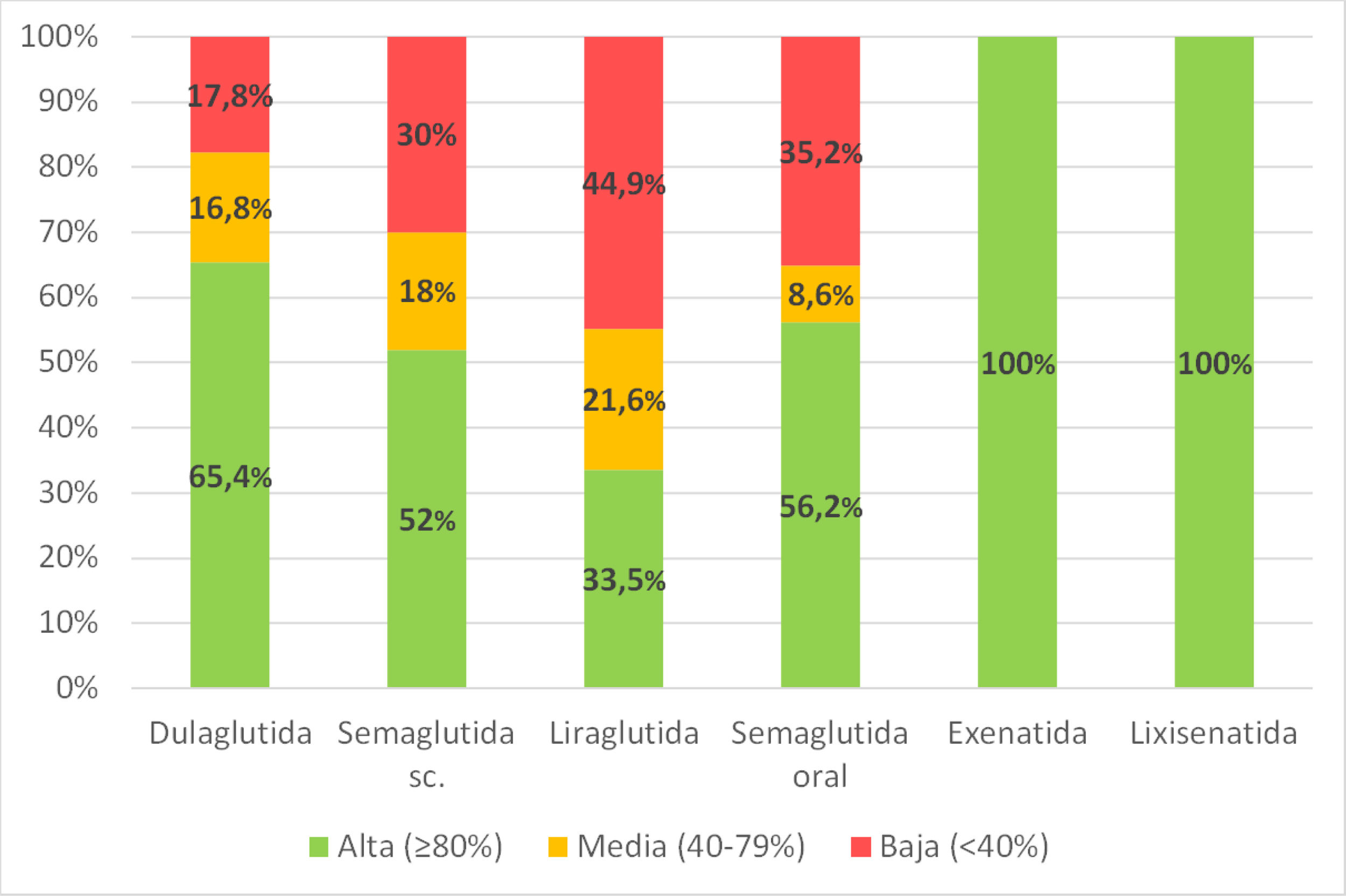
La figura 2 muestra la distribución de los pacientes según la adherencia al tratamiento con el arGLP-1 fuese buena (≥80%), media (40-79%) o baja (<40%).
Efectividad en la reducción de la HbA1c%La efectividad de los arGLP-1 en la reducción de la HbA1c se evaluó en 763 (62,2%) pacientes con un registro previo al inicio del tratamiento con arGLP-1 y otro tras ≥90 días desde su inicio. La reducción media de la HbA1c% fue de 0,5% (p<0,001) tras un tiempo medio de uso de 472 (DE 415) días. El análisis multivariante mostró una reducción estimada de 0,65% (DE 0,03; p<0,001) por cada punto porcentual adicional en la HbA1c previa al inicio de tratamiento en los pacientes con un valor basal >6,11%; una disminución en la intensidad del efecto sobre la HbA1c del arGLP-1 de 0,03% (DE 0,01; p<0,001) por cada año de evolución de la DM2; y una disminución del efecto de 0,11% (DE 0,03; p<0,004) por cada año de uso del arGLP-1. No se observaron diferencias en la reducción de la HBA1c según el arGLP-1 utilizado, el grado de adherencia al tratamiento, el sexo, la presencia de FRCV, la presencia de enfermedad cardiovascular ni el número de antidiabéticos no insulínicos asociados.
Efectividad en la reducción del pesoLa efectividad de los arGLP-1 en la reducción del peso se evaluó en 650 (53%) pacientes que disponían de un registro previo al inicio del tratamiento con arGLP-1 y otro tras ≥90 días desde su inicio. La reducción media fue de 3,08 (DE 7,21; p<0,001) kg tras 471 (DE 409) días de tratamiento. Los pacientes no insulinizados mostraron una reducción significativa de peso respecto a los insulinizados (−3,64kg vs. −2,46kg, respectivamente [p=0,037]). En el análisis multivariante se mostró una reducción de 0,09 (DE 0,02; p<0,001) kg por cada kg de peso adicional para los pacientes con peso basal superior a 91,7kg, mientras que entre los pacientes con peso inferior a este valor se mostró un aumento de 0,09 (DE 0,02; p<0,001) kg por cada kilo de peso adicional. No se observaron diferencias de eficacia en la reducción del peso entre los arGLP-1, y tampoco entre los diferentes grupos de adherencia al tratamiento, según el sexo, la presencia de diferentes FRCV, enfermedad cardiovascular establecida, ni por la presencia de otros antidiabéticos no insulínicos.
Efectividad en la reducción del IMCSe evaluaron 640 pacientes con un registro previo al inicio de un arGLP-1 y otro tras ≥90 días desde su inicio. La reducción del IMC fue de 0,99kg/m2 (DE 3,72; p<0,001) tras 462 (DE 400) días de tratamiento. Se observó una reducción significativa del IMC entre los pacientes no insulinizados respecto a los insulinizados (−1,36kg/ m2 vs. −0,9kg/m2, respectivamente [p=0,031]). No se observaron diferencias en la reducción del IMC entre sexos, por la presencia de FRCV, enfermedad cardiovascular establecida, por la presencia de otros antidiabéticos no insulínicos, así como entre los diferentes grupos de adherencia al tratamiento.
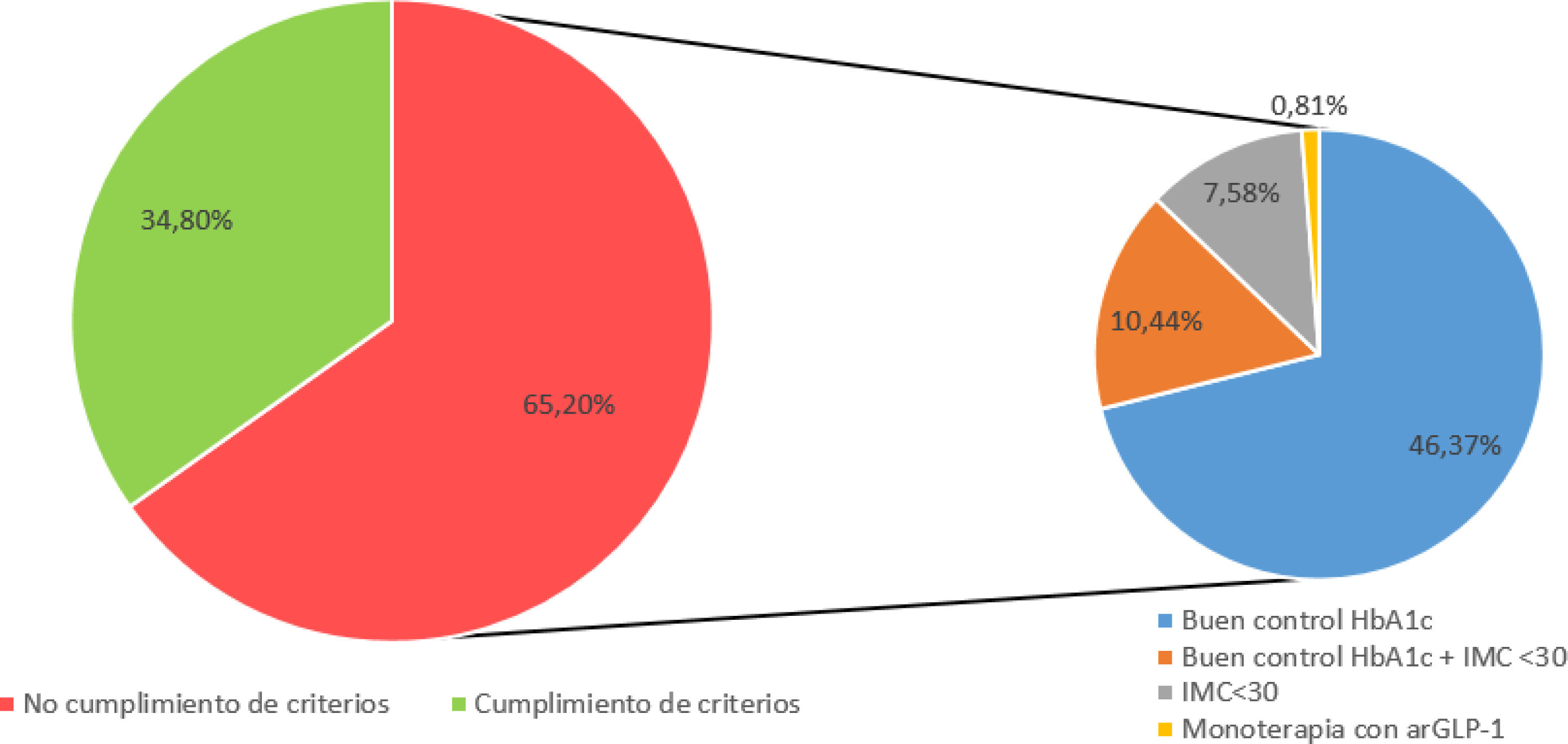
Criterios de financiaciónEn España los arGLP-1 están financiados en pacientes con DM2 y obesidad (IMC>30), con mal control metabólico a pesar de las medidas no farmacológicas y el tratamiento con otro hipoglicemiante (incluida la insulina). Se estableció el cumplimiento de los criterios de financiación en 1.179 pacientes para los que se disponían de los valores basales de HbA1c y de IMC. La figura 3 muestra los resultados para el cumplimiento de estos criterios, con un valor de HbA1c ≤7% como objetivo de buen control21.
Se observaron reducciones significativas a favor de los pacientes que cumplían con criterios de financiación respecto a los que no cumplían, tanto para la reducción de la HbA1c (−0,9% vs. −0,06%; p<0,001) como para la del peso (−3,79kg vs. −2,36kg; p<0,012).
SeguridadDurante el tratamiento con arGLP-1 se diagnosticaron 6 casos de cáncer de tiroides, uno de colecistitis y 2 de pancreatitis.
DiscusiónLos arGLP-1 han demostrado su eficacia en el manejo de la DM2 y de la obesidad, logrando mejoras significativas en el control glicémico y la reducción ponderal13–18. Nuestro trabajo muestra unos efectos consistentes con los de estos estudios, pero las reducciones son menores que las reportadas en ensayos clínicos.
Aunque en nuestro estudio el efecto observado en la reducción de HbA1c es menor que el de un reciente metaanálisis de ensayos clínicos24, que muestra una reducción entre el 1,04% con liraglutida y el 1,4% con semaglutida, y al observado en otros estudios con datos de vida real, en los que el efecto varía entre una reducción del 0,86% y del 1,02%1,25, estas diferencias podrían deberse a las características de los pacientes, con una población de mayor edad y una diabetes de mayor evolución en nuestro estudio, a la mayor representatividad de los fármacos menos potentes (liraglutida y dulaglutida), que representan el 74,9% de arGLP-1 en nuestro estudio, y al desabastecimiento de todas las especialidades de administración subcutánea, que ha dificultado la adherencia y persistencia al tratamiento. La adherencia, especialmente baja para la liraglutida y la semaglutida, también podría ser un motivo de la ausencia de diferencias entre los arGLP-1 en nuestro estudio.
La relación directa entre la HbA1c inicial y la magnitud de la reducción observada es similar a la de otros estudios. De la misma manera, nuestro estudio muestra un peor resultado sobre la HbA1c en función del tiempo de evolución de la DM2 y de la duración del tratamiento con arGLP-1, en línea con lo observado en estudios previos1,25–27.
Respecto a la efectividad en la reducción ponderal, en nuestro estudio la pérdida de peso media observada fue de 3,08kg que, aunque significativa, es inferior a la reportada en el anterior metaanálisis, que varía entre una reducción de 0,73kg para dulaglutida hasta 3,3kg para semaglutida. Los pacientes incluidos en los estudios de este metaanálisis tenían una edad media de 56,8 años, una diabetes de 8,5 años de evolución media y un IMC medio de 31,7. En diferentes estudios con datos de vida real25,28 la reducción de peso varía entre 1,44kg a los 6 meses hasta 10,5kg a los 12 meses, observándose un efecto más pronunciado que en nuestro trabajo en aquellos estudios con una población de menor edad, con un IMC mayor y una duración de uso de los arGLP-1 mayor. En cambio, el efecto es inferior en los estudios con población de edad más avanzada, cuanto menor es la duración del uso del arGLP-1 y cuanto menor es el IMC. Cabe destacar que, a diferencia de nuestro estudio, en una población de características similares se observó un efecto superior en la reducción del peso entre las mujeres que entre los hombres (3,11kg vs. 2,23kg, respectivamente)1. Es posible que esta diferencia sea debida a que el perfil de uso de los arGLP-1 en ambos estudios es diferente, y a que en el estudio de Franch había una mayor proporción de mujeres con IMC ≥35 que la de hombres.
Las principales limitaciones de nuestro estudio incluyen su diseño retrospectivo y la falta de grupo control. El desabastecimiento de presentaciones subcutáneas de arGLP-1 durante el periodo de estudio puede haber afectado los resultados, ya que puede haberse relacionado con la falta de adherencia a los tratamientos. La naturaleza retrospectiva del estudio también ha limitado la capacidad de detectar los efectos adversos. Al basarnos en una explotación de registros informáticos, pueden haberse infrarregistrado los efectos adversos graves, y en mucha mayor medida los efectos adversos leves. De hecho, la ausencia de registro de los efectos adversos gastrointestinales, que son los más frecuentes con el uso de los arGLP-129, nos ha impedido poder cuantificar el impacto de estos en el abandono del tratamiento y la falta de adherencia.
ConclusionesEn nuestro estudio el tratamiento con arGLP-1 ha demostrado su efectividad en la reducción de la HbA1c, el peso y el IMC en los pacientes diabéticos, sin diferencias según el sexo. Sin embargo, la magnitud del efecto observado para este grupo terapéutico en la práctica clínica habitual es inferior al obtenido en ensayos clínicos.
- •
Existe una relación entre diabetes y obesidad.
- •
Los arGLP-1 son eficaces en la reducción de la HbA1c y el peso en pacientes diabéticos tipo 2.
- •
La eficacia de los arGLP-1 sobre la reducción de la HbA1c y la pérdida de peso en la práctica clínica habitual es inferior a la observada en los ensayos clínicos.
- •
Su eficacia es superior en los pacientes diabéticos que cumplen con los criterios de financiación.
La presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro.
Consideraciones éticasEl estudio fue aprobado por el Comité Ético de Investigación con medicamentos del Institut d’Investigació Sanitària Pere Virgili (Referencia CEIM: 109/2024).
Conflicto de interesesFerran Bejarano Romero. Declaración de interés: ninguna.
Vicente Aragó Molés. Declaración de interés: ninguna.
Daniel Morón Porrúa. Declaración de interés: ninguna.
Eva López Guerrero. Declaración de interés: ninguna.
Helena Suñer Barriga. Declaración de interés: ninguna.
Laura Canadell Vilarrasa. Declaración de interés: ninguna.