Investigar la relación entre género y supervivencia después de un episodio de ictus tratado con fibrinólisis.
DiseñoEstudio de cohortes.
EmplazamientoAtención primaria.
ParticipantesLos casos tratados con fibrinólisis por un ictus agudo desde el 1 de abril de 2006 al 13 de septiembre de 2013.
IntervencionesSeguimiento del estado vital.
Mediciones principalesRiesgos vasculares: escala Framingham, REGICOR, CHA2DS2-VASc, Essen, NIHSS, índice Barthel; densidad de incidencia; análisis de supervivencia por Kaplan-Meier; bivariado entre supervivientes y fallecidos; y multivariante de Cox.
ResultadosNoventa y un pacientes con edad media 68,02±11,9 años. Los hombres tienen mayor riesgo cardiovascular basal. El tiempo medio de seguimiento fue de 2,95±2,33 años. La razón de tasa de incidencias mostró un mayor riesgo en los hombres respecto a las mujeres IR=3,2 (IC 95%: 1,2-8,0). Los fallecidos en relación con los supervivientes son mayores (p=0,032); mayor riesgo cardiovascular basal (p=0,040) y de recidiva de ictus (p<0,001); mayor severidad del episodio (p=0,002); y una mayor caída en la puntuación Barthel un año después del ictus (p=0,016). El porcentaje de muertes es significativamente más alto cuando el paciente es derivado a centros de agudos o de larga estancia (p=0,006) que cuando se deriva al domicilio, pero solo el género (HR: 1,12; IC 95%: 1,05-1,20) y la prevención cardiovascular secundaria (HR: 0,13; IC 95%: 0,06-0,28) se asociaron con la mortalidad de los pacientes.
ConclusionesDespués de un episodio de ictus tratado con fibrinólisis los hombres tienen un 12% más de riesgo de morir que las mujeres, y la ausencia de prevención cardiovascular secundaria aumenta 7,7 veces el riesgo de mortalidad.
To seek if there is gender survival difference among patients treated with thrombolytic therapy.
DesignCohort study.
LocationCommunity based register.
Participants91 subjects with an episode of stroke collected since April 2006 up to September 2013 and treated with thrombolytic therapy.
InterventionsMonitoring of vital status.
MeasurementsWe collected baseline characteristics in Framingham, Regicor, CHA2DS2-VASc, Essen, NIHSS, Barthel scales and outcomes according to gender; person-time incidence rate; survival analysis by Kaplan-Meier's curves, bivariate analysis between survivors and deaths, and Cox multivariate.
Results91 patients with middle age 68.02±11.9 years. The men have higher cardiovascular basal risk. The average time of follow-up was 2.95±2.33 years. Incidence rate ratio (IR) shown higher risk in men than in women IR=3.2 (CI 95% 1.2-8.0). The dead cases were older (P=.032); with higher cardiovascular basal risk (P=.040) and more risk of stroke recurrence (P=<.001), with cardiovascular pathology before the stroke (P=.005); more stroke severity (P=.002); and a major fall in the score Barthel one year after the episode (P=.016). The percentage of deaths is significantly higher when the patient is referred by complications to other centres (P=.006) in relation to those referred to home, but just the gender (HR: 1,12; IC 95%: 1,05-1,20) and secondary cardiovascular prevention (HR: 0,13; IC 95%: 0,06-0,28) were associated with higher risk of mortality.
ConclusionsAfter stroke episode treated with thrombolytic therapy, men have 12% higher risk of dying than women and don’t be treated with secondary cardiovascular prevention rise 7.7 times the mortality risk.
Estudios previos han descrito diferencias entre hombres y mujeres tanto en el pronóstico funcional como en la supervivencia después de un episodio de ictus1–3. Las mujeres tienen un pronóstico funcional menos favorable4, pero una mayor supervivencia a los 6 meses del episodio5 y a los 3 años6. Más allá de diferencias epidemiológicas, la implantación del tratamiento fibrinolítico aporta nuevas controversias en los resultados según el género. Mientras unos estudios7–9 parecen demostrar que beneficia más a las mujeres basándose en diferencias en la edad10, en la prevención secundaria11, en la base biológica12, en la severidad clínica o en la presencia de insuficiencia cardíaca13 y en la recurrencia de eventos cardiovasculares6, otros sugieren que no hay diferencias14 o incluso objetivan que las mujeres tienen menor probabilidad de ser tratadas con fibrinolíticos15.
Se trata de pacientes tratados en el hospital mediante fibrinólisis por un episodio agudo de ictus, y la mayoría de ellos serán tratados y seguidos en el ámbito de atención primaria. El objetivo del estudio es investigar si hay alguna relación entre el género y la supervivencia de pacientes tratados rutinariamente después de un episodio de ictus con fibrinólisis6,16 desde la implantación del código ictus territorial, y cuyos resultados iniciales apuntaban hacia la existencia de diferencias en el sentido de una mayor supervivencia en las mujeres.
Material y metodologíaEl proyecto Ebrictus6,16 es un estudio de una cohorte fija histórica de base poblacional formada por los casos incidentes de un primer episodio de ictus agudo desde el 1 de abril de 2006, fecha de implantación del código ictus en el territorio, al 31 de marzo de 2008 en cuanto a la incidencia, y hasta el 13 de septiembre de 2013 en cuanto al seguimiento del estado vital a partir de la información existente en cualquiera de los ámbitos asistenciales. Las causas de exclusión fueron: no tener su residencia habitual o la asignación a un EAP del territorio en los 5 años anteriores al episodio; pacientes<15 años o≥90 años; haber padecido un episodio de ictus previamente a la fecha de inicio del estudio, cualquiera que fuera su tipo o etiología; y imposibilidad de obtener datos suficientes por ausencia/déficit o no accesibilidad a los registros clínicos.
La principal fuente de información clínica son los registros de los programas de historia clínica informatizada utilizados por los profesionales de l’Institut Català de la Salut (ICS). Los datos proceden de la explotación automatizada y periódica de las bases de datos:
- 1.
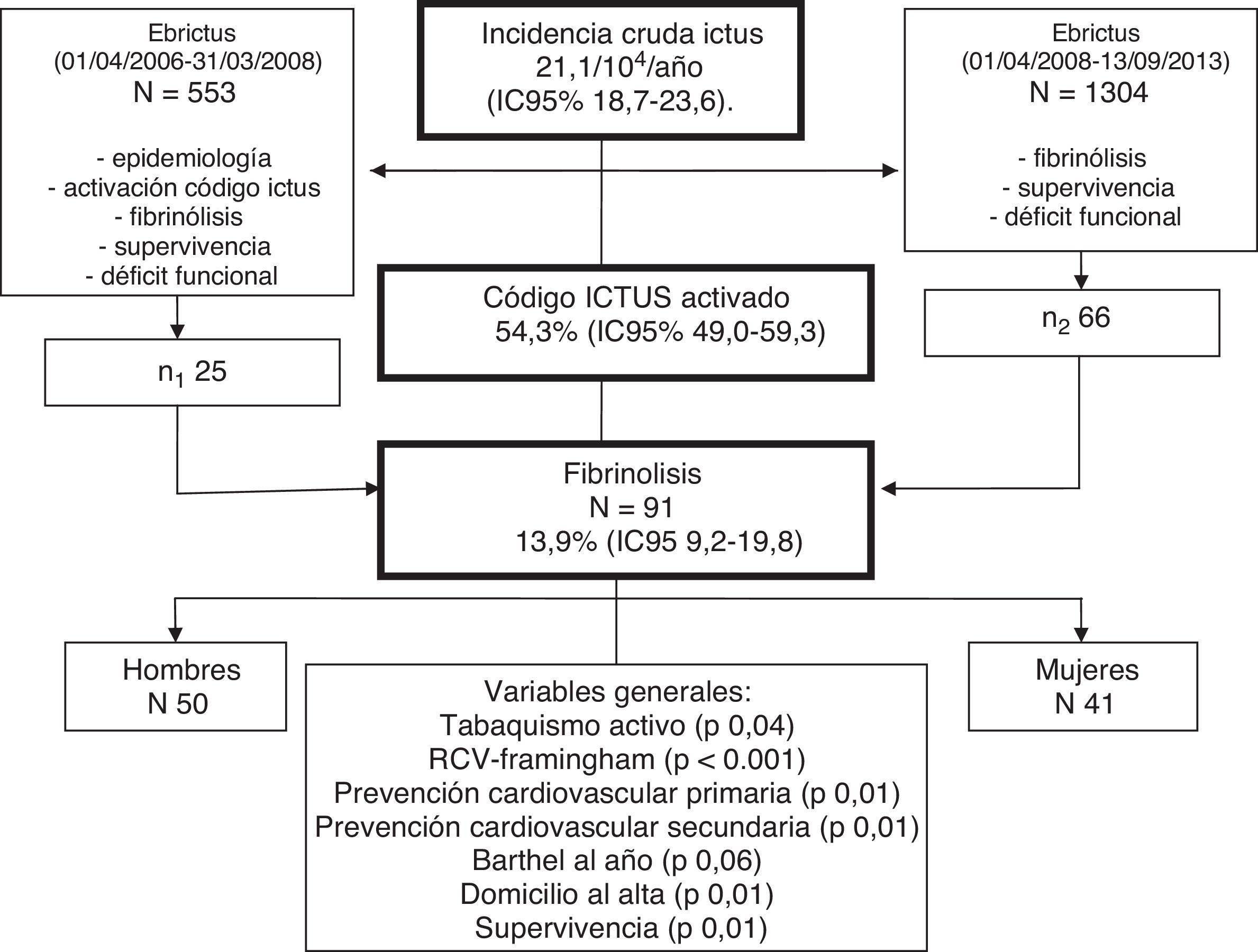
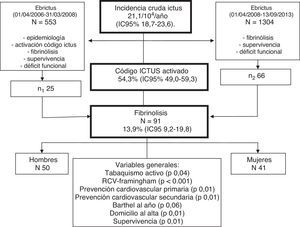
El programa de historia clínica informatizada de atención primaria, la estación clínica de Atención Primaria (e-CAP), utiliza la codificación internacional CIE-10 (OMS, 1992). Incluye la población asignada a los 8 equipos de atención primaria (EAP) participantes (fig. 1).
- 2.
El programa de historia clínica informatizada del ámbito hospitalario, la tecnología sistemas, aplicaciones, productos (SAP). Utiliza la codificación CIM-9.
Los casos diagnosticados como ictus entre los habitantes del territorio de les Terres de l’Ebre son derivados al hospital de referencia de Tortosa Virgen de la Cinta para la atención aguda del episodio y su evaluación en cuanto a la posibilidad de ser tratados mediante fibrinólisis. El protocolo de tratamiento fibrinolítico cambió en el año 2011, ampliándose a todas las personas en función de su puntuación Rankin.
En el estudio inicial el número de pacientes tratados con fibrinólisis era insuficiente, y se incrementó con los nuevos casos con un episodio de ictus y tratados con fibrinólisis hasta el 13 de septiembre de 2013, sumando un total de 91 pacientes tratados con fibrinólisis desde la implantación del código ictus en el territorio en 1 de abril de 2006. Las variables de las que se recogió información se describen en los estudios originales y se agruparon en los siguientes grandes grupos, independientemente de su origen e-CAP o SAP: datos demográficos; factores de riesgo cardiovascular; escalas de cálculo de riesgos vasculares Framingham, REGICOR (para ambas opciones existe la disponibilidad del cálculo automatizado en el registro e-CAP del paciente), CHA2DS2-VASc17 en los pacientes con fibrilación auricular registrada y riesgo de recurrencia del ictus mediante el uso de la escala Essen18; clínicas: activación del código ictus, valor en la escala de ictus del National Institute of Health (escala NIHSS)19 al ingreso, y destino al alta hospitalaria (hospital de mayor complejidad, domicilio, hospital de convalecencia/larga estancia); prescripción activa registrada; incidencia de nuevos episodios cardiovasculares (cardiopatía isquémica o/y recidiva ictus) intercurrentes agudos en el postepisodio; autonomía funcional previa y postictus medida por el índice de Barthel20; y estado vital del paciente (vivo/muerto). En el proceso6 se distinguen diferentes etapas: basal, previo al episodio; en el episodio; y en el postepisodio primeros 90 días y/o al año. La prevención cardiovascular secundaria preictus era la realizada en aquellos pacientes con enfermedad vascular diferente y previa al episodio actual de ictus.
Los pacientes fallecidos durante el ingreso por el ictus inicial o dentro del primer mes se consideran «mortalidad inmediata». Los fallecidos con posterioridad se califican de «mortalidad posterior». Los datos de mortalidad se han obtenido del registro central de asegurados del CatSalut y el seguimiento activo de las historias clínicas de los casos incidentes. Comprende la cuantificación de las muertes ocurridas durante el periodo de estudio cualquiera que sea su causa.
Se evaluó si existían diferencias entre hombres y mujeres respecto a las variables categóricas mediante la Chi-cuadrado. Las diferencias estadísticamente significativas entre los 2 sexos en las variables continuas se evaluaron mediante la «t» de Student. Para la estimación de la supervivencia el punto de inicio es la fecha diagnóstica del episodio y el punto final es la fecha de defunción por cualquier causa o la fecha final del estudio. Por cada sexo se calculó la densidad de incidencia, cuyo numerador es el número de fallecidos en el periodo de estudio y el denominador el total de casos tratados con fibrinólisis/tiempo de seguimiento (personas-año), la razón de tasas de incidencia (IR) calculada como la ratio entre las 2 densidades de incidencia, y la hazard ratio (HR). Se utiliza el método actuarial o el de Kaplan-Meier para el cálculo de la curva de supervivencia de todos los pacientes; el test de Log-rank para comparar el número de muertes observadas con el número de muertes esperadas; y el modelo de riesgos proporcionales de Cox para el análisis multivariante de supervivencia.
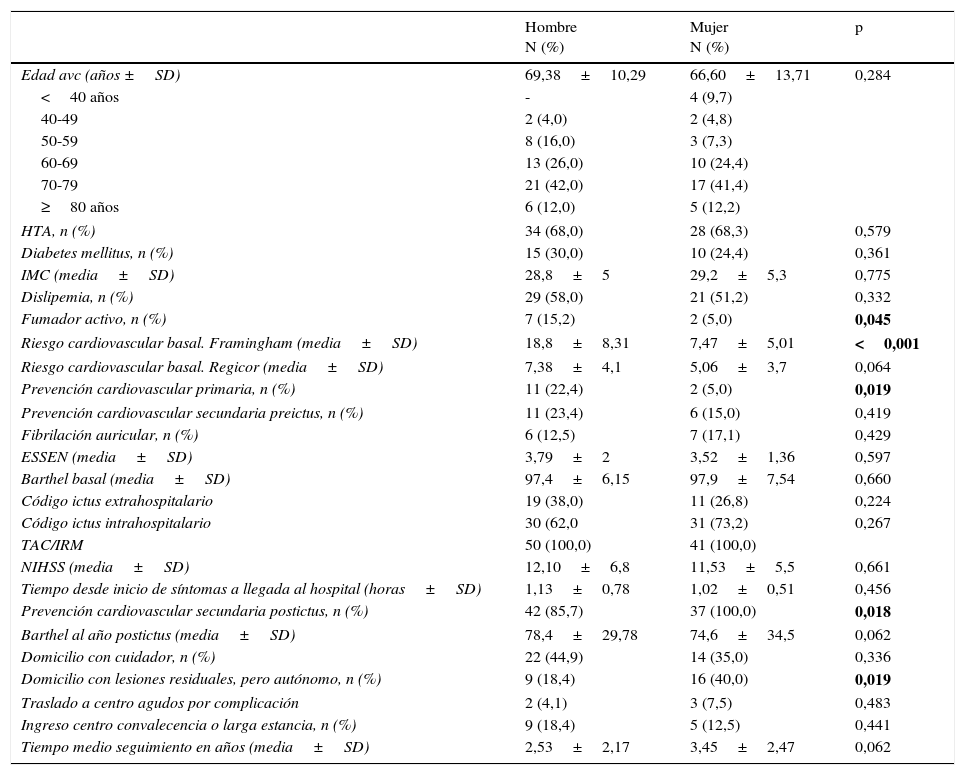
ResultadosDesde el inicio del código ictus el 13,9% (IC 95%: 9,2-19,8) de los pacientes con código ictus activado fueron tratados con fibrinólisis. En total son 91 pacientes. En la tabla 1 se describen las características de cada grupo por género. La edad media fue 68,02±11,9 años. Fueron mujeres 41 (45,1%), con una edad media de 66,6±13,7 años, y hombres 50 (54,9%) con una edad media de 69,3±10,3 años. Más del 50% de las fibrinólisis se realizaron en pacientes >70 años de edad. Se encontraron diferencias significativas en los hombres en el riesgo cardiovascular basal y un porcentaje de fumadores activos más alto que las mujeres. El porcentaje de mujeres <50 años (14,6%) con fibrinólisis es superior al de los hombres (4,0%), aunque no llega a ser significativo (p=0,075). Tras el episodio de ictus tratado con fibrinólisis la prevención cardiovascular secundaria es significativamente menor entre los hombres, aunque en el 93,2% del total que se realizaba. No se identificaron diferencias en la edad media (p=0,284), en la puntuación media en la escala Barthel (p=0,660), en el tiempo transcurrido desde el inicio de los síntomas hasta la llegada al hospital (p=0,456), en la gravedad del episodio según la escala NIHSS (p=0,661) ni en el riesgo de recidiva de ictus según el valor en la escala Essen (p=0,597). La activación del código ictus extrahospitalaria fue mayor entre los hombres, mientras que la intrahospitalaria lo fue entre las mujeres, aunque sin diferencias significativas.
Características de los pacientes tratados con fibrinólisis según el sexo. Ebrictus, 2013
| Hombre N (%) | Mujer N (%) | p | |
|---|---|---|---|
| Edad avc (años ±SD) | 69,38±10,29 | 66,60±13,71 | 0,284 |
| <40 años | - | 4 (9,7) | |
| 40-49 | 2 (4,0) | 2 (4,8) | |
| 50-59 | 8 (16,0) | 3 (7,3) | |
| 60-69 | 13 (26,0) | 10 (24,4) | |
| 70-79 | 21 (42,0) | 17 (41,4) | |
| ≥80 años | 6 (12,0) | 5 (12,2) | |
| HTA, n (%) | 34 (68,0) | 28 (68,3) | 0,579 |
| Diabetes mellitus, n (%) | 15 (30,0) | 10 (24,4) | 0,361 |
| IMC (media±SD) | 28,8±5 | 29,2±5,3 | 0,775 |
| Dislipemia, n (%) | 29 (58,0) | 21 (51,2) | 0,332 |
| Fumador activo, n (%) | 7 (15,2) | 2 (5,0) | 0,045 |
| Riesgo cardiovascular basal. Framingham (media±SD) | 18,8±8,31 | 7,47±5,01 | <0,001 |
| Riesgo cardiovascular basal. Regicor (media±SD) | 7,38±4,1 | 5,06±3,7 | 0,064 |
| Prevención cardiovascular primaria, n (%) | 11 (22,4) | 2 (5,0) | 0,019 |
| Prevención cardiovascular secundaria preictus, n (%) | 11 (23,4) | 6 (15,0) | 0,419 |
| Fibrilación auricular, n (%) | 6 (12,5) | 7 (17,1) | 0,429 |
| ESSEN (media±SD) | 3,79±2 | 3,52±1,36 | 0,597 |
| Barthel basal (media±SD) | 97,4±6,15 | 97,9±7,54 | 0,660 |
| Código ictus extrahospitalario | 19 (38,0) | 11 (26,8) | 0,224 |
| Código ictus intrahospitalario | 30 (62,0 | 31 (73,2) | 0,267 |
| TAC/IRM | 50 (100,0) | 41 (100,0) | |
| NIHSS (media±SD) | 12,10±6,8 | 11,53±5,5 | 0,661 |
| Tiempo desde inicio de síntomas a llegada al hospital (horas±SD) | 1,13±0,78 | 1,02±0,51 | 0,456 |
| Prevención cardiovascular secundaria postictus, n (%) | 42 (85,7) | 37 (100,0) | 0,018 |
| Barthel al año postictus (media±SD) | 78,4±29,78 | 74,6±34,5 | 0,062 |
| Domicilio con cuidador, n (%) | 22 (44,9) | 14 (35,0) | 0,336 |
| Domicilio con lesiones residuales, pero autónomo, n (%) | 9 (18,4) | 16 (40,0) | 0,019 |
| Traslado a centro agudos por complicación | 2 (4,1) | 3 (7,5) | 0,483 |
| Ingreso centro convalecencia o larga estancia, n (%) | 9 (18,4) | 5 (12,5) | 0,441 |
| Tiempo medio seguimiento en años (media±SD) | 2,53±2,17 | 3,45±2,47 | 0,062 |
Los datos en negrita resaltan la presencia de diferencias significativas.
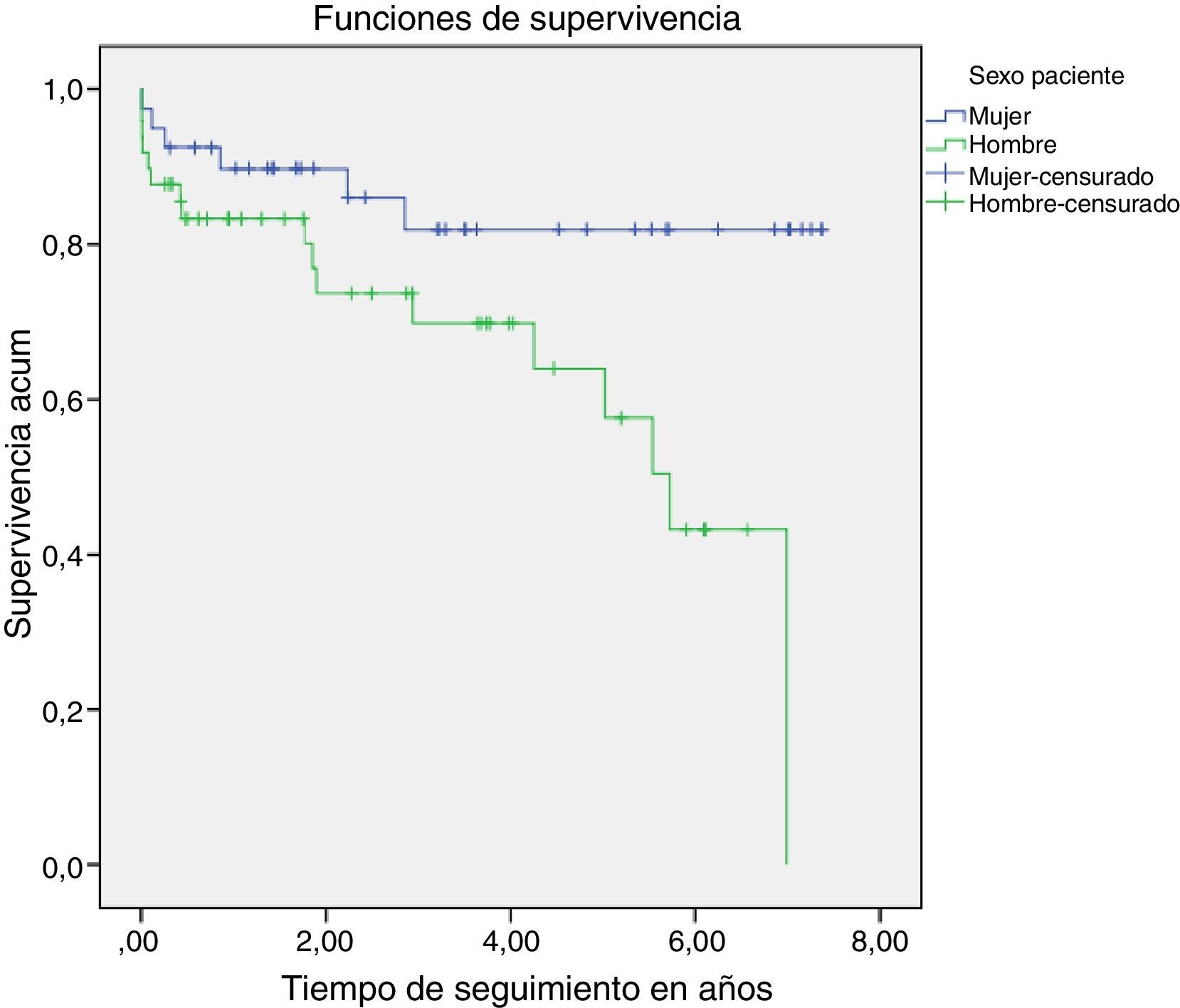
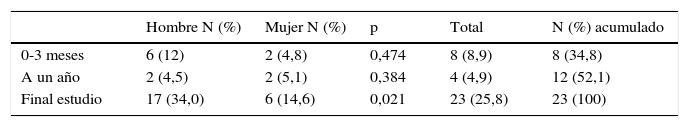
El tiempo medio de seguimiento fue de 2,95±2,33 años, mayor en las mujeres (p=0,061). La distribución de casos por cuartiles demuestra su uniformidad, siendo 2,46 el valor del percentil 50 (Q1 0,88; Q2 2,46; Q3 4,97). Al cierre del estudio los hombres tienen mayor mortalidad en relación con las mujeres (tabla 2). Se produjeron 23 (25,8%) defunciones, de las cuales 17 (73,9%) fueron hombres. La densidad de incidencia fue 8,5/100 personas-año de seguimiento (IC 95%: 5,4-12,8); en las mujeres fue 4,2/100 casos-año (IC 95%: 1,5-9,2) y en los hombres 13,4/100 casos-año (IC 95%: 7,8-21,5). La IR fue significativa (p=0,01) y mostró un mayor riesgo en los hombres: IR=3,2 (IC 95%: 1,2-8,0).
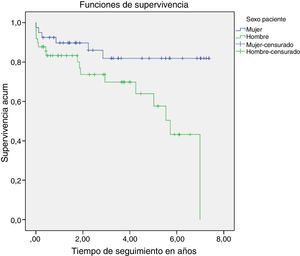
La mortalidad total a los 90 días fue similar en hombres y mujeres, produciéndose el 34,8% de las defunciones; al año se producen la mitad de todas las defunciones (52,1%). La diferencia en las defunciones según el género aumenta progresivamente con la duración del periodo de seguimiento, de modo que al final la supervivencia es significativamente inferior en los hombres. La probabilidad de supervivencia al final del estudio entre las mujeres fue 0,81±0,06 y en los hombres 0,43±0,02 (p=0,012).
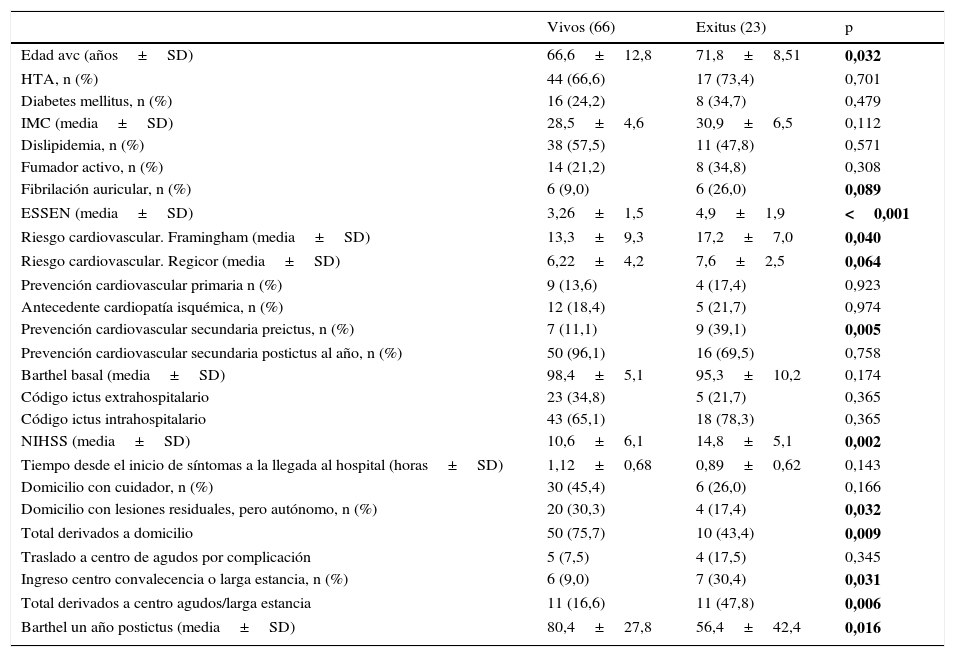
En cuanto a las diferencias de los fallecidos en relación con los supervivientes (tabla 3), aquellos son significativamente mayores (p=0,032), tienen un mayor riesgo cardiovascular basal (p=0,040) y de recidiva de ictus en la escala Essen (p<0,001), un mayor porcentaje de prevención cardiovascular secundaria previamente al episodio de ictus (p=0,005), una mayor severidad clínica del ictus (0,002) y una mayor caída en la puntuación Barthel un año después del episodio (p=0,016). El porcentaje de muertes también es más alto cuando el paciente es derivado a centros de agudos por complicaciones o a centros de larga estancia (p=0,006) en relación con aquellos derivados al domicilio.
Características de los pacientes tratados con fibrinólisis según el estado vital (fallecidos vs vivos). Ebrictus, 2013
| Vivos (66) | Exitus (23) | p | |
|---|---|---|---|
| Edad avc (años±SD) | 66,6±12,8 | 71,8±8,51 | 0,032 |
| HTA, n (%) | 44 (66,6) | 17 (73,4) | 0,701 |
| Diabetes mellitus, n (%) | 16 (24,2) | 8 (34,7) | 0,479 |
| IMC (media±SD) | 28,5±4,6 | 30,9±6,5 | 0,112 |
| Dislipidemia, n (%) | 38 (57,5) | 11 (47,8) | 0,571 |
| Fumador activo, n (%) | 14 (21,2) | 8 (34,8) | 0,308 |
| Fibrilación auricular, n (%) | 6 (9,0) | 6 (26,0) | 0,089 |
| ESSEN (media±SD) | 3,26±1,5 | 4,9±1,9 | <0,001 |
| Riesgo cardiovascular. Framingham (media±SD) | 13,3±9,3 | 17,2±7,0 | 0,040 |
| Riesgo cardiovascular. Regicor (media±SD) | 6,22±4,2 | 7,6±2,5 | 0,064 |
| Prevención cardiovascular primaria n (%) | 9 (13,6) | 4 (17,4) | 0,923 |
| Antecedente cardiopatía isquémica, n (%) | 12 (18,4) | 5 (21,7) | 0,974 |
| Prevención cardiovascular secundaria preictus, n (%) | 7 (11,1) | 9 (39,1) | 0,005 |
| Prevención cardiovascular secundaria postictus al año, n (%) | 50 (96,1) | 16 (69,5) | 0,758 |
| Barthel basal (media±SD) | 98,4±5,1 | 95,3±10,2 | 0,174 |
| Código ictus extrahospitalario | 23 (34,8) | 5 (21,7) | 0,365 |
| Código ictus intrahospitalario | 43 (65,1) | 18 (78,3) | 0,365 |
| NIHSS (media±SD) | 10,6±6,1 | 14,8±5,1 | 0,002 |
| Tiempo desde el inicio de síntomas a la llegada al hospital (horas±SD) | 1,12±0,68 | 0,89±0,62 | 0,143 |
| Domicilio con cuidador, n (%) | 30 (45,4) | 6 (26,0) | 0,166 |
| Domicilio con lesiones residuales, pero autónomo, n (%) | 20 (30,3) | 4 (17,4) | 0,032 |
| Total derivados a domicilio | 50 (75,7) | 10 (43,4) | 0,009 |
| Traslado a centro de agudos por complicación | 5 (7,5) | 4 (17,5) | 0,345 |
| Ingreso centro convalecencia o larga estancia, n (%) | 6 (9,0) | 7 (30,4) | 0,031 |
| Total derivados a centro agudos/larga estancia | 11 (16,6) | 11 (47,8) | 0,006 |
| Barthel un año postictus (media±SD) | 80,4±27,8 | 56,4±42,4 | 0,016 |
Los datos en negrita destacan las diferencias significativas entre ambos grupos.
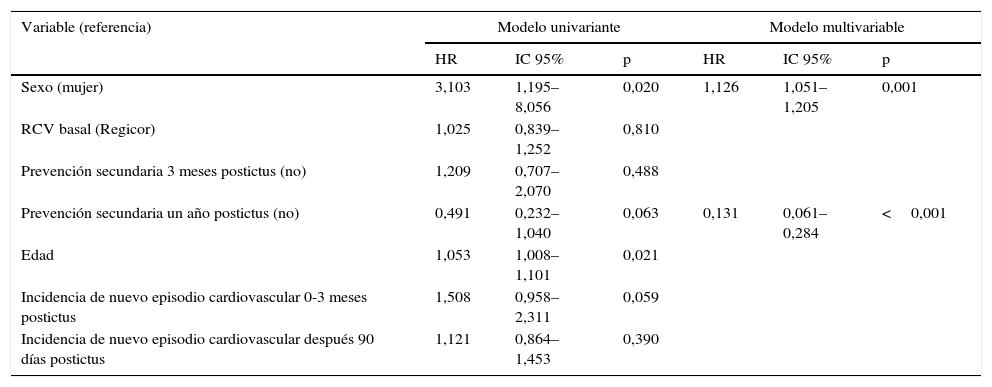
En la regresión de Cox (tabla 4) después de ajustar por sexo, edad, riesgo cardiovascular previo al episodio, valor en la escala NIHSS, valor en la escala Essen, recidiva de nuevo episodio cardiovascular (cardiopatía isquémica o ictus), estado funcional al año del episodio y tipo de prevención secundaria cardiovascular solo el género (HR: 1,12; IC 95%: 1,05-1,20) y la prevención cardiovascular secundaria (HR: 0,13; IC 95%: 0,06-0,28) fueron estadísticamente significativas con la mortalidad. La HR del género muestra que los hombres tienen un 12% más de riesgo que las mujeres de mortalidad. Recibir prevención cardiovascular secundaria después del ictus mostró ser un factor de protección frente a la mortalidad. No recibir prevención secundaria tiene 7,7 (1/0,13) veces más riesgo de mortalidad independientemente del género. Este riesgo se calculó con la inversa de la HR de la prevención cardiovascular de la tabla 4.
Modelo de regresión de Cox. Variables asociadas a la mortalidad. Ebrictus, 2013
| Variable (referencia) | Modelo univariante | Modelo multivariable | ||||
|---|---|---|---|---|---|---|
| HR | IC 95% | p | HR | IC 95% | p | |
| Sexo (mujer) | 3,103 | 1,195–8,056 | 0,020 | 1,126 | 1,051–1,205 | 0,001 |
| RCV basal (Regicor) | 1,025 | 0,839–1,252 | 0,810 | |||
| Prevención secundaria 3 meses postictus (no) | 1,209 | 0,707–2,070 | 0,488 | |||
| Prevención secundaria un año postictus (no) | 0,491 | 0,232–1,040 | 0,063 | 0,131 | 0,061–0,284 | <0,001 |
| Edad | 1,053 | 1,008–1,101 | 0,021 | |||
| Incidencia de nuevo episodio cardiovascular 0-3 meses postictus | 1,508 | 0,958–2,311 | 0,059 | |||
| Incidencia de nuevo episodio cardiovascular después 90 días postictus | 1,121 | 0,864–1,453 | 0,390 | |||
Estudios observacionales sobre la historia natural de pacientes con ictus han mostrado que las mujeres tienen peor pronóstico que los hombres, más mortalidad y son más frecuentemente institucionalizadas5. La edad, los antecedentes de mayor riesgo cardiovascular, el papel protector de la prevención secundaria, la severidad clínica del episodio de ictus y la capacidad funcional residual medida por la escala de Barthel pueden considerarse factores que influyen en el pronóstico después de un ictus, independientemente de haber sido tratado con fibrinólisis o no, pero el efecto género sobre la mortalidad parece ser clínicamente superior al efecto del azar. Mayor probabilidad de reperfusión, respuesta del cerebro a la isquemia, diferencias en los mecanismos de coagulación, efectos hormonales o diferencias en la anatomía vascular del ictus han sido propuestos como mecanismos explicativos12, pero siguen siendo poco esclarecedores. El reto es si con estos datos podemos conseguir mejores resultados de salud mediante la selección de pacientes con un perfil más favorable frente a los riesgos de la fibrinólisis21.
La mortalidad acumulada de los pacientes con ictus es similar sean tratados o no con fibrinólisis. En el primer año postictus mueren alrededor del 50%6,22. En cuanto al género las tasas de incidencia de 0,042 casos-año en mujeres frente a la de 0,134 casos-año en hombres parecen indicar que la fibrinólisis en las mujeres es más protectora que en los hombres. No obstante, la mayoría de estudios no ha aportado diferencias de pronóstico, a pesar de la evidencia de diferencias en sujetos no tratados5,6,23. Una de las razones puede ser las diferentes definiciones14 utilizadas como pronóstico favorable. La diferencia aumenta progresivamente cuando se calcula más allá de los 90 días que utilizan como indicador la mayoría de estudios14. En diversos estudios7,10,24 se han aportado diferencias en cuanto a que las mujeres tratadas con fibrinólisis tenían menor riesgo cardiovascular basal y mayor prevalencia de fibrilación auricular, pero, a diferencia de nuestro estudio, eran mayores en edad. Dado que la edad6 es uno de los factores pronóstico con más peso en la supervivencia, y que la edad media de los pacientes en los que se activa el código ictus es significativamente inferior, la menor edad de nuestro grupo de mujeres podría ser el resultado de la selección de pacientes en una activación mayoritariamente intrahospitalaria del código ictus y actuar como factor de confusión en la diferencia de los resultados de supervivencia, y/o ser realmente una consecuencia de una mayor incidencia de ictus entre las mujeres por debajo de los 50 años que en los hombres. Dado que la cohorte del estudio Ebrictus6 tiene una edad media de 73,3 años y las mujeres son significativamente (p=0,01) mayores (74,4±11,9) que los hombres (72,1±11,2) cabría esperar un reflejo de la diferencia de edad también en los resultados del tratamiento con fibrinólisis. En todo caso existe un mayor porcentaje de mujeres <50 años con fibrinólisis, lo que puede explicar la edad media inferior de las mismas. En los resultados publicados de nuestro estudio Ebrictus6 ya describimos que las tasas ajustadas de mortalidad en el periodo de 65-79 años era significativamente mayor en los hombres (37,7/104; IC 95%: 26,2-49,3) que en las mujeres (14,7/104; IC 95%: 7,7-21,8), de modo que en las mujeres el 64,6% (IC 95%: 52,1-75,9) de la mortalidad se producía a partir de los 80-89. Dado que la edad media del grupo de hombres tratados con fibrinólisis está incluida en el intervalo de mayor mortalidad en hombres que sufren un episodio de ictus, y que la edad de las mujeres es inferior, debería tenerse en cuenta la posibilidad de que la fibrinólisis en nuestro grupo de mujeres aumentase un pronóstico de supervivencia ya inherentemente mejor al de los hombres.
En cuanto a la evolución de la puntuación en la escala Barthel es conocido que 1/3 de los pacientes que sufren un ictus tienen una dependencia moderada al año, con una pérdida superior en las mujeres que en los hombres6,25,26 no atribuible a una mayor edad ni a una mayor severidad clínica del episodio. Nuestros resultados no muestran diferencias significativas al año del episodio, aunque sí una puntuación Barthel<60 está asociada a la mortalidad. Esto también sugeriría que el tratamiento con fibrinólisis puede reducir la conocida diferencia entre géneros en el pronóstico funcional después de un ictus27.
La eficacia del código ictus ha sido demostrada, pero paradójicamente existen 2 factores de interés. Se produce un uso por debajo de las expectativas28,29 y su activación sigue siendo mayoritariamente intrahospitalaria (¾ partes de los casos)16.
La prevención cardiovascular secundaria se comporta como una covariable protectora con el género, y aunque los resultados solo evalúan la realización de la misma, se evidencia su impacto6. Que el grupo de hombres tenga un mayor riesgo cardiovascular antes del episodio de ictus que las mujeres y una menor cobertura en prevención secundaria podría favorecer el diferente pronóstico. Las mujeres tienden a tener más criterios de salud cardiovascular, y la mayoría de criterios identificados como diferencias entre los supervivientes y los fallecidos estarían incluidos entre los que definen el nuevo concepto de salud cardiovascular ideal30. Si bien nuestros resultados sugieren que el género mujer se asocia a una mayor supervivencia y es un marcador clínico entre aquellos pacientes con mayor probabilidad de beneficiarse del tratamiento con fibrinólisis, la prevención secundaria después del episodio parece el recurso con mayor valor en atención primaria para disminuir la mortalidad.
Después de un episodio de ictus las mujeres parecen tener un pronóstico funcional menos favorable1, pero una mejor supervivencia a los 6 meses del episodio2.
La implantación de nuevos protocolos de tratamiento mediante fibrinólisis aporta nuevas evidencias acerca de si hay o no diferencias en los resultados4–11. Existen diferencias entre hombres y mujeres tanto en el pronóstico funcional como en la supervivencia después de un episodio de ictus25–27.
Qué aporta este estudioDetecta diferencias significativas en la mortalidad por género tras un episodio de ictus tratado con fibrinólisis. La densidad de incidencia de 0,042 casos-año en mujeres frente a la de 0,134 casos-año en hombres parece indicar que la fibrinólisis en las mujeres es más protectora que en los hombres.
El perfil de mayor riesgo para morir tras un episodio de ictus tratado con fibrinólisis sería un varón alrededor de 71 años de edad con enfermedad cardiovascular previa, que ha sufrido un episodio de ictus con una severidad clínica alta (14,8), cuyo Barthel al año del episodio refleja dependencia moderada (<60), y que fue derivado a un centro de larga estancia o a un centro de agudos por complicaciones del episodio.
No recibir prevención secundaria aumenta 7,7 (1/0,13) veces el riesgo de mortalidad después de un episodio de ictus tratado con fibrinólisis.
Existe una mayor probabilidad de supervivencia entre las mujeres, que aumenta progresivamente más allá de los 3 meses, que utilizan la mayoría de estudios14. La densidad de incidencia de mortalidad en el grupo de mujeres fue 4,2/100 casos-año y en los hombres 13,4/100 casos-año.
No recibir prevención cardiovascular secundaria después del ictus aumenta 7,7 (1/0,13) veces el riesgo de mortalidad.
Otra informaciónEste trabajo contiene la continuidad de los resultados iniciales de la tesis doctoral Estudio Ebrictus. Epidemiología del primer episodio de ictus: incidencia, abordaje clínico, pronóstico, supervivencia y años potenciales de vida perdidos, presentada en 2011 en la Universidad Miguel Hernández y cuyos resultados iniciales se publicaron en:
Clua-Espuny JL, Piñol-Moreso JL, Panisello-Tafalla A, Lucas-Noll J, Gil-Guillen VF, Orozco-Beltran D, et al. Estudio Ebrictus. Resultados funcionales, supervivencia y años potenciales de vida perdidos después del primer episodio de ictus. Aten Primaria. 2012;44:223-31.
Clua-Espuny JL, Piñol-Moreso JL, Gil-Guillén FV, Orozco-Beltran D, Panisello-Tafalla A, Lucas-Noll J. La atención sanitaria del ictus en el área Terres de l’Ebre desde la implantación del código ictus: Estudio Ebrictus. Med Clin (Barc). 2012;138:609-11.
Clua-Espuny JL, Piñol-Moreso JL, Gil-Guillén FV, Orozco-Beltran D, Panisello-Tafalla A, Lucas-Noll J, et al. Resultados de prevención cardiovascular primaria y secundaria en pacientes con ictus. Riesgo de recurrencia y supervivencia asociada. Estudio Ebrictus. Rev Neurol. 2012;54:81-92.
FinanciaciónSe recibió como apoyo económico la Beca Isabel Fernández de la Sociedad Española de Medicina Familiar y Comunitaria, convocatoria 2010 a la tesis doctoral Estudio Ebrictus. Epidemiología del primer episodio de ictus: incidencia, abordaje clínico, pronóstico, supervivencia y años potenciales de vida perdidos.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.