Los signos y síntomas de la trombosis venosa profunda (TVP) en las extremidades suelen ser inespecíficos y a menudo influidos por la comorbilidad del paciente.
ObjetivoAnálisis de variables clínicas de los pacientes con sospecha clínica de un primer episodio de TVP en Atención Primaria.
Material y métodosEstudio observacional transversal y analítico de pacientes ambulatorios con sospecha de un primer episodio de TVP en extremidades inferiores. Se correlacionan los factores de riesgo y comorbilidades con la confirmación diagnóstica de TVP mediante ecografía-doppler.
ResultadosSe estudió a 116 pacientes, de los cuales en 22 (18,9%) se confirmó el diagnóstico. Las comorbilidades más frecuentes fueron la hipertensión, la hipercolesterolemia y la diabetes tipo 2. Solo la presencia de un diagnóstico alternativo probable y la inmovilización prolongada se asociaron con la exclusión o el diagnóstico final de TVP, respectivamente. Las enfermedades del aparato locomotor conllevaron una mayor probabilidad de falsa sospecha de TVP y el único signo clínico que se correlacionó con el diagnóstico fue la tumefacción de la extremidad afecta.
ConclusionesEn la práctica clínica, la tumefacción o el antecedente de parálisis de la extremidad nos ha de hacer sospechar firmemente una TVP. Sin embargo, la presencia de un posible diagnóstico alternativo prácticamente descartará dicha enfermedad.
Deep vein thrombosis (DVT) has unspecific signs and symptoms that are often influenced by the comorbidity of the patient.
ObjectiveTo analyze the clinical features and the associated comorbidity of patients with symptoms compatible with a first DVT in a Primary Care setting.
Material and methodsObservational, cross-sectional and analytical study of patients with a first episode of suspected DVT. The risk factors and comorbidities are correlated with the DVT diagnostic confirmation by ultrasound.
ResultsA total of 116 patients were included, of whom 22 had DVT (18,9%) confirmed by ultrasound. The most frequent associated comorbidities were hypertension, hypercholesterolemia, and type 2 diabetes mellitus. Only the presence of an alternative diagnosis more likely than DVT and the lower extremity immobilization were associated with the exclusion or confirmation of the diagnosis, respectively. Musculoskeletal diseases were correlated with a greater probability of a false suspicion of DVT. The only sign associated with the final diagnosis was the swelling of lower limbs.
ConclusionsIn clinical practice, swelling or a history of limb paralysis should lead to the suspicion of DVT. However, the presence of a possible alternative diagnosis could rule out this disease.
La enfermedad tromboembólica venosa es una entidad que engloba la trombosis venosa profunda (TVP) y el tromboembolismo pulmonar (TEP). La incidencia anual de TVP en Europa se sitúa aproximadamente entre 143 y 183 por 100.000 habitantes1,2. Concretamente en España existe un estudio que observó una incidencia de dicha enfermedad de 63 casos por 100.000 habitantes año3. Se sabe que la incidencia de la enfermedad tromboembólica aumenta con la edad, y en pacientes mayores de 80 años alcanza los 450-900 casos por 100.000 habitantes4. Esta entidad conlleva una elevada morbimortalidad, que incluye principalmente la muerte, la embolia pulmonar, la hipertensión arterial pulmonar y el síndrome postrombótico5,6. De hecho, hoy en día, la enfermedad tromboembólica es la tercera causa de muerte cardiovascular, tras la cardiopatía isquémica y el accidente cerebrovascular7,8.
Los pacientes con sospecha de TVP que son derivados desde la Atención Primaria a los centros hospitalarios no suelen ser diagnosticados de dicha enfermedad. Más concretamente, en un 75% de los casos tras la realización de pruebas complementarias se descarta el diagnóstico9. En el Reino Unido, más de 140.000 personas con clínica compatible de TVP son atendidos habitualmente en atención primaria cada año10. La prevalencia global de la enfermedad tras la realización de pruebas complementarias se sitúa en torno al 20%11,12.
A pesar de que no existen características clínicas específicas para el diagnóstico de TVP, se han descrito una serie de signos, síntomas y antecedentes patológicos que se relacionan más frecuentemente con esta enfermedad13. Todas estas circunstancias han sido utilizadas para crear diferentes escalas de probabilidad clínica que se incluyen dentro del proceso diagnóstico de la TVP14,15.
No obstante, debido a la inespecificidad de la sintomatología con que se presenta la TVP, la clínica puede variar dependiendo de las características del paciente16. La comorbilidad asociada puede enmascarar, asemejar o confundir la clínica de TVP y dificultar el diagnóstico4.
En este artículo describimos las características clínicas, sociodemográficas y la comorbilidad asociada en pacientes que presentan sintomatología compatible con un primer episodio de TVP en Atención Primaria. Estos datos pueden aportar información adicional que ayuden a guiar un proceso diagnóstico tan heterogéneo.
Material y métodosEstudio observacional, transversal y analítico en el que se estudió a pacientes derivados al Servicio de Urgencias del Hospital de la Santa Creu i Sant Pau desde los 15 centros de Atención Primaria de su área de referencia en Barcelona ciudad.
Se incluyó consecutivamente a todos los pacientes mayores de 18 años, con clínica compatible con un primer episodio de TVP y que aportaban un informe de derivación desde la medicina primaria.
Se excluyó a aquellos pacientes sin informe de derivación de Atención Primaria que no aceptasen participar o que no perteneciesen a la zona de referencia. También se excluyó a los pacientes con clínica superior a 30 días, con sospecha clínica de TEP concomitante, que estuviesen en tratamiento con anticoagulantes orales, presentasen antecedentes de TEP o TVP previas, o que presentasen cualquier enfermedad física o psíquica concomitante incapacitante o terminal.
A todos los que cumplían los criterios de inclusión se les solicitó su participación. El protocolo fue aprobado por el Comité Ético de Investigación Clínica (CEIC) del Instituto de Investigación en Atención Primaria IDIAP Jordi Gol y el CEIC del hospital de la Santa Creu i Sant Pau.
La selección de pacientes fue consecutiva hasta alcanzar la muestra estimada. Los datos necesarios se recogieron mediante entrevista clínica, exploración física, determinación de laboratorio y ecografía doppler. Se registraron motivos de consulta, tiempo de evolución de la sintomatología, variables sociodemográficas, medidas antropométricas, estilo de vida y fármacos que tomaban de manera habitual. También se recogieron las variables de los ítems incluidos en las escalas de probabilidad clínica más frecuentemente utilizadas7,17: presencia de cáncer activo; inmovilización, parálisis o paresias recientes de extremidades inferiores; encamamiento o cirugía mayor reciente; edema en toda la extremidad; diagnóstico alternativo probable; uso de anticonceptivos orales. Entre las variables de la exploración física se recogieron los signos y síntomas de estas escalas: signo de Homans13,17; tumefacción en toda la extremidad; diferencia de 3 o más cm del perímetro entre pantorrillas; edema con fóvea; venas superficiales colaterales. Se incluyeron otras variables de exploración no incluidas en las escalas como el calor local, cianosis, eritema y el empastamiento muscular (desplazamiento en bloque de los gemelos al movilizarlos en decúbito supino y extremidades en semiflexión). A todos los participantes se les realizó una ecografía doppler de la extremidad afecta tras la valoración clínica, que fue utilizada como prueba de referencia para confirmar o excluir el diagnóstico de TVP.
Se consideró comorbilidad la presencia de enfermedades concomitantes crónicas presentes en el momento de la inclusión en el estudio.
En los pacientes en los que se descartó la presencia de TVP, se intentó identificar alguno de los diagnósticos diferenciales. En los pacientes en los que se confirmó la TVP, se inició el tratamiento con heparina de bajo peso molecular a dosis terapéuticas y se les derivó al Servicio de Hematología para su seguimiento.
Análisis estadísticoBasándose en la prevalencia de un 20% de TVP descrita en estudios previos, con una confianza del 95% y una precisión del 10%, en el supuesto de máxima incertidumbre se precisó un tamaño muestral de 113 individuos. Se realizó un sobremuestreo del 15%.
Con relación al análisis descriptivo, las variables categóricas se presentan en forma de porcentajes totales o estratificados por categorías y las variables cuantitativas con las correspondientes medidas de tendencia central y dispersión.
Para el análisis bivariante se realizó el test de la t de Student en el caso de variables dicotómicas que seguían una distribución paramétrica o, cuando procedía, las pruebas no paramétricas correspondientes. Para la comparación de variables categóricas se utilizaron tablas de contingencia, utilizando siempre que fue posible el test exacto de Fisher, o el test de la Chi-cuadrado.
Se construyeron modelos de regresión logística para determinar la asociación de las variables recogidas y la confirmación o no del diagnóstico de TVP. Se construyó un modelo de introducción manual con las variables principales según la bibliografía, resultasen o no significativas en el análisis bivariante.
En todos los contrastes de hipótesis realizados para valorar la asociación entre variables se consideró como estadísticamente significativo un nivel α de 0,05 (p < 0,05). El tratamiento estadístico de los datos se realizó con el paquete estadístico SPSS® versión 18 para Windows®.
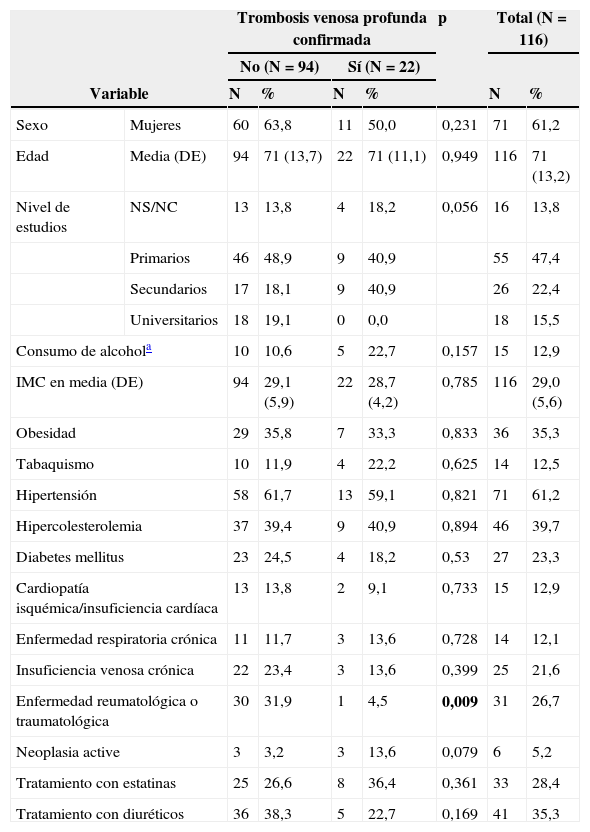
ResultadosEntre enero de 2012 y junio de 2013 se valoró a 138 pacientes, de los cuales 116 cumplieron criterios de inclusión. Se excluyó a 22 pacientes: 3 sin informe de derivación de la Atención Primaria, 4 por presentar clínica de más de 30 días de evolución, 7 por estar en tratamiento anticoagulante y 8 con antecedentes de TVP. De los 116 pacientes incluidos, se confirmó el diagnóstico de TVP en 22 casos (18,9%) con ecografía-doppler. La edad media de los pacientes fue de 71 años (DE: 13,2) y un 61% fueron mujeres (tabla 1). Los antecedentes patológicos observados con mayor frecuencia fueron la hipertensión arterial, la hipercolesterolemia y la diabetes mellitus tipo 2.
Características de la población atendida por sospecha de trombosis venosa profunda
| Trombosis venosa profunda confirmada | p | Total (N=116) | ||||||
|---|---|---|---|---|---|---|---|---|
| No (N=94) | Sí (N=22) | |||||||
| Variable | N | % | N | % | N | % | ||
| Sexo | Mujeres | 60 | 63,8 | 11 | 50,0 | 0,231 | 71 | 61,2 |
| Edad | Media (DE) | 94 | 71 (13,7) | 22 | 71 (11,1) | 0,949 | 116 | 71 (13,2) |
| Nivel de estudios | NS/NC | 13 | 13,8 | 4 | 18,2 | 0,056 | 16 | 13,8 |
| Primarios | 46 | 48,9 | 9 | 40,9 | 55 | 47,4 | ||
| Secundarios | 17 | 18,1 | 9 | 40,9 | 26 | 22,4 | ||
| Universitarios | 18 | 19,1 | 0 | 0,0 | 18 | 15,5 | ||
| Consumo de alcohola | 10 | 10,6 | 5 | 22,7 | 0,157 | 15 | 12,9 | |
| IMC en media (DE) | 94 | 29,1 (5,9) | 22 | 28,7 (4,2) | 0,785 | 116 | 29,0 (5,6) | |
| Obesidad | 29 | 35,8 | 7 | 33,3 | 0,833 | 36 | 35,3 | |
| Tabaquismo | 10 | 11,9 | 4 | 22,2 | 0,625 | 14 | 12,5 | |
| Hipertensión | 58 | 61,7 | 13 | 59,1 | 0,821 | 71 | 61,2 | |
| Hipercolesterolemia | 37 | 39,4 | 9 | 40,9 | 0,894 | 46 | 39,7 | |
| Diabetes mellitus | 23 | 24,5 | 4 | 18,2 | 0,53 | 27 | 23,3 | |
| Cardiopatía isquémica/insuficiencia cardíaca | 13 | 13,8 | 2 | 9,1 | 0,733 | 15 | 12,9 | |
| Enfermedad respiratoria crónica | 11 | 11,7 | 3 | 13,6 | 0,728 | 14 | 12,1 | |
| Insuficiencia venosa crónica | 22 | 23,4 | 3 | 13,6 | 0,399 | 25 | 21,6 | |
| Enfermedad reumatológica o traumatológica | 30 | 31,9 | 1 | 4,5 | 0,009 | 31 | 26,7 | |
| Neoplasia active | 3 | 3,2 | 3 | 13,6 | 0,079 | 6 | 5,2 | |
| Tratamiento con estatinas | 25 | 26,6 | 8 | 36,4 | 0,361 | 33 | 28,4 | |
| Tratamiento con diuréticos | 36 | 38,3 | 5 | 22,7 | 0,169 | 41 | 35,3 | |
DE: desviación estándar; IMC: índice de masa corporal.
Los resultados resaltados en negrita indican signficación estadística.
De las variables analizadas en el análisis bivariante, solo la presencia de enfermedad del aparato locomotor concomitante se relacionó con una menor probabilidad de presentar una TVP, es decir, con una falsa sospecha de TVP (p: 0,009). El resto de variables de la tabla 1 no mostró asociación significativa con la probabilidad de tener un diagnóstico confirmado de TVP.
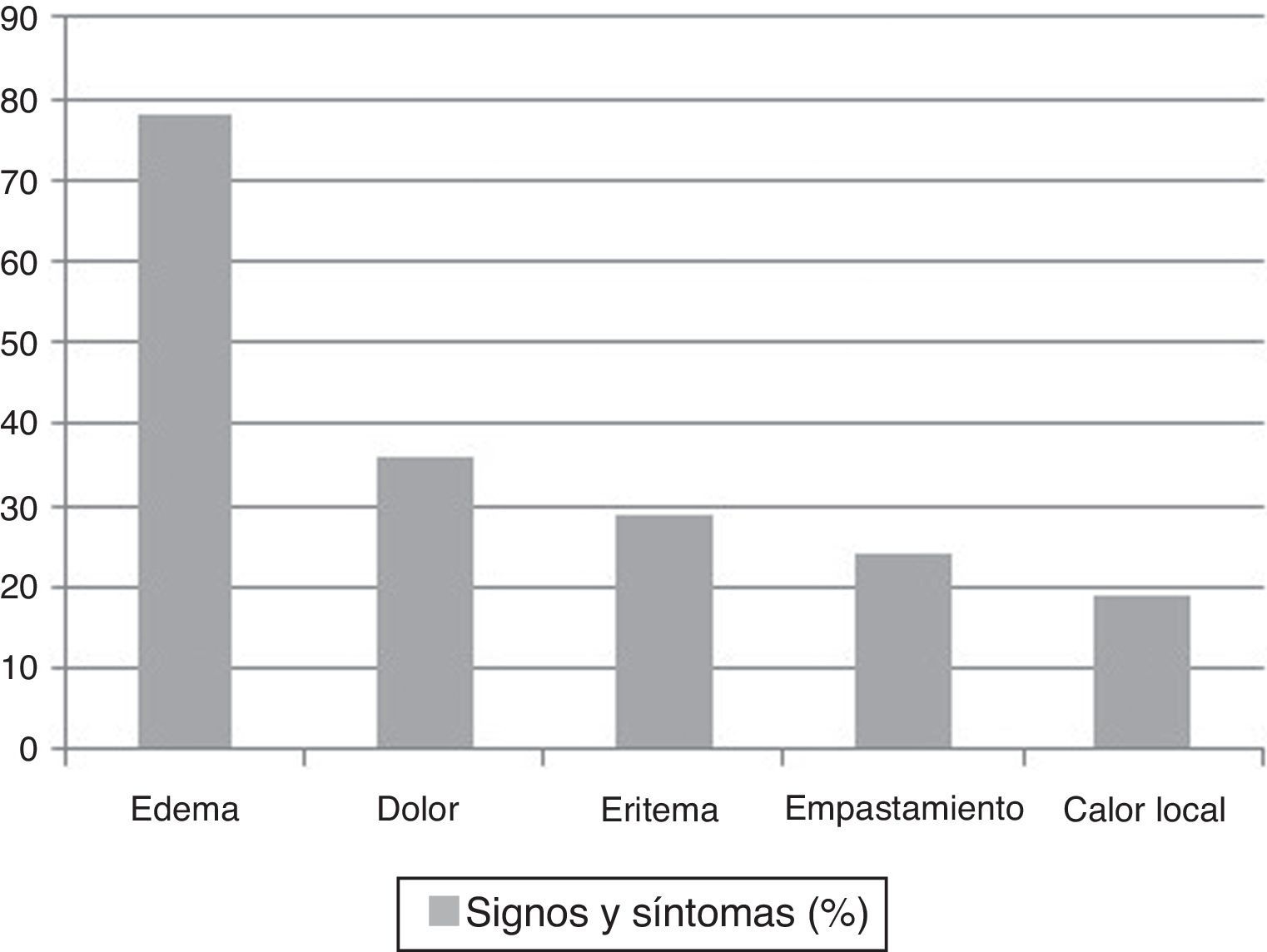
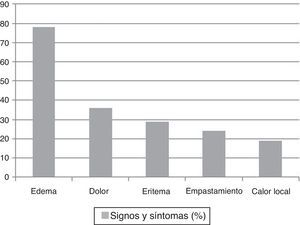
La tumefacción de la extremidad afecta fue el signo más frecuentemente observado en el momento de la visita inicial (79%) y este signo fue el único que se correlacionó con una confirmación diagnóstica en el análisis bivariante (p: 0,009). En la figura 1 se muestran el resto de signos y síntomas encontrados.
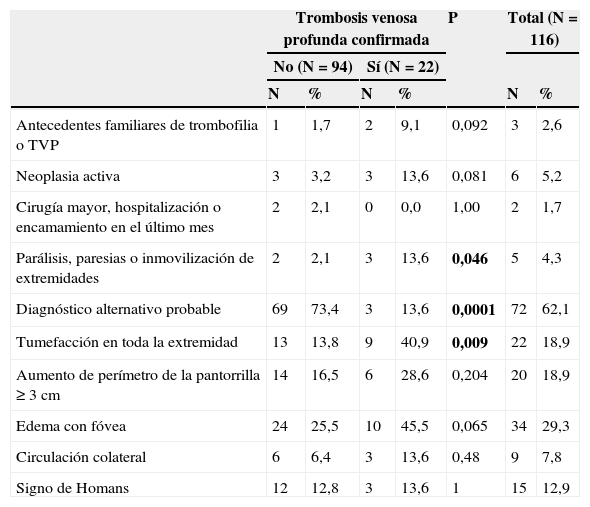
En la tabla 2 se describen los factores de riesgo de TVP utilizados por las principales escalas de probabilidad clínica18. El presentar un diagnóstico alternativo probable o el haber sufrido una inmovilización prolongada fueron los únicos factores de riesgo que, en nuestro estudio, se correlacionaron con el diagnóstico (p: 0,0001 y p: 0,046 respectivamente). En el caso del diagnóstico alternativo se correlacionó, de forma significativa, con la exclusión de la TVP. En la población estudiada no se encontró ningún paciente en tratamiento con anticonceptivos orales o que hubiera realizado un viaje largo reciente.
Distribución de factores de riesgo relacionados con el diagnóstico de trombosis venosa profunda
| Trombosis venosa profunda confirmada | P | Total (N=116) | |||||
|---|---|---|---|---|---|---|---|
| No (N=94) | Sí (N=22) | ||||||
| N | % | N | % | N | % | ||
| Antecedentes familiares de trombofilia o TVP | 1 | 1,7 | 2 | 9,1 | 0,092 | 3 | 2,6 |
| Neoplasia activa | 3 | 3,2 | 3 | 13,6 | 0,081 | 6 | 5,2 |
| Cirugía mayor, hospitalización o encamamiento en el último mes | 2 | 2,1 | 0 | 0,0 | 1,00 | 2 | 1,7 |
| Parálisis, paresias o inmovilización de extremidades | 2 | 2,1 | 3 | 13,6 | 0,046 | 5 | 4,3 |
| Diagnóstico alternativo probable | 69 | 73,4 | 3 | 13,6 | 0,0001 | 72 | 62,1 |
| Tumefacción en toda la extremidad | 13 | 13,8 | 9 | 40,9 | 0,009 | 22 | 18,9 |
| Aumento de perímetro de la pantorrilla ≥ 3cm | 14 | 16,5 | 6 | 28,6 | 0,204 | 20 | 18,9 |
| Edema con fóvea | 24 | 25,5 | 10 | 45,5 | 0,065 | 34 | 29,3 |
| Circulación colateral | 6 | 6,4 | 3 | 13,6 | 0,48 | 9 | 7,8 |
| Signo de Homans | 12 | 12,8 | 3 | 13,6 | 1 | 15 | 12,9 |
TVP: trombosis venosa profunda.
Los resultados resaltados en negrita indican signficación estadística.
En el 73% de los pacientes en los que la ecografía fue negativa se obtuvo un diagnóstico alternativo (principalmente un 39% presentaron otras causas vasculares como la tromboflebitis superficial o insuficiencia venosa crónica; 30% causa infecciosa como la celulitis y 27% causa traumatológica como las roturas fibrilares).
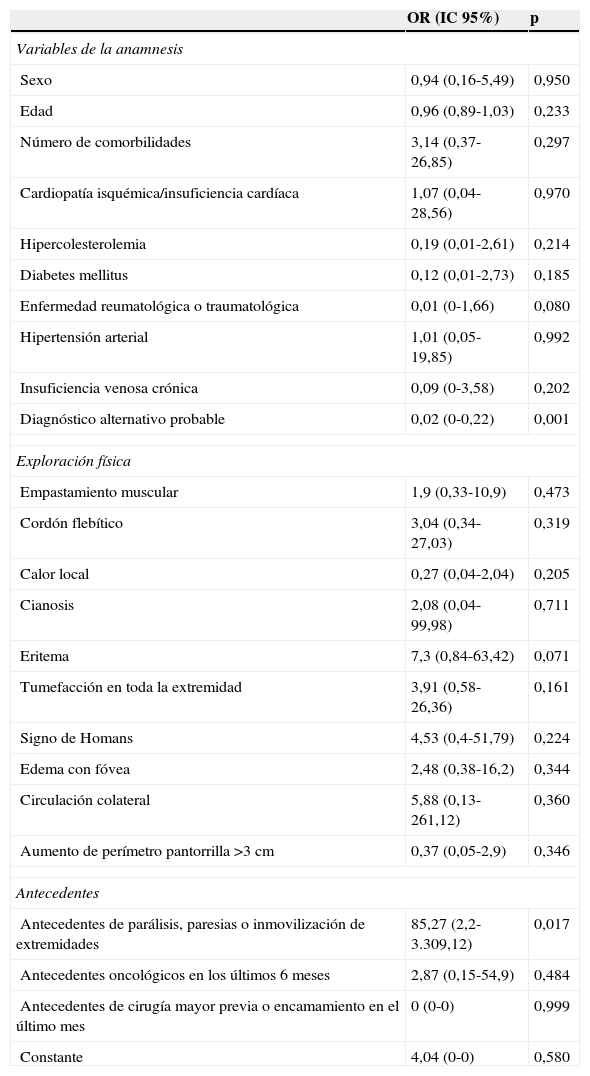
En el estudio multivariante (tabla 3) se confirmó la influencia de la presencia de diagnósticos alternativos probables (OR: 0,02; IC 95%: 0-0,22) y de los antecedentes de parálisis, paresias o inmovilización de las extremidades (OR: 85,27; IC 95%: 2,2-3.309,12) en la confirmación o la exclusión del diagnóstico de TVP. En cambio, las enfermedades del aparato locomotor y la tumefacción en toda la extremidad no tuvieron influencia en la probabilidad pretest del diagnóstico.
Análisis multivariante de las características relacionadas con la probabilidad de tener un diagnóstico confirmado de trombosis venosa profunda mediante ecodoppler
| OR (IC 95%) | p | |
|---|---|---|
| Variables de la anamnesis | ||
| Sexo | 0,94 (0,16-5,49) | 0,950 |
| Edad | 0,96 (0,89-1,03) | 0,233 |
| Número de comorbilidades | 3,14 (0,37-26,85) | 0,297 |
| Cardiopatía isquémica/insuficiencia cardíaca | 1,07 (0,04-28,56) | 0,970 |
| Hipercolesterolemia | 0,19 (0,01-2,61) | 0,214 |
| Diabetes mellitus | 0,12 (0,01-2,73) | 0,185 |
| Enfermedad reumatológica o traumatológica | 0,01 (0-1,66) | 0,080 |
| Hipertensión arterial | 1,01 (0,05-19,85) | 0,992 |
| Insuficiencia venosa crónica | 0,09 (0-3,58) | 0,202 |
| Diagnóstico alternativo probable | 0,02 (0-0,22) | 0,001 |
| Exploración física | ||
| Empastamiento muscular | 1,9 (0,33-10,9) | 0,473 |
| Cordón flebítico | 3,04 (0,34-27,03) | 0,319 |
| Calor local | 0,27 (0,04-2,04) | 0,205 |
| Cianosis | 2,08 (0,04-99,98) | 0,711 |
| Eritema | 7,3 (0,84-63,42) | 0,071 |
| Tumefacción en toda la extremidad | 3,91 (0,58-26,36) | 0,161 |
| Signo de Homans | 4,53 (0,4-51,79) | 0,224 |
| Edema con fóvea | 2,48 (0,38-16,2) | 0,344 |
| Circulación colateral | 5,88 (0,13-261,12) | 0,360 |
| Aumento de perímetro pantorrilla >3cm | 0,37 (0,05-2,9) | 0,346 |
| Antecedentes | ||
| Antecedentes de parálisis, paresias o inmovilización de extremidades | 85,27 (2,2-3.309,12) | 0,017 |
| Antecedentes oncológicos en los últimos 6 meses | 2,87 (0,15-54,9) | 0,484 |
| Antecedentes de cirugía mayor previa o encamamiento en el último mes | 0 (0-0) | 0,999 |
| Constante | 4,04 (0-0) | 0,580 |
La prevalencia de TVP determinada en nuestra muestra (18,9%) fue similar a la de estudios realizados en otros países. En un estudio prospectivo realizado en Suecia se observó una prevalencia de un 23,5%19 y en una revisión sistemática publicada en el 2011 la prevalencia osciló del 15 al 39%20 de la población estudiada, dependiendo de los subgrupos de edad. A pesar de que existe un estudio de características similares realizado en nuestro país en el que se observó un aumento de las TVP en mujeres3, en la mayoría de trabajos publicados, y en nuestra muestra, no se evidenciaron dichas diferencias21.
En nuestro estudio no detectamos una relación significativa entre las principales comorbilidades y el diagnóstico de TVP. La única comorbilidad que demostró una relación significativa con el diagnóstico final de TVP en el estudio bivariante fue la presencia de enfermedades del aparato locomotor, que fue más frecuente en los pacientes que presentaron una falsa sospecha. Dentro de este subgrupo de enfermedades se incluyó a pacientes con intervención traumatológica reciente, gonartrosis, meniscopatía, hernia discal, fibromialgia y enfermedades reumatológicas autoinmunes. El hecho de que con posterioridad no se confirmase esta correlación en el análisis multivariante es probablemente debido al tamaño de la muestra. Las comorbilidades más frecuentes detectadas, como la hipertensión, la diabetes y la hipercolesterolemia, no se asociaron con la presencia de TVP.
A diferencia de otros estudios, el único factor de riesgo que mostró una asociación estadísticamente significativa en el análisis bivariante con el diagnóstico de TVP fue el antecedente de inmovilización de extremidades inferiores22–24. Respecto a la clínica que referían los pacientes, los síntomas y signos más frecuentes fueron la tumefacción y el dolor, coincidiendo con otros estudios publicados25,26.
De todas las variables estudiadas, la única que se correlacionó con el diagnóstico de TVP, como factor protector, fue la presencia de un diagnóstico alternativo. Sin embargo, esta circunstancia es altamente subjetiva y está claramente determinada por la experiencia del clínico en esta enfermedad14.
Creemos que el aspecto más positivo de nuestro estudio es que está centrado en el diagnóstico en la Atención Primaria, el lugar donde más frecuentemente se generan las sospechas diagnósticas y donde existen menos recursos para poder orientar los casos. Este estudio puede aportar un mayor conocimiento sobre el perfil de los pacientes y los puntos clave que pueden orientar al clínico sobre la necesidad de derivación a un centro hospitalario.
Sin embargo, también existen limitaciones como la de que algún paciente, a pesar de haber sido derivado desde la Atención Primaria, decidiese voluntariamente no acudir al hospital o que fuese atendido en otro centro hospitalario público o privado diferente del hospital de referencia. Ello podría haber provocado una potencial pérdida de información que podría limitar la validez externa del estudio. No obstante, consideramos que este hecho es improbable debido a la elevada accesibilidad de las urgencias hospitalarias de referencia. Otra de las limitaciones del estudio podría ser la del pequeño tamaño muestral, que podría derivar en un mayor error beta.
Creemos que existe un elevado desconocimiento de esta enfermedad en la Atención Primaria y consideramos imprescindible una mejor formación. Una de las herramientas útiles son las escalas de probabilidad clínica, que pretenden determinar la probabilidad pretest de TVP para así ayudar al clínico en el proceso diagnóstico. Estas escalas también incluyen la evaluación de los variados diagnósticos diferenciales y la posibilidad de diagnósticos alternativos que son los que prácticamente nos descartarán la enfermedad. De hecho, este estudio pone de manifiesto que, si se construyera una nueva escala de probabilidad clínica en nuestro entorno, probablemente algunos de los ítems incluidos no tendrían el mismo peso específico que tienen en la actualidad, como es el caso del diagnóstico alternativo probable.
Por todo ello, creemos que es imprescindible la formación y el conocimiento por parte del clínico de esta enfermedad y de sus herramientas diagnósticas para poder llegar a un correcto manejo de la TVP.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
FinanciaciónEste trabajo ha recibido 2 becas XB de investigación de la Gerencia del Ámbito de Atención Primaria de Barcelona Ciudad del Institut Català de la Salut (XB 2011 y XB 2012) y ha estado financiado por Laboratorios Sanofi para la realización de las pruebas complementarias.
Conflicto de interesesLos autores declaran que no existe conflicto de intereses.
Parte de este trabajo ha sido presentada en el Congreso de la semFYC (Sociedad Española de Medicina Familiar y Comunitaria) en Gran Canaria, del 12 al 14 de junio de 2014.