El tratamiento de la isquemia crítica de la extremidad involucra un bypass o terapia endovascular. Ya se han desarrollado herramientas para predecir la sobrevida libre de amputación, como PREVENT-III, que ha demostrado su utilidad únicamente en injertos autógenos.
ObjetivoDemostrar la aplicabilidad de PREVENT-III con injerto no autógeno.
Material y métodosSe revisaron 87 expedientes de pacientes tratados mediante bypass infragenicular entre marzo de 2011 y marzo de 2013. Un total de 40 pacientes reunieron los criterios de inclusión; se calculó su puntuación PREVENT-III, se anotó el tipo de injerto utilizado, comorbilidades y su sobrevida libre de amputación a 12 meses.
ResultadosSe incluyó a 40 pacientes, con media de edad de 68,4±9 años (47-90), 19 mujeres y 21 hombres. Las comorbilidades fueron diabetes mellitus (n=28; 70%), tabaquismo suspendido (n=24), hipertensión arterial sistémica (n=19), tabaquismo activo (n=11), angina o infarto cardiaco previo (n=8), tabaquismo negado (n=5), hipercolesterolemia (n=4), dislipidemia mixta (n=4), y ningún paciente tuvo enfermedad renal crónica. Se utilizó injerto sintético (n=27; 67,5%) e injertos compuestos (n=13). Fueron tratados mediante amputación mayor 7 pacientes (3 sintéticos+4 compuestos) con riesgo bajo, y 8 (6 sintéticos+2 compuestos) con riesgo moderado (p = 0,062). Al subdividir los grupos, 9 (3 riesgo bajo+6 moderado) con injerto sintético fueron amputados (p = 0,034), y 6 con compuesto (4 riesgo bajo+2 moderado) (p = 0,0657).
ConclusionesLa escala PREVENT-III es aplicable con injerto sintético, sin embargo, el comportamiento en presencia de injerto compuesto es errático.
Treating critical limb ischemia involves a bypass or endovascular therapy. Tools, such as PREVENT-III have been developed to predict amputation-free survival, but their usefulness has only been demonstrated in autologous grafts.
ObjectiveTo demonstrate the applicability of PREVENT-III with non-autologous grafts.
Material and methodsA study was conducted on 87 cases of patients who underwent below-knee bypass between March 2011 and March 2013. Of the 40 patients that met the inclusion criteria, the PREVENT-III score, the type of graft used, comorbidity, and survival free of amputation at 12 months, were recorded.
ResultsThe 40 patients included had a mean age of 68.4±9 years (47-90), and there were 19 women and 21 men. Comorbidities were diabetes mellitus (n=28; 70%), ex-smoker (n=24), systemic hypertension (n=19), active smoking (n=11), angina or history of myocardial infarction (n=8), non-smokers (n=5), hypercholesterolemia (n=4), hypercholesterolemia+hypertriglyceridemia (n=4), and with no patients with end stage renal disease. Synthetic grafts were used in (n=27; 67.5%) and composite grafts in (n=13). Major amputation was performed on 7 low risk patients (3 synthetic+4 composite), and 8 moderate risk patients (6 synthetic+2 composite) (P=.062). By dividing into sub-groups, 9 (3 moderate+6 low risk) with synthetic graft were amputees (P=.034), and 6 with composite (4 moderate+2 low risk) (P=.0657)
ConclusionsThe PREVENT-III can be applied to synthetic grafts; however, the behavior in the presence of composite graft is erratic.
Se estima que una persona que puede deambular una distancia de 70 m, puede tener una vida dentro de la normalidad1. La enfermedad arterial oclusiva periférica o isquémica crónica de la extremidad genera limitación funcional2 por una obstrucción al flujo que consecuentemente disminuye el aporte de nutrientes en los tejidos ocasionando isquemia crónica3 que, de progresar, puede manifestarse como isquemia crítica de la extremidad (ICE), que se caracteriza por una pérdida de tejido, gangrena o dolor de la extremidad en reposo que no cede con la administración de analgésicos. La diabetes mellitus incrementa el riesgo de desarrollar ICE en 2 o 3 veces4. Parte de su tratamiento incluye los procedimientos de bypass (cirugía convencional) y la terapia endovascular5, con la finalidad de aliviar el dolor, cicatrizar las úlceras isquémicas, prevenir la pérdida de la extremidad, mejorar el estado funcional y la calidad de vida de los pacientes6.
La derivación vascular por debajo de la rodilla con vena safena invertida continúa siendo el mejor tratamiento para el salvamento de la extremidad7–10.
No existe un consenso sobre qué injerto es el mejor cuando no se tiene disponible la vena safena, pero el politetrafluoroetileno expandido con o sin la utilización de parches venosos se utiliza en la mayoría de los casos desde hace 40 años11. Una alternativa diferente para los injertos son los compuestos, que fueron utilizados por primera vez por McCaughan en 1961 y por Linton en 197312.
Para el paciente que ha sido diagnosticado con ICE, las probabilidades de padecer una amputación mayor son muy altas y su sobrevida es de solo el 26,7% a 5 años si solo recibe tratamiento médico13,14.
Cuando falla el injerto en los pacientes con ICE se genera morbilidad, pérdida de la extremidad y consumo adicional de recursos, generando un costo aproximado anual de 3.100.000.000 dólares en los Estados Unidos15, que supone un importante impacto en el presupuesto asignado a los sistemas de salud, no solo de Estados Unidos, sino del mundo.
La estatificación del riesgo ha adquirido mucha importancia en los pacientes con ICE8, ya que la predicción sirve para una mejor toma de decisión por parte del médico, planeación de utilización de recursos, comparación entre instituciones o cirujanos y para proveer al paciente información sobre su riesgo16.
Actualmente existen en la literatura sistemas de puntación para asignar un pronóstico de riesgo de amputación posterior a un procedimiento de derivación vascular, como la puntuación PREVENT-III17, que ya ha demostrado su utilidad en poblaciones heterogéneas8. Desafortunadamente, no existe en la literatura ningún antecedente de la utilidad de esta herramienta en pacientes tratados mediante bypass infragenicular con injertos sintéticos o compuestos.
ObjetivoDemostrar la aplicabilidad de la escala PREVENT-III en pacientes con ICE tratados mediante derivación vascular infragenicular con injerto sintético o compuesto.
Material y métodosSe realizó un estudio observacional, analítico, transversal y retrospectivo, que se llevó a cabo mediante la recolección de datos de los archivos clínicos de los pacientes tratados mediante bypass infragenicular por ICE, con injerto sintético o compuesto entre marzo del 2011 y marzo del 2013 en el Departamento de Angiología y Cirugía Vascular del Hospital de Cardiología, Unidad Médica de Alta Especialidad No. 34 (UMAE No. 34), un centro médico especializado en enfermedades cardiovasculares y del tórax localizado en el noreste de México, en la ciudad de Monterrey, en el estado de Nuevo León, que pertenece al Instituto Mexicano del Seguro Social.
Se tomaron en cuenta como criterios de inclusión para el estudio los expedientes de hombres y mujeres con más de 18 años de edad, con diagnóstico clínico de ICE (Fontaine III-IV) o claudicación incapacitante (Fontaine IIB) y que hubieran sido tratados mediante una derivación vascular infragenicular con injerto sintético o compuesto. Como criterios de exclusión se tomaron en cuenta datos incompletos en expediente clínico o diagnóstico de enfermedades autoinmunes, y de eliminación el haber amputado por causas no asociadas a ICE o haber sido reintervenido.
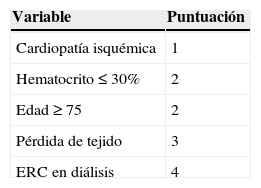
Sistema de puntuación PREVENT-IIIEs una escala pronóstica de amputación a un año posterior a derivación vascular infragenicular, mediante la asignación de una puntuación, que es otorgada por la sumatoria de la presencia de diálisis=4 puntos, pérdida de tejido=3 puntos, edad ≥ 75 años=2 puntos, hematocrito ≤ 30%=2 puntos, cardiopatía isquémica=1 punto, quedando como riesgo bajo los pacientes con ≤ 3puntos, riesgo moderado con 4-7puntos y con riesgo alto si ≥ 8puntos con un porcentaje de riesgo de amputación de 14, 27 y 55% a un año respectivamente17 (tabla 1).
DesarrolloSe analizaron de manera retrospectiva los expedientes, recopilando de estos, 1) género, 2) edad, 3) estadio clínico de Fontaine, 4) resultado de biometría hemática de ingreso, 5) tipo de injerto, 6) sobrevida libre de amputación mayor a 12 meses, 7) antecedentes o no de reintervención de cualquier tipo y 8) las comorbilidades asociadas: hipertensión arterial sistémica, cardiopatía isquémica, tabaquismo, diabetes mellitus, dislipidemia, enfermedad renal crónica y enfermedades autoinmunes. Al contar con todos los datos, a los pacientes que reunieron los criterios de inclusión se les calculó el PREVENT-III y se investigó la sobrevida libre de amputación a 12 meses.
Todos los pacientes acudieron a nuestra unidad hospitalaria de manera espontánea o referidos de un 2.° o 1.er nivel de atención médica con diagnóstico de ICE. Se les realizó una arteriografía con técnica de sustracción digital con arco fijado a techo (Artis Zee, Siemens®) y, a partir de los hallazgos angiográficos, previa sesión médico-quirúrgica colegiada, se decidió si el paciente era candidato a un bypass o a tratamiento endovascular. Todos los injertos sintéticos fueron de politetrafluoroetileno expandido de configuración recta con paredes regulares y con soporte externo anillado de 6 × 700mm, que posteriormente era ajustado a las necesidades de longitud de cada paciente. Todos los pacientes recibieron de manera rutinaria desde el momento del diagnóstico e indefinidamente antiagregación plaquetaria (ácido acetilsalicílico 150mg VO c/24h), estatinas (pravastatina 40mg VO c/24h) y un vasodilatador (cilostazol 100mg/VO c/12h), así como control estricto de comorbilidades y factores de riesgo cardiovascular.
Análisis estadísticoSe ingresaron y procesaron los datos recolectados en el programa para análisis estadístico IBM - SPSS Statistics No. 20 Se realizó el análisis descriptivo mediante las medidas de tendencia central y análisis de variables nominales mediante tablas de contingencia y estadística inferencial.
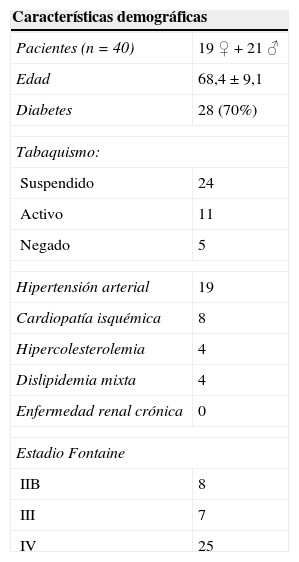
ResultadosSe analizaron un total de 87 expedientes; de ese total, 44 pacientes recibieron un injerto autógeno y 3 fueron excluidos por haber sido reintervenidos. Se logró admitir al estudio una muestra total de 40 pacientes que reunieron los criterios de inclusión. Del total de la muestra incluida, la media de edad de los pacientes fue de 68,4±9,1 años (47-90), 19 pacientes fueron mujeres y 21 fueron hombres. Las comorbilidades asociadas fueron diabetes mellitus (n=28 pacientes; 70%), tabaquismo suspendido (n=24), hipertensión arterial sistémica (n=19), tabaquismo activo (n=11), angina o infarto cardiaco previo (n=8), tabaquismo negado (n=5), hipercolesterolemia (n=4), dislipidemia mixta (n=4), y ningún paciente tuvo enfermedad renal crónica (tabla 2).
Características clínicas de pacientes
| Características demográficas | |
|---|---|
| Pacientes (n=40) | 19 ♀+21 ♂ |
| Edad | 68,4±9,1 |
| Diabetes | 28 (70%) |
| Tabaquismo: | |
| Suspendido | 24 |
| Activo | 11 |
| Negado | 5 |
| Hipertensión arterial | 19 |
| Cardiopatía isquémica | 8 |
| Hipercolesterolemia | 4 |
| Dislipidemia mixta | 4 |
| Enfermedad renal crónica | 0 |
| Estadio Fontaine | |
| IIB | 8 |
| III | 7 |
| IV | 25 |
En la clasificación clínica de Fontaine, 25 pacientes (62,5%) tenían Fontaine IV, 8 un F-IIB y 7 F-III. Se catalogó, según el PREVENT-III en riesgo moderado a 14 pacientes y como riesgo bajo a 26 de los casos. Ningún paciente presentó riesgo alto.
El injerto sintético se utilizó en un total de 27 pacientes (67,5%) y, de injertos compuestos, la muestra fue de 13. Quince pacientes fueron amputados, 7 (3 sintéticos y 4 compuestos) fueron de riesgo bajo, y 8 (6 sintéticos y 2 compuestos) de riesgo moderado (p = 0,062). Al subdividir los grupos, en el grupo sintético 9 pacientes fueron amputados 3 de riesgo bajo y 6 de moderado (p = 0,034), y del grupo compuesto 6 pacientes (n=4; 66,6% con riesgo bajo y n=2; 33,3% moderado; p = 0,065) (tabla 3).
DiscusiónLa ICE genera un alto riesgo de amputación mayor a corto y mediano plazo9,13. La terapia con mejor efectividad actualmente sigue siendo la derivación vascular. Sin embargo, una mala evolución posterior a una derivación vascular genera gran morbilidad, pérdida de las extremidades y consumo importante adicional de recursos. De ahí que la estatificación del riesgo de amputación sea importante para una mejor toma de decisión médica, planeación de utilización de recursos, comparación entre instituciones o cirujanos y para facilitar al paciente un pronóstico de su enfermedad.
El sistema de puntuación PREVENT-III es una herramienta fácilmente reproducible y constituye una escala valiosa para ofrecer un pronóstico a mediano plazo a los pacientes que son tratados mediante una revascularización infragenicular, sin embargo, su utilidad únicamente había sido probada en injertos autógenos. Hasta esta fecha no se contaba, dentro de nuestro conocimiento, con ningún reporte en la literatura que demostrara su aplicabilidad en una población donde se utilizan distintos tipos de injertos. Más aún, que demostrara su utilidad en nuestra población.
Cabe señalar que el presente estudio no involucró ningún caso que reuniera los criterios de inclusión con un riesgo de PREVENT-III alto, destacando que según el protocolo de intervención de nuestro departamento y las características clínicas de la gran mayoría de este tipo de casos, la terapia quirúrgica de elección que se aplica a estos pacientes es una intervención endovascular como se comentó previamente, lo que distancia a esta población de los objetivos del presente estudio.
Consideramos importante hacer mención de que nuestra población de pacientes con enfermedad oclusiva periférica presenta una incidencia de diabetes mellitus en el 74,4% de los casos, mayor al 50% reportado en la literatura4. Desafortunadamente, esta entidad ha demostrado que empeora el pronóstico de sobrevida libre de amputación18. A pesar de ello, los resultados mostrados en nuestra población de sobrevida libre de amputación a un año (72%) son muy similares a los reportados en la literatura. La supervivencia de los pacientes al concluir un año después de su intervención quirúrgica fue de un 80,5%, porcentaje muy similar al encontrado en otras poblaciones19–21.
Otro punto a considerar es que el 86,6% de los pacientes que fueron tratados mediante una derivación infragenicular se encontraban en ICE, 69,5% en estadio Fontaine-IV y 17,1% en estadio Fontaine-III, que refleja nuestro apego a los criterios internacionales para que un paciente sea intervenido quirúrgicamente22.
Con base en los hallazgos del presente estudio, se puede considerar que la escala pronóstica PREVENT-III puede ser aplicada a nuestra población de pacientes tratados mediante una derivación vascular infragenicular, ya que se corroboró que, a mayor riesgo dentro de la escala PREVENT-III, mayores son las probabilidades de padecer una amputación en un año posterior a la cirugía, según las validaciones previas de la escala PREVENT-III8,16.
Si se analizan nuestros datos según el tipo de injerto utilizado y la escala de puntuación PREVENT-III, la tendencia de la aplicabilidad de la escala se mantiene en los pacientes con injerto autógeno como lo referenciado en la literatura8. Adicionalmente encontramos que también es aplicable cuando se utiliza un injerto sintético.
Referente al injerto compuesto, se encontró nula aplicabilidad de la escala PREVENT-III, por presentar mayor número de amputaciones en grupo con menor riesgo (60% en riesgo bajo vs. 40% en riesgo moderado). Consideramos que una de las razones para este hallazgo fue la escasa población con injerto compuesto. Lo anterior es consecuencia de que un número muy reducido de casos que se atendieron carecían de un injerto autógeno, requerían de un injerto con una longitud mayor a los injertos sintéticos comercializados, o su anastomosis distal se realizaba a vasos de muy pequeño calibre (arteria peronea, tibial anterior o tibial posterior). Generalmente este tipo específico de población, de acuerdo a la literatura, presenta un cuadro clínico muy avanzado y severo, lo que conlleva un mayor riesgo de oclusión de injerto y de amputación temprana23–30. En estos pacientes la terapia más utilizada en nuestro departamento es una intervención endovascular. Quizá, de incrementarse la muestra de la población con injerto compuesto, podría corroborarse la utilidad de PREVENT-III, o bien descartarse debido a un comportamiento del injerto completamente diferente por contar con una estructura de 2 materiales diferentes o por el sitio de anastomosis.
ConclusionesEl sistema de puntuación PREVENT-III es una herramienta fácilmente reproducible y constituye una escala valiosa para ofrecer un pronóstico a mediano plazo a los pacientes que son tratados mediante una revascularización infragenicular. Sin embargo, a la fecha no se cuenta, dentro de nuestro conocimiento, con ningún reporte en la literatura que demuestre su aplicabilidad en pacientes en los que fue utilizado un injerto sintético o compuesto. Basándonos en los resultados del presente trabajo y en los antecedentes de la literatura16,17, podemos concluir que la escala PREVENT-III es aplicable a los pacientes que son tratados mediante un bypass infragenicular con injerto sintético y autógeno, ya que los pacientes con injerto compuesto no muestran un patrón de predicción de amputación acorde a su riesgo de PREVENT-III.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
XLVI Congreso Nacional de Angiología y Cirugía Vascular, del 28 de octubre al 1.° de noviembre del 2014, Guadalajara, Jalisco, México.