Puntos clave
- •
El lupus eritematoso sistémico (LES) es una enfermedad autoinmune crónica con afectación multisistémica y presencia de autoanticuerpos.
- •
El diagnóstico es improbable si los anticuerpos antinucleares son negativos.
- •
Los síntomas constitucionales, la artritis y el exantema malar son habituales al debut en niños y jóvenes.
- •
La afectación renal y neurológica inicial o acumulada se consideran más frecuentes en el LES de inicio pediátrico que en el del adulto, aunque es posible que factores socioeconómicos y casos leves no diagnosticados actúen como factores de confusión en los estudios.
- •
El daño orgánico lo favorecen la enfermedad y los fármacos.
- •
Tiene una evolución impredecible con recaídas y remisiones.
- •
Para optimizar el tratamiento es preciso conocer las diferentes opciones terapéuticas y las necesidades específicas de la adolescencia.
El lupus eritematoso sistémico (LES) es una enfermedad autoinmune con morbilidad y mortalidad significativas, que se caracteriza por afectar a cualquier sistema del organismo y por la presencia de autoanticuerpos. El diagnóstico debe ser considerado en los pacientes con enfermedad multisistémica y anticuerpos antinucleares (ANA) positivos. Su forma de comienzo es variable desde casos leves con exantema facial y artritis, a casos muy graves en los que existe riesgo para la vida. Tiene un curso intermitente, con periodos de actividad seguidos por otros de remisión. El objetivo del tratamiento es controlar el trastorno inmunológico y evitar la actividad y el subsiguiente daño orgánico, del que son responsables tanto los fármacos como la propia enfermedad1.
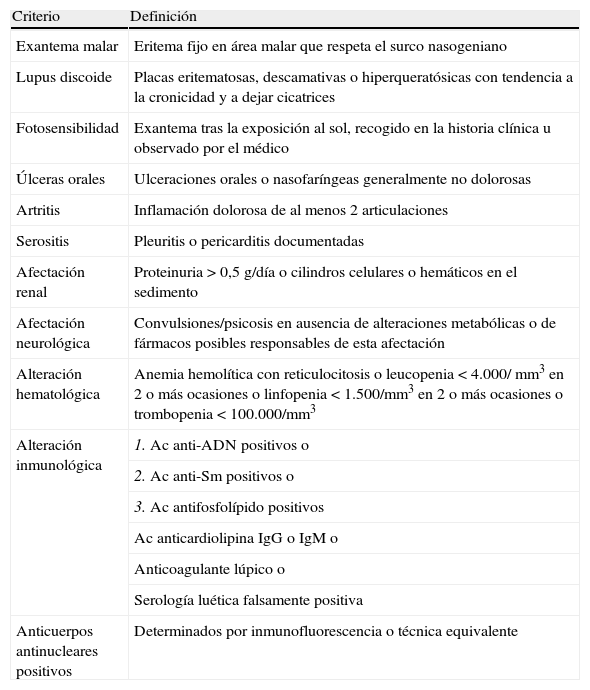
Criterios de clasificaciónEn 1971 la American College of Rheumatology (ACR) definió un sistema de clasificación para el LES, que posteriormente ha sido modificado (tabla 1)2,3. Para clasificar a un paciente son necesarios 4 de los 11 criterios y, aunque no se trata de criterios diagnósticos, más del 90% de los casos los cumplen al ser diagnosticados
Lectura rápida
El lupus eritematoso sistémico (LES) es una enfermedad autoinmune que se caracteriza por afectar a cualquier sistema orgánico y por la presencia de autoanticuerpos. Cursa con periodos de actividad seguidos por otros de remisión y puede ser leve o muy grave.
Se trata de una inflamación de los vasos sanguíneos y el tejido conectivo, atribuida a una combinación de susceptibilidad genética y factores ambientales.
El mecanismo patogénico lo desencadenan anomalías en el aclaramiento del material de deshecho tras la apoptosis. Este material contiene autoantígenos, ausentes en los individuos sanos, que inducen la producción de autoanticuerpos. La diversidad de alteraciones inmunológicas ha permitido identificar nuevas dianas terapéuticas, entre ellas se encuentran las células B.
La American College of Rheumatology (ACR) definió un sistema de clasificación, que incluye los siguientes criterios: exantema malar, lupus discoide, fotosensibilidad, úlceras orales, artritis, serositis, citopenia, afectación renal, neurológica o inmunológica, y anticuerpos antinucleares positivos. Para clasificar a un paciente son necesarios 4 de los 11 criterios. Se ha comprobado que la mayoría los reúnen al diagnóstico.
La incidencia de LES pediátrico (LESp) es inferior a 1/100.000/ niños/año y la prevalencia de unos 3,5/100.000/ niños. Tiene preferencia por el sexo femenino (5 niñas por cada varón).
Al comienzo de la enfermedad las más frecuentes son: artritis, exantema malar, cefalea, alteración hematológica, cansancio y glomerulonefritis. A su vez, la afectación acumulada hematológica, musculoesquelética, renal y neurológica alcanza el 91, el 82, el 80 y el 26% a los 5 años de evolución.
Se realiza con las infecciones víricas, las infecciones bacterianas, los procesos malignos y algunas enfermedades inflamatorias.
Las descritas con mayor frecuencia son las infecciones, el síndrome de activación del macrófago y la ateroesclerosis prematura.
Desde los años noventa es del 90% a los 10 años de evolución. Se ha observado que el LESp tiene un curso más agresivo que el de comienzo en adultos, aunque el nivel socioeconómico y la posibilidad de que casos leves no diagnosticados queden excluidos de los estudios, pueden actuar como factores de confusión.
En el primer año, las causas de defunción se relacionan con la actividad lúpica y las infecciones, mientras que la mortalidad tardía lo hace con las infecciones, el fracaso renal, la enfermedad cardiovascular por ateroesclerosis y los tumores, sobre todo con el linfoma.
El objetivo es controlar el trastorno inmunológico y evitar el daño orgánico. Consta de 2 fases: a) inducción de la remisión, y b) mantenimiento de la misma. La aproximación clásica utiliza: antimaláricos, glucocorticoides e inmunosupresores. La ciclofosfamida fue durante años de elección para la inducción de remisión en las manifestaciones más graves, aunque hoy algunos autores prefieren administrar micofenolato mofetilo (MMF). El mantenimiento se realiza con azatioprina o MMF.
Recientemente, se han incorporado rituximab y belimumab, que se usan asociados a los anteriores y cuya diana terapéutica es la célula B.
Incluye recomendaciones variadas: protección solar, hábitos de vida saludables, adecuada nutrición, suplementos de calcio y vitamina D, ejercicio y reposo equilibrados, administración de vacunas recombinantes o de virus muertos, incluida la anual de la gripe y seguimiento en un centro especializado. Asimismo es de interés evitar un embarazo no deseado y conocer los posibles riesgos de agudización de la enfermedad durante la gestación y de LES neonatal. La gestación en una paciente con LES debe ser rigurosamente controlada. Por último, la transición a un servicio de adultos tiene que ser cuidadosa y evitar la sensación de desamparo.
Criterios de clasificación de lupus eritematoso sistémico
| Criterio | Definición |
| Exantema malar | Eritema fijo en área malar que respeta el surco nasogeniano |
| Lupus discoide | Placas eritematosas, descamativas o hiperqueratósicas con tendencia a la cronicidad y a dejar cicatrices |
| Fotosensibilidad | Exantema tras la exposición al sol, recogido en la historia clínica u observado por el médico |
| Úlceras orales | Ulceraciones orales o nasofaríngeas generalmente no dolorosas |
| Artritis | Inflamación dolorosa de al menos 2 articulaciones |
| Serositis | Pleuritis o pericarditis documentadas |
| Afectación renal | Proteinuria > 0,5g/día o cilindros celulares o hemáticos en el sedimento |
| Afectación neurológica | Convulsiones/psicosis en ausencia de alteraciones metabólicas o de fármacos posibles responsables de esta afectación |
| Alteración hematológica | Anemia hemolítica con reticulocitosis o leucopenia < 4.000/ mm3 en 2 o más ocasiones o linfopenia < 1.500/mm3 en 2 o más ocasiones o trombopenia < 100.000/mm3 |
| Alteración inmunológica | 1. Ac anti-ADN positivos o |
| 2. Ac anti-Sm positivos o | |
| 3. Ac antifosfolípido positivos | |
| Ac anticardiolipina IgG o IgM o | |
| Anticoagulante lúpico o | |
| Serología luética falsamente positiva | |
| Anticuerpos antinucleares positivos | Determinados por inmunofluorescencia o técnica equivalente |
Ac: anticuerpos; Ig: inmunoglobulina.
El LES es una inflamación de los vasos sanguíneos y del tejido conectivo, atribuida a la combinación de susceptibilidad genética y factores ambientales. Estos últimos incluyen la exposición a la luz solar (radiación ultravioleta), el fenotipo hormonal (mayor frecuencia en sexo femenino) y algunas infecciones víricas (virus herpes y virus de Epstein-Barr). No hay evidencia de que el parvovirus B19 predisponga a la enfermedad; en cambio, mimetiza sus manifestaciones clínicas. Además, algunos fármacos (hidralacina e isoniazida, entre otros) y productos químicos, como la L-canavanina, están relacionados con el comienzo.
Se considera que el mecanismo patogénico lo desencadenan anomalías en el aclaramiento del material de deshecho tras la apoptosis. Ese material contiene autoantígenos, ausentes en los individuos sanos, que inducen la producción de autoanticuerpos, el depósito de inmunocomplejos y el daño orgánico4. Los trabajos de laboratorio en modelos animales han demostrado alteraciones inmunológicas diversas, lo que ha permitido la identificación de nuevas dianas terapéuticas, entre las que se encuentran las células B5.
EpidemiologíaLa incidencia del LES pediátrico (LESp) oscila de 0,3 a 0,9 por 100.000 niños al año y la prevalencia es de aproximadamente 3,5 por cada 100.000 niños6. Supone el 20% del total de los lupus y la edad media de comienzo ronda los 12 años, siendo excepcional en menores de 5 años. Tiene preferencia por el sexo femenino, comprometiendo a unas 5 niñas por cada varón, mientras que en el LES adulto la relación entre mujeres y hombres es de 10:1. Por otra parte, en el LESp se ha descrito un curso más severo7 y en las razas no caucásicas mayor gravedad8.
Manifestaciones clínicasLa variabilidad clínica se explica por la posible afectación de cualquier órgano o sistema. En un estudio en 256 niños las manifestaciones más frecuentes al comienzo de la enfermedad fueron: artritis, exantema malar, cefalea, alteración hematológica, cansancio y glomerulonefritis (GN)9. A su vez, los resultados de una serie de pacientes seguidos una media de 4,5 años mostraron afectación hematológica acumulada en el 91% de los casos, musculoesquelética en el 82%, renal en el 80% y neurológica en el 26%10.
Síntomas constitucionalesConsisten en fiebre, pérdida de peso, cansancio y anorexia. Se observan en al menos la mitad de los LESp al inicio. La hepatoesplenomegalia y las adenomegalias ocurren en alrededor de la tercera parte de los pacientes con enfermedad activa.
Alteraciones mucocutáneasLa tabla 2 especifica las más habituales. El exantema en la cara «en alas de mariposa» es característico y lo presentan más del 60%. Es un eritema fijo y fotosensible, que suele incluir las prominencias malares, el puente nasal e incluso los pabellones auriculares y la barbilla, respetando el surco nasogeniano. Cura sin secuelas, a diferencia del lupus discoide, que deja cicatrices atróficas, y, aunque infrecuente en la infancia, se debe reconocer y diferenciar de la tiña en el cuero cabelludo. Las manifestaciones mucosas son úlceras orales y nasales, en general indoloras.
Alteraciones musculoesqueléticasLa artritis, sobre todo en rodillas y en articulaciones pequeñas de las manos, así como las artralgias (dolor articular sin signos inflamatorios) son frecuentes. Las artralgias podrían ser secundarias a un síndrome de amplificación del dolor11. En cuanto a la osteoporosis y la necrosis avascular, son afecciones tardías relacionadas con los glucocorticoides (GC). La miositis cursa con dolor, debilidad muscular y aumento de la creatincinasa y es signo de actividad.
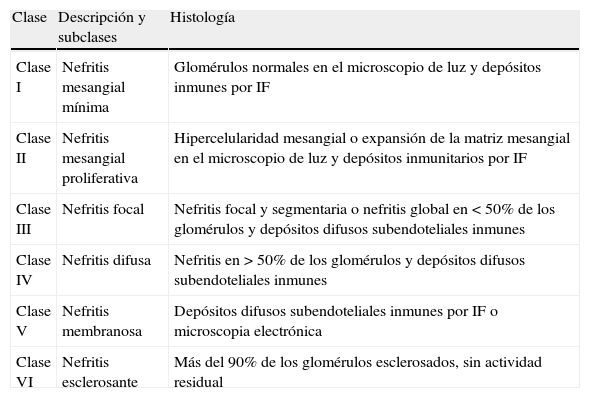
Afectación renalIncluye desde mínima proteinuria hasta proteinuria en rango nefrótico, hematuria, cilindruria, insuficiencia renal e hipertensión arterial. La clasificación estandarizada de la GN lúpica se muestra en la tabla 312Las GN de clases III y IV se han subdividido en función del grado de actividad (hipercelularidad, trombos hialinos e infiltrado intersticial) y de cronicidad (atrofia, fibrosis, esclerosis glomerular y esclerosis intersticial), lo que tiene interés pronóstico y terapéutico. La mayoría de los LESp con participación renal presentan GN de clase IV y un riesgo elevado de progresión a insuficiencia renal terminal (IRT)13.
Clasificación de la nefritis lúpica.
| Clase | Descripción y subclases | Histología |
| Clase I | Nefritis mesangial mínima | Glomérulos normales en el microscopio de luz y depósitos inmunes por IF |
| Clase II | Nefritis mesangial proliferativa | Hipercelularidad mesangial o expansión de la matriz mesangial en el microscopio de luz y depósitos inmunitarios por IF |
| Clase III | Nefritis focal | Nefritis focal y segmentaria o nefritis global en < 50% de los glomérulos y depósitos difusos subendoteliales inmunes |
| Clase IV | Nefritis difusa | Nefritis en > 50% de los glomérulos y depósitos difusos subendoteliales inmunes |
| Clase V | Nefritis membranosa | Depósitos difusos subendoteliales inmunes por IF o microscopia electrónica |
| Clase VI | Nefritis esclerosante | Más del 90% de los glomérulos esclerosados, sin actividad residual |
IF: inmunofluorescencia
Afecta al sistema nervioso central y al sistema nervioso periférico (tabla 4). La frecuencia del neurolupus en las series es desigual, oscilando entre el 10 y el 90%, lo que se atribuye a que síntomas como la cefalea, el trastorno del carácter o la ansiedad, a veces se consideran secundarias al LES y otras no. El problema persiste a pesar de que la ACR propuso unas definiciones de los síndromes neuropsiquiátricos para facilitar la investigación clínica y ser una guía práctica14. La alteración neurológica hay que distinguirla de las infecciones, la meningitis aséptica y de los procesos psiquiátricos primarios.
Alteraciones neuropsiquiátricas del lupus eritematoso sistémico.
| Sistema nervioso central |
| Cefalea |
| Meningitis aséptica |
| Enfermedad cerebrovascular |
| Accidente cerebrovascular |
| Ataque isquémico transitorio |
| Hemorragia |
| Trombosis |
| Enfermedad desmielinizante |
| Mielitis transversa |
| Movimientos anómalos |
| Corea |
| Convulsiones |
| Manifestaciones psiquiátricas |
| Ansiedad |
| Psicosis |
| Deterioro cognitivo (memoria, atención) |
| Trastorno del carácter (depresión, manía) |
| Confusión (delirio, encefalopatía) |
| Sistema nervioso periférico |
| Mononeuritis simple/múltiple |
| Polineuritis sensorial/motora |
| Guillain-Barré |
| Miastenia gravis |
La serositis (pericarditis y/o pleuritis) aparece en menos de un tercio de los casos y asocia un aumento importante de la proteína C reactiva (PCR). La miocarditis, la endocarditis, la neumonía intersticial, la hemorragia pulmonar y el pulmón menguante son infrecuentes.
Afectación digestivaEl dolor abdominal casi siempre es la consecuencia de una serositis abdominal y menos veces de pancreatitis15.
Manifestaciones vascularesEn la piel se observa vasculitis en forma de pequeños nódulos dolorosos en los dedos o como púrpura palpable por vasculitis leucocitoclástica. La vasculitis retiniana se manifiesta con exudados algodonosos y/o hemorragias. Por último, aunque la livedo reticularis y el fenómeno de Raynaud no son propiamente vasculíticos; están relacionados y se atribuyen a vasoespasmo.
Datos complementariosCitopeniaOcurre en la mayoría de los pacientes pediátricos16. La leucopenia por linfopenia (< 1.500células/mm3) es frecuente; en cambio, la neutropenia suele ser provocada por los inmunosupresores. La anemia tiene varias etiologías: trastorno crónico, déficit de hierro, déficit de eritropoyetina en la insuficiencia renal y hemólisis con test de Coombs positivo. La trombopenia puede ser discreta (< 150.000plaquetas/ mm3) o intensa (< 100.000plaquetas/mm3).
AnticuerposLos anticuerpos antifosfolípido (AAF), que incluyen el anticoagulante lúpico y los anticuerpos anticardiolipina, están presentes en el 40% de los LESp e incrementan el riesgo de trombosis. No obstante, el síndrome antifosfolípido (SAF) secundario a LES no es habitual en edades pediátricas. Cuando aparece, suele manifestar trombosis venosa en miembros inferiores, cerebro o pulmón y con menos frecuencia arterial cerebral. A su vez, el denominado SAF catastrófico es una microangiopatía que se caracteriza por púrpura trombótica trombocitopénica (trombopenia, insuficiencia renal y afectación neurológica central) con AAF positivos17.
AutoanticuerposLa sensibilidad de los ANA para el diagnóstico de LES supera el 95%, aunque su especificidad es inferior al 36%. De hecho el test es positivo en más del 20% de niños sanos o con trastornos banales18. Por el contrario, los anti-ADN de doble cadena (anti-dsADN) y los anti-Smith (anti-Sm) son muy específicos. El antiproteína ribonuclear (anti-RNP), el anti-Ro (también conocido como anti- SSA) y el anti-La (o anti-SSB). que muestran menos del 30% de los casos, se asocian con lupus neonatal19.
Otras alteracionesLa disminución del complemento, sobre todo de C3 y C4, sugiere actividad de la enfermedad. En las exacerbaciones contrasta la velocidad de sedimentación globular elevada con la PCR casi normal, salvo que la agudización curse con serositis y/o poliartritis, se trata de una infección o exista un síndrome de activación del macrófago. Las enzimas hepáticas aumentados pueden indicar actividad y el análisis de orina mostrar proteinuria de diferente cuantía, hematuria y cilindruria. La creatinina y su aclaramiento indican el estado de la función del riñón. En casos de neurolupus, y dependiendo de los síntomas, se valora efectuar: punción lumbar, electroencefalograma, anticuerpos anti-P-ribosomales y AAF, así como las técnicas de imagen correspondientes. Pero todas estas pruebas son poco específicas y, con cierta frecuencia, aun existiendo patología neurológica no es posible objetivarla.
El diagnóstico y la monitorización de la enfermedad se realizan con los datos clínicos y de laboratorio, junto a los estudios histológicos y de imagen hasta aquí mencionados20.
Diferencias según la edadNumerosos estudios han comparado el LES infantil con el del adulto. Un metanálisis reciente concluye que en el LESp son más frecuentes el exantema malar, las úlceras mucocutáneas, la afectación renal, las convulsiones, la trombopenia, la anemia hemolítica, la fiebre y la linfadenopatía, mientras que el fenómeno de Raynaud, la pleuritis y el síndrome seco predominan en el adulto21. En cuanto al pronóstico a largo plazo, una cohorte de pacientes puso de manifiesto que la mortalidad de los niños y jóvenes casi duplicaba la de sus controles adultos22.
Por otra parte, se han buscado diferencias en LESp antes y después de la pubertad. Un trabajo canadiense revela que los más pequeños necesitaron más ingresos en Cuidados Intensivos23; otro europeo, que el riesgo de daño orgánico se incrementa cuanto menor es la edad al debut24 y en un tercero realizado en China, el grupo preescolar tuvo más manifestaciones neurológicas y peor pronóstico25.
DiagnósticoEn general, el diagnóstico de sospecha se establece en un adolescente con síntomas constitucionales, leucopenia por linfopenia, exantema malar y artritis o artralgias, máxime si asocia hematuria o proteinuria, úlceras orales, adenomegalias, serositis o algún trastorno neurológico.
Las principales entidades a tener en cuenta en el diagnóstico diferencial son las infecciones víricas (parvovirus B19, citomegalovirus, infección por el virus de la inmunodeficiencia humana, virus de Epstein-Barr), las infecciones bacterianas (sepsis por Salmonella), los procesos malignos (leucemia, linfoma) y algunas enfermedades inflamatorias (artritis idiopática juvenil, dermatomiositis juvenil, vasculitis sistémicas).
Determinadas afecciones a menudo indican un LES concomitante o subyacente, caso del hipotiroidismo de Hashimoto, la hepatitis autoinmune, la pericarditis autoinmune, la anemia hemolítica autoinmune, la púrpura trombopénica idiopática, la vasculitis primaria del sistema nervioso central, la esquizofrenia y la enfermedad de Kikuchi-Fujimoto11.
ComplicacionesInfeccionesSon el resultado del estado de inmunosupresión intrínseco de la enfermedad y extrínseco por el tratamiento. Forman parte del diagnóstico diferencial al comienzo y en las agudizaciones. Los pacientes se defienden mal de las bacterias encapsuladas, como Pneumococcus, Meningococcus, Haemophilus influenzae tipo B y Salmonella. Además, los virus pueden simular una exacerbación, concretamente la reactivación del citomegalovirus se ha descrito como muy grave. El riesgo de herpes zóster es alto, con independencia de que los pacientes hayan presentado o sido vacunados de la varicela. La infección oportunista por Pneumocystis es otra posibilidad que se debe tener en cuenta.
Síndrome de activación del macrófagoSe trata de una complicación potencialmente fatal de diferentes enfermedades reumáticas, entre ellas el LES. Cuando surge, el paciente empeora con fiebre persistente, tendencia a la citopenia, hepatoesplenomegalia, alteración de la función hepática y coagulopatía. Hallazgos que se asemejan a los de una exacerbación lúpica, de la que hay que distinguirlo. Este síndrome es una forma secundaria de linfohistiocitosis hemofagocítica y parece debido a la proliferación incontrolada de las células T, que secretan grandes cantidades de citocinas proinflamatorias y a la activación exagerada de los macrófagos que da lugar a una hemofagocitosis desmedida. La hiperferritinemia es característica26.
AteroesclerosisEl riesgo de aterosclerosis prematura y sus consecuencias clínicas, convulsiones o infarto de miocardio a edades tempranas, es una complicación emergente que preocupa a los facultativos responsables de los niños y jóvenes con LES27.
PronósticoPara monitorizar la actividad del lupus, se dispone de diversos índices, que se han utilizado en LESp, entre ellos el Systemic Lupus Erythematosus Disease Activity Index8 y el British Isles Lupus Assessment Group Index28. Sin embargo, para cuantificar el daño, el más aceptado es el Systemic Lupus International Collaborating Clinics/American College of Rheumatology Damage Index for Systemic Lupus Erythematosus, SLICC/ACR (SDI)24, que se muestra en la tabla 5. El SDI se aplicó en 1.015 LESp y resultó que el 58% de los casos presentaba algún tipo de daño a partir de los 5 años de evolución. Los autores del trabajo propusieron añadir 2 dominios a la versión pediátrica, el fallo de crecimiento y el retraso de la pubertad observados en el 15 y el 11% de los pacientes, respectivamente29. Este índice se relaciona con el riesgo de mortalidad30 y los corticoides son responsables de su incremento31.
Índice de daño en el lupus eritematoso sistémico. Damage Index for Systemic Lupus Erythematosus (SDI)
| Daño no reversible durante al menos 6 meses | Puntuación |
| Ocular (cada ojo independiente) | |
| Catarata | 1 |
| Cambios en la retina o atrofia óptica | 1 |
| Neuropsiquiátrico | |
| Trastorno cognitivo (p. ej., dificultad para el cálculo, para hablar o escribir, psicosis, etc.) | 1 |
| Convulsiones que requieren tratamiento más de 6 meses | 1 |
| Accidente cerebrovascular (puntuar 2 si > de 1 localización) | 1 (2) |
| Mielitis transversal | 1 |
| Neuropatía excluida la del nervio óptico | 1 |
| Renal | |
| Filtrado glomerular < al 50% | 1 |
| Proteinuria ≥ 3,5g/24h | 1 |
| Insuficiencia renal terminal en diálisis o trasplante | 3 |
| Pulmonar | |
| Hipertensión | 1 |
| Fibrosis | 1 |
| Pulmón menguante | 1 |
| Infarto pulmonar | 1 |
| Cardiovascular | |
| Angina o bypass de arteria coronaria | 1 |
| Infarto de miocardio (puntuar 2 si >1) | 1 (2) |
| Cardiomiopatía (disfunción ventricular) | 1 |
| Enfermedad valvular | 1 |
| Pericarditis o pericardiectomía | 1 |
| Vascular periférico | |
| Claudicación durante 6 meses | 1 |
| Pérdida de tejido pequeña | 1 |
| Pérdida de tejido importante (puntuar 2 si >1) | 1 (2) |
| Trombosis venosa con inflamación y ulceración | 1 |
| Gastrointestinal | |
| Infarto/resección de intestino delgado o a otro nivel (puntuar 2 si >1) | 1 (2) |
| Insuficiencia mesentérica | 1 |
| Peritonitis crónica | 1 |
| Musculoesquelético | |
| Atrofia muscular | 1 |
| Artritis erosiva o deformante | 1 |
| Osteoporosis con fractura vertebral | 1 |
| Necrosis avascular (puntuar 2 si >1) | 1 (2) |
| Cutáneo | |
| Alopecia crónica | 1 |
| Ulceración >6 meses | 1 |
| Fallo gonadal primario | 1 |
| Diabetes | 1 |
| Enfermedad maligna (puntuar 2 si >1) | 1 (2) |
La supervivencia a los 10 años de un grupo de pacientes seguidos desde 1969 a 1980 fue del 40%, mientras que en los controlados entre 1980 y 2000 alcanzó el 90%32. La mejoría de la supervivencia en los años ochenta y noventa se atribuye a la asociación de los inmunosupresores (ciclofosfamida y azatioprina) al tratamiento corticoideo. Posteriormente la supervivencia se ha estabilizado, no ha seguido mejorando. Las causas fundamentales de muerte en el primer año de enfermedad son la actividad lúpica y las infecciones, mientras que la mortalidad tardía se debe a las infecciones, la enfermedad cardiovascular por ateroesclerosis, el fracaso renal y los tumores, sobre todo el linfoma.
El análisis de 12.344 casos de insuficiencia renal terminal por nefritis lúpica en EE. UU. puso de manifiesto un aumento significativo de la misma entre los más jóvenes, la raza afroamericana y la residencia en el sureste del país. La proporción de trasplantes renales en los 3 primeros años, cuando el pronóstico es mejor, había disminuido. Asimismo, más pacientes recibían hemodiálisis que diálisis peritoneal, con la que se ha comprobado mejor supervivencia del injerto. No obstante, la mortalidad se mantenía estable33. Estos hechos sugieren que el nivel socioeconómico puede actuar como factor de confusión en las publicaciones relativas al curso del LES. Además, en lo que se refiere al LESp, cabe que casos leves no diagnosticados queden excluidos de los estudios.
Por último, no se han encontrado diferencias en los aspectos psíquicos y sociales entre sanos y enfermos cuando la enfermedad está inactiva34, pero la actividad y el tratamiento repercuten desfavorablemente en el rendimiento escolar35.
Manejo del lupus eritematoso sistémicoTratamiento farmacológicoLa mayoría de los fármacos se utilizan fuera de ficha técnica porque, exceptuando los GC, las agencias reguladoras no han aprobado su uso pediátrico. El referente es la experiencia en adultos36.
Puesto que todos los agentes tienen efectos adversos, la primera consideración del reumatólogo es valorar el riesgobeneficio de cada uno de ellos. Asimismo, según el órgano afectado requerirá la colaboración del nefrólogo, cardiólogo, neurólogo, psiquiatra, dermatólogo u otro. El tratamiento suele ser agresivo y depende de la intensidad de las manifestaciones. Consta de 2 fases: a) inducción de la remisión, y b) mantenimiento. La aproximación terapéutica estándar o clásica incluye37:
- –
Los antimaláricos, que se administran en exantemas y artritis leves o moderadas y como terapia de mantenimiento. A veces con aspirina a dosis antiagregante, cuando los AAF son positivos.
- –
Los glucocorticoides orales o en bolos por vía intravenosa (10–30mg/kg/dosis, máximo 1g) son fármacos muy eficaces en el control de la actividad y los reciben casi todos los pacientes, a pesar de sus numerosos efectos no deseables20. La dosis y el tiempo de administración han de ser individualizados.
- –
En cuanto a los inmunosupresores, se indican según la gravedad del cuadro clínico. La ciclofosfamida (CF) en pulsos intravenosos ha sido de elección en las manifestaciones más graves, caso de la GN proliferativa difusa o la psicosis, y en la resistencia o dependencia de GC en citopenias y serositis. En la actualidad algunos autores prefieren el micofenolato mofetilo (MMF)38. La primera serie de LESp tratados con MMF fue publicada en el año 2000 y en ese trabajo se concluyó que era similar a CF en el porcentaje de pacientes que alcanzaba la remisión39. Posteriormente, otros autores encontraron menor eficacia de MMF para prevenir la progresión a IRT de la GN clase IV40. Una revisión sistemática de la literatura no ha demostrado su superioridad sobre CF. Si bien es cierto que disminuyeron la alopecia y la amenorrea, no había diferencias en la incidencia de infecciones, de insuficiencia renal terminal, ni en el riesgo de muerte41. El tratamiento de mantenimiento del LES se suele realizar con azatioprina o MMF. Los inhibidores de la enzima convertidora de angiotensina, los antidepresivos, los anticomiciales y los anticoagulantes pueden ser necesarios. Las inmunoglobulinas por vía intravenosa y la plasmaféresis se emplean en situaciones puntuales. Hasta el momento no ha sido establecida la indicación de las estatinas42 y los bifosfonatos.
En los últimos años, se han incorporado nuevos agentes farmacológicos, cuya diana terapéutica es la célula B43. Se administran junto al tratamiento estándar. Rituximab es un anticuerpo monoclonal quimérico anti-CD20, que produce depleción de las células B. Hay experiencia en series pediátricas44. No obstante, el resultado de los estudios controlados con este fármaco en adultos fue decepcionante para la comunidad científica. El fracaso parece ser una consecuencia del diseño, porque el grupo placebo recibía el tratamiento clásico, que controla la enfermedad en un gran número de pacientes. A pesar de ello, su eficacia en LES refractarios ha determinado que la mayoría de los autores lo indiquen en situaciones de falta de respuesta a los fármacos tradicionales. Por otra parte, belimumab es un anticuerpo monoclonal humanizado, que inhibe la actividad de BLyS (estimulador de la supervivencia y la diferenciación del linfocito B). Ha sido aprobado por la Food and Drug Administration para el tratamiento del LES. Sin embargo, algunas cuestiones continúan pendientes de resolución con belimumab, por ejemplo su papel en la nefritis lúpica o en neurolupus activos (específicamente excluidos de los ensayos) o si será más útil como inductor de remisión o en la fase de mantenimiento. Un análisis retrospectivo de más de 1.000 pacientes sugiere que belimumab mejora al tratamiento clásico en los casos con mayor actividad serológica45. Recientemente, se ha puesto en marcha un estudio controlado en LESp, del que se esperan conclusiones relevantes. Otras moléculas implicadas en la patogenia de la enfermedad están en distintas fases de investigación y es muy posible que, en un futuro cercano, las opciones terapéuticas aumenten.
Por último, para estandarizar el seguimiento de los pacientes The Pediatric Rheumatology International Trials Organization y la ACR propusieron unos criterios provisionales que valoran la respuesta al tratamiento46,47 y se ha alcanzado un consenso internacional para definir enfermedad inactiva y remisión clínica48.
Tratamiento no farmacológicoEl caso típico de LESp es una adolescente que, además de los cambios y retos propios de la edad, presenta una enfermedad crónica y grave. Es necesario ofrecerle toda la información que le permita aprender a convivir con ella. La apariencia física, importante en cualquier época de la vida, lo es más en la adolescencia, y no sorprende que la actividad escolar y las relaciones familiares se acaben resintiendo. Tampoco es infrecuente que rechace fármacos como los GC y que la adherencia general al tratamiento sea pobre. Nuestro objetivo es convencerla de que lograr la remisión y mantener la enfermedad inactiva es el mejor camino para una vida normalizada e independiente40.
El manejo del LES incluye algunas recomendaciones: protección solar, hábitos de vida saludables, adecuada nutrición, suplementos de calcio y vitamina D, ejercicio y reposo equilibrados, y seguimiento en un centro especializado. También es importante administrar las vacunas recombinantes o de virus muertos, incluida la anual de la gripe, sin que se haya logrado acuerdo sobre las vacunas neumocócica y meningocócica. Interesa evitar un embarazo no deseado y la colaboración con un ginecólogo interesado en estos aspectos resulta esencial. Las píldoras contraceptivas con estrógenos aumentan el riesgo de trombosis, sobre todo si los AAF son positivos y el preservativo es aconsejable por la ventaja añadida de protección frente a las enfermedades de transmisión sexual. Igualmente, conviene ofrecer información sobre 2 riesgos potenciales, la agudización de la enfermedad durante la gestación y el LES neonatal en las portadoras de los anticuerpos antes mencionados. En cualquier caso, la gestación en una paciente con LES precisa de un estrecho control médico. Para terminar, y como en las demás enfermedades crónicas, la transición a un servicio de adultos ha de ser cuidadosa y evitar la sensación de desamparo.
Los autores declaran no tener ningún conflicto de intereses.