Evaluamos el resultado técnico y el resultado inmediato de la reparación aórtica endovascular torácica (RAEVT) para la disección aguda de la aórtica torácica de tipo B, tratada mediante un dispositivo comercialmente disponible. A partir de un registro de cirugía vascular mantenido prospectivamente, se identificaron todos los pacientes con disección aguda de la aórtica torácica de tipo B, sintomática, tratados con RAEVT desde la aprobación por parte de la Food and Drug Administration de la endoprótesis Gore (Flagstaff, AZ) TAG®. Se analizaron las indicaciones clínicas, técnica quirúrgica, complicaciones perioperatorias, los resultados de los exámenes de diagnóstico por imagen obtenidos durante el seguimiento y la mortalidad. Entre marzo de 2005 y noviembre de 2007, se efectuaron 127 RAEVT utilizando la endoprótesis TAG, de las que, en 15 (11,8%), la indicación fue una disección aguda de la aórtica torácica de tipo B. Las indicaciones de la corrección fueron la perfusión insuficiente (53%), el dolor persistente (27%), y la insuficiencia aórtica primaria (33%). La viabilidad y el resultado técnico con un despliegue proximal en el desgarro de entrada fueron del 93,3%, requiriendo siete casos (46,7%) la cobertura como mínimo parcial de la arteria subclavia izquierda. Los procedimientos adyuvantes necesarios en el momento de la RAEVT incluyeron la implantación de un stent en la arterial renal (n=2), en la arteria ilíaca (n=3), y una corrección abierta con abordaje de la arteria (n=2). En 12 pacientes (80%) se obtuvo la resolución inmediata del déficit de perfusión. Las complicaciones perioperatorias mayores incluyeron paraplejía (13,3%), insuficiencia renal que requirió hemodiálisis (13,3%), e ictus (6,7%). La mortalidad perioperatoria fue del 13,3%, afectando a un paciente que presentó rotura e insuficiencia cardíaca profunda en el momento del ingreso. Para la disección aórtica torácica complicada, de tipo B, la RAEVT con la utilización de endoprótesis disponibles comercialmente demostró un elevado resultado técnico, resultados excelentes en la resolución de las anomalías de la perfusión y una mortalidad y complicaciones perioperatorias aceptablemente bajas.
Continúa suscitando debate el tratamiento apropiado de la disección aórtica aguda de tipo B. El bypass quirúrgico tradicional de la aorta torácica descendente para una disección aguda se asocia a una tasa de mortalidad del 25-46%1. Como consecuencia, la implantación de endoprótesis en la aorta torácica se está convirtiendo rápidamente en la opción alternativa para las disecciones de tipo B complicadas. En múltiples artículos se ha documentado la capacidad de las endoprótesis para excluir el flap de entrada en la mayoría de las disecciones de tipo B2-6. Las principales ventajas de este tratamiento incluyen la estabilización del flap intimal, preservación de la luz verdadera, remodelado positivo de la aorta a través de la trombosis de la falsa luz y, en último término, la falta de complicaciones relacionadas con la disección durante el seguimiento. Aunque todavía no se conoce la permeabilidad a largo plazo de esta modalidad, las primeras pruebas sugieren que el tratamiento con implantación de una endoprótesis puede ser cuestionable comparado con el mejor tratamiento médico con respecto a la mortalidad aguda4. El objetivo del presente estudio fue evaluar el resultado de la implantación de endoprótesis en disecciones agudas de tipo B, desde la aprobación por parte de la Food and Drug Administration (FDA) de un modelo disponible comercialmente.
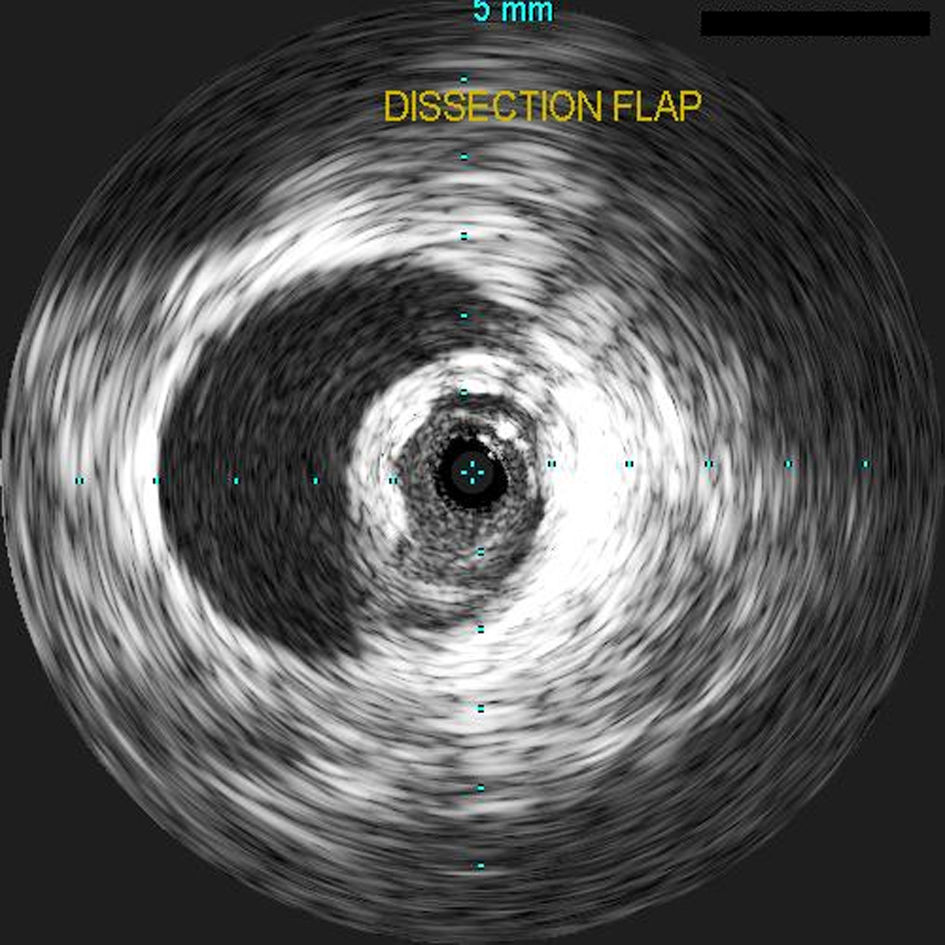
MétodosPacientesDesde marzo de 2005 hasta noviembre de 2007, se revisó un registro de cirugía vascular mantenido prospectivamente para identificar a los pacientes tratados en nuestro centro con la endoprótesis Gore (Flagstaff, AZ) TAG® para el tratamiento de la patología de la aorta torácica, tras aprobación por parte de la FDA. Se obtuvo la autorización del comité ético del centro para estudiar retrospectivamente a los pacientes tratados con el dispositivo Gore TAG por disección aórtica aguda de tipo B. Se incluyeron los pacientes que se presentaron con disecciones aórticas torácicas agudas de tipo B (< 14 días desde la presentación), en todos los cuales estaba presente un flap de entrada en la arteria subclavia izquierda o distal a ésta, confirmado mediante angiografía por tomográfica computarizada (ATC) y/o ecografía intravascular (EIV). Todos los pacientes experimentaban disecciones complicadas tipo B, definidas por la perfusión anómala de un órgano diana o una extremidad, dolor persistente, insuficiencia cardíaca aguda, paraplejía de la médula espinal, insuficiencia renal, isquemia mesentérica o hipertensión arterial refractaria. Los datos obtenidos incluyeron la edad, estado de la supervivencia, componentes utilizados para el injerto, arterias de abordaje, longitud de la aorta cubierta, cobertura de la arteria subclavia, pérdida hemática, duración de la estancia hospitalaria, complicaciones, resultados durante el seguimiento y estado de la falsa luz y del mayor diámetro aórtico en los resultados de las técnicas de imagen obtenidas durante el seguimiento.
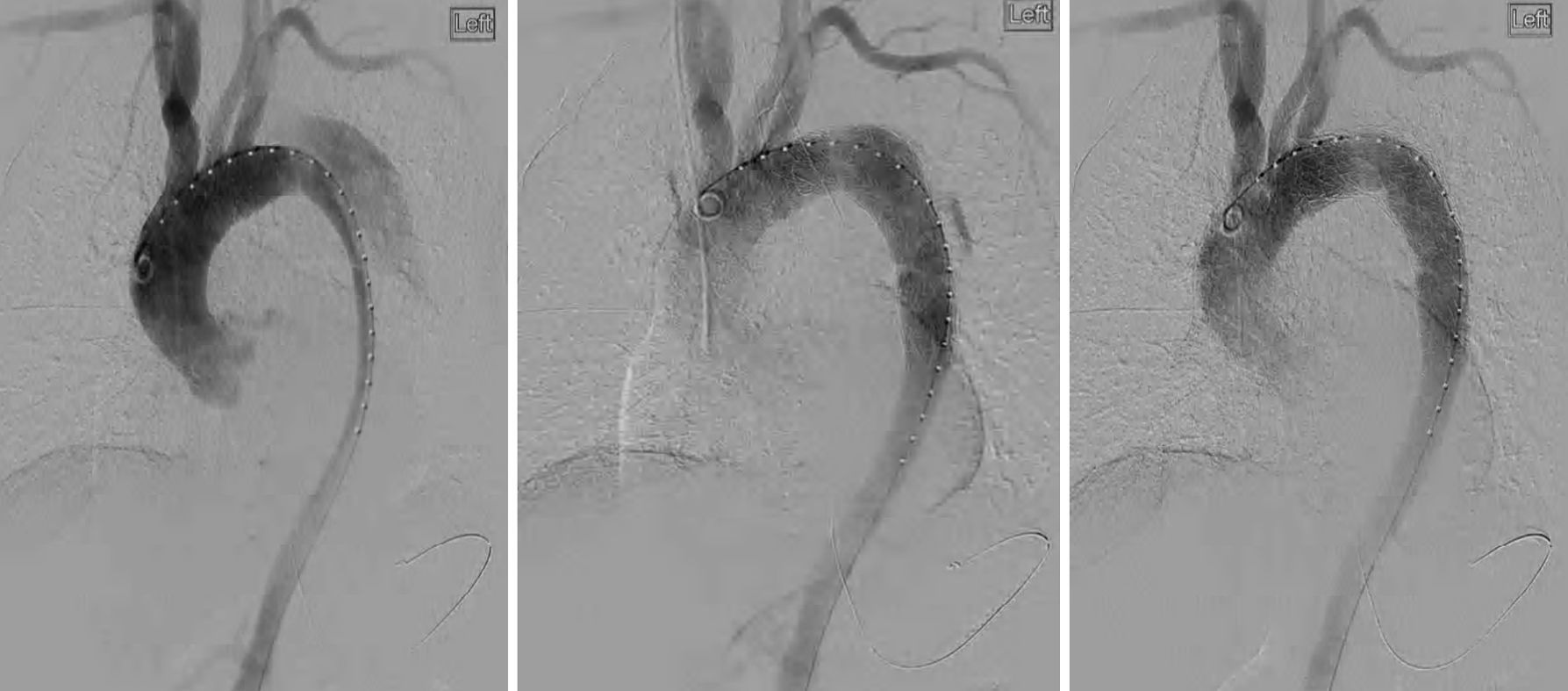
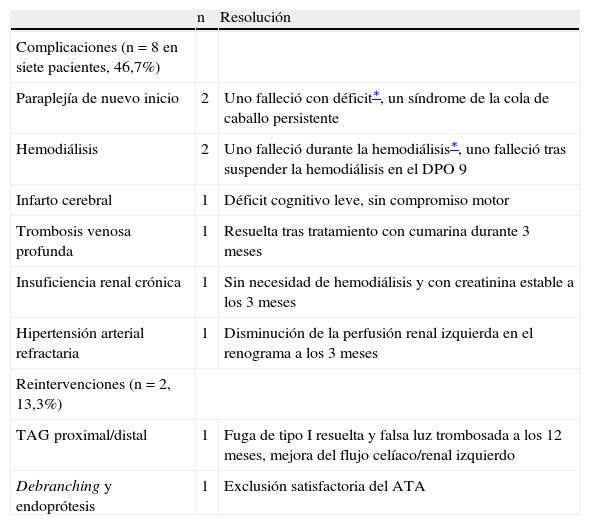
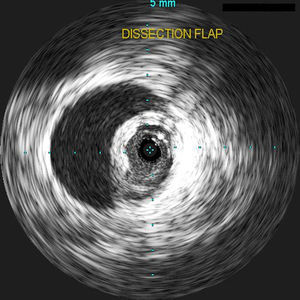
TécnicaEn otra publicación se ha descrito el diseño estructural de la endoprótesis Gore TAG®7. Los procedimientos de implantación de la endoprótesis torácica se efectuaron en un área quirúrgica endovascular utilizando fluoroscopia montada en el techo (fig. 1). En todos los casos se administró anestesia general y no se realizó drenaje de líquido cefalorraquídeo profiláctico. Todos los injertos se desplegaron a través de un abordaje en la arteria femoral común por medio de un abordaje femoral unilateral y/o bilateral; no se requirieron conductos ilíacos. Para confirmar la entrada en la luz real, localización del flap de entrada y determinaciones del tamaño en todos los pacientes se utilizó EIV (fig. 1). Una vez se confirmó el abordaje de la guía en la luz real en el cayado aórtico, se efectuó una angiografía a este nivel. Si las imágenes indicaron la necesidad de cobertura de la arteria subclavia izquierda (fig. 2), se efectuó una angiografía vertebral selectiva para evaluar la suficiencia del flujo colateral de la arteria vertebral y confirmar la ausencia de injertos de la mamaria interna. Acto seguido, se heparinizó sistemáticamente a los pacientes con un bolo intravenoso de 100 UI/kg. Los stents se distribuyeron mediante guía fluoroscopia para cubrir el flap de entrada proximal con el objetivo de excluir el flujo en la falsa luz. Cuando el flap de disección no pareció estabilizado lo suficiente en la fluoroscopia en vivo para mejorar la perfusión distal, el cirujano desplegó componentes distales adicionales. Se completó la angiografía para documentar la situación de la falsa luz y evaluar la perfusión distal. Cuando estuvo indicado, se efectuaron procedimientos complementarios, incluida la extensión proximal, implantación de un stent en la arteria renal y en la arteria ilíaca. En todos los abordajes se efectuó una corrección directa de la arteriotomía, y para el abordaje percutáneo, se usaron dispositivos de cierre. Todos los pacientes fueron trasladados a la unidad de cuidados intensivos quirúrgicos para la vigilancia postoperatoria.
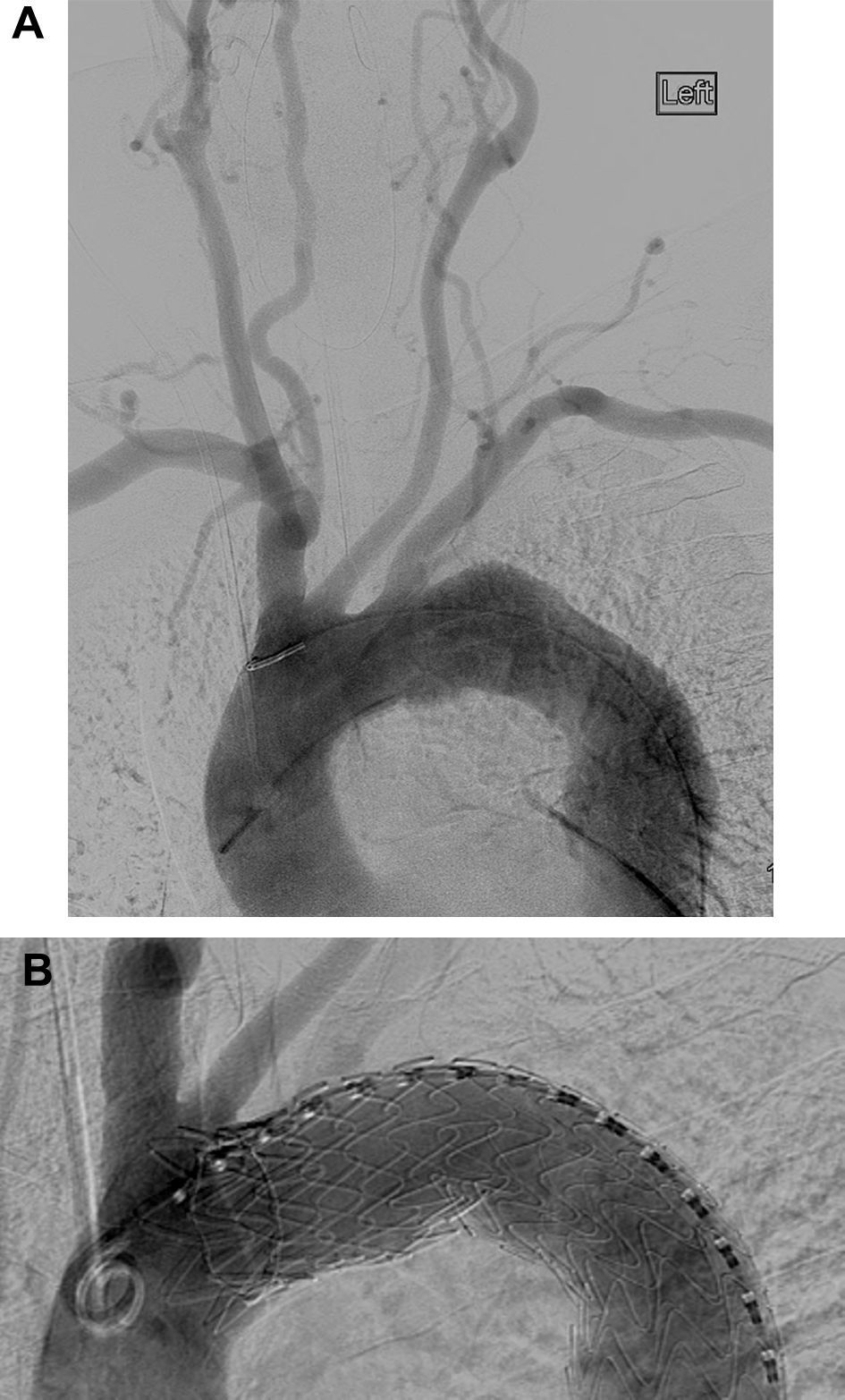
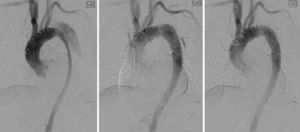
A Angiografía preimplante del cayado con una gran arteria vertebral derecha y sin injerto de arteria mamaria interna a coronaria. B Visión con aumento que demuestra la cobertura de la arteria subclavia con el mantenimiento de flujo anterógrado en la carótida izquierda a pesar de los struts de la endoprótesis que se extienden hasta su origen.
En nuestro hospital no se efectúa un drenaje raquídeo ni un control sistemático de la presión arterial media (PAM). Todos los pacientes fueron trasladados a la unidad de cuidados intensivos para su seguimiento con monitorización neurovascular. Junto con el servicio de neurocirugía, nuestra norma es una actitud expectante frente a la isquemia de la médula espinal. En diversas series sobre reparaciones aórticas torácicas abiertas y endovasculares se ha descrito la eficacia de dicha estrategia8-11. Cualquier paciente con un cambio en el examen requiere tratamiento inmediato con fármacos vasoactivos para una PAM>110 mmHg, una evaluación quirúrgica inmediata, resonancia magnética raquídea inmediata y drenaje raquídeo a discreción del neurocirujano responsable.
Análisis estadísticoEl presente estudio fue un análisis retrospectivo, no comparativo. Toda la estadística fue descriptiva y se utilizó el principio por intención de tratar. Las variables discretas se presentan como porcentajes, las continuas como recuentos, medias y desviaciones estándar. Para evaluar a los pacientes perdidos de seguimiento y generar análisis de tablas de vida, se revisaron los registros de la Seguridad Social.
ResultadosPara la patología aórtica torácica, incluido aneurisma, disección y úlcera penetrante, se efectuaron 127 correcciones mediante endoprótesis. En un total de 26 pacientes se evidenció una disección como indicación de la intervención; de ellos, en 15 (11,8%) correspondió a disección aórtica B de tipo agudo. La edad media en el momento del tratamiento fue de 61±11,5 años (límites 45-87), con una distribución de sexos de 12 hombres y tres mujeres. Las indicaciones de la intervención incluyeron perfusión anómala en un 53%, dolor persistente en un 27%, e insuficiencia aórtica en un 33%, con la presencia de múltiples indicaciones en dos pacientes (tabla I). En el momento de la presentación, todos los pacientes eran hipertensos, requiriendo 14/15 (93,3%) monitorización en la unidad de cuidados intensivos y una infusión IV continua de fármacos antihipertensivos.
Indicaciones de la corrección
| Indicación∗ | n |
| Perfusión anómala (53%) | 8 |
| Isquemia extremidad inferior | 5 |
| Paraplejía | 2 |
| Hipertensión arterial refractaria y encefalopatía | 1 |
| Perfusión anómala en la arteria renal | 2 |
| Dolor (27%) | 4 |
| Dolor torácico/abdominal persistente | 3 |
| Progresión del flap | 1 |
| Insuficiencia aórtica (33%) | 5 |
| Rotura contenida | 2 |
| Expansión rápida | 2 |
| Colapso agudo de la luz real e insuficiencia cardíaca | 1 |
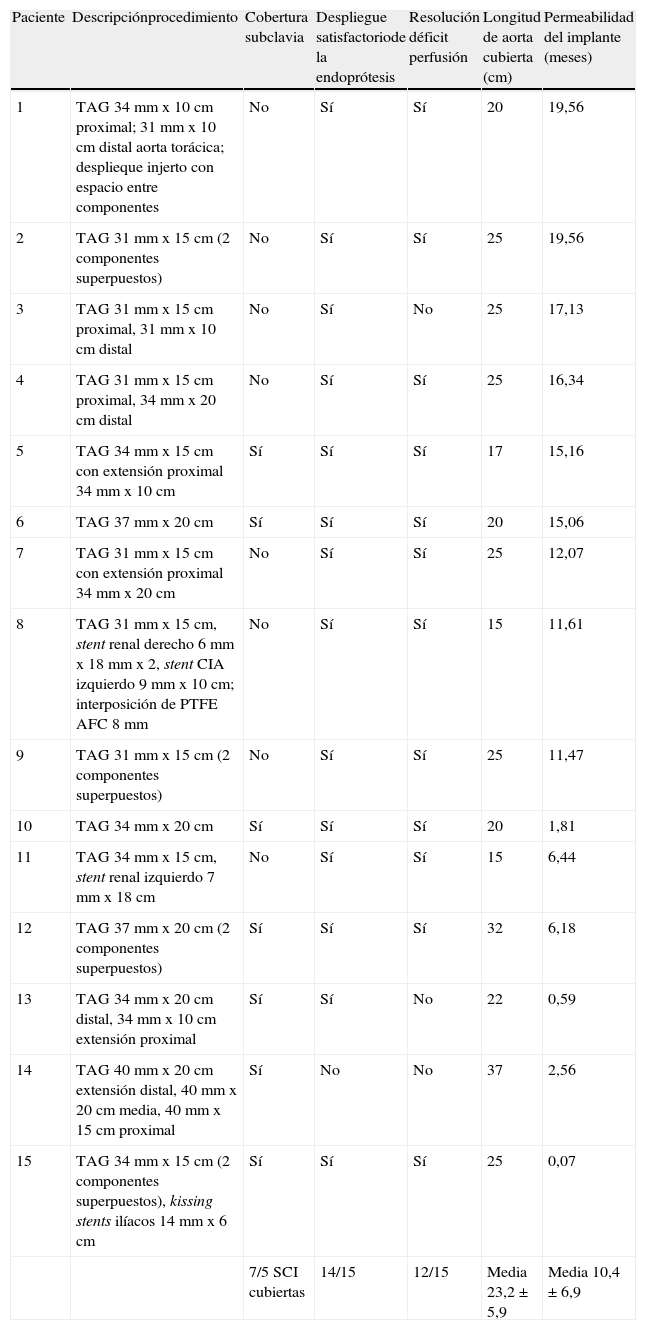
El resultado técnico fue del 93,3%, según lo definido por la exclusión del flap de entrada proximal en la angiografía de comprobación. La tabla II resume las características del implante. El despliegue satisfactorio requirió una cobertura, como mínimo parcial, de la arteria subclavia izquierda en 7/15 (46%) pacientes. Los tamaños del injerto variaron de 31 a 40mm y la longitud media de la aorta cubierta fue de 23,2±5,9cm (límites 15-37). La introducción a través del abordaje femoral fue satisfactoria en los 15 pacientes, requiriendo un abordaje femoral bilateral un 20%, unilateral sola en un 20%, y unilateral con abordaje percutáneo contralateral en el 60%. Las complicaciones relacionadas con el abordaje sólo afectaron a un paciente (6,7%), requiriendo un injerto de interposición iliofemoral. La pérdida hemática estimada fue de 318,8±533,8ml (límites 75-2.000). La duración media de la estancia hospitalaria fue de 8,9±9,9 días (límites 2-19). Partiendo del aspecto angiográfico y de los síntomas de los pacientes, en 12/15 (80%) se obtuvo la resolución inmediata de la perfusión anómala que había motivado la intervención. Un fracaso sintomático fue una endofuga conocida de tipo I al completar la angiografía, a pesar de la cobertura completa hasta la arteria carótida izquierda, y dos se debieron a la imposibilidad de circulación de retorno a las arterias renales, lo que originó hipertensión arterial persistente.
Variables quirúrgicas clave
| Paciente | Descripciónprocedimiento | Cobertura subclavia | Despliegue satisfactoriode la endoprótesis | Resolución déficit perfusión | Longitud de aorta cubierta (cm) | Permeabilidad del implante (meses) |
| 1 | TAG 34mm x 10cm proximal; 31mm x 10cm distal aorta torácica; desplieque injerto con espacio entre componentes | No | Sí | Sí | 20 | 19,56 |
| 2 | TAG 31mm x 15cm (2 componentes superpuestos) | No | Sí | Sí | 25 | 19,56 |
| 3 | TAG 31mm x 15cm proximal, 31mm x 10cm distal | No | Sí | No | 25 | 17,13 |
| 4 | TAG 31mm x 15cm proximal, 34mm x 20cm distal | No | Sí | Sí | 25 | 16,34 |
| 5 | TAG 34mm x 15cm con extensión proximal 34mm x 10cm | Sí | Sí | Sí | 17 | 15,16 |
| 6 | TAG 37mm x 20cm | Sí | Sí | Sí | 20 | 15,06 |
| 7 | TAG 31mm x 15cm con extensión proximal 34mm x 20cm | No | Sí | Sí | 25 | 12,07 |
| 8 | TAG 31mm x 15cm, stent renal derecho 6mm x 18mm x 2, stent CIA izquierdo 9mm x 10cm; interposición de PTFE AFC 8mm | No | Sí | Sí | 15 | 11,61 |
| 9 | TAG 31mm x 15cm (2 componentes superpuestos) | No | Sí | Sí | 25 | 11,47 |
| 10 | TAG 34mm x 20cm | Sí | Sí | Sí | 20 | 1,81 |
| 11 | TAG 34mm x 15cm, stent renal izquierdo 7mm x 18cm | No | Sí | Sí | 15 | 6,44 |
| 12 | TAG 37mm x 20cm (2 componentes superpuestos) | Sí | Sí | Sí | 32 | 6,18 |
| 13 | TAG 34mm x 20cm distal, 34mm x 10cm extensión proximal | Sí | Sí | No | 22 | 0,59 |
| 14 | TAG 40mm x 20cm extensión distal, 40mm x 20cm media, 40mm x 15cm proximal | Sí | No | No | 37 | 2,56 |
| 15 | TAG 34mm x 15cm (2 componentes superpuestos), kissing stents ilíacos 14mm x 6cm | Sí | Sí | Sí | 25 | 0,07 |
| 7/5 SCI cubiertas | 14/15 | 12/15 | Media 23,2±5,9 | Media 10,4±6,9 |
AFC: arteria femoral común; PTFE: politetrafluoroetileno; SCI: arteria subclavia izquierda.
Las complicaciones globales a los 30 días afectaron a 7/15 (46,7%) pacientes (tabla II). En 2/15 (13,3%) se produjo isquemia de la médula espinal de nuevo inicio, que, más tarde, requirió la implantación de un drenaje lumbar y un aumento de la PAM≥110 mmHg según el protocolo de nuestro hospital. Un paciente que desarrolló paraplejía postoperatoria falleció antes de la resolución de los síntomas; en el otro paciente se observó una mejora de la paraplejía hasta la deambulación con muletas pero persistió la incontinencia de esfínteres. En el preoperatorio dos pacientes presentaron paraplejía relacionada con la isquemia (extremidades sin pulso): uno falleció tras una estancia prolongada en la unidad de cuidados intensivos y el otro mejoró hasta una función motora normal al cabo de un mes postoperatorio. Un paciente experimentó un infarto cerebral de la zona marginal detectado en la resonancia magnética, efectuada debido a los cambios postoperatorios del estado mental con déficit cognitivo leve pero sin déficit motor. Otras complicaciones incluyeron trombosis venosa profunda (n=1), insuficiencia renal crónica debida a nefropatía por contraste (n=1), e hipoperfusión persistente del riñón izquierdo con hipertensión arterial refractaria (n=1). En el postoperatorio dos pacientes requirieron diálisis: uno presentó disfunción renal y requirió diálisis permanente y en el otro se suspendió en el día 9 postoperatorio.
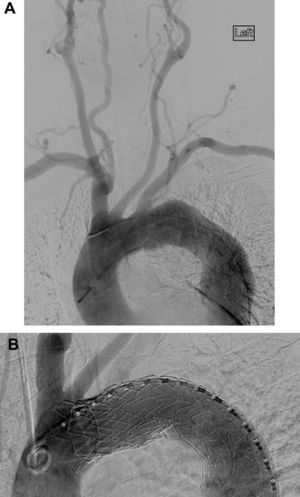
La mortalidad perioperatoria a los 30 días fue del 13,3%. Un paciente, que presentó una rotura aórtica torácica contenida, falleció en el día postoperatorio 18 tras un curso prolongado que incluyó hemodiálisis, dependencia del respirador e isquemia visceral. La segunda muerte a los 30 días se produjo en un paciente que presentó un compromiso sustancial de la luz real que dio lugar a insuficiencia cardíaca aguda (fig. 3). A pesar de la angiografía de comprobación, que demostró la exclusión del flap de entrada proximal y una mejora inicial del gasto cardíaco, el paciente falleció en el segundo día postoperatorio, probablemente como consecuencia de una disección retrógrada en la raíz aórtica. Dos meses después del procedimiento, una paciente adicional falleció de una insuficiencia respiratoria en un centro de rehabilitación, donde había sido ingresada por paraparesia leve de la extremidad inferior. En la cohorte del presente estudio al cabo de una media de 11,0±6,9 meses postoperatorios (límites 0,1-19,6) la mortalidad global fue de 3/15 (20%). Mediante análisis de tablas de vida, la mortalidad fue del 79% a los 2 años (error estándar del 10%).
El seguimiento clínico y radiológico medio fue de 5,8±4,4 meses (límites 0-12). Al mes, en 8/10 pacientes se produjo trombosis de la falsa luz a través del segmento tratado de la aorta torácica según la ATC. Un paciente sin trombosis de la falsa luz era portador de una endofuga proximal conocida de tipo I al completar la intervención con un aumento del tamaño aórtico de 3mm durante este intervalo. El segundo paciente desarrolló una nueva endofuga de tipo I y, más tarde, se sometió a la implantación satisfactoria de una extensión proximal TAG para cubrir la arteria subclavia. Después de esta reintervención la TC demostró una falsa luz trombosada y la estabilización del diámetro aórtico. De los injertos seguidos a los 6 meses, 7/7 eran portadores de trombosis de la falsa luz y en 6/7 no se detectó ningún cambio (en un radio de 2mm) del tamaño aórtico máximo. A los 12 meses, 3/3 experimentaron trombosis de la falsa luz y 2/3, ningún cambio del tamaño aórtico máximo. En un paciente continúa aumentando el tamaño aórtico máximo con un crecimiento de 7mm, a pesar de la trombosis de la falsa luz. En conjunto, dos pacientes (13,3%) se sometieron a una reintervención, uno por endofuga de tipo I y el otro para una degeneración aneurismática posterior de la aorta abdominal no cubierta (tabla III).
Complicaciones/reintervenciones
| n | Resolución | |
| Complicaciones (n=8 en siete pacientes, 46,7%) | ||
| Paraplejía de nuevo inicio | 2 | Uno falleció con déficit∗, un síndrome de la cola de caballo persistente |
| Hemodiálisis | 2 | Uno falleció durante la hemodiálisis∗, uno falleció tras suspender la hemodiálisis en el DPO 9 |
| Infarto cerebral | 1 | Déficit cognitivo leve, sin compromiso motor |
| Trombosis venosa profunda | 1 | Resuelta tras tratamiento con cumarina durante 3 meses |
| Insuficiencia renal crónica | 1 | Sin necesidad de hemodiálisis y con creatinina estable a los 3 meses |
| Hipertensión arterial refractaria | 1 | Disminución de la perfusión renal izquierda en el renograma a los 3 meses |
| Reintervenciones (n=2, 13,3%) | ||
| TAG proximal/distal | 1 | Fuga de tipo I resuelta y falsa luz trombosada a los 12 meses, mejora del flujo celíaco/renal izquierdo |
| Debranching y endoprótesis | 1 | Exclusión satisfactoria del ATA |
ATA: aneurisma toracoabdominal; DPO: día postoperatorio.
Durante mucho tiempo la disección aórtica aguda ha sido una causa sustancial de mortalidad relacionada con la patología aórtica, describiéndose en 1986 tasas de mortalidad quirúrgica del 45% para el bypass aórtico torácico descendente y sin que se hayan producido notables progresos, puesto que en 2000, en el estudio The International Registry of Acute Aortic Dissection (IRAD), la mortalidad documentada fue del 31,4%12,13.
Con tasas de mortalidad significativamente más bajas en pacientes sometidos a tratamiento médico, durante mucho tiempo, éste ha sido la base terapéutica de la disección aórtica no complicada, de tipo B. Sin embargo, esto ha dado lugar a un sesgo de selección hacia el tratamiento médico porque los pacientes que requerían cirugía eran aquellos con una disección complicada, es decir, isquemia visceral o de la extremidad, disección retrógrada del cayado, colapso agudo de la luz real, dolor persistente e hipertensión arterial refractaria. Comprensiblemente, sería de esperar que los pacientes con disecciones más complicadas presentaran peores resultados, con independencia de los retos técnicos inherentes a un paciente con una disección aórtica aguda.
No obstante, el tratamiento médico también se asocia a una morbilidad y mortalidad sustanciales. En el estudio IRAD no sólo se demostró una mortalidad hospitalaria del 10,7% entre pacientes con disección aguda de tipo B que recibieron tratamiento médico13, sino también que las secuelas a largo plazo de la disección son considerables. Onitsuka et al14 demostraron una tasa de conversión a la cirugía del 13% en un grupo de 76 pacientes asignados aleatoriamente a tratamiento médico y una incidencia del 23% de eventos relacionados con la disección, incluida la rotura y muerte súbita en la cohorte médica estudiada durante hasta 10 años. Otros investigadores han descrito un riesgo de rotura del 18% durante el seguimiento de pacientes con disección de tipo B, tratados médicamente15 y que en el 20% de todos los aneurismas toracoabdominales la etiología es una disección crónica1. En la base de datos IRAD entre pacientes con disección de tipo B que sobrevivieron a la hospitalización inicial, la tasa de mortalidad global a los 3 años fue del 24,9%16. De hecho, en el análisis intermedio de los datos IRAD, los pacientes con la mayor supervivencia al año y a los 3 años son los que sobrevivieron a una intervención quirúrgica abierta durante la presentación inicial17.
Entre pacientes con una disección de tipo B se han evaluado numerosos factores de esta mejora de los resultados. Es probable que, en la fase aguda, la corrección quirúrgica satisfactoria dé lugar a una mayor supervivencia a largo plazo a través de la obliteración de la falsa luz, al mismo tiempo que se restablece la perfusión normal del segmento aórtico distal y se estabiliza el tamaño aórtico. Akutsu et al18 demostraron que, en las disecciones de tipo B, tratadas médicamente y seguidas durante 10 años, una falsa luz permeable fue una variable pronóstica significativa de mortalidad relacionada con la disección (cociente de riesgo [CR]=5,6) y de un evento relacionado con la disección (CR=7,6). Se ha demostrado que el tamaño aórtico medio y la tasa de crecimiento aórtico son variables pronósticas independientes de eventos relacionados con la disección durante el seguimiento de pacientes tratados médicamente14. Estas observaciones respaldan el beneficio potencial de excluir el punto de entrada de la disección aórtica con un stent. En un ensayo no aleatorizado, Dialetto et al2 demostraron una tasa de falsa luz trombosada del 75% en pacientes sometidos a la implantación de un stent comparado con el 10,7% en los tratados médicamente. En la misma cohorte sólo se demostró una degeneración aneurismática en el 3,5% de los pacientes a los que se implantó un stent comparado con un 28,5% en los tratados médicamente.
La tecnología endovascular está reemplazando rápidamente a la cirugía abierta mediante bypass como tratamiento de elección de la disección complicada de tipo B. En condiciones ideales, el stent debe ofrecer al paciente una disminución de la mortalidad hospitalaria comparado con la corrección tradicional, al mismo tiempo que se mantiene el beneficio de supervivencia demostrado por la corrección quirúrgica17. Buena parte de la experiencia publicada inicial incluyó injertos adaptados y el uso de componentes abdominales para el tratamiento de la disección complicada de tipo B. El presente estudio se limita a la disección aórtica torácica tratada con la endoprótesis TAG, y representa el resultado actual de un dispositivo disponible comercialmente. Aunque la FDA la aprobó para tratar el aneurisma aórtico torácico, la endoprótesis TAG se ha utilizado cada vez más para tratar la disección aórtica.
La eficacia del 93,3% obtenida en el presente estudio en la exclusión del desgarro de entrada proximal es proporcional a la tasa del 86-95%, descrita en otros estudios publicados5,6,19,20, aunque identificamos una mayor necesidad de cobertura deliberada de la arteria subclavia izquierda del 46%. Según han demostrado otros autores, esto es bien tolerado en pacientes cuando se efectúa una evaluación adecuada de las arterias vertebrales y cuando se practica un bypass con la mamaria interna21,22. El bajo umbral de cobertura de la subclavia izquierda es atribuible a nuestra preferencia de que es esencial la exclusión completa del flap de entrada para el tratamiento adecuado de la disección de tipo B. Por fortuna, no obtuvimos eventos adversos relacionados con isquemia de la extremidad superior o síntomas vertebrobasilares.
En todos los pacientes el objetivo de la intervención fue estabilizar la luz real y corregir la perfusión anómala. En cada caso se observó una mejora del flujo a través de la luz real con la estabilización de la obstrucción dinámica en los segmentos viscerales demostrada en la fluoroscopia ulterior. Pudimos tratar satisfactoriamente los casos de obstrucción estática en los segmentos viscerales y de la extremidad, observados en la angiografía de comprobación en todos los casos excepto en uno. Desde un punto de vista técnico, contribuyó la utilización de la exposición de la arteria femoral en los casos de disección en el sistema ilíaco, lo que permite una identificación más rápida de la luz real. En la cohorte del presente estudio no fue necesario utilizar un abordaje humeral.
En el presente estudio la tasa de mortalidad perioperatoria a los 30 días del 13,3% es similar a la descrita en los estudios publicados, que varía del 3,2 al 10,7%2,4-6. Esta tasa de mortalidad corresponde a la documentada en pacientes tratados médicamente entre controles históricos y es más baja que la mortalidad quirúrgica predecible a partir de una intervención abierta para estos pacientes. Las técnicas endovasculares han hecho que este grupo de pacientes, en los que se describía una mortalidad elevada asociada a la disección complicada, haya pasado a ser un grupo con una mortalidad más baja en proporción a la disección no complicada.
En este estudio se produjeron complicaciones sustanciales, como diálisis permanente, déficit neurológico e ictus en un 20% de los casos. En un metaanálisis de estudios que usaron stents para disección aórtica de tipo B, se demostró una tasa de complicaciones mayores del 11,2%4. Nathanson et al20 demostraron una tasa de complicaciones globales del 38% cuando investigaron este dispositivo en un ensayo en pacientes con disección de tipo B. Aunque la tasa documentada de isquemia de la médula espinal es mayor en la presente investigación que en otras series, el tamaño de la muestra es demasiado reducido para que alcance significación. En tres pacientes con paraplejía postoperatoria documentada (incluido un caso de paraplejía preoperatoria) se efectuó cobertura de la arteria subclavia izquierda. Se ha sugerido este procedimiento para excluir la circulación colateral de las distribuciones de la arteria intercostal y las arterias espinales23. El paciente con paraplejía preoperatoria que se resolvió en el postoperatorio no se sometió a cobertura de la subclavia izquierda. La longitud de la aorta cubierta fue variable en estos pacientes (20-32cm); por lo tanto, no está claro si es un factor contribuyente. Con frecuencia, la hipotensión postoperatoria contribuye a un déficit neurológico tardío8,10,11. La naturaleza inestable de las disecciones agudas sintomáticas de tipo B puede entrañar un mayor riesgo de alteración hemodinámica postoperatoria y déficit neurológico. En último término, la isquemia de la médula espinal es multifactorial y no recomendamos un drenaje lumbar profiláctico o una revascularización carótida-subclavia debido a la necesidad urgente de un tratamiento.
Durante el seguimiento, la exclusión persistente del flap de entrada ha demostrado una trombosis constante de la falsa luz torácica en los pacientes del presente estudio, pero no se observó una reducción del tamaño aórtico global durante este período relativamente breve. Nathanson et al20 tampoco observaron una reducción del tamaño aórtico a pesar de la ausencia de endofugas en el 71% de los pacientes, lo que pone en duda el destino de la aorta abdominal no cubierta, según lo demostrado por la tasa del 56% de aumento del diámetro de la falsa luz aórtica abdominal. En la cohorte del presente estudio, se requirió una reintervención en dos pacientes por patología aórtica abdominal al cabo de menos de un año del tratamiento de la disección aguda de tipo B. Los resultados postoperatorios de las técnicas de imagen demostraron un flujo persistente en la falsa luz en la aorta perivisceral de los tres pacientes evaluados a los 12 meses, y esta área continúa siendo una preocupación con el tratamiento mediante implantación de un stent sólo en la aorta torácica.
En un análisis a corto plazo, las endoprótesis disponibles comercialmente pueden utilizarse con una tasa elevada de eficacia en la exclusión del flap de entrada en las disecciones agudas de tipo B. Además, en la implantación de endoprótesis con carácter agudo para una lesión no complicada, éstas pueden reducir la mortalidad perioperatoria a niveles proporcionales a los de pacientes tratados médicamente por una disección no complicada. La implantación de endoprótesis debe ser el tratamiento de elección en pacientes con indicación de corrección quirúrgica. Aunque en las imágenes del seguimiento inmediato es evidente un remodelado positivo del segmento torácico, se requerirá vigilancia para evaluar el resultado de los segmentos no cubiertos de la aorta durante el seguimiento. La evolución del tratamiento para la disección aórtica de tipo B tanto complicada como no complicada continuará con los resultados anticipados de los ensayos aleatorizados en curso que comparan la implantación de endoprótesis con el mejor tratamiento médico24,25.