Realizar la adaptación transcultural al español y la validación psicométrica del cuestionario Nasal Polyposis Quality of Life Questionnaire (NPQ) para su uso en los pacientes con rinosinusitis crónica con pólipos nasales (RSCcPN).
MetodologíaSe incluyeron 140 pacientes adultos diagnosticados de RSCcPN. El cuestionario original NPQ fue adaptado del italiano al español siguiendo las directrices internacionales establecidas. La validez de constructo se evaluó mediante análisis factorial exploratorio (AFE) con componentes principales. La consistencia interna se analizó con el coeficiente alfa de Cronbach. La fiabilidad test-retest se determinó mediante el coeficiente de correlación intraclase (CCI). La validez concurrente se examinó mediante correlaciones de Pearson con los cuestionarios SNOT-22 y NOSE-E. La validez discriminativa se analizó mediante las curvas ROC.
ResultadosEl AFE reveló una estructura de 5 factores que explicaban el 67% de la varianza total. El NPQ en español mostró una excelente consistencia interna (α de Cronbach=0,917) y una alta fiabilidad test-retest (CCI=0,991; IC 95%: 0,983-0,996). El error estándar de medida (EEM) fue de 2 puntos, y el cambio mínimo detectable con un 95% de confianza (CMD95) de 5 puntos. Se observaron correlaciones fuertes con el NOSE-E (r=0,802) y el SNOT-22 (r=0,870). La puntuación total del NPQ presentó una alta capacidad discriminativa para síntomas graves (AUC=0,947), con un punto de corte >41 que ofreció una sensibilidad del 88,9% y una especificidad del 93,3%.
ConclusionesLa versión española del NPQ es un instrumento válido, fiable y clínicamente útil para evaluar la carga sintomática en los pacientes con RSCcPN. Su estructura multidimensional permite captar el impacto específico de este fenotipo y respalda su uso en la práctica clínica y en investigación.
To perform the cross-cultural adaptation into Spanish and the psychometric validation of the Nasal Polyposis Quality of Life Questionnaire (NPQ) for use in patients with chronic rhinosinusitis with nasal polyps (CRSwNP).
MethodsA total of 140 adult patients diagnosed with CRSwNP were included. The original NPQ was adapted from Italian into Spanish following established international guidelines. Construct validity was assessed through exploratory factor analysis (EFA) with principal components. Internal consistency was analyzed using Cronbach's alpha coefficient. Test-retest reliability was determined by the intraclass correlation coefficient (ICC). Concurrent validity was examined using Pearson correlations with the SNOT-22 and NOSE-E questionnaires. Discriminant validity was analyzed using ROC curves.
ResultsEFA revealed a five-factor structure explaining 67% of the total variance. The Spanish NPQ showed excellent internal consistency (Cronbach's α=0.917) and high test-retest reliability (ICC=0.991; 95% CI: 0.983-0.996). The standard error of measurement (SEM) was 2 points, and the minimal detectable change (MDC95) was 5 points. Strong correlations were observed with the NOSE-E (r=0.802) and SNOT-22 (r=0.870). The NPQ total score demonstrated high discriminative ability for severe symptoms (AUC=0.947), with a cutoff point >41 providing 88.9% sensitivity and 93.3% specificity.
ConclusionsThe Spanish version of the NPQ is a valid, reliable, and clinically useful instrument for assessing symptom burden in patients with CRSwNP. Its multidimensional structure allows capturing the specific impact of this phenotype and supports its use in both clinical practice and research.
La rinosinusitis crónica con pólipos nasales (RSCcPN) es una enfermedad inflamatoria persistente de la mucosa nasal y paranasal, caracterizada por la presencia de pólipos nasales bilaterales y síntomas como obstrucción nasal, presión facial, rinorrea y una disminución importante o pérdida del sentido del olfato1. Se estima que afecta hasta al 4% de la población general y tiene un impacto significativo en la calidad de vida, especialmente debido a su asociación con alteraciones del sueño, fatiga y deterioro social y emocional2.
La evaluación de la carga de enfermedad en la RSCcPN depende cada vez más de los cuestionarios de resultados percibidos por los pacientes (patient-reported outcome measures [PROMs]), que ofrecen una visión esencial de la experiencia subjetiva del paciente más allá de los hallazgos endoscópicos o radiológicos. Herramientas como el Sinonasal Outcome Test de 22 ítems (SNOT-22) o la escala NOSE se han utilizado ampliamente en la práctica clínica y la investigación; sin embargo, no son específicas para la RSCcPN y pueden no reflejar síntomas especialmente relevantes de este fenotipo, como la anosmia, las manifestaciones orales o las preocupaciones sobre la recurrencia de la enfermedad y los resultados quirúrgicos, que son más frecuentes e incapacitantes en los pacientes con poliposis nasal en comparación con aquellos con RSC sin pólipos3–5.
Para cubrir esta necesidad, Baiardini et al. desarrollaron el cuestionario Nasal Polyposis Quality of Life (NPQ), un instrumento de 27 ítems diseñado específicamente para medir el impacto físico, emocional y funcional de la RSCcPN6. El NPQ fue desarrollado y validado originalmente en italiano en 2022, demostrando excelentes propiedades psicométricas y fuertes correlaciones con otros PROMs generales de rinopatología. No obstante, hasta la fecha no existe una versión validada en español, a pesar de la relevancia global de las poblaciones hispanohablantes.
La adaptación transcultural de los PROMs no consiste en una mera traducción literal, sino que requiere una validación sistemática que garantice la equivalencia conceptual, semántica y cultural. Las guías internacionales, como las propuestas por Beaton et al., el grupo de trabajo de ISPOR y la iniciativa COSMIN, subrayan la necesidad de una traducción directa e inversa rigurosa, consenso de expertos, prueba piloto y validación psicométrica formal7–9.
El objetivo de este estudio fue realizar la adaptación transcultural y la validación psicométrica de la versión española del cuestionario Nasal Polyposis Quality of Life (NPQ) para su aplicación en los pacientes con RSCcPN. El instrumento está concebido para su uso clínico en el diagnóstico, evaluación del tratamiento y seguimiento longitudinal, tanto quirúrgico como farmacológico.
Materiales y métodosDiseño del estudioSe llevó a cabo un estudio transversal de validación en el Hospital Universitario Público de Jaén, España, entre julio y diciembre de 2024. El protocolo fue aprobado por el Comité de Ética de la Investigación de Andalucía (SICEIA-2024-001376) y todos los participantes firmaron un consentimiento informado por escrito. El estudio se desarrolló conforme a los principios de la Declaración de Helsinki y la normativa nacional vigente.
Traducción y adaptación transculturalEl NPQ original fue desarrollado y validado en italiano. Aunque los resultados fueron publicados en inglés, no se dispone actualmente de una versión oficial validada en ese idioma. Por ello, el presente estudio toma como documento fuente la versión italiana para su traducción y adaptación transcultural al español.
El proceso de traducción siguió las guías internacionales ampliamente aceptadas7–11:
- 1.
Traducción directa: Dos traductores nativos de español con conocimientos médicos realizaron traducciones independientes de la versión original.
- 2.
Síntesis: Un comité de expertos multidisciplinar, formado por especialistas en otorrinolaringología, un metodólogo y un lingüista, elaboró una versión consensuada.
- 3.
Traducción inversa: Dos traductores independientes, nativos del idioma original y ajenos al NPQ, realizaron la traducción inversa al italiano.
- 4.
Revisión por comité de expertos: Se compararon todas las versiones para garantizar la equivalencia conceptual, semántica e idiomática.
Se detectaron discrepancias en un número limitado de ítems durante las fases de revisión experta y traducción inversa. Estas fueron resueltas por consenso y se detallan en el Anexo 1.
- 5.
Prueba piloto: La versión prefinal en español se administró a 20 pacientes con RSCcPN para evaluar claridad, comprensión y adecuación cultural. No fue necesario realizar modificaciones tras este paso.
Se mantuvo el sistema de puntuación original del NPQ (escala tipo Likert de 1 a 5 por ítem, puntuación total de 27 a 135) para asegurar la equivalencia conceptual y métrica con el instrumento original.
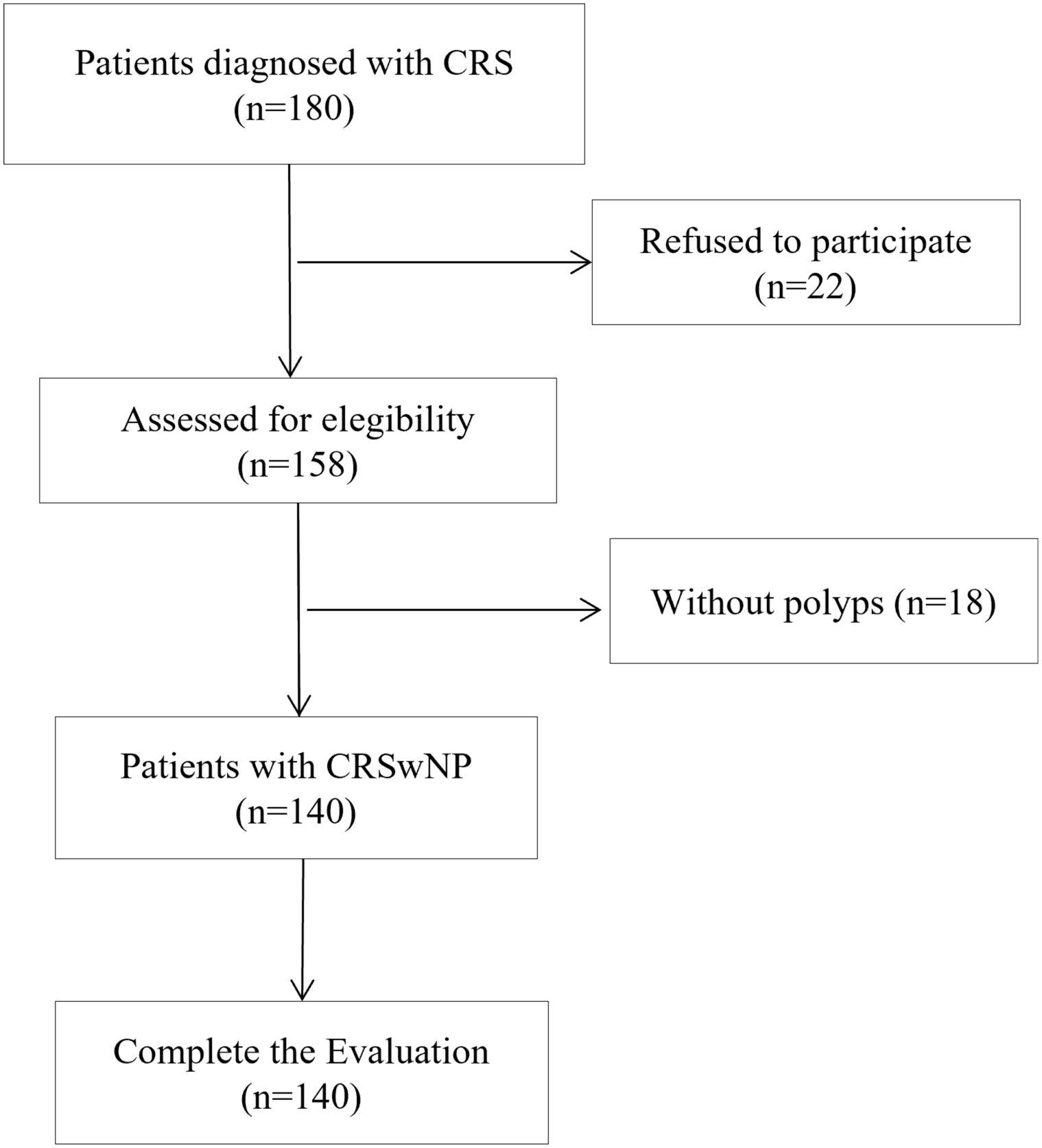
ParticipantesSe reclutaron consecutivamente un total de 140 adultos hispanohablantes nativos con diagnóstico de RSCcPN. El proceso de selección se resume en la figura 1. El diagnóstico fue confirmado por un especialista sénior en otorrinolaringología siguiendo los criterios EPOS 20201.
Criterios de inclusión: Edad ≥18 años, hablantes nativos de español, pólipos nasales bilaterales confirmados por endoscopia o imagen.
Criterios de exclusión: Trastornos del sistema nervioso central, neoplasias activas, infecciones agudas, radioterapia previa en cabeza/cuello o enfermedades sistémicas significativas.
Los datos sociodemográficos (edad, sexo, peso, talla, IMC) fueron registrados por un investigador capacitado. Un subgrupo de 35 participantes volvió a completar el NPQ a los 7-14 días para evaluar la fiabilidad test-retest.
Variables e instrumentosLas variables sociodemográficas recogidas incluyeron: edad (en años), sexo (clasificado como varón, mujer o no binario), peso (en kilogramos), talla (en metros, medida con una báscula médica mecánica Detecto Modelo 2391 con tallímetro), índice de masa corporal (IMC, calculado como peso en kilogramos dividido entre la talla en metros al cuadrado) y diagnóstico médico. Estos datos fueron codificados por un investigador ajeno al diagnóstico clínico y a la selección de los participantes, con el fin de reducir sesgos.
El cuestionario NPQ6 es un PROM de 27 ítems diseñado específicamente para evaluar el impacto de la RSCcPN sobre la calidad de vida relacionada con la salud (CVRS). Cada ítem refleja un síntoma o limitación funcional experimentado en las 2 semanas previas, y se puntúa de 1 («nada») a 5 («mucho»). Las puntuaciones más altas indican mayor deterioro.
Para clarificar el anclaje de respuesta, 1 equivalía a «ningún síntoma» y 5 a «máxima intensidad»; por tanto, la puntuación mínima teórica del NPQ (27 puntos) correspondía a un paciente asintomático, manteniendo equivalencia métrica con el instrumento original.
Análisis estadísticoLos análisis estadísticos se realizaron con IBM SPSS® Statistics para Windows, versión 27 (IBM Corp., Armonk, NY, EE. UU.) y MedCalc® Statistical Software, versión 22.021 (MedCalc Software Ltd., Ostende, Bélgica). Se consideró significación estadística un valor de p bilateral <0,05, y todos los intervalos de confianza (IC) se calcularon al 95%.
Se emplearon estadísticas descriptivas para caracterizar la muestra. Las variables continuas se expresaron como medias y desviaciones estándar; las categóricas, como frecuencias y porcentajes. La normalidad se evaluó mediante la prueba de Kolmogorov-Smirnov.
Los efectos suelo y techo se calcularon como el porcentaje de pacientes que obtuvieron la puntuación mínima (27) o máxima (135); se consideró relevante un valor >15%12.
La validez de constructo se examinó mediante análisis factorial exploratorio (AFE) con componentes principales y rotación Varimax. La adecuación muestral se evaluó con el determinante de la matriz de correlaciones, el índice KMO y la prueba de esfericidad de Bartlett.
Dado que dominios como sueño, fatiga e impacto emocional podían correlacionarse, se consideró esta dependencia potencial al interpretar la estructura y la abordaremos en la fase confirmatoria.
En PROMs suele recomendarse extraer factores y permitir correlación entre dimensiones (rotaciones oblicuas). Se optó por componentes principales con rotación ortogonal (Varimax) por parsimonia y estabilidad en muestras moderadas; se reconocío esta elección como limitación y se planificó una fase confirmatoria con análisis factorial confirmatorio (AFC) que informará CFI, TLI y RMSEA.
La consistencia interna se valoró con el alfa de Cronbach. Se consideraron inaceptables los valores <0,70; aceptables o buenos los valores entre 0,70 y 0,90; y excesivamente redundantes los valores >0,9013.
La fiabilidad test-retest se calculó mediante el coeficiente de correlación intraclase (CCI), empleando un modelo de efectos aleatorios bidireccional con acuerdo absoluto. Los umbrales del CCI fueron: <0,40 pobre; 0,40-0,75 moderado; 0,75-0,90 sustancial; >0,90 excelente. También se calcularon el error estándar de medida (EEM) y el cambio mínimo detectable con un 95% de confianza (CMD95)14.
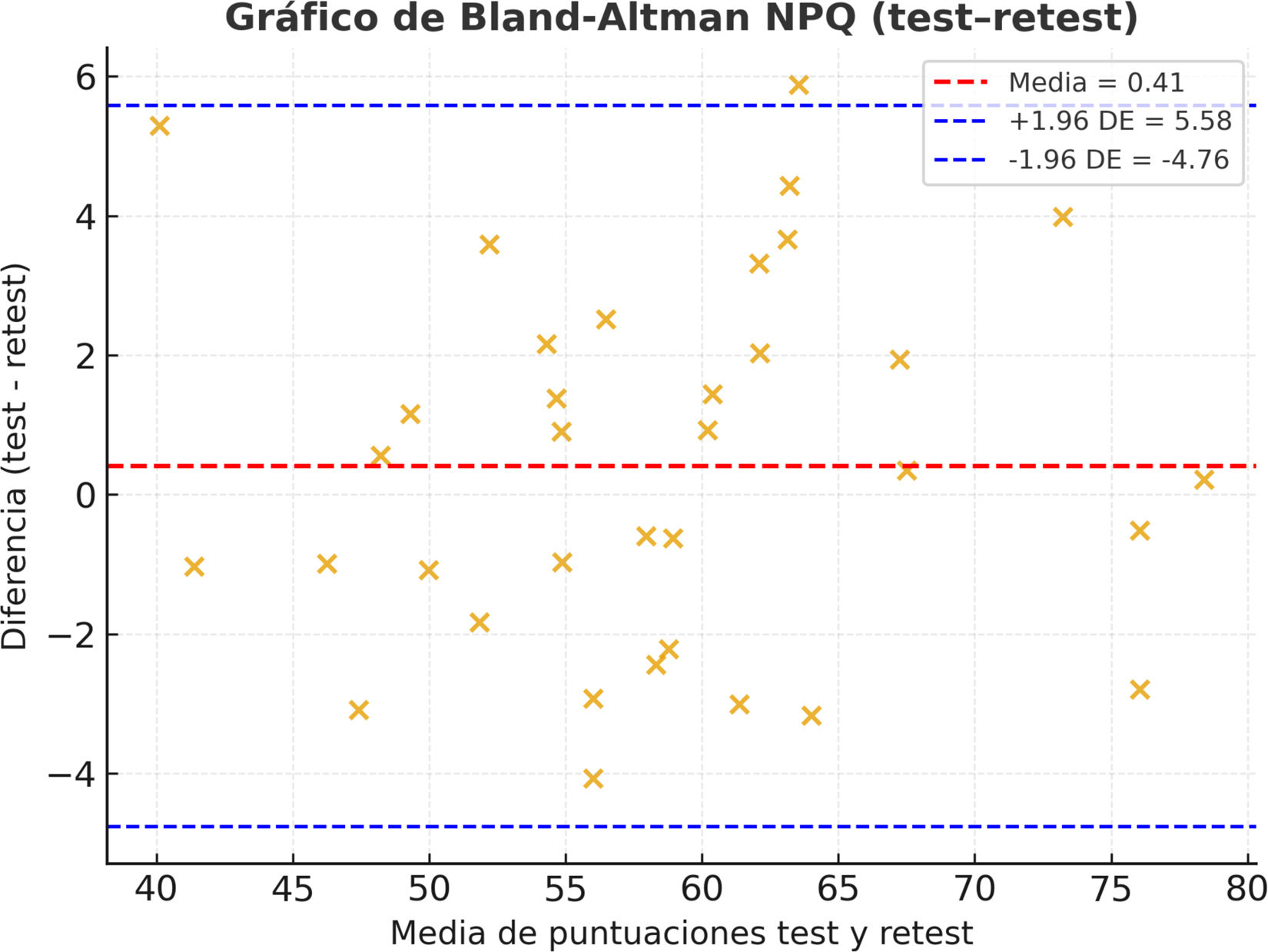
Se incorporó el método de Bland-Altman para la puntuación total, estimando sesgo medio y límites de acuerdo (DE: ±1,96), junto con EEM y CMD95.
La validez concurrente se evaluó correlacionando las puntuaciones del NPQ con las del SNOT-22 y el NOSE-E mediante el coeficiente r de Pearson. Se interpretaron como fuertes las correlaciones >0,50; moderadas entre 0,30-0,50; y débiles <0,3015.
La validez discriminativa se analizó mediante curvas ROC16, empleando como referencia la puntuación total del SNOT-2217. El área bajo la curva (AUC) cuantificó la capacidad del NPQ para identificar una carga sintomática grave. Se interpretaron como excelentes los valores de AUC>0,90; buenos entre 0,70-0,90; bajos entre 0,50-0,70; y no discriminativos ≤0,5018.
A partir del análisis ROC se estableció un punto de corte óptimo, calculando sensibilidad, especificidad, valor predictivo positivo (VPP) y valor predictivo negativo (VPN) correspondientes.
ResultadosEl NPQ en español fue adaptado conforme a las directrices internacionales de adaptación transcultural, tal como se describe en el apartado de Métodos. La fase de prueba piloto confirmó la comprensibilidad y adecuación cultural de la versión prefinal.
Un total de 140 pacientes adultos diagnosticados de RSCcPN participaron en el estudio de validación, con una edad media de 46,36 años (DE±15,02); el 60% eran varones. El índice de masa corporal (IMC) medio fue de 26,8kg/m2 (DE±4,9). Todos los participantes eran hablantes nativos de español y cumplían los criterios diagnósticos EPOS 2020, incluida la presencia de pólipos nasales bilaterales confirmados por endoscopia o imagen. Para evaluar la fiabilidad test-retest, un subgrupo de 35 pacientes completó el NPQ en 2 ocasiones, con un intervalo de 7 a 14 días entre evaluaciones.
No se observaron efectos suelo ni techo significativos.
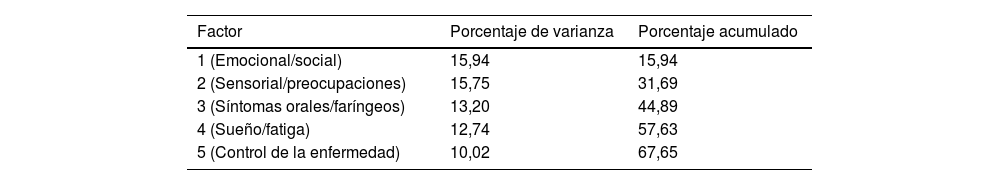
Estructura factorialEl AFE con rotación Varimax y normalización de Kaiser reveló una estructura de 5 factores que explicaban el 67,65% de la varianza total (tabla 1). El determinante de la matriz de correlaciones fue próximo a cero, y tanto el índice KMO como la prueba de Bartlett confirmaron la idoneidad de los datos para el análisis factorial.
Varianza explicada por los factores principales del NPQ
| Factor | Porcentaje de varianza | Porcentaje acumulado |
|---|---|---|
| 1 (Emocional/social) | 15,94 | 15,94 |
| 2 (Sensorial/preocupaciones) | 15,75 | 31,69 |
| 3 (Síntomas orales/faríngeos) | 13,20 | 44,89 |
| 4 (Sueño/fatiga) | 12,74 | 57,63 |
| 5 (Control de la enfermedad) | 10,02 | 67,65 |
NPQ: Nasal Polyposis Quality of Life Questionnaire.
Nota: Se retuvieron 5 factores con valores propios >1, explicando el 67,65% de la varianza total.
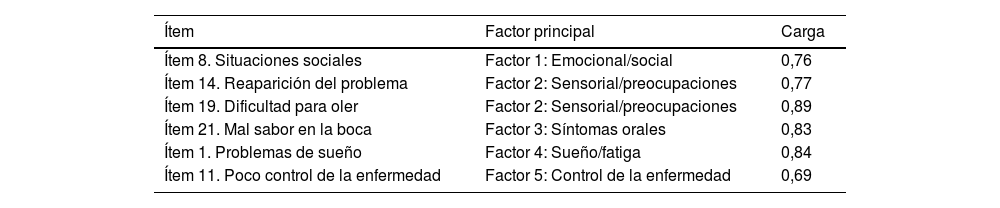
La matriz de componentes rotados (tabla 2) mostró una distribución factorial coherente. Los 5 factores extraídos agruparon ítems correspondientes a:
- 1.
Aspectos emocionales y sociales (p. ej., vergüenza, estrés, preocupación quirúrgica).
- 2.
Síntomas sensoriales (p. ej., alteraciones del olfato y del gusto).
- 3.
Molestias orales y faríngeas (p. ej., boca seca, mal sabor).
- 4.
Trastornos del sueño y fatiga.
- 5.
Control de la enfermedad y manejo sintomático.
Matriz de componentes rotados (cargas principales por ítem)
| Ítem | Factor principal | Carga |
|---|---|---|
| Ítem 8. Situaciones sociales | Factor 1: Emocional/social | 0,76 |
| Ítem 14. Reaparición del problema | Factor 2: Sensorial/preocupaciones | 0,77 |
| Ítem 19. Dificultad para oler | Factor 2: Sensorial/preocupaciones | 0,89 |
| Ítem 21. Mal sabor en la boca | Factor 3: Síntomas orales | 0,83 |
| Ítem 1. Problemas de sueño | Factor 4: Sueño/fatiga | 0,84 |
| Ítem 11. Poco control de la enfermedad | Factor 5: Control de la enfermedad | 0,69 |
Nota: Se muestran solo las cargas >0,30. Los ítems se agrupan en 5 factores conceptualmente coherentes.
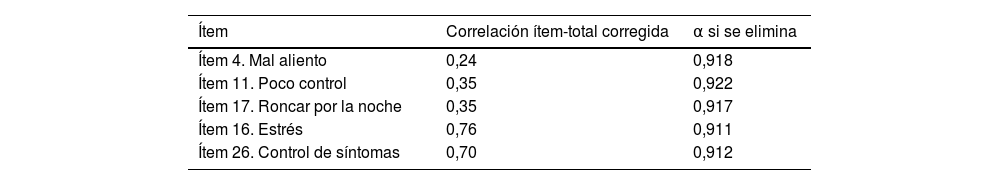
La consistencia interna global del NPQ fue excelente, con un coeficiente alfa de Cronbach de 0,917. Las correlaciones ítem-total corregidas oscilaron entre 0,24 y 0,76. La eliminación de cualquier ítem individual no mejoró significativamente el valor alfa global (tabla 3). El análisis ítem a ítem reveló que los ítems 4 y 11 presentaban valores de correlación ítem-total ligeramente inferiores, aunque dentro de un rango aceptable.
Análisis ítem a ítem (resumen)
| Ítem | Correlación ítem-total corregida | α si se elimina |
|---|---|---|
| Ítem 4. Mal aliento | 0,24 | 0,918 |
| Ítem 11. Poco control | 0,35 | 0,922 |
| Ítem 17. Roncar por la noche | 0,35 | 0,917 |
| Ítem 16. Estrés | 0,76 | 0,911 |
| Ítem 26. Control de síntomas | 0,70 | 0,912 |
Nota: Los ítems 4, 11 y 17 presentaron correlaciones más bajas, aunque aceptables. Ningún ítem mejoró el alfa global al eliminarlo (α=0,917).
El intervalo real fue de 7-14 días y no se produjeron cambios clínicos ni terapéuticos entre administraciones.
El CCI para la fiabilidad test-retest fue de 0,991 (IC 95%: 0,983-0,996), lo que indica una excelente reproducibilidad. El EEM fue de 2 puntos, y el CMD95 de 5 puntos.
El diagrama de Bland-Altman (fig. 2) se presentó como complemento a los parámetros de error de medida, mostrando EEM=2 y CMD95=5 puntos.
Validez concurrenteLas puntuaciones del NPQ se correlacionaron fuertemente con las del NOSE-E (r=0,802; p<0,001) y del SNOT-22 (r=0,870; p<0,001), lo que respalda la validez concurrente del instrumento.
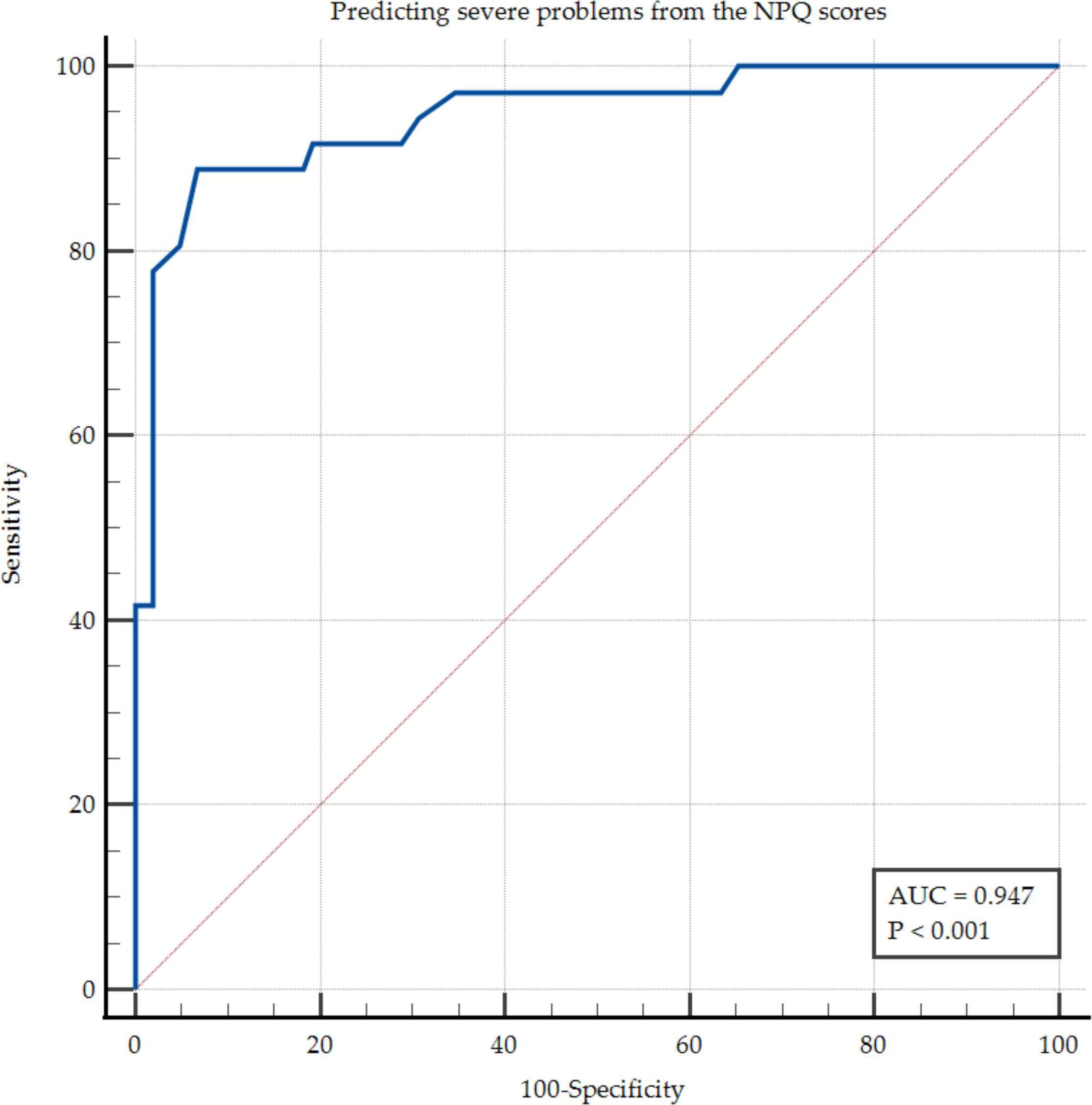
Validez discriminativa y punto de corteEl NPQ mostró una alta precisión para identificar a los pacientes con impacto sintomático grave. El área bajo la curva ROC (AUC) fue de 0,947 (IC 95%: 0,896-0,978; p<0,001), indicando una excelente capacidad discriminativa. Se identificó un punto de corte óptimo de >41 puntos como umbral de discapacidad severa (fig. 3).
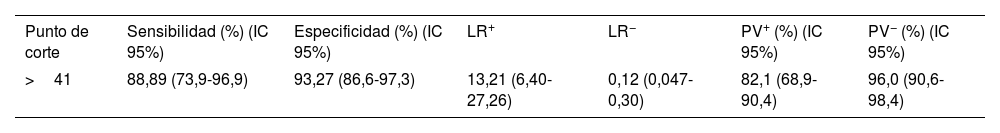
Con este umbral, la sensibilidad fue del 88,89% y la especificidad del 93,27%. La tabla 4 muestra los valores predictivos y los cocientes de probabilidad derivados del análisis ROC.
Valores predictivos derivados del análisis de la curva ROC
| Punto de corte | Sensibilidad (%) (IC 95%) | Especificidad (%) (IC 95%) | LR+ | LR− | PV+ (%) (IC 95%) | PV− (%) (IC 95%) |
|---|---|---|---|---|---|---|
| >41 | 88,89 (73,9-96,9) | 93,27 (86,6-97,3) | 13,21 (6,40-27,26) | 0,12 (0,047-0,30) | 82,1 (68,9-90,4) | 96,0 (90,6-98,4) |
IC 95%: intervalo de confianza del 95%; LR: razón de verosimilitud; PV: valor predictivo.
La consistencia interna del instrumento, medida mediante el alfa de Cronbach, alcanzó un valor de 0,917, lo que indica un alto grado de homogeneidad interna, aunque con un ligero grado de redundancia. Este resultado es coherente con el estudio original en italiano (α=0,93)6 y se alinea con otros instrumentos validados como el SNOT-22, cuya consistencia interna varía entre 0,83 y 0,94 en diferentes versiones lingüísticas4,19. Este nivel de consistencia sugiere que la versión española mantiene la cohesión conceptual del instrumento original, conservando además la claridad lingüística en la población diana.
Pese al alfa elevado, los ítems cubren dominios diferenciados y la eliminación de ítems no mejoró sustantivamente el coeficiente (tabla 3), por lo que se mantuvo la versión completa.
La estructura de 5 factores extraída del análisis factorial explicó el 67% de la varianza total. La distribución factorial resultó conceptualmente coherente, agrupando ítems en dimensiones que reflejan alteraciones sensoriales (olfato, gusto), impacto psicológico (estrés, vergüenza), limitación funcional (sueño, fatiga), síntomas orales (boca seca, mal sabor) y control de la enfermedad (preocupaciones sobre el manejo sintomático y la medicación). Esta estructura multidimensional subraya la capacidad del NPQ para captar la complejidad de la carga sintomática en la RSCcPN. Aunque los autores del NPQ original también identificaron múltiples dominios, nuestro análisis refina la estructura en población hispanohablante, sugiriendo una posible influencia cultural en la agrupación de los ítems.
El análisis de fiabilidad test-retest mostró un CCI de 0,991, lo que confirma la excelente estabilidad temporal del cuestionario. Este es uno de los valores más altos reportados en validaciones comparables: por ejemplo, el SNOT-22 en italiano mostró un CCI de 0,8519, la versión española un CCI de 0,874, la versión árabe del CRS-PRO un CCI de 0,9120 y la versión española del CRS-PRO también demostró una excelente reproducibilidad21. El EEM y el CMD95, estimados en 2 y 5 puntos respectivamente, sugieren una precisión excelente para monitorizar cambios clínicos a lo largo del tiempo.
La validez concurrente se confirmó mediante fuertes correlaciones positivas con el NOSE-E (r=0,802) y el SNOT-22 (r=0,870), lo que indica que el NPQ en español es altamente coherente con otras medidas de calidad de vida ampliamente utilizadas en rinología. Si bien esto demuestra la validez convergente del instrumento con herramientas generales, también resalta la necesidad de contar con cuestionarios específicos para la RSCcPN como el NPQ, capaces de reflejar síntomas no capturados por instrumentos más generales.
Asimismo, el NPQ en español mostró una alta precisión para identificar pacientes con impacto sintomático grave. El AUC fue de 0,947. Un punto de corte de >41 puntos proporcionó una sensibilidad del 88,9% y una especificidad del 93,3%, lo que subraya su utilidad clínica como herramienta de cribado de gravedad e instrumento de seguimiento de resultados terapéuticos. Estos valores son comparables o incluso superiores a los reportados por otros instrumentos específicos para RSC: por ejemplo, la versión francesa del SNOT-22 informó un AUC de 0,9322, la versión española de 0,914, la versión chilena de 0,86123 y el CRS-PRO validado en árabe (AUC=0,85)20, francés24 y español21. El umbral de >41 puntos puede servir como referencia práctica en protocolos clínicos para identificar candidatos a cirugía o tratamiento médico intensivo.
Desde una perspectiva práctica, el NPQ es conciso (27 ítems), autoadministrado y muy bien aceptado por los pacientes, como lo demuestra la ausencia de datos perdidos o dificultades de comprensión en la prueba piloto. Aunque es ligeramente más extenso que el ampliamente utilizado SNOT-22, el NPQ incluye dominios especialmente relevantes para pacientes con poliposis nasal, como la pérdida olfativa, los efectos secundarios de la medicación o el control de la enfermedad, aspectos no recogidos por instrumentos más generales. Esto lo hace especialmente valioso en los pacientes con enfermedad avanzada, indicación quirúrgica o necesidad de seguimiento longitudinal.
El NPQ-ES complementa a SNOT-22 y NOSE-E porque se centra en la calidad de vida específica de la poliposis y recoge con mayor sensibilidad dominios que suelen quedar en segundo plano: olfato/gusto, molestias orales, control percibido de la enfermedad y preocupaciones (recurrencia, resultado quirúrgico, medicación). Este enfoque mas centrado en la calidad de vida resulta especialmente útil cuando la permeabilidad nasal es adecuada, pero persisten anosmia o hipogeusia, en la selección y priorización de terapias biológicas cuando el impacto funcional es desproporcionado respecto a la obstrucción, y en el seguimiento postquirúrgico para identificar residuo de carga en la calidad de vida, entre otros contextos de práctica clínica.
Este estudio presenta diversas fortalezas, entre ellas un proceso de traducción riguroso basado en guías internacionales como las de Beaton et al.7 y el grupo de trabajo de ISPOR8, un tamaño muestral robusto que supera las recomendaciones estándar (5 participantes por ítem), y un análisis psicométrico completo. Además, la inclusión del análisis test–retest y el modelo ROC refuerzan la aplicabilidad clínica de los resultados.
Sin embargo, deben reconocerse algunas limitaciones. En primer lugar, la validación se realizó en un único centro en España, lo que puede limitar la generalización a otras poblaciones hispanohablantes de diferentes países o contextos culturales. En segundo lugar, aunque el NPQ mostró una fuerte validez transversal, no se evaluó su sensibilidad al cambio ni su capacidad de respuesta a tratamientos, aspectos que deben abordarse en futuras investigaciones.
La validación se realizó en un único centro, lo que limita la generalización. Proponemos validación multicéntrica y multinacional (España y Latinoamérica), incluyendo análisis de invariancia y un AFC con índices de ajuste.
Las líneas futuras de investigación incluyen la validación externa en otras poblaciones hispanohablantes (p. ej., América Latina), la evaluación de la sensibilidad al cambio ante intervenciones médicas y quirúrgicas, y el estudio de correlaciones con marcadores clínicos objetivos (endoscopia, puntuaciones TC, pruebas olfativas). Asimismo, podría explorarse la invariancia transcultural mediante análisis multigrupo y perfeccionar la estructura de dominios mediante análisis factorial confirmatorio.
FinanciaciónEsta investigación no recibió financiación específica por parte de agencias del sector público, comercial o sin ánimo de lucro.
Consideraciones éticasEl estudio fue aprobado por el Comité de Ética de la Investigación de Andalucía (SICEIA-2024-001376) y todos los participantes firmaron consentimiento informado por escrito.
Contribución de los autoresMontilla-Ibáñez MA: Participó en el reclutamiento de pacientes, coordinó la recogida de datos y contribuyó a la redacción inicial del manuscrito.
García-Fernández JM: Concibió el estudio, supervisó el proceso de adaptación transcultural, coordinó al equipo de investigación y lideró la redacción final del manuscrito.
Sánchez-Torices MS: Realizó los análisis estadísticos, preparó tablas y figuras, y revisó los apartados de resultados y discusión.
Gómez-Gallego MP: Asistió en el desarrollo metodológico, supervisó la gestión de datos y revisó críticamente el manuscrito por su contenido intelectual.
Feliz-Fernández MA: Participó en el consenso del comité de expertos y en la prueba piloto, colaboró en la resolución de equivalencias de traducción y en la revisión del manuscrito.
Lomas-Vega R: Proporcionó orientación metodológica durante todo el proceso de validación, supervisó los procedimientos estadísticos y aprobó la versión final del manuscrito.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Disponibilidad de los datosLos datos que respaldan los hallazgos de este estudio están disponibles previa solicitud razonable al autor de correspondencia.