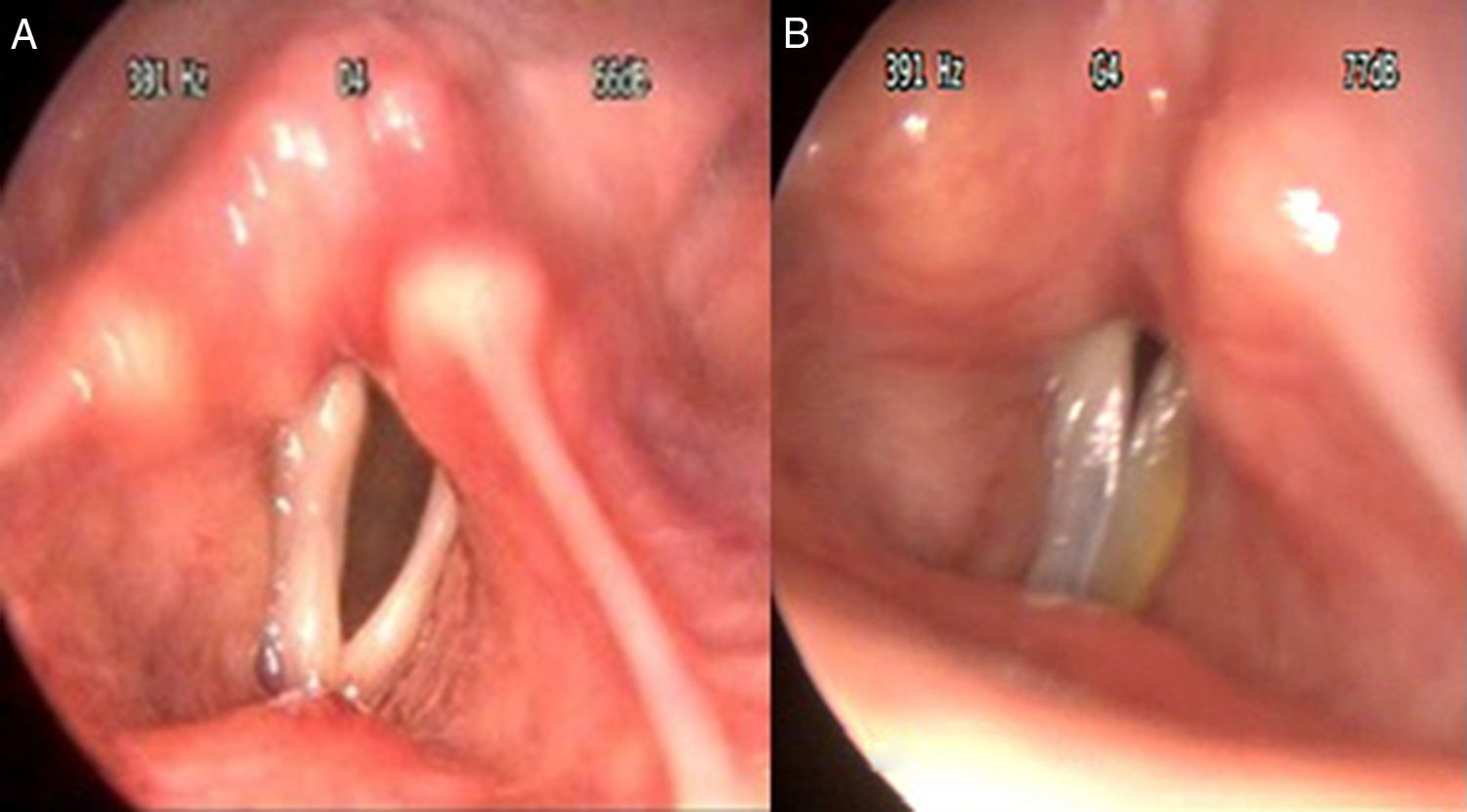
Evaluar la efectividad de la laringoplastia de inyección con ácido hialurónico guiada por electromiografía en la etapa precoz de la parálisis unilateral de cuerda vocal en función de la mejoría de la disfonía y de la calidad de vida del paciente.
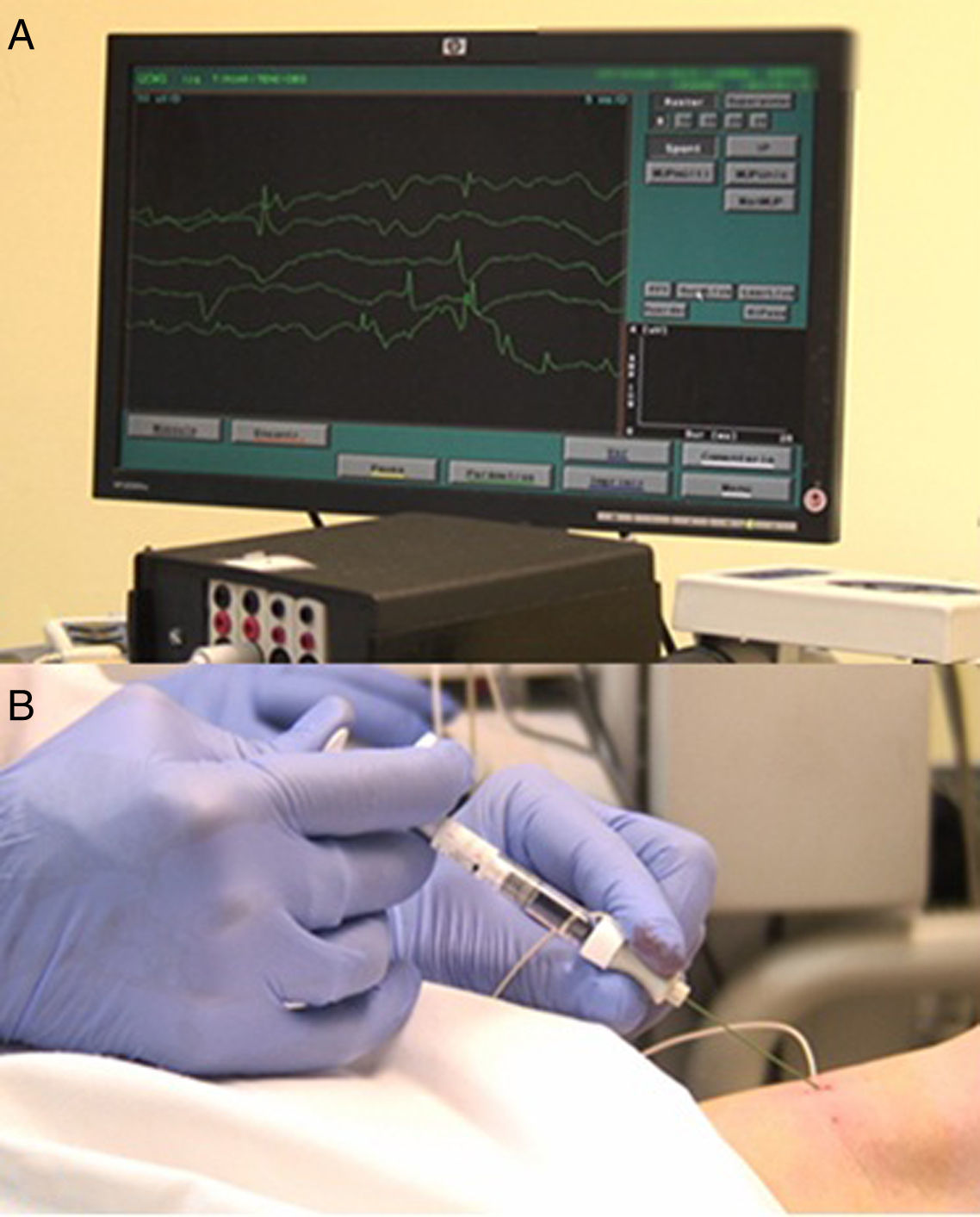
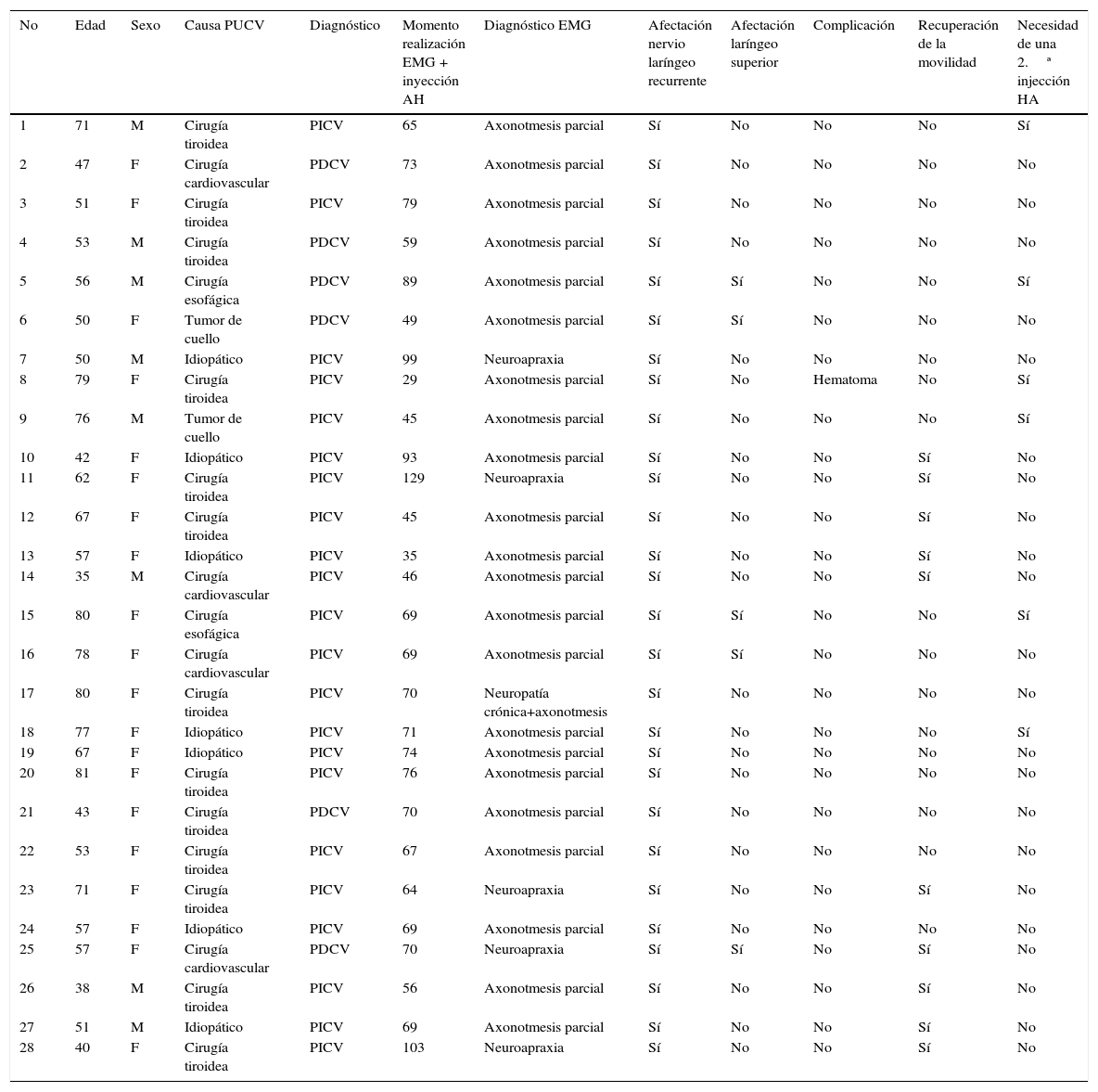
MétodosSe realizó estudio electromiográfico y laringoplastia de inyección con ácido hialurónico a 28 pacientes con parálisis unilateral de cuerda vocal entre diciembre del 2013 y diciembre del 2014. Se analizaron los resultados del cuestionario de índice de incapacidad vocal, escala de GRABS,tiempo máximo de fonación y valoración videoestroboscópica, preintervención, a los 15 días y a los 6 meses, con el Wilcoxon rank test no paramétrico.
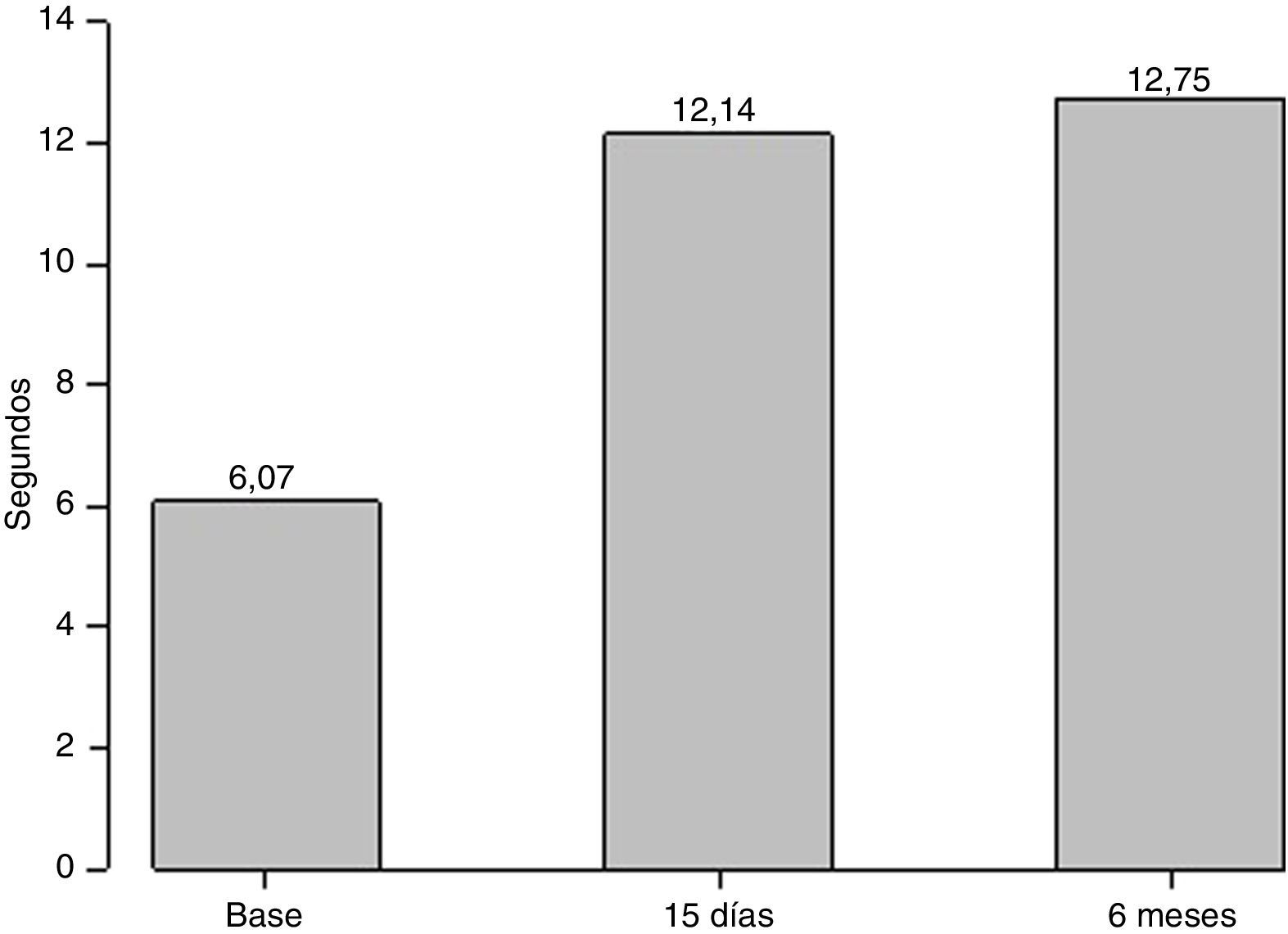
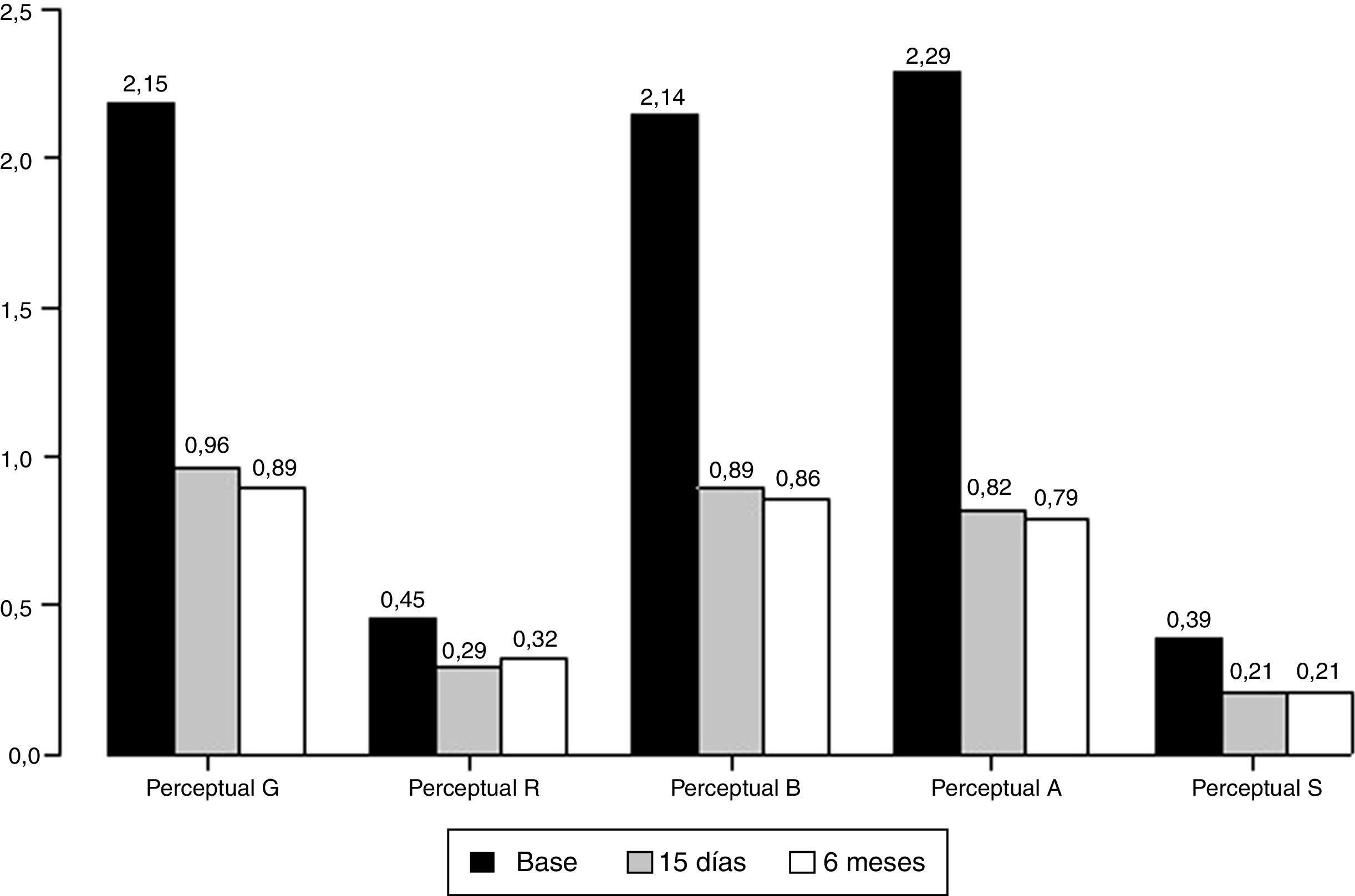
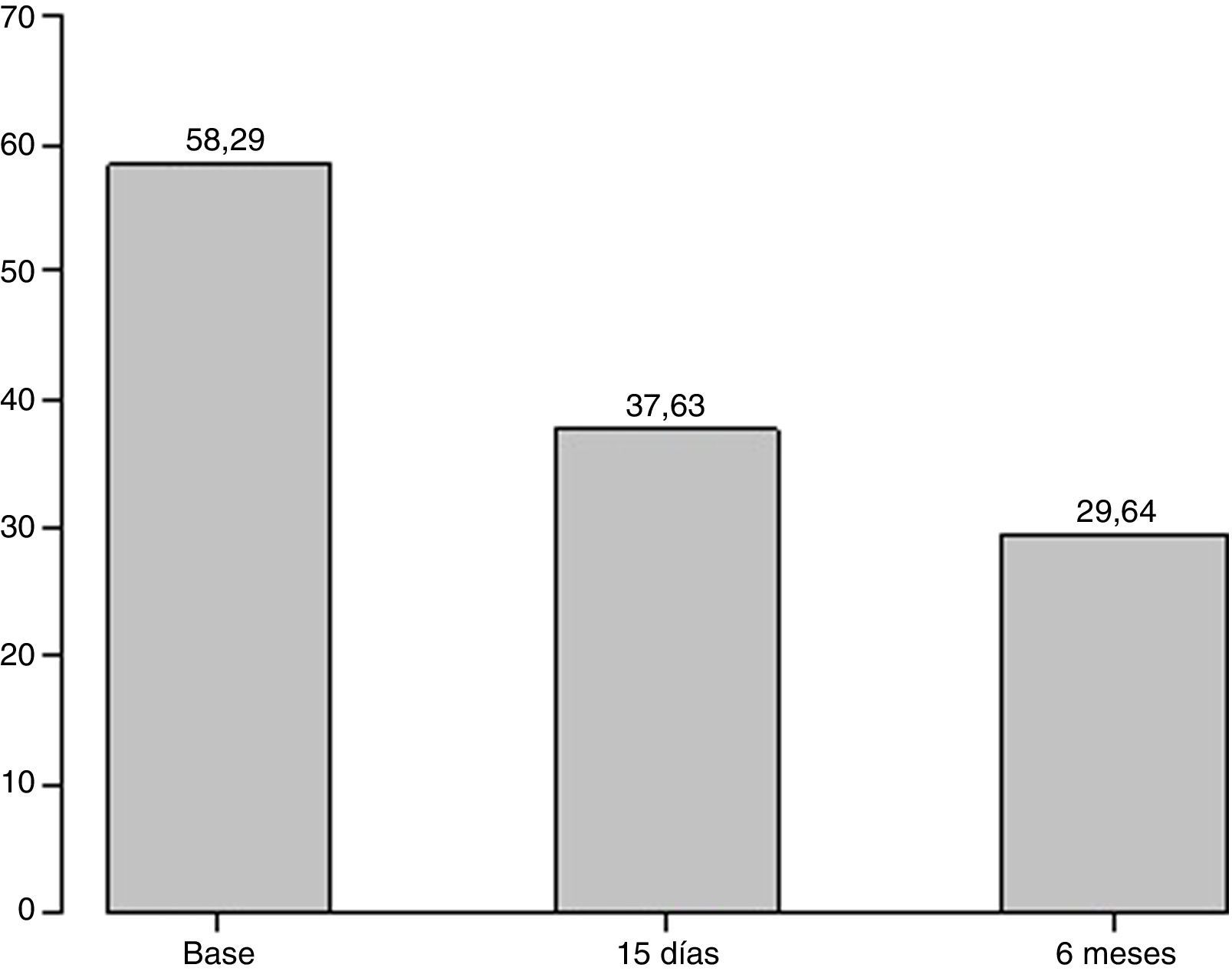
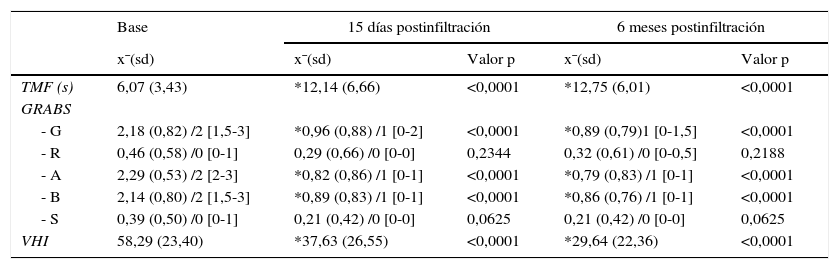
ResultadosDe los 28 pacientes, 1 tuvo un hematoma en la cuerda vocal infiltrada (3,57%) y 6 requirieron una segunda infiltración. Los parámetros evaluados muestran una mejoría estadísticamente significativa a los 15 días y 6 meses postinfiltración; el tiempo máximo de fonación aumentó de 6,07 a 12,14 seg.(15 días), 12,75 (6 meses); la escala de GRABS muestra una mejoría estadísticamente significativa en los parámetros de G, B y A. El valor del índice de incapacidad vocal se redujo de 58,29 a 37,63 (15 días) y 29,64 (6 meses).
ConclusionesLa laringoplastia de inyección guiada por electromiografía en la etapa precoz de parálisis unilateral de cuerda vocal proporciona, en un mismo acto, la evaluación neuromuscular y el tratamiento temporal del defecto de cierre glótico con bajo riesgo de complicaciones y mejoría de la calidad de vida del paciente. Podría disminuir la necesidad de tratamientos ulteriores, aunque son necesarios estudios con más pacientes.
To assess the effectiveness of electromyography-guided hyaluronic acid injection laryngoplasty in the early stage of unilateral vocal fold paralysis in terms of patient recovery from dysphonia and quality of life.
MethodsBetween January and December 2014, 28 patients with unilateral vocal fold paralysis underwent electromyography and injection of hyaluronic acid in the thyroarytenoid muscle. We compared the voice handicap index, grade, roughness, breathiness, asthenia, strain scale (GRBAS), videostroboscopic parameters and maximum phonation time assessed before, 15 days and 6 months after the intervention, using the non-parametric Wilcoxon rank test.
ResultsOut of the 28 patients, 1 had a haematoma in the injected vocal fold (3.57%) and 6 required second injections. The maximum phonation time of the vowel /e/ increased from 6.07 to 12.14 sec. (15 days post-intervention) and subsequently 12.75 (6 months post-intervention). There was also a significant improvement in the grade, roughness, breathiness, asthenia, strain scale in parameters G, B and A both 15 days and 6 months after the intervention. The voice handicap index score decreased from 58.29 to 37.63 (15 days post-intervention) and 29.64 (6 months post-intervention).
ConclusionsElectromyography-guided hyaluronic injection laryngoplasty in unilateral vocal fold paralysis enables, in the same intervention, neuromuscular assessment and temporary treatment of glottic insufficiency with a low risk of complications and improvement in patient's quality of life. This may reduce the need for subsequent treatments, but further research is required to confirm these findings.