SONOLÊNCIA RESIDUAL EM PACIENTE COM SÍNDROMA DE APNEIA/HIPOPNEIAS DE SONO TRATADOS COM CPAP: AVALIAÇÃO E TRATAMENTO
RESUMO
A pressão positiva contínua na via aérea (CPAP) é um tratamento eficaz para a maioria dos pacientes com síndroma de apneia/hipopneia de sono (SAHS), melhorando a sonolência, função cognitiva e o humor. Contudo, um certo número de pacientes continuam queixando-se de sonolência após o CPAP. Nestes casos é recomendável refazer a história clínica, confirmar o diagnóstico de SAHS, comprovar o grau de adesão ao tratamento e descartar trnstornos de sono associados como uma parca higiene de sono, depressão, narcolepsia ou hipersomnia idiopática. Se necessário deve-se repetir o estudo posissonográfico (PSG) seguido de um teste de latências multiplas de sono (MSLT) ou então realizar a PSG completa com titulação do CPAP. Estudos experimentais em animais parecem sugerir que a hipóxia intermitente crónica produzida pelas apneias poderia deteriorar as estruturas cerebrais que regulam a vigília. Se esta alteração estiver presente em humanos poderia ser outra causa da sonolência resigual apesar do CPAP. Está comprovado que o modafinil reduz a sonolência subjectiva após CPAP em paciente com SAHS.
Palavras-chave: Pressão positiva contínua na via aérea. Sindroma da apneia/hipopneia de sono. Sonolência residual. Depressão. Narcolepsia. Hipersomnia idiopática.
CONSIDERACIONES GENERALES
La presión positiva continua de la vía aérea (CPAP) es un tratamiento efectivo para la mayoría de los pacientes con síndrome de apneas-hipopneas durante el sueño (SAHS). La CPAP reduce la fragmentación del sueño, las desaturaciones de oxihemoglobina y la somnolencia diurna excesiva (SDE), además de mejorar la función cognitiva y psicosocial1,2. La mejoría suele ocurrir poco después de iniciar el tratamiento con CPAP y se mantiene en el tiempo. Hay algunos pacientes, sin embargo, en quienes, a pesar de una reducción importante en las alteraciones respiratorias durante el sueño con la CPAP, la somnolencia diurna mejora escasamente. Este problema no es infrecuente en la práctica clínica diaria, aunque su prevalencia no fue bien documentada. Conocemos sólo un estudio en el cual se describió que "cansancio, fatiga y/o somnolencia" persistieron en el 5% de 4.218 pacientes con SAHS después del tratamiento apropiado con CPAP en la mayoría de los casos3. En los últimos años se han realizado algunos ensayos clínicos con medicamentos estimulantes en este grupo de pacientes4-6, que enfatizan la importancia de este problema.
Cuando nos enfrentamos a un paciente tratado con CPAP que presenta somnolencia persistente es imprescindible realizar una revisión de su historia clínica para confirmar el diagnóstico de SAHS y verificar que la presión y el cumplimiento son adecuados. Además, se deben excluir problemas asociados, como la mala higiene del sueño, el tratamiento con medicamentos sedantes o una alteración del sueño coexistente no diagnosticada, como narcolepsia. Sin embargo, después de excluir todos estos factores, hay un grupo de pacientes con SAHS tratados con CPAP que continúan con somnolencia.
¿Cuál es la explicación? Hay varios aspectos que hay que considerar:
La somnolencia en el SAHS no es producida sólo por las apneas
Se suele considerar que las apneas durante el sueño son la única causa de somnolencia, ya que usualmente interrumpen la continuidad del sueño, y la fragmentación del sueño ocasiona somnolencia en personas sanas. La somnolencia, sin embargo, no es una consecuencia inevitable del SAHS. De hecho, el SAHS es un factor de riesgo para somnolencia más que su causa directa7. Por ejemplo, la prevalencia de un índice apnea/hipopnea (IAH) > 5 es del 17-24% en la población masculina, pero la prevalencia de IAH > 5 y somnolencia diurna es sólo del 3,1-4,1%7. No hay una relación estrecha entre el IAH y la somnolencia medida con la prueba de latencias múltiples del sueño (MSLT), la prueba de mantenimiento de la vigilia (MWT) o la escala de somnolencia de Epworth8,9. El rango de vigilia diurna es amplio en todos los niveles de la apnea del sueño8, lo que sugiere que existen otros mecanismos que participan en la inducción de somnolencia en los pacientes con SAHS. Por ejemplo, la obesidad10 y el ronquido11, dos hallazgos comunes en los pacientes con SAHS, se asocian con SDE, independientemente del índice de alteración respiratoria. Aunque el ronquido desaparece con la CPAP, la obesidad usualmente no cambia con este tratamiento, lo cual, al menos en parte, podría explicar esta somnolencia residual. La somnolencia residual después de la CPAP no parece resultar de la fragmentación persistente del sueño, de los movimientos periódicos de las piernas durante el sueño (PLMS)12 o de la hipoxemia previa al tratamiento con la CPAP (al menos la hipoxemia medida durante el estudio basal del sueño)13. Finalmente, se debe señalar que la somnolencia es un síntoma común en la población general, y probablemente resulta de la privación de sueño. Este tipo de somnolencia no mejora con la CPAP.
La somnolencia en el SAHS persiste a pesar de la CPAP
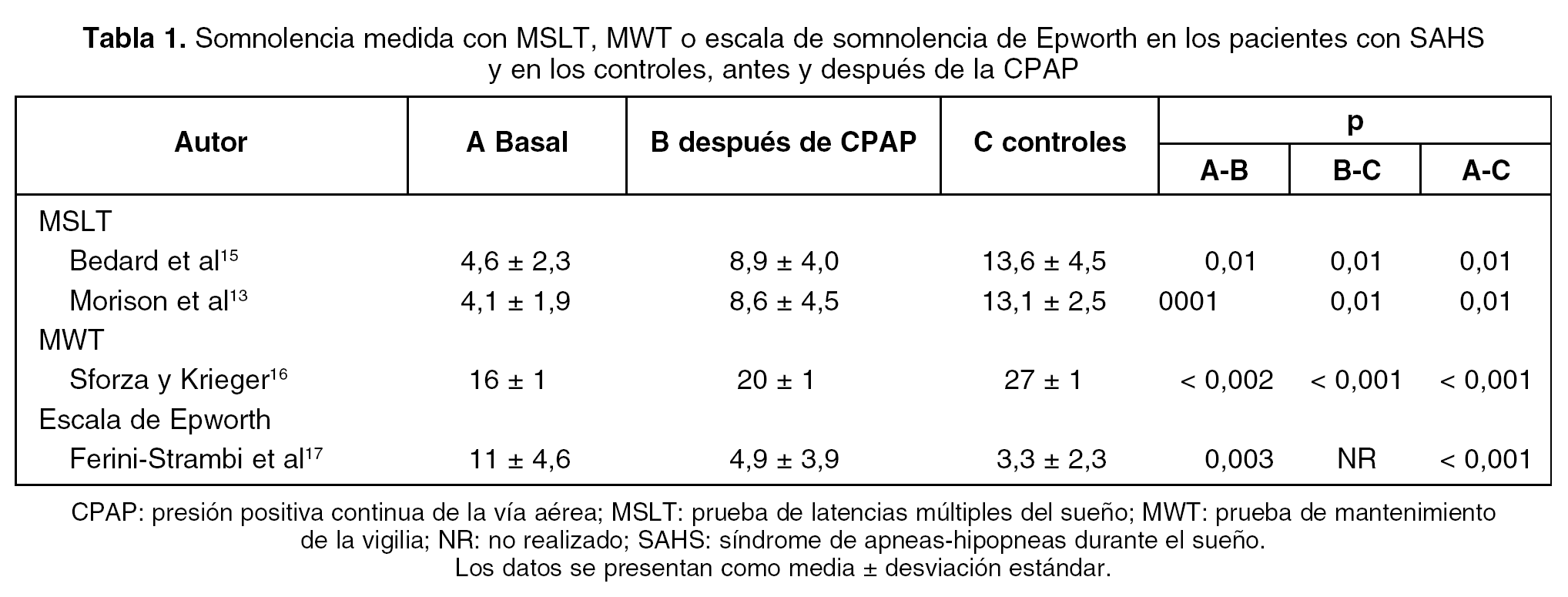
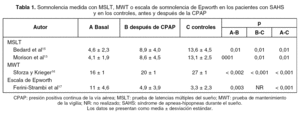
La CPAP reduce la somnolencia más que el placebo en el SAHS14, con una reducción media en la puntuación de la escala de somnolencia de Epworth de 4,75 puntos y un incremento en la media de MSLT/MWT de 0,93 min. Esto es consistente con la experiencia clínica de muchos pacientes que refieren una mejoría significativa de su somnolencia con la CPAP. Sin embargo, los escasos estudios que han medido la somnolencia después de la CPAP y la comparan con controles sanos (tabla 1) ponen de manifiesto que la somnolencia en los pacientes tratados permanece mayor que en los controles, incluso aunque los pacientes no se quejen de somnolencia.
Otros estudios han puesto de manifiesto que los valores de MSLT/MWT después de la CPAP siguen siendo anormales18-21, resultado que es menos evidente utilizando la escala de somnolencia de Epworth1,2. Aunque es necesaria mayor información, esto sugiere que hay otros factores, además de las apneas, que participan en la somnolencia, tanto antes como después del tratamiento con CPAP.
¿Evaluamos correctamente la respuesta a la CPAP?
La mayoría de las medidas que utilizamos en la práctica diaria para evaluar la respuesta al tratamiento con la CPAP no son objetivas. Simplemente preguntamos al paciente cómo se siente comparado con su situación antes del tratamiento, particularmente en relación con el sueño nocturno y la somnolencia diurna. Este procedimiento difiere de los utilizados en otras alteraciones médicas (diabetes, hepatopatías, anemia, insuficiencia renal, etc.), donde los exámenes de laboratorio son utilizados rutinariamente para medir la respuesta al tratamiento. Se desconoce la variabilidad de las mediciones objetivas en los pacientes tratados con CPAP, ya que no se utilizan habitualmente en el seguimiento de la respuesta al tratamiento.
¿Qué se entiende por somnolencia residual?
La somnolencia no es un concepto claro y puede reflejar diferentes estados12. Igual que el hambre o la sed, es una experiencia básica y universal que es difícil de definir y medir. Aunque hay un gran número de técnicas que miden la somnolencia, no hay un método que sea definitivo. Tanto los métodos objetivos como los subjetivos tienen sus limitaciones. Un hallazgo consistente en los estudios que miden los efectos de la CPAP en la función neuropsicológica es la presencia de mejoría en el estado anímico1, pero se desconoce si la mejoría en el estado de ánimo y en la somnolencia van paralelas en todos los pacientes. Los pacientes deprimidos pueden describir la carencia de energía o empuje, que es típica de la depresión, como "somnolencia" 22, a pesar de tener resultados normales en el MSLT.
Guilleminault y Philip3 encontraron que el MSLT es normal y la escala de somnolencia de Epworth es ligeramente anormal en la mayoría de los pacientes con "somnolencia, cansancio o fatiga" después de la CPAP. Bardwell et al23 encontraron que los síntomas depresivos están claramente asociados a quejas de fatiga en los pacientes con SAHS, independientemente del IAH. Por tanto, es posible que la queja de "somnolencia" persistente después de la CPAP sea, en parte, una descripción de la ausencia de mejoría en el estado anímico.
La gravedad de la somnolencia residual en los pacientes con SAHS tratados con CPAP que no tienen otros trastornos de sueño asociados es probablemente menor que la que ocurre en la narcolepsia o en el SAHS no tratado, particularmente cuando la somnolencia es medida objetivamente. Por ejemplo, en la mayoría de los pacientes con "somnolencia, cansancio o fatiga" post-CPAP, la escala de somnolencia de Epworth fue sólo ligeramente anormal y el MSLT fue normal3. En los 3 estudios de tratamiento de somnolencia residual después de la CPAP con modafinil4-6, la puntuación media basal en la escala de somnolencia de Epworth fue alrededor de 14-16, mientras que el MSLT (alrededor de 7 min) o el MWT (14-16 min) fueron claramente menos anormales que en los pacientes con SAHS no tratados (véase tabla 1) o con narcolepsia (MSLT = 3,3 min; MWT = 5,1 min)24.
PRESENTACION CLINICA DEL PACIENTE CON SOMNOLENCIA RESIDUAL POST-CPAP
La somnolencia persistente después de la CPAP puede aparecer clínicamente en 2 formas, cada una con causas diferentes:
1. El paciente que nunca experimenta una mejoría significativa en la somnolencia con la CPAP. Esto puede deberse a:
Diagnóstico incorrecto del SAHS.
Tratamiento con CPAP inadecuado.
Condiciones asociadas no diagnosticadas (pobre higiene de sueño, depresión, otras alteraciones del sueño, simulación de mejoría).
Otras causas desconocidas.
2. El paciente que inicialmente mejora con la CPAP, pero después de un período regresa otra vez la somnolencia. Esta situación puede aparecer en las siguientes circunstancias:
Pérdida del buen cumplimiento previo (desarrollo de rinitis, nuevo compañero de cama con pobre tolerancia a la máquina).
Incremento de peso.
Desarrollo de una nueva condición asociada (pobre higiene de sueño, depresión, otras alteraciones del sueño, simulación de mejoría).
Pérdida del efecto luna de miel/placebo que revela condiciones asociadas no diagnosticadas previamente.
CAUSAS DE SOMNOLENCIA RESIDUAL POST-CPAP
Tratamiento deficiente del SAHS
Diagnóstico incorrecto del SAHS
El diagnóstico incorrecto del SAHS puede ser una causa de somnolencia persistente después de la CPAP. Es de gran importancia una historia clínica adecuada. El diagnóstico correcto del SAHS no se puede realizar solamente con una máquina, sigue requiriendo de un médico. En la evaluación nocturna de los pacientes con SAHS, se deben considerar 2 pruebas diagnósticas diferentes: la polisomnografía (PSG) estándar y los estudios simplificados, como la poligrafía respiratoria (PR). La historia clínica deberá determinar el tipo de estudio que se realizará en cada paciente. Aunque la PSG se considera el estándar de oro para el diagnóstico de SAHS, la gran prevalencia de esta alteración y sus consecuencias sobre la salud han promovido el desarrollo de nuevas estrategias para su diagnóstico. Los estudios simplificados son una vía para resolver este problema, al menos en parte. Debe señalarse, no obstante, que el registro cardiopulmonar ambulatorio tiene algunas limitaciones y puede ser impreciso, especialmente en los casos leves25. Cuando el médico no está familiarizado con las limitaciones de estas técnicas, el diagnóstico de SAHS puede ser erróneo y, por tanto, no funcionará la CPAP.
Tratamiento con CPAP inadecuado
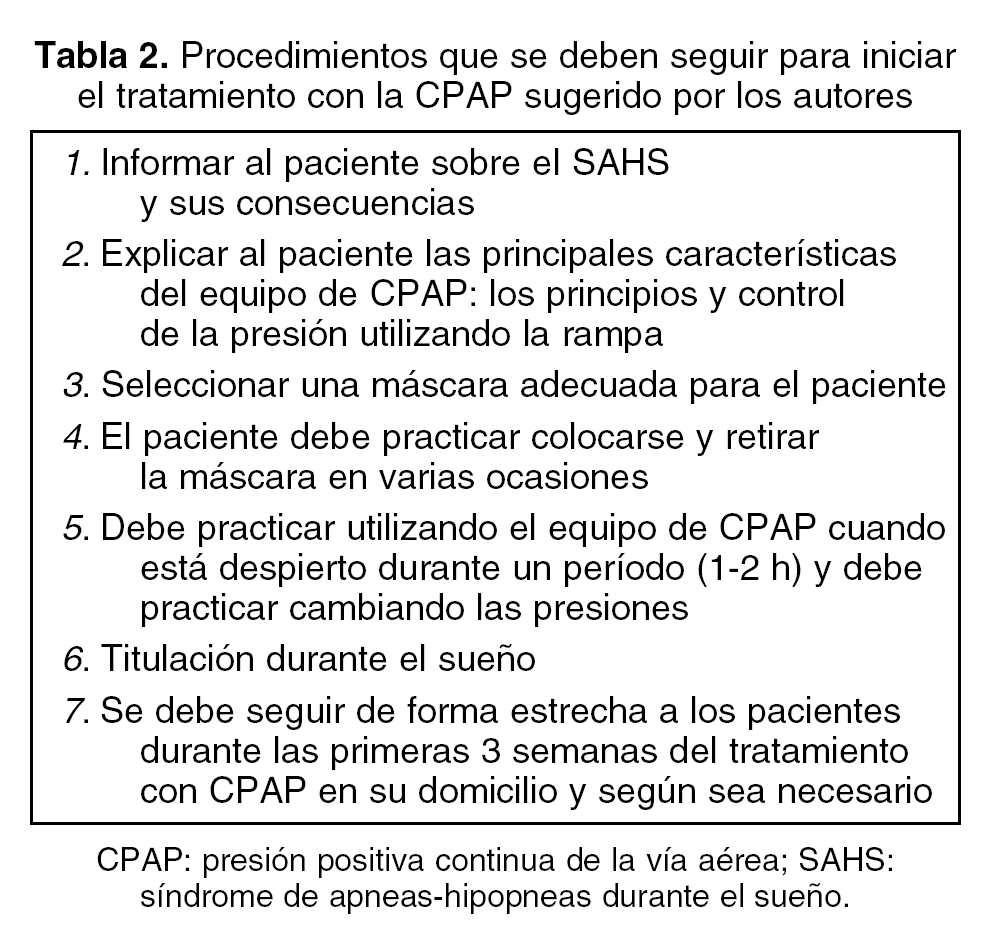
El tratamiento inadecuado con la CPAP puede inducir somnolencia residual, principalmente por 2 razones: a) titulación inadecuada de la presión y b) falta de cumplimiento. El tratamiento con CPAP se divide en 3 partes: 1) entrenamiento del paciente en el procedimiento de la CPAP; 2) titulación de la CPAP, y 3) seguimiento clínico. Las sesiones educacionales, el entrenamiento y la elección de la masacrilla adecuada son cruciales para obtener una buena tolerancia a la CPAP desde el inicio (tabla 2). Como en el diagnóstico, la titulación se puede realizar mediante la PSG o por métodos simplificados. Aunque la titulación con PSG es el estándar de oro, se ha demostrado que la titulación también se puede realizar utilizando dispositivos automáticos en un gran número de casos26. Sin embargo, los dispositivos automáticos no son recomendados en pacientes con rinitis grave, o en enfermedad médica o psiquiátrica notoria.
Titulación de CPAP incorrecta
Durante la titulación de la CPAP con PSG, la presión debe incrementarse en respuesta a los diferentes eventos respiratorios (apneas, hipopneas, períodos cortos de limitación del flujo y ronquido). La CPAP debe aumentarse 1-2 cm de H2O cada 5-10 min hasta que ocurran muy pocos o nulos eventos. Esta presión debe mantenerse y no variarse en respuesta sólo a un evento. En ausencia de eventos respiratorios en todos los estados del sueño y posiciones corporales, la presión de la CPAP debe disminuirse lentamente, hasta obtener la presión mínima suficiente27. Los períodos prolongados de limitación del flujo también deben corregirse, ya que éstos pueden inducir somnolencia residual28. En los pacientes con insomnio o en aquellos con otras alteraciones médicas, el proceso de titulación no tiene reglas claras. Durante la titulación, la medición del flujo debe realizarse, preferentemente, con un neumotacógrafo, pero es aceptable medir las oscilaciones de la señal de presión con los filtros apropiados29. Finalmente, debe señalarse que durante el sueño REM el flujo puede ser irregular y no debe confundirse con hipopneas. En la revisión de la PSG o durante la titulación de la CPAP, la señal del flujo debe compactarse (2-4 min en una pantalla) mientras que los parámetros del EEG deben monitorizarse cada 30 s. Esto permite al técnico medir las señales respiratorias y neurológicas más eficientemente. Todas estas mediciones presumiblemente prevendrán una titulación deficiente que pueda inducir somnolencia residual.
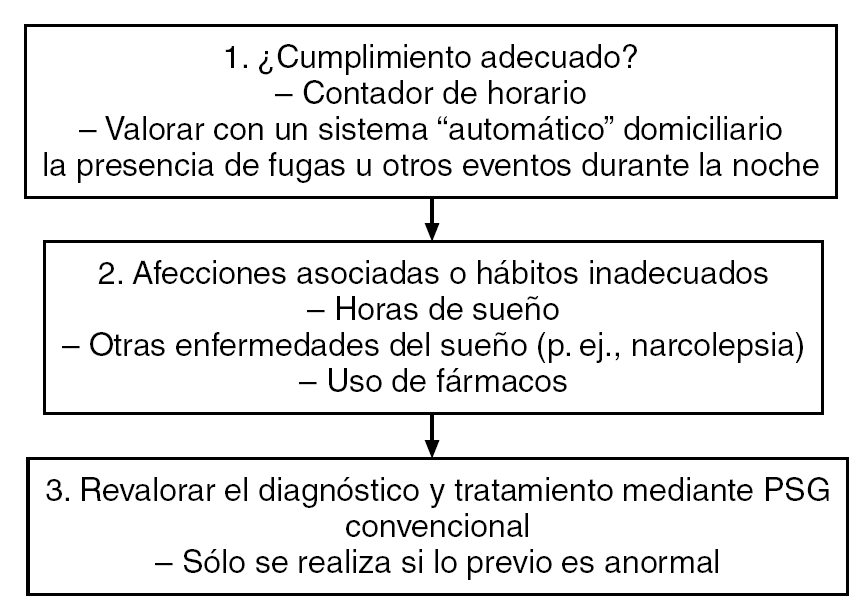
Comparado con la CPAP, la presión positiva de la vía aérea automática (APAP) disminuye la presión media durante la noche, ajustando automáticamente la presión aplicada para proveer sólo la presión necesaria en cada momento para corregir todos los eventos respiratorios, aunque la tolerancia es similar. La APAP actualmente es utilizada en 2 formas: 1) como tratamiento con la misma eficacia que la CPAP fija (en este caso, no es necesaria la titulación en el laboratorio), y 2) para la titulación de la CPAP. Sin embargo, como se afirmó previamente, se deben considerar algunos aspectos30: 1) la APAP debe ser válida y fiable, 2) es necesario la selección adecuada del paciente (fig. 1), y 3) se debe asegurar el conocimiento adecuado de la técnica.
Figura 1. Procedimientos que se debe seguir en casos de somnolencia pospresión positiva continua de la vía aérea (CPAP). PSG: polisomnografía.
Si se tienen en cuenta los puntos previamente mencionados, la APAP constituye un paso importante en el tratamiento del SAHS. Algunos autores sugieren que la APAP debe utilizarse más en un subgrupo de pacientes, como aquellos con apneas relacionadas a REM o con apneas posicionales31. Cuando la APAP se utiliza para titulación es muy importante seleccionar cuidadosamente a los pacientes, y evitar a los pacientes con problemas nasales manifiestos, insuficiencia cardíaca asociada a un patrón de respiración tipo Cheyne-Stokes, psiquiátricos u otros problemas serios de salud26 (fig. 1).
Falta de cumplimiento
El cumplimiento adecuado a la CPAP fue definido muy libremente como el uso de la máquina durante al menos 4 h, 5 noches a la semana. La frecuencia del cumplimiento utilizando estos criterios es del 48-67%32,33. Sin embargo, deben tenerse en cuenta 2 situaciones: 1) la mejoría clínica puede ocurrir aún con pocas horas de sueño34 y 2) el tiempo de sueño varía en diferentes personas. Lo que puede ser sueño suficiente para un paciente puede ser insuficiente para otro, y resulta en somnolencia residual. En los pacientes con SAHS que utilizan CPAP durante mucho tiempo, el cumplimiento es adecuado en alrededor del 70%35, una cifra que es comparable con otros tipos de tratamientos en otras alteraciones médicas.
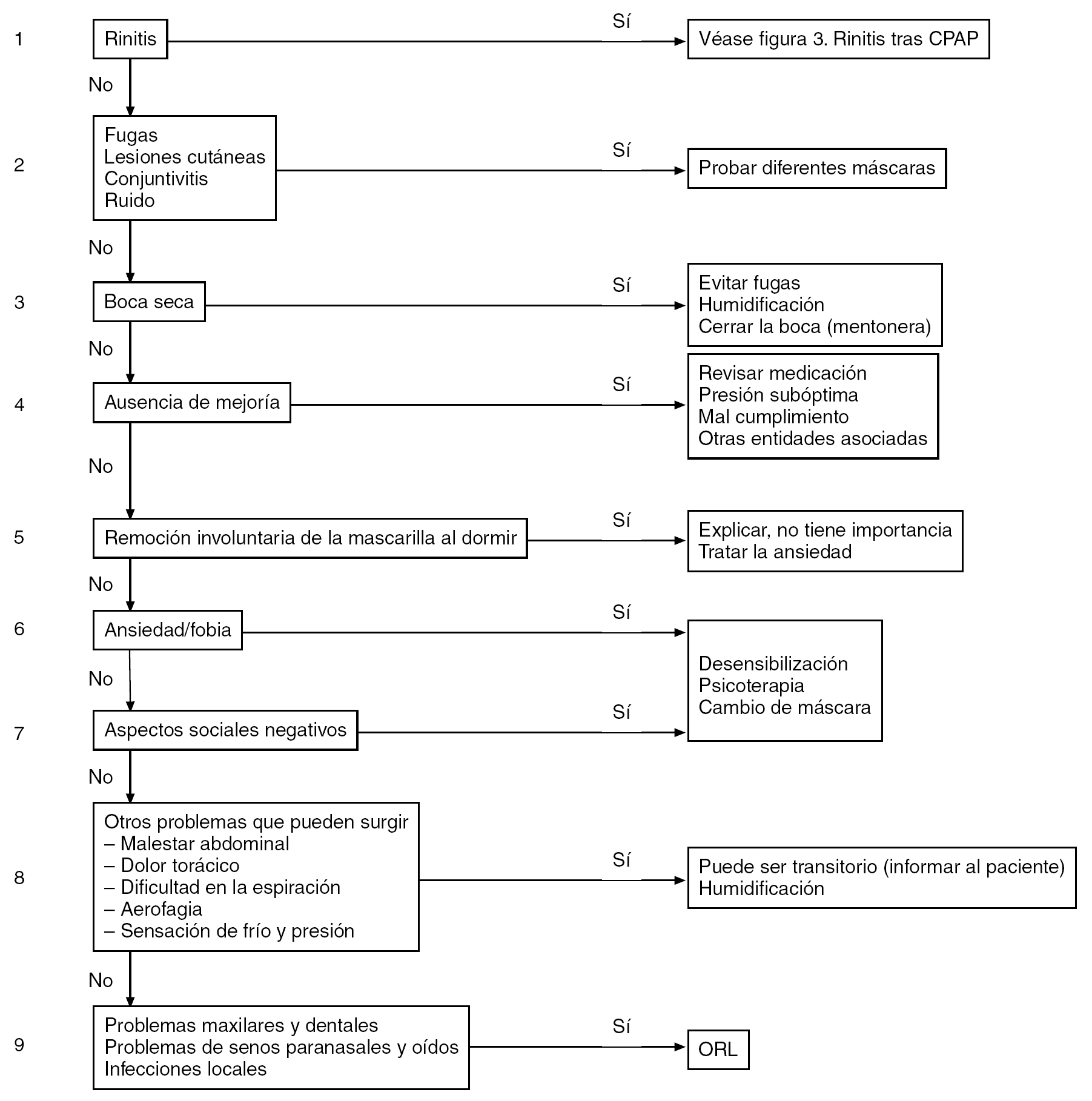
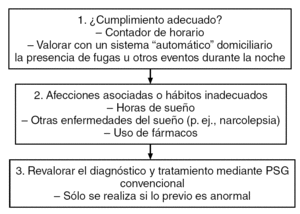
La mejoría en la somnolencia con CPAP no es fácilmente predecible. Ésta no siempre depende de las variables fisiológicas (p. ej., IAH, número de despertares) o de los efectos colaterales de la CPAP. En un estudio reciente, la humidificación de la vía aérea superior después de la CPAP no aportó un mayor cumplimiento o mejoría en la somnolencia o calidad de vida, aunque se asoció a menos síntomas nasales36. Las figuras 2 y 3 muestran las razones para un mal cumplimiento, así como algunas posibles soluciones.
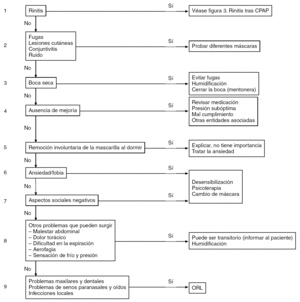
Figura 2. Procedimiento clínico sugerido en la evaluación de pacientes que no cumplen con la presión positiva continua de la vía aérea (CPAP).
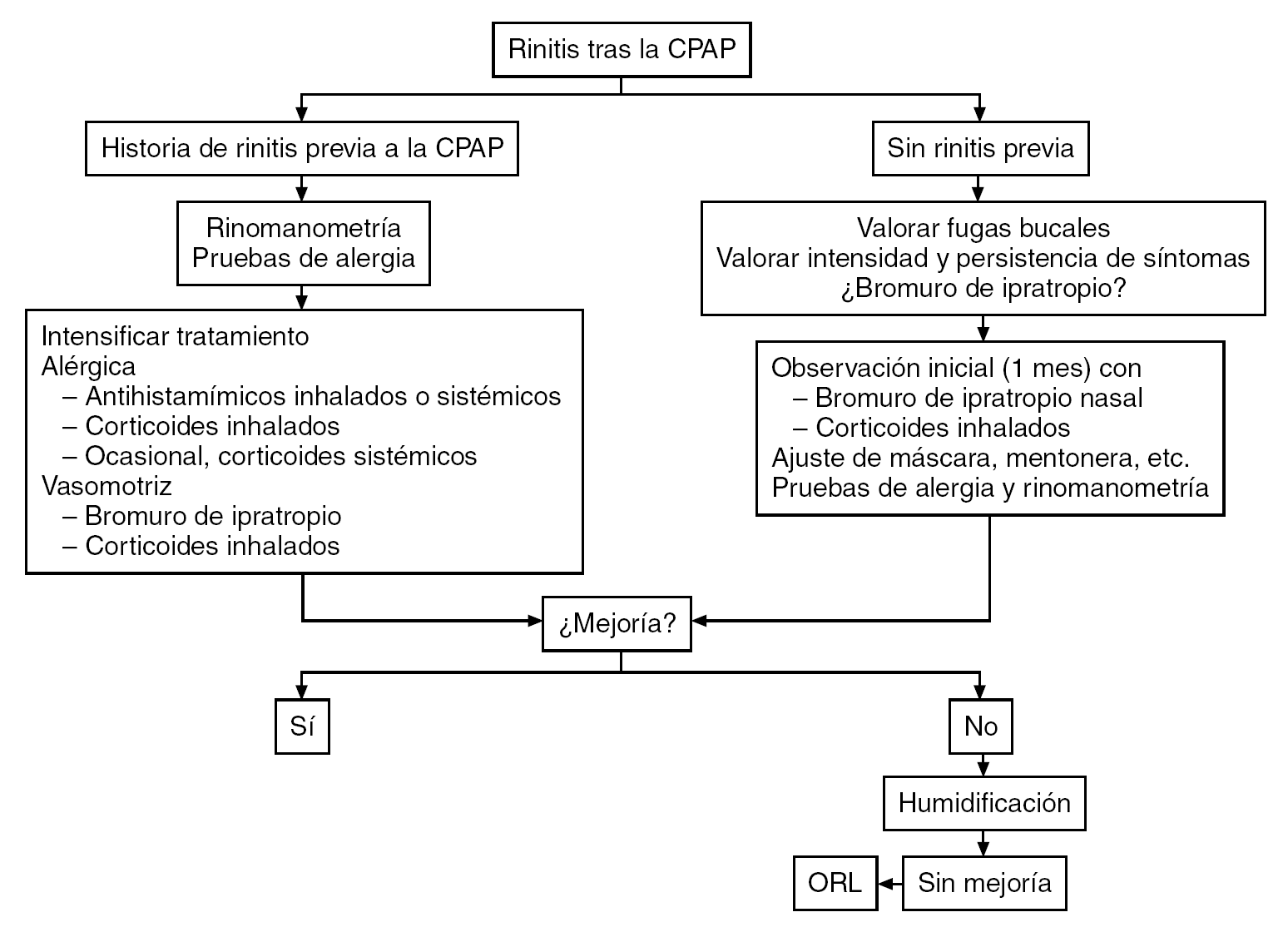
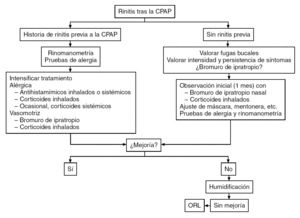
Figura 3. Manejo de la rinitis asociada al uso de presión positiva continua de la vía aérea (CPAP).
El patrón de respuesta al tratamiento con la CPAP nasal se define pronto, usualmente en el primer mes35, y la rinitis es uno de los problemas más importantes. Hay que considerar 3 aspectos: 1) las intervenciones relativamente costosas que mejoran el uso de la CPAP ("CPAP inteligente" y humidificación) se emplean frecuentemente pero con pobres resultados; 2) un abordaje multidisciplinario, así como ofrecer instrucciones y apoyo al paciente, son de mucho mayor valor coste-efectivo, y 3) se debe de identificar la causa del mal cumplimiento y ofrecer el tratamiento específico32. Nuestro abordaje de trabajo es similar: 1) sesiones de información y educación previo a la titulación de la CPAP (tabla 2); seguimiento cuidadoso, especialmente durante las primeras 4 semanas, y 3) identificación inmediata y tratamiento de los problemas. La falta de cumplimiento es difícil de predecir, pero puede resultar de una combinación de factores, como ausencia de beneficios clínicos, efectos colaterales (rinitis y fugas) e instrucciones y apoyo inadecuados (figs. 2 y 3).
Somnolencia residual debido a otros trastornos de sueño no diagnosticados
Sueño insuficiente
Una causa común de somnolencia es el sueño insuficiente37. Ésta es una de las principales posibilidades que se deben considerar en cualquier paciente que se queja de somnolencia y también en el paciente con somnolencia residual después del tratamiento con la CPAP. El uso de diarios del sueño o de registros actigráficos puede ser de ayuda en la evaluación de los hábitos de sueño del paciente. No es fácil determinar cuál es la mínima cantidad de sueño que se necesita para prevenir la somnolencia, pero la restricción crónica de sueño debe sospecharse cuando: 1) se tiene una eficiencia de sueño inusualmente alta; 2) el paciente refiere, aproximadamente, 2 h más de sueño en los días festivos que en los días laborables37, o 3) cuando la aparición de la somnolencia es precedida por un cambio en los patrones de sueño del paciente, particularmente una disminución en el número usual de horas de sueño.
Depresión
La depresión es una alteración común que puede asociarse a SDE. Alternativamente, la depresión se presenta frecuentemente en los pacientes con SAHS. Por tanto, la relación entre depresión, somnolencia y SAHS es compleja y se puede evaluar de la siguiente manera: a) depresión como una causa de somnolencia; b) depresión con SAHS coexistente, y c) depresión como predisponente a somnolencia persistente en los pacientes tratados con CPAP.
Depresión como causa de somnolencia. En estudios epidemiológicos, las alteraciones depresivas están asociadas a quejas de somnolencia diurna grave38. En la práctica psiquiátrica, la somnolencia se asocia a un síndrome depresivo específico llamado depresión atípica. Se han publicado pocos estudios que evalúan la somnolencia en pacientes deprimidos con pruebas objetivas, como el MSLT22,39,40, que obtuvieron resultados contradictorios. En conjunto, estos estudios mostraron que la mayoría de los pacientes deprimidos se quejan de somnolencia en lugar de mostrar síntomas como falta de interés, disminución de energía y fatiga, los cuales pueden simular somnolencia diurna excesiva. De hecho, los síntomas depresivos se asocian a sensación de fatiga en los pacientes con SAHS23. Un estudio mostró que entre los pacientes inicialmente referidos a un centro de sueño por SDE y diagnosticados de depresión, el 36% tenía una latencia del sueño media moderadamente reducida (< 10 min) en el MSLT40. Por tanto, esto muestra que algunos pacientes depresivos que se quejan de SDE tienen valores anormales en el MSLT.
Depresión coexistente con SAHS. Los pacientes con SAHS comúnmente refieren tener síntomas depresivos. En un estudio reciente, el 41% de los pacientes con SAHS referidos a una unidad de sueño mostró síntomas depresivos y el 39% recibió tratamiento antidepresivo41, lo que sugiere una estrecha relación entre ambas alteraciones. Ya que el SAHS y la depresión son muy frecuentes en la población general, ambas condiciones pueden sobreponerse en algunos pacientes. En primer lugar, los pacientes con SAHS tienen síntomas depresivos más intensos (pesimismo, inactividad, culpa) y ansiedad somática42 que aquellos con ronquido simple. En segundo lugar, la SDE en los pacientes con SAHS aparentemente está más estrechamente relacionada con la depresión que con la alteración respiratoria asociada al sueño43. En tercer lugar, el estado de ánimo es mejor predictor de la calidad de sueño percibida que la PSG44. En cuarto término, el tratamiento con CPAP en los pacientes con SAHS mejora algunos síntomas depresivos, como irritabilidad, apatía o ansiedad1,19,45. Finalmente, se ha sugerido que la presencia de SAHS no tratado en los pacientes con depresión primaria puede producir resistencia al tratamiento farmacológico46,47. La asociación entre síntomas depresivos y SAHS puede tener 4 diferentes explicaciones:
1. La depresión primaria es coincidente pero no relacionada con el SAHS.
2. Un estado de ánimo depresivo ocasionado por los síntomas durante el sueño (ronquido, somnolencia) o por las condiciones asociadas (obesidad) en la vida social y familiar48.
3. Una depresión debida a las consecuencias del SAHS en la fisiología del estado de ánimo. Por ejemplo, hiperintensidades en la materia blanca subcortical ocurren en pacientes con SAHS grave y se ha observado que se correlacionan con puntuaciones neuropsicológicas y de depresión49.
4. Finalmente, el SAHS puede ser inducido por los mismos mecanismos biológicos productores de depresión. Una deficiencia neurobiológica en la actividad serotoninérgica se asocia a depresión. Los sistemas serotoninérgicos participan en la regulación del tono muscular de la vía aérea superior; normalmente durante el sueño disminuye la liberación de serotonina a las neuronas motrices dilatadoras de la vía aérea superior. Esta reducción puede contribuir a la obstrucción de la vía aérea superior en el SAHS50. Una disminución en la transmisión serotoninérgica en la depresión puede facilitar la obstrucción de la vía aérea superior durante el sueño. Además, los medicamentos con una poderosa acción serotoninérgica, como los inhibidores de la recaptación de serotonina que se utilizan como antidepresivos, también se han utilizado en el SAHS51, aunque con resultados limitados.
La presencia de depresión en un paciente con sospecha de SAHS es, en nuestra opinión, una indicación para realizar una PSG convencional en lugar de un estudio respiratorio simplificado. Ya que la somnolencia en un paciente deprimido puede ser secundaria a otras causas además de la apnea del sueño, es muy probable que finalmente sea necesaria la PSG convencional en su evaluación.
Depresión como factor favorecedor de somnolencia residual en los pacientes tratados con CPAP. Cuando se detecta somnolencia residual después de la CPAP, se deben considerar 3 posibles formas de interacción entre la depresión y el SAHS:
1. La depresión por sí misma puede ser causa de somnolencia y cuando es comórbida con el SAHS, el tratamiento sólo con CPAP no mejorará los síntomas depresivos relacionados con la SDE.
2. Algunos tratamientos farmacológicos utilizados en los pacientes con depresión, como las benzodiacepinas o los antidepresivos con efecto sedante, pueden producir somnolencia.
3. La depresión está asociada a la falta de cumplimiento del tratamiento con CPAP. Kjelsberg et al52 demostraron que un nivel alto de síntomas depresivos se relaciona con somnolencia diurna, así como con la falta de cumplimiento del tratamiento con CPAP.
Narcolepsia
La narcolepsia es una enfermedad neurológica de origen desconocido relacionada con un deterioro en el sistema hipotalámico promotor de la vigilia del neuropéptido hipocretina. Clínicamente se manifiesta por SDE y otros hallazgos de disfunción del sueño REM, como cataplejía, parálisis del sueño, alucinaciones hipnagógicas, y por la presencia de 2 o más períodos REM (SOREMP) en el MSLT53. El término cataplejía se refiere a episodios de pérdida súbita transitoria del tono muscular, con preservación del estado de consciencia desencadenado por un estímulo emocional; este signo es casi patognomónico de la enfermedad. Sin embargo, hay algunos pacientes narcolépticos sin cataplejía en quienes el MSLT muestra 2 o más SOREMP, condición conocida como narcolepsia sin cataplejía. En la mayoría de los narcolépticos la enfermedad comienza en la adolescencia53, pero también se puede presentar después de los 40 años54. La prevalencia de narcolepsia es 100 veces menor que la del SAHS; se calcula en un 0,02-0,18% de la población general53. La narcolepsia se puede confundir con el SAHS coexistente debido a: 1) que la mayoría de los narcolépticos se encuentran sin diagnóstico55; 2) que la narcolepsia y el SAHS están asociados a un incremento en el índice de masa corporal56, y 3) que los narcolépticos frecuentemente buscan atención médica por primera vez en la edad adulta54.
La comorbilidad de pacientes con apnea del sueño y narcolepsia se ha evaluado en pocos estudios, que muestran resultados que varían del 2 al 68%57,58. En nuestra unidad del sueño, se diagnosticaron 152 pacientes con narcolepsia desde el años 1991 hasta el año 2006; 32 (21%) pacientes tenían un IAH > 10 (media IAH = 32), y 10 (31%) de ellos fueron diagnosticados inicialmente como SAHS en otros centros, y de éstos, 9 fueron tratados con CPAP sin tener cambios claros en la somnolencia. El diagnóstico de narcolepsia se realizó cuando se reevaluaron por la somnolencia residual posterior a la CPAP, en una media de 3,5 años después. En los otros 22 pacientes, se diagnosticaron simultáneamente narcolepsia y SAHS, y en 6 de éstos se inició la CPAP ya que tenían un IAH > 30. No hubo cambios en la somnolencia; sin embargo, algunos pacientes refirieron una mejoría en la calidad del sueño nocturno. No hay estudios que demuestren que el SAHS sea más frecuente en la narcolepsia que en la población general, ni estudios prospectivos, bien diseñados, que evalúen la coexistencia del SAHS con la narcolepsia, así como el efecto terapéutico de la CPAP en la severidad de la SDE de estos pacientes.
Es importante realizar un diagnóstico preciso de la narcolepsia, ya que es una condición que dura toda la vida, que no sólo influye en la calidad de vida del paciente, sino que también incrementa el riesgo de que se quede dormido en el trabajo o mientras conduce. Los pacientes con narcolepsia se pueden beneficiar con medidas conductuales (siestas con horario y una buena higiene de sueño), agentes estimulantes (modafinilo y metilfenidato)59 y fármacos específicos para la cataplejía. Para descartar la narcolepsia, los médicos deben evaluar los síntomas clásicos de narcolepsia: cataplejía, parálisis del sueño y alucinaciones hipnagógicas. El uso del MSLT ayuda en la evaluación de los pacientes con somnolencia residual inexplicable sin cataplejía; es diagnóstico tener una latencia del sueño < 8 min adicionado a 2 o más SOREMP, posterior a un sueño nocturno suficiente, evaluado con una PSG previa53.
Hipersomnia idiopática
La hipersomnia idiopática, también llamada hipersomnia esencial, se caracteriza por SDE crónica y severa, usualmente antes de los 30 años de edad, la ausencia de cataplejía y de otras características indicativas de alteración del sueño REM, pero no del sueño nocturno fragmentado. En contraste con la mayoría de los pacientes con narcolepsia, los pacientes con hipersomnia idiopática refirieron tener largas siestas de varias horas, no refrescantes53. Algunos pacientes se presentaron con un tiempo de sueño nocturno prolongado > 10 h (hipersomnia idiopática con tiempo de sueño largo). El diagnóstico de hipersomnia idiopática requiere de la exclusión de todas las otras alteraciones que pueden ocasionar SDE. La PSG muestra sueño nocturno normal > 6 h, excluidas las anormalidades, como alteraciones de la respiración asociadas al sueño. El MSLT muestra una disminución en la media de la latencia del sueño y menos de 2 SOREMP, excluida la narcolepsia. La causa de hipersomnia idiopática es desconocida, pero se sospecha de una disfunción en los mecanismos del sistema nervioso central moduladores del sueño y del despertar. Como en la narcolepsia, los pacientes pueden responder a estimulantes como el modafinilo y el metilfenidato.
Otras causas de somnolencia
Como se muestra en la tabla 3, estas causas incluyen una variedad de alteraciones del sueño, como el síndrome del sueño insuficiente, el síndrome de Kleine-Levin y los patrones alterados del ritmo circadiano (cambio de trabajo, retraso en la fase del sueño, fase del sueño avanzada y patrones sueño-vigilia irregulares). La SDE también puede ser secundaria a alteraciones neurológicas (enfermedad vascular cerebral, enfermedades neurodegenerativas, tumores cerebrales, distrofia miotónica, traumatismo craneoencefálico y encefalitis límbica) o enfermedades médicas (infecciones virales, encefalopatía metabólica, hipotiroidismo). La SDE también puede estar ocasionada por el uso crónico de fármacos como hipnóticos (benzodiacepinas, zolpidem, zaleplon), antidepresivos sedantes (trazodona, mirtazapina, clorfeniramina), antihipertensivos (clonidina, labetalol) y virtualmente todos los opioides, antiepilépticos, antipsicóticos y agentes dopaminérgicos.
Síndrome de piernas inquietas60
El síndrome de piernas inquietas (SPI) es una alteración motriz-sensorial caracterizada por una urgencia de mover las piernas debido a una incomodidad sensorial, inquietud motriz, agravamiento de los síntomas por la tarde y alivio de éstos con el movimiento. El SPI se incrementa con la edad, es más prevalente que el SAHS y afecta al 5-15% de los adultos. Por tanto, es probable que los pacientes con SAHS puedan tener SPI debido a la alta prevalencia de estas 2 alteraciones en la población general.
Se suele aceptar comúnmente que el SPI puede ocasionar somnolencia diurna excesiva. Esto puede ser porque el SPI puede asociarse con sueño insuficiente y fragmentado debido a que la inquietud sensorial de las piernas puede alterar la capacidad del paciente de dormirse o retornar al sueño después de despertarse. Sin embargo, no hay estudios que muestren que la SDE está asociada con el SPI y, de hecho, muchos pacientes con SPI refieren tener una incapacidad para tomar siestas. Se debe de tener en cuenta que el cansancio, el estado de ánimo depresivo y la disminución en la concentración son quejas frecuentes entre los pacientes con SPI severo, los cuales deben diferenciarse de la SDE. Sin embargo, la información disponible indica que el SPI probablemente no contribuye significativamente a la SDE. No hay evidencia que sugiera que la introducción de tratamientos específicos para el SPI pueda reducir la SDE percibida por algunos pacientes con SAHS tratados con CPAP.
Movimientos periódicos de piernas durante el sueño
Entre el 80 y 90% de los pacientes con SPI tienen PLMS; éstos se caracterizan por tener episodios periódicos cortos, de movimientos involuntarios de las piernas, repetitivos y estereotipados, durante el sueño que pueden estar asociados o no con microdespertares. En la PSG, los PLMS se deben diferenciar de los movimientos de piernas no estereotipados que ocurren durante el microdespertar al final de cada evento apneico. Los PLMS también pueden ocurrir en pacientes sin SPI e incrementar su prevalencia con la edad. Los PLMS son muy frecuentes en el adulto mayor sin quejas del sueño, como SDE60. Se ha considerado que los PLMS pueden ocasionar somnolencia porque algunas veces van acompañados de microdespertares que alteran la continuidad del sueño. Los estudios en pacientes con y sin SPI no han encontrado relación entre los PLMS y las mediciones subjetivas u objetivas de SDE60. Recientemente, 2 estudios mostraron que aunque los PLMS son frecuentes en los pacientes con SAHS, éstos no participan en la SDE antes o después del tratamiento exitoso con la CPAP. Estos informes indican que los PLMS, asociados o no a microdespertares, no ocasionan SDE en los pacientes con SAHS12,61. Nuestro grupo de trabajo ha observado, en muchos casos de pacientes con PLMS y SAHS tratados con CPAP, que el uso de agentes dopaminérgicos para disminuir los movimientos de las piernas no disminuye la severidad de la somnolencia residual. En resumen, los datos disponibles indican que los PLMS no se asocian a SDE, y pueden ser parte del envejecimiento normal.
Hipoxia prolongada y lesión en sistema nervioso central
Algunos pacientes continúan con la queja de SDE a pesar del tratamiento adecuado con CPAP y la exclusión de todas las condiciones comórbidas que puedan ocasionar somnolencia. En estos casos, no queda clara la causa de la somnolencia persistente. Sin embargo, se ha sugerido que la hipoxia crónica relacionada a años de SAHS no tratada puede resultar en un daño neuronal cerebral que conduce a SDE. Esto se basa en modelos animales que simulan las características de la hipoxia intermitente que ocurre en el SAHS en humanos. Estos estudios han mostrado que la exposición a la hipoxia intermitente durante mucho tiempo induce cambios neuronales en el cerebro, como activación proinflamatoria, disminución de los valores extracelulares de dopamina, incremento del estrés oxidativo, apoptosis y gliosis. Esas anormalidades ocurren en diferentes estructuras del cerebro, incluidas algunas asociadas con la modulación del sueño-vigilia (hipotálamo posterior y lateral, núcleo relacionado con el sistema dopaminérgico, locus coeruleus, rafe dorsal y área preóptica ventrolateral). El deterioro de estas estructuras se ha asociado con SDE en modelos animales62-65. Por tanto, podemos especular que la SDE, en algunos pacientes tratados óptimamente con CPAP, puede ser resultado de una hipoxia intermitente crónica, que puede ocasionar una disfunción neuronal importante en las áreas del cerebro que regulan el sueño. Esto se debe a que los agentes estimulantes, como el modafinilo, se han propuesto como tratamiento adjunto para la SDE persistente en los pacientes con SAHS tratados con CPAP.
MANEJO DEL PACIENTE CON SOMNOLENCIA RESIDUAL POST-CPAP
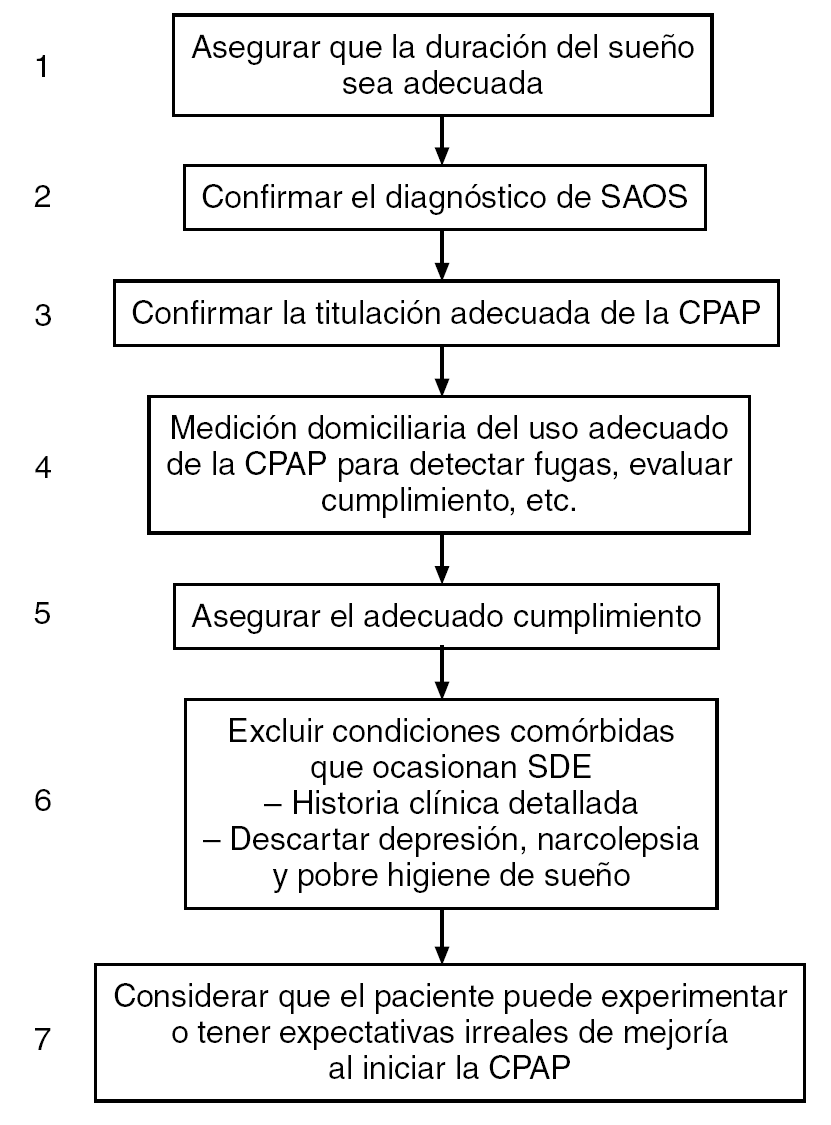
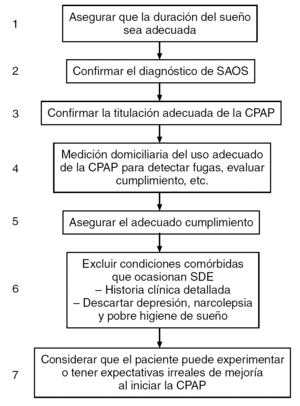
Los pacientes con somnolencia residual después de la CPAP representan, en general, un desafío a los médicos especialistas del sueño. La evaluación y el tratamiento adecuados de estos pacientes se obtienen mejor con un abordaje multidisciplinario. En esta consideración, se ha propuesto un abordaje terapéutico que se muestra en la figura 4.
Figura 4. Procedimiento sugerido en el manejo de pacientes con somnolencia persistente después de la presión positiva continua de la vía aérea (CPAP). SDE: somnolencia diurna excesiva; SAOS: síndrome de apneas obstructivas durante el sueño.
1. Debemos asegurar que la duración del sueño sea suficiente. El uso de diarios de sueño o de actimetría puede ayudar.
2. Comprobar el diagnóstico y los procedimientos de la titulación. Por ejemplo, un paciente con un IAH de 19 y que tiene somnolencia debido a hábitos deficientes de sueño no mejorará con la CPAP. La misma situación puede ocurrir cuando la titulación se realiza con un equipo de APAP y el paciente padece de insomnio o tiene pobre tolerancia a la máscara.
3. Verificar el cumplimiento y medirlo objetivamente con un contador del tiempo de presión real. Esto es de gran importancia. Los nuevos equipos de CPAP ofrecen información relevante, como la presencia de fugas o el uso deficiente de la CPAP, etc. En un paciente con pobre cumplimiento, la presencia de rinitis, fugas, depresión o pobre adaptación a la máquina puede requerir abordajes específicos (figs. 2 y 3). Las sesiones educacionales con reentrenamiento de los pacientes son importantes para mejorar el uso de la CPAP, especialmente en los pacientes con claustrofobia a la máscara, en quienes pueden ayudar los procedimientos de desensibilización. Está empíricamente aceptado que el cumplimiento es satisfactorio cuando el paciente utiliza la máquina más de 4,5 h cada noche. Dormir con la CPAP durante más horas probablemente resultará en una mejoría de la somnolencia. La eficiencia del tratamiento debe evaluarse en el domicilio, utilizando los nuevos equipos disponibles, y sólo en los casos donde el cumplimiento es satisfactorio se debe repetir la PSG diagnóstica y la titulación de la CPAP.
4. Descartar trastornos de sueño asociados, especialmente depresión y narcolepsia. La recurrencia de la somnolencia en un paciente que inicialmente se benefició de la CPAP se puede explicar por un incremento en el peso3. Con el incremento en el conocimiento de las alteraciones del sueño en la población general, hay pacientes que con la intención de obtener una pensión por enfermedad crónica pueden persistir con su queja de somnolencia o pueden inducirla con un uso insuficiente de la CPAP. Sólo con una PSG convencional con CPAP y una MSLT/MWT al día siguiente se puede identificar a estos pacientes. El tratamiento de la depresión puede ayudar a mejorar la somnolencia, ya sea incrementando el cumplimiento deficiente de la CPAP o por disminución directa de las quejas de somnolencia. Para detectar esta condición, es necesaria la evaluación sistemática de los síntomas depresivos en los pacientes con SAHS. Los pacientes con depresión leve a moderada pueden manejarse con antidepresivos por un médico especialista del sueño. Los pacientes con síntomas depresivos severos o sin respuesta al tratamiento antidepresivo se deben referir a un psiquiatra para su evaluación.
5. Finalmente, cuando el paciente ha seguido estos pasos y se continúa quejando de somnolencia, se puede prescribir estimulantes. El modafinilo, un agente promotor del despertar utilizado en el tratamiento de la narcolepsia, se ha evaluado en un número de estudios aleatorizados y controlados con placebo, y ha demostrado que disminuye la somnolencia subjetiva y, en algún grado, la somnolencia objetiva4-6.
Correspondencia:
Dr. J. Santamaría.
Unidad Multidisciplinaria de Trastornos del Sueño. Servicio de Neurología. Hospital Clínic.
Av. Villarroel, 170.
08036 Barcelona. España.
Correo electrónico: jsantama@clinic.ur.es
Aceptado tras revisión externa: 27-07-2007.