Objetivo: Evaluar la seguridad de la vacuna adyuvada-MF59 en la gripe estacional en población adulta frente a las vacunas antigripales convencionales.
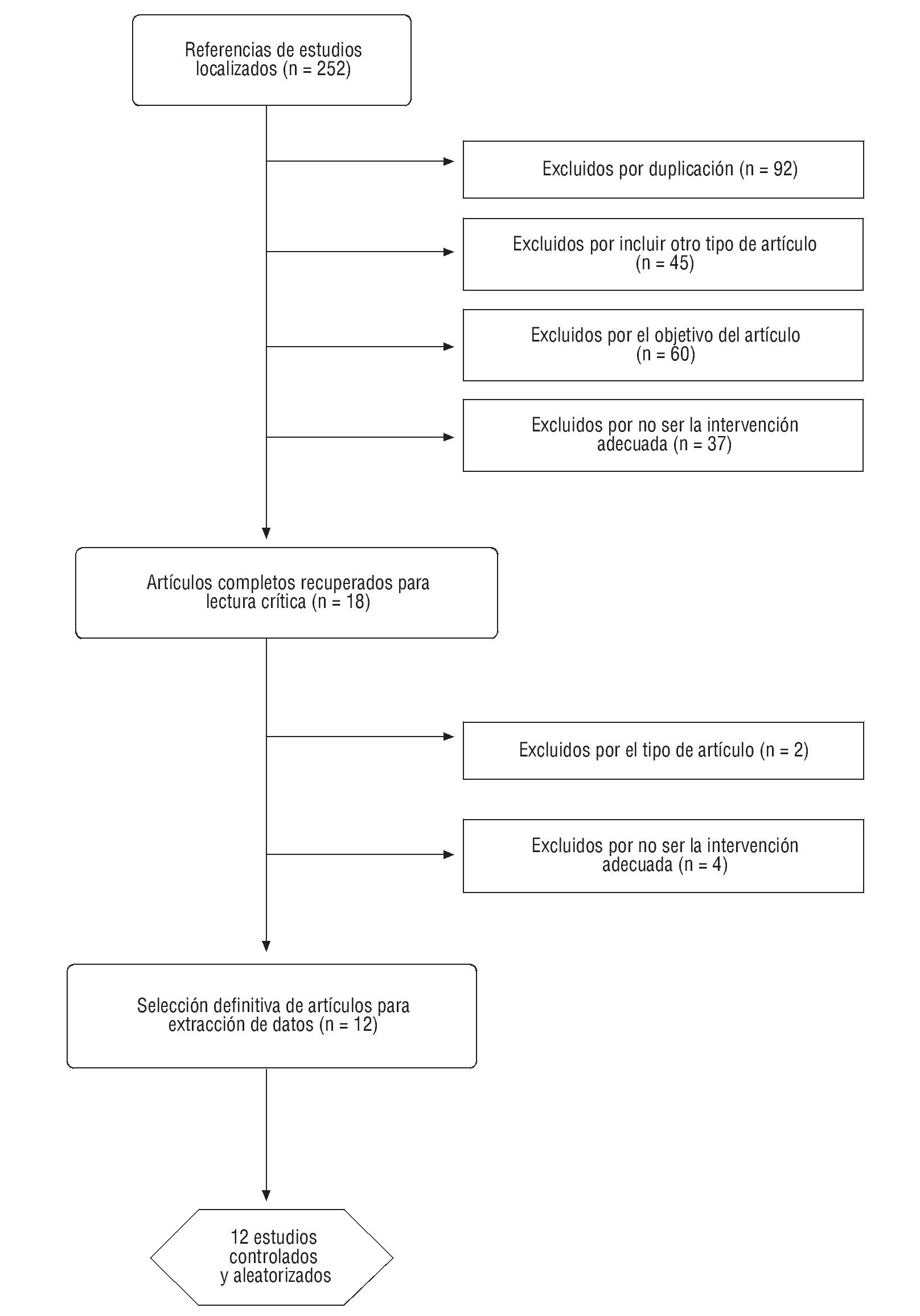
Diseño del estudio: Revisión sistemática de la literatura (2000-2011).
Fuente de datos: MEDLINE, EMBASE, CRD (Center for Review Dissemination), ECRI, Hayes, bases de datos de Agencias de Evaluación de Tecnologías Sanitarias, el registro de ensayos norteamericano ClinicalTrials.gov, y búsqueda manual en revistas especializadas. Entre los términos MeSH se encontraban "influenza", "vaccine", "adults", "safety" y los términos libres "adjuvant vaccine" "Chiromas", "Fluad" y "MF59".
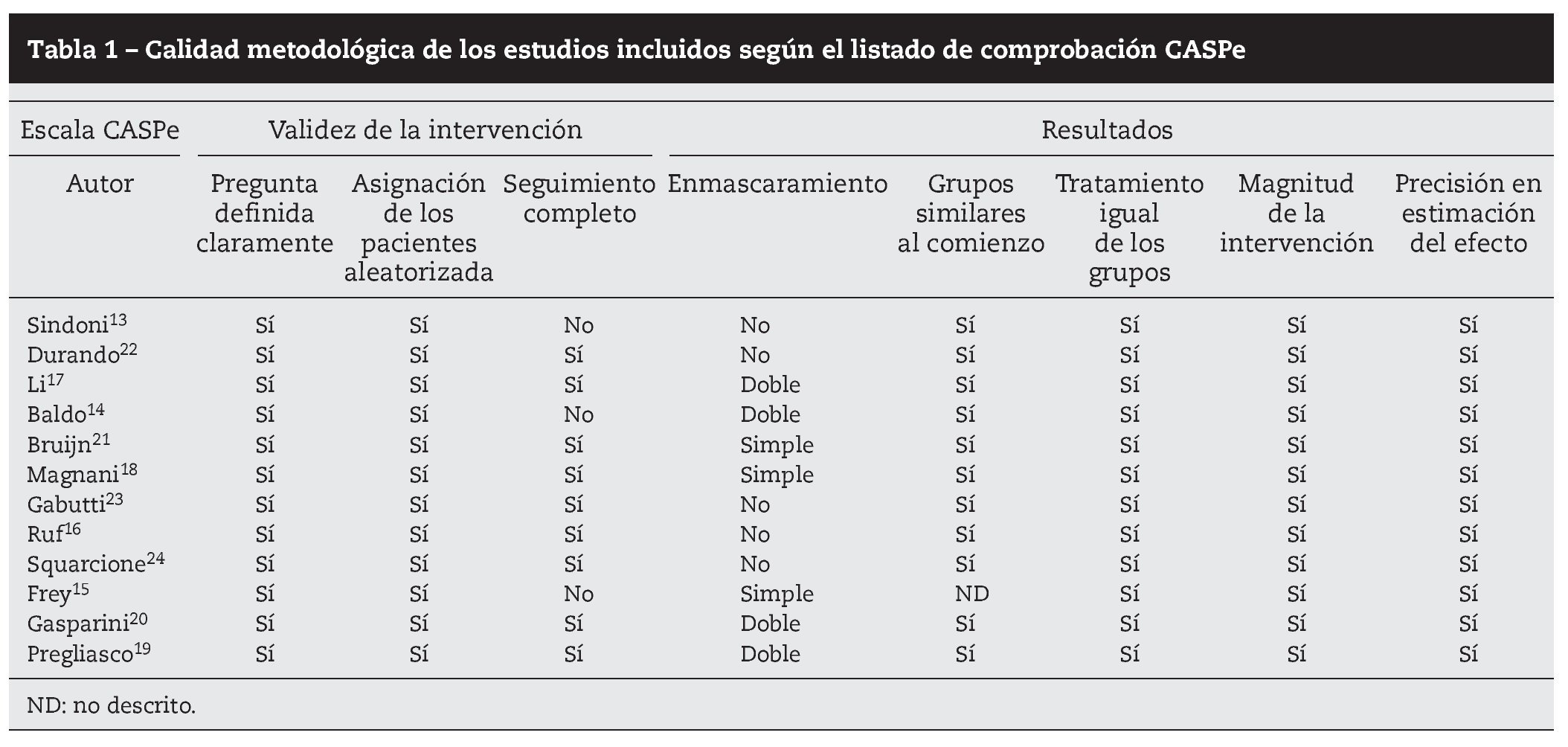
Métodos: Los criterios de inclusión fueron ensayos clínicos que incluyeran a adultos a los que se vacunaba con la vacuna adyuvada MF59 para la gripe estacional, y se comparaba frente a otras vacunas antigripales o placebo, registrando resultados de seguridad. La calidad de los estudios se valoró mediante criterios del programa CASPe.
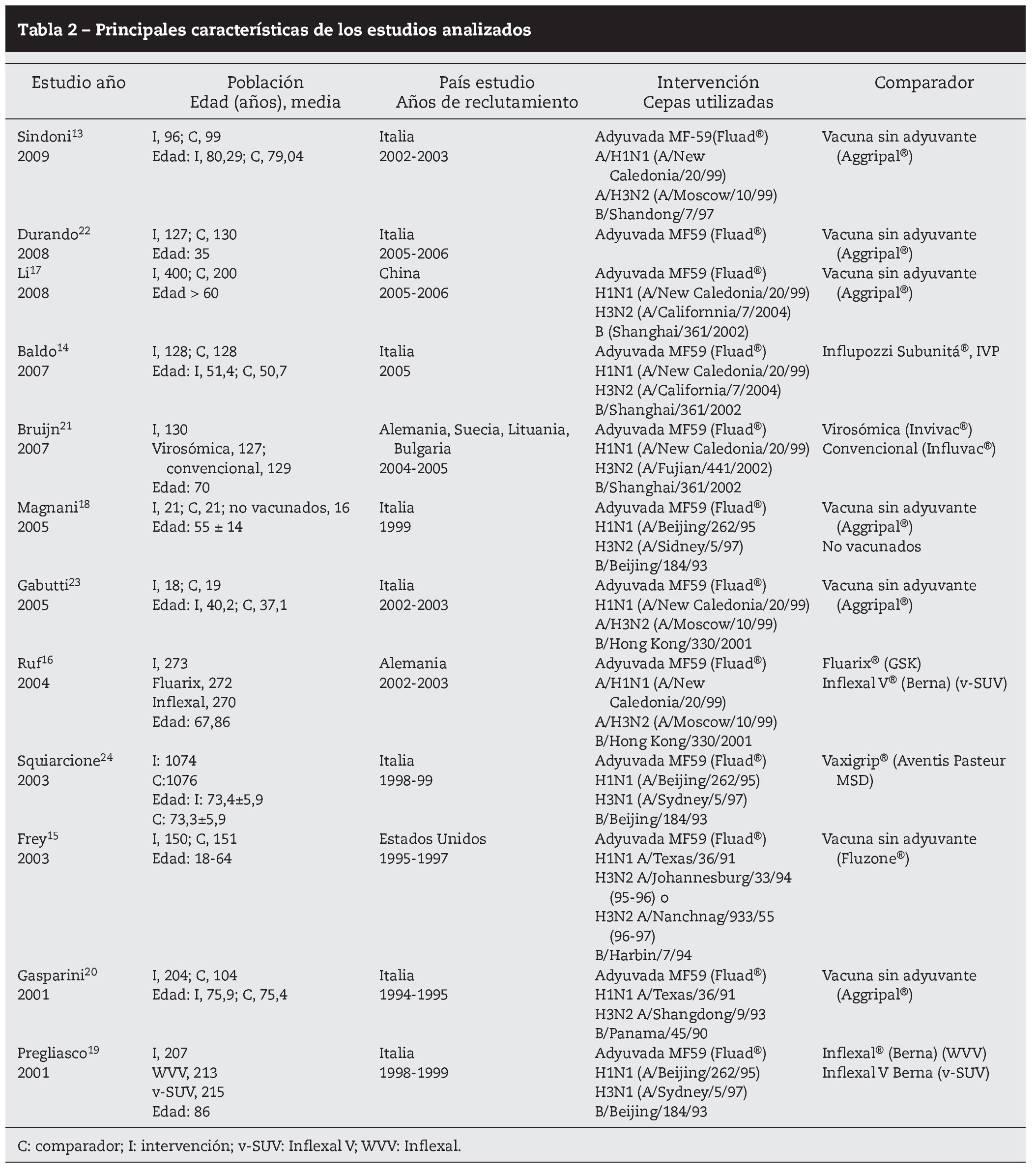
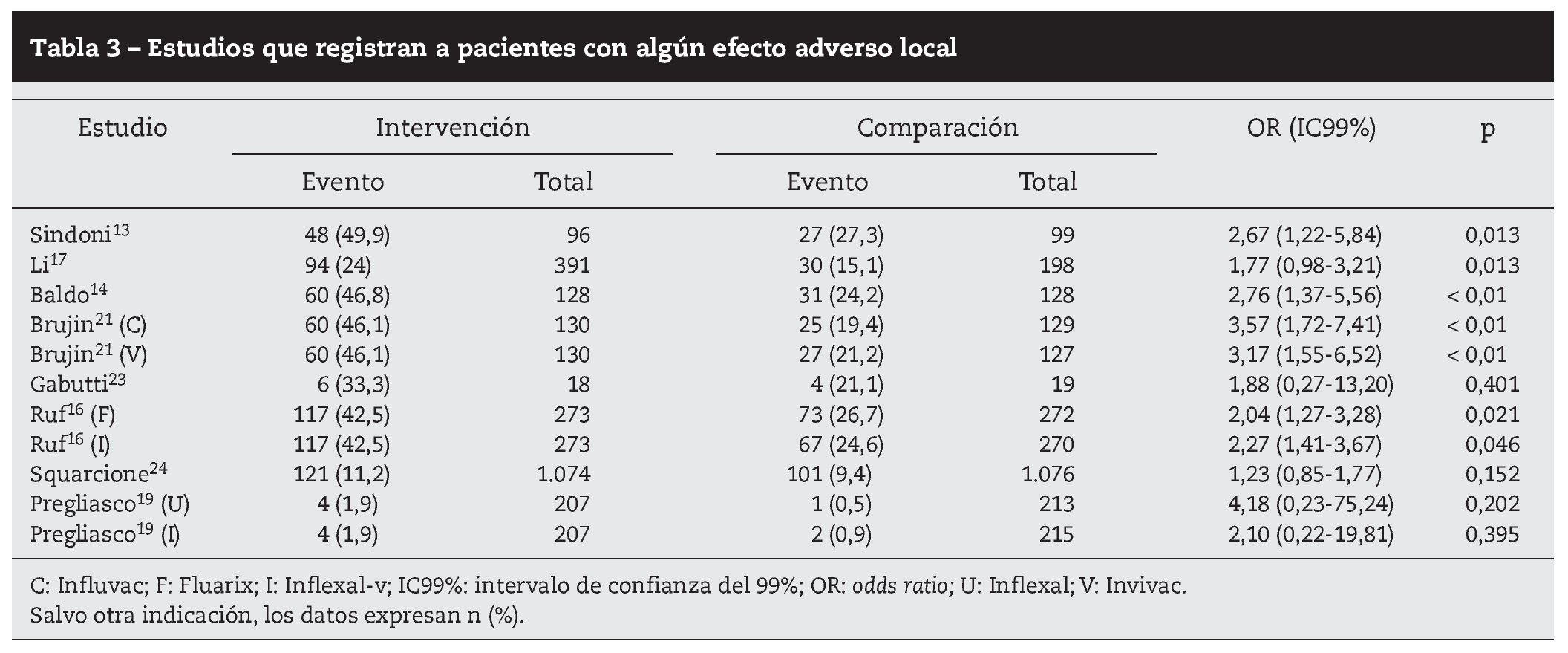
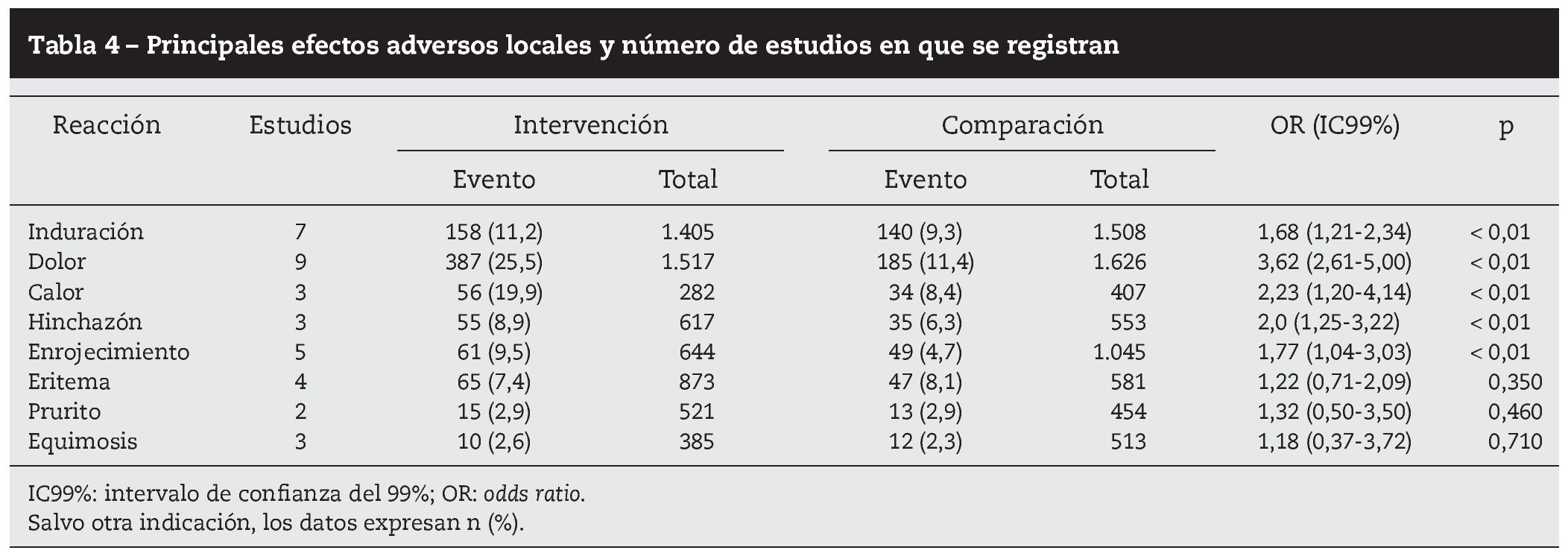
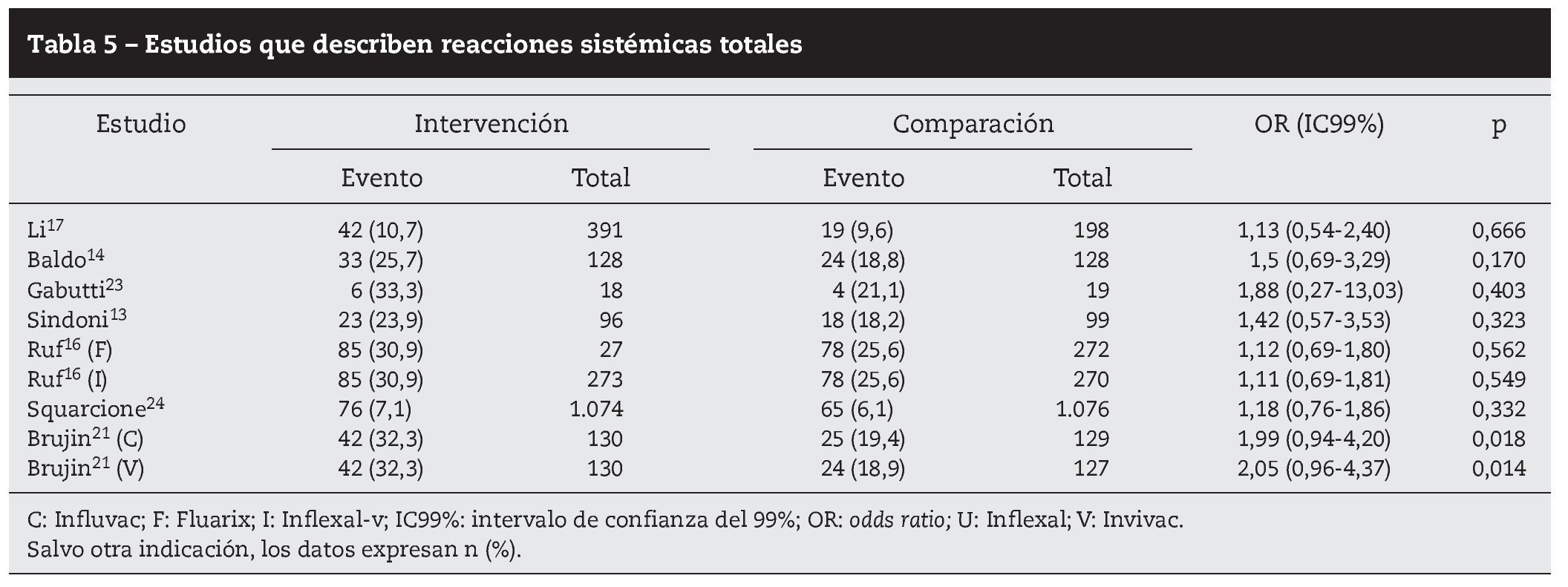
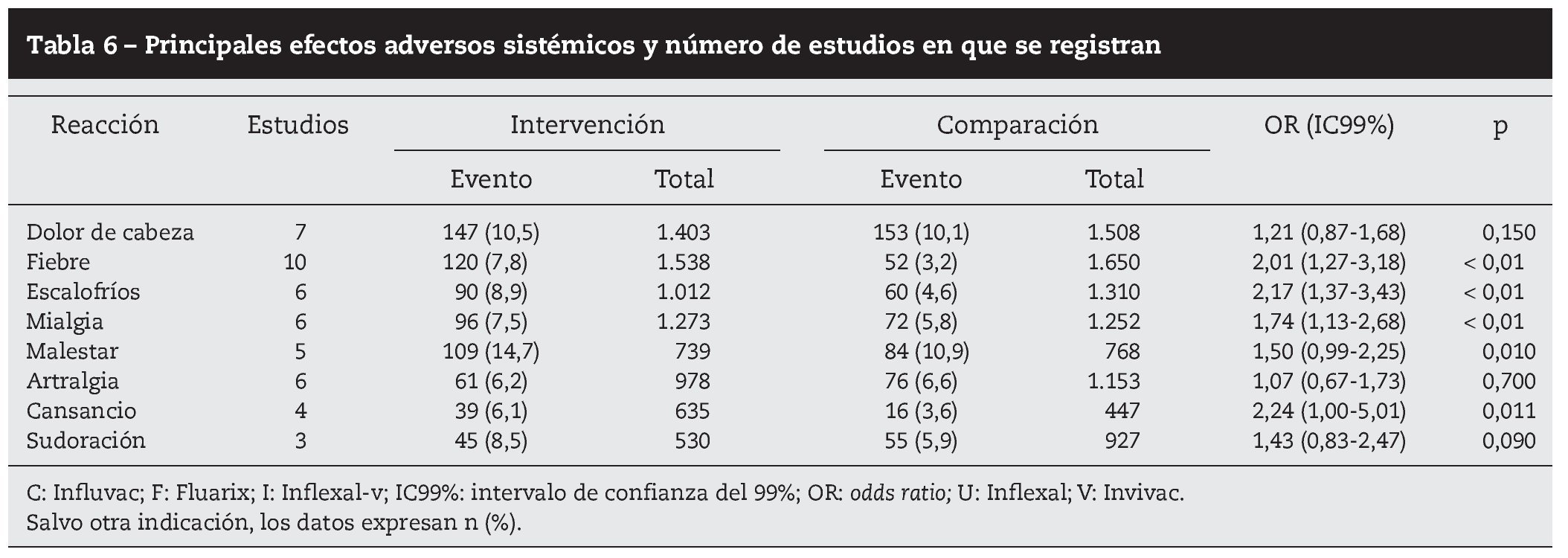
Resultados: Se seleccionaron 12 ensayos clínicos de calidad moderada-alta. Los efectos adversos locales y sistémicos fueron escasos y de carácter leve. La mayoría de las reacciones no presentaron diferencias estadísticamente significativas (p < 0,01) entre las vacunas ensayadas. Los efectos adversos de la vacuna adyuvada más frecuentes y significativos fueron dolor (25,5%), calor (19,9%) e induración local (11,2%), escalofríos (8,9%), fiebre (7,8%) y mialgia (7,5%).
Conclusiones: La vacuna adyuvada MF59 presenta un buen perfil de seguridad. Los efectos adversos locales y sistémicos que puede ocasionar son típicos de cualquier vacuna inyectada y pueden presentarse con frecuencia similar que al utilizar vacunas antigripales convencionales.
Objective: To assess the safety of the MF59-adjuvanted influenza vaccine in adults versus conventional influenza vaccines.
Design: Systematic literature review.
Data sources: MEDLINE, EMBASE, CRD (Center for Review Dissemination), ECRI, Hayes, Health Technology Assessment Agencies databases, the USA clinical trial register ClinicalTrials.gov, and manual search of specialized journals. MeSH terms were "influenza", "vaccine", "adults", "safety", and free terms were "adjuvant vaccine" "Chiromas", "Fluad", and "MF59".
Methods: Inclusion criteria were studies including adults vaccinated with MF59-adjuvanted influenza vaccine, compared with conventional vaccines or placebo group, and including results on vaccine safety. The quality of studies included studies was assessed using the CASPe checklist.
Results: We selected 12 clinical trials with moderate-high quality. Local and systemic adverse effects were scarce and mild. There were no significant differences (P<.01) between the vaccines tested for most reactions. The most frequent and significant adverse effects of the adjuvant vaccine were pain (25.5%), heat (19.9%), local induration (11.2%), chills
(8.9%), fever (7.8%), and myalgia (7.5%).
Conclusions: The MF59-adjuvanted vaccine has a good safety profile. The local and systemic adverse effects that may result are typical of any injected vaccine and their frequency is similar to that of conventional influenza vaccines.