Determinar la distribución de los diferentes fenotipos tumorales del carcinoma mamario en pacientes venezolanas. Caracterizar las variables clinicopatológicas en cada subgrupo y establecer los patrones de supervivencia para cada fenotipo.
Pacientes y métodosSe evaluaron de forma retrospectiva los datos de 266 pacientes con diagnóstico de carcinoma de mama y estudio inmunohistoquímico de la biopsia inicial. Las pacientes fueron clasificadas en 3 grupos de fenotipos tumorales (receptor estrogénico positivo, HER2/neu sobreexpresado y triple negativo). Se determinaron y correlacionaron variables epidemiológicas, clínicas y patológicas.
ResultadosLos grupos de fenotipos tumorales estuvieron distribuidos en receptor estrogénico positivo con un 60,9%, triple negativo con un 27,8% y HER2/neu sobreexpresado con un 11,3%. El 92% de las pacientes con fenotipo triple negativo eran de raza negra. La mejor supervivencia correspondió al fenotipo receptor estrogénico positivo, y la peor, al fenotipo triple negativo, aunque las diferencias no fueron significativas.
ConclusionesLa distribución fenotípica del cáncer de mama en Venezuela es parecida a la de la literatura general. El subtipo triple negativo, que tuvo la peor supervivencia, aunque no de forma significativa, presentó una incidencia más elevada que la de otros grupos poblacionales. La mayoría de las pacientes en este subgrupo eran de raza negra.
To determine the distribution of the distinct breast carcinoma phenotypes in Venezuelan patients, characterize the clinicopathologic variables in each subgroup, and establish survival patterns for each phenotype.
Patients and methodsWe retrospectively evaluated data from 266 patients diagnosed with breast carcinoma and an immunohistochemical study of the initial biopsy. The patients were classified into 3 groups of tumor phenotypes (estrogen receptor-positive, HER2/neu overexpression and triple-negative). We determined and correlated epidemiological, clinical and pathological variables.
ResultsThe tumor phenotype groups were distributed as follows: estrogen receptor-positive in 60.9%, triple-negative in 27.8%, and HER2/neu overexpression in 11.3%. A total of 92% of the patients with triple-negative phenotype were African American. Survival was best with the estrogen receptor-positive phenotype and worst with the triple-negative phenotype, but these differences were not significant.
ConclusionsThe phenotypic distribution of breast carcinoma in Venezuela is similar to that reported in the general literature. The incidence of the triple-negative subtype, which showed the worst survival –although this result was not significant– was higher than in other populations. Most patients in this subgroup were African American.
El cáncer de mama es la afección neoplásica más frecuente en el hemisferio occidental. En el año 2010, se estimaron 1,6 millones de casos nuevos a nivel mundial1. En los Estados Unidos de Norteamérica ocurrieron alrededor de 229.060 casos en el año 2011, con una mortalidad de 39.920 mujeres2. En Venezuela, en el año 2010 se registraron 4.073 nuevos casos y 1.723 defunciones, representando la primera causa de incidencia y mortalidad en mujeres3, respectivamente.
Un dato digno de resaltar lo constituye la forma de presentación clínica de la enfermedad, mientras que en EE. UU. el porcentaje de enfermedad localizada en la mama alcanzó un 61% en el lapso 1996-20044, en Venezuela las cifras de enfermedad confinadas a la mama, registradas en los Institutos Públicos de Salud, apenas llegan a un 20% (solo en 2009), destacándose una mayoría de estadios donde la enfermedad se ha extendido fuera de la mama, traduciéndose esto en una mayor morbimortalidad y costes elevados del tratamiento respectivo3. Un hecho adicional es que la expresión de receptores hormonales y HER2/neu en el tumor proporciona información valiosa para instaurar el tratamiento y establecer el pronóstico de las pacientes. Sin embargo, a pesar de que existen muchos estudios que caracterizan los tumores de pacientes en ciertas localizaciones geográficas en cuanto a receptores hormonales y HER2/neu5,6, en Venezuela son muy escasos los antecedentes de estudios científicos al respecto7.
El término fenotipo tumoral se refiere a las características del tumor en términos de expresión de proteínas (receptores de membrana, proteínas intracitoplasmáticas, etc.), en este caso determinado en el análisis inmunohistoquímico (receptores hormonales, HER2/neu, Ki67, etc.). Actualmente es posible determinar las características genéticas (genotipo tumoral) de los carcinomas de mama a través de microarrays de ADN, lo cual nos da una idea acerca del pronóstico de la enfermedad. Esto permite establecer una clasificación molecular que consta de 4 categorías: Luminal A, Luminal B, Basal-like y HER2/neu sobreexpresado8. Existe cierta correspondencia entre estos tipos moleculares y la expresión de receptores hormonales y proteína HER2/neu, que, sin embargo, no se da en todos los casos9. Así, en general, los carcinomas tipo Luminal A expresan en la mayoría de los casos receptores hormonales, pero no muestran sobreexpresión de HER2/neu; esto cambia en el caso del Luminal B, que en la mayoría de los casos tiene positividad en el estudio inmunohistoquímico para receptores de estrógenos, baja expresión o ausencia de receptores de progesterona, y el HER2/neu puede o no estar sobreexpresado, con un Ki67 mayor a 14%10. Los del tipo Basal-like, en un porcentaje elevado de casos (75% aproximadamente) no expresan receptores hormonales ni HER2/neu (triple negativo)11. Los del grupo HER2/neu sobreexpresado no expresan receptores hormonales, pero si HER2/neu12.
El objetivo de nuestro estudio fue determinar la distribución de los diferentes fenotipos tumorales del carcinoma mamario en pacientes venezolanas, caracterizar las variables clinicopatológicas en cada subgrupo, y establecer patrones de sobrevida para cada fenotipo.
MétodosSe evaluaron de forma retrospectiva los datos de las pacientes que acudieron a la consulta de Patología Mamaria del Instituto de Oncología Dr. Luis Razetti, centro de referencia nacional, que recibe pacientes de toda Venezuela, en el período entre enero de 2003 y diciembre de 2005, previa aprobación del Comité de Ética del hospital y firma de consentimientos informados. El muestreo fue intencional no probabilístico. Los criterios de inclusión fueron: pacientes mujeres de cualquier edad con diagnóstico histológico de carcinoma de mama en cualquier estadio. Los criterios de exclusión fueron: pacientes masculinos e imposibilidad para la realización de estudio inmunohistoquímico.
Las pacientes con diagnóstico de lesión clínica o subclínica de mama fueron sometidas a estudio anatomopatológico por diversos métodos (aguja gruesa, biopsia ecoguiada, biopsia estereotáxica, biopsia radioquirúrgica, mastectomía).
Los datos se expresaron en tablas de una o 2 entradas; a las variables nominales se les calcularon las frecuencias y porcentajes; en el caso de las variables continuas, se calcularon sus medias y desviaciones estándar. Se utilizó el test de Log Rank para la comparación de supervivencia y curvas de sobrevida de Kaplan-Meier.
Se establecieron 3 grupos de fenotipos tumorales: receptor estrogénico positivo, HER2/neu sobreexpresado y triple negativo. De forma consensuada, decidimos no hablar de subgrupos luminal o basal, ya que no contamos con las plataformas de perfiles genéticos o moleculares para definir dichos subtipos intrínsecos.
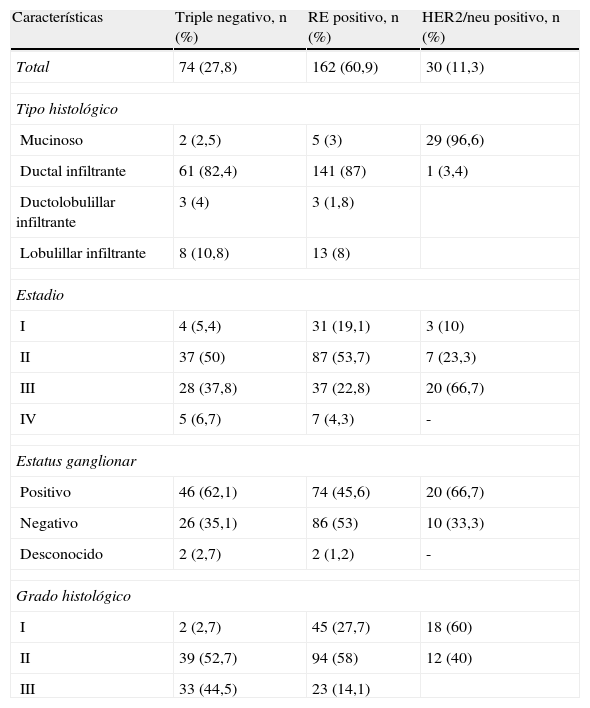
ResultadosSe estudiaron un total de 266 pacientes con diagnóstico de carcinoma de mama y estudio inmunohistoquímico de la biopsia inicial. Los grupos de fenotipos tumorales estuvieron distribuidos en receptor estrogénico positivo con un 60,9%, triple negativo con un 27,8% y HER2/neu sobreexpresado con un 11,3%. La media de edad fue de 51,2 años, y desglosado según fenotipo, las pacientes con receptores de estrógeno positivos, HER2/neu positivo y triple negativo tuvieron una media de 52,2, 49,8 y 50,7 años, respectivamente. El 81% (217) de las mujeres eran de raza negra, siendo esta característica predominante en el subtipo triple negativo (92%). La mediana de seguimiento fue de 40 meses (tabla 1).
Características generales de los fenotipos tumorales
| Características | Triple negativo, n (%) | RE positivo, n (%) | HER2/neu positivo, n (%) |
| Total | 74 (27,8) | 162 (60,9) | 30 (11,3) |
| Tipo histológico | |||
| Mucinoso | 2 (2,5) | 5 (3) | 29 (96,6) |
| Ductal infiltrante | 61 (82,4) | 141 (87) | 1 (3,4) |
| Ductolobulillar infiltrante | 3 (4) | 3 (1,8) | |
| Lobulillar infiltrante | 8 (10,8) | 13 (8) | |
| Estadio | |||
| I | 4 (5,4) | 31 (19,1) | 3 (10) |
| II | 37 (50) | 87 (53,7) | 7 (23,3) |
| III | 28 (37,8) | 37 (22,8) | 20 (66,7) |
| IV | 5 (6,7) | 7 (4,3) | - |
| Estatus ganglionar | |||
| Positivo | 46 (62,1) | 74 (45,6) | 20 (66,7) |
| Negativo | 26 (35,1) | 86 (53) | 10 (33,3) |
| Desconocido | 2 (2,7) | 2 (1,2) | - |
| Grado histológico | |||
| I | 2 (2,7) | 45 (27,7) | 18 (60) |
| II | 39 (52,7) | 94 (58) | 12 (40) |
| III | 33 (44,5) | 23 (14,1) | |
Ambas mamas estuvieron afectadas en un 2,3%. El 86,5% de las pacientes tuvo un diagnóstico histopatológico de carcinoma ductal infiltrante, seguido del de carcinoma lobulillar infiltrante en un 7,9%. Es reseñable que en todos los grupos fenotípicos hubo presencia de carcinoma lobulillar infiltrante, excepto en el grupo de HER2/neu sobreexpresado. La mayoría de las pacientes se encontraban en un estadio ii de la enfermedad (49,2%), y un 32% en estadio iii. El grado histológico predominante fue el grado ii (56,8%).
Se hallaron ganglios positivos en el 52,6% de los casos. La mayoría de las pacientes con estatus ganglionar negativo tuvieron como fenotipo el receptor estrogénico positivo (70,5%). El tipo de cirugía más frecuente fue la mastectomía radical modificada de Madden con un 57%, seguida de la mastectomía parcial oncológica más disección axilar linfática con un 29,7%.
De las 266 pacientes, 215 (80,8%) recibieron tratamiento quimioterápico antes o después de la cirugía, y 204(76,7%) recibieron radioterapia postoperatoria. Todas las pacientes con tumores triple-negativo recibieron quimioterapia. No recibieron quimioterapia las pacientes con tumores menores a un centímetro, ganglios negativos o contraindicaciones médicas. Todas las pacientes con receptores hormonales positivos recibieron terapia endocrina. El esquema de quimioterapia más utilizado, en todos los grupos, fue adriamicina-ciclofosfamida por 4 ciclos, seguido de paclitaxel por 4 ciclos. El 74,4% de las pacientes se encuentran vivas sin enfermedad, el 14,7% fallecieron a causa de su dolencia, y el 9,8% se encuentran vivas con metástasis a distancia. La mayor parte de las pacientes que fallecieron por enfermedad eran de fenotipo triple negativo.
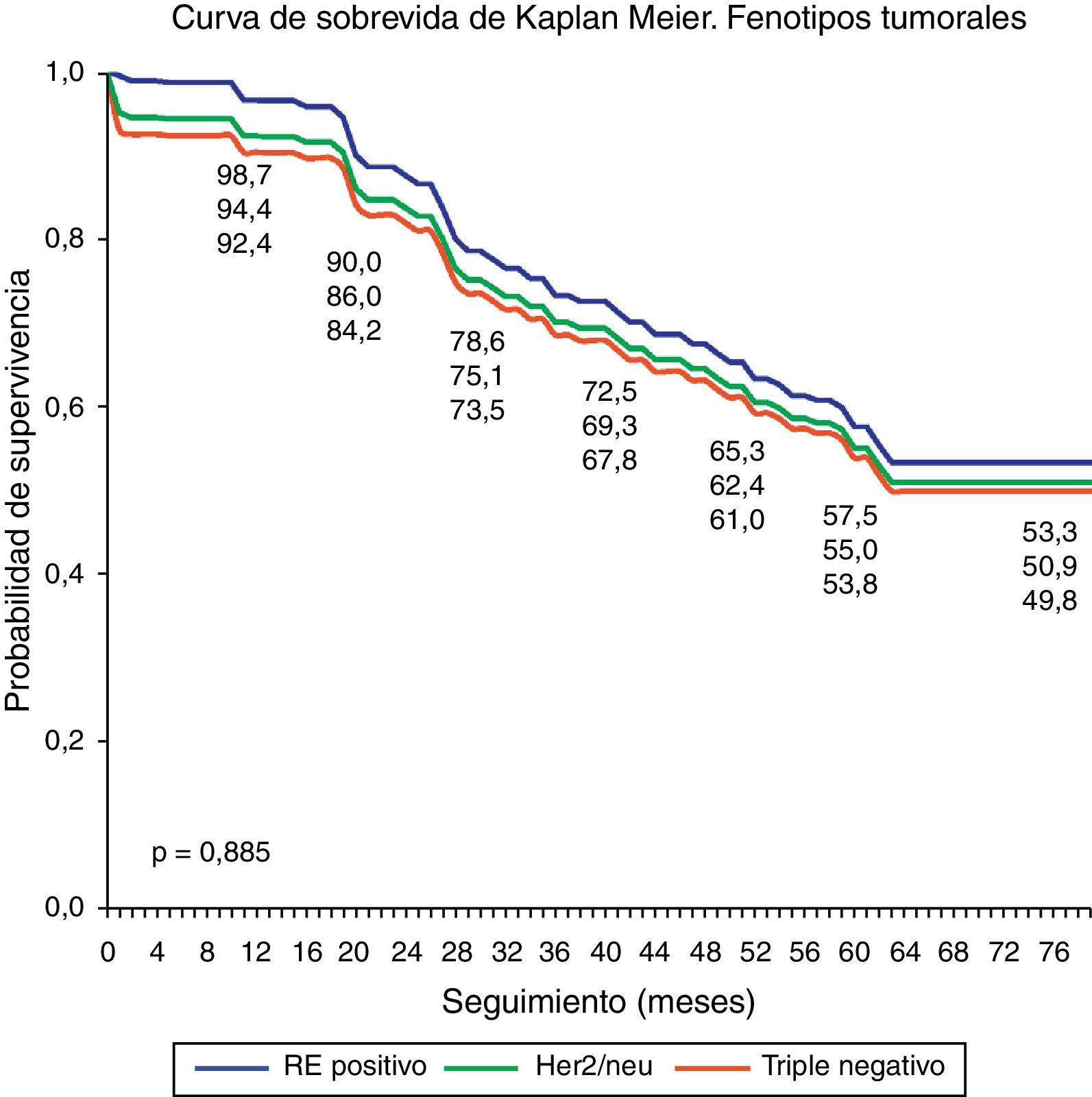
Un gran número de pacientes con HER2/neu sobreexpresado presentaron T3 patológico. El fenotipo receptor estrogénico positivo presentó la mejor supervivencia global, y la peor la presentó el fenotipo triple negativo, aunque estas diferencias no fueron significativas (p=0,885) (fig. 1).
DiscusiónEn este trabajo se presenta una casuística de pacientes con diagnóstico de carcinoma de mama, describiendo sus características fenotípicas, clínicas y epidemiológicas. El término fenotipo tumoral se refiere a las características del tumor en términos de expresión de proteínas (receptores de membrana, proteínas intracitoplasmáticas, etc.), en este caso determinados en el análisis inmunohistoquímico (receptores hormonales, HER2/neu, Ki67, etc.). Existen muy pocos estudios en nuestro país que describan el patrón de expresión de receptores hormonales y proteína HER2/neu en mujeres venezolanas con carcinoma de mama13. Hay que resaltar que la población venezolana es bastante homogénea en cuanto a su distribución racial en todo el territorio nacional, exceptuando la zona del Amazonas fronteriza con Brasil, que es predominantemente indígena, representando un 0,5% de la población nacional. El Instituto de Oncología Dr. Luis Razetti es uno de los 3 hospitales oncológicos del país. Es el más grande de ellos y está situado en Caracas, capital de Venezuela. Este centro recibe pacientes de todos los estados de la nación, por lo que inferimos que nuestra muestra es representativa de la población venezolana.
Los grupos de fenotipos tumorales estuvieron distribuidos en receptor estrogénico positivo con un 60,9%, triple negativo con un 27,8% y HER2/neu sobreexpresado con un 11,3%. En este último, los receptores hormonales fueron negativos. Sin embargo, en el grupo de receptores positivos hubo 23 (8,6%) pacientes con HER2/neu sobreexpresado (triple positivo), con lo cual tendríamos un total de 53 (19,9%) pacientes con HER2 sobreexpresado en la inmunohistoquímica. A pesar de esto, fueron incluidos dentro del grupo de receptores positivos por tratarse muy posiblemente desde el punto de vista molecular del subtipo Luminal B, es decir, nuestro grupo de receptores positivos incluiría los fenotipos Luminal A y B. Esta distribución es parecida a la establecida en la literatura internacional, aunque observamos un porcentaje del fenotipo triple negativo levemente superior en nuestra muestra8,14,15. Carey et al. demostraron una alta prevalencia de tumores triple negativo en mujeres de raza negra16, como en nuestra muestra. Cuando comparamos nuestros hallazgos con los encontrados en otros grupos poblacionales, observamos en un estudio publicado por Spitale et al.17 que la prevalencia de pacientes con tumores triple negativo en el sur de Suiza es de 7,4%, porcentaje sustancialmente más bajo que el de esta muestra. En una investigación más reciente, Xue et al.18 estudiaron las características inmunohistoquímicas de 5.809 pacientes chinas, encontrando un 16,5% de tumores triple negativo. Es de resaltar que un elevado porcentaje de las pacientes triple negativo tuvieron tumores mal diferenciados, lo cual coincide con lo establecido previamente por otros autores19–21.
La mayoría de las pacientes se encontraba en estadio ii o iii, como es usual en nuestro medio, donde la mayoría de las pacientes que recibimos se encuentran en fases avanzadas de la enfermedad, a diferencia de otros países donde han desarrollado sistemas de screening y diagnóstico precoz, lo que se ha traducido en un aumento de las pacientes que acuden a los hospitales en estadios tempranos22,23. Probablemente este fenómeno pueda explicar que la mastectomía radical modificada haya sido el tipo de cirugía más común en nuestro grupo de estudio.
En cuanto a la supervivencia global, se ha establecido que los tipos de receptores estrogénicos positivos (y luminales en general) tienen mejor supervivencia y que las pacientes triple negativo tienen el peor pronóstico24. Esto se reprodujo en nuestro estudio, en donde también observamos que el grupo con comportamiento intermedio en términos de supervivencia es el de las pacientes con HER2/neu sobreexpresado, aunque en nuestro estudio estas diferencias no alcanzaron la significación estadística.
Además, en pacientes con HER2/neu sobreexpresado existen fármacos tan específicos como el trastuzumab (Herceptin®), que es utilizado tanto en tratamiento adyuvante como neoadyuvante, o el TDM1, que sigue bajo investigación en ensayos clínicos para esta diana25. El tamoxifeno y los inhibidores de la aromatasa son empleados en pacientes con receptores hormonales positivos, y más recientemente los fármacos inhibidores de la poli-ADP ribosa polimerasa, como el iniparib y el olaparib, que están siendo analizados en estudios fase iii, en pacientes triple negativos26, con lo cual observamos la importancia de establecer el fenotipo de los tumores y su implicación en el tratamiento.
Concluimos que la distribución fenotípica del carcinoma de mama en Venezuela es parecida a la ya establecida en otras latitudes. Sin embargo, observamos que el subtipo triple negativo tiene una incidencia más elevada en Venezuela, sobre todo en mujeres de raza negra. Los datos obtenidos en cuanto a la supervivencia tienen un valor limitado, ya que no pudieron ser estratificados en base al tratamiento recibido y por estadios, por razones inherentes a la muestra. Se requieren estudios adicionales para mejorar la información epidemiológica existente en nuestro país.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido información suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
AutoríaLos autores han leído y aprobado el manuscrito y declaran que los requisitos para la autoría se han cumplido.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.