El hipogonadismo de inicio tardio en el hombre puede ser definido como un síndrome clinico y de laboratorio asociado al envejecimiento del individuo, caracterizado por la presencia concomitante de síntomas y una disminución de los niveles séricos de testosterona (bajo los niveles séricos normales del adulto joven sano). La deficiencia de andrógenos se expresa por sintomatologia variada y poco especifica, destacando las manifestaciones de la estera sexual. En estos pacientes se debe solicitar los niveles séricos de testosterona total. No se recomienda el tamizaje de hipogonadismo en población general. Los riesgos y beneficios de la terapia con testosterona deben ser discutidos con el paciente. La ausencia de respuesta sintomática en 3-6 meses debe hacer suspender la suplementación y buscar otras patologías que expliquen el cuadro clínico. El adecuado diagnóstico y tratamiento de estos pacientes se traduce en una significativa mejoría de la calidad de vida, de la función sexual y sus parámetros metabólicos.
Late-Onset Hypogonadism (LOH) is a clinical and biological syndrome associated with advancing age and characterized by symptoms and a deficiency in serum testosterone levels (below the young healthy adult male reference range). The androgen deficiency is expressed by a variety of non-specific symptoms, particularly in terms of sexual activity.
This patients require the measurement of total testosterone serum levels. It is not recommended to screen the general population for hypogonadism. The benefits and risks of testosterone replacement must be discussed with the patient. If no improvement is seen in 3-6 month, the treatment should be suspended and alternative causes should be investigated. The correct diagnosis and treatment of patients with LOH results in a enhanced sexual function, improved metabolic parameters, and a better quality of life.
En 1889, el fisiólogo Francés Charles-Edouard Brown-Séquard, se inyectó extrados de testículo de perro y al hacerlo, probablemente se convirtió en el primer ser humano en beneficiarse de la terapia hormonal de reemplazo (1). Escribió en el Lancet; “El día posterior a la primera inyección subcutánea... un cambio radical ocurrió en mi”(2), e ilustró cómo sus capacidades tanto físicas como mentales mejoraron. Señalando inclusive que experimentó “una gran mejoria con respecte a la eliminación de deposiciones más que ninguna otra función”(2).
En la actualidad, es sabido que la cantidad de testosterona que BrownSéquard se inyectó, resultó ser cuatro veces menor a la magnitud necesaria para tener una acción biológica (3). Por lo que es probable que los cambios ocurridos hayan sido efecto placebo.
Sin embargo a partir de ese entonces, comenzó a adquirir más in terés el estudio de las hormonas masculinas y su función en la vida diaria. Finalmente se identificaron las hormonas masculinas: los andrógenos.
Fisiología de los andrógenosLos andrógenos son producidos por los testículos y las glándulas suprarrenales y juegan un rol esencial en la función sexual y reproductiva masculina. Además son esenciales para el desarrollo normal del aparato reproductor masculino, como el epidídimo, conducto deferente, vesículas seminales, próstata y pene (4). Los andrógenos son necesarios tanto para la pubertad como la para la fertilidad y es sabido su requerimiento en la formación muscular, mineralización ósea, metabolismo de triglicéridos y funciones cognitivas (5).
En la próstata, pene y escroto, la testoterona (T) es convertida a un metabolite más potente, la Dihidrotestosterona (DHT) a través de la enzima 5 alfa reductasa y ambas estimulan al receptor de andrógenos (RA) (6). Además la Testosterona puede ser metabolizada en estradiol, a través de la enzima Aromatasa, que se encuentra en el tejido graso, próstata y hueso.
La mayor proporción testosterona sérica se encuentra unida a SHBG y Albúmina, la testosterona en forma libre representa entre el 0,5-3% de la testosterona total (7).
La producción de testosterona es controlada por la Hormona Luteinizante (LH), secretada por la glándula hipófisis. Inmediatamente después del nacimiento, los niveles séricos de T alcanzan concentraciones semejantes a las del adulte. Posteriormente y hasta la pubertad, sus niveles son bajos. El desarrollo puberal comienza con la producción de gonadotrofinas, iniciada por pulsos de GnRH que es secretada por el hipotálamo y que resulta en la producción de T, con la consecuente aparición de caracteres sexuales secundarios y espermatogénesis (4).
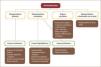
Hipogonadismo y subtiposEl hipogonadismo masculino, se puede definir con un síndrome causado por la deficiencia de andrógenos que puede afectar de manera adversa la función de múltiples órganos y la calidad de vida del individuo (8). Y puede ser clasificado en 4 grupos, dependiendo el nivel a la cual ocurre la disfunción como muestra la figura 1 (9).
El hipogonadismo primario (HP) es consecuencia de una falla a nivel testicular, por lo que los niveles de testosterona son bajos, las gonadotrofinas son altas y como consecuencia hay ausencia de espermatogénesis que es irreversible.
El hipogonadismo secundario (HS) es aquel en que la falla se pro duce a nivel de Hipotalamo-Hipófisis, por lo que los niveles de testosterona son bajos, las gonadotrofinas son bajas y hay ausencia de espermatogénesis que se revierte ante la administración de gonadotrofinas.
El hipogonadismo por defectos de los receptores (HDR), son causas raras de hipoandrogenismo. Hay defectos completos y parciales que escapan a los objetivos de esta revisión.
La clasificación del hipogonadismo tiene implicancias terapéuticas. En pacientes con hipogonadismo secundario, la estimulación hormonal con hCG, FSH o GnRH puede restaurar la fertilidad en la mayoria de los pacientes (10,11).
Cuando el déficit de testosterona se produce antes de la pubertad, no se desarrollan caracteres sexuales secundarios y se producen alteraciones esqueléticas con proporciones eunucoides. Una vez que el individuo ha adoptado proporciones eunucoides, el proceso es irreversible.
Cuando el déficit de testosterona se produce post pubertad, el cuadro clinico de hipogonadismo se presenta con síntomas y signos que pueden diferir de un caso a otro. Dentro de estos se encuentra la regresión de los caracteres sexuales secundarios, las proporciones corporales no se modifican, el tamaño del pene y el tono de voz no varían, sin embargo, hay disminución de la potencia sexual, pérdida de la libido e infertilidad. A las manifestaciones clinicas causadas por el déficit hormonal, se añaden las dependientes de la causa que determina el hipogonadismo.
En la Tabla 1 se mencionan los síntomas y signos de hipogonadismo en el hombre (7). Es importante mencionar que el sintoma que más se asocia a hipoandrogenismo es la disminución de la libidoy que ninguno de estos síntomas son especificos de deficiencia sérica de andrógenos (10). Por lo tanto, la presencia de alguno de estos síntomas debe hacer sospechar la deficiencia de testosterona sérica y ser corroborado con la medición de testosterona total.
Signos y síntomas de hipogonadismo en hombres
| -Desarrollo sexual incompleto o retardado. |
| -Proporciones eunocoides. |
| -Disminución de la libido y actividad sexual. |
| -Disminución de erecciones espontáneas. |
| -Ginecomastia |
| -Disconfort mamario |
| -Pérdida de vello axilar y púbico |
| -Testículos pequeños (especialmente < a 5ml) o disminución del tamaño testicular |
| -Infertilidad, bajo recuento espermático |
| -Fracturas patológicas |
| -Baja densidad mineral ósea. |
| -Bochornos |
| -Sudoración |
| -Disminución de fuerza y masa muscular |
| -Aumento del tejido graso |
| -Baja Vitalidad |
| -Ánimo Depresivo. |
Bhasin S, Cunningham GR, Hayes FJ, et al. Testosterone Therapy in adult men with androgen difieency syndromes: An Endocrine Society clinical practice guideline. J Clin Encrinol Metab. 2010;95(6):2536-2559 (traducido y adaptado).
El hipogonadismo de inicio tardio, también llamado sindrome de deficiencia androgénica asociado a la edad (TDS) puede ser definido como un síndrome clínico y de laboratorio asociado al envejecimiento, caracterizado por síntomas y una disminución de los niveles séricos de testosterona (bajo los niveles séricos normales del adulto joven sano) (12). Esta condición puede resultar en un significativo deteriora de la calidad de vida y afectar negativamente la función de múltiples órganos y sistemas (12).
El TDS es consecuencia de la disminución del nivel de testosterona (1-2% anual) por el envejecimiento normal del varón. Solo afecta a un porcentaje de los hombres y su prevalencia aumenta progresivamente con la edad: 7% entre los 40-60 años, 21 % entre los 60-80 años y 35% en mayores de 80 años (13).
Los bajos niveles de testosterona relacionados con la edad tienen ele-mentos de hipogonadismo primario y secundario, y presentan las siguientes características: Una disminución de los niveles plasmáticos de testosterona total, libre y un aumento de la SHBG (13), disminución de la secreción de testosterona en respuesta a estimulación con gonadotrofinas (14) y cambios en el patrón de liberación de LH(15).
Los valores séricos de testosterona pueden variar en forma significativa por las condiciones señaladas en la Tabla 2 (16). Cabe señalar que hasta un 30% de los hombres con hipogonadismo leve, presentarán niveles séricos de testosterona normales en mediciones repetidas (7). Además, existen medicamentos que alteran los niveles plasmáticos de testosterona (Tabla 3) y condiciones que alteran la concentración de SHBG (7) (Tabla 4). Estas condiciones deben ser tomadas en cuenta al momento de plantear el diagnóstico.
Variaciones en los niveles plasmáticos de testosterona
| -Edad (disminución de los niveles plasmáticos de testosterona 1 a 2% por año). |
| -Ritmo circadeano (pick entre las 8 am y 11 am) |
| -Secreción episódica: 30% de los hombres con hipogonadismo leve, presentaran niveles séricos de testosterona normales en repetición de examen. |
| -Ejercicio intenso reduce los niveles plasmáticos de testosterona. |
| -Comorbilidades que producen cambios en los niveles de SHBG. |
| -Desórdenes alimentarios |
| -Medicamentos |
| -Variaciones en las mediciones de laboratorio (ausencia de un gold standard) |
Bhasin S et al Guidelines & Protocols Advisory committee. Testosterone testing protocol. Effective date: June 2011 bcguidelines.ca (traducido y adaptado)
Medicamentos que pueden alterar los niveles plasmáticos de testosterona
| Aumentan los niveles séricos | Disminuyen los niveles séricos |
|---|---|
| Cimetidina | Esteroides Anabólicos |
| Finasteride | Carbamacepina |
| Rafampicina | Corticoides |
| Tamoxifeno | Ciclofosfamida |
| Acido Valproico | Digoxina |
| Fenitoina | Estrógenos |
| Ketoconazol | |
| Opioides | |
| Espironolactona | |
| Tetraciclina | |
| Verapamilo | |
| Ciproterona |
Ref 7. Bhasin S, Cunningham GB, Hayes FJ, et al. Testosterone Therapy in adult men with androgen difieency syndromes: An Endocrine Society clinical practice guideline. J Clin Encrinol Metab. 2010;95(6):2536-2559 (traducido y adaptado)
Condiciones asociadas a alteraciones en concentración de shbg
| Disminución concentración SHBG | Aumento concentración SHBG |
|---|---|
| Diabetes Mellitus* | Edad* |
| Obesidad Moderada* | Cirrosis Hepática y hepatitis* |
| Síndrome Nefrótico* | Anticonculsivantes* |
| Glucocorticoides, | Estrógenos |
| progestinas y | Infección porVIH |
| esteroides* | Hipertiroidismo |
| Hipotiroidismo | |
| Acromegalia | |
| Hipertiroidismo |
Ref 7. Bhasin S, Cunningham GB, Hayes El, et al. Testosterone Therapy in adult men with androgen difieency syndromes: An Endocrine Society clinical practice guideline. J Clin Encrinol Metab. 2010;95(6):2536-2559 (traducido y adaptado)
Existen diferentes cuestionarios, como el Aging Male Symptom Score (AMS) y el Androgen Dificiency in Aging Men (ADAM), que no son recomendados para el diagnóstico de hipogonadismo debido a su baja especificidad (12). Las diversas Sociedades Científicas que estudian hipogonadismo tardio no recomiendan el tamizaje en población sana utiizando este tipo de cuestionarios, como tampoco mediciones masivas de niveles séricos de andrógenos.
En los pacientes que presenten los síntomas antes mencionados, debe realizarse una historia clínica y examen físico detallado, como también se debe solicitar testosterona sérica total, ya que el diagnóstico de TDS requiere necesariamente de la asociación tanto clínica como bioquímica.
Enfermedades agudas producen una disminución de la testoterona total, por lo que debe ser evitada su medición cuando un paciente presenta una de estas condiciones. Además, la obesidad y las enfermedades crónicas, como la diabetes mellitus, enfermedad pulmonar obstructiva crónica, VIH y síndrome metabólico son factores de riesgo para hipogonadismo, por lo que deben ser investigadas y tratadas en caso de estar presentes (12).
La muestra de testosterona total debe ser tornada durante la mañana, preferiblemente antes de las 10 am (17) y además ser confirmada con una segunda muestra (14) debido a que como fue mencionado previamente, hasta un 30% de los hombres con hipogonadismo leve, presentaran niveles séricos de testosterona normales en mediciones repetidas y un 15% de hombres sanos pueden presentar niveles de testosterona bajo el rango normal en un periodo de 24 horas (7).
Existe consenso que valores superiores a 12 nmol/l (350 ng/dl) no requerirán terapia de sustitución y que valores inferiores a 8 nmol/l (230 ng/dl) se podrian beneficiar de la terapia con testosterona. En casos de valores entre los 8 nmol/l (230 ng/dl) y 12 nmol/l (350 ng/dl), es recomendable repetir la medición de testosterona y solicitar a su vez SHBG y albúmina para calcular la testosterona libre y/o biodisponible (12). Los inmunoensayos de testosterona libre actuales no tienen una precisión adecuada y existe variabilidad es su estandarización, por lo que no se recomienda su uso (18). No existen valores de cortes preestablecidos, sin embargo niveles de testosterona libre menores a 225 pmol/l (65 pg/ml) pueden aportar evidencia que apoye el tratamiento con testosterona (12). Además se debe solicitar niveles de FSH y LH, los cuales pueden es estos casos aparecer normales, levemente elevados o disminuidos, sin embargo permiten hacer la distinción entre el mecanismo predominante de hipogonadismo (hipogonadismo primario o secundario). La Figura 2 describe cómo enfrentar la evaluación diagnóstica del hombre con hipogonadismo (7).
Resumen de la evaluación y diagnóstica del hombre adulto con sospecha de hipogonadismo
Bhasin S, Cunningham GR, Hayes FJ, et al. Testosterone Therapy in adult men with androgen difiecency syndromes: An Endocrine Society clinical practice guideline. J Clin Encrinol Metab. 2010;95(6):2536-2559 (traducido y modificado)
Existe evidencia de que la terapia con testosterona produce un aumento de la masa muscular y densidad minerai ósea y una disminución del tejido graso. Beneficios secundarios como mejoría en la fuerza muscular, del síndrome metabólico y de la disfunción cardiovascular son sugeridos por la literatura actual, pero requieren confirmación por estudios de mayor tamaño (12).
A pesar de que la osteopenia, osteoporosis y fracturas son más frecuentes en hombres con hipogonadismo, y que la terapia con testosterona aumenta la densidad mineral ósea, (12) no hay estudios por el momento que reporten el efecto beneficioso de la suplementación con testosterona en la prevención de fracturas óseas (7).
Los objetivos de la terapia con testosterona son: mejorar la calidad de vida, la función psico-sexual, restaurar los parámetras a un estado eugonadal en rango inferior de normalidad (T sérica mayor 300ng/dl), mejorar la función neuropsicológica, mantener la densidad minerai ósea y aumentar la masa muscular.
Además, a hombres con disfunción eréctil o disminución de la libido, dentro del estudio inicial se sugiere incluir niveles séricos de testosterona, los cuales, si se encuentran inferiores a los rangos antes señalados, serían candidates a la suplementación de testosterona. En caso de ausencia de respuesta a la testosterona, se debe revaluar el mecanismo responsable de la disfunción (12).
Existe relación entre el síndrome metabólico e hipogonadismo. Entre el 20-64% de los hombres obesos tienen bajos niveles de testosterona total (19). Asimismo, hay asociación entre la Diabetes Mellitus y bajos niveles de testosterona. Por lo que a hombres con Diabetes Mellitus o síndrome metabólico y síntomas de hipogonadismo se les debe solicitar rutinariamente testosterona total (12).
TratamientoPara la suplementación con testosterona, deben utilizarse preparaciones de origen natural. Todas las vías de administración: intramuscular, subdérmica o transdermal, bucal y oral han demostrado ser eficientes y seguras (12). El clínico debe conocer la farmacocinética, y las ventajas y desventajas de cada forma de presentación, siendo la decisión tomada en conjunto con el paciente (12). No existe evidencia suficiente para recomendar la sustitución con dihidrotestosterona (DHT) y tampoco se recomienda el uso de precursores de la testosterona (DHEA, DHEA-S, androstenediol o androstenediona). El uso de 17 alfametil testosterona está contraindicado por la hepatotoxicidad potencial (12). Actualmente los niveles séricos de testosterona apropiados como margen terapéutico son entre el nivel inferior y medio del rango de testosterona sérica normal de adultos jóvenes (12).
En el anexo 1 se detallan las diferentes formas de presentación, dosis, farmacocinética, relación con DHT y E2, ventajas y desventajas de la Testosterona disponible (7). En Chile, se encuentra en forma de Gel de 5gr y 2.5gr (50 y 25mg de T respectivamente), en forma de Enantato de Testosterona para inyección cada 3-4 semanas y Undecanoato de testosterona intramuscular (1000mg). Las presentaciones orales de testosterona son poco recomendables y su dispo-nibilidad es escasa.
Anexo 1
| Formulación | Régimen | Farmacocinética | DHT y E2 | Ventajas | Desventaajs |
|---|---|---|---|---|---|
| Enantato o cipionato T | 150-200mg lM cada 2 So 75-100mg/S | Posterior a una injección los niveles séricos de T aumentan a rangos suprafisiológicos y después declinan gradualmente a rangos infrafisiológicos al final del intervalo de la dosis | DHTy E2 aumentan en niveles proporcionales al aumento de T T:DHT y T:E2 proporciones no cambian | Corrige síntomas de deficiencia de andrógenos. Relativamente económico. Flexibilidad en la dosis | Requiere inyección intramuscular. Hay picks (supra e infrafisiologicos) en los niveles plasmaticos de T |
| 1% Gel Testosterona* | Disponible en tubos y surtidores 5-10g T gel contiene 50-100mg T por dia | Restaura los valores de T y E2 a niveles fisiológicos masculinos | Nivelés séricos de DHT son mayores y la proporción T:DHT son menores en Hombres con hipogonadismo que H eugonadales | Corrige sintomas de deficiencia de andrógenos. Flexibilidad en dosis. Fácil aplicación. Buena tolerabilidad de la piel | Potenciál transferencia compañera / hijos por contacta directe piel a piel. Irritacion de la piel en pequeños porcentajes. Niveles moderadamente aumentados de DHT |
| Parches Transdérmicos de T | 1 o 2 parches, diseñados para aportar 5-10mg T en 24hrs.Aplicado en zonas de no presión | Restaura los niveles de T, DHT y E2 a niveles fisiológicos masculinos | T:DHT yT:E2en niveles fisiológicos masculinos. | Fácil aplicación. Corrige síntomas de deficiencia de andrógenos | Niveles Serológicos de T en algunos hombres en el rango inferior normalidad. Estos pueden requerir 2 parches dia. Irritación de la piel ocurre frecuentemente. |
| Bucal, bioadesivo, Capsulas T | 30mg liberación controlada, tabletas bioadhesivas 2 veces al día | Absorbidos por la mucosa oral | Normaliza niveles serológicos de T y DHT en hombres con hipogonadismo | Corrige síntomas de deficiencia de andrógenos | Problemas gingivales en 16 % de los hombres en tratamiento. |
| Pellets T | 3-6 pellets implantados SC. Dosis y régimen varían según formulación | Piek serológico de T al mes, y después niveles normales por 3-6 meses dependiendo formulación | T:DHT yT:E3 proporciones no varían | Corrige síntomas de deficiencia de andrógenos | Requiere insertión quirúrgica. Pueden salirse espontáneamente. |
| T Oral Undecanoato* | 40 a 80mg vía oral 2-3 veces al día con comidas | Cuando es administrado con acido oleico, la T undecanoato es absorbida a través del sist. Linfático, con bypass del sistema portal. Variación considerable en el mismo individuo en diferentes dias, y entre individuos | Proporción DHT:T aumenta | Conveniencia de administración oral | No aprobado para uso en EE.UU.Variabilidad en respuesta clínica, variables niveles serológicos de T y alta proportión DHT:T |
| T Undecanoato Injectable de acción prolongada.* | Regimen Europeo: 1000mg lM, seguido por 1000mg a la 6a Semanay 1000mg cada 10-14 Semanas | Cuando administrado a dosis de 750mg a 100mg lM los niveles serológicos de T son mantenidos en rango normal en la mayoria de los pacientes | DHT y E2 aumentan en proporción al aumento de T T:DHT y T:E2 proporciones no cambian | Corrige síntomas de deficiencia de andrógenos. Requiere administraciones poco frecuentes. | Requiere inyecciones de 4ml. Tosreportada inmediatamente posinyeccion en un bajo número de pacientes. |
| Testosterona en parches adheslvos “matrix” | 2 × 60cm2 parches, entregando aprox 4,8mg T/ dia | Restaura los niveles sericos de T, DHT y E2 a rangos fisiológicos | T:DHT y T:E2 se encuentran en rangos fisiológicos | Dura 2 días | Irritación de la piel en algunos pacientes. |
El paciente debe ser evaluado a los 3 y 6 meses de iniciado el tratamiento para evaluar la regresión de síntomas y aparición de efectos adversos (7). Se sugiere monitorizar los niveles de testosterona a los 3-6 meses (7), siendo el objetivo el aumento de testosterona séricos a rangos normales. Para esto es fundamental conocer las propiedades farmacocinéticas del fármaco involucrado. En cuanto al Enantato y Cipionato de uso intramuscular, se deben medir los niveles séricos en medio de una inyección y otra, ajustando dosis o frecuencia si T > 700mg/dl o <400mg/dl). En el Undecanoato IM, los niveles de T deben ser solicitados justo antes de la siguiente inyección y en la formulación GEL, los niveles de T pueden ser medidos en cualquier momento luego de una semana de aplicación (7).
Se debe solicitar hematocrito previo inicio del tratamiento, a los 3 y 6 meses y luego anualmente de comenzado este. Frente a Hematocrito >54% se sugiere suspender la terapia hasta que disminuya a niveles fisiológicos (7). También se sugiere realizar una densitometría ósea posterior a 1-2 años de terapia. Además se debe monitorizar la prós-tata con APE y tacto rectal a los 3-6 meses y luego de forma anual. (7) En caso de un incremento de concentración del APE > 1,4 ng/ ml en 12 meses o una velocidad de ascenso >0,4ng/ml en 6 meses, una anormalidad al tacto rectal o HPB muy sintomática (Score AUA IPSS >19) el paciente deber ser derivado a evaluación urológica con rapidez.
Si la respuesta clínica es inadecuada a la sustitución hormonal, para las alteraciones del ámbito sexual y los síntomas del paciente en un periodo de 3-6 meses, la terapia debe ser suspendida y las causas de los síntomas reinvestigados (12).
En pacientes con cuadro clínico de disfunción sexual y niveles séricos de testosterona límite, una vez evaluada las comorbilidades (ej : Diabetes Mellitus, Sindrome Metabólico, Enfermedad vascular periférica, entre otros) se justifica realizar una prueba terapéutica (12).
La terapia con testosterona se encuentra contraindicada en forma ab-soluta en hombres con cáncer de próstata o cáncer de mama, (12) tanto en aquellos casos sospechosos como confirmados. Hombres que hayan sido tratados satisfactoriamente de cáncer de próstata y con severos síntomas de deficiencia androgénica, son potenciales candidatos a terapia de sustitución, siempre y cuando no haya evidencia tanto clínica ni de laboratorio de cáncer residual. Sin embargo no existen series clínicas a largo plazo que permitan dar una recomendación en cuanto al lapso de tiempo necesario (12). Es por esto que la decisión debe ser realizada a través del buen juicio clínico.
La apnea obstructiva del sueño no controlada, insuficiencia cardiaca congestiva no compensada, policitemia (>52%) e hiperplasia prostática benigna con uropatía obstructiva severa (IPSS > 21), representan contraindicaciones relativas (12), debiéndose tratar y/o controlar la comorbilidad previo al tratamiento.
Previo al inicio de terapia con testosterona, se debe realizar un tacto rectal, solicitar un APE sérico y excluir el riesgo de cáncer de próstata preexistente.
ConclusiónEl hipogonadismo de inicio tardío puede ser defnido como un síndrome clínico y de laboratorio asociado al envejecimiento del individuo, caracterizado por la presencia concomitante de síntomas y una disminución de los niveles séricos de testosterona (bajo los niveles séricos normales del adulto joven sano) (12). La defciencia de andrógenos se expresa por sintomatología variada y poco específica, destacando las manifestaciones de la esfera sexual. En estos pacientes se debe solicitar la medición de los niveles séricos de testosterona total. No se recomienda el uso de tamizaje en hipogonadismo en población general. Los riesgos y beneficios de la terapia con testosterona deben ser discutidos con el paciente. La ausencia de respuesta sintomática en un periodo de 3-6 meses debe hacer suspender la suplementación y buscar otras patologías que expliquen dicha sintomatología. El adecuado diagnóstico y tratamiento de estos pacientes se traduce en una significativa mejoría de la calidad de vida, de la función sexual y sus parámetros metabólicos.
Los autores declaran no tener conflictos de interés, con relación a este artículo.