El aumento progresivo de la esperanza de vida ha impuesto nuevos desafíos en el abordaje de las patologías que sufren los adultos mayores. Las demencias son unas de las patologías más frecuentes en este grupo etario, causando la pérdida de autonomía de los pacientes y afectando la salud y calidad de vida de sus cuidadores. En conjunto con otros exámenes, la evaluación neuropsicológica cumple un rol fundamental en el proceso de diagnóstico de las demencias, objetivando el Deterioro Cognitivo, entregando información sobre la autonomía de los pacientes y cumpliendo un rol indispensable en el seguimiento de estas enfermedades. La siguiente revisión presentará la problemática y los primeros estudios cognitivos de las demencias, finalizando con una síntesis de las investigaciones que han contribuido a establecer los perfiles neuropsicológicos de las demencias con mayor incidencia en la población.
The progressive increase in life expectancy has imposed new challenges in addressing the diseases suffered by older adults. Dementia is among the most common diseases in this age group, causing a loss of autonomy of patients and affecting the health and quality of life of their caregivers. In conjunction with other tests, neuropsychological evaluation plays a key role in the diagnostic process of dementia, substantiating cognitive impairment, providing information on the autonomy of patients, and fulfilling a vital role in monitoring this disease. The following review will present the problems and early the cognitive studies of early dementia, ending with a summary of the research that has helped establish the neuropsychological profiles of dementia with the highest incidence in the population.
La Organización Mundial de la Salud (OMS) estima que hay actualmente cerca de 600 millones de personas con más de 60 años; esta cifra se duplicará el año 2025 y llegará a los 2000 millones en el año 2050. También proyecta que en el 2050, el 22% de los habitantes del mundo tendrá más de 60 años y que 400 millones de personas superarán los 80 años 1.
El gran crecimiento de este grupo etario a nivel mundial es un fenómeno que se observa también en Chile. Según cifras de la Encuesta CASEN 2013 hay 2.885.157 de adultos mayores de 60 años, equivalente al 16.7% de la población 2.
Las demencias son una de las principales causas de discapacidad en la vejez 3. Se estima que existen actualmente 46.8 millones de personas que padecen algún tipo de demencia en el mundo. Las proyecciones indican que esta cifra se duplicará cada 20 años, llegando a los 74.7 millones en el 2030 y los 131.5 millones en el 2050. A nivel regional, se estima que en el continente americano existirían 9.4 millones de pacientes con demencia 4. En Chile, los estudios consideran que 181.000 personas padecen algún tipo demencia en la actualidad 5.
Los trastornos cognitivos y principalmente las quejas subjetivas de memoria son un motivo de consulta frecuente en los servicio de neurología, psiquiatría y geriatría. Es en este contexto, que han aumentado considerablemente las investigaciones para evaluar la forma en que las Funciones Cognitivas superiores envejecen.
La neuropsicología del envejecimiento tiene por objetivo, entre otros, conocer y definir los procesos cognitivos, estableciendo perfiles o patrones en las diferentes patologías que se observan y se desarrollan en este ciclo vital 6.
En este artículo se abordarán las demencias más observadas y se presentarán las principales investigaciones y pruebas destinadas a valorar el perfil cognitivo de estas.
LAS DEMENCIASLas demencias son patologías que se producen por lesiones cerebrales degenerativas o secundarias a eventos como accidentes cerebrovasculares o traumatismos, las cuales provocan un deterioro cognitivo progresivo, afectando la realización adecuada de actividades diarias y a su vez, alterando la conducta y la autonomía de las personas.
Las demencias no sólo afectan a los que las padecen, sino que también afectan a sus cuidadores y su entorno. Una serie de estudios ha identificado el impacto en los ámbitos sociales, económicos y por sobre todo en la salud mental y física de los cuidadores a cargo de un paciente con demencia 7–9.
En Chile, el estudio “CUIDEME” que investigó a 291 cuidadores de pacientes con demencia, evidenció que el 47% padece algún tipo de patología de salud mental causado por la sobrecarga diaria debido al estrés y el desgaste emocional. Además, observó que el 56% no recibe ayuda en los cuidados, debiendo reducir su jornada laboral lo que lleva a una disminución del ingreso, provocando un impacto económico al grupo familiar 10.
Según las estimaciones, el 56% de las demencias corresponden al tipo Alzheimer, el 14% a demencias vasculares, el 10% a demencias por Cuerpos de Lewy y a demencia Parkinson, el 8% demencias FrontoTemporales y el 12% restante a demencias por otras casusas 11. Hay algunos estudios que sugieren controversia sobre estos porcentajes de subtipos de demencia, siendo las demencias mixtas la que se observarían con mayor frecuencia 12.
Establecer el diagnóstico de una Demencia es una tarea compleja ya que requiere contar con la historia clínica detallada del paciente, conocer el orden de aparición de trastornos cognitivos y/o conductuales y como estos se manifiestan en las actividades diarias. En conjunto con exámenes de laboratorio, de imagenología y biomarcadores, la Evaluación Neuropsicología (EN) toma especial relevancia para determinar el diagnóstico de la demencia y su posterior seguimiento.
LA NEUROPSICOLOGÍA Y LAS DEMENCIASDonald Hebb utilizó por primera vez el término “neuropsicología” en 1949. Hécaen la definió en 1972 como una disciplina que trata las funciones mentales superiores en relación con las estructuras cerebrales 13. Esta disciplina intenta identificar las funciones cognitivas deterioradas, con la ayuda de pruebas estandarizadas, en pacientes con algún tipo de lesión cerebral.
El objetivo principal de la EN es establecer un diagnóstico de las funciones mentales superiores que han sido afectadas por lesiones cerebrales y las que se mantienen preservadas. El aporte de la EN en el diagnóstico y seguimiento de pacientes en la demencia Alzheimer y otros tipos está respaldado por el Subcomité de Evaluación de Tecnología y Terapéutica de la Academia de Neurología 14. Para la realización de la EN, es necesario conocer el origen de la demanda, su contexto, el tipo de cambios cognitivos y conductuales presentados y el grado de conciencia de los trastornos que afectan a los pacientes. Con frecuencia los adultos mayores presentan alteraciones sensoriales (auditivas y visuales principalmente) y variados niveles educacionales, factores que deben ser identificados para seleccionar las pruebas a administrar y el baremo de corrección a utilizar.
Para confirmar los cambios cognitivos y conductuales que presentan los pacientes, existen diferentes cuestionarios dirigidos a los cuidadores y cercanos. Los más utilizados son el Alzheimer Disease 8 (AD8) 15 o el Informant Questionnaire on Cognitive Decline in the Elderly (IQCODE) 16 entre otros.
Una vez identificadas las principales áreas deficientes se realiza una selección de las pruebas que permitirán poner en evidencia el perfil cognitivo del paciente. Posteriormente con los resultados de la EN el neuropsicólogo clínico, profesional con formación especializada en pruebas cognitivas y su interpretación, elabora un informe clínico detallando el perfil cognitivo y formulando una propuesta de intervención y seguimiento. Debido a la tecnicidad del informe de EN, se realiza una sesión con el pacientes, sus familiares, cercanos y/o cuidadores para presentar de manera individualizada los alcances de la evaluación y las etapas de seguimiento.
ESTUDIOS COGNITIVOS DE LAS DEMENCIASBlessed, Tomlinson y Roth en 1968, fueron unos de los primeros en intentar medir los cambios patológicos y sus consecuencia en la cognición de pacientes con demencia Alzheimer (DA) utilizando diferentes pruebas disponibles en esa época y subpruebas del Wechsler Adult Intelligence Scale (WAIS) 17.
Algunos años más tarde en 1975, Marshal y Susan Folstein y Paul McHugh presentan un test rápido y breve para detectar el deterioro cognitivo en pacientes psiquiátricos hospitalizados, el MiniMental State Examintation (MMSE) 18. Después de más de 40 años de su publicación es el test “screening” más traducido y uno de los test cognitivos más validado y citado en el mundo 19. Si bien, es muy discutido por su sensibilidad en el diagnóstico de demencias 20 continúa siendo una herramienta utilizada por diferentes profesionales de salud tanto a nivel clínico como de investigación. En la década de los 70, 80 y 90 se crearon una serie de pruebas que tenían por objetivo determinar el grado de deterioro cognitivo y trastornos en la conducta principalmente en la demencia Alzheimer, debido a su alta frecuencia de aparición. Por ejemplo, para evaluar los cambios cognitivos en 1976 Steven Mattis presenta la Dementia Rating Scale, en 1977 aparece el Cognitive Capacity Screening Examination21, ocho años más tarde, Rosen y colaboradores presentaron la Alzheimer Disease Assesseemnt Scale (ADAS) 22 y en 1995 Huppert y colaboradores crearon el Cambridge Cognitive Examination (CAMCOG) 23. Para evaluar los cambios conductuales fueron desarrollados en 1987 por Reisberg y colaboradores la Behavioral Pathology in Alzheimer Disease Rating Scale BEHAVE-ED 24 y Cumming y colaboradores en 1994 el Neuropsychiatric Inventory (NPI) 25 entre otros. Poco a poco se fueron desarrollando pruebas específicas para evaluar cada función cognitiva en esta y otros subtipos de demencias que serán presentadas a continuación.
Deterioro cognitivo leveEl término de Deterioro Cognitivo Leve (DCL) fue propuesto por Reisberg y colaboradores en 1988 en una investigación realizada en sujetos quienes presentaban diferentes niveles de deterioro sin poder categorizarlos 26.
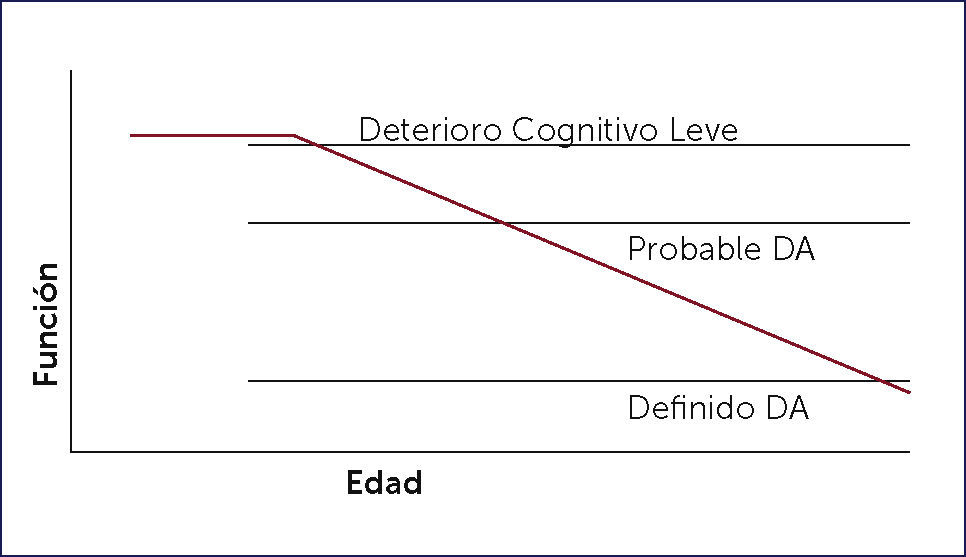
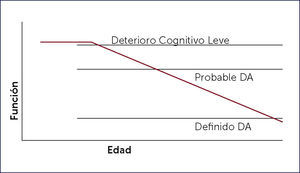
Ronald Petersen en 1999 describió un cuadro clínico caracterizado por queja subjetiva de memoria pero sin pérdida de autonomía, este cuadro clínico se conoce como Deterioro Cognitivo Leve (DCL) o Mild Cognitive Impairement (MCI) 27. Este cuadro es considerado por los especialistas como el pródromo de una demencia Alzheimer (Figura 1). Se han publicado varias propuestas para establecer los criterios clínicos del DCL. La primera de ellas en 1999 por Petersen y colaboradores 27, la segunda en 2006 realizada por el grupo internacional de trabajo del DCL 28, la tercera en 2011 formulada por el Instituto Nacional de Alzheimer de Estados Unidos 29 y la más reciente por la quinta edición del Diagnostic and Statistical Manual of Mental Disorders (DSM 5) 30, donde es incluido el DCL por primera vez en sus versiones.
De acuerdo a Petersen 31 el DCL se clasifica en tres tipos:
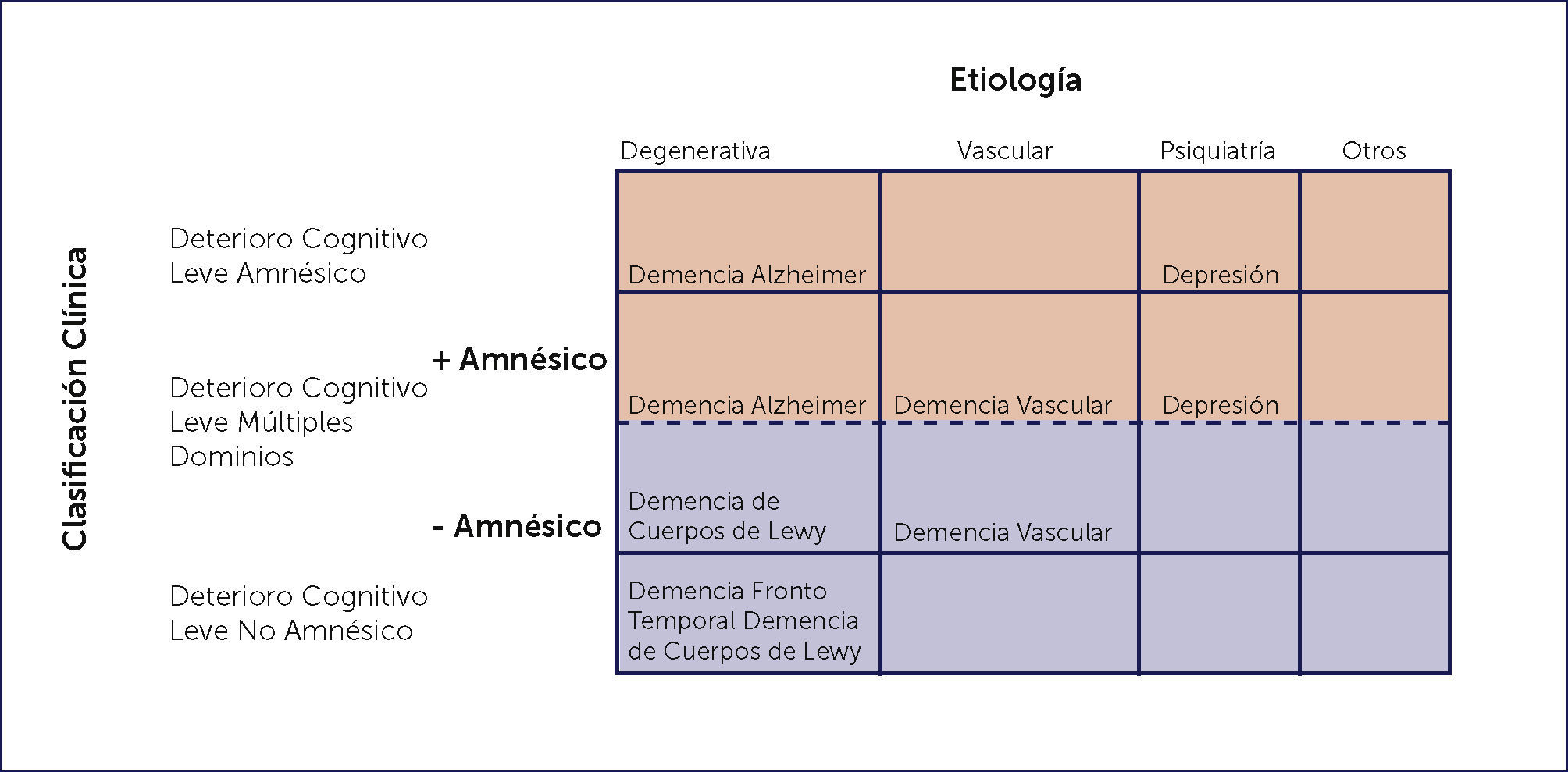
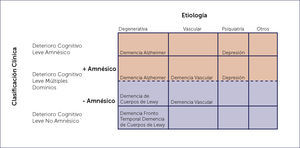
El primero, el DCL de tipo amnésico, donde existe una queja objetivada de la memoria, sin afectar la autonomía y donde se preservan las otras funciones cognitivas. El segundo, el DCL de tipo no amnésico y multidominio, que se caracteriza por disminución objetiva de dos o más funciones cognitivas, preservando el funcionamiento en las actividades diarias. El tercer tipo es el DCL de tipo no amnésico y de un único dominio, donde se objetiva una disminución cognitiva como el lenguaje, alguna función ejecutiva o la función visuoespacial. En la figura 2 se presentan los distintos DCL y sus probables etiologías.
LA DEMENCIA ALZHEIMERLa demencia Alzheimer (DA) se caracteriza en los análisis neuropatológicos por la aparición de depósitos anormales de placas de amiloide y de ovillos neurofibrilares afectando progresivamente las neuronas de las regiones temporales y extendiéndose posteriormente a otras áreas del cerebro que comienzan un proceso de neurodegeneración. Las regiones temporales medias y específicamente el complejo hipocampal participan en el proceso de memoria. Así, el principal síntoma que indican los pacientes y cercanos con esta patología es la pérdida de memoria, mientras que al extenderse la patología a otras áreas de la corteza cerebral aparecen síntomas relacionados con la orientación temporal espacial, la apraxia y la agnosia.
Los criterios diagnósticos establecidos por el grupo de trabajo del National Institute of Neurological and Communicative Disorders and Stroke (NINCDS) y la Alzheimer's Disease and Related Disorders Association (ADRDA) 32 y del DSM 5 30 ponen énfasis en objetivar el Deterioro Cognitivo. Para identificarlo, los profesionales de la salud utilizan regularmente pruebas de screening. El test Mini Mental State Examination (MMSE) 18 y el test Addenbrooke's Cognitive Examination (ACE) 33 son lo más utilizados debido a sus respectivos altos niveles de sensibilidad y especificidad. Una vez constado el deterioro cognitivo con estas pruebas, se realiza una evaluación neuropsicológica completa para detallar el patrón o perfil del deterioro.
- Trastornos cognitivosCaracterísticamente en la DA se observan dificultades sistemáticas para recordar hechos recientes, conversaciones y aprender nuevas informaciones. Esta memoria se conoce como Episódica (sistema que recibe y almacena las informaciones que conciernen los episodios y los eventos temporales y su relación de tipo espacio temporal). Para evaluarla se utilizan diferentes pruebas de aprendizaje, tanto visuales como verbales. Las más utilizadas en esta última modalidad, son por ejemplo, el Free and Cued Selective Reminding Test (FCSRT) 34 y el Test de aprendizaje Verbal de California 35. En estas pruebas los pacientes con DA presentan importantes dificultades, por una parte en el almacenamiento y recuperación de la información, pero además, se observa la presencia sistemática de intrusiones semánticas (producción no intencional, en una tarea de memoria de una palabra del mismo campo semántico) y de falsos recuerdos (que se traducen en un sesgo de respuesta afirmativa en un test de reconocimiento de palabras) 36.
En relación con los trastornos de memoria, se observa anosognosia (ausencia de consciencia de un déficit luego de una lesión cerebral). Las investigaciones indican que los pacientes con DA presentan alteraciones de la metamemoria (la capacidad para reflexionar sobre el propio rendimiento de la memoria) especialmente cuando necesitan acceder a los detalles asociados al episodio del aprendizaje 37.
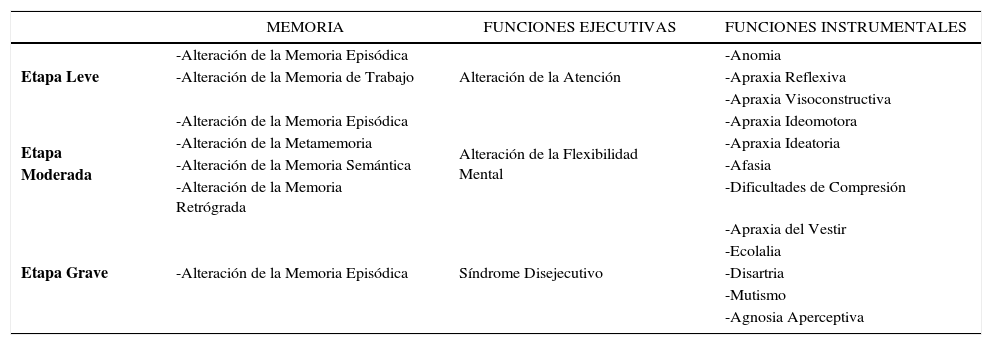
ALTERACIONES COGNITIVAS EN LAS DISTINTAS ETAPAS DE LA DEMENCIA ALZHEIMER
| MEMORIA | FUNCIONES EJECUTIVAS | FUNCIONES INSTRUMENTALES | |
|---|---|---|---|
| Etapa Leve | -Alteración de la Memoria Episódica | Alteración de la Atención | -Anomia |
| -Alteración de la Memoria de Trabajo | -Apraxia Reflexiva | ||
| -Apraxia Visoconstructiva | |||
| Etapa Moderada | -Alteración de la Memoria Episódica | Alteración de la Flexibilidad Mental | -Apraxia Ideomotora |
| -Alteración de la Metamemoria | -Apraxia Ideatoria | ||
| -Alteración de la Memoria Semántica | -Afasia | ||
| -Alteración de la Memoria Retrógrada | -Dificultades de Compresión | ||
| Etapa Grave | -Alteración de la Memoria Episódica | Síndrome Disejecutivo | -Apraxia del Vestir |
| -Ecolalia | |||
| -Disartria | |||
| -Mutismo | |||
| -Agnosia Aperceptiva |
También se observan alteraciones en la Memoria de Trabajo (MDT), (sistema con la capacidad de simultáneamente almacenar, procesar y monitorear información. Existen diversos estudios que concluyen la presencia de alteraciones en este tipo de memoria en la DA. Es más, se ha avanzado incluso en la hipótesis cognitiva de que la DA sería a la base una alteración de MDT 38. Los pacientes presentan dificultades para seguir una conversación, leer, seguir la historia de una película o de un programa de televisión.
La Memoria Semántica es la memoria de las palabras y de los conceptos, esta almacena la información independientemente del contexto del aprendizaje. Los pacientes con DA presentan dificultades en la denominación y definición de objetos, de apareamiento imagen-palabra y para responder a preguntas de información general.
A nivel de la atención en pacientes con DA, se observa una alteración sistemática de los procesos atencionales 39.
A nivel instrumental, el lenguaje de los pacientes con DA es caracterizado por la presencia de Anomia, por la sustitución del nombre de un objeto por otro del mismo campo semántico o también se observa la formulación de la utilización de los objetos en lugar de formular el nombre adecuado. En función del avance de la enfermedad, aparecen alteraciones del lenguaje comprensivo complejo. En etapas avanzadas y graves de la enfermedad se pueden observar ecolalias y mutismo.
Por otra parte, es común observar una alteración para realizar gestos en la DA. Aparece tempranamente una apraxia reflexiva y una apraxia visoconstructiva y en función del avance de esta enfermedad este deterioro se acentúa. En etapas avanzadas de la enfermedad se observa apraxia ideomotora y apraxia del vestir.
Finalmente, es posible observar en estos pacientes un trastorno en el reconocimiento de objetos e imágenes. Se observa una agnosia de tipo asociativa, probablemente causada por una alteración en las representaciones semánticas.
- Trastornos neuropsiquiátricosLos trastornos del ánimo como apatía, ansiedad y depresión son frecuentes en la DA 40 y aparecen desde la primera etapa de la enfermedad junto con trastornos neuropsiquiátricos como delirios, agitación y estados confusionales. Los trastornos del sueño y las alucinaciones aparecen en etapas más avanzadas.
LAS DEMENCIAS VASCULARESEn un estudio de pacientes con demencia Tomlinson en 1970 introdujo el término Demencia Aterosclerótica para diferenciar a los pacientes con infartos cerebrales de los pacientes con enfermedad neurodegenerativa 41. Cuatro años más tarde Hachinski planteó el término Demencia Multiinfarto para describir pacientes con deterioro de sus funciones cognitivas y con antecedentes de enfermedades cerebro-vasculares. En 1993, el mismo Hachinski junto a Bower proponen el término de Deterioro Cognitivo Vascular. Las Demencias Vasculares (DV) son cuadros clínicos con un origen hemorrágico, isquémico o isquémico-hipoxico, donde el comienzo suele ser abrupto con un deterioro progresivo, con quejas somáticas y una cierta incontinencia emocional. La existencia de hipertensión y/o accidentes cerebrovasculares, entre otros, son antecedentes mórbidos relevantes en el diagnóstico diferencial.
Los criterios diagnósticos más utilizados son los de la Organización Mundial de la Salud (International Classification of Diseases, ICD-10) 42, los del DSM 5 30, los del National Institute of Neurological Disorders and Stroke-Association Internationale pour la Reserche et lNNEnseignement en Neuroscience (NINDS/AIREN) 43 y los criterios propuestos por el grupo de trabajo del State of California Alzheimer's Disease Diagnostic and Treatment Centres (ADDTC) 44.
Es posible clasificar en 6 las DV en función del tipo de lesión basándose en las clasificaciones de la NINDS/AIREN (Ver Tabla 2).
CLASIFICACIÓN NINDS/AIREN DE LA DEMENCIA VASCULAR
| 1 | Demencia multiinfarto |
| 2 | Demencia por infarto único en un área estratégica |
| Gyrus Angular | |
| Arteria cerebral posterior | |
| Arteria cerebral anterior | |
| Arteria cerebral media derecha | |
| Oclusión carotídea bilateral | |
| Lóbulo parietal | |
| Lesiones frontobasales | |
| Infarto talámico | |
| 3 | Demencia por enfermedad de pequeño vaso |
| Infartos lacunares múltiples (ganglios basales, protuberancia, sustancia blanca frontal) | |
| Enfermedad de Binswanger | |
| Angiopatía amiloide cerebral | |
| 4 | Demencia por hipoperfusión |
| 5 | Demencia hemorrágica |
| 6 | Demencia por otros mecanismos vasculares |
La elección de pruebas para la realización de la evaluación neuropsicológica en el contexto de una probable DV es bastante compleja debido a la heterogeneidad de lesiones. En 1999 Rockwood y colaboradores observaron que más del 70% de las lesiones son del pequeño vaso con cambios de la sustancia blanca de origen subcortical 45. Además, Tullbert observó que los pacientes con DV tienen un hipometabolismo del lóbulo frontal 46.
La escala isquémica de Hachinski 47 es de gran utilidad para identificar la presencia de un cuadro DV y DA ya que puntajes menores a 4 puntos en esta escala son sugerentes de trastornos neurodegenerativos (Ver Tabla 3).
ESCALA DE ISQUEMIA DE HACHINSKI
| Inicio brusco | 2 |
| Deterioro escalonado | 1 |
| Curso fluctuante | 2 |
| Confusión nocturna | 1 |
| Conservación relativa de la personalidad | 1 |
| Depresión | 1 |
| Síntomas somáticos | 1 |
| Labilidad emocional | 1 |
| Antecedentes de hipertensión | 1 |
| Antecendentes de enfermedad cerebrovascular | 2 |
| Evidencia de arteriosclerosis asociada | 1 |
| Síntomas neurológicos focales | 2 |
| Signos neurológicos focales | 2 |
| Una puntuación de 7 o más puntos indica mayor probabilidad de demencia vascular y de 4 o menos de demencia de Alzheimer. | |
La revisión de la literatura indica que cuando se comparan los resultados de la EN de pacientes con DA y DV, estos últimos tienen más alteraciones de las Funciones Ejecutivas. Por su parte, los pacientes con DA tienen alteraciones de Memoria Episódica considerablemente afectadas en comparación con los pacientes con DV.
Respecto a las Funciones Ejecutivas alteradas en la DV, los estudios confirman alteraciones de la Atención, de la Fluencia Verbal, de la Flexibilidad Mental y de la Velocidad tratamiento de la información. Un grupo de investigadores sugiere la utilización de pruebas que evalúen las Funciones Ejecutivas para el diagnóstico diferencial 48.
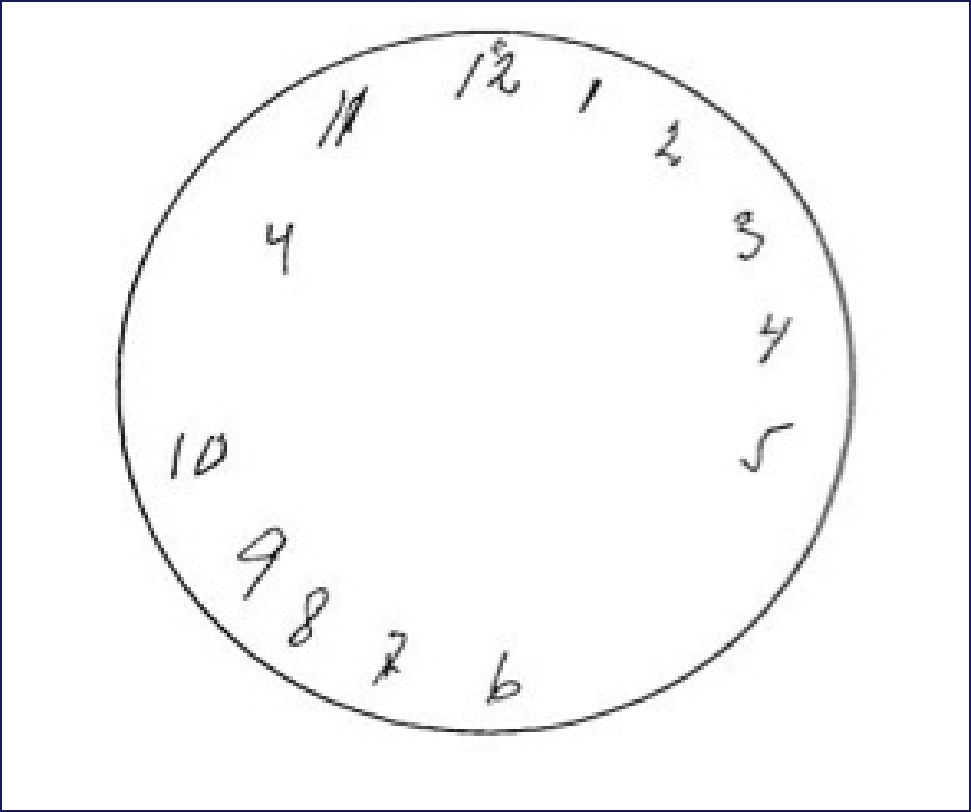
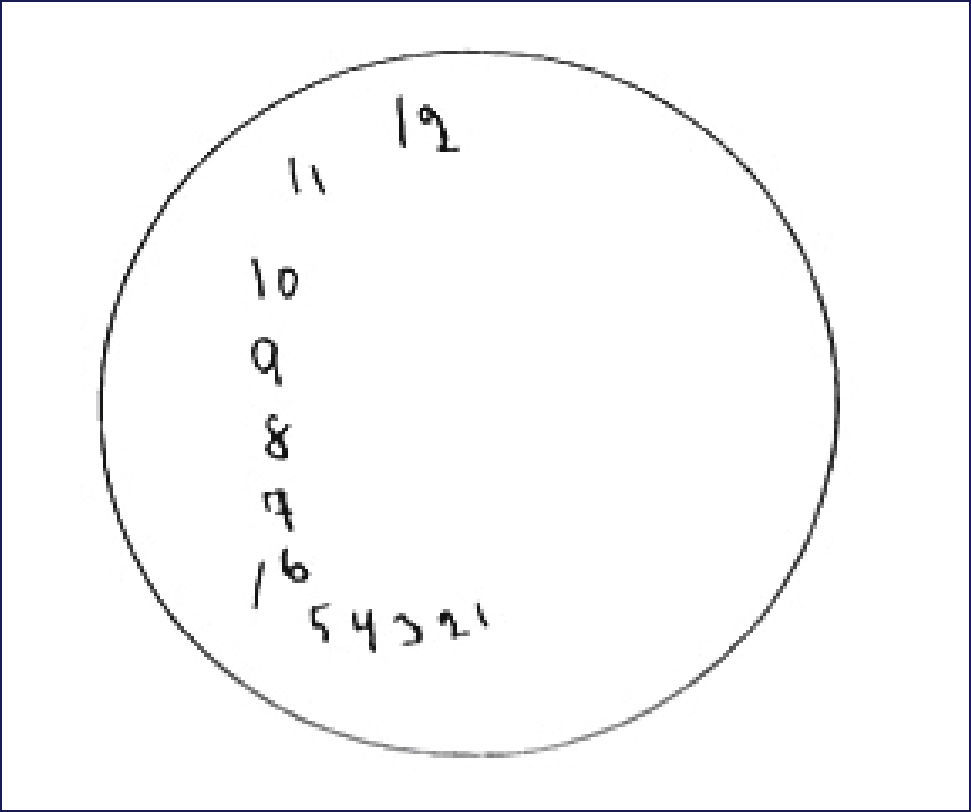
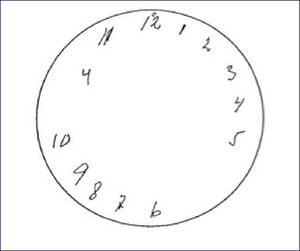
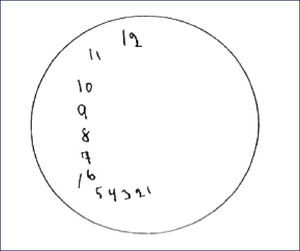
-Trastornos neuropsiquiátricosSe asocian comúnmente al deterioro cognitivo de origen vascular síntomas como depresión, apatía, irritabilidad, agresividad, ansiedad, agitación y episodios psicóticos (Figuras 3 y 4) 49,58.
RESULTADO DEL DIBUJO DE LA PRUEBA DEL RELOJ
Resultado prueba del reloj con círculo de 10cm de diámetro pre-dibujado que fue realizada por una mujer de 76 años de edad con enfermedad de Alzheimer con un puntaje de 17 en el Mini Mental State Examination (MMSE).
(Tomado y traducido de Agrel et Dehljn, 1998).
En la demencia por Cuerpos de Lewy (DLB por sus siglas en inglés, Dementia with Lewy Bodies) se acumulan estructuras proteicas anormales denominadas neuritas de Lewy, descritas por primera vez por Frederich Heinrich Lewy en 1912 en las regiones límbicas, tronco cerebral, corteza cerebral, entre otras. Esta demencia se caracteriza por la presencia progresiva de alucinaciones, síntomas parkinsonianos y alteraciones cognitivas. Debido a la similitud de síntomas con la DA y con la demencia asociada a la enfermedad de Parkinson (DP), el diagnóstico diferencial es bastante complejo. El perfil temporal de la aparición de los síntomas puede ser de ayuda en esta diferenciación, ya que en la DLB la demencia aparece cerca del año desde la aparición de síntomas motores, mientras que en la DP los síntomas de demencia aparecen tardíamente.
-Trastornos cognitivosDiversos estudios ponen en evidencia importantes alteraciones atencionales de paciente con DLB en comparación con otros pacientes con DA. Los resultado a los estudios han sugerido que probablemente el sistema colinérgico tendría incidencia en las tareas atencionales 51 y 52.
Las funciones ejecutivas y las capacidades visuoespaciales, son tempranamente afectadas en la DLB 53.
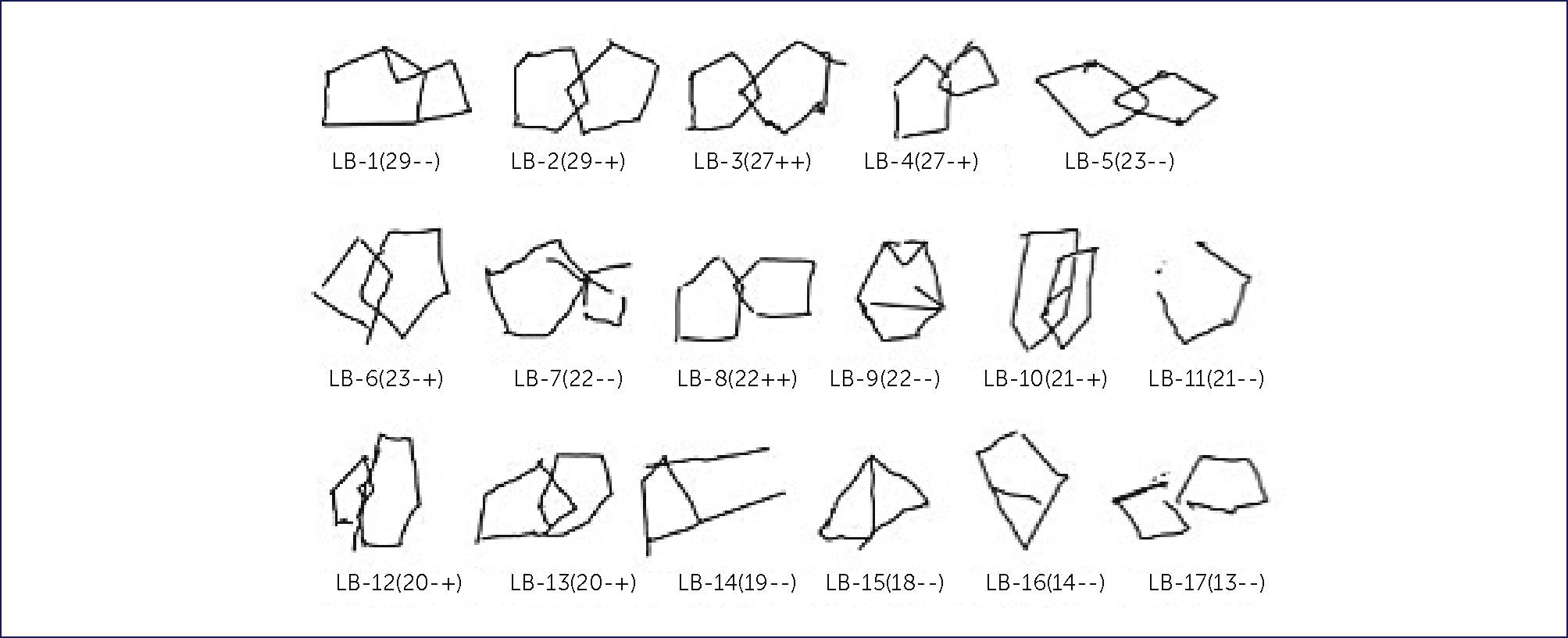
A nivel del funcionamiento de la memoria, diversos estudios indican alteraciones en fases ya tardías de la memoria. Sin embargo, en pruebas de memoria episódica verbal de aprendizaje de palabras, donde se solicita el recuerdo de palabras aprendidas anteriormente, los pacientes con DLB presentan intrusiones semánticas, pero asociadas al entorno visual, diferente al tipo de errores que comenten los pacientes con EA 54Figuras 5 y 6.
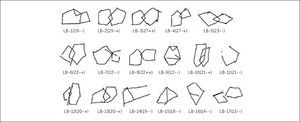
COPIA DE PENTÁGONOS ENTRELAZADOS DEL MMSE REALIZADA POR LOS PACIENTES CON DIAGNÓSTICO DE DEMENCIA POR CUERPOS DE LEWY
El código de debajo de cada figura indica el número del paciente seguido entre paréntesis por el puntaje obtenido al MMSE y con signos positivo y negativo si cumple con los dos criterios originales de calificación (primer y segundo grado).
(Tomado y traducido de Ala y cols, 2001.).
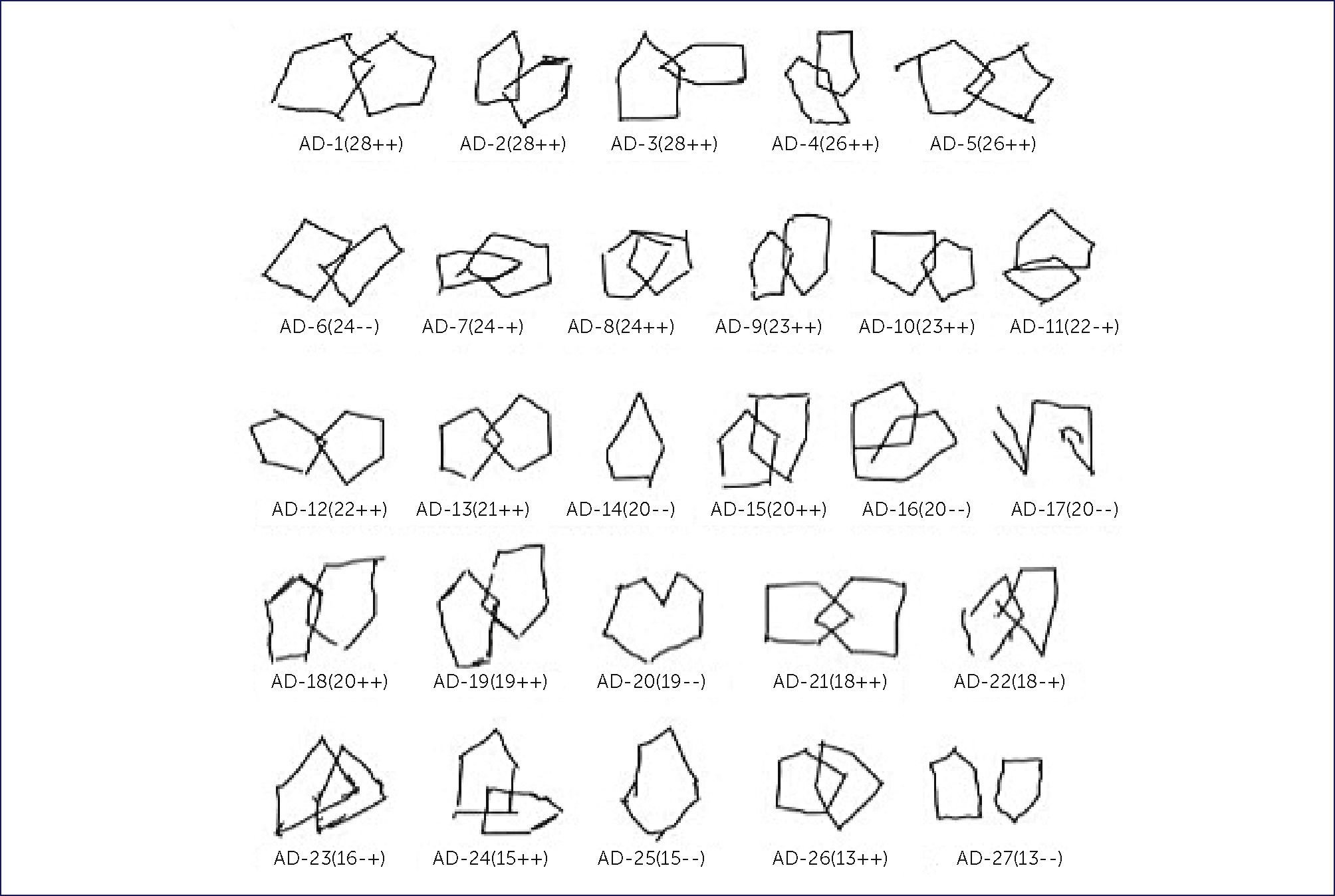
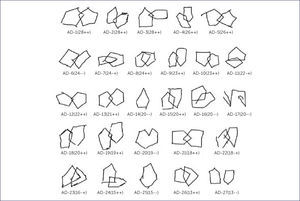
COPIA DE PENTÁGONOS ENTRELAZADOS DEL MMSE REALIZADA POR LOS PACIENTES CON DIAGNÓSTICO DE DEMENCIA ALZHEIMER
El código de abajo de cada figura indica el número del paciente seguido entre paréntesis por el puntaje obtenido al MMSE y con signos positivo y negativo si cumple con los dos criterios originales de calificación (primer grado y segundo grado).
(Tomado y traducido de Ala et al., 2001.).
Las alucinaciones son altamente frecuentes en la DLB 55. Estas se caracterizan por ser detalladas y consideradas un síntoma mayor en este tipo de demencia. También, se ha planteado la hipótesis que las alteraciones perceptivas de estos pacientes predispondrían a los pacientes a tener alucinaciones visuales y trastornos del sueño REM.
LA DEMENCIA ASOCIADA A LA ENFERMEDAD DE PARKINSONEn 1817 James Parkinson describió casos de pacientes que presentaban una marcha inestable, temblor y lentitud de movimientos lo que él llamó “parálisis agitante” 56. En 1872 Jean Martin Charcot, propone el nombre de enfermedad de Parkinson (EP), en honor al médico inglés que la describió por primera vez 57. La EP es una patología de tipo neurodegenerativa que afecta la sustancia negra, parte de los ganglios basales, donde se produce el neurotransmisor dopamina que participa en el control de los movimientos voluntarios del cuerpo.
Si bien, los síntomas motores como bradicinesia, hipertonía y temblor en reposo son característicos de esta enfermedad, es sólo a partir de los años 70 comenzaron a ser estudiados además los síntomas cognitivos y neuropsiquiátricos. La EN permite objetivar la presencia de trastornos cognitivos y conductuales y evaluar si estos interfieren en la autonomía del paciente para así establecer si se trata de una demencia asociada a la enfermedad de Parkinson (DP).
El diagnóstico diferencial con la demencia por Cuerpos de Lewy es una de las principales complejidades de la EN debido a la similitud de síntomas y de lesiones neurológicas.
- El deterioro cognitivo leve en la enfermedad de ParkinsonHasta hace algunos años se estimaba que ciertos pacientes con EP desarrollaban demencia en etapas avanzadas de la enfermedad, pero se desconocía cómo este proceso se instalaba. El DCL se estableció como una entidad premórbida especialmente en los trastornos de tipo amnésico con una evolución hacia una DA. Sin embargo, también existen criterios de DCL no amnésico que corresponderían al perfil de deterioro que se observa en la EP. Una serie de investigaciones ponen en evidencia un perfil de DCL en la EP 58,59. Estos estudios muestran sistemáticamente que el DCL no amnésico de un dominio corresponde en general a alteraciones de las funciones ejecutivas. Cuando el DCL es no amnésico y multidominio, este disfuncionamiento ejecutivo es seguido por trastornos de la Atención, disminución en la velocidad de procesamiento de la información y un deterioro en las capacidades visoconstructivas 60,61.
Las investigaciones indican que un 26% de pacientes con diagnóstico de EP presentan un DCL asociado 62. El interés de objetivar con una EN el grado de deterioro y la presencia o no de DCL es predictor de una probable demencia. Los criterios clínicos para determinar DCL en la EP y DP fueron establecidos por la Movement Disorder Society (MDS) 63.
- Trastornos cognitivosEn 2007, un grupo de investigadores de la MDS estableció un consenso de pruebas cognitivas para valorar el deterioro cognitivo en la EP. Destacan pruebas relacionas con las funciones ejecutivas, específicamente de flexibilidad mental, de planificación, de conceptualización y de capacidades de abstracción. También se sugiere evaluar la Atención y las capacidades visoconstructivas 64,65.
- Trastornos neuropsiquiátricosExiste evidencia de que los trastornos depresivos son frecuentes en la EP. Sin embargo, ha existido un avance considerable en los estudios que ponen en evidencia trastornos como ansiedad, apatía, psicosis, descontrol de impulsos y trastornos del sueño 66.
LAS DEMENCIAS FRONTOTEMPORALESLas demencias frontotemporales (DFT) son un término propuesto por Neary 67 y colaboradores para reagrupar las atrofias progresivas que afectan los lóbulos frontales y temporales. Se desconoce la causa exacta de esta atrofia, aunque varios estudios indican que al menos un gran porcentaje correspondería a factores genéticos que podrían estar involucrados en su desarrollo. Estas pueden ser clasificadas en tres variantes. La primera con predominancia conductual (DFTc), donde existe una atrofia de regiones frontales y temporales que se relacionan con trastornos en la conducta. La segunda, denominada Afasia Progresiva Primaria no fluente (APPNF), que se caracteriza por lesiones fronto-temporales izquierdas, donde se presentan trastornos del lenguaje como en denominación de palabras y dificultades en el orden gramatical. La tercera variante es la demencia semántica (DS), donde se observa generalmente una atrofia con predominio en el lóbulo temporal. Estas lesiones se caracterizan por causar alteraciones de la memoria semántica (responsable de almacenar nuestros conocimientos generales) que se traduce en dificultades para encontrar las palabras y a su vez en la comprensión del lenguaje.
- Trastornos conductualesA diferencia de otras demencias, en la DFTc los trastornos conductuales y cambios de personalidad que perciben los cercanos de los pacientes, son las primeras manifestaciones de estas patologías (apatía, desinhibición, depresión, euforia, disforia, etc.) 68. Existen varias escalas conductuales que permiten identificar cambios con la ayuda de algún familiar o cercano. Sin embargo, el límite de estas escalas, como lo señalan Boutoleau-Bretonniere y colaboradores, es que solo permiten objetivar las alteraciones conductuales, pero no permiten conocer la evolución de estos trastornos 69.
- Trastornos cognitivosA nivel neuropsicológico los pacientes con una DFT presentan alteraciones de predominio disejecutivo, como alteraciones en la planificación, en la flexibilidad mental, en la inhibición de la información y en las capacidades de abstracción.
Además, se observan alteraciones en el lenguaje, como anomia y parafasias semánticas que en muchos casos no son evidentes en un comienzo de la aparición de los trastornos. Las alteraciones del lenguaje son la principal característica de las variantes APPNF y de la DS. Ver resumen de las principales en la Tabla 4.
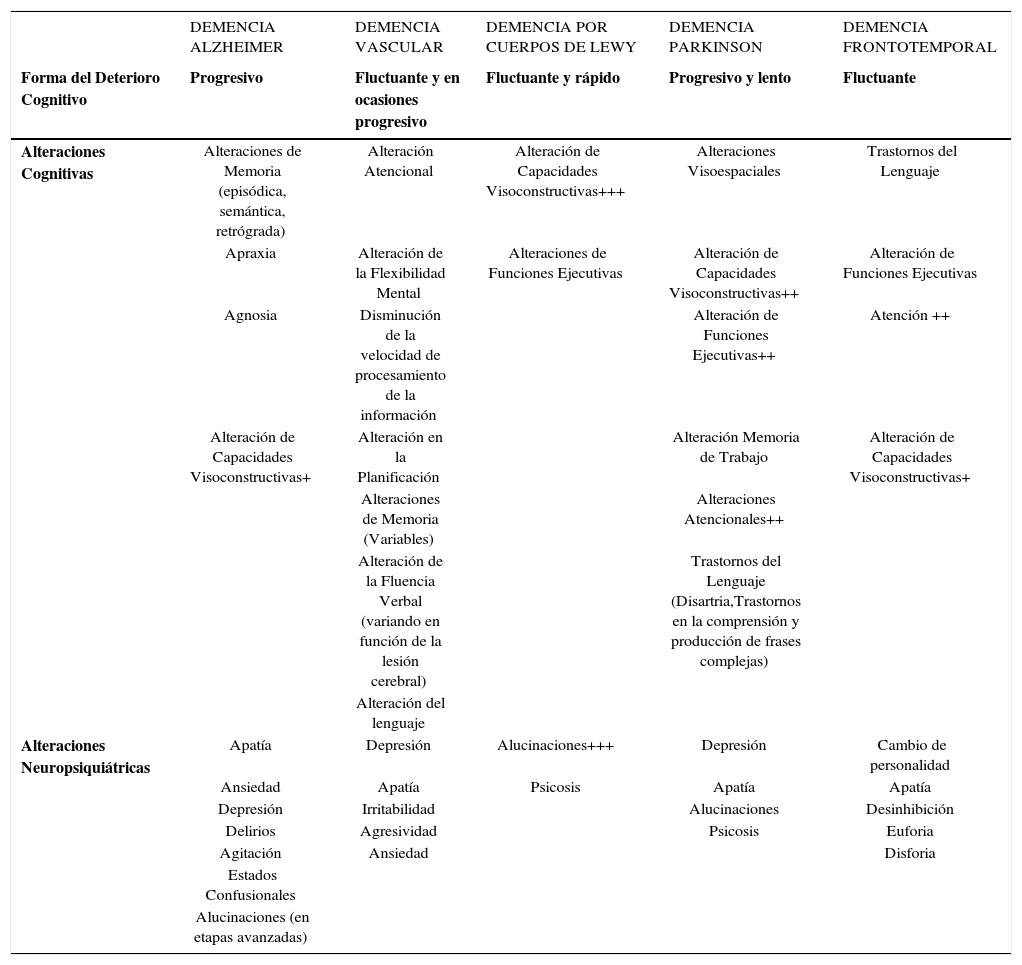
PRINCIPALES ALTERACIONES COGNITIVAS Y NEUROPSIQUIÁTRICAS DE LAS DEMENCIAS
| DEMENCIA ALZHEIMER | DEMENCIA VASCULAR | DEMENCIA POR CUERPOS DE LEWY | DEMENCIA PARKINSON | DEMENCIA FRONTOTEMPORAL | |
|---|---|---|---|---|---|
| Forma del Deterioro Cognitivo | Progresivo | Fluctuante y en ocasiones progresivo | Fluctuante y rápido | Progresivo y lento | Fluctuante |
| Alteraciones Cognitivas | Alteraciones de Memoria (episódica, semántica, retrógrada) | Alteración Atencional | Alteración de Capacidades Visoconstructivas+++ | Alteraciones Visoespaciales | Trastornos del Lenguaje |
| Apraxia | Alteración de la Flexibilidad Mental | Alteraciones de Funciones Ejecutivas | Alteración de Capacidades Visoconstructivas++ | Alteración de Funciones Ejecutivas | |
| Agnosia | Disminución de la velocidad de procesamiento de la información | Alteración de Funciones Ejecutivas++ | Atención ++ | ||
| Alteración de Capacidades Visoconstructivas+ | Alteración en la Planificación | Alteración Memoria de Trabajo | Alteración de Capacidades Visoconstructivas+ | ||
| Alteraciones de Memoria (Variables) | Alteraciones Atencionales++ | ||||
| Alteración de la Fluencia Verbal (variando en función de la lesión cerebral) | Trastornos del Lenguaje (Disartria,Trastornos en la comprensión y producción de frases complejas) | ||||
| Alteración del lenguaje | |||||
| Alteraciones Neuropsiquiátricas | Apatía | Depresión | Alucinaciones+++ | Depresión | Cambio de personalidad |
| Ansiedad | Apatía | Psicosis | Apatía | Apatía | |
| Depresión | Irritabilidad | Alucinaciones | Desinhibición | ||
| Delirios | Agresividad | Psicosis | Euforia | ||
| Agitación | Ansiedad | Disforia | |||
| Estados Confusionales | |||||
| Alucinaciones (en etapas avanzadas) |
Las cifras actuales y las proyecciones futuras indican un aumento sistemático de la prevalencia de demencias en el mundo. El avance de una demencia variará de un paciente a otro debido a la evolución de las lesiones cerebrales que afectarán la cognición y la conducta de los pacientes. El impacto de estos cambios en las actividades diarias dependerá en gran medida de las intervenciones a la cuales tendrá acceso el paciente. Disminuir este impacto es uno de los principales objetivos de las intervenciones que realizan los equipos de salud contando con un diagnóstico objetivado y un plan de seguimiento adecuado.
Históricamente las investigaciones neuropsicológicas de las demencias han contribuido a establecer cómo las lesiones neurológicas alteran el funcionamiento cognitivo y conductual por cada subtipo de demencia. Además, se han desarrollado una serie de pruebas, escalas y cuestionarios con los cuales la EN explora la función cognitiva y los cambios conductuales determinando la presencia de un perfil de deterioro, contribuyendo al diagnóstico y al seguimiento de estas enfermedades.
Es indispensable continuar investigando cómo las funciones mentales superiores varían en el envejecimiento normal y patológico, pero también queda pendiente desarrollar pruebas específicas considerando los factores socioculturales de cada país, constituyéndose como herramientas con alta sensibilidad y especificidad y así la EN contribuirá de mejor manera al diagnóstico y seguimiento de las demencias.
El autor declara no tener conflictos de interés, en relación a este artículo.