El tratamiento actual de la depresión mayor, una condición de alta prevalencia a nivel mundial, aún no resulta satisfactorio por las significativas tasas de falta de respuesta o de síntomas residuales. Esto, entre otras razones, ha motivado a la búsqueda de nuevos modelos de comprensión de los procesos biológicos que están a la base de esta enfermedad, con el propósito de encontrar mejores estrategias terapéuticas, al menos desde el punto de vista farmacológico. Se examinan algunas correspondencias entre los fenómenos clínicos y la articulación de los sistemas inmune, nervioso y endocrino, y se revisa algunas relaciones entre depresión y enfermedades inflamatorias sistémicas.
The current treatment of major depression, a condition of high prevalence worldwide, is still unsatisfactory due to the elevated rates of non-response or residual symptoms. This, among other reasons, has motivated the search for new models of understanding the biological processes that could better explain this disease, with the purpose of finding better therapeutic strategies, at least from the pharmacological point of view. Some correspondences between clinical phenomena and the interplay of the immune, nervous and endocrine systems are examined. Also, some relationships between depression and systemic inflammatory diseases are reviewed.
La depresión mayor (DM) es un trastorno de alta prevalencia en la población mundial, superando los 300 millones de personas que la sufren, de acuerdo a las estimaciones de la Organización Mundial de la Salud y con un incremento de más del 18% entre 2005 y 20151,2. Si tomamos en cuenta los estudios de Carga Global de Enfermedad (GDB), es posible apreciar que la depresión se ha mantenido como una de las tres principales causas de Años Vividos con Discapacidad a nivel mundial dentro de las últimas dos décadas3. Más allá de estas cifras, la práctica clínica nos revela a diario el drama de personas y familias devastadas por la enfermedad depresiva: biografías mutiladas, parejas y proyectos familiares destruidos y trabajos o estudios paralizados. Y todo ello sin considerar aún la dramática realidad del suicidio, de elevada prevalencia dentro de quienes presentan una enfermedad depresiva.
Aunque los avances de la psicofarmacología junto a otros métodos terapéuticos han traído esperanza a los pacientes y sus familias logrando importantes retrocesos de los cuadros depresivos y a veces exitosas mejorías, continúa siendo una realidad que un porcentaje importante de los enfermos no logra una recuperación satisfactoria. Muchas personas obtienen algún grado de “respuesta” con el uso de agentes antidepresivos, entendiendo por ello una mejoría de al menos un 50% de los síntomas iniciales al utilizar una medición estandarizada del tipo de la escala de Hamilton para depresión (HDSR)4. Sin embargo conseguir una “remisión”, es decir, un estado asintomático o con síntomas mínimos, sin limitaciones psicosociales y que alcancen una funcionalidad óptima, es bastante más complejo5. Lo cierto es que un porcentaje importante de las personas que sufren estados depresivos (alrededor de un tercio) no alcanza la remisión completa (“recuperación”), muchas recaen o recidivan y no pocos pacientes desarrollan estados crónicos, donde los síntomas residuales más característicos son los de naturaleza cognitiva además de la anhedonia (incapacidad para sentir placer) e inhibición social.
Es habitual considerar a la depresión como una condición multifactorial tanto en su génesis como en su evolución. Si bien las teorías y definiciones de carácter neurobiológico son las que han dominado la literatura sobre el tema, también han cobrado gran relevancia las hipótesis psicosociales, tomando en cuenta que la prevalencia de la enfermedad depresiva no es homogénea y que se expresa con mayor frecuencia en mujeres y en grupos deprivados social y económicamente6. Por lo mismo, además del empleo de nuevos fármacos y métodos terapéuticos biológicos, se ha hecho énfasis en la utilización de terapias psicológicas, técnicas psicoeducativas o el entrenamiento para la recuperación de capacidades cognitivas tanto en depresión como en bipolaridad (functional remediation)7,8. Parece indudable que la combinación de métodos biológicos con terapias como las descritas expanden los resultados del tratamiento, pero aún así continúan existiendo las limitaciones terapéuticas señaladas.
Estas insuficiencias en los resultados del tratamiento de la depresión son las que han llevado a clínicos e investigadores a una permanente búsqueda de nuevas ideas e hipótesis que permitan comprender mejor el fenómeno depresivo y que sean capaces de optimizar el escenario actual de resultados. Uno de los temas que ha ocupado de manera creciente la atención de los expertos es el de las relaciones entre depresión y procesos inflamatorios, que es el tema central de la presente revisión.
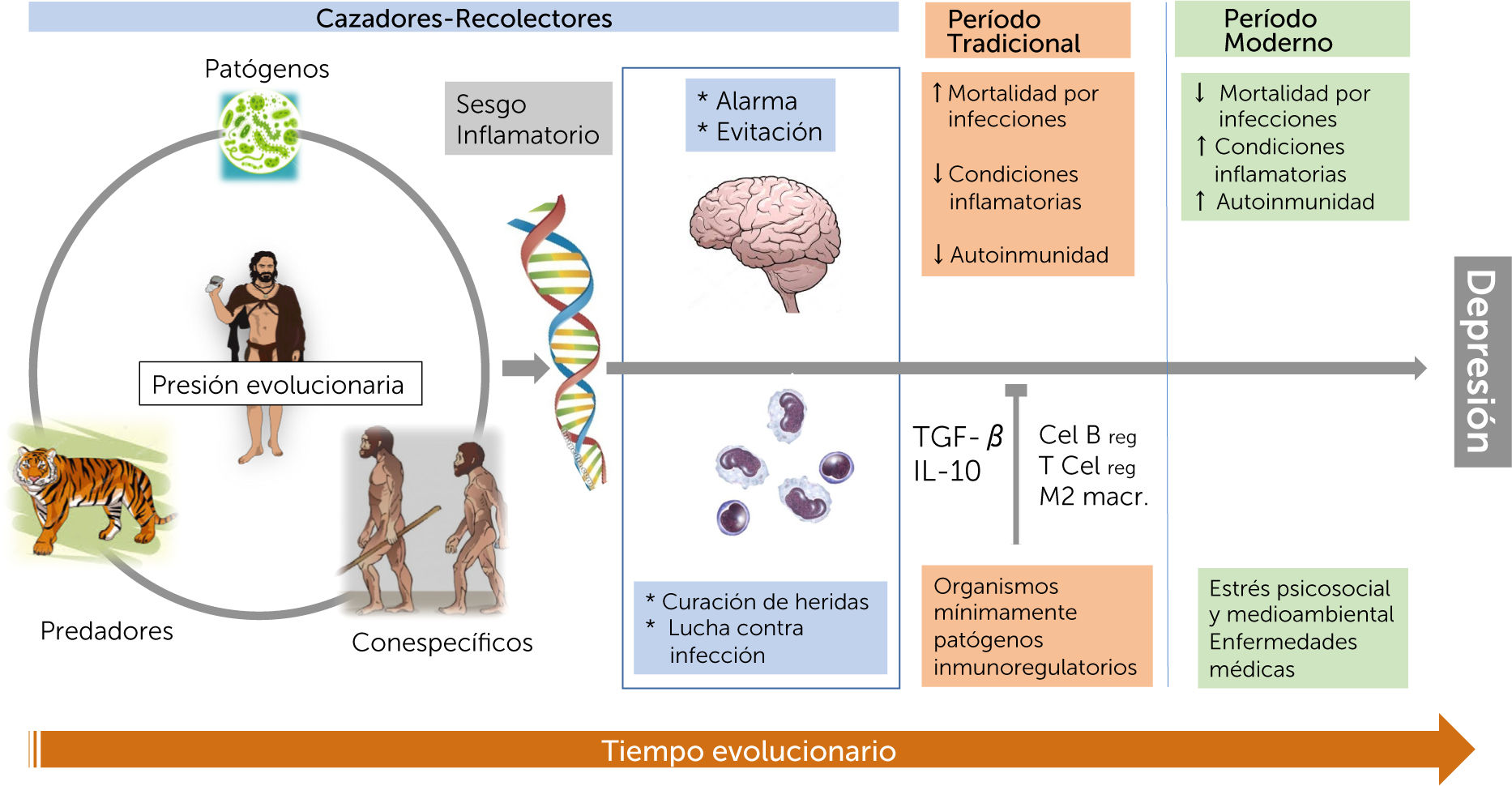
Una perspectiva evolucionariaAlgunas hipótesis señalan que las presiones evolucionarias tempranas derivadas de las interacciones humanas con predadores, agentes patógenos y rivales conespecíficos, fueron generando un “sesgo inflamatorio” genético que habría dado lugar a un conjunto de respuestas inmunológicas y conductuales. Éstas, habrían permitido a aquellos primeros humanos conservar la energía para defenderse contra las infecciones y a cicatrizar heridas junto con mantenerse alerta frente a un posible ataque. Se postula que este sesgo inflamatorio se mantuvo vigente durante gran parte de la evolución humana como consecuencia de la exposición a organismos mínimamente patógenos, particularmente en entornos rurales, lo que habría permitido el desarrollo de una serie de respuestas inmunes moduladoras (inducción de células T y B regulatorias (Tregs y Bregs), interleuquinas antiinflamatorias como IL-10, factor de crecimiento transformante-β (TGF-β) y otras.
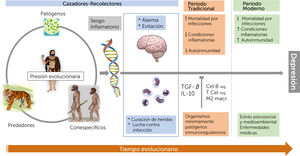
En los entornos urbanos (generalmente menos contaminados por bacterias) de las sociedades desarrolladas actuales, los sujetos están sometidos a intensos desafíos psicológicos, pero carecen del estímulo de las amenazas infecciosas que fueron las principales fuentes de morbilidad y mortalidad durante la mayor parte de la evolución humana. En ausencia de los controles y equilibrios inmunológicos tradicionales, los desafíos psicológicos del mundo moderno evocarían repertorios inmunológicos y de comportamiento ancestrales, tales como las altas tasas de trastornos relacionados con la inflamación, incluida la depresión. Es decir, desde esta perspectiva, la pérdida de estas disposiciones inmunológicas regulatorias estaría favoreciendo el desarrollo actual de enfermedades autoinmunes, alérgicas e inflamatorias. Así, de acuerdo a esta perspectiva, los elementos biológicos de la DM provendrían de aquel linaje9 (Figura 1).
Legado evolucionario de un sesgo inflamatorio.
La interacción de los primeros humanos con predadores, gérmenes patógenos y rivales de la misma especie habría producido un sesgo inflamatorio que incluiría un conjunto integrado de respuestas conductuales e inmunológicas que les permitía tener energía suficiente para la defensa contra las infecciones junto con de reponerse de las heridas, al mismo tiempo que podían mantener la vigilancia contra los ataques. Este sesgo, se plantea, se mantuvo durante la mayor parte de la evolución de la especie humana por la exposición a gérmenes mínimamente patógenos, lo que desarrollo respuestas inmunes caracterizadas por la inducción de linfocitos T y B regulatorios (T reg y B reg) y macrófagos inmunoregulatorios M2, así como la producción de las citoquinas anti inflamatorias interleuquina 10 (IL-10) y factor de crecimiento transformante-β (TGF-β). En ausencia de dichos estímulos y regulaciones inmunológicas, la sociedad moderna, abrumada por el estrés y las presiones psicosociales habría recurrido a los antiguos repertorios inmunológicos del pasado, desencadenando altas tasas de trastornos inflamatorios y también, dentro de ellos, depresión. (Modificado por el autor a partir de Miller A, Raison C, Nat Rev Immunol. 2016).
A fines de la década de los años 80 y comienzos de la siguiente, una serie de hallazgos comenzaron a hacer evidente la relación entre ciertas enfermedades crónicas, tales como diabetes, cáncer, ateroesclerosis, obesidad y un antiguo conocido: la inflamación.
La investigación actual ha profundizado su interés en la relación de los procesos inflamatorios en estas patologías, sumando además a enfermedades neurodegenerativas como el Alzheimer; pero no pasó demasiado tiempo para que apareciera también la depresión mayor agregada a la lista de las enfermedades en que tal relación parecía más que ocasional o azarosa. Así, durante los últimos diez o quince años se ha venido acumulando una creciente investigación sobre el ámbito de confluencia de ambas entidades (Figura 2).
Uno de los primeros trabajos que apuntaron a tal asociación fue el de Maes et al10, cuyos resultados constituyeron alguna sorpresa, ya que hasta entonces la literatura sobre sistema inmune y depresión estaba dominada por reportes que hablaban de una disminución de la respuesta celular (linfocítica) y una reducción de la actividad de las células “natural killer” (NK). En la investigación de Maes, por el contrario, aparecía un aumento de biomarcadores inflamatorios en los pacientes deprimidos, incluyendo un aumento en las proteinas de fase aguda, como la proteina C-reactiva (PCR) y también en la producción de citoquinas proinflamatorias.
Sin duda que una parte de estos hallazgos estuvieron vinculados a un cambio paradigmático: la neuroinmunología temprana consideraba que los sistemas inmune (SI) y nervioso central (SNC) se encontraban aislados, separados por la barrera hémato-encefálica (BHE). La excepción a aquello, obviamente, eran las enfermedades que lograban encontrar una “fisura” en la BHE, como en las infecciones o trauma del SNC, es decir, cuando la unión de ambos necesariamente se tornaba una patología.
El debate sobre las citoquinas pasó a ser central en las ideas sobre las relaciones inter-sistémicas (SNC-SI) de finales de los 80 y toda la década de los 90. Se hizo evidente que tanto las células inmunes como las del SNC tenían la capacidad de producir y de responder a las citoquinas, apuntando así a un mecanismo que les era común. Fue posible observar, por ejemplo, que la inyección intracerebral de interleuquina-1 (IL-1) provocaba el tipo de respuestas autonómicas, neuroendocrinas y conductuales que los animales exhiben de manera típica cuando presentan una infección y que corresponden a un tipo de reacción adaptativa y coordinada llamada “conducta de enfermedad” (sickness behaviour). Todo aquello solo tendría sentido en un contexto neuroinmune11.
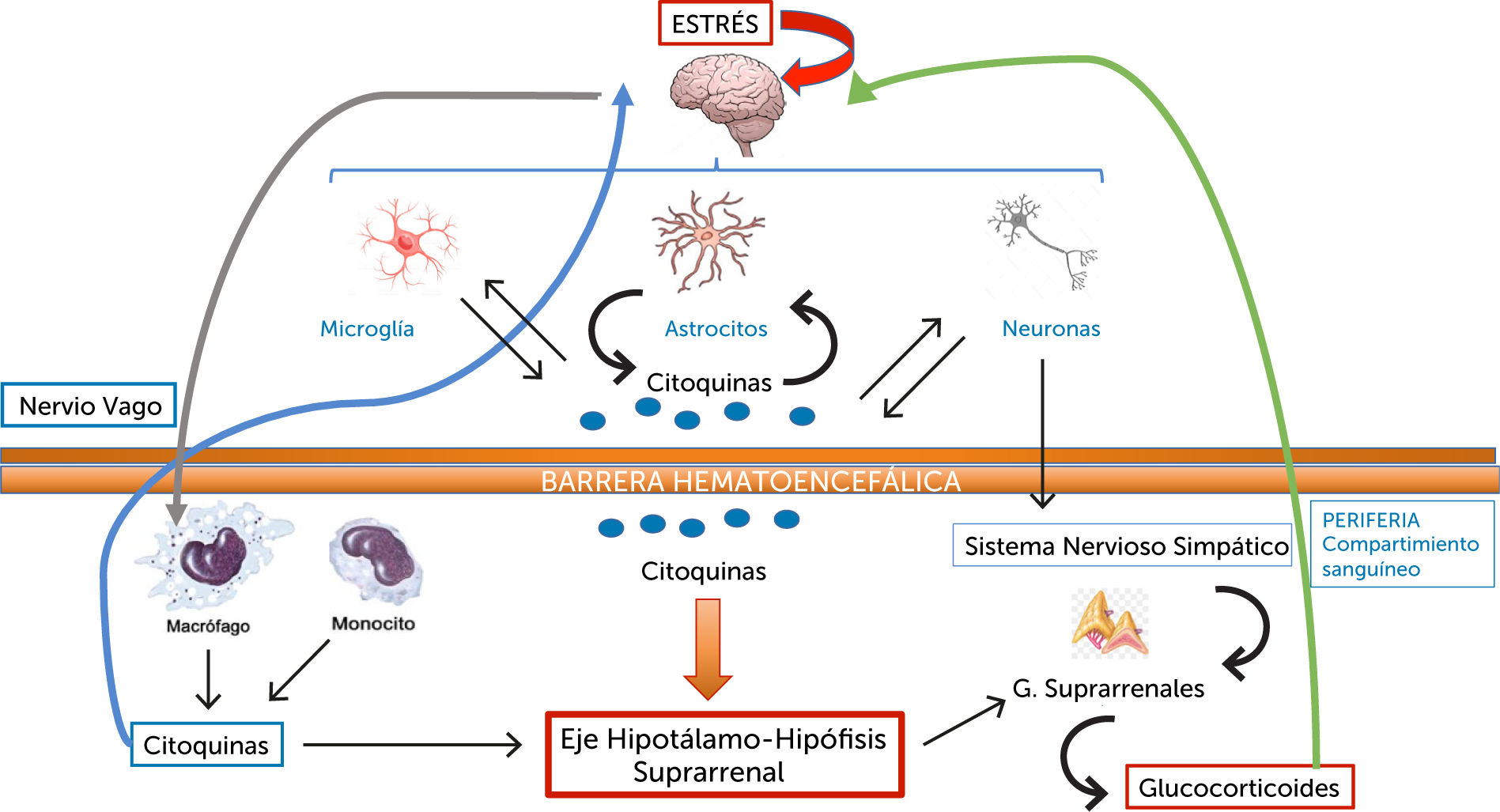
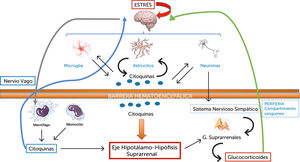
Además del transporte de citoquinas hacia y desde el cerebro, la investigación sobre otras vías de comunicación entre el sistema inmune y el sistema nervioso se ha multiplicado. Existen además vías neurales autonómicas simpáticas y parasimpáticas, comunicación a través de los órganos circunventriculares y secreción de sustancias inmunoactivas a partir de las células que constituyen la BHE (Figura 3).
Todas estas vías y otras aún no completamente estudiadas, constituyen las bases sobre las que se ha ido asentando una comprensión más completa de lo que aparece ahora como un complejo entramado comunicacional entre los sistemas nervioso, endocrino e inmune (Figura 4).
¿Es entonces la depresión una enfermedad inflamatoria?Esta es una pregunta que ya se han planteado muchos investigadores, sin duda animados por el creciente número de pruebas y resultados, algunos de los cuales se ha examinado en este artículo. Sin embargo, hay un conjunto de elementos provenientes de las mismas investigaciones que salen al paso de esa hipótesis y que incluso permiten negar de manera categórica esta afirmación:
- 1.
La existencia de inflamación ha sido documentada solo en un subgrupo de pacientes con depresión, sin que hasta ahora se encuentre dilucidado el patrón clínico sintomático de aquel grupo.
- 2.
La existencia de marcadores inflamatorios no es específica para la depresión, sino que se ha documentado también en otros trastornos mentales, tales como esquizofrenia, bipolaridad, trastornos de ansiedad (TOC, ansiedad generalizada, crisis de pánico, trastorno de estrés postraumático), Parkinson, HIV y Alzheimer.
Es decir, los efectos inflamatorios sobre el comportamiento no ocurren dentro de ningún trastorno específico, sino que parecen estar relacionados con su posible acción sobre sistemas complejos de neurotransmisores y circuitos neurales que subyacen a los mismos, pero sin que sea posible establecer hasta ahora una singularidad en la respuesta sintomática atribuible a la inflamación.
Más allá de estos argumentos biológicos y, más aún desde la clínica que de la investigación en ciencias básicas, se entiende a la depresión como una condición compleja y multifactorial, donde los componentes histórico-evolutivos de cada sujeto, los contextos sociales en que estos se desenvuelven y de manera muy especial las relaciones interpersonales que establecen, por solo citar a algunas de ellas, son cruciales en la génesis y desarrollo de esta afección. Nada de esto obsta, sin embargo, para continuar indagando en el complejo entramado inmuno-neuro-endocrino en el que participan los procesos inflamatorios vinculados a la depresión.
Depresión y enfermedades inflamatoriasComo se ha dicho antes, la inflamación como proceso participa en una larga lista de condiciones de alta prevalencia en la actualidad, tales como obesidad, infecciones (hepatitis), enfermedades crónicas (enfermedad cardiovascular, cáncer, diabetes, Alzheimer, etc.), disbiosis (alteración de equilibrios en la composición de la masa bacteriana en el tubo digestivo); estrés crónico, y por cierto, también como consecuencia de un importante número de procedimientos terapéuticos (cirugías, radio, quimio o inmunoterapia). Tomando en cuenta la alta frecuencia en la población general de cada una de estas condiciones, es también habitual encontrar en ellas la co-ocurrencia de síntomas depresivos e incluso de depresión mayor propiamente tal. Sin embargo, se trata de un conjunto de condiciones y de enfermedades altamente heterogéneo en sus características y delimitaciones; de hecho, muchas de ellas se traslapan y por lo mismo resulta más difícil de estudiar la vinculación de alguna de ellas con otro fenómeno complejo como es la depresión.
A continuación, se examina de manera somera el modo en que se vinculan con la depresión, en particular, y con los trastornos del ánimo en general, dos condiciones crónicas que tienen a la inflamación como su componente principal: la artritis reumatoide (AR) y el lupus eritematoso sistémico (LES). Aunque el universo de condiciones inflamatorias crónicas es muy extenso, la elección que se ha hecho de estas enfermedades tiene que ver con su alta prevalencia y con el importante compromiso funcional y deterioro en la calidad de vida de quienes las padecen. Adicionalmente, existe bastante investigación sobre comorbilidad entre estas enfermedades inflamatorias con la depresión, además de un creciente cuerpo de investigación y resultados sobre los fenómenos que podrían subyacer a ellas.
Artritis Reumatoide y DepresiónEl conocimiento respecto de la fisiopatología de la artritis reumatoide ha ido en creciente aumento y lo mismo ha ocurrido con el desarrollo de las nuevas terapias, especialmente sobre aquellas orientadas a los procesos inmunitarios que le subyacen. Sin embargo, la comprensión respecto de los factores emocionales que la acompañan no ha tenido el mismo éxito.
La coexistencia de trastornos de salud mental en la AR es conocida desde hace mucho, apareciendo la DM con tasas variables de uno a otro estudio que van del 14 al 48%12, es decir, con tasas de depresión mucho más altas que las observadas en la población general. Con el fin de explicar la relación entre AR y DM, tradicionalmente se invocaban como explicación (plausible, por lo demás) los efectos de la discapacidad funcional y al dolor crónico, consecuencias habituales de la enfermedad inflamatoria. Sin embargo, han ido apareciendo nuevas pruebas acerca de otras posibles explicaciones de esta correlación.
La mayoría de los estudios que han analizado la comorbilidad de AR y depresión muestran en general una direccionalidad desde la AR a la depresión11 y no al contrario, excepto unos pocos trabajos que ha mostrado una naturaleza bidireccional entre ambas, pudiendo la depresión también predecir la aparición de AR, de acuerdo a ciertos autores12. No existen suficientes elementos de juicio aún para explicar ese fenómeno, sin embargo, una posible interpretación sería la alteración de la funcionalidad inmunitaria subyacente a ambas condiciones.
Desde luego son numerosos los motivos por los que la comorbilidad entre depresión y AR resultan preocupantes. Quizá el más importante de todos sea la influencia de los síntomas depresivos en la reducción de las tasas de remisión de la AR, uno de los objetivos centrales en las nuevas terapias de la enfermedad. Con frecuencia, la existencia de depresión asociada a AR conlleva un impacto negativo agregado en la funcionalidad del paciente. Entre otros de estos efectos negativos de la comorbilidad se cuenta la reducción en la adherencia a tratamiento de los pacientes con AR. En el estudio ya citado de Matcham10, se alude a una reducción de aproximadamente un 30% en las oportunidades de respuesta positiva a las terapias biológicas de la AR.
La AR es una enfermedad inflamatoria crónica inmuno-mediada, caracterizada por un aumento (up-regulation) de las citoquinas proinflamatorias más importantes, tales como interleuquina 1β (IL-1β), TNF-α e IL-6, y que refleja una fisiopatología inmunitaria desregulada tanto en forma innata como adaptativa13. Como se ha dicho más arriba, las concentraciones de todas estas citoquinas se encuentran también aumentadas en las mediciones de sangre periférica de un grupo de pacientes con depresión respecto de controles sanos14.
Así, en una enfermedad mediada por inmunidad como la AR, sería factible que se echaran a andar tanto mecanismos humorales como neurales. Respecto de los primeros: a) los mediadores circulantes podrían activar el endotelio de la BHE, b) la BHE podría transportar de manera activa moléculas como el TNF-β dentro de SNC y c) las moléculas inflamatorias podrían acceder al SNC a través de los órganos circunventriculares. Respecto de las vías neurales, el modelo que mejor describe este proceso es el que señala al nervio vago como responsable de trasmitir información ascendente aferente sobre la condición de la inmunidad periférica, mientras que la información eferente descendente modularía las respuestas periféricas inmunitarias (ver Figura 3).
Por otra parte, algunos estudios han discutido el rol que podría jugar la IL-6 tanto en el dolor como la fatiga y por ello, también en la depresión asociada a la AR. Aunque algunos trabajos señalan la reducción de estos tres factores utilizando medicación anti IL-6, se hace difícil determinar si es que las acciones sobre alguno de estos dominios es el causante principal de los efectos sobre los restantes15.
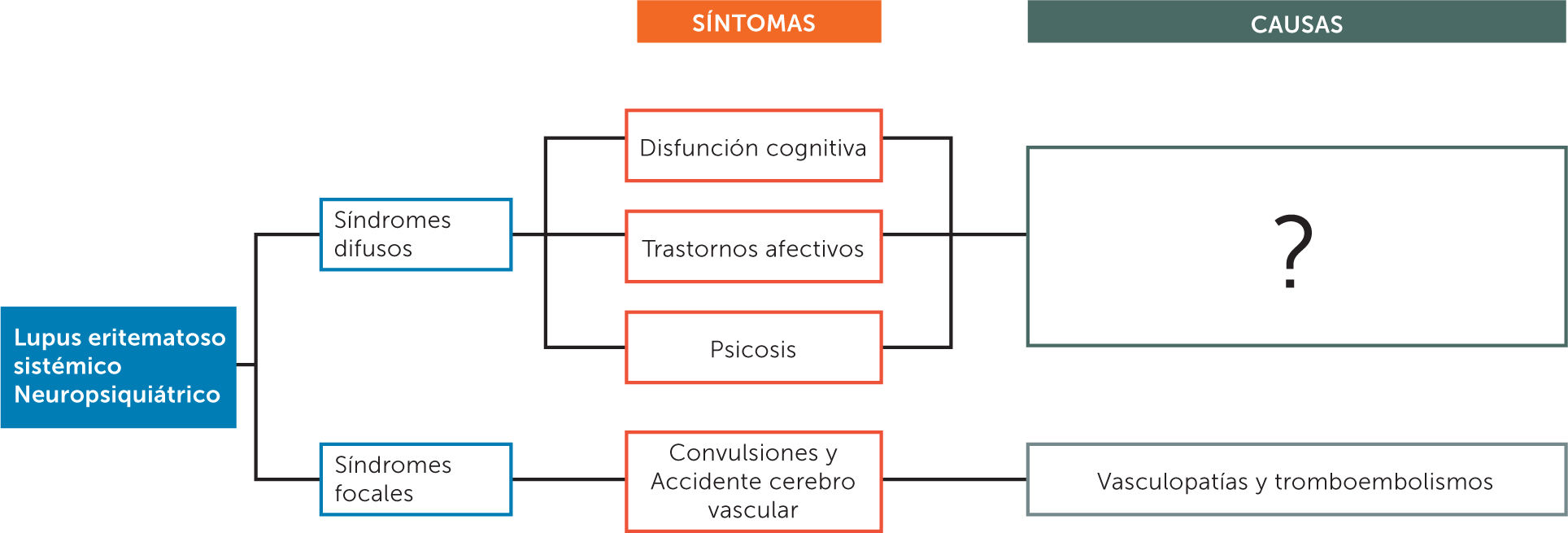
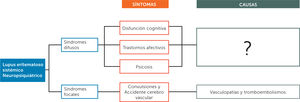
Lupus Eritematoso Sistémico y Trastornos AnímicosUna de las diferencias clínicas importantes entre la AR y el LES es el frecuente compromiso del sistema nervioso en el lupus, uno de los blancos más relevantes de esta enfermedad autoinmune, lo que ha dado origen, por lo demás, a la conceptualización del lupus eritematoso sistémico neuro-psiquiátrico (LES-NP). Lo pleomorfo de las manifestaciones del LES-NP, que comprende desde cefaleas hasta convulsiones, por una parte y por otra, desde manifestaciones neurotiformes hasta depresiones severas y psicosis, pareciera estar determinado por muy diversas expresiones de la fisiopatogenia vinculada al LES. No obstante, es necesario hacer una primera distinción, considerando que existen agrupaciones sintomáticas neuro-psiquiátricas que se pueden adscribir con claridad a síndromes focales, mientras que existe otro tipo de condiciones que se pueden considerar como un síndrome difuso (Figura 5).
Como se puede ver ahí, en el caso de los síndromes focales, donde los síntomas más frecuentes son convulsiones y accidentes vasculares encefálicos, las causas de los mismos parecen relacionados principalmente con tromboembolismos venosos, isquemias por vasculopatías y acción de anticuerpos anti- fosfolípidos.
Sin embargo, en el caso de los síndromes difusos, las posibles causas de los trastornos cognitivos, afectivos y psicóticos son aún especulativos o carentes de datos que sustenten de manera convincente los mecanismos planteados, yendo desde trastornos del señalamiento glutamatérgico en los desórdenes cognitivos hasta propuestas de anticuerpos anti receptor NMDA (R-NMDA) o el aumento de los niveles de proteína S 100 en las psicosis, pasando por los posibles de trastornos de la modulación de sistemas serotoninérgicos y adrenérgicos y del eje hipotálamo-hipófisis-adrenal, en el caso de los trastornos del ánimo 16. Es interesante señalar que, en el caso de estos últimos, se repite la posibilidad de alteraciones vinculadas con un aumento de las interleuquinas IL-1, IL-6, IL-2 y de TNF-α e IFN-α que se han señalado más arriba en el texto como relacionadas a la AR.
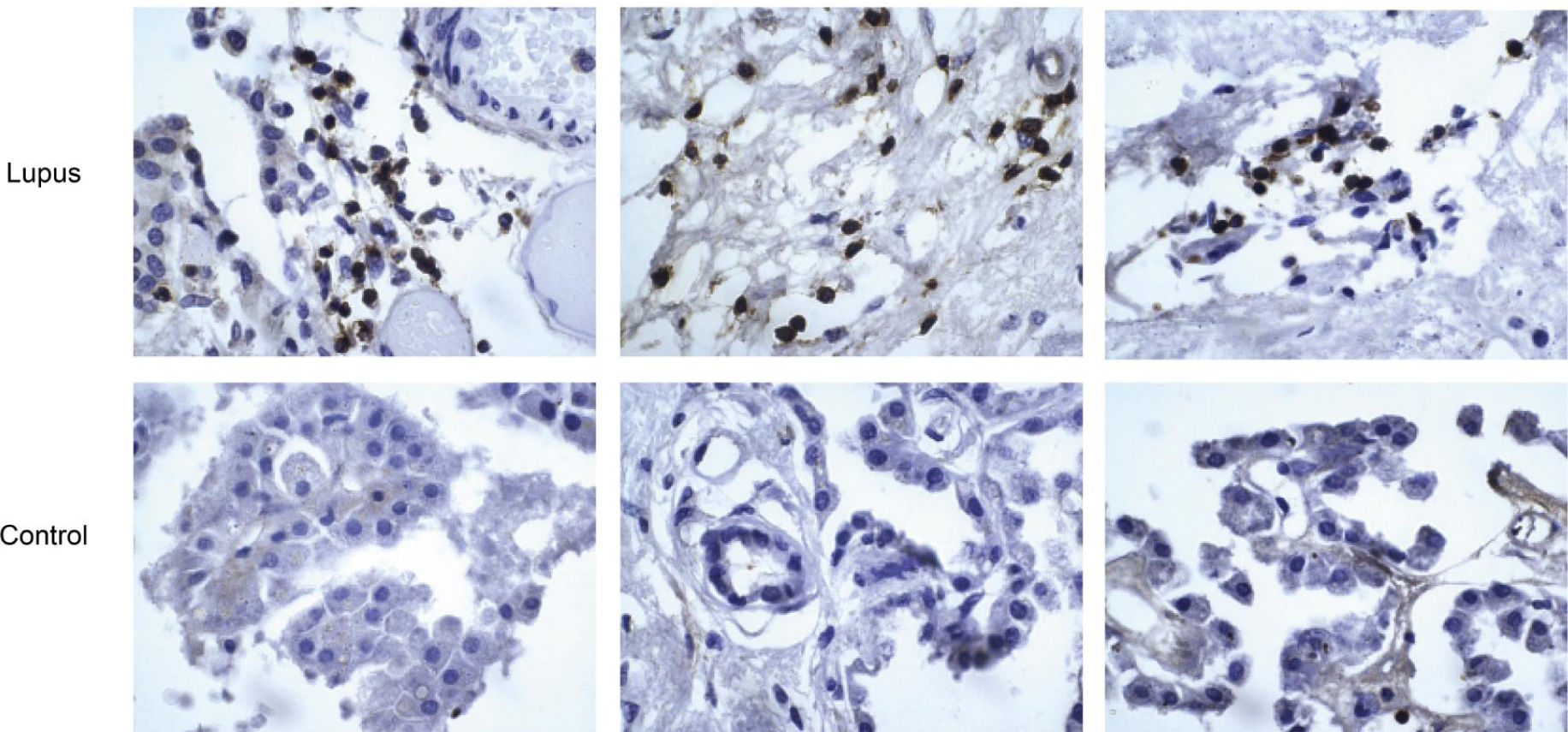
En otro ámbito, hemos hablado anteriormente de ciertos flancos o debilidades que podría exhibir la protección que brinda la BHE en el sentido de su impermeabilidad en relación a la migración celular desde el territorio vascular hacia el SNC. En esa línea, es interesante evaluar la evidencia existente sobre la conformación de una estructura u órgano linfoide terciario dentro del plexo coroideo (PC) en el LES-NP, dando cuenta de una de las vías que haría más posible la comunicación entre los productos inflamatorios del sistema inmune y el sistema nervioso central, como se muestra en la Figura 4, otorgando así nuevos argumentos a la hipótesis de una comunicación muy estrecha entre las enfermedades inflamatorias sistémicas que llegan a tener repercusión cerebral y síntomas psíquicos severos, en especial el de los trastornos del ánimo, que serían los de mayor frecuencia17 (Figura 6).
Tejido del plexo coroideo humano (PCH) con infiltración leucocítica
La tinción revela clusters de células +CD45 [cluster de diferenciación +45] con las características morfológicas de linfocitos en el estroma del PCH de pacientes con LES, pero no en los controles. (Modificado de Stoke, JCIInsight. 2019).
Hasta ahora no hay estudios dirigidos a investigar la respuesta y evolución de síntomas depresivos como objetivo principal en pacientes con enfermedades inflamatorias, utilizando los agentes biológicos existentes para el tratamiento de tales enfermedades. Sin embargo, existe un buen número de trabajos que han investigado el efecto de la reducción de citoquinas proinflamatorias en la mejoría de síntomas depresivos como un objetivo secundario18–23. Algunos de estos incluyen inhibidores de TNF e inhibidores de IL-6 (tocilizumab) en pacientes con AR. Aunque existen numerosos factores inductores de confusión en algunos de estos estudios, existe una tendencia a encontrar respuestas “antidepresivas” favorables. Una de las variables que resulta compleja de determinar es la mejoría sobre la fatiga, un síntoma neurovegetativo que suele encontrarse en ambas condiciones y cuyo alivio, por lo mismo, es difícil de adscribir a la mejoría de una u otra condición.
Algunos autores han enfatizado la necesidad de continuar enfocando el manejo de la depresión en el contexto de la artritis reumatoide de una manera convencional e integrada respecto de las intervenciones de salud mental, dado que los resultados meta-analíticos, al menos hasta ahora, no resultan convincentes a la hora de atribuir mejorías de la sintomatología del ánimo basadas solo en la utilización de la farmacoterapia de la AR.
Por otra parte, existen estudios meta-analíticos sobre grupos importantes de pacientes que han utilizado antiinflamatorios no esteroidales (AINEs) y sus efectos sobre los síntomas depresivos o episodios depresivos propiamente tales. Algunos de ellos muestran efectos significativos de mejoría de síntomas depresivos, no explicables solamente por el alivio de síntomas inflamatorios o dolor24.
El estudio de Raison25 por otra parte, mostró cierta mejoría de síntomas depresivos utilizando el antagonista del factor de necrosis tumoral infliximab en pacientes que presentaban una elevada línea base inflamatoria, medida a través de PCR. Esta mejoría no se encontraba, sin embargo, en pacientes depresivos que presentaban niveles menores de inflamación. Actualmente existen protocolos de investigación de otros agentes monoclonales como tocilizumab y sirukumab, aunque sus resultados aún no se encuentran publicados.
ConclusiónAunque aún no existen pruebas definitivas para una vinculación causal entre procesos inflamatorios y enfermedad depresiva, lo cierto es que la investigación tanto básica como clínica, ha abierto un fecundo terreno para indagar los complejos modos de interrelación entre ambos fenómenos. Es posible que los diferentes dominios en que uno y otro se mueven, induzcan a menudo a conclusiones precipitadas respecto hasta dónde se puedan extrapolar las conexiones entre una y otra. Pero quizá uno de los aspectos más interesantes de la investigación contemporánea respecto de la depresión clínica y los procesos inflamatorios lo constituye el análisis de los ámbitos de articulación entre sistema inmune, sistema nervioso central y sistema endocrino. La relación entre estos dos últimos ya es bastante conocida desde hace mucho y ha provisto de modelos exitosos para la comprensión del estrés, por ejemplo. Lo novedoso está en cómo ha ingresado a este interjuego nuestro conocimiento sobre sistema inmune y los otros dos.
El extenso desarrollo de psicofármacos basado en el modelo monoaminérgico de neurotransmisión ya supera con creces el medio siglo y ciertamente que ha provisto a la medicina de herramientas terapéuticas en extremo valiosas y cada vez más sofisticadas. Es virtualmente imposible imaginar a la psiquiatría contemporánea sin el aporte de los antipsicóticos atípicos, los antidepresivos de nueva generación o los estabilizadores del ánimo, por ejemplo, medicamentos que han cambiado de manera fundamental nuestras prácticas y la evolución de los cuadros más graves que nos corresponde tratar, mejorando no solo la sintomatología, sino también la calidad de vida de los pacientes.
Sin embargo, como hemos comentado a través de este trabajo, también es cierto que no hemos logrado los estándares de avance tanto en ciencias básicas como en clínica que consiguen otras especialidades de la medicina y ello es particularmente cierto (y grave) en el caso de la depresión mayor, con la alta tasa de síntomas residuales que el tratamiento no es capaz de erradicar.
Continuar investigando en un área como el de la respuesta inflamatoria y sus vinculaciones con el fenómeno depresivo es de crucial importancia. Más aún si consideramos que la inflamación es un proceso que parece vinculado a un número tan importante de condiciones médicas crónicas de alta prevalencia.
Conflictos de interésDeclaración de conflictos de interés
El autor no posee conflictos de interés.








![Tejido del plexo coroideo humano (PCH) con infiltración leucocítica La tinción revela clusters de células +CD45 [cluster de diferenciación +45] con las características morfológicas de linfocitos en el estroma del PCH de pacientes con LES, pero no en los controles. (Modificado de Stoke, JCIInsight. 2019). Tejido del plexo coroideo humano (PCH) con infiltración leucocítica La tinción revela clusters de células +CD45 [cluster de diferenciación +45] con las características morfológicas de linfocitos en el estroma del PCH de pacientes con LES, pero no en los controles. (Modificado de Stoke, JCIInsight. 2019).](https://static.elsevier.es/multimedia/07168640/0000003100000002/v1_202005010644/S0716864020300225/v1_202005010644/es/main.assets/thumbnail/gr6.jpeg?xkr=ue/ImdikoIMrsJoerZ+w96p5LBcBpyJTqfwgorxm+Ow=)
