La catarata es la primera causa de ceguera en el mundo, responsable de un 48% de los casos, la mayoría relacionados con la edad y por tanto no existe forma de prevenir su aparición. Teniendo en cuenta el envejecimiento progresivo de nuestra población, sin duda su prevalencia e importancia como problema de salud pública se van a mantener en el tiempo. Con los avances en el estudio preoperatorio, anestesia, instrumental, tecnología de los lentes intraoculares y en la técnica de facoemulsificación, la cirugía ha pasado de ser un procedimiento enfocado a la extracción segura de la catarata, a uno que apunta a alcanzar el mejor resultado refractivo posible, idealmente liberando al paciente del uso de anteojos y con un muy breve tiempo de recuperación.
Se describirán los avances más importantes en los aspectos enumerados anteriormente, enfocados a mostrar cómo estos benefician a nuestros pacientes, haciendo de la cirugía actual de la catarata un procedimiento seguro y predecible.
Cataract is the first cause of blindness worldwide, responsible of 48% of cases. Most of them are age-related, therefore, without possible prevention. Due to our population ageing, its prevalence and importance as a public health problem will persist over time. With the advances in preoperative studies, anesthesia, instrumentation, intraocular lens technology and phacoemulsification technique, cataract surgery has evolved from a procedure mainly focused in a safe cataract extraction to a new one, aiming to reach the best possible refractive outcome, freeing patients of spectacle use with a minimal recovery time.
Principal advances related to these topics will be described, showing how these changes benefit our patients, turning cataract surgery into a safe and predictable procedure.
En datos de la Organización Mundial de la Salud, si consideramos las causas de ceguera a nivel mundial, la catarata (opacificación del cristalino) ocupa el primer lugar con un 47,9% de los casos (1), en rangos de un 5% en Europa y Norteamérica a más de un 50% en países con altos niveles de pobreza.
Debido al envejecimiento progresivo de la población mundial, no esperamos una disminución en su incidencia. En EE.UU. los resultados del Censo de 1994 proyectan que para el año 2.030 uno de cada 5 personas será mayor de 65 años (2).
El tipo mas común de catarata es el relacionado a la edad (catarata senil), comienza a aparecer desde la sexta década en adelante (3). Como no existe tratamiento farmacológico para la catarata, el tratamiento estándar es la extracción quirúrgica del cristalino opacificado y la implantación de un lente intraocular (LIO) artificial.
La cirugía de catarata en los últimos 20 años ha sido en general una historia de éxitos sucesivos. Las mejoras constantes en la técnica quirúrgica, como también en la tecnología de los lentes intraoculares (LIOs), instrumental, medicamentos, ha permitido tiempos operatorios cada vez más cortos, procedimientos cada vez menos traumáticos, postoperatorios cada vez más breves y mejor tolerados, y resultados cada vez más satisfactorios y predecibles para nuestros pacientes (4).
Esto es avalado por la reducción progresiva de las complicaciones postoperatorias (5), como ejemplo las endoftalmitis post-quirúrgicas actualmente se tabulan en cifras tan bajas como 0,015% (6).
Este artículo mostrará las manifestaciones clínicas de la catarata, el método de tratamiento actual y los cuidados perioperatorios. Se discutirán los beneficios de los distintos tipos de LIOs, como también las posibles complicaciones y su frecuencia.
Tipos de catarataExisten numerosas causas y variedades, por lo cual también muchas maneras de clasificarlas. Una forma básica de diferenciarlas es separarlas en congénitas y adquiridas (senil, traumática, tóxica, por radiación, medicamentos).
Catarata congénita se define como la opacidad del cristalino presente al nacimiento o que se desarrolla durante el primer año de vida (7). Sus causas incluyen infecciones intrauterinas, enfermedades metabólicas, y una amplia variedad de síndromes congénitos. Las infecciones intrauterinas que más comúnmente causan catarata son rubéola, sarampión, herpes simplex, varicela, influenza, sífilis y toxoplasmosis. Las causas congénitas incluyen galactosemia, trisomía 21, trisomía 13, catarata congénita familiar y síndrome de Lowe (8).
Las adquiridas son mucho más frecuentes y dentro de ellas el tipo más habitual es la catarata senil, con sus 3 variedades principales: periférica, nuclear y subcapsular posterior. Los diferentes tipos de opacidad comprometen la visión de distinta forma (9); por ejemplo, la opacidad nuclear disminuye la agudeza visual y la subcapsular posterior hace al paciente muy sensible al deslumbramiento.
Manifestaciones clínicasLa manifestación central de la catarata es el empeoramiento de la visión, el cual es en general lentamente progresivo. El impedimento no se limita a la agudeza visual, también compromete otros aspectos como la visión de contraste, la saturación de color y el deslumbramiento (Figura 1 y 2). El paciente refiere dificultades al cambiar de ambientes con distinto grado de iluminación, puede presentar halos alrededor de las luces, problemas para conducir en la noche (especialmente con las luces de los vehículos que circulan en sentido contrario) y lectura limitada con iluminación habitual. La opacificación del núcleo del cristalino se puede manifestar como un incremento en el poder refractivo de éste, lo que permite al paciente por un tiempo variable leer sin usar anteojos, hasta que finalmente la visión de cerca también se compromete.
Estudio preoperatorioLa evaluación inicial del paciente incluye anamnesis detallada, buscando específicamente causas de catarata distintas al propio envejecimiento, como enfermedades metabólicas, degenerativas, uso de esteroides, antecedentes de trauma ocular u otra patología intraocular concomitante.
Exámenes generales (hemograma, orina, electrocardiograma de reposo, uremia y glicemia) complementan la evaluación.
Dentro de los antecedentes es muy importante consignar el uso de medicamentos específicos como aspirina, anticoagulantes y últimamente Tamsulosina.
El uso de anticoagulantes o aspirina no es una contraindicación de cirugía de catarata, pues ésta se realiza sobre estructuras avasculares (córnea y cristalino), y en la gran mayoría de los casos se utiliza anestesia tópica (10), con lo cual se elimina el riesgo de la punción de la anestesia local (retrobulbar o peribulbar).
En el 2005 David Chang (11) describió el Síndrome del Iris Fláccido Intraoperatorio (IFIS) secundario al uso de Tamsulosina. Este antagonista selectivo α1A utilizado para el tratamiento de la hiperplasia prostática benigna (también usado en mujeres con retención urinaria) provoca alteraciones en el comportamiento del iris durante la cirugía (ondulación del estroma iridiano, propensión al prolapso del iris hacia las incisiones operatorias y constricción progresiva de la pupila), el cirujano debe estar conciente del antecedente para modificar el plan quirúrgico y prevenir posibles complicaciones, las cuales aumentan en forma significativa en estos pacientes.
El examen oftalmológico completo permite descartar la presencia de alguna patología ocular asociada que pudiera contribuir o causar por si sola la disminución de agudeza visual.
La oftalmoscopía binocular indirecta (examen de fondo de ojo con el paciente dilatado) es fundamental, la periferia retinal debe ser evaluada en busca de lesiones que puedan predisponer al desprendimiento de retina. Los pacientes sometidos a cirugía de catarata tienen mayor riesgo de esta complicación durante el primer año después del procedimiento (1/1000 versus 1/10.000 en la población general), el riesgo se iguala al tercer año post-cirugía. Si hay lesiones predisponentes, éstas se deben tratar antes de la cirugía de catarata.
Se realiza una queratometría (medición del poder refractivo de la córnea) para identificar la presencia de astigmatismo y permitir el posterior análisis de las opciones de tratamiento, el que generalmente se realiza en el mismo acto quirúrgico.
El estudio debe incluir además una biometría ocular, pues para el cálculo del LIO es fundamental determinar el largo axial del globo ocular. En este momento existen dos métodos de medición; la ecografía ocular (ecobiometría), usada actualmente en cataratas más densas, que no permiten el adecuado paso de la luz y la biometría óptica (IOLMaster®, Carl Zeiss Meditec®) que mide la longitud con un haz infrarrojo de 780nm, sin embargo, presenta el inconveniente de no lograr buena penetración en cristalinos cataratosos muy densos.
Plan quirúrgicoDebe ser analizado con el paciente de acuerdo a sus necesidades y expectativas.
La técnica utilizada con mayor frecuencia es la facoemulsificación (12), en la cual el cristalino es emulsificado y aspirado a través de una punta o aguja que vibra a alta frecuencia (ultrasónica).
Esta punta o aguja está conectada a la consola del facoemulficador, donde se ajustan los poderes de las tres funciones principales: la irrigación que permite mantener los espacios dentro del ojo, la emisión de ultrasonido (poder) que provoca la disrupción y emulsificación del cristalino cataratoso y el flujo de aspiración que va retirando el material emulsificado. Estas funciones son controladas por el cirujano a través de un pedal.
Mucho se ha avanzado en la técnica durante los últimos años, mejorando sustancialmente en términos de seguridad y eficiencia (12, 13), este avance va ligado y sólo es posible por la constante evolución tecnológica.
Esta evolución ha permitido la utilización de cada vez menos poder, pero de forma mucho más eficiente, con lo cual se reduce el tiempo operatorio, la cantidad de energía liberada y la producción de calor. El disminuir el tiempo operatorio disminuye el trauma sobre las estructuras intraoculares, especialmente el endotelio (capa celular que recubre la cara interna de la córnea, responsable de su deshidratación y consiguiente transparencia). Esta reducción es siempre beneficiosa, como ejemplo en EE.UU. la primera causa de transplante de córnea es la falla endotelial secundaria a cirugía de catarata (queratopatía bulosa pseudofáquica). La disminución de los tiempos operatorios se relaciona también con la reducción de la incidencia de endoftalmitis post-quirúrgica, estas devastadoras infecciones (5, 6) se producen por flora habitual que penetra al ojo durante la cirugía o en el periodo perioperatorio inmediato. Por otro lado la disminución de energía liberada y de producción de calor reduce los cambios térmicos en las heridas operatorias, haciéndolas más estables y herméticas, haciendo más difícil la colonización bacteriana (14).
El análisis de las opciones se realiza según las necesidades del paciente, si requiere privilegiar la visión de cerca, la visión de lejos o prefiere una solución para ambas. Es fundamental identificar su nivel de exigencia, actividad, deseo de independencia de anteojos y la presencia de astigmatismo.
La cirugía actual pretende entregar una solución integral al problema refractivo, es por eso que existen soluciones asociadas al LIO (multifocalidad, corrección de astigmatismo) y procedimientos coadyuvantes que se realizan en el mismo acto quirúrgico o en tiempo posterior.
Los lentes intraoculares ofrecen dos alternativas básicas: lentes monofocales y lentes multifocales. Dentro de los monofocales existen con y sin corrección de astigmatismo (lentes tóricos). El astigmatismo corresponde a una condición muy común, en que la córnea es más curva en uno de sus meridianos, lo que provoca mayor o menor distorsión en la visión. Las imágenes se perciben con sombra, difusas o dobles.
Los lentes monofocales entregan una visión de muy buena calidad, con muy buena sensibilidad al contraste y pocos problemas nocturnos (halos), pero tienen la limitación de que sólo ve nítido en una distancia focal, ya sea de lejos (elección más frecuente dentro de los monofocales) o de cerca; para el resto de las distancias es necesario utilizar anteojos. En los pacientes que elijan monofocales y que tengan un astigmatismo (15) bajo, se hace la herida operatoria en el meridiano de mayor curvatura corneal con el fin de aplanar ese eje, la biomecánica de la córnea hace que por acoplamiento el meridiano más plano se encorve y el astigmatismo desaparezca. Esto es útil en astigmatismos pequeños de 0,50 a 0,75 dioptrías.
En pacientes con astigmatismos mayores se realizan incisiones limbares relajantes (Figura 3), que consisten en cortes circunferenciales precisos, realizados en la periferia de la córnea, centrados en el meridiano más curvo. Los grados de arco de las incisiones varias de acuerdo a la magnitud del astigmatismo y la edad del paciente. La profundidad es fija en 600 micrones.
Si el astigmatismo es mayor de 1.50–1.75 dioptrías se utilizan lentes monofocales tóricos (con corrección de astigmatismo). Estos permiten corrección de hasta 4 dioptrías de astigmatismo. Cuando el astigmatismo es mayor se puede subcorregir, utilizar LASIK (cirugía refractiva con láser) o una combinación de lente intraocular tórico y LASIK (Bioptics).
Los lentes multifocales tienen como gran ventaja la liberación de los anteojos en la mayor parte de las situaciones. Entregan una muy buena visión de cerca y una buena visión de lejos, considerando además que permiten por su multifocalidad, una buena a muy buena visión intermedia.
La limitación en su uso está dada por condiciones del paciente. Si existe patología (problemas retinales, glaucoma con daño en campo visual) no se recomienda su uso. De la misma forma pacientes muy exigentes no son los mejores candidatos.
El diseño del lente (Figura 4) todavía tiene algunas limitaciones; la sensibilidad al contraste está disminuida, lo que en la práctica limita la visión en situaciones de pobre iluminación. Presentan visión de halos y deslumbramiento al conducir de noche. La nitidez no es completa, es muy buena, pero pacientes muy exigentes notan esta diferencia.
La gran mayoría de los pacientes sobrellevan muy bien estas limitaciones al estar concientes de que es producto del diseño, que es el “precio a pagar” por la liberación de los anteojos. Estas molestias disminuyen significativamente con el paso del tiempo.
Se combinan con las mismas técnicas descritas previamente en caso de astigmatismo. A fines de octubre estarán disponibles en Chile lentes intraoculares multifocales tóricos los que permitirán corregir visión de cerca, de lejos, intermedia y hasta 2,5 dioptrías de astigmatismo.
CirugíaLa cirugía no requiere preparación especial, salvo la dilatación farmacológica de la pupila, este proceso toma alrededor de 30 minutos. Durante ese periodo se instilan gotas de antibióticos profilácticos (cuyo uso no ha demostrado en forma estadísticamente significativa la prevención de la endoftalmitis post-quirúrgica) y antiinflamatorios no esteroidales (cuyo uso ha demostrado prevenir la miosis intraoperatoria).
Previo a la colocación de los paños quirúrgicos se debe instilar 1 gota de polividona iodada al 5% en cada fondo de saco conjuntival (16, 17), medida que ha demostrado disminuir en forma estadísticamente significativa el riesgo de endoftalmitis post-quirúrgica crónica (fundamentalmente por P. Acnes).
La cirugía se hace bajo anestesia tópica (18), instilando gotas de pro-paracaína o tetracaína, la sedación debe ser superficial pues permite la cooperación del paciente durante el procedimiento. La anestesia tópica, sumada al abordaje quirúrgico por córnea, hace posible la cirugía en pacientes bajo tratamiento anticoagulante o antiagregante plaquetario.
En los casos que requieran corrección de astigmatismo se debe marcar la córnea del paciente en posición sentado, identificando el eje de los 0−180°.
La cirugía dura aproximadamente 30 a 45 minutos.
Luego de aislar las pestañas, que corresponden a la fuente principal de contaminación bacteriana, se utiliza un espéculo palpebral (blefarostato) para mantener el ojo abierto durante la cirugía, lo que permite que el paciente se pueda desentender del parpadeo.
Bajo microscopio se realiza una herida principal de entre 1,8 y 2,75 milímetros, a través de la cual más adelante se introduce la punta o aguja del facoemulsificador y una o dos paracentesis (heridas secundarias para instrumental de apoyo).
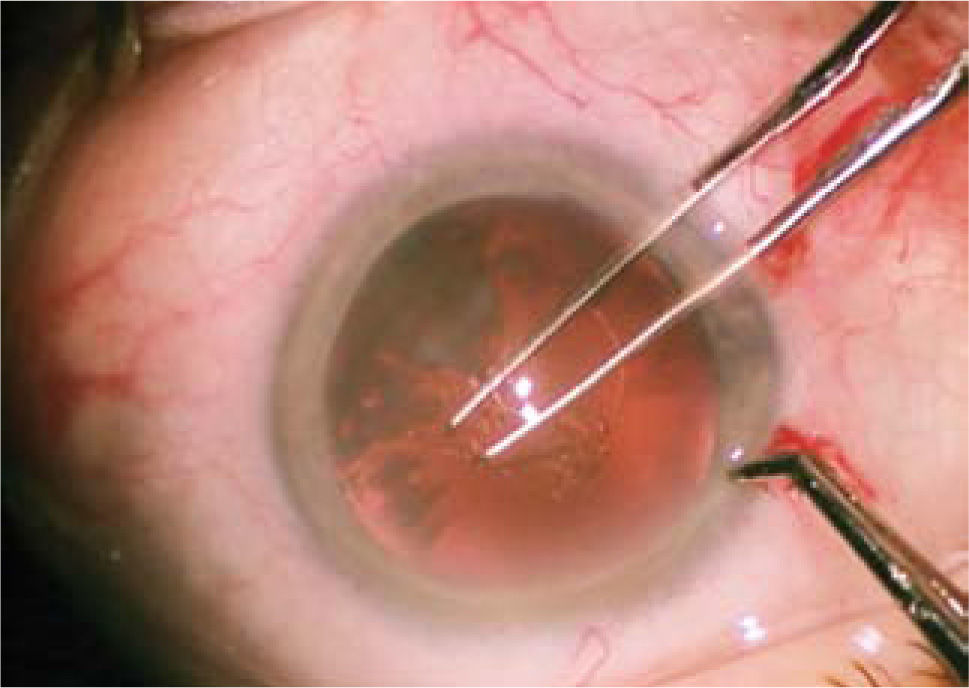
La cámara anterior se rellena con material viscoelástico, éste permite la mantención de los espacios y protege las estructuras intraoculares, fundamentalmente el endotelio corneal. En estas condiciones de estabilidad y seguridad se construye una apertura circular continua (capsulorhexis) en la cápsula anterior del cristalino, de unos 4,5 a 5 milímetros de diámetro (Figura 5). Esto se realiza con pinzas o una aguja modificada (quistótomo).
Utilizando suero se separan las fibras del cristalino del saco capsular que las rodea, en un proceso denominado hidrodisección (este saco corresponde a la membrana basal del epitelio cristaliniano, y tiene un espesor entre 9 y 20 micrones).
Luego se realiza la facoemulsificación del cristalino cataratoso, introduciendo la punta o aguja del facoemulsificador por la herida principal e instrumentos de apoyo por las paracentesis o heridas secundarias, que ayudan a fragmentar la catarata y ofrecen estos fragmentos a la punta de la aguja en forma secuencial y sistemática.
El saco se limpia de restos de fibras, las que son aspiradas de forma manual o automatizada. Luego se rellena el saco de viscoelástico para expandirlo y se procede a inyectar el lente intraocular (Figura 6) en su interior.
Si es un lente tórico se rota hasta lograr alinear las marcas del lente con los ejes marcados previamente en la córnea.
Un cuidadoso lavado del material remanente es crítico, con retiro de todo el viscoelástico presente; es especialmente importante limpiar el saco detrás del lente intraocular para evitar complicaciones post-operatorias.
Se hidratan las heridas comprobando su hermeticidad. Si las heridas no son herméticas se deben suturar para evitar la filtración. Esta sutura se realiza con nylon monofilamento 10–0 y se retira a los 7 días post-operatorios.
Se debe proteger el ojo operado con algún tipo de escudo, el de elección es de plástico transparente, el que debe ser usado durante 3 noches, para evitar un trauma accidental durante el sueño.
Evolución post-operatoriaLa recuperación después de la cirugía es bastante rápida. Muchos pacientes están en condiciones de retomar sus actividades habituales desde el día siguiente.
La visión mejora progresivamente a medida de que la pupila retoma su tamaño habitual, proceso que toma generalmente menos de 24 horas. Durante las primeras horas es frecuente que los pacientes describan ver de color rojizo o la presencia de halos en forma transitoria. Esto está dado por el efecto de la luz del microscopio sobre la retina.
El tratamiento post-operatorio consiste en instilación de colirios de antibiótico (actualmente se prefieren quinolonas de 4ta generación (19), corticoides (prednisolona 1%) y antiinflamatorios no esteroidales. Estos últimos (20) se utilizan en la prevención del edema macular quístico, complicación subclínica frecuente de la cirugía intraocular, que al hacerse clínica provoca disminución tanto aguda como crónica de visión. No es necesario medicamentos orales pues las concentraciones intraoculares alcanzadas por los colirios son muchísimo más altas.
ComplicacionesLas complicaciones en general son infrecuentes (21) (menos del 1% de los casos).
Dentro de las intraoperatorias las asociadas a anestesia local (con inyección peribulbar o retrobulbar) como la hemorragia retrobulbar, perforación del globo ocular e incluso parálisis respiratoria (por inyección en la vaina del nervio óptico y a través de esta al espacio subaracnoideo) son extremadamente raras en si mismas (22) (0,066%), ahora con el uso casi de regla de anestesia tópica (colirios anestésicos) son eventos extraordinarios. El riesgo de hemorragia no aumenta significativamente con el uso de anestesia tópica, aun en pacientes anticoagulados (22). Otras complicaciones incluyen desgarro capsular, pérdida vítrea, efusión coroidea y hemorragia expulsiva.
En el postoperatorio las más frecuentes son por lo general transitorias (edema corneal, aumento de la presión intraocular).
Las complicaciones graves como endoftalmitis, hemorragia y pérdida de visión son raras en frecuencia (21) (0,015%, 0,02% y menor de 0,01% respectivamente).
El riesgo de desprendimiento de retina es 10 veces mayor que en la población general durante el primer año, igualándose al tercero postoperatorio (23). Los pacientes deben tener indicación de consultar si aparece visión de luces (como relámpagos), visión de manchas o una combinación de ambas. Todos estos síntomas traducen tracción retinal y requieren un examen de fondo de ojo dilatado en busca de un desgarro retinal o un desprendimiento de ésta. Mientras más precoz es el diagnóstico, mejor es la respuesta al tratamiento, sea este con láser o cirugía.
La complicación post-operatoria más frecuente es la mal llamada “catarata secundaria”, que en realidad no corresponde a una nueva catarata (pues el cristalino se extrae por completo durante la cirugía), sino a la opacificación del saco capsular por proliferación y metaplasia fibrosa de células epiteliales aisladas, llegó a ser tan frecuente como 50% a 5 años (24) con los diseños antiguos de LlOs, pero actualmente no alcanza al 3% en 5 años (25) con los nuevos modelos. Su manejo es muy simple y consiste en realizar una capsulotomía con láser, procedimiento ambulatorio y prácticamente exento de morbilidad.
Una pregunta muy frecuente de los pacientes es cuanto dura el LIO, o si tiene que cambiarse cada cierto tiempo. Desde el primer LIO implantado en 1949 (26) no hay ninguna publicación que sugiera desgaste del material que lleve a su recambio o reemplazo.
ResultadosEl criterio mayor de éxito en la cirugía de catarata, en una cirugía no complicada, es la agudeza visual (cuanto logra ver nuestro paciente).
Actualmente, en ojos sin patología asociada sobre el 95% de los pacientes logra agudeza visual de 20/30 o mejor (21) (que corresponde a un 90% o más).
Por otro lado estamos obligados a medir la calidad de visión, que corresponde a la capacidad de ver bien en el contexto de requerimientos visuales individuales (como logra ver nuestro paciente). Varias mediciones objetivas y subjetivas se usan para determinarla (21).
A modo de ejemplo, en el caso de los LIOs multifocales (27), entre el 85 y el 96% de los pacientes refieren liberarse del uso de anteojos en toda situación. Sobre el 90% califica su visón de cerca y de lejos como muy buena o excelente (28).
Sin embargo los lentes multifocales requieren de un periodo de adaptación para aprovechar todos sus beneficios, este periodo de entrenamiento es variable de una persona a otra y va desde un par de días a 2–3 meses.
ConclusiónLa tecnología continúa su evolución, y muy pronto tendremos disponibles lentes intraoculares ajustables, que podrán ser modificados en el postoperatorio, de forma no invasiva, para corregir todo defecto residual. La cirugía será cada vez más automatizada para disminuir el riesgo de error. Heridas más pequeñas y mejor construidas permitirán disminuir el riesgo de infección. Se encuentre en pleno desarrollo la cirugía con láser, lo que llevará a una mayor estandarización y consiguiente seguridad.
Como hemos revisado en estas páginas, la cirugía actual de la catarata ofrece altos niveles de predictibilidad (más de 95% de agudeza visual mejor o igual a 20/30) y seguridad (pérdida de agudeza visual en menos del 1% de los casos) (21, 27, 28).
Esto permite ofrecer a nuestros pacientes un resultado visual y una mejora en calidad de vida muy significativa, con niveles de satisfacción subjetiva y mejora objetiva por sobre el 90%, asociados a complicaciones graves en niveles menores a 0,02%.
Por las características de nuestra población esta cirugía será cada vez más frecuente, pero las mejoras constantes y sostenidas en su tratamiento hacen mirar este futuro con fundado optimismo.
El autor declara no tener conflictos de interés, en relación a este artículo.