La incontinencia fecal sigue un siendo un problema cuya incidencia no es despreciable y con una repercusión sociosanitaria importante.
No cabe la menor duda que en las últimas décadas este proceso se ha visto beneficiado de la incorporación de nuevos métodos diagnósticos y terapéuticos.
Cabe destacar la extensión de la ecografía tridimensional como elemento fundamental en el diagnóstico, permitiendo obtener una idea morfológica de los esfínteres, hasta el momento impensable. Por otro lado, en el tratamiento, la utilización de la neuromodulación, ha permitido obtener tasas de curaciones sorprendentes.
A pesar de todo lo anterior, se sigue investigando de forma intensa, en un intento de conocer su etiopatogenia, pero a nivel molecular.
Se trabaja en tratamientos médicos efectivos y técnicas mínimamente invasivas con nuevas sustancias aumentadoras de volumen.
La ingeniería busca la construcción de esfínteres anales artificiales que se toleren bien por el paciente; o la bioingeniería en construirlos a partir de andamios y células madre.
Fecal incontinence remains being a problem which incidence is not despicable such an important social and health impact. Is no doubt that in last decades, this process has been benefited from the introduction of new diagnostic and therapeutics methods.
It should be noted the spread of the 3D scan as essential element to diagnosis, allowing to obtain an idea of morphological sphincters, unimaginable to the moment. Moreover, for treatment, using neuromodulation, has allowed to obtain surprising healings rates. Despite the previous, it is still under intensively investigation in order to understand its pathogenesis, but at the molecular level.
Currently, effective medical treatments and minimally invasive tecnics with bulking agents are working on. Engineering seeks to build artificial sphincter being well tolerated by the patient, and Bioengineering build them from scaffolds and stem cells.
La incontinencia fecal (IF) supone la incapacidad para retener los gases y/o el material fecal hasta que su expulsión sea socialmente aceptable. Se estima que hasta el 1 al 7.4% en la población general y hasta un 25% en ancianos pueden padecerla (1-3).
Por lo tanto, nos encontramos ante un problema no despreciable, muchas veces invalidante y costoso desde el punto de vista económico.
El presente artículo pretende dar una visión práctica del tema. En una primera parte establecemos todos los aspectos y avances etiológicos, diagnósticos y terapéuticos que pueden ser utilizados en la actualidad por poseer suficiente evidencia científica. En la segunda parte, pondremos en jaque algunos de las cuestiones expresadas, fruto de las investigaciones que se están llevando a cabo, e indicaré el futuro que nos espera.
La incontinencia fecal manejo y avances actualesSabemos hasta hoy, que la continencia anal es una función compleja que depende de la interacción de múltiples mecanismos (4), entre los que se incluyen: la consistencia y el volumen de las heces, el transporte del contenido fecal del colon al recto, la capacidad, distensibilidad rectal y sensación anorrectal, el complejo esfinteriano así como, la musculatura e inervación del suelo pélvico (5). Establecer la etiología exacta de la IF es en ocasiones complejo.
Si atendemos a lo anteriormente expuesto puede ser clasificada en 4 categorías según esté alterado: el complejo esfinteriano, los nervios y sus vías, la consistencia de las heces o la ampolla rectal (compliance y sensación). Actualmente las causas más frecuentes son debidas a lesión tras el parto o cirugía anal (6).
El diagnóstico nos debe permitir conocer de forma concreta, no sólo los aspectos clínicos y etiológicos, sino también la severidad de los síntomas y su impacto sobre la calidad de vida.
La valoración clínica debe ser exhaustiva, para ello es fundamental que el paciente se sienta cómodo y relajado, y realice una descripción detallada de su problema. Se debe llevar a cabo una anamnesis dirigida para evaluar fundamentalmente antecedentes personales de otras patologías, etiología y duración de la incontinencia fecal, e intervenciones quirúrgicas previas para su tratamiento. Es importante conocer la historia obstétrica (episiotomía, desgarro, uso de fórceps, peso excesivo del niño en el nacimiento). La coincidencia entre incontinencia fecal y urinaria es muy frecuente.
Para la obtención de información específica acerca de la función intestinal habitual de los pacientes se les debe entregar un diario evacuatorio a completar durante 4 semanas (aunque se puede hacer también sólo 7 días), dónde se recogen características de las deposiciones y episodios de incontinencia y urgencia evacuatoria (7).
La fusión de la anamnesis con el diario defecatorio permite la clasificación por puntos, del fenómeno de la incontinencia fecal. Estos diferentes sistemas de evaluación relacionan, fundamentalmente, el tipo de heces perdido con el intervalo entre cada episodio de incontinencia.
Las escalas de valoración del grado de incontinencia son muy numerosas y de complejidad diferente. La escala de la Cleveland Clinic (8) proporciona de forma objetiva y sencilla, una valoración tanto de las características de las heces como de la frecuencia de los episodios de incontinencia, donde 0 representa la continencia perfecta y 20 el máximo grado de incontinencia. Una escala simple analógica que vaya del 0 (nada de continencia) a 10 (continencia completa) es muy útil, aunque la correlación con la manometría sea baja (9). Los sistemas valorativos son muy útiles para clasificar a un paciente, pero sobre todo para monitorizar los cambios habidos después de un tratamiento.
No hace mucho que Mínguez y cols. han validado la escala de calidad de vida en la incontinencia fecal (FIQL) de la Sociedad Americana de Cirugía Colorrectal en español. Éste consta de un total de 29 preguntas que, a su vez, están divididas en 4 subescalas:
- 1.
Estilo de vida (10 preguntas)
- 2.
Comportamiento (9 preguntas
- 3.
Depresión / percepción (7 preguntas)
- 4.
Vergüenza (3 preguntas) (10).
La FIQL creemos que es un instrumento muy adecuado para valorar efectividad de un tratamiento determinado mediante la mejora de la puntuación en la calidad de vida.
Tanto las escalas de severidad, como la de calidad de vida, serán herramientas fundamentales para valorar la eficacia del tratamiento aplicado.
La exploración física debe ser sistemática, e incluye inspección y palpación anorrectal, y tacto rectal. La exploración neurológica y de los reflejos también sigue siendo muy útil (8, 11, 12).
Además el diagnóstico debe incluir pruebas morfológicas (de imagen) y funcionales. Sin miedo a equivocarnos, pensamos que la ecografía anal tridimensional es uno de los avances más importantes de los últimos años, siendo hoy en día una de las únicas pruebas imprescindibles en el estudio de estos pacientes; ya que pueden obtenerse imágenes objetivas de los esfínteres anales de mayor calidad que las que se pueden conseguir por otros métodos (13, 14). Su sensibilidad y especificidad para la detección de defectos esfinterianos está en el orden de un 83 al 100% en la mayoría de estudios. Aunque la RM se ha mostrado equivalente a la ecografía endoanal en la detección de defectos del esfínter anal externo, no lo es a la hora de valorar el esfínter anal interno, en la que la ecografía endoanal es superior (15).
Se ha llegado incluso a establecer un sistema de gravedad de las lesiones de origen obstétrico utilizando como herramienta la ecografía (16). Consiste en una puntuación de 0-3, en cada uno de los tres ejes del espacio, y para los dos esfínteres, oscilando la puntuación total entre 0 (sin lesión en el complejo esfinteriano) y la máxima de 16 (lesión máxima en EAI y EAE).
El estudio del funcionalismo esfinteriano, aún se sigue realizando con la manometría anal. Los avances en este campo son fruto de la mejora en los catéteres (que han pasado ha ser electrónicos) y en el software empleado; de manera que se obtiene resolución más fiel a la realidad (17).
Como indicamos, la IF es un problema complejo que depende la mayoría de las veces, de la interacción de múltiples causas; por ello, se debe individualizar el tratamiento, de manera que en un mismo paciente puede ser necesario utilizar varios tratamientos de forma simultánea o escalonada. Estas medidas pueden ser clasificadas atendiendo a la agresividad y complejidad de las mismas en tres grandes grupos: conservadoras, mínimamente invasivas e invasivas.
La medidas conservadoras contemplan tanto medidas básicas como dietéticas, en un intento de modificar el tránsito intestinal y facilitar la continencia o minimizar su deterioro, como higiénicas para disminuir en la medida de lo posible los efectos adversos de la incontinencia (18).
Se debe intentar que el paciente adquiera una rutina horaria en la defecación con el objeto de estar libre durante todo el día de un eventual episodio de incontinencia. Así como recomendar una dieta rica en fibra, con el fin de aumentar el volumen de las heces y conseguir una mejor continencia. Se deben identificar y retirar los alimentos que puedan desencadenar los episodios (lactosa, etc.).
Los agentes antidiarreicos como el clorhidrato de loperamida, el fosfato de codeína o el difexilato/sulfato de atropina son la base del tratamiento farmacológico. La amitriptilina -20mg- también ha sido citada como útil en el tratamiento de pacientes con incontinencia urinaria y fecal sin evidencia de defectos estructurales o neuropatía (19). Los enemas y supositorios de Glicerina y Bisacodil son útiles en los pacientes con incontinencia pasiva y ensuciamiento secundario a una incompleta evacuación (incontinencia por retención). Se emplean con el fin de provocar el vaciado completo de la ampolla rectal. Los medicamentos antiflatulentos (dimeticona o lactasa, enzima que ayuda a la digestión de los carbohidratos) permiten evitar los escapes de gases al disminuir la formación de los mismos.
El biofeedback continúa teniendo en la actualidad un papel relevante. Es un método de enseñanza y entrenamiento, que intenta lograr un control sobre los esfínteres y la musculatura pelviana asociada. Utiliza diversos instrumentos eléctricos o de presión para mostrar al paciente los resultados de dicha enseñanza. En diversos estudios se ha mostrado que puede llegar a eliminar los síntomas hasta en un 50% de los pacientes, tras una cuidadosa selección. Los resultados son superiores si el paciente es mujer, padece síntomas severos y realiza al menos seis sesiones (20).
Los grandes avances terapéuticos incorporados en los últimos años al arsenal terapéutico han venido de la mano de las denominadas terapias mínimamente invasivas, en un intento de buscar una buena solución sin muchas complicaciones.
El tratamiento con aumentadores del volumen consiste en inyectar una sustancia a nivel del canal anal (en la submucosa o en el espacio interesfinteriano) con el fin de permitir un cierre efectivo del mismo. La sustancia ideal debe ser biocompatible, sin capacidad de migración, no alergénica, no carcinogénica y por último, que sea fácil de inyectar. Aunque existen diversos materiales, los más utilizados en la actualidad son: la silicona, el carbón y el hialurónico. Los buenos resultados 60-70%, que se publicaron inicialmente disminuyen con el tiempo de seguimiento, por lo que pueden ser necesarios nuevos implantes para conseguir de nuevo la mejoría. El enfermo idóneo para esta terapia es aquel que tiene un único defecto del esfínter anal interno, debiendo siempre estar el externo indemne (21).
La Neuroestimulación percutánea del nervio tibial posterior, ampliamente utilizado por los urólogos para tratar la vejiga hiperactiva, resurge en los últimos años, como una alternativa válida para los pacientes con incontinencia fecal. Intenta modular el plexo sacro indirectamente, a través del nervio tibial posterior, el cual contiene fibras sensoriales, motoras y autónomas derivadas de la cuarta a quinta lumbar y de primera a tercera raíces sacras. El tratamiento es ambulatorio, el paciente lo recibe en sesiones de 30 minutos uno o dos días a la semana, durante 3 meses. Las tasas de curación rondan el 50%, pero es posible que sean necesarios tratamientos de recuerdo en algunos pacientes. En principio se puede utilizar en las mismas indicaciones que la neuromodulación sacra (22).
Precisamente es esta última, la que mejores resultados ha tenido, de todos los tratamientos que han surgido en las dos últimas décadas. Aunque las indicaciones en la actualidad son amplias, el paciente ideal es aquel en la que el esfínter externo está intacto o ha sido reparado. Los pacientes son seleccionados después de un periodo de estimulación transitoria donde se valora la respuesta. Las tasas de curación oscilan entre el 85- 90%. El mecanismo de funcionamiento es desconocido en profundidad, aunque al igual que en la estimulación periférica, parece que debe intervenir estructuras corticales. Uno de los principales inconvenientes es el alto costo que tiene (23).
Por último los tratamientos más invasivos, que vienen de la mano de la cirugía, y cuyos avances han sido escasos.
El tratamiento quirúrgico de la incontinencia fecal se centra fundamentalmente en reparar el complejo esfintérico dañado a través de la realización de una plastia esfintérica o, menos frecuentemente y cuando el daño esfinteriano es muy extenso, a su sustitución por colgajos autólogos de músculo esquelético o el implante de un esfínter artificial.
La esfinteroplastia o superposición de los extremos del esfínter dañado junto con la plicatura del músculo puborectalis es la intervención frecuentemente realizada en defectos esfinterianos menores de 120º (23).
Otros tratamientos, que hace una década eran muy utilizados, en pacientes con graves daños estructurales del complejo esfinteriano (como la graciloplastia o la implantación de un esfínter anal artificial neumático), hoy tiene indicaciones excepcionales.
El lavado anterógrado de Malone, en determinados casos adecuado para niños, consiste en la realización de una cecostomía a través de la base apendicular y la instilación de enemas periódicos a través de ella (24).
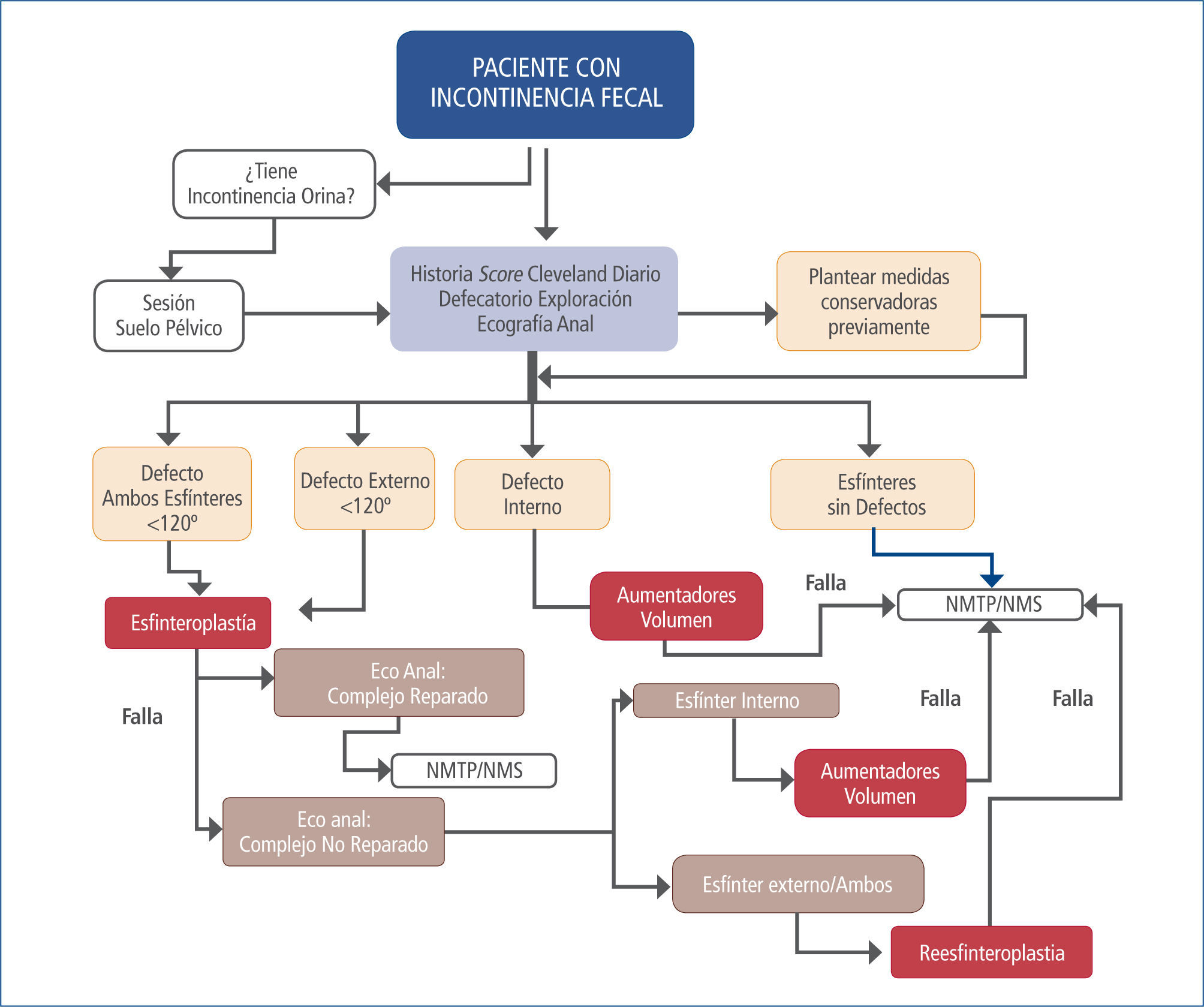
En contadas ocasiones y determinados pacientes la colostomía puede ser una solución satisfactoria para restaurar la calidad de vida cuando no ha sido posible realizar otras técnicas o ha existido fracaso de las mismas (Tabla 1 y Figura 1).
Medidas diagnósticas y terapéuticas actuales en la incontinencia fecal
| Diagnóstico: |
| • Anamnesis |
| • Exploración física |
| • Diario defecatorio, Escalas de Severidad y de Calidad de vida |
| • Ecografía anal |
| • Manometría anorrectal |
| Medidas Conservadoras |
| • Cambio hábitos dietéticos y defecatorios |
| • Biofeedback |
| Tratamiento Médico |
| • Loperamida |
| • Codeína |
| • Amitriptilina |
| • Supositorios de glicerina y bisacodil |
| • Antiflatulentos: dimeticona |
| Tratamiento Mínimamente Invasivo |
| • Aumentadores de volumen |
| • Neumodulación (Tibial posterior o sacra) |
| • Esfinteroplastia |
| • Lavado anterógrado de Malone |
| • Colostomía |
En los últimos años, gracias a la existencia de grupos con especial dedicación a esta patología, son muchos los estudios y líneas de investigación emprendidas, no sólo orientadas a conocer nuevos tratamientos, sino también la epidemiología, etiopatogenia y diagnóstico integral.
Efectivamente, aunque se disponen de datos sobre incidencia, aún hoy en día no existe porcentajes precisos, que nos permitan conocer su verdadera epidemiología. Por ello se intenta conocerla por grupos de edad y sexo, analizando los diversos factores y eventos que pueden influir a lo largo del tiempo, y su trascendencia en la calidad de vida (25). Otros estudios prestan su atención en saber en qué momento la continencia fecal alcanza su plena madurez y cuándo empieza su decadencia (26); o simplemente conocer cuál es el costo económico actual de esta enfermedad (27).
Son también varios los grupos que estudian de forma especial la incidencia de la IF tras el parto obstétrico, de manera que en los próximos años asistiremos a la asunción de varios trabajos al respecto, que sin duda tendrán implicación en nuestra práctica diaria. Bharucha (28).
Asistimos ya, a una verdadera revolución en el entendimiento etiopatogénico de la IF. Se conoce poco sobre la disfunción del esfínter a nivel molecular. Por ejemplo, varias hipótesis apuestan sobre el papel de la edad y el estrés mecánico, desde este punto de vista.
Se han encontrado en el músculo elevador del ano de mujeres mayores multíparas cambios miogénicos, consistente en: aparición de fibrosis, variaciones en el diámetro de las fibras, pequeñas angulaciones y en el tipo de agrupación de las mismas. También se ha descrito en el esfínter uretral externo de conejas viejas multíparas, una disminución selectiva en el volumen de las fibras musculares tipo 2 (rápida), la conversión de tipo 2 a el tipo 1 (lento), o ambas. El envejecimiento puede alterar la expresión de genes estructurales y afectar el crecimiento celular y la muerte. Hay también fenómenos de isquemia-reperfusión que pueden afectar a la función mitocondrial en el tracto urinario. En definitiva, observamos que el entendimiento actual de por qué se provoca la IF y urinaria, está muy alejado de la concepción que se tendrá en el futuro, pudiendo entender muchas de las cosas que hoy en día no explicamos con la visión morfológica y funcional simplista que actualmente manejamos (29).
En el diagnóstico se están intentando mejorar aún más las imágenes que nos aporta la ecografía, sobre todo en la fibrosis esfinteriana, utilizando la elastografía. Esta nueva técnica de imagen está basada en las diferencias existentes en las señales de radiofrecuencia según las diferentes propiedades elásticas del tejido u órgano a estudiar. Los resultados hasta el momento no han sido todo lo que realmente se esperaba (30).
Más esperanzas tenemos con la incorporación de los potenciales evocados somatosensoriales en el diagnóstico de la IF y aún más como determinante pronóstico de los pacientes tratados con neuromodulación. Nuestro grupo trabaja intensamente en esta línea, con el deseo de aportar en los próximos años alguna información que den peso a lo anteriormente expuesto.
Aparecerán fármacos, algunos ya están en ensayos Fase III, que ayudarán al tratamiento de los pacientes con incontinencia fecal leve o moderada. Estos fármacos se basan en el mejor conocimiento de los receptores del complejo esfinteriano. Por ejemplo, la fenilefrina (y otros como la L-eritrometoxamina o el Racemato) permiten un aumento del tono del esfínter anal interno, y aunque ya había sido utilizada para el tratamiento de pacientes con IF, hoy se ensayan otras vías de aplicación más efectivas, diferentes a la tópica (31).
En un intento de buscar el agente aumentador volumen ideal, se están estudiando varias moléculas que puedan ser susceptibles de su inyección, evitando los inconvenientes de las existentes en la actualidad.
La neuromodulación seguirá teniendo un papel relevante, aún más con la construcción de dispositivos más pequeños, recargables y con capacidad de ser microimplantados (32).
Se siguen investigando nuevos esfínteres artificiales, que permitan rebajar la tasas de explantaciones registradas con los existentes. En este sentido, existe una experiencia limitada con el denominado esfínter anal magnético, pero todavía hacen falta estudios multicéntricos y con seguimientos largos, para poder definir el papel que tendrá en el futuro (33).
En Alemania se ha diseñado otro tipo de esfínter telemétrico y de bajo voltaje -The German Artificial Sphincter System (GASS) II-, basado en la deformación de las placas piezoeléctricas debido al efecto piezoelectricidad (34).
Como en otras ramas de la medicina, la Terapia Celular también tendrá un papel relevante, al menos de forma teórica en el tratamiento de la IF. La hipótesis es sencilla, inyectamos células madre con el objetivo de regenerar lo que no existe, en este caso el músculo esfinteriano.
Se han dado los primeros pasos en animales de experimentación, demostrando su éxito a la hora de regenerar la función del esfínter anal dañado de forma experimental, mediante una evaluación clínica, histológica y electromiográfica. Hay estudios realizados con células madres mesenquimales procedentes de médula ósea en un modelo murino (34), y también existe un interesante trabajo en conejos utilizando células madres mesenquimales de cordón umbilical humano y de médula ósea (36). Todos han arrojado resultados favorables, tanto histológicos como funcionales.
En esta misma línea existe experiencia preclínica con las células mesenquimales en un modelo experimental (más de 160 ratas) y el efecto de éstas para el tratamiento de la incontinencia fecal estructural. En este estudio se utilizaron tanto células autólogas como alogénicas, sin haber encontrado eventos adversos relacionables y cuyos resultados de eficacia fueron muy alentadores (37).
Recientemente se ha registrado un ensayo clínico en la que se estudia la seguridad de CMMAd autólogas en el esfínter anal (Safety Study of Autologous Cultured Adipose -Derived Stem Cells for the Incontinence. ClinicalTrials.gov. Identifier: NCT01011686). Hay también publicado un estudio piloto observacional, con células mioblásticas autólogas en el esfínter anal externo con el fin de tratar a 10 mujeres con incontinencia fecal por daño obstétrico. Los autores concluyen que la inyección es segura y los síntomas de incontinencia fecal mejoran significativamente (38).
Nuestro grupo trabaja en este campo de forma intensa, tanto a nivel preclínico con células extraídas de músculo; como a nivel clínico con células procedentes de grasa abdominal, aún por validar por la Agencia Española del Medicamento.
Tantos los estudios preclínicos como clínicos en incontinencia urinaria (que presenta grandes similitudes con la fecal) y los preclínicos en incontinencia fecal, nos hacen pensar que las células madre mesenquimales de tejido adiposo pueden ser adecuadas para el tratamiento de los pacientes con incontinencia fecal por daño del complejo esfinteriano; ya que al menos de forma teórica podríamos recuperar el tejido fibroso periesfinteriano, restituir el músculo y regenerar las vías nerviosas dañadas.
El objetivo principal de nuestro estudio fase I/II, multicéntrico, doble ciego, aleatorizado y comparativo en dos grupos, es evaluar la seguridad y la factibilidad de la terapia con células troncales mesenquimales autólogas procedente de grasa en el tratamiento de la incontinencia fecal estructural, a través de la incidencia de acontecimientos adversos relacionados con el producto en investigación hasta los 12 meses post-administración intralesional. La sustancia control es Ringer Lactato.
El objetivo secundario es evaluar la posible eficacia de la terapia con células madre mesenquimales autólogas procedentes de grasa preferentemente abdominal en el tratamiento de la incontinencia fecal estructural en 16 pacientes. Para ello se medirá el cambio a los 6 y los 12 meses respecto al nivel basal en las siguientes variables: número de episodios de incontinencia fecal de heces sueltas o sólidas (según datos del diario defecatorio del paciente), score de Wexner y FIQL (escala de calidad de vida de incontinencia fecal).
La evaluación de los objetivos se realizará: comparando los resultados post-administración celular con los basales y comparando los resultados en el grupo experimental con los valores obtenidos en el grupo control.
¿Por qué elegimos tejido adiposo? El tejido adiposo contiene sólo un 40% a 60% adipocitos maduros, pero también se compone de la fracción vascular estromal (FVE). Este consiste en fibroblastos, macrófagos, mastocitos, células endoteliales, células hematopoyéticas y preadipocitos. Este último tipo de célula es considerado como el precursor de los adipocitos maduros. Una vez cultivadas, estas células se llaman células madre derivadas de tejido adiposo (ASC).
Numerosos estudios han demostrado la naturaleza pluripotente (capaces de diferenciarse en células de la capa de germen de lo mismo), o incluso la naturaleza multipotente (capaces de diferenciarse en células de otra capa de germen) de células ASC, capaz de adquirir in vitro células, musculares, condrocitos, neuronales, epiteliales, musculares lisas, macrofágos e incluso fenotipos hepáticos. Por otra parte, estudios recientes de animales han puesto de relieve el interés potencial de la ASC o células de FVE en terapia celular, en particular para la reparación de tejidos mesodérmicos y en la revascularización.
Teniendo en cuenta lo anterior y de forma más precisa el interés potencial de las células de FVE para el tratamiento de la incontinencia urinaria y el nuestro en la fecal se ve apoyada por muchas otras características de estas células que se describen a continuación.
- 1)
Las células de la FVE contienen un gran número de fibroblastos capaces de secretar colágeno, así como, la capacidad de las ASC para segregar y organizar sustancias endógenas de la matriz extracelular ya se ha puesto de relieve y el gran potencial para la fabricación de tejido conjuntivo.
- 2)
Por otro lado, varios estudios han demostrado claramente que las células mesenquimatosas del tejido adiposo tiene el potencial de diferenciarse en células de músculo liso o estriado. En lo que se refiere a músculo estriado, varios estudios han reiterado el potencial de la ASC.
Hace años que se publicaron los primeros intentos en animales de experimentación de realizar un trasplante anorrectal, con cierto éxito (39). Esta línea de investigación quizás haya quedado frenada, en el momento que la Bioingeniería Tisular declara que puede aportar lo mismo en el futuro (40, 41).
Nuestro grupo estudia también a nivel preclínico, la posibilidad de construir un esfínter in Vitro, para implantarlo posteriormente.
SíntesisNo cabe la menor duda que asistiremos en los próximos años a cambios significativos en este campo de la coloproctología. Lo que hoy es dogma el mañana será historia.
El autor declara no tener conflictos de interés, con relación a este artículo.