Introducción
Las radiografías constituyen la técnica de imagen tradicionalmente usada para objetivar las consecuencias patológicas de la inflamación articular en la artritis reumatoide (AR). Las erosiones, que representan la destrucción del hueso yuxtaarticular, y la disminución del espacio articular (DEA), que traduce la pérdida difusa del cartílago, son las lesiones radiográficas que mejor caracterizan el daño anatómico articular en esta enfermedad. Por esta razón los estudios radiológicos se suelen practicar de forma seriada para detectar la presencia de estas lesiones, así como su progresión a lo largo del tiempo en los enfermos con AR. Hoy por hoy, en la práctica clínica las radiografías se consideran «estándar oro» para medir el potencial modificador de la enfermedad de las terapias propuestas para la reducción de la progresión de la AR y, en cierto modo, para la monitorización de la respuesta terapéutica. El demostrar la capacidad de alterar el curso de la enfermedad frenando o deteniendo la destrucción articular, medida radiográficamente, se considera actualmente un requisito indispensable para que un agente sea aceptado como un fármaco modificador de la enfermedad (FAME)1.
El daño estructural de las articulaciones, estimado radiográficamente (erosiones, disminución del espacio articular), se inicia tempranamente en el curso de la enfermedad y predomina en las pequeñas articulaciones de las manos y los pies. La progresión ulterior se hace predominantemente a expensas de las articulaciones previamente lesionadas, más que por la aparición de lesiones en articulaciones previamente intactas radiográficamente2. Esto indica que el tratamiento de la AR debe iniciarse tempranamente y con terapias capaces de evitar o retrasar el daño estructural.
Métodos de cuantificación de las alteraciones radiográficas de la artritis reumatoide
Las lesiones radiológicas se consideran una de las medidas más importantes de desenlace (outcome) en la AR. Del mismo modo, uno de los objetivos mayores del tratamiento de esta enfermedad es la prevención o el retraso del daño radiológico y de su progresión.
Las alteraciones radiográficas habituales en la AR son el aumento de la densidad de las partes blandas articulares, osteoporosis yuxtaarticular, erosiones óseas, DEA y deformidades articulares. Entre todas estas alteraciones, las erosiones y la DEA son las lesiones más cualificadas para valorar radiográficamente, y de manera cuantitativa, el daño estructural articular en la AR. Por otra parte, aunque indudablemente se correlacionan, los mecanismos lesionales de las erosiones y de la DEA son probablemente de diferente naturaleza3.
Desde hace décadas se han propuestos numerosos métodos radiográficos, algunos de ellos con varias versiones, que permiten identificar y en cierto modo cuantificar el daño radiológico en la AR3,4 (tabla 1). El análisis de estos métodos radiográficos indica que, especialmente en ensayos clínicos, las articulaciones más rentables para valorar la progresión de la AR son las de las manos (radiocarpianas, carpianas, metacarpofalángicas, interfalángicas proximales) y los pies (metatarsofalángicas, primera interfalángica proximal). La abundancia y diversidad de estos métodos revelan que ninguno de ellos es el ideal, pero en la bibliografía los más utilizados son el de Larsen, el de Sharp, y el método de Sharp modificado por Van der Heidje.
En un futuro próximo es muy probable que la resonancia magnética (RM), con equipos de tamaño reducido y con menor coste que en la actualidad, será la técnica de elección para evaluar la presencia de lesiones articulares tempranas y su evolución posterior. La RM permite identificar la inflamación de la membrana sinovial articular y de las vainas tendinosas, las erosiones óseas así como la pérdida focal o difusa del cartílago articular, con una precisión y precocidad inalcanzables con la radiología convencional5. En un reciente estudio, las radiografías detectaron erosiones en el 15% de pacientes con AR de menos de 6 meses de duración, frente al 45% con RM. El 80% de los que no tenían erosiones en las radiografías basales y aproximadamente la mitad de los que tampoco las tenían en la RM basal no las presentaban después de un año 6. Este hecho puede ser importante para el diseño de ensayos clínicos. Del mismo modo, por la capacidad de la RM de detectar mínimos cambios de progresión del daño estructural, esta técnica es válida para el tratamiento de pacientes individuales con el fin de valorar la eficacia o la ineficacia de los tratamientos utilizados para evitar la progresión del daño estructural articular.
Relación entre daño estructural (radiográfico) y discapacidad en la artritis reumatoide
En un estudio longitudinal de 256 pacientes con AR seguidos durante 19 años se confirma la progresión constante del daño estructural. Es decir, que en contra de lo que se creía en los años ochenta, la progresión no es significativamente mayor en la AR temprana ni se reduce en las fases más tardías de la enfermedad7. La tasa media anual de nuevas erosiones y de nuevas articulaciones con DEA es, en este estudio, de 1,0 y 1,3, respectivamente, cifras que aumentan a 3,5 para ambos tipos de alteraciones en los pacientes con VSG mayor de 30 mm/1 h. Este valor predictivo de progresión radiográfica de la VSG se ha confirmado recientemente, junto a otros factores como la proteína C reactiva (PCR), positividad del factor reumatoide y de anticuerpos antiperinucleares, grado de afectación radiográfica basal y HLA DRB1*048.
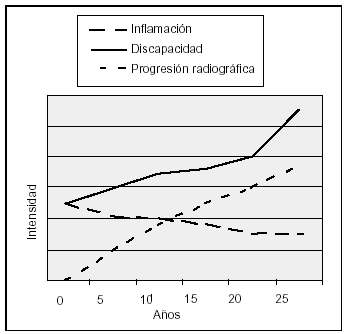
La explicación convencional de la discapacidad que se presenta más tarde o más temprano en los pacientes con AR asume que la persistencia de la inflamación sinovial conduce a la destrucción progresiva de las estructuras articulares y, por ende, a la incapacidad funcional. En la fase temprana de la AR la inflamación articular es el principal determinante de la discapacidad. Esta correlación disminuye con la duración de la enfermedad a favor del daño estructural como causante de la discapacidad9 (fig. 1). Como consecuencia de lo expuesto, se concluye que un tratamiento capaz de reducir tempranamente la progresión radiográfica reduce igualmente la discapacidad funcional futura.
Figura 1. Relación entre progresión radiográfica, inflamación y discapacidad en el curso de la artritis reumatoide. (Adaptada de Kirwan9.)
En una revisión reciente que evaluaba la relación entre daño articular y discapacidad en la AR analizando la bibliografía al respecto10, se confirma que el daño estructural progresa de manera constante en los primeros 20 años de la enfermedad, y que tanto el daño estructural como la discapacidad funcional aumentan a una tasa prácticamente constante con la duración de la enfermedad. La relación entre daño estructural y discapacidad es especialmente notable en la AR tardía (de más de 8 años de duración). Inicialmente los pacientes no presentan lesiones radiográficas o éstas son discretas, aunque puedan tener ya entonces una importante incapacidad funcional relacionada estrechamente con el grado de la actividad inflamatoria de la enfermedad. Sin embargo, en fases más tardías la relación entre daño estructural y disfunción es bastante más estrecha y notoria.
Es importante tener en cuenta que en cualquier momento de la evolución de la AR pueden aparecer otros factores, distintos del daño estructural articular y de la actividad inflamatoria de la enfermedad que pueden influir de otro modo, y a veces de forma importante, en el grado de discapacidad. Estos factores pueden ser de orden demográfico (edad y sexo), social, familiar, laboral, psicológico o terapéutico (sistema asistencial, utilización correcta de los recursos terapéuticos, relación médico-paciente, etc.). Estos factores podrían distorsionar la relación entre discapacidad y daño estructural. Por otra parte, también es cierto que existen variaciones individuales en las cuales todo lo anterior no se cumple totalmente. En todo caso, las conclusiones de esta revisión sostienen la política de utilización de FAME que eviten o reduzcan el daño estructural tanto en la AR reciente como en la establecida, sin pérdida de tiempo, para poder evitar o limitar la discapacidad inherente a esta enfermedad.
Evidencia de la eficacia de la leflunomida en el retraso de la progresión radiográfica de la artritis reumatoide
La leflunomida (LEF) es un nuevo inmunomodulador aprobado para el tratamiento de la AR que inhibe la síntesis de novo de la pirimidina en los linfocitos activados provocando un cese reversible del ciclo celular.
La eficacia y la seguridad de la LEF han sido avaladas por los resultados de varios estudios. En una publicación reciente11 se recogen los resultados de tres de ellos (US301, MN301 y MN302), multicéntricos, aleatorios y controlados, dos de ellos con un grupo placebo, que confirman que la LEF retrasa la progresión radiográfica de la AR.
El estudio US301 ha sido llevado a cabo en EE.UU. en 482 pacientes que fueron asignados por aleatorización a tratamiento con placebo (PL) (n = 118), o metotrexato (MTX) (n = 182) y LEF (n = 182) durante 12 meses. La dosis de LEF era de 20 mg diarios, después de una dosis de carga inicial de 100 mg/día durante tres días. El MTX se administró a dosis semanales de 7,5 mg, aumentando a 15 mg/semana si la actividad de la AR persistía a las 6-9 semanas de iniciado el tratamiento. En caso de ineficacia o intolerancia en 4 meses con el tratamiento asignado inicialmente, se recibía otro tratamiento. Así, los que inicialmente tomaban PL o MTX pasaban a recibir LEF, y los que recibían esta última pasaban a recibir MTX, después de un período de lavado de cuatro semanas.
Los estudios MN301 y MN302, realizados en Europa, comparan LEF contra sulfasalacina (SSZ) y MTX en 358 y 999 pacientes, respectivamente, seguidos durante 12 meses. La dosis de LEF y de MTX eran similares a las del estudio US301; la SSZ se administró a dosis diarias de 2 g.
En los tres estudios se realizaron radiografías de manos y pies al inicio, a los 6 y a los 12 meses, o cuando un paciente abandonaba el estudio. La interpretación de las radiografías fue realizada por un radiólogo experimentado siguiendo el método de Sharp modificado. Las erosiones fueron puntuadas según una escala de 0 a 5 en 34 articulaciones de las manos y en 12 de los pies, y la DEA en una escala de 0 a 4 en 36 articulaciones de las manos y en 12 de los pies. Se consideró que existía progresión de un grado a otro cuando aparecía una nueva erosión en una zona previamente indemne de una articulación o cuando una erosión existente aumentaba claramente de tamaño. El espacio articular normal se cuenta como 0 puntos; la DEA < 11%, 1 punto; entre 11 y 50%, 2 puntos; entre 50 y 99%, 3 puntos, y cuando existe anquilosis de una articulación, 4 puntos. La adición de las puntuaciones por erosiones y DEA en cada paciente da la puntuación radiográfica total, con un máximo posible de 422.
Todos los análisis estadísticos se realizaron sobre la base de intención de tratar, es decir, incluyendo a todos los pacientes en su grupo original de tratamiento aunque hubiesen cambiado posteriormente de grupo o salido del estudio. La primera medida de los efectos del tratamiento sobre la progresión radiográfica fue la puntuación radiográfica total, suma de puntos por erosiones y DEA. Los análisis secundarios efectuados son los siguientes: cálculo separado de los cambios en erosiones y en DEA, número de pacientes con nuevas articulaciones erosionadas y número de pacientes con progresión radiográfica definida como un aumento en erosiones superior a 3 puntos. Asimismo se estudiaron las características demográficas, la puntuación radiográfica basal, los cambios radiográficos según la duración de la enfermedad, la puntuación basal o ausencia de erosiones basalmente, el uso concomitante de corticoides, la utilización o no previa de FAME y los cambios en VSG, PCR, y el Cuestionario de Salud Health Assessment Questionnaire (HAQ) para probar la asociación entre variables clínicas y progresión radiográfica.
Las características demográficas, la proporción de pacientes que no habían recibido FAME previamente y las características basales de la enfermedad eran comparables en cada uno de los tres estudios. En el estudio US301, el 73% de los pacientes tienen radiografías basales y a los 12 meses (87%), o en el momento que abandonan el estudio (13%), mientras que en los estudios MN301 y MN302 el 65 y el 64% de los pacientes evaluables tenían radiografías basales y finales.
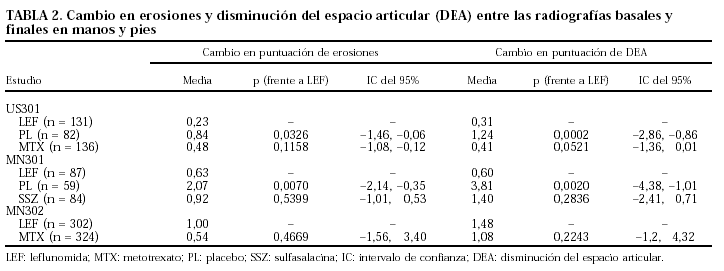
El tratamiento con LEF, MTX y sulfasalacina (SSZ) fue significativamente mejor que PL en la reducción de la progresión radiográfica de la enfermedad (tabla 2). En los estudios US301 y MN301 la puntuación de erosiones era significativamente más baja (p < 0,05) en los pacientes tratados con LEF comparados con PL (p = 0,0326 y 0,0070, respectivamente). Otro tanto ocurre con la DEA (p = 0,0002 y 0,0020).
Para calcular la rapidez de la destrucción articular entre el comienzo de la enfermedad y el momento de entrada al estudio, los autores estiman una tasa anual de progresión radiológica dividiendo la puntuación radiográfica individual total por la duración de la artritis. Esta tasa anual de progresión es similar entre los grupos de tratamiento de cada estudio. Comparando la tasa anual de progresión estimada basalmente con los cambios observados en la puntuación total al final del estudio, la progresión de las lesiones radiográficas es significativamente menor en los pacientes que recibieron tratamiento activo que en el grupo placebo, y también fue menor que la progresión radiográfica estimada a los 6 y a los 12 meses. En el estudio MN301 la progresión en el grupo placebo fue superior a la esperada, mientras que en el estudio US301 sucedió lo contrario a los 12 meses. Esta discrepancia probablemente sea debida a que en el estudio US301 el 63% de los participantes recibió un tratamiento activo durante una media de 24 semanas, y los restantes recibieron tratamiento, fuera del protocolo, durante más de 33 semanas.
En los estudios con grupo placebo como control (US301 y MN301), el número de pacientes con progresión radiográfica, definida como un aumento en la puntuación de erosiones mayor de 3 unidades, era significativamente mayor en los grupos placebo que en los grupos con LEF (tabla 3).
El efecto sobre los cambios radiográficos de la LEF no difieren estadísticamente de los de SSZ en el estudio MN301 (p = 0,6854). En los dos estudios que comparan LEF y MTX tampoco hay diferencias significativas ni en lo concerniente a erosiones ni a DEA (p = 0,0499 en US301 y p = 0,2940 en MN302). En el estudio MN301 la progresión radiográfica a los 6 meses en el grupo placebo excede la esperada, mientras que disminuye significativamente en los grupos tratados con LEF o SSZ. A los 12 meses se mantiene esa tendencia, lo que indica que el beneficio observado a los 6 meses se mantiene posteriormente.
Para definir la relación entre progresión radiográfica y respuesta clínica se separaron los respondedores de los no respondedores de acuerdo con los criterios del American College of Rheumatology (20% ACR20). En cada grupo de los tres estudios los respondedores tienen menor progresión radiográfica, con una diferencia entre 0,8 y 3,8 unidades. Entre los dos grupos de tratamiento, la diferencia era menos llamativa (0,1-1 unidades). Esta correlación, menos fuerte de lo esperado según estudios previos, entre progresión radiográfica y respuesta ACR es consecuente con la débil asociación entre las variables clínicas y los cambios radiográficos observados durante el tratamiento.
En estos tres estudios queda patente que la LEF es efectiva para reducir la progresión del daño articular en la AR, tanto en erosiones como en disminución del espacio articular, de forma similar a los dos FAME tradicionalmente más utilizados en el tratamiento de la AR, como son MTX y SSZ. Los datos del estudio MN301 demuestran que este efecto es evidente a los 6 meses de tratamiento, lo que indica que la LEF es también un fármaco que actúa con rapidez. Por todo ello, la LEF se comporta como un fármaco modificador del daño estructural al mismo nivel que la SSZ o el MTX.
Utilizando el método de Larsen, la progresión radiográfica de la AR en tratamiento con LEF y SSZ se ha analizado en otro estudio multicéntrico europeo, doble ciego contra placebo, durante 6 meses (228 pacientes) con extensión posterior a 12 y 24 meses (136 y 65 pacientes, respectivamente), en la cual los pacientes del grupo placebo pasaban a recibir SSZ12. Los cambios en la puntuación de Larsen y el número de erosiones demuestran una progresión radiográfica significativamente menor en los tratados con LEF y SSZ que con placebo, y este retraso en la progresión se mantiene a los 24 meses. De esta manera, este estudio demuestra que la reducción de la progresión del daño estructural con LEF observada ya a los 6 meses se mantiene a más largo plazo en los pacientes que completan dos años de tratamiento (LEF: 0,92, SSZ: 0,80).
Como conclusión, se puede afirmar que la LEF es un fármaco que se incluye en el pequeño grupo de los FAME que han demostrado fehacientemente que frenan la progresión radiográfica en la AR, constituyendo una importante aportación para el tratamiento de esta enfermedad.