Introducción
La reumatología se encuentra en un gran momento. Los reumatólogos estamos disfrutando de notables avances en enfermedades tan dispares como la artrosis, la osteoporosis y la artritis reumatoide (AR). Se puede afirmar sin exagerar que tenemos la suerte de asistir a una época fascinante con importantes cambios en el seguimiento y tratamiento de las enfermedades reumáticas. Una característica de la reumatología moderna es la utilización de instrumentos de evaluación estandarizados en el seguimiento de los enfermos. Esto mismo ha ocurrido antes en otras especialidades médicas. Se trata de una necesidad ineludible si se quiere avanzar. En la actualidad, con un conjunto reequilibrado de variables podemos describir las características clínicas de los pacientes de una forma mucho más precisa, válida y sobre todo útil que antaño con el ya obsoleto: peor, igual o mejor. Es indudable que la aparición de nuevos y superiores tratamientos para la AR debe ir acompañada de la utilización de métodos clínicos más sensibles y completos, capaces de detectar las mejorías terapéuticas de una forma consistente. Entre las áreas de mayores avances en los últimos años destaca la evaluación de la calidad de vida, producto de un interés por aspectos cualitativos, centrados en el paciente, dando paso a una visión menos anatómica y más funcional de las enfermedades crónicas. En las siguientes líneas se revisan algunos conceptos básicos sobre la evaluación de la calidad de vida y los métodos más extendidos para su medición en la AR. Se pasa revista a los principales cuestionarios genéricos y específicos, haciendo especial hincapié en el Health Assessment Questionnaire (HAQ). Al final se añade un anexo donde se explica de forma detallada el procedimiento estándar de puntuación del cuestionario de discapacidad HAQ que esperamos facilite su utilización y resuelva las dudas más frecuentes.
Calidad de vida relacionada con la salud
Si nos preguntaran por nuestro nivel de calidad de vida, a buen seguro que cada uno de nosotros sería capaz de dar una respuesta más o menos ajustada a la realidad, basada en una idea más bien intuitiva del significado de calidad de vida. Sin embargo, la dificultad surge al dar un paso más y tratar de definir el concepto de calidad de vida. Enseguida se da uno cuenta de que varía con las personas, las circunstancias, los lugares y las culturas. Es más, una misma persona puede cambiar de opinión a lo largo de los años en función de su edad, estado de salud, relaciones personales o nivel adquisitivo, por citar algunos de los factores posibles. Y nadie negará que la calidad de vida también depende de factores medioambientales (clima, polución), sociales (conflictos, migraciones, guerras, entre otros), políticos (derechos, libertades) o económicos (PIB de un país) que no tienen una vinculación tan directa con la salud. Se trata, pues, de un concepto complejo, multidimensional, que no sólo guarda relación con elementos relativamente objetivos como la salud, el tipo de trabajo o el nivel socioeconómico, sino que también depende de cuestiones tan subjetivas como la escala de valores, las creencias y las expectativas de cada persona, todo ello, a su vez, integrado en un marco biográfico individual, familiar, social y medioambiental que cambia para cada persona, grupo o país. Un concepto demasiado abstracto e impreciso, carente de consenso previo sobre su significado y, por tanto, sin una base suficiente para construir una teoría o un modelo de medición.
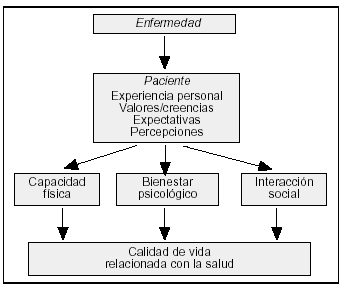
En ciencias de la salud se prefiere hablar de calidad de vida relacionada con la salud (CVRS) cuando se intenta evaluar aquélla en función del grado de salud, en un intento de acotar el problema, con una visión más realista, que huye de la ambigüedad e imprecisión, dada la imposibilidad de definir el concepto de calidad de vida1,2. Los contenidos de la CVRS se suelen dividir en tres dimensiones: física, psicológica y social, en una clara referencia a las distintas áreas en que se ha dividido el concepto de salud. Se trata de conocer cómo los estados de salud o si se prefiere, las distintas formas de enfermar modifican la calidad de vida de las personas física, piscológica y socialmente, pero desde el punto de vista del paciente (fig. 1). Muchos autores añaden una cuarta dimensión: las sensaciones somáticas, en referencia a los síntomas o experiencias desagradables relacionados con la enfermedad (dolor, rigidez, malestar, náuseas, disnea, etc.). Desde un punto de vista pragmático se podría definir la CVRS como el efecto que una enfermedad y su tratamiento tienen sobre la distintas funciones del enfermo, pero tal como lo percibe el propio enfermo.
Figura 1. Esquema conceptual de calidad de vida relacionada con la salud.
A su vez, cada una de esas dimensiones se puede dividir en subdimensiones, dominios, categorías o componentes, lo que suele depender de las preferencias de los autores en la forma de enumerarlas. Así, el dolor y la movilidad serían categorías, o dominios, de la dimensión física, mientras que la ansiedad y la depresión constituirán categorías de la dimensión psicológica. Por supuesto, se puede avanzar en el nivel de subclasificación, pero a medida que se subdividen los dominios y categorías, es cada vez mayor el grado de superposición y resulta menos clara la diferenciación entre los mismos, en especial en lo referente a las dimensiones psicológica y social. El lector debe tener presente que, a grandes rasgos, éste es el esquema seguido por los cuestionarios de CVRS; aunque con frecuencia se utilizan denominaciones diferentes para referirse a escalas o dominios que abordan conceptos idénticos o muy similares, lo que favorece cierta confusión. Esto puede parecer extraño, pero se trata de una consecuencia bastante lógica si se tiene en cuenta que los cuestionarios de CVRS más que ser el resultado de una elaborada teoría sobre el concepto de salud y su forma de medirlo surgen de necesidades de medición concretas y diferentes, transformadas en ítems, dominios, categorías o dimensiones por los investigadores en función de los intereses operativos de cada momento3-5; esto no significa que los cuestionarios carezcan de bases conceptuales, sino que se trata de las respuestas dadas por los distintos creadores a una realidad más que a una teoría.
Importancia
En los dos últimas décadas se ha producido un rápido crecimiento de la producción científica en el área de la CVRS. Las razones de este llamativo interés son diversas. Por un lado, el aumento de la prevalencia de las enfermedades crónicas como consecuencia de un envejecimiento de la población y más altos niveles de bienestar, seguido de una mayor sensibilidad por conocer el punto de vista del propio enfermo sobre su estado de salud ante procesos que carecen de curación y cuyo principal objetivo puede ser la mejoría de la calidad de vida. En cierto sentido, es el resultado de una humanización de la atención sanitaria, pero también el fruto de un deseo de aumentar el conocimiento sobre la historia natural de estos procesos y establecer su interrelación con factores pronósticos. Por último, los avances tecnológicos, acompañados de un rápido incremento en el gasto sanitario, han motivado una mayor preocupación por la evaluación de los nuevos tratamientos y tecnologías, desde el punto de vista del individuo y de la sociedad, para contar con mejores elementos de juicio ante la toma de decisiones en planificación sanitaria. Bajo todos esos planteamientos subyace una idea: toda atención sanitaria, además de aliviar los síntomas y prolongar la supervivencia, debe mejorar la calidad de vida y el bienestar de las personas.
Evaluación
Los cuestionarios son el método convencional de medir de forma operativa la CVRS. Se parte de la base de que el mejor informador es el propio sujeto, por lo que estos instrumentos facilitan información sobre salud autopercibida. Esta subjetividad ha sido tenida por muchos cada vez menos como uno de sus puntos débiles («datos blandos»), lo que no deja de ser un reflejo de cierto desconocimiento de los problemas de medición que plantean muchos de los considerados «datos duros». Por otra parte, ¿de qué otra forma se podría evaluar la CVRS? ¿Quién mejor que el propio enfermo para explicar cómo su enfermedad afecta a su calidad de vida? Otras opciones basadas en la observación o el juicio de terceras personas no son menos complejas ni están exentas de problemas. Además, se ha demostrado que los valores y preferencias que los pacientes y los médicos priorizan en esta materia pueden diferir bastante6.
Los cuestionarios son instrumentos de medición, compuestos por preguntas agrupadas (ítems) en una o más escalas que aportan información sobre los componentes de la salud. Como ya se ha dicho, existe cierta arbitrariedad en la elección del término escala, dominio, categoría, componente bajo el cual se agrupan los ítems que evalúan un constructo específico (p. ej., desplazamiento, cuidado personal, rol social o distrés psicológico). Es indudable que la presencia de dolor, discapacidad, ansiedad o limitación en la interrelación social son consecuencias importantes de la enfermedad que reducen la calidad de vida y modifican el pronóstico. Otra cuestión es cómo medir estos constructos de una forma válida y fiable.
Los autores tratan de capturar dicha información de la forma más sencilla posible mediante la utilización de ítems y escalas que evalúan cuestiones relacionadas con actividades frecuentes de la vida diaria y que han demostrado su relevancia con respecto al concepto que se intenta medir. Por tanto, tras una apariencia relativamente sencilla, a menudo se esconde una compleja y prolongada elaboración destinada a obtener el mejor instrumento de medida que permita conseguir el objetivo propuesto. Los cuestionarios de CVRS evalúan aspectos de la salud relevantes para el enfermo, el clínico, el investigador o el gestor de los servicios sanitarios, que no se pueden medir de otra forma y que van más allá del ámbito biológico, fisiológico o clínico, evaluado con otras técnicas Las características métricas de un cuestionario vienen dadas por su fiabilidad, validez y sensibilidad al cambio. Si bien su eficacia y cualidades métricas se han puesto de manifiesto en numerosas investigaciones, su uso no está exento de críticas3,5,7. En la actualidad se han convertido en herramientas imprescindibles para la evaluación de la salud en grupos de población, la medición del impacto de las enfermedades crónicas o la evaluación de nuevos tratamientos1,8-10.
Conviene no confundir los cuestionarios de CVRS, verdaderos instrumentos de medición con características psicométricas bien conocidas, con los cuestionarios utilizados en las encuestas u otros tipos de estudios epidemiológicos o clínicos, de validez menos contrastada y que obedecen a objetivos de otra índole como, por ejemplo, la recogida sistemática de datos.
Los cuestionarios de CVRS, en función de sus objetivos, se suelen clasificar en dos grandes grupos: cuestionarios genéricos de salud y cuestionarios específicos para enfermedades o situaciones concretas11.
Cuestionarios genéricos
Proporcionan una estimación del estado de salud físico, psicológico y social, autopercibido por el sujeto, basándose en diferentes ítems sobre actividades, sentimientos y emociones que abarcan un gran número de situaciones de la vida diaria. Predomina, por tanto, el componente subjetivo. Los ítems agrupados en escalas, dominios o categorías varían de un cuestionario a otro, pero finalmente permiten obtener una puntuación para la salud física, psicológica y social. En ocasiones la información de todo el cuestionario se puede resumir en una única puntuación, a menudo denominada índice. Dado que permiten obtener una imagen del nivel de salud de una población, también se les conoce como perfiles de salud. Entre sus ventajas cabría citar que permiten describir el grado de salud de grupos de población o de enfermos, con una misma o diferentes enfermedades, y compararlos entre sí, o evaluar el resultado de una intervención: un nuevo fármaco, un programa de ejercicios, una estrategia de prevención.
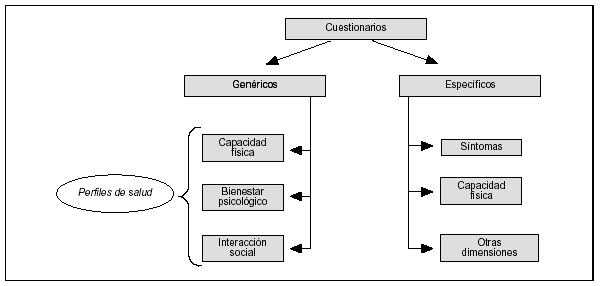
A diferencia de los cuestionarios específicos, los cuestionarios genéricos no están orientados a ninguna enfermedad en particular (fig. 2). Precisamente por ello no incluyen síntomas en sus escalas, con la excepción del dolor común a toda dolencia; de ahí que sean menos sensibles a los cambios de la enfermedad, puestos de manifiesto con variaciones de los síntomas que habitualmente sí recogen los cuestionarios específicos. En este sentido suelen tener un contenido cuya apariencia es de menor relevancia para el clínico, en especial si se comparan con los cuestionarios específicos, aunque proporcionan información complementaria. Además, suelen ser algo más largos y más complejos de administrar, lo que va seguido de cierta dificultad en su interpretación. A su favor está que ofrecen una visión más global del estado de salud al incorporar el efecto de la morbilidad asociada y permiten comparar diferentes procesos entre sí.
Figura 2. Diferencias entre cuestionarios genéricos y específicos.
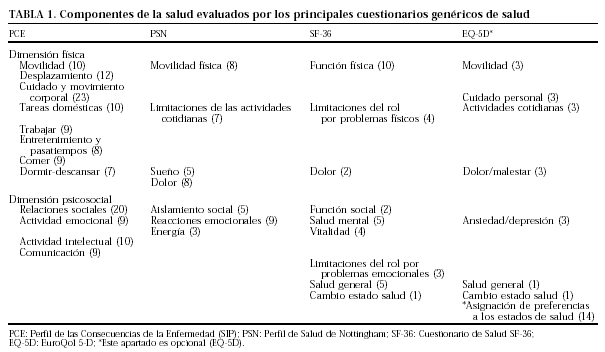
Entre los perfiles de salud de uso más extendido cabe citar el Perfil de las Consecuencias de la Enfermedad (Sickness Impact Profile), el Perfil de Salud de Nottingham (Nottingham Health Profile), el Cuestionario de Salud SF-36 (Short-Form-36) y el European Quality of Life Measure (EuroQol 5-D). Todos cuentan con una versión adaptada de forma rigurosa a nuestro país12-15. En la tabla 1 se resumen las principales características de estos cuestionarios. Se puede encontrar información adicional en revisiones recientes16,17.
Es importante comprender que el contenido de un cuestionario depende de su objetivo y las bases conceptuales sobre las que se ha construido. Para el profano es fácil caer en la tentación de juzgar por igual todos los cuestionarios de salud, como si se trataran de herramientas equiparables con idénticas finalidades y funciones. Nada más lejos de la realidad. Para entender las diferencias que existen entre ellos es fundamental prestar atención al objetivo de cada uno. En este sentido puede ser de interés intentar conocer las circunstancias o los retos que trataron de afrontar los autores con la creación de un nuevo cuestionario. En cualquier caso, una comparación detallada de los mismos permitirá establecer las diferencias.
Valoración de los cuestionarios genéricos en la artritis reumatoide (tabla 1). Los cuestionarios genéricos de CVRS han demostrado ser válidos en el estudio de los enfermos con AR.
El Perfil de las Consecuencias de la Enfermedad (PCE), por ser el más antiguo, fue utilizado en primer lugar con éxito en la AR18,19. La información que proporciona es muy completa, pero su extensión 136 ítems agrupados en 12 categorías lo convierten en inviable para su uso clínico, por lo que queda relegado a la investigación.
El Perfil de Salud de Nottingham (PSN) consta de dos partes. La primera contiene 38 ítems, de respuesta sí/no, agrupados en 6 categorías: energía, dolor, movilidad física, reacciones emocionales, sueño y aislamiento social13,20,21. La segunda incluye siete ítems, también de respuesta sí/no, sobre limitación funcional en 7 actividades de la vida diaria. Houssien et al22 estudiaron el comportamiento de la primera parte del PSN en un estudio transversal con 200 pacientes consecutivos y su relación con las variables de actividad incluidas en el conjunto mínimo de parámetros se incluyeron el Disease Activity Score (DAS) y el HAQ. Los resultados presentaron diferencias significativas en todas las subescalas del PSN entre los pacientes agrupados en tres niveles de actividad, según valores del DAS. Así, las personas con mayor actividad inflamatoria tenían peores puntuaciones para las escalas de dolor, sueño, movilidad, energía, reacciones emocionales o aislamiento social. Estos datos apoyan la capacidad discriminativa del cuestionario en relación con el grado de actividad de la enfermedad. Estos autores prefirieron el PSN al SF-36 o el EuroQoL, por presentar unos ítems redactados en lenguaje muy sencillo, de la calle, de fácil comprensión y respuesta (ítems de respuesta sí/no). Las características de este cuestionario facilitan su uso en la clínica diaria, aunque es algo menos sensible al principio de la enfermedad.
El EuroQol-5D (EQ-5D) consta de tres partes. La primera permite evaluar el estado de salud a través de 5 dimensiones: movilidad, cuidado personal, actividades cotidianas, dolor/malestar y ansiedad/depresión15,23. Cada una tiene tres ítems que definen tres niveles de gravedad sin problemas, con algunos problemas, con muchos problemas, con lo que es posible obtener 243 estados de salud diferentes (3 ×3 × 3 ×3 × 3). El enfermo sólo tiene que escoger en cada dimensión el ítem que mejor refleja su estado de salud. La información de esta parte es equivalente a un cuestionario genérico de salud. La segunda parte facilita una puntuación global del estado de salud mediante una escala análoga visual milimetrada vertical termómetro de 200 mm cuyos extremos indican: 0, peor estado de la salud imaginable, y, 100, mejor estado de salud imaginable. La tercera parte, más compleja, incluye 14 estados de salud diferentes que el individuo deberá evaluar para conocer los valores asignados por él a cada estado. También se pueden aplicar los valores obtenidos en muestras estándar de la población. Este último apartado corresponde a un cuestionario de utilidad y se utiliza en estudios económicos de coste-efectividad. La primera y segunda parte son las de mayor uso por su sencillez.
Hurst et al24 evaluaron en un amplio estudio las características métricas de las tres partes del EQ-5D en 233 pacientes con AR. Observaron unos valores adecuados de fiabilidad, validez y sensibilidad al cambio, sobre todo para la escala visual análoga global y el módulo de utilidad. Sin embargo, Wolfe y Hawley25, en un estudio publicado el mismo año, manifestaron serias dudas sobre la validez de este cuestionario en pacientes con AR, aunque estos autores usaron pesos obtenidos de la población general sana para calcular el módulo de utilidad.
El Cuestionario de Salud SF-36 (SF-36) consta de 35 ítems agrupados en 8 categorías: función física, limitaciones del rol por problemas físicos, dolor, percepción de la salud general, vitalidad, función social, limitaciones del rol por problemas emocionales y salud mental; cada una de las cuales proporciona una puntuación individual14,26,27. Un ítem adicional evalúa el cambio de salud en el tiempo. Las 8 categorías se pueden resumir en dos escalas: una física y una mental, con una puntuación para cada una de ellas27, pero no se puede obtener un índice global para todo el cuestionario. La puntuación final de las 8 categorías del cuestionario se basa en algoritmos complejos que precisan de un programa informático para su cálculo.
Ruta et al28 evaluaron las características psicométricas del SF-36 en la misma población utilizada para evaluar el EQ-5D24. Observaron una buena fiabilidad en cada una de sus 8 categorías y también una aceptable validez en 6 de ellas, con excepción de dos: limitaciones del rol por problemas físicos y limitaciones del rol por problemas emocionales y salud mental. El comportamiento de las dos escalas resumen, física y mental, fue igualmente correcto. Posteriormente se han realizado muchos estudios que permiten afirmar que el SF-36 es el cuestionario genérico de CVRS más ampliamente utilizado en reumatología.
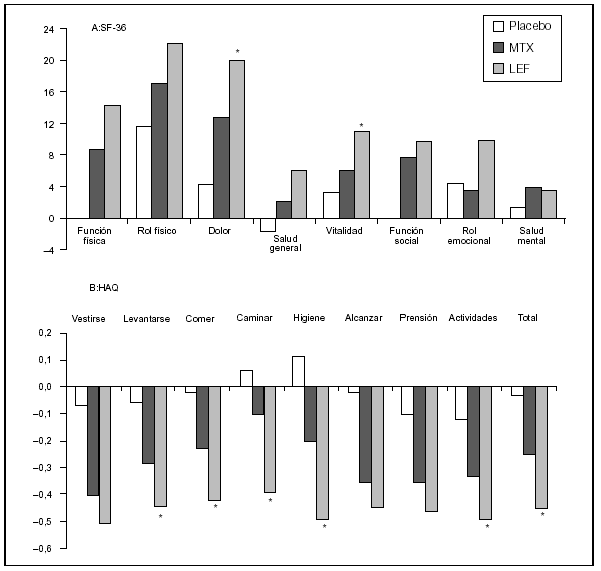
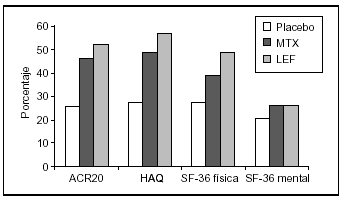
Consideraciones prácticas. Las dudas iniciales sobre la utilidad de los cuestionarios genéricos de CVRS, sobre todo respecto a su sensibilidad29, resultado de los escasos estudios realizados hasta 1997, se han ido disipando gracias a la intensa investigación llevada a cabo en los últimos 5 años30,31. Los ensayos clínicos más recientes sobre terapias biológicas y leflunomida han demostrado la capacidad de detectar cambios de estos instrumentos y la importancia de la información complementaria que aportan. A partir de ahora cualquier fármaco nuevo con efecto modificador de la enfermedad deberá demostrar su eficacia en la mejoría de la CVRS. A modo de ejemplo, en la figura 3 se exponen los resultados de comparar la eficacia de leflunomida, metotrexato y placebo en la CVRS medida con el SF-36 a los 12 meses de tratamiento32,33. La leflunomida no sólo presentó una clara superioridad frente a placebo, sino que demostró una mejoría significativa frente a metotrexato en las categorías de dolor y energía.
Figura 3. Mejoría en cada una de las 8 categorías del SF-36 (A) y cada una de las 8 áreas del HAQ (B) tras 12 meses de tratamiento con placebo, metotrexato (MTX) o leflunomida (LEF). Las barras representan diferencia media (valor final menos valor basal). En el SF-36 los valores positivos indican mejoría. En el HAQ los valores negativos indican mejoría. Análisis por intención de tratar. *P < 0,05 leflunomida frente a metotrexato. Modificada de Strand et al32.
Las recomendaciones sobre la utilización de estos cuestionarios van más allá de los ensayos clínicos, siendo deseable su uso en estudios observacionales34. Debe tenerse en cuenta que la CVRS y las alteraciones radiológicas pueden ser las únicas variables capaces de detectar cambios a largo plazo; mientras que los indicadores de actividad inflamatoria VSG, recuentos articulares, DAS fluctúan e incluso mejoran, la discapacidad física, la interacción social, o el daño radiológico tienden a aumentar y acumularse35.
Los cuestionarios genéricos permiten comparar poblaciones diferentes entre sí. Por ejemplo, en el ensayo de leflunomida se compararon las puntuaciones de los enfermos con AR y la población sana norteamericana32. Así se pudo comprobar que los enfermos con AR presentaban peores niveles de CVRS en todas las categorías del SF-36, con una diferencia más acentuada en las categorías del componente físico de la salud: limitaciones del rol por problemas físicos, dolor, función física y vitalidad. Los cuestionarios genéricos también permiten analizar el perfil de salud de distintas enfermedades (se ha comparado el perfil de salud de los pacientes con AR y lupus eritematoso sistémico36, artritis psoriásica37, artrosis y fibromialgia25, así como comparar el impacto de la AR con el de otras enfermedades crónicas38.
Aunque ningún cuestionario genérico ha demostrado una clara superioridad sobre los demás, la realidad pone de manifiesto que el SF-36 se ha impuesto en la mayoría de los estudios39. Cuando el lector desee elegir un cuestionario de CVRS, conviene tener presente las razones que motivaron su creación y el objetivo para el que fue diseñado, sus características psicométricas, los resultados previos en otros estudios y la opinión de los expertos17,40. A menudo aspectos como la facilidad de comprensión de los enfermos a los que irá dirigido el cuestionario, los recursos disponibles tiempo, disponibilidad de personal de apoyo para la cumplimentación, facilidad de puntuación y gestión electrónica o la experiencia previa del equipo investigador condicionarán la elección.
Cuestionarios específicos
Los cuestionarios específicos para enfermedades reumáticas están centrados en la enfermedad y, por tanto, incluyen las dimensiones de la salud más afectadas por dichas dolencias, en especial la dimensión física, y dentro de ésta la discapacidad y el dolor (fig. 2). En algunos cuestionarios se abordan, además, aspectos psicológicos (ansiedad y depresión) y sociales (interrelación social).
El HAQ es el instrumento específico para enfermedades reumáticas más conocido por los reumatólogos. La experiencia con este cuestionario es amplísima. Se ha aplicado a casi todo tipo de procesos con buenos resultados y numerosos estudios han demostrado su fiabilidad, validez y sensibilidad al cambio41. Conviene recordar que el HAQ completo es un cuestionario muy extenso que incluye 5 dimensiones: malestar, discapacidad, toxicidad por fármacos, coste económico y muerte42-44. Su creación se basó en un modelo elaborado por Fries a principios de los ochenta para evaluar el impacto o desenlace (outcome) de las artritis crónicas42,45, basado en el punto de vista de los enfermos, y que se puede considerar todavía vigente. Los enfermos desean, en primer lugar, permanecer con sus funciones normales; en segundo lugar, no tener dolor ni otros síntomas de carácter físico, psicológico o social; tercero, no sufrir ninguna iatrogenia como consecuencia del tratamiento; cuarto, permanecer económicamente solventes a pesar de la enfermedad, y por último vivir el mayor tiempo posible. Por tanto, este modelo divide el desenlace en 5 dimensiones, también denominadas «cinco D»: malestar (discomfort), discapacidad (disability), fármacos (drugs), coste (dollars) y muerte (death). A su vez, cada una de ellas se puede dividir en subdimensiones y éstas en componentes (tabla 2). Por ejemplo, la dimensión malestar se puede dividir en física y psíquica. En la subdimensión física se incluirían el dolor y el cansancio, mientras que en la psíquica cabrían la depresión y la ansiedad. Es interesante que ninguna de estas dimensiones implica la realización de pruebas complementarias, radiografías o exploraciones físicas44. Las variables consideradas de desenlace están relacionadas con la evolución de la enfermedad y, por tanto, adquieren mayor importancia a medida que pasa el tiempo.
La popularidad alcanzada por la escala de discapacidad ha convertido la denominación HAQ en sinónimo de la misma, pasando a un segundo plano el resto de los componentes. El cuestionario de discapacidad del HAQ consta de 20 ítems que evalúan el grado de dificultad (discapacidad física) autopercibida para realizar 20 actividades de la vida diaria agrupadas en 8 áreas: vestirse y asearse, levantarse, comer, caminar/pasear, higiene personal, alcanzar, prensión y otras actividades42,43. En el anexo, al final del artículo, se hace una descripción más detallada del cuestionario y se especifica su forma de puntuación. El HAQ se puede administrar de forma autoaplicada, si bien con frecuencia el enfermo puede necesitar de cierta ayuda. El tiempo necesario para su cumplimentación varía entre 5 y 10 min. Existe una versión adaptada a nuestro país46.
Se han utilizado otros cuestionarios como HAQ Modificado (Modified Health Assessment Questionnaire, MHAQ), que es una versión reducida del HAQ, con solo 8 ítems, uno de cada área47,48. Utiliza el mismo tipo de escala (Likert, de 4 niveles) que el HAQ y se puntúa como el valor medio de los 8 ítems. Aunque el MHAQ deriva del HAQ, la información que proporciona no es comparable. La versión española del MHAQ pudo ser autoaplicada por la mayoría de una muestra de pacientes con AR49. Su principal ventaja es su sencillez, lo que facilita su uso sistemático en el seguimiento de pacientes. Sin embargo, esa ventaja constituye su principal inconveniente, pues aporta menos información que el HAQ estándar y plantea problemas psicométricos50. Sus autores han aumentado el número de ítems para mejorar las características del cuestionario51.
El Arthritis Impact Measurement Scales (AIMS) es un cuestionario más completo que, además de la capacidad funcional y el dolor, evalúa aspectos psicológicos y sociales. Consta de 45 ítems agrupados en 9 escalas: movilidad, actividad física, destreza, actividades del hogar, actividades de la vida diaria, ansiedad, depresión, interacción social y dolor52. El AIMS puede cumplimentarse de forma autoaplicada como el HAQ, pero precisa de más tiempo, unos 20 min, y su corrección es más compleja. A principios de los noventa los mismos autores, tras realizar una profunda revisión del cuestionario, crearon el AIMS253. Se añadieron tres nuevas escalas función del brazo, trabajo y apoyo social, con un total de 12 escalas, se modificaron los nombres de las antiguas escalas para evitar confusiones, se estandarizaron las respuestas de los ítems y el marco temporal al último mes. Esta parte central contiene 57 ítems. Se agregaron secciones para evaluar la satisfacción, los problemas atribuidos a la artritis y la autoasignación de áreas prioritarias en las que mejorar. Posteriormente se ha propuesto una forma reducida del AIMS2; el AIMS2-SF (Short-form), que aportaría información similar pero de forma más eficiente54. En los últimos años se han creado algunos cuestionarios específicos para la AR55,56 que intentan de forma sencilla evaluar la CVRS de estos pacientes.
Valoración de los cuestionarios específicos en la AR. Los cuestionarios específicos tienen por objeto evaluar las consecuencias más inmediatas de la AR y que más preocupan al enfermo: la discapacidad física y el dolor. La experiencia disponible demuestra que consiguen esa meta57. Características como la fiabilidad o la validez, de criterio o de constructo, han quedado probadas en numerosos estudios42,46,58,59. De igual forma su capacidad de detectar cambios, no sólo en los ensayos, sino también en el ámbito clínico, ha sido confirmada57. Los ensayos clínicos realizados con leflunomida mostraron una mejoría en la puntuación global del HAQ y en cada una de las 8 áreas que lo forman (fig. 3), con un porcentaje de respondedores similar al observado en otras variables (fig. 4)32. Es más, la evaluación de la eficiencia relativa de las distintas variables demostró que el HAQ fue tan eficiente como el número de articulaciones tumefactas en su capacidad para detectar cambios entre metotrexato y placebo (fig. 5)33. En el grupo tratado con leflunomida, la evaluación de la eficiencia relativa ofreció aún mejores resultados para el HAQ, ocupando el segundo lugar después de la evaluación global de la enfermedad efectuada por el enfermo33. Aunque existen discrepancias, y es muy importante contar con experiencia propia, se ha señalado que en la práctica clínica diaria una variación de dos pasos en la escala del HAQ (el HAQ se puntúa en una escala de 0 a 3 graduada en pasos de 0,125), es decir, una variación de 0,250 puntos equivaldría a un cambio real57. Algunos autores han puesto en duda esta cifra elevándola a 0,31 para tener una confianza del 80% de que el cambio es real, o de 0,500 para una confianza del 95%60. En respuesta al trabajo anterior, los autores del HAQ consideran que se trata de una variación excesiva que equivaldría a pedir un cambio de 10 articulaciones tumefactas o una variación de 40 mm en la VSG para considerarlas reales, según sus propios análisis61. Al igual que en la interpretación de otros parámetros, es fundamental poseer una mínima experiencia con el HAQ para poder interpretar sus resultados, y siempre en el contexto del enfermo, y no de forma aislada, sino conjuntamente con otras variables.
Figura 4. Mejoría ≥ 20% en diferentes cuestionarios de calidad de vida tras 12 meses de tratamiento con placebo, metotrexato (MTX) o leflunomida (LEF). Las barras representan porcentajes de respondedores (mejoría ≥ 20%) en el HAQ, la escala física del SF-36 y la escala mental del SF-36, y ACR20. Valores tomados de Strand V et al32.
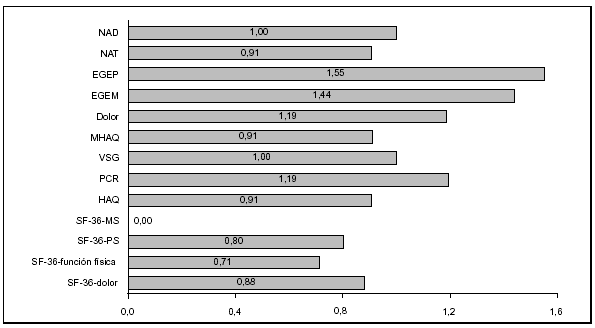
Figura 5. Eficiencia relativa de las variables de evaluación clínica utilizadas en el grupo tratado con metotrexato frente a placebo. Se toma como referencia el número de articulaciones dolorosas (NAD). Los valores más altos indican mayor capacidad de la variable de encontrar diferencias entre metotrexato y placebo. NAT: número de articulaciones tumefactas; EGEP: evaluación global de la enfermedad efectuada por el paciente; EGEM: evaluación global de la enfermedad efectuada por el médico; SF-36-MS: escala mental del SF-36; SF-36-PS: escala física del SF-36. Modificada de Tugwell P et al33.
Figura 6. Versión española del Health Assessment Questionnaire (HAQ) traducida y adaptada por J. Esteve-Vives, E. Batlle-Gualda, A. Reig y Grupo para la Adaptación del HAQ a la Población Española.
Por último, conviene tener presente que durante el seguimiento clínico de los enfermos el HAQ puede ser la única variable capaz de detectar cambios a largo plazo (5 o 10 años) cuando otras no varían o incluso mejoran62.
Es evidente que un objetivo básico del tratamiento es prevenir y evitar la aparición de discapacidad. La relevancia para el enfermo y el clínico de la discapacidad física convirtieron su evaluación en un elemento más del conjunto mínimo de parámetros recomendados en la evaluación de los enfermos con AR incluidos en los ensayos clínicos, y base de los criterios de mejoría individual definidos por el American College of Rheumatology63,64. Posteriormente estas recomendaciones se ampliaron en la conferencia OMERACT IV al campo de los estudios observacionales34. Las recomendaciones realizadas en nuestro país por un grupo de expertos de la Sociedad Española de Reumatología sobre el tratamiento con terapias biológicas van más allá e incluyen la evaluación de la discapacidad física y el dolor entre los parámetros recomendados para el seguimiento de estos enfermos65. En esta misma línea cabe ver las recomendaciones de la primera Guía de Práctica Clínica publicada por la Sociedad Española de Reumatología para el tratamiento de la AR, que también aconseja la evaluación sistemática de la discapacidad física y el dolor66. A pesar de su relevancia, la mayoría de los reumatólogos no incluyen estas variables en su evaluación clínica habitual. Así Wolfe y Pincus, basándose en los datos de una encuesta realizada a 645 reumatólogos de Estados Unidos, afirmaban que, si bien la mayoría de las personas acuden al reumatólogo por dolor, discapacidad, cansancio o estrés psicológico, menos del 15% de los reumatólogos recogen de forma cuantificada esa información57. En nuestro país, en una encuesta realizada por Enrique Batlle y Alejandro Balsa (datos no publicados) durante el Congreso de la Sociedad Española de Reumatología en un taller de evaluación clínica de la AR, más del 95% de los reumatólogos manifestaron utilizar la VSG proteína C reactiva (PCR), la rigidez matutina y los recuentos articulares, un 64% el dolor y el 46% el HAQ, en su práctica habitual. Estos últimos datos son alentadores, aunque deben contemplarse con cautela pues se obtuvieron de clínicos muy motivados e indican un aumento del interés por la utilización de estos instrumentos en la práctica clínica diaria, dejando de ser sólo una herramienta de investigación.
Consideraciones prácticas. Un aspecto novedoso que se ha destacado en los últimos años es la relación entre HAQ, actividad inflamatoria y daño estructural. Para muchas personas la idea de discapacidad va asociada a lesión anatómica y daño estructural; sin embargo, hoy día se sabe que la discapacidad es el resultado de múltiples factores, siendo la actividad inflamatoria de la enfermedad el más importante de ellos. Factores como el dolor, la fatiga o el número de articulaciones tumefactas son determinantes más importantes que el daño radiográfico en el grado de discapacidad. Drossaers-Baker et al67 estudiaron la evolución de la capacidad funcional (HAQ), la actividad inflamatoria (DAS) y el daño radiográfico (método de Sharp) en 132 mujeres con AR de inicio prematuro seguidas durante 12 años. Observaron un deterioro radiográfico progresivo y constante a lo largo de todo el seguimiento, pero con fluctuaciones en el DAS y el HAQ. Las variaciones en el DAS explicaron mucho mejor los cambios del HAQ que el deterioro radiográfico. Al inicio de la enfermedad, la correlación entre HAQ e índice de Sharp fue muy débil, aunque con el tiempo (a los 6 y 12 años) fue mejorando pero sin superar al DAS. En definitiva, HAQ y DAS presentan una relación mucho más estrecha que HAQ y daño radiográfico. Hallazgos parecidos han sido descrito por varios autores68,69. Esto explica por qué el HAQ puede alcanzar valores muy altos al principio de la enfermedad para luego mejorar con el tratamiento y más adelante aumentar de forma gradual a medida que aparece el deterioro estructural69. Otros trabajos han puesto de manifiesto que la relación entre daño estructural y discapacidad (HAQ) es mejor a partir de los 7-8 años de evolución; aun así el daño radiográfico sólo alcanza a explicar el 25% de la variabilidad del HAQ68,70. Cuando se han analizado otros determinantes de la discapacidad, aparecen de forma sistemática factores de carácter psicosocial, que en las primeras fases de la enfermedad no deberían despreciarse, y que explican una parte significativa de la varibilidad del HAQ67,69,71,72.
Los estudios también demuestran que un tratamiento temprano y secuencial con fármacos modificadores de la enfermedad comporta una mejor capacidad funcional en comparación con estrategias previas asociadas a mayor discapacidad73-77. A su vez, el valor del HAQ al inicio de la enfermedad es capaz de predecir la evolución posterior mejor que otras variables57. Por ejemplo, los datos del estudio ERAS Early Rheumatoid Arthritis Study demostraron que una peor capacidad funcional (clase funcional III-IV) a los 5 años de seguimiento estuvo asociada con ser mujer y con un HAQ > 1 en el momento de acudir el enfermo por primera vez78. En la misma línea, la remisión fue más probable en los varones y en los pacientes con HAQ basal < 1. Todos estos datos apoyan la utilización en la práctica clínica diaria de los cuestionarios, que además de ser instrumentos muy eficientes para el seguimiento de los enfermos, son una valiosa fuente de información en estudios observacionales tan decisivos en el conocimiento de enfermedades crónicas como la AR35.