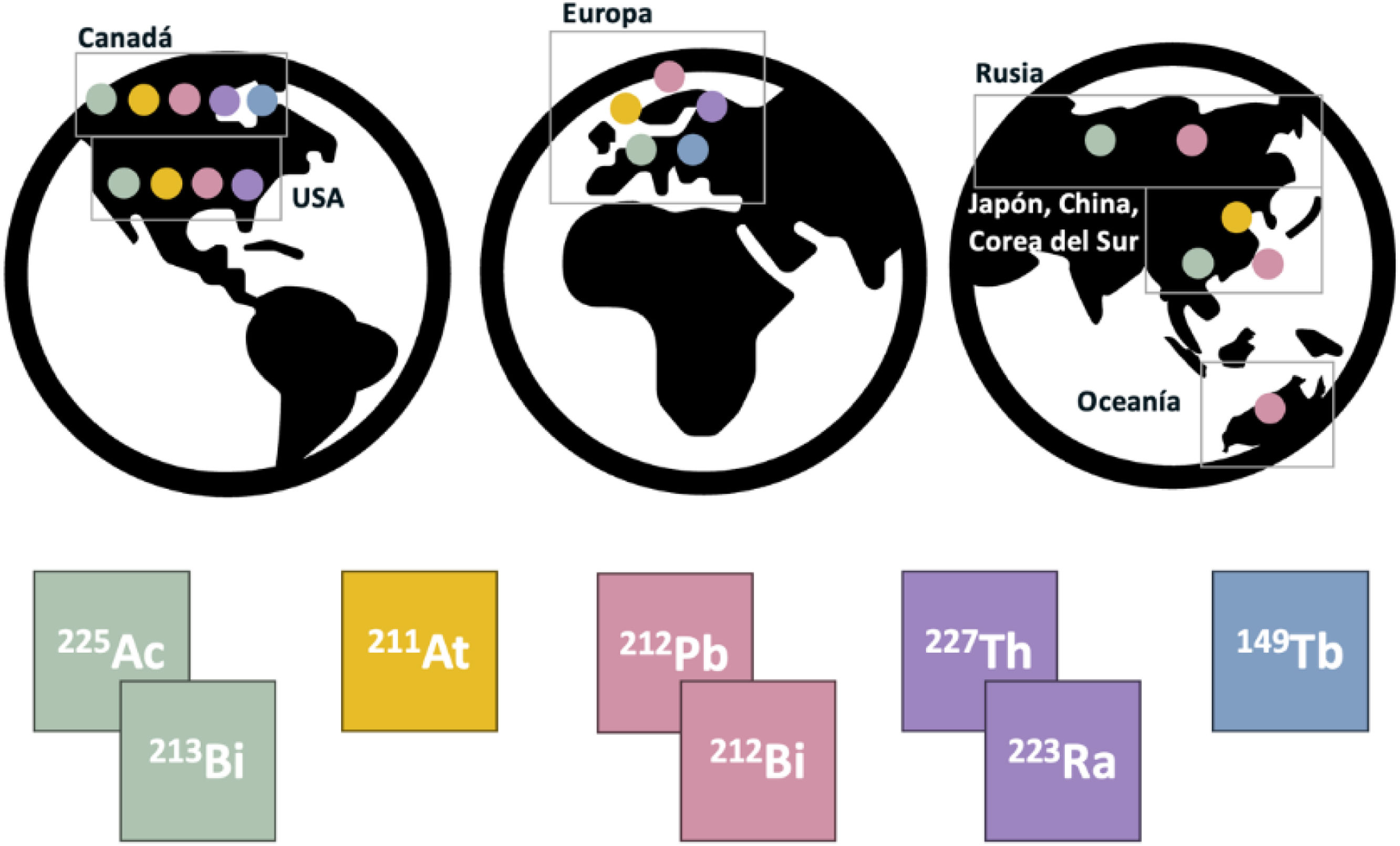
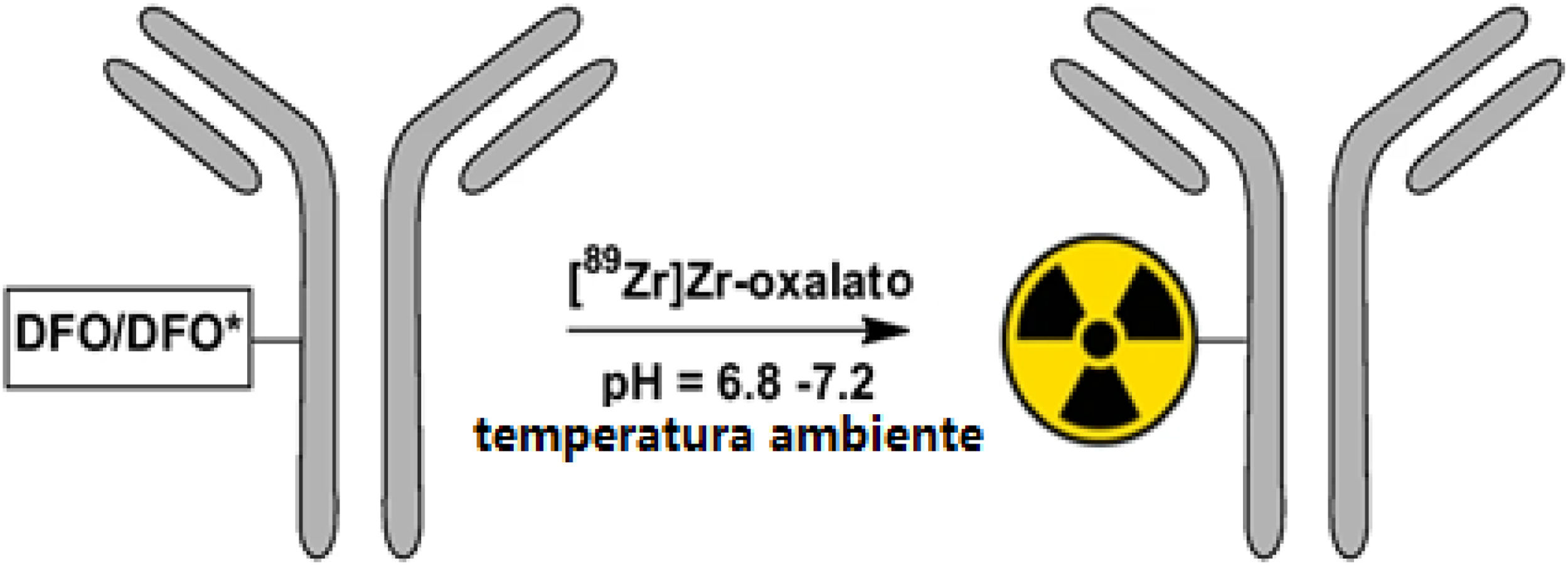
En esta tercera entrega de la serie de formación continuada, se analizan en profundidad las aplicaciones clínicas y terapéuticas del zirconio, astato y torio. Aunque no se describen como pares teragnósticos, cada uno de los radionúclidos descritos está jugando un papel fundamental dentro de la medicina de precisión, que evoluciona dando pasos agigantados en la Medicina Nuclear. Empezamos analizando el zirconio-89, emisor de positrones, cuya vida media larga lo hace interesante para unirlo a moléculas grandes con cinética lenta, como los anticuerpos, con un papel fundamental en la inmunoterapia. Se describe el uso del radioisótopo astato-211, que presenta un esquema de desintegración alfa sencillo y un comportamiento químico similar al del yodo; su principal reto es la producción, ya que se necesitan ciclotrones que produzcan haces de partículas alfa muy energéticos. Asimismo se revisa el torio-227, un emisor alfa (100%) que tiene gran facilidad para ser quelado y permite el radiomarcaje de partes dirigidas al tumor para producir conjugados de torio dirigidos. Esta técnica está mostrando resultados preclínicos muy interesantes, aunque el uso del torio tiene la limitación de la posible separación del radio-223 de la molécula y la medida en el activímetro depende del momento de producción, ya que tarda 100 días en llegar al equilibrio y las medidas de actividad se basan en fotones provenientes de los radionúclidos hijos.
A pesar de los retos a los que nos enfrentamos, estos radionúclidos están impulsando la evolución de la medicina de precisión y ampliando las posibilidades terapéuticas y diagnósticas en Medicina Nuclear.
In this third installment of the continuing education series, the clinical and therapeutic applications of zirconium, astatine and thorium are analyzed in depth. Although they are not described as theragnostic pairs, each of these radionuclides plays a fundamental role in precision medicine, which is rapidly advancing within Nuclear Medicine.
We begin by analyzing zirconium-89, a positron emitter whose long half-life makes it particularly suitable for labeling large molecules with slow kinetics, such as antibodies, playing a crucial role in immunotherapy. The use of astatine-211, an alpha-emitting radionuclide with a simple decay scheme and chemical behavior similar to iodine, is also discussed. Its main challenge lies in its production, as it requires cyclotrons capable of generating highly energetic alpha particle beams. Furthermore, thorium-227, a 100% alpha emitter, is reviewed. This radionuclide exhibits excellent chelation properties, enabling its conjugation with tumor-targeting molecules to produce thorium-labeled conjugates. While this technique is yielding promising preclinical results, the use of thorium faces challenges, including the potential separation of radium-223 from the molecule and the dependence of activity measurements on the time of production. Since it takes 100 days to reach equilibrium, activity assessment is based on photons emitted by its daughter radionuclides.
Despite these challenges, these radionuclides are driving the evolution of precision medicine, expanding therapeutic and diagnostic possibilities within Nuclear Medicine.
Nuclear Medicine.
Artículo
Si tiene problemas de acceso puede contactar con la Secretaría Técnica de la SEMNIM en el correo electrónico secretaria.tecnica@semnim.es o en el teléfono: + 34 619 594 780