Los fármacos anticolinérgicos reducen la eficacia de los inhibidores de la acetilcolinesterasa (IACE) y se consideran inapropiados en pacientes de edad avanzada. El objetivo fue conocer la prevalencia de prescripción concomitante de IACE y anticolinérgicos en un Área de Salud, identificar pacientes afectados e informar a los médicos responsables para que valorasen la idoneidad de los tratamientos.
Material y métodosEstudio descriptivo transversal y observacional de prevalencia. Se seleccionó a pacientes en tratamiento con IACE y algún fármaco anticolinérgico en el primer trimestre de 2015. Para la identificación de anticolinérgicos, se utilizó como referencia la revisión de Durán et al., asignando una puntuación a cada fármaco en función de su potencia anticolinérgica. Se proporcionó a cada médico una nota informativa sobre la interacción, relación de pacientes afectados y recomendaciones.
ResultadosSe incluyó a 486 pacientes, lo que supone el 59,0% sobre el total de pacientes con enfermedad de Alzheimer del área. El 66,0% eran mujeres, el 86,8% mayores de 75 años, con una media de 9,2 fármacos/paciente. El número medio de fármacos anticolinérgicos fue 1,6; el 38,3% de los pacientes tenían prescritos varios fármacos anticolinérgicos y el 23,9% algún fármaco de alta potencia anticolinérgica. Se encontró asociación estadísticamente significativa entre tomar IACE y anticolinérgicos de forma concomitante (p=0,000; OR: 3,9).
ConclusionesLa prevalencia de interacción entre IACE y anticolinérgicos es relevante, considerando que además afecta a población vulnerable. Proporcionar a los médicos información sobre la interacción podría ayudar a la toma de decisiones clínicas, mejorar la seguridad y los resultados en salud de los pacientes.
Anticholinergic drugs reduce the efficacy of acetylcholinesterase inhibitors (AChEI) and are inappropriate in elderly patients. The aim of this study is to determine the prevalence rate of prescription AChEI drugs and anticholinergics in a Healthcare Area, to identify the affected patients, and to inform the attending physicians, in order to evaluate the suitability of treatments.
Material and methodsA descriptive cross-sectional observational study of prevalence. Patients on treatment with AChEI and any anticholinergic drug in the first quarter of 2015 were selected. The review of Duran et al. was used as reference to identify anticholinergics, assigning a score to each drug according to its anticholinergic potency. Physicians were provided with a report about the interaction, the list of affected patients, and recommendations.
ResultsA total of 486 patients were included in the study, representing 59.0% of total patients with Alzheimer's disease in the Area. There were 66.0% women, and 86.8% of the patients were older than 75 years, and with a mean of 9.2 drugs per patient. The mean number of anticholinergic drugs was 1.6, and 38.3% of patients were prescribed various anticholinergic drugs, with 23.9% on high potency anticholinergic drugs. A statistically significant association was found between taking an anticholinergic and AChEI concomitantly (P=.000; OR: 3.9).
ConclusionsThe prevalence of interactions between AChEI and anticholinergic drugs is relevant, considering that it affects vulnerable members of the population. Providing physicians with information about the interaction could help them make clinical decisions, and could improve patient safety, as well as health outcomes.
La enfermedad de Alzheimer (EA) es una enfermedad neurodegenerativa, progresiva e irreversible relacionada directamente con la edad, que afecta al 5-7% de la población de más de 65 años y casi al 25% de los mayores de 85 años. Es el tipo de demencia más frecuente y representa hasta el 70% de los casos de demencia1,2.
Con la evolución de la enfermedad hay una pérdida progresiva de autonomía en las actividades habituales de la vida diaria. La mayoría de los enfermos presentan, además, síntomas psicológicos y conductuales2.
Los objetivos del tratamiento son mejorar la calidad de vida del paciente y del cuidador, retrasar el deterioro cognitivo y prevenir trastornos del estado de ánimo y de la conducta, así como posibles complicaciones (caídas, fracturas o infecciones). Actualmente no se conoce ningún tratamiento capaz de curar o prevenir la EA. Están comercializados en España para su tratamiento sintomático:
- a)
Inhibidores de la acetilcolinesterasa (IACE): donepezilo, rivastigmina y galantamina; autorizados para la EA leve o moderada.
- b)
Antagonista no competitivo de los receptores de N-metil D-aspartato: memantina; autorizado para la EA moderada y grave.
Sin embargo, estos medicamentos tan solo consiguen leves mejorías cognitivas y funcionales1.
Con el fin de tratar comorbilidades asociadas a los IACE, es frecuente la prescripción de fármacos con efectos anticolinérgicos en pacientes con EA3–5. Su uso contrarresta la modesta eficacia de los IACE6,7, dado que ejercen su efecto farmacológico por un mecanismo de acción opuesto y favorecen la aparición de toxicidad anticolinérgica, que se asocia con múltiples efectos adversos sobre el sistema nervioso, tanto periféricos (sequedad de boca, estreñimiento, retención urinaria o visión borrosa, entre otros) como centrales (delirium y deterioro cognitivo). Por estos motivos se consideran fármacos inapropiados en pacientes de edad avanzada8 y con demencia9–11.
La intensidad de los efectos adversos anticolinérgicos depende de la carga anticolinérgica acumulada en el conjunto de los medicamentos, de la función cognitiva de base y de la variabilidad intraindividual farmacocinética y farmacodinámica12. Además, no hay que olvidar que el metabolismo y excreción de estos fármacos decrece con la edad, por lo que los pacientes de edad avanzada son más susceptibles de desarrollar efectos adversos.
La determinación in vitro de la actividad anticolinérgica sérica se ha considerado durante años el gold standard para cuantificar la carga anticolinérgica acumulada en un paciente, sin embargo, es un método caro, no siempre accesible y de difícil interpretación en la práctica clínica. Como alternativa, se han desarrollado y publicado diferentes escalas, como son la Anticholinergic Drug Scale (ADS)13, la Anticholinergic Risk Scale (ARS)14 o la Anticholinergic Cognitive Burden Scale (ACBS)15, que asignan diferentes puntos a cada fármaco (desde 1 hasta 3) en función de su actividad anticolinérgica (baja, media o alta).
Los objetivos del estudio fueron: conocer la prevalencia de prescripción concomitante de IACE y anticolinérgicos en un Área de Salud, identificar los pacientes afectados por esta interacción e informar a los médicos responsables, con el fin de que valorasen la idoneidad de los tratamientos y, con ello, mejorar su eficacia y seguridad.
Material y métodosEstudio descriptivo transversal y observacional de prevalencia que incluyó a pacientes de un Área de Salud, a los que se les dispensó en el primer trimestre de 2015, con receta del Sistema Nacional de Salud (SNS), algún fármaco IACE (rivastigmina, galantamina o donepezilo) y, además, fármacos con efectos anticolinérgicos. Los datos de fármacos dispensados, edad y sexo de los pacientes fueron obtenidos del Sistema de Información de Consumo Farmacéutico Concylia16, que contiene información sobre especialidades farmacéuticas dispensadas con receta del SNS por las oficinas de farmacia de Castilla y León.
Para seleccionar y clasificar los fármacos con efectos anticolinérgicos, se utilizó como referencia el listado de Durán et al.17, al que se añadieron otros identificados en Micromedex®18 y se excluyeron los de uso hospitalario y los que no están comercializados ni financiados en España. La relación final de fármacos con alta y baja potencia anticolinérgica utilizada para este estudio se muestra en la tabla 1.
Fármacos con efectos anticolinérgicos
| Alta potencia | Baja potencia |
|---|---|
| Aclidinio bromuro | Amantadina |
| Amitriptilina | Baclofeno |
| Atropina | Bromocriptina |
| Biperideno | Carbamazepina |
| Butilescopolamina | Cetirizina |
| Clomipramina | Citalopram |
| Clorpromazina | Clonazepam |
| Clozapina | Codeína |
| Dexclorfeniramina | Ciclobenzaprina |
| Doxepina | Diazepam |
| Escopolamina | Disopiramida |
| Fesoterodina | Domperidona |
| Flufenazina | Entacapona |
| Glicopirronio bromuro | Fentanilo |
| Hidroxizina | Fexofenadina |
| Imipramina | Fluoxetina |
| Ipratropio | Fluvoxamina |
| Levomepromazina | Haloperidol |
| Mebeverina | Ketorolaco |
| Mepiramina | Litio |
| Nortriptilina | Loratadina |
| Oxibutinina | Meperidina |
| Pinaverio bromuro | Metadona |
| Prociclidina | Metocarbamol |
| Tiotropio bromuro | Mirtazapina |
| Tizanidina | Morfina |
| Tolterodina | Olanzapina |
| Trihexifenidilo | Oxcarbazepina |
| Trimipramina | Oxicodona |
| Paroxetina | |
| Pimozida | |
| Quetiapina | |
| Ranitidina | |
| Risperidona | |
| Teofilina | |
| Tramadol | |
| Trazodona | |
| Triazolam |
Fuente: clasificación modificada de Durán et al.17.
Para cuantificar la exposición total del paciente a los fármacos anticolinérgicos (carga anticolinérgica acumulada por paciente), se asignó una puntuación a cada fármaco en función de su potencia anticolinérgica (1: baja potencia; 2: alta potencia).
Desde el Servicio de Farmacia de Atención Primaria se envió a cada médico, en mayo de 2015, una nota informativa sobre la interacción y los fármacos comercializados y financiados en España con efectos anticolinérgicos clínicamente significativos clasificados en función de su potencia. Además, la nota contenía recomendaciones para optimizar la farmacoterapia en la EA y la relación de pacientes de su cupo afectados por la interacción, con el fin de que se realizara una revisión de la eficacia e idoneidad de estos tratamientos. En esa relación se incluyeron para cada paciente: código de identificación de paciente, edad, sexo y los fármacos IACE y anticolinérgicos prescritos en el periodo estudiado.
Por otro lado, se analizó a través del programa Concylia si en los meses postintervención (junio-julio de 2015) se había reducido o eliminado la carga anticolinérgica de los pacientes, o bien, se había eliminado el IACE.
Con el fin de establecer si existe correlación entre tomar IACE y anticolinérgicos de forma concomitante, se realizó un análisis sobre la prescripción de estos fármacos en mayores de 65 años.
En el análisis estadístico se utilizó la media, la desviación estándar (DE) y el intervalo de confianza (IC) del 95% para las variables continuas y los porcentajes para las categóricas. El coeficiente de correlación de Spearman se utilizó para estudiar la relación entre variables cuantitativas y el test chi-cuadrado de Pearson para estudiar la relación entre variables categóricas. La prueba U de Mann-Whitney se utilizó para la comparación de medias entre poblaciones independientes. Para realizar los análisis estadísticos se utilizó el programa IBM SPSS Statistics para Windows (versión 23.0.0.0)19.
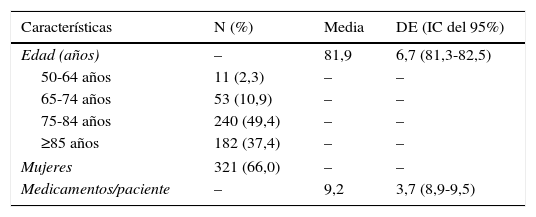
ResultadosEn el estudio se incluyó a 486 pacientes de cualquier edad en tratamiento con IACE y algún fármaco anticolinérgico, lo que supone el 59,0% sobre el total de pacientes con EA en tratamiento con IACE del Área de Salud; 247 pacientes (50,8%) estaban siendo tratados con rivastigmina. Las características de los pacientes se muestran en la tabla 2.
Características de la muestra de pacientes
| Características | N (%) | Media | DE (IC del 95%) |
|---|---|---|---|
| Edad (años) | – | 81,9 | 6,7 (81,3-82,5) |
| 50-64 años | 11 (2,3) | – | – |
| 65-74 años | 53 (10,9) | – | – |
| 75-84 años | 240 (49,4) | – | – |
| ≥85 años | 182 (37,4) | – | – |
| Mujeres | 321 (66,0) | – | – |
| Medicamentos/paciente | – | 9,2 | 3,7 (8,9-9,5) |
DE: desviación estándar; IC: intervalo de confianza; N: frecuencia.
En la muestra analizada se registraron 759 fármacos anticolinérgicos. El número medio de fármacos anticolinérgicos por paciente fue 1,6 (DE: 0,85; IC 95%: 1,49-1,64), con un máximo de 5. Un total de 300 (61,7%) pacientes tenían prescrito un fármaco anticolinérgico, 121 (24,9%) 2 y 65 (13,4%) 3 o más, con una relación inversa entre el número de fármacos anticolinérgicos y la edad (rho = −0,125; p = 0,006). No se encontraron diferencias estadísticamente significativas en el número de fármacos anticolinérgicos (p=0,474) entre mujeres y hombres.
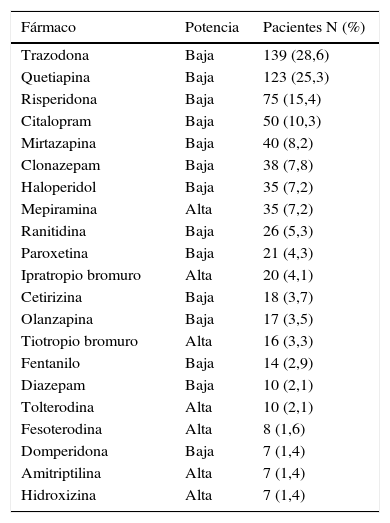
En la tabla 3 se muestran los fármacos anticolinérgicos más frecuentemente implicados y su potencia. Cabe destacar que 116 pacientes (23,9%) tenían prescrito algún fármaco de alta potencia anticolinérgica y, en cuanto a la carga anticolinérgica acumulada por paciente, 442 (90,9%) obtuvieron una puntuación entre 1 y 3 (1=255 [52,5%] pacientes; 2=127 [26,1%] pacientes y 3=60 [12,3%] pacientes) y 44 (9,1%) obtuvieron una puntuación entre 4 y 6 (4=30 [6,2%] pacientes; 5=8 [1,6%] pacientes y 6=6 [1,2%] pacientes); estos últimos, con un promedio de 80,3 años y 3,5 fármacos anticolinérgicos/paciente.
Fármacos con efectos anticolinérgicos prescritos con mayor frecuencia
| Fármaco | Potencia | Pacientes N (%) |
|---|---|---|
| Trazodona | Baja | 139 (28,6) |
| Quetiapina | Baja | 123 (25,3) |
| Risperidona | Baja | 75 (15,4) |
| Citalopram | Baja | 50 (10,3) |
| Mirtazapina | Baja | 40 (8,2) |
| Clonazepam | Baja | 38 (7,8) |
| Haloperidol | Baja | 35 (7,2) |
| Mepiramina | Alta | 35 (7,2) |
| Ranitidina | Baja | 26 (5,3) |
| Paroxetina | Baja | 21 (4,3) |
| Ipratropio bromuro | Alta | 20 (4,1) |
| Cetirizina | Baja | 18 (3,7) |
| Olanzapina | Baja | 17 (3,5) |
| Tiotropio bromuro | Alta | 16 (3,3) |
| Fentanilo | Baja | 14 (2,9) |
| Diazepam | Baja | 10 (2,1) |
| Tolterodina | Alta | 10 (2,1) |
| Fesoterodina | Alta | 8 (1,6) |
| Domperidona | Baja | 7 (1,4) |
| Amitriptilina | Alta | 7 (1,4) |
| Hidroxizina | Alta | 7 (1,4) |
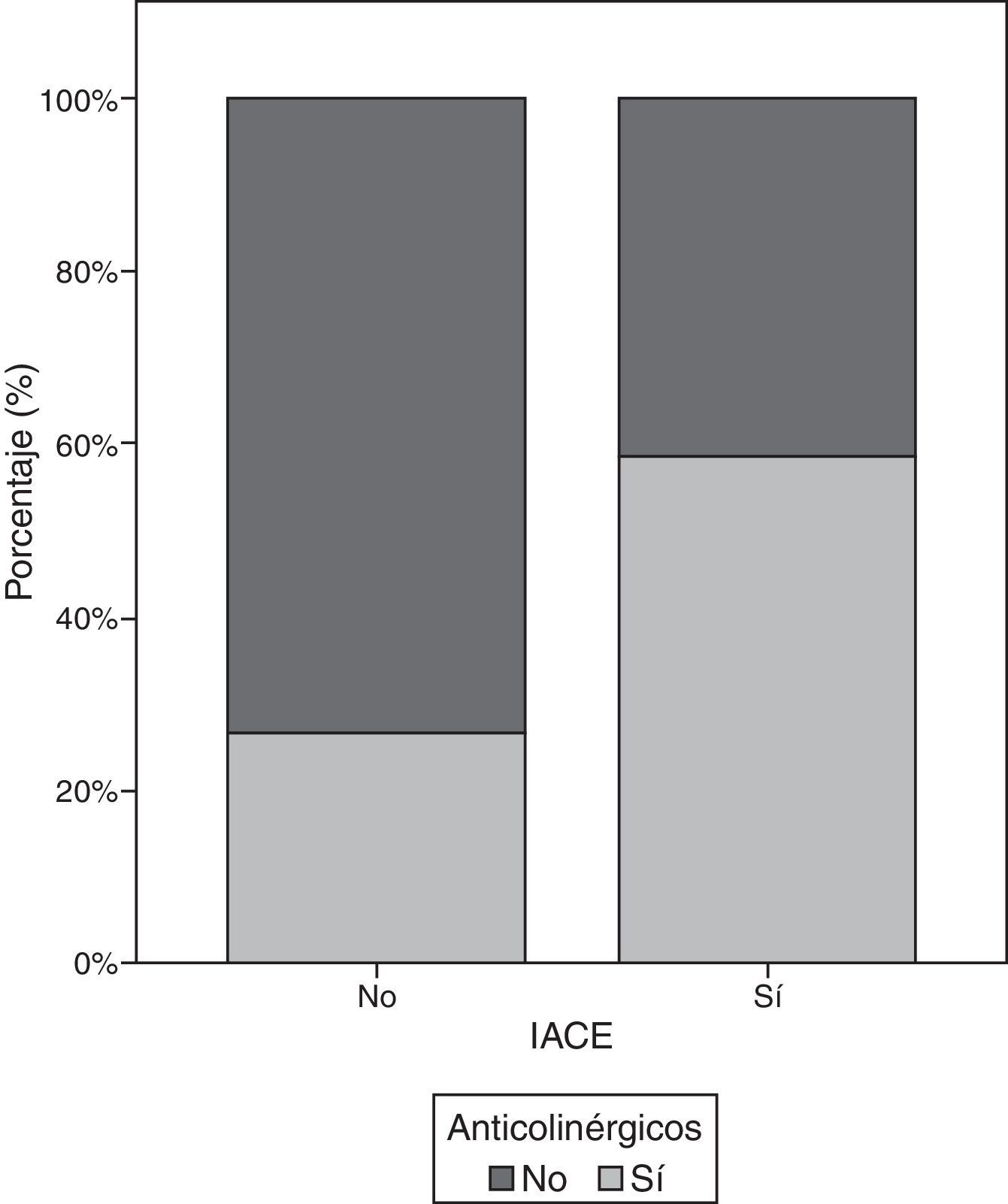
En la población mayor de 65 años, se encontró una asociación estadísticamente significativa entre tomar IACE y tomar anticolinérgicos de forma concomitante (p=0,000) (ver fig. 1). Es más probable tomar anticolinérgicos entre quienes toman IACE que entre los que no toman IACE (OR = 3,9; IC=[3,4-4,6]).
Se comunicó, al total de médicos de Atención Primaria del Área (213), la nota informativa con recomendaciones y la relación de pacientes de su cupo afectados por la interacción. El análisis realizado en el mes de julio reveló que a 85 (17,5%) pacientes (edad media: 82,3±6,2 años) se les retiraron todos los fármacos anticolinérgicos y a 70 (14,4%) (edad media: 83,1±7,3 años) los IACE, y que desapareció la interacción en 155 (31,9%) de los pacientes comunicados. A 49 (10,1%) pacientes se les retiró algún fármaco anticolinérgico, lo que disminuyó la carga total del tratamiento. Los pacientes con carga anticolinérgica acumulada más elevada (de 4 a 6), la redujeron una media de 1,5 puntos. El número de fármacos anticolinérgicos/paciente también se redujo: a 2,2.
Se retiraron un total de 129 fármacos anticolinérgicos. Los más frecuentes fueron trazodona (n=20; 15,5%), mepifilina (n=19; 14,7%), risperidona (n=15; 11,6%) y haloperidol (n=15; 11,6%). Los antipsicóticos (n=45; 34,9%), antidepresivos (n=32; 24,8%) y broncodilatadores (n=29; 22,5%) fueron los grupos terapéuticos más frecuentemente eliminados.
DiscusiónLos medicamentos anticolinérgicos pueden producir alteraciones cognitivas, delirium y caídas. Los pacientes de edad avanzada son los más susceptibles de sufrir estos efectos. A pesar de ello, diferentes estudios epidemiológicos apuntan a que aproximadamente el 50% de las personas mayores están en tratamiento con estos fármacos (en el área de estudio, el 27%) y que con frecuencia, se prescriben simultáneamente varios en un mismo paciente10.
Por otro lado, es habitual la utilización de anticolinérgicos en pacientes con EA, lo que puede contrarrestar el modesto efecto terapéutico de los anticolinesterásicos y exacerbar el declinar cognitivo4,20. En este sentido, varios estudios han tratado de estimar la prevalencia de la asociación: un estudio australiano reveló que el 32% de los pacientes que iniciaron tratamiento con IACE también recibieron de forma concomitante, durante 28 semanas, al menos un fármaco anticolinérgico, con incremento de su uso tras el inicio del anticolinesterásico21. Otro análisis prospectivo, que incluyó una cohorte de 28.961 pacientes canadienses, reportó una prevalencia de en torno al 37%22. En nuestro estudio, casi el 60% de los pacientes del Área de Salud tratados con IACE estaban, además, en tratamiento con fármacos anticolinérgicos. El 86,8% eran mayores de 75 años y estaban polimedicados (más de 9 fármacos por paciente). Además de encontrar que esta asociación es estadísticamente significativa, se observó que el riesgo de estar en tratamiento con fármacos anticolinérgicos es 4 veces mayor en los pacientes que toman IACE, por lo que es posible que algunos anticolinérgicos (por ejemplo: antiespasmódicos gastrointestinales o urinarios) se prescriban con el fin de manejar ciertos efectos adversos de los IACE.
Aproximadamente el 25% de los pacientes analizados tenían prescritos simultáneamente 2 anticolinérgicos y más del 13% tenían más de 3. Con relación a lo anterior, un reciente estudio de cohortes relacionó el consumo de fármacos anticolinérgicos con mayor riesgo de hospitalización por delirium o demencia: el riesgo era 2,6 veces mayor en los pacientes que tomaban 2, y casi 4 veces mayor en los que tomaban 3 o más23.
Con el fin de estimar la carga anticolinérgica acumulada en el paciente y predecir el riesgo de efectos adversos a nivel central, se han publicado diversas escalas13–15 y un método in vitro. Dichas escalas otorgan a cada fármaco de 0 a 3 puntos en función de su potencia anticolinérgica, sin embargo, simplifican los complejos mecanismos farmacológicos al no tener en cuenta las particularidades de cada paciente (función renal y hepática, comorbilidades, otros tratamientos, etc.), lo que resulta especialmente problemático en las personas mayores. Además, no han sido estandarizadas y no existe consenso ni en la selección de los fármacos incluidos ni en su clasificación. Tampoco hay consenso en el impacto de las distintas vías de administración, ya que algunas escalas han excluido los que se administran por vía tópica, oftálmica, ótica e inhalatoria.
Para la selección de fármacos anticolinérgicos en nuestro estudio, se ha utilizado como referencia la revisión publicada recientemente por Durán et al.17, que incluye una lista de 100 fármacos con efectos anticolinérgicos clínicamente relevantes, basada en el análisis y consenso de 7 escalas de riesgo descritas en la literatura. La lista se ha modificado para adaptarla al ámbito de Atención Primaria.
Con relación a la carga anticolinérgica acumulada, un estudio europeo publicado recientemente, con seguimiento de más de 20.000 pacientes durante 11 años, identificó una relación directa entre la intensidad de la exposición a anticolinérgicos y la mortalidad cardiovascular y por todas las causas24.
En nuestro estudio, más del 38% de los pacientes tenían prescritos varios fármacos inapropiados tanto para su edad como para su enfermedad y casi un 50% presentaban una carga anticolinérgica que podría considerarse clínicamente significativa (igual o superior a 2), que supone la toma de uno o varios fármacos de alta potencia o varios fármacos de baja potencia.
Resulta difícil comparar nuestros resultados con estudios ya publicados, debido a que se ha utilizado una escala de riesgo diferente. Ello implica distintos fármacos seleccionados, distintas categorías de riesgo y diferente puntuación en función de la potencia anticolinérgica.
Los grupos terapéuticos más frecuentemente implicados en la interacción con los IACE fueron antidepresivos (37,0%) y antipsicóticos (31,9%), resultado similar a lo descrito por otros autores25. No es de extrañar si tenemos en cuenta que los síntomas conductuales y psicológicos son muy frecuentes en la EA.
Sin embargo, los antidepresivos tienen una eficacia controvertida en el tratamiento de la depresión en pacientes con demencia y su uso se ha asociado a la aparición de mayores efectos adversos26,27. Los antipsicóticos, por su parte, se han asociado con efectos adversos cerebrovasculares graves, e incluso muerte28,29.
Le siguen a estos grupos farmacológicos, antihistamínicos (8%), benzodiacepinas (6,3%) y broncodilatadores anticolinérgicos por vía inhalatoria (5,5%). Es ampliamente conocido que los antihistamínicos de primera generación y el uso prolongado de benzodiacepinas de vida media larga se consideran potencialmente inapropiados en pacientes de edad avanzada por aumentar, entre otras cosas, el riesgo de delirium, caídas y fracturas; sin embargo, su uso continúa siendo muy frecuente, incluso en pacientes con deterioro cognitivo. En cuanto a los broncodilatadores anticolinérgicos, si bien es cierto que ejercen su mecanismo de acción bloqueando los receptores muscarínicos, la mayoría de las escalas de riesgo no los incluyen por no considerar la vía inhalatoria con suficiente impacto a nivel sistémico.
Los fármacos que se prescriben específicamente por sus propiedades anticolinérgicas son bien reconocidos por los médicos (por ejemplo, oxibutinina para tratar la incontinencia urinaria), sin embargo, pueden ser menos conscientes de que algunos medicamentos prescritos para otros fines también tienen propiedades anticolinérgicas. Incluso, medicamentos con propiedades anticolinérgicas menores pueden contribuir a efectos adversos centrales y periféricos si se utilizan en combinación con otros agentes anticolinérgicos.
La iatrogenia y los efectos de la interacción se podrían disminuir si en el momento de la prescripción se valorara la necesidad de utilizar fármacos anticolinérgicos en pacientes con demencia, se evaluara periódicamente su efectividad y se interrumpieran o reemplazaran estos fármacos por otros con menos potencia anticolinérgica.
Por todo ello, la información sobre la interacción entre IACE y anticolinérgicos se comunicó al total de médicos de Atención Primaria del Área de Salud. Cabe destacar que, según el análisis realizado posteriormente, se retiró la interacción a casi un 32% de los pacientes, bien porque se retiraron los fármacos anticolinérgicos (14,4%), bien porque se retiró el IACE (17,5%) y, en algo más de un 10% de los pacientes, se redujo la carga anticolinérgica acumulada en el tratamiento. No podemos asegurar que todos estos cambios los haya realizado el médico de Atención Primaria ni que se hayan producido como consecuencia de la intervención, sin embargo, puede que la información y las recomendaciones, así como la valoración de la eficacia de estos tratamientos, se hayan tenido en cuenta, dado que la mayoría de los fármacos retirados son de prescripción crónica (antidepresivos, antipsicóticos y los propios IACE).
Dentro de las limitaciones del estudio está el hecho de que solo se identificó a pacientes a los que se les prescribió en receta del SNS entre enero-marzo de 2015, sin poder valorar el riesgo en pacientes del ámbito privado, en los que retiraron fármacos anticolinérgicos no financiados (por ejemplo, difenhidramina para el insomnio, o clorfenamina para procesos alérgicos), en los que no retiraron sus medicamentos en los meses de estudio o en los que fue imposible su identificación por ser recetas de médicos de Atención Especializada o prescripción manual. Tampoco se tuvo en cuenta la duración del tratamiento concomitante.
Por otro lado, para hacer una mejor estimación de la potencia anticolinérgica de cada fármaco, habría que considerar las dosis con efectos clínicamente relevantes y el impacto de la vía de administración. Además, sería necesario que en futuras investigaciones se evaluaran los resultados en salud o el riesgo de hospitalización, para conocer el alcance y relevancia clínica de estos hallazgos.
Para concluir, la prevalencia de interacción entre IACE y anticolinérgicos en el Área de Salud es relevante (50,9%), considerando que además afecta a población vulnerable. Los resultados del estudio ponen en evidencia la necesidad de implantar sistemas de apoyo a la prescripción que alerten de la interacción y sus consecuencias. Mientras tanto, proporcionar a los médicos información basada en la evidencia disponible sobre la interacción, los fármacos implicados y su potencia anticolinérgica podría ser una herramienta de ayuda a la toma de decisiones clínicas que permitiría mejorar la seguridad y los resultados en salud de los pacientes.
Conflicto de interesesLos autores expresamos que no hay conflicto de intereses al redactar el manuscrito.
A Rosa Sepúlveda Correa, profesora contratada, doctora del Departamento de Estadística de la Universidad de Salamanca, por el apoyo en los análisis estadísticos.