La prevalencia e incidencia de insuficiencia cardíaca (IC) sigue aumentando de manera especial en las personas de mayor edad, constituyendo un importante problema geriátrico. En el paciente anciano las características etiopatogénicas, epidemiológicas e incluso clínicas de la IC difieren significativamente de las presentes en el paciente más joven, pero el tratamiento que se aplica deriva del resultado de ensayos clínicos con escasa participación de pacientes de edad avanzada. Más allá de la cardiopatía, resulta esencial evaluar al paciente en su globalidad, atendiendo a la interrelación entre la IC y los diferentes síndromes geriátricos característicos del paciente anciano. Esta revisión analiza estos aspectos diferenciales del tipo de paciente con IC más frecuente en el “mundo real”.
The prevalence and incidence of heart failure (HF) is increasing, especially in the elderly population, and is becoming a major geriatric problem. Elderly patients with HF usually show etiopathogenic, epidemiological, and even clinical characteristics significantly different from those present in younger patients. Their treatment, however, derives from clinical trials performed with only a few elderly subjects. Moreover, beyond the cardiovascular disease itself, it is essential to evaluate the patient as a whole, given the interrelationship between HF and the characteristic geriatric syndromes of the elderly patient. This review examines the peculiarities in the most prevalent “real world” HF patient.
El síndrome clínico de insuficiencia cardíaca (IC) había sido históricamente una enfermedad propia del adulto, relacionada principalmente con patología valvular o isquémica, con un pronóstico a corto/medio plazo grave que impedía al paciente alcanzar una edad avanzada. Sin embargo, en las últimas décadas la prevalencia de IC se ha desplazado paulatinamente hacia el grupo de pacientes de más edad, con una proporción cada vez más elevada de muy ancianos: según el estudio NHANES, el 22% de los pacientes ambulatorios diagnosticados de IC en Estados Unidos son octogenarios o nonagenarios1. Esta «epidemia geriátrica» es un problema sanitario de creciente importancia no limitado tan solo al ámbito de la práctica clínica2, ya que genera importantes problemas de salud pública. Esta revisión abordará aspectos etiopatogénicos, epidemiológicos y clínicos, con especial hincapié en la interrelación de la IC con los síndromes geriátricos característicos del paciente anciano, así como en la falta de datos de eficacia en esta población para muchas de las intervenciones terapéuticas habituales.
Epidemiología y etiopatogenia de la Insuficiencia Cardíaca en el ancianoLa IC afecta de forma primordial a pacientes de edad avanzada. Los datos de prevalencia disponibles son variables, ya que dependen de la población estudiada (población general, consultas especializadas, hospitalización de agudos) y los criterios diagnósticos aplicados (codificación administrativa, criterios exclusivamente clínicos o criterios basados en clínica más ecocardiografía). Por lo que respecta a la población general española, los estudios PRICE3 y EPISERVE4, basándose en criterios clínicos, estiman una prevalencia de IC entre el 4,7 y el 6,8% en la población de 45 o más años. En ambos estudios se demuestra un incremento lineal de las tasas de prevalencia a medida que aumenta la edad de la población estudiada, llegando a alcanzar valores cercanos al 16% en pacientes mayores de 75 años. Restringiendo los datos a población ingresada, destaca que el 1% del total de altas de hospitalización en España corresponde a episodios de IC descompensada, siendo la edad media de los pacientes hospitalizados por este motivo de 75 años5.
Considerando como criterio diagnóstico las alteraciones estructurales cardíacas relacionadas con la IC, un estudio americano6 demuestra que, si bien la prevalencia de IC en población general definida por criterios clínicos diagnósticos no alcanzaba el 2%, un 6% presentaba disfunción sistólica del VI, y hasta un 30% algún grado de disfunción diastólica, siendo estas dos últimas cifras del 13 y el 70% respectivamente en septuagenarios6. El mismo estudio muestra que la incidencia de IC es del 10 ‰ a los 65 años y crece de forma exponencial a partir de esta edad hasta alcanzar tasas superiores al 40% en octogenarios. Aunque las tasas de incidencia parecen haber iniciado una tendencia a la baja en adultos jóvenes siguen aumentando paulatinamente en la población anciana, especialmente en hombres; por este motivo se calcula que un octogenario, a pesar de su reducida esperanza de vida, presenta un riesgo similar al de una persona de 40 años (cercano al 20%) de desarrollar IC en el futuro7.
La presencia de IC se asocia a un 50% de reducción de la expectativa de vida en los pacientes de 75 o más años8. En pacientes con antecedente de hospitalización por IC, la mortalidad al año del primer ingreso oscila entre el 24 y el 50%, y llega a alcanzar en octogenarios tasas de hasta el 81% a los cinco años9. Los reingresos repetidos se asocian en ancianos también a tasas altísimas de mortalidad. No parecen existir diferencias significativas en la mortalidad en pacientes con fracción de eyección del VI reducida (ICFER) y la IC con fracción de eyección del VI preservada (ICFEP), con tasas globales a los 5 años del primer episodio de descompensación próximas al 50%10.
Los datos epidemiológicos disponibles no permiten discernir con seguridad si la ICFEP es, como se suele sugerir, más prevalente en los pacientes ancianos que la ICFER. El arquetipo de paciente con ICFEP sería una mujer anciana hipertensa, que presenta múltiple patología asociada y que, en contraposición a una función sistólica del VI normal (generalmente definida por una fracción de eyección ≥ 50%), presenta una función diastólica del VI alterada, de acuerdo a los criterios11 de la Sociedad Europea de Cardiología (SEC). Sin embargo, conviene matizar que, como concepto clínico, la categoría «ICFEP» es más inclusiva que la de «disfunción diastólica», dado que permite añadir pacientes con clínica de IC y función del VI estrictamente normal tanto en sístole como en diástole cuya clínica deriva de anomalías cardíacas estructurales o funcionales de otra índole como las valvulopatías, la disfunción contráctil del ventrículo derecho, la hipertensión pulmonar sistólica, la dilatación o disfunción contráctil auricular, las taquiarritmias o la IC hiperdinámica. Además, no es infrecuente que en un mismo paciente coexistan datos ecocardiográficos de disfunción diastólica y sistólica12. La prevalencia de ICFEP dependerá por tanto de la «generosidad» del criterio diagnóstico aplicado, como se aprecia al comparar los criterios de inclusión y exclusión utilizados en los diferentes ensayos clínicos de tratamiento de ICFEP con la definición de esta entidad que utilizan los estudios retrospectivos o los registros clínicos basados solo en ecocardiografía o codificación diagnóstica.
Teniendo en cuenta esta variabilidad del criterio diagnóstico y la frecuente coexistencia de más de una enfermedad o anomalía cardíaca potencialmente generadoras de IC, resulta difícil determinar con precisión cuál es la causa más frecuente de IC en el paciente anciano. Tradicionalmente se ha considerado que en esta población la miocardiopatía secundaria a hipertensión arterial sería la principal responsable, seguida de la cardiopatía isquémica, y de la patología valvular cardíaca13. Sin embargo, es probable que el rol de la cardiopatía isquémica esté infravalorado, ya que confirmar su presencia puede obligar a la práctica de estudios diagnósticos (pruebas de estrés o cateterismo coronario) que no es infrecuente que no lleguen a considerarse o resulte imposible realizar en los pacientes ancianos más frágiles o pluripatológicos.
Características clínicas y diagnósticas específicasSegún las Guías de Práctica Clínica (GPC) de la SEC el diagnóstico de IC en ancianos sigue los mismos criterios que el diagnóstico en adultos jóvenes, basado en la asociación de datos clínicos con exploraciones que proporcionen evidencias objetivas de disfunción cardíaca14. En ancianos, sin embargo, la clínica puede ser atípica o poco expresiva, y los síntomas y signos pierden sensibilidad y especificidad en presencia de patología asociada o simplemente los cambios fisiológicos de la senescencia, por lo que sin un elevado grado de sospecha la IC puede pasar desapercibida excepto en descompensaciones graves. Por el contrario, algunos síntomas o signos considerados «clásicos» de IC pueden ser secundarios a otras enfermedades y conducir a un diagnóstico erróneo si no se investigan adecuadamente las causas15. Esta complejidad clínica se pone de manifiesto en un estudio reciente desarrollado en una consulta de geriatría con población octogenaria ambulatoria16: datos clínicos no característicos como el bajo peso, la anorexia o la ausencia de sibilantes se asocian significativamente a una mayor probabilidad diagnóstica de IC en la población estudiada, mientras que signos y síntomas clásicos estaban ausentes en un tercio de los pacientes finalmente diagnosticados de IC.
Para completar el diagnóstico resulta esencial disponer de un electrocardiograma, una radiografía de tórax y una analítica; sin embargo, en la actualidad la exploración complementaria por excelencia para el diagnóstico de IC es la ecografía cardíaca, que además de confirmar la presencia de anomalías estructurales del corazón permite caracterizar el mecanismo fisiopatológico subyacente a la clínica. La proporción de pacientes ancianos con IC en los que se dispone de ecocardiograma ha aumentado progresivamente en la última década17. Debe hacerse notar que los valores de normalidad no han sido específicamente validados en población anciana, por lo que en edades muy avanzadas deberían interpretarse con cautela.
Para solventar las limitaciones del diagnóstico clínico y contribuir así a un uso más racional de la ecocardiografía, evitando practicar esta técnica diagnóstica en pacientes con muy baja probabilidad «pretest» de IC, se han intentado desarrollar programas de cribado diagnóstico basados en biomarcadores, en particular los péptidos natriuréticos (BNP o NT-proBNP) plasmáticos. El papel diagnóstico más válido de las concentraciones de BNP o Nt-proBNP en ancianos deriva de su valor predictivo negativo: por debajo de un determinado punto de corte (<100ng/L de BNP o<300-400ng/L de NT-proBNP en situación de enfermedad aguda, o<35ng/L y 125ng/L respectivamente en pacientes más estables14) resulta altamente improbable que la clínica de un paciente, aun siendo sugestiva, sea imputable a IC. Los valores elevados de BNP o Nt-proBNP, en cambio, pese a estar incluidos dentro de los criterios diagnósticos de ICFEP11, y haber sido evaluados en pacientes ancianos con IC aguda18, no están explícitamente recomendados para el estudio diagnóstico de esta población: existe un gran intervalo de concentraciones, mayor cuanto más alta sea la edad del paciente, que no aportan mayor sensibilidad al diagnóstico (por encima de los 75 años el punto de corte que aporta valor diagnóstico probablemente no sea inferior a 1.800ng/L de Nt-proBNP). Además, la concentración de los péptidos natriuréticos suele elevarse también en presencia de otras enfermedades crónicas (insuficiencia renal, fibrilación auricular, hipertensión pulmonar secundaria a enfermedad pulmonar…) habituales en pacientes de edad avanzada. Datos recientes abonan sin embargo la utilidad de evaluar el aumento porcentual de los valores de BNP «basal» en pacientes ambulatorios para detectar con mayor precisión y de forma más precoz los episodios de descompensación19, así como el uso de las concentraciones de Nt-proBNP para determinar la intensidad del tratamiento, más allá de la clínica de congestión, en pacientes ancianos con ICFER20.
Tratamiento de la Insuficiencia Cardíaca en ancianosSensu stricto, el tratamiento farmacológico de la IC en el paciente geriátrico no debería diferir del que se prescribe a pacientes más jóvenes, y así se refleja en las GPC de la SEC14, donde ningún medicamento aparece específicamente indicado o proscrito en función de la edad del paciente. Sin embargo, faltan datos robustos de eficacia del tratamiento en pacientes ancianos: las recomendaciones de mayor calidad de las guías (ICFER) derivan de los resultados de ensayos clínicos con una participación casi exclusiva de adultos relativamente jóvenes, mientras que para la ICFEP, si bien la población estudiada en ensayos clínicos es de mayor edad, los resultados obtenidos no han permitido hasta el momento identificar fármacos que ofrezcan beneficios significativos21. A esta incertidumbre en cuanto a la eficacia se suman las dificultades de implementación de las recomendaciones terapéuticas, ya que resulta habitual la presencia en el paciente de mayor edad de factores que limitan la prescripción o reducen la eficacia del tratamiento farmacológico: farmacocinética y farmacodinámica alteradas, pluripatología y polifarmacia significativas, y barreras cognitivas, funcionales, sensoriales o socioeconómicas que pueden influir en la toma correcta de medicación22. Los registros de pacientes con IC certifican que los pacientes con IC reciben un tratamiento cada vez más adecuado, pero aún se detectan déficits significativos cuando la población analizada es la de edad más avanzada23. De hecho, algunos autores se han cuestionado la eficacia real en términos de morbimortalidad en población muy anciana con IC de las pautas de tratamiento basadas en la aplicación estricta de las recomendaciones de las GPC, hasta el punto de que un ensayo clínico está intentando dilucidar si en pacientes octogenarios estas pautas pueden sustituirse por un tratamiento o manejo más laxo, siendo la autoevaluación de la calidad de vida relacionada con la IC el resultado que se valorará como objetivo principal24.
Tratamiento farmacológico: Insuficiencia Cardíaca con Fracción de Eyección Reducida (ICFER)La tabla 1 muestra un resumen de los ensayos clínicos aleatorizados de tratamiento de ICFER desarrollados con pacientes cuyo promedio de edad en el momento de la inclusión era igual o superior a 65 años. Las especificidades de cada grupo farmacológico de tratamiento de la ICFER en cuanto a beneficios, tolerabilidad y efectos secundarios en pacientes ancianos son las siguientes:
- •
Inhibidores de la enzima conversora de la angiotensina (IECA) y antagonistas del receptor de la angiotensina II (ARA II): son fármacos de primera línea que en población general con ICFER reducen de forma muy significativa el riesgo de morbimortalidad y reingreso; sin embargo, ninguno de los grandes ensayos clínicos que demostraron estos beneficios incluyó una proporción significativa de pacientes ancianos. Un metaanálisis de los ensayos clínicos más relevantes25 demostró que el uso de IECA seguía ofreciendo beneficios si se restringía el análisis a pacientes de>60 años, aunque partiendo de la premisa de que las dosis utilizadas fueran la dosis diana de estos estudios, difíciles de alcanzar en la población anciana. El beneficio del tratamiento con ARA II vs. IECA (losartán vs. captopril) en población septuagenaria con ICFER fue comparado en el ensayo clínico aleatorizado ELITE-II26, sin que se observaran diferencias a favor de uno u otro clínicamente significativas; un reciente análisis retrospectivo de pacientes de>65 años ingresados por agudización de IC no encontró tampoco diferencias significativas en ICFER (aunque sí en ICFEP a favor de ARA II) en términos de mortalidad o reingreso al comparar los pacientes tratados tras el alta con IECA con aquellos tratados con ARA II27. El uso de IECA y ARA II en ancianos puede verse limitado por la presencia de hipotensión (o el desarrollo de hipotensión ortostática que suele acompañar las primeras dosis) o el riesgo de desencadenar o agravar la insuficiencia renal; ambos efectos adversos son relativamente habituales en ancianos pero pueden minimizarse iniciando el tratamiento con dosis bajas y evitando el uso de dosis máximas: el uso de dosis intermedias confiere también beneficios clínicos, aunque probablemente de menor intensidad que los obtenidos con las dosis diana de los ensayos28. Es preferible evitar el uso de ambos grupos farmacológicos cuando la tasa de filtrado glomerular (FG) sea<30ml/min, y aplicar mayores precauciones (ajuste de vasodilatadores, retirada de nefrotóxicos, control precoz de función renal) si el FG se sitúa entre 30 y 60ml/min; la hiponatremia aumenta también el riesgo de toxicidad renal por lo que debe ser corregida antes de añadir IECA o ARA II. Está bien demostrado que la combinación IECA+ARA II se asocia a un mayor riesgo de efectos adversos (especialmente deterioro de función renal e hiperpotasemia), por lo que el uso combinado resulta desaconsejable, especialmente en población anciana. Por último, mencionar que no existen aún en ancianos con ICFER datos ni experiencia suficientes relacionados con el efecto clínico de la inhibición combinada del eje renina-angiotensina y la neprisilina29.
- •
Betabloqueantes: son también fármacos de primera línea con significativo efecto beneficioso en morbimortalidad que, al igual que los IECA/ARA II, fueron evaluados en ensayos clínicos con baja participación de pacientes ancianos. El estudio SENIORS30, que confirmó el beneficio del tratamiento con nebivolol en pacientes tanto con ICEFR como ICFEP (aunque con una FEVI promedio del 35%), se desarrolló sin embargo con pacientes con una edad promedio de 76 años. Posteriormente, un metaanálisis confirmó que el beneficio en términos de mortalidad y reingreso se mantenía en pacientes de edad superior a 65 años31 A esta edad la limitación para el uso de betabloqueantes no depende tanto de contraindicaciones genéricas (hiperreactividad bronquial, bloqueos de conducción auriculoventricular), como de hipotensión (especialmente si el paciente ya está recibiendo IECA/ARA II u otros vasodilatadores antes de iniciar el tratamiento), o una frecuencia cardíaca baja, especialmente tras el inicio del tratamiento, resultando a menudo difícil alcanzar las dosis máximas recomendadas para el tratamiento de la ICFER en las GPC. El estudio CIBIS-ELD32 evaluó en población septuagenaria este fenómeno, confirmando la dificultad de alcanzar las dosis diana de los ensayos clínicos en esta población. Sin embargo, se ha demostrado que el beneficio del betabloqueo depende probablemente más de la reducción de la frecuencia cardíaca alcanzada que de la dosis administrada33, por lo que probablemente no sea necesario forzar incrementos de dosis si se ha alcanzado una frecuencia cardíaca entre 60 y 70 latidos por minuto y el paciente no tolera dosis más elevadas.
- •
Diuréticos del asa y diuréticos tiazídicos: a diferencia de lo que ocurre con IECA/ARA II y betabloqueantes, no se ha demostrado que el tratamiento diurético ofrezca beneficios a los pacientes en ICFER en términos de morbimortalidad; sin embargo, el uso de diuréticos es casi universal en estos pacientes para el control sintomático de la congestión. Aún son más escasos los datos sobre tratamiento diurético con pacientes ancianos, dado que no existen ensayos clínicos aleatorizados desarrollados exclusivamente en esta población; los estudios retrospectivos de hecho parecen sugerir que el uso prolongado de diuréticos en población anciana con ICFER a altas dosis puede asociarse a un mayor riesgo de morbimortalidad34. El tratamiento diurético en pacientes de edad avanzada, que suelen presentar aun en presencia de un FG conservado alteraciones en el funcionalismo renal y la regulación del estímulo de la sed, se asocia a un mayor riesgo de efectos adversos. Resulta muy común el desarrollo de hiponatremia e hipopotasemia, especialmente con el uso de tiazídicos. La habitual presencia de cierto grado de insuficiencia renal puede obligar a un uso de dosis más elevadas de diuréticos de asa o a instaurar pautas combinadas de diuréticos. El uso prolongado de diuréticos del asa en monoterapia suele acabar generando un cierto grado de resistencia que obliga asimismo a aumento de dosis o al uso de combinaciones. Por todo ello, la prescripción de diuréticos en ancianos debe revisarse periódicamente, ajustando fármacos y dosis en función de la respuesta diurética, la clínica congestiva y la evolución del FG, y tanto una diuresis excesiva que conlleve deshidratación como un estado de retención hidrosalina secundario a un tratamiento no efectivo pueden acabar por limitar el uso o potenciar el riesgo de efectos secundarios de IECA/ARA II y betabloqueantes35.
- •
Antagonistas de la aldosterona: más allá del efecto diurético a dosis altas, las dosis bajas de estos fármacos confieren beneficios en morbimortalidad de intensidad similar a la observada con IECA/ARA II y betabloqueantes. Su uso en ancianos puede asociarse a hiperpotasemia y alteraciones significativas en la función renal, especialmente cuando se usan en combinación con IECA y diuréticos36, por lo que la prescripción debe ser meticulosa, evitándolos siempre en pacientes con FG<30ml/min y controlando estrechamente al paciente si presenta FG entre 30 y 60ml/min. Un efecto molesto de la espironolactona, la ginecomastia, es de desarrollo más probable e intenso en varones ancianos, cuyos niveles de testosterona plasmática suelen estar reducidos.
- •
Digoxina: actualmente se considera un fármaco de segunda línea, cuyo beneficio se limita al control sintomático, especialmente en presencia de FA, así como a la reducción del riesgo de hospitalización por agudización de IC. Un subestudio del ensayo clínico DIG37 confirmó que, aunque la incidencia de complicaciones y efectos secundarios aumentaba a mayor edad, el uso de digoxina seguía confiriendo beneficios clínicos significativos frente a placebo incluso en pacientes octogenarios. En ancianos el uso de digoxina debe ser especialmente prudente, ya que el riesgo de toxicidad digitálica es más elevado debido a la menor capacidad de depuración renal y la pérdida de masa magra habituales en edades avanzadas, que alteran la excreción y el volumen de distribución del fármaco facilitando su acumulación en plasma. Aunque no se ha evaluado de forma prospectiva, probablemente el perfil de paciente anciano con ICFER que puede beneficiarse del uso de digoxina sea aquel que presenta simultáneamente FA con frecuencia ventricular media en reposo no controlada con otros fármacos bradicardizantes. Está bien documentado que usar dosis bajas permite alcanzar niveles plasmáticos no excesivamente elevados (0,5-0,9ng/ml) que minimizan el riesgo de efectos secundarios conservando la efectividad clínica38.
- •
Otros vasodilatadores: el uso de combinaciones de nitratos e hidralazina o de amlodipino es habitual y bien tolerado en pacientes ancianos que no toleran la introducción de IECA o ARA II o que presentan insuficiencia renal crónica en estadio IV. Sin embargo, los datos de mayor calidad sobre eficacia y seguridad de estos tratamientos vasodilatadores alternativos proceden de ensayos clínicos muy antiguos, con participación muy escasa de pacientes ancianos39,40. La principal complicación del uso de la terapia combinada con hidralazina y nitratos en pacientes de edad avanzada es el desarrollo de hipotensión ortostática y la cefalea. En el caso del amlodipino no resulta infrecuente el estreñimiento y sobre todo la aparición o empeoramiento de edema en extremidades inferiores, que puede inducir a un uso inadecuado de diuréticos.
- •
Ivabradina: en el corazón este fármaco actúa de forma exclusiva en el nodo sinusal reduciendo la frecuencia cardíaca sin afectar a la presión arterial o el inotropismo. El estudio SHIFT demostró que añadir ivabradina a pacientes que no podían usar betabloqueantes o no toleraban incrementos de dosis reducía significativamente la morbimortalidad asociada a ICFER si la frecuencia cardíaca basal era ≥ 70 latidos por minuto. Aunque la edad promedio de los pacientes del ensayo no era muy elevada, un análisis por cuartiles de edad confirma que el beneficio se mantiene en pacientes de edad superior a 60 años41. En pacientes ancianos la ivabradina ofrece un perfil de seguridad muy favorable, ya que a excepción de la bradicardia sintomática (que puede atenuarse iniciando el tratamiento con dosis bajas y usando dosis intermedias de mantenimiento) la incidencia de efectos secundarios asociados a su uso es muy baja y poco relevante.
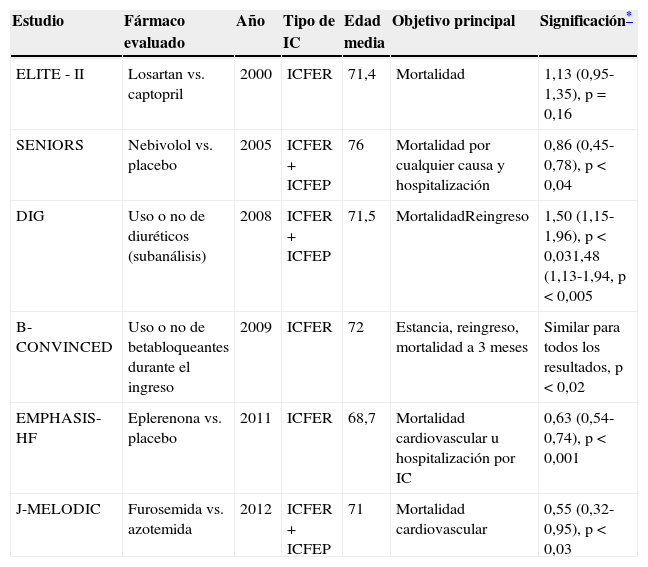
Ensayos clínicos de tratamiento farmacológico en ICFER crónica con participación principal de pacientes ancianos (promedio edad participantes>65 años): resultados en morbimortalidad
| Estudio | Fármaco evaluado | Año | Tipo de IC | Edad media | Objetivo principal | Significación* |
|---|---|---|---|---|---|---|
| ELITE - II | Losartan vs. captopril | 2000 | ICFER | 71,4 | Mortalidad | 1,13 (0,95-1,35), p=0,16 |
| SENIORS | Nebivolol vs. placebo | 2005 | ICFER+ICFEP | 76 | Mortalidad por cualquier causa y hospitalización | 0,86 (0,45- 0,78), p<0,04 |
| DIG | Uso o no de diuréticos (subanálisis) | 2008 | ICFER+ICFEP | 71,5 | MortalidadReingreso | 1,50 (1,15-1,96), p<0,031,48 (1,13-1,94, p<0,005 |
| B-CONVINCED | Uso o no de betabloqueantes durante el ingreso | 2009 | ICFER | 72 | Estancia, reingreso, mortalidad a 3 meses | Similar para todos los resultados, p<0,02 |
| EMPHASIS-HF | Eplerenona vs. placebo | 2011 | ICFER | 68,7 | Mortalidad cardiovascular u hospitalización por IC | 0,63 (0,54-0,74), p<0,001 |
| J-MELODIC | Furosemida vs. azotemida | 2012 | ICFER+ICFEP | 71 | Mortalidad cardiovascular | 0,55 (0,32-0,95), p<0,03 |
Fuente: Alagiakrishnan et al.94.
La tabla 2 muestra un resumen de los ensayos clínicos aleatorizados de tratamiento de ICFEP; en la mayor parte de los casos los pacientes incluidos son de edad moderadamente avanzada, aunque en general con una carga de comorbilidad baja. Como ya se ha comentado en la introducción de este apartado, hasta la fecha ningún ensayo clínico ha permitido identificar un fármaco capaz de reducir de forma significativa la morbimortalidad en los pacientes con ICFEP. De todas maneras, ya sea como objetivo secundario de algunos ensayos clínicos o a través de metaanálisis y estudios retrospectivos, se han podido objetivar algunos efectos beneficiosos de los fármacos estudiados o de uso habitual en pacientes con ICFEP en términos de reingreso, calidad de vida o control de síntomas42,43. A falta de datos de mayor calidad para guiar el tratamiento, en la actualidad el control de la ICFEP en pacientes ancianos sigue estando basado en una combinación empírica de tratamiento sintomático (principalmente diurético) y el de los factores causales y posibles desencadenantes (hipertensión arterial, cardiopatía isquémica y arritmias).
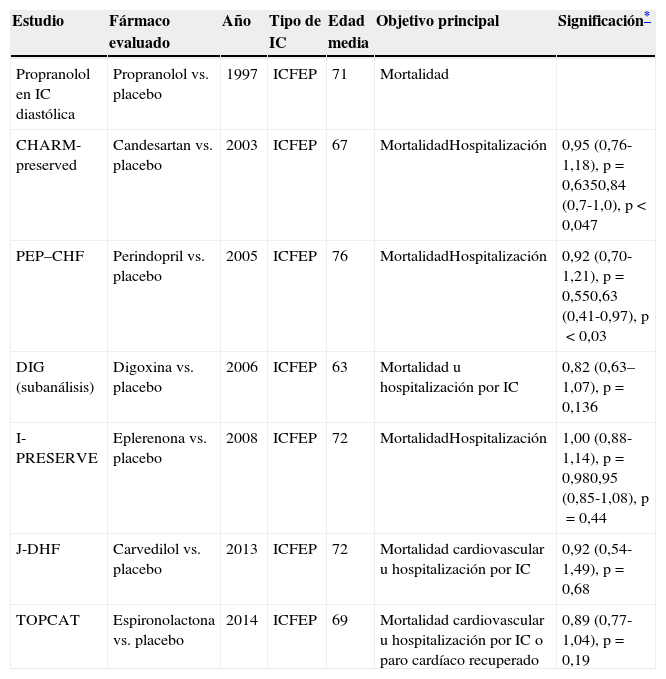
Ensayos clínicos de tratamiento farmacológico en ICFEP crónica: resultados en morbimortalidad
| Estudio | Fármaco evaluado | Año | Tipo de IC | Edad media | Objetivo principal | Significación* |
|---|---|---|---|---|---|---|
| Propranolol en IC diastólica | Propranolol vs. placebo | 1997 | ICFEP | 71 | Mortalidad | |
| CHARM-preserved | Candesartan vs. placebo | 2003 | ICFEP | 67 | MortalidadHospitalización | 0,95 (0,76-1,18), p=0,6350,84 (0,7-1,0), p<0,047 |
| PEP–CHF | Perindopril vs. placebo | 2005 | ICFEP | 76 | MortalidadHospitalización | 0,92 (0,70-1,21), p=0,550,63 (0,41-0,97), p<0,03 |
| DIG (subanálisis) | Digoxina vs. placebo | 2006 | ICFEP | 63 | Mortalidad u hospitalización por IC | 0,82 (0,63–1,07), p=0,136 |
| I-PRESERVE | Eplerenona vs. placebo | 2008 | ICFEP | 72 | MortalidadHospitalización | 1,00 (0,88-1,14), p=0,980,95 (0,85-1,08), p=0,44 |
| J-DHF | Carvedilol vs. placebo | 2013 | ICFEP | 72 | Mortalidad cardiovascular u hospitalización por IC | 0,92 (0,54-1,49), p=0,68 |
| TOPCAT | Espironolactona vs. placebo | 2014 | ICFEP | 69 | Mortalidad cardiovascular u hospitalización por IC o paro cardíaco recuperado | 0,89 (0,77-1,04), p=0,19 |
Fuente: Alagiakrishnan et al.94.
- •
Actividad física: ofrece beneficios contrastados tanto en ICFEP e ICFER, aunque limitados a una mejoría leve de la función física/capacidad de esfuerzo, sin impacto significativo en la supervivencia; en edades avanzadas se recomiendan pautas de intensidad moderada y creciente de trabajo aeróbico. Algunos programas han incluido elementos de terapia ocupacional, estimulación cognitiva y ejercicios destinados a la mejora del tono y postura corporal44.
- •
Desfibriladores y resincronizadores: en las últimas décadas se ha extendido el uso de estos dispositivos en pacientes con ICFER, pero las guías recomiendan explícitamente limitar su implantación a pacientes con expectativa de vida superior a un año con buena situación funcional, por lo que muchas veces se desestima su uso en pacientes ancianos. Sin embargo, en Europa cerca de un tercio de dispositivos de resincronización se implantan en pacientes de ≥ 75 años y existen datos que demuestran su utilidad en pacientes septuagenarios e incluso octogenarios45.
- •
Tratamiento percutáneo de valvulopatías: de aplicación en pacientes muy seleccionados, pero con resultados muy aceptables en casos no tributarios de cirugía convencional cuya IC depende de la presencia de valvulopatía mitral o aórtica grave46,47.
Entre un 40 y un 70% de los ancianos con IC presenta simultáneamente cinco o más enfermedades asociadas48,49. La edad media de los pacientes es cada vez más elevada y la comorbilidad asociada ha ido aumentando en paralelo, por lo que resulta cada vez más frecuente la presencia de patología cardiovascular (excepto la cardiopatía isquémica) y no cardiovascular simultánea, así como la presencia de pacientes con 5 o más diagnósticos asociados (42% en 1988-1994 vs. 58% en 2003-2008)1. Analizando con mayor detalle el segmento de pacientes ancianos, se constata que el patrón de comorbilidad varía en función de la edad: mientras que la prevalencia de cardiopatía isquémica, FA, insuficiencia renal, diabetes e ictus decrece significativamente a partir de los 70 años, la patología no cardiovascular (demencia, déficits visuales, osteoporosis, artrosis, cáncer…) muestra una trayectoria inversa, con prevalencias crecientes a medida que los pacientes envejecen50–52.
El rol de la comorbilidad es importante: a mayor número de enfermedades presente, mayor riesgo de ingreso, relacionado o no con descompensación de la IC49,53. Con relación a la mortalidad, los datos del INH Registry alemán muestran que a mayor número de enfermedades, mayor resulta el riesgo de mortalidad por cualquier causa en población general ambulatoria con IC54. En un estudio reciente la comorbilidad, cuantificada mediante el índice de Charlson en pacientes ambulatorios octogenarios con IC, constituye el principal factor de riesgo de mortalidad a medio plazo (3 años)55. El riesgo aumenta a medida que el índice de Charlson es más elevado, fenómeno que no se observó sin embargo en un estudio similar56, pero desarrollado a partir de pacientes de edad no tan avanzada, que evaluó también mortalidad pero a largo plazo. Un estudio reciente ha evaluado el impacto de la comorbilidad como factor de riesgo de hospitalización, reingreso y estancia hospitalaria prolongada en población general con IC controlada en atención primaria: la insuficiencia renal, la diabetes, la cardiopatía isquémica, la hipertensión arterial y la enfermedad pulmonar obstructiva crónica se identificaron como factores de riesgo independientes para el desarrollo de estos end-points57. También muy recientemente se ha evaluado, a partir de una amplia muestra de pacientes con más de 65 años, si existen diferencias significativas en el patrón de comorbilidad entre los pacientes con ICFER o ICFEP; certificando que: a) globalmente la comorbilidad es discreta pero significativamente más elevada en los pacientes con ICFEP; b) en ICFEP es más común la presencia de FA y algunas enfermedades no cardiovasculares mientras que en ICFER resulta más habitual el antecedente o presencia de cardiopatía isquémica, y c) los «patrones» de comorbilidad (las formas de presentación conjunta de diferentes entidades clínicas con la IC), en cambio, no varían significativamente entre ambas entidades58.
La presencia de comorbilidad influye también en los patrones de prescripción: en más de la mitad de los pacientes ancianos con prescripción no acorde a las GPC en IC existen limitaciones objetivas derivadas de la patología acompañante o de su tratamiento59. Finalmente, cabe destacar que puntuaciones elevadas del índice de Charlson se correlacionan con menor capacidad de autocuidado en IC, fenómeno que se asocia a mayor riesgo de reingreso y mortalidad60.
Discapacidad física e Insuficiencia CardíacaLa relación entre IC y discapacidad física es bidireccional, ya que no tan solo la presencia de IC, especialmente en fases avanzadas o tras una hospitalización por agudización puede generar discapacidad, sino que también la presencia de discapacidad, incluso leve, puede actuar como factor de riesgo para el desarrollo de IC61. En pacientes con IC establecida, los datos del estudio NHANES confirman la elevada prevalencia de discapacidad física en ancianos: a partir de los 60 años más de la mitad de los pacientes presentan dificultades para la movilización y un 11% precisa ayuda para vestirse, comer o trasladarse a la cama1.
La presencia de discapacidad física es también un factor de riesgo de mala evolución: valores bajos del índice de Barthel son predictores de mortalidad tanto intrahospitalaria como a corto y largo plazo en población anciana con IC que precisa de hospitalización por agudización62,63, independientemente de la edad, las características del episodio de IC o el tipo de disfunción del VI presente. De forma recíproca, el ingreso por IC condiciona un riesgo elevado de desarrollo o agravamiento de discapacidad: un estudio reciente objetiva que en población octogenaria el riesgo de deterioro funcional, manifestado por la aparición de mayor dificultad para el desempeño de actividades básicas (y también instrumentales) de la vida diaria, aumenta de forma muy significativa (40%) si existe el antecedente de ingreso por agudización de IC64.
Deterioro cognitivo e Insuficiencia CardíacaLa asociación de la IC con el deterioro cognitivo deriva de la existencia de factores de riesgo compartidos para el desarrollo de ambos síndromes (cardiopatía isquémica, hipertensión arterial y diabetes), la presencia habitual junto a la IC de otras enfermedades que también pueden contribuir a la aparición de demencia (FA, síndrome de apnea/hipoapnea obstructiva del sueño o depresión), y los cambios estructurales y funcionales que experimenta el sistema nervioso central directamente atribuibles a la presencia de IC: hipoperfusión cerebral por reducción del gasto cardíaco, cambios en la arquitectura y la capacidad de regulación vasomotora de la microvasculatura encefálica, y mayor riesgo de fenómenos tromboembólicos, incluso en ausencia de arritmias65. La escasa actividad física que suele desarrollar el paciente con IC parece también desempeñar un papel en la génesis del deterioro cognitivo en estos pacientes66.
La prevalencia de deterioro cognitivo es más elevada en pacientes con IC: en pacientes septuagenarios se ha reportado una prevalencia del 15% de demencia y del 24% de deterioro cognitivo leve, significativamente superior a la presente en población de edad equivalente no diagnosticada de IC67. En población con IC más anciana la prevalencia de deterioro cognitivo es aún más elevada; además, la incidencia de demencia o deterioro cognitivo leve en estos pacientes es significativamente superior a la esperable en sujetos sin IC de esta misma franja de edad68.
Desgraciadamente, pese a que instrumentos de uso habitual como el Mini Mental Status Examination parecen ser válidos para el cribado de deterioro cognitivo en esta población69, este suele pasar desapercibido o no se documenta en la historia clínica, fenómeno que se asocia a un mayor riesgo de mortalidad o reingreso con relación a los pacientes correctamente detectados70. Este fenómeno impide que los pacientes mal diagnosticados puedan beneficiarse de los mecanismos de apoyo o de la prescripción de tratamiento apropiados para la demencia, comprometiendo potencialmente el nivel de competencia cognitiva necesaria para las tareas de autocuidado y reconocimiento de síntomas que requiere un paciente con IC.
No existen aún estudios que hayan evaluado de forma específica cómo influye el control o el tratamiento específico del deterioro cognitivo en la evolución clínica global de los pacientes con IC y deterioro cognitivo leve o demencia, más allá de los resultados reportados en programas de manejo multidisciplinar de la enfermedad, que en ocasiones incluyen algún tipo de intervención en este sentido.
Fragilidad-caquexia e Insuficiencia CardíacaLa «caquexia cardíaca», un síndrome de base neurohumoral caracterizado por astenia asociada a pérdida progresiva de peso, masa magra y densidad mineral ósea en fases avanzadas del síndrome, asociado a una elevada letalidad y que afecta a un 15% aproximado de los pacientes con IC, es a menudo interpretada como expresión clínica de fragilidad en esta población, ya que estos síntomas suelen presentarse como marcadores fenotípicos del síndrome de fragilidad en fases avanzadas. Sin embargo, si bien es probable que los pacientes con caquexia cardíaca puedan ser considerados frágiles, y que el mecanismo subyacente sea compartido, no todos los pacientes con IC y fragilidad desarrollarán esta grave complicación.
La relación entre fragilidad e IC es compleja. Probablemente existen mecanismos fisiopatológicos interrelacionados, así como algunas manifestaciones clínicas compartidas: a) citoquinas proinflamatorias (relacionadas con la pérdida de masa muscular y modificaciones en la neurotransmisión implicadas en la génesis de la anorexia, la fatiga, el enlentecimiento psicomotor o la depresión), b) trastornos metabólicos como la diabetes, la ferropenia o la hipovitaminosis D, c) la comorbilidad, que forma parte de algunas definiciones de fragilidad basadas en modelos de acúmulo de déficits y patología, y d) los déficits nutricionales, secundarios a escasa ingesta y a malabsorción, incluyendo la falta de micronutrientes generadores de desequilibrios metabólicos asociados a saciedad precoz, náuseas y anorexia.
La prevalencia de fragilidad en población con IC, en función de la población evaluada y el criterio aplicado, puede llegar a oscilar entre un 25 y un 50% en ancianos con IC, en marcado contraste con la prevalencia observada en población general de la misma edad y sexo libres de la enfermedad. Pocos estudios han evaluado el impacto de la fragilidad en población anciana con IC, y la definición aplicada es extremadamente heterogénea, pero en todos se ha constatado que su presencia condiciona mayor riesgo no tan solo de morbimortalidad, sino también de peor calidad de vida y capacidad de esfuerzo en esta población71,72.
Otros elementos característicos de la Insuficiencia Cardíaca en el anciano: polifarmacia, depresión, nutrición, problemática socialEl uso de fármacos usados bajo prescripción médica en pacientes con IC estable ha pasado de un promedio de 4,1 a finales de los años 90 del siglo XX a 6,4 a finales de la primera década del siglo XXI; un 10% de los pacientes toma simultáneamente 10 o más medicamentos1. Si bien este fenómeno es reflejo de la aplicación cada vez más cuidadosa de las GPC (no tan solo de IC) y por lo tanto a priori resulta correcto, está bien documentado que la adición secuencial de fármacos incrementa exponencialmente el riesgo de interacciones fármaco-fármaco y el riesgo de efectos secundarios derivados de la interacción fármaco-enfermedad. La intervención de farmacólogos expertos en geriatría a la hora de revisar el plan general de prescripción en ancianos con IC ha demostrado ser útil para reducir la tasa de efectos secundarios y otros acontecimientos adversos en esta población73.
La depresión es una patología con elevada prevalencia en IC y cuya asociación con mayor riesgo de morbimortalidad, peor calidad de vida y utilización inapropiada de dispositivos sanitarios ha sido bien documentada en pacientes con IC, incluso cuando se presenta en forma de depresión leve o distimia74. La presencia de depresión se asocia también con peor capacidad de autocuidado y mayor riesgo de efectos secundarios derivados del uso de antidepresivos, aunque hoy en día es menos habitual el uso de antidepresivos cardiotóxicos. El beneficio del tratamiento no está aún bien documentado, pero los escasos datos disponibles derivados de algún ensayo clínico son alentadores, aunque el número de pacientes ancianos incluidos resulta muy escaso75.
En ancianos con IC está bien documentada la «paradoja de la obesidad», es decir, el efecto protector en términos de morbimortalidad del sobrepeso y la obesidad en contraposición al mayor riesgo de acontecimientos adversos observado en pacientes con normopeso o peso bajo. Un estudio reciente desarrollado en nuestro medio con pacientes octogenarios hospitalizados por IC76 mostró que aquellos con índice de masa corporal ≥ 25 presentaban un mejor estado nutricional, así como una mejor capacidad funcional. En el seguimiento, aquellos que experimentaron un empeoramiento en la situación nutricional presentaron mayores tasas de mortalidad. Es probable que el IMC normal o elevado sea un marcador de una situación metabólica y funcional de base robusta que confiera una mayor protección al organismo ante los desarreglos neurohumorales propios de la IC77.
Con respecto a la situación socioeconómica de los pacientes con IC una revisión reciente78 indica que los déficits sociales y económicos se asocian a mayor incidencia de IC, a mayores tasas de reingreso tras hospitalizaciones por descompensación y a mayor riesgo de mortalidad, aunque los autores concluyen que resulta muy difícil determinar cuáles son los factores que determinan esta asociación. En nuestro ámbito, un estudio prospectivo79 demuestra que, incluso tras ajustar por variables clínicas y funcionales relacionadas con morbimortalidad en IC, las condiciones inapropiadas del condicionaban en población septuagenaria ingresada por IC un mayor riesgo de mortalidad tras el alta hospitalaria.
Evaluación multidimensional del paciente ancianos con Insuficiencia Cardíaca -herramientas pronósticasParece razonable suponer que más allá de las causas de la IC y la mayor o menor complejidad del proceso diagnóstico y terapéutico, la presencia de comorbilidad elevada y de síndromes geriátricos debería influir de manera significativa en la evolución clínica y funcional de un paciente anciano con IC. Un estudio relativamente reciente desarrollado también en nuestro ámbito80, además de documentar de nuevo la elevada prevalencia de síndromes geriátricos en esta población, demostró que su presencia se asociaba de forma independiente a mayor riesgo posterior de declive funcional, reingreso y mortalidad.
Establecer el pronóstico vital, clínico o funcional de un paciente con IC debe tener en cuenta estas variables, pero los datos derivados de la valoración geriátrica integral (VGI) tradicionalmente no habían formado parte de los modelos de predicción. Las primeras recomendaciones pronósticas, basadas en la presencia de datos exclusivamente clínicos relacionados con la IC, han sido progresivamente arrinconadas al demostrarse su escasa fiabilidad81. Posteriormente se desarrolló el instrumento EFFECT82, derivado y validado a partir de datos de pacientes con IC aguda y un promedio de edad de 75 años, que incorporaba al score pronóstico la edad y la comorbilidad cardiovascular y no cardiovascular. El rol de los síndromes geriátricos en el pronóstico fue evaluado por primera vez en un estudio retrospectivo desarrollado a partir de datos de más de 60.000 pacientes de Medicare que habían sufrido una hospitalización por IC83, donde se observó que la presencia de demencia o alguna dificultad para la movilización se asociaban significativamente a un mayor riesgo de mortalidad tanto a corto como a largo plazo tras el ingreso.
Posteriormente (tabla 3) se han validado de forma prospectiva varios instrumentos que incorporan parámetros de la VGI para la estimación pronóstica en pacientes hospitalizados, como el instrumento BI-EFFECT84, que deriva de añadir la puntuación del IB al instrumento EFFECT, o el MPI Score85 basado exclusivamente en parámetros de la VGI, que proporciona una estimación pronóstica de riesgo de mortalidad precoz postingreso (al mes del alta) superior a la predicha por la clase funcional NYHA o el instrumento EFFECT. De forma similar, un estudio realizado en nuestro ámbito86,87ha demostrado que un score aún más sencillo, basado en cinco elementos habituales de la VGI predice de forma significativa e independiente de los parámetros clínicos un mayor riesgo de mortalidad durante el ingreso y a los dos años del alta en población de>75 años hospitalizada por IC agudizada.
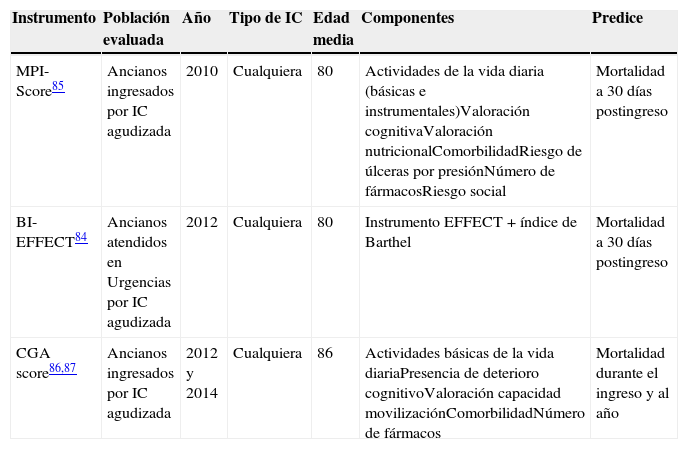
Modelos pronósticos multidimensionales que incluyen componentes de la VGI
| Instrumento | Población evaluada | Año | Tipo de IC | Edad media | Componentes | Predice |
|---|---|---|---|---|---|---|
| MPI-Score85 | Ancianos ingresados por IC agudizada | 2010 | Cualquiera | 80 | Actividades de la vida diaria (básicas e instrumentales)Valoración cognitivaValoración nutricionalComorbilidadRiesgo de úlceras por presiónNúmero de fármacosRiesgo social | Mortalidad a 30 días postingreso |
| BI-EFFECT84 | Ancianos atendidos en Urgencias por IC agudizada | 2012 | Cualquiera | 80 | Instrumento EFFECT+índice de Barthel | Mortalidad a 30 días postingreso |
| CGA score86,87 | Ancianos ingresados por IC agudizada | 2012 y 2014 | Cualquiera | 86 | Actividades básicas de la vida diariaPresencia de deterioro cognitivoValoración capacidad movilizaciónComorbilidadNúmero de fármacos | Mortalidad durante el ingreso y al año |
No existen aún estudios que hayan evaluado específicamente el papel de la VGI en la estratificación pronóstica de pacientes ancianos con IC en situación de estabilidad clínica. Sin embargo, herramientas de evaluación multidimensional habitual como el RAI 2.0 también han demostrado ser más útiles que los parámetros específicos de evaluación de función física (NYHA) para predecir el riesgo de mortalidad a medio plazo en el segmento de pacientes institucionalizados88. De todos modos, no se ha comprobado aún si existen intervenciones que, aplicadas en función del resultado obtenido con estos instrumentos, modifiquen significativamente el pronóstico.
Intervenciones multidisciplinares específicas para población ancianaEn los últimos veinte años se han desarrollado programas de intervención multidisciplinar en IC basados en el abordaje por parte de múltiples especialistas y en diferentes ámbitos de todos los componentes de tratamiento, apoyo y monitorización necesarios para el manejo integral del paciente anciano, especialmente tras ingresos por descompensación. Los resultados acumulados en este periodo han demostrado que estos programas son efectivos para reducir de forma significativa la necesidad de hospitalización, las tasas de reingreso e incluso la mortalidad en este subgrupo de pacientes89, por lo que su implementación se recomienda ya en las GPC de la SEC14. La edad media de los pacientes incluidos en los estudios que han evaluado la efectividad de estos programas no supera los 73 años, con exclusión explícita en muchos casos de pacientes más ancianos, con mayor comorbilidad, mayor complejidad farmacológica y mayor grado de discapacidad. La información disponible en pacientes con ICFEP es asimismo muy escasa, y los datos sobre efectividad de estos programas más allá de los 6-12 meses también; no está tampoco bien definido el criterio de selección de pacientes que pueden beneficiarse claramente de estos programas. Está en marcha un ensayo clínico que evalúa un programa dirigido a pacientes recientemente ingresados por un episodio de descompensación de IC, pero que deben tener al menos 75 años y presentar al menos un cierto grado preestablecido de comorbilidad y dependencia90.
Insuficiencia Cardíaca en el anciano en las Guías de Práctica ClínicaDentro de las recomendaciones globales del tratamiento del síndrome clínico de IC presentes en las GPC de mayor difusión (SEC14, American Heart Association/American College of Cardiology91, Heart Failure Society of America92) las específicas para el diagnóstico y tratamiento de los pacientes ancianos ocupan un apartado minúsculo, comparado con la extensión y calidad de las recomendaciones generales de tratamiento de la ICFER o la IC aguda. Las últimas guías europeas se limitan a ofrecer algunos datos de los ensayos clínicos con mayor participación de pacientes ancianos y comentarios genéricos relacionados con la dificultad diagnóstica. Más prácticas y explícitas son las recomendaciones IC que ofrece el proyecto ACOVE93, doce indicadores razonados de calidad asistencial elaborados por expertos en geriatría, aunque con la limitación de que la mayor parte de las recomendaciones son aplicables solo a pacientes con ICFER.
ConclusionesLa IC en el paciente anciano es la más habitual en números absolutos, es la IC del mundo real. Alejada de las descripciones académicas y de las características casi ideales de las cohortes de pacientes jóvenes que participan en la mayoría de los ensayos clínicos, constituye prácticamente un síndrome con entidad propia en el que confluyen además de la miocardiopatía los cambios del envejecimiento, las comorbilidades y los componentes funcionales, cognitivos, afectivos y sociales propios de la vejez. Gestionar adecuadamente el proceso diagnóstico y terapéutico de un anciano con IC obliga a un conocimiento amplio en todos estos ámbitos que probablemente sea deseable compartir entre varios profesionales en el ámbito de intervenciones multidisciplinares, aunque mucho de lo que hacemos sigue sin estar refrendado por datos científicos robustos. El manejo de la IC en el anciano sigue constituyendo por lo tanto un reto para el médico. Será necesario insistir en el desarrollo de proyectos de investigación, básica y clínica, centrados en esta población, para disponer en el futuro de datos objetivos que ayuden a elaborar estrategias de manejo integral realmente beneficiosas para este tipo de paciente.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.